文档内容
贵州省(黔东南,黔南,黔西南)2018 年中考理综化学试题
可能用到的相对原子质量: H-1 C-12 O-16 Na-23 C1-35.5 Fe-56 Cu-64
一、单项选择题
1. 中华民族的发明创造为人类文明进步做出了巨大贡献。下列不涉及化学变化的是
A. 粮食酿酒 B. 侯氏制碱 C. 蚕丝纺织 D. 制造火药
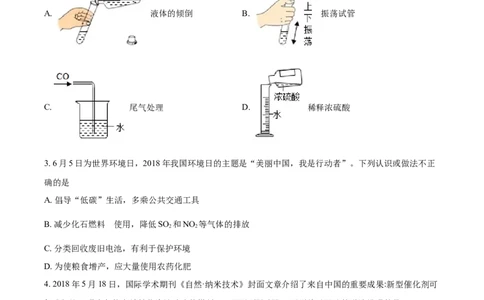
2. 下图中的实验方法或操作正确的是
A. 液体的倾倒 B. 振荡试管
C. 尾气处理 D. 稀释浓硫酸
3. 6月5日为世界环境日,2018年我国环境日的主题是“美丽中国,我是行动者”。下列认识或做法不正
确的是
A. 倡导“低碳”生活,多乘公共交通工具
的
B. 减少化石燃料 使用,降低SO 和NO 等气体的排放
2 2
C. 分类回收废旧电池,有利于保护环境
D. 为使粮食增产,应大量使用农药化肥
4. 2018年5月18日,国际学术期刊《自然·纳米技术》封面文章介绍了来自中国的重要成果:新型催化剂可
把CO 这一溫室气体高效转化为清洁液体燃料——甲醇(CHOH)。下列关于甲醇的说法错误的是
2 3
A. 甲醇属于有机物
B. 甲醇中碳元素的质量分数是37.5%
C. 甲醇的相对分子质量是32g
D. 甲醇分子中C、H、O原子个数比为1:4:1
5. 除去下列物质中的少量杂质,所选用试剂及操作方法均正确的是
选项 物质(括号内为杂质) 选用试剂(过量) 操作方法A FeCl 溶液(CuCl ) 铁粉 过滤
2 2
B NaCO (NaCl) 盐酸 蒸发、结晶
2 3
C AlCl 溶液(MgSO ) Ba(OH) 溶液 过滤、蒸发
3 4 2
D CO (CO) O 点燃
2 2
A. A B. B C. C D. D
6. 下列各种溶质的溶液混合后无明显现象的一组是
A. HCl、NaCO、 KSO B. KNO 、Ba(OH) 、 NaCl
2 3 2 4 3 2
C. KCl、AgNO、HNO D. NaOH、FeCl 、(NH )SO
3 3 3 4 2 4
二、非选择题部分
7. 用化学用语填空:
(1) 2个汞原子_______ (2)3个铁离子________;
(3) 4个氨分子________ (4)加碘盐KIO 中I元素的化合价________ ;
3
(5)核电荷数分别为8、12 的两种元素所形成的化合物________ ;
(6)绿色植物光合作用产生的单质________。
8. 化学与生活、生产息息相关,根据所学知识回答下列问题:
(1) 随意丟弃塑料会造成“白色污染”,塑料不属于_____ ( 填选项);
A.有机物 B.合成材料 C.纯净物
的
(2)能使硬水软化 方法是________ (填选项);
A.加入明矾 B.加入活性炭 C.煮沸
(3)铁制品表面涂一层油漆能防锈蚀,其原理是阻止了铁与________接触;
(4)碳酸氢钠是治疗胃酸过多症的一种药剂,它与盐酸反应的化学方程式为________。
(5)医用生理盐水中含有一定量的氯离子,请面出Cl-的离子结构示意图________。
的
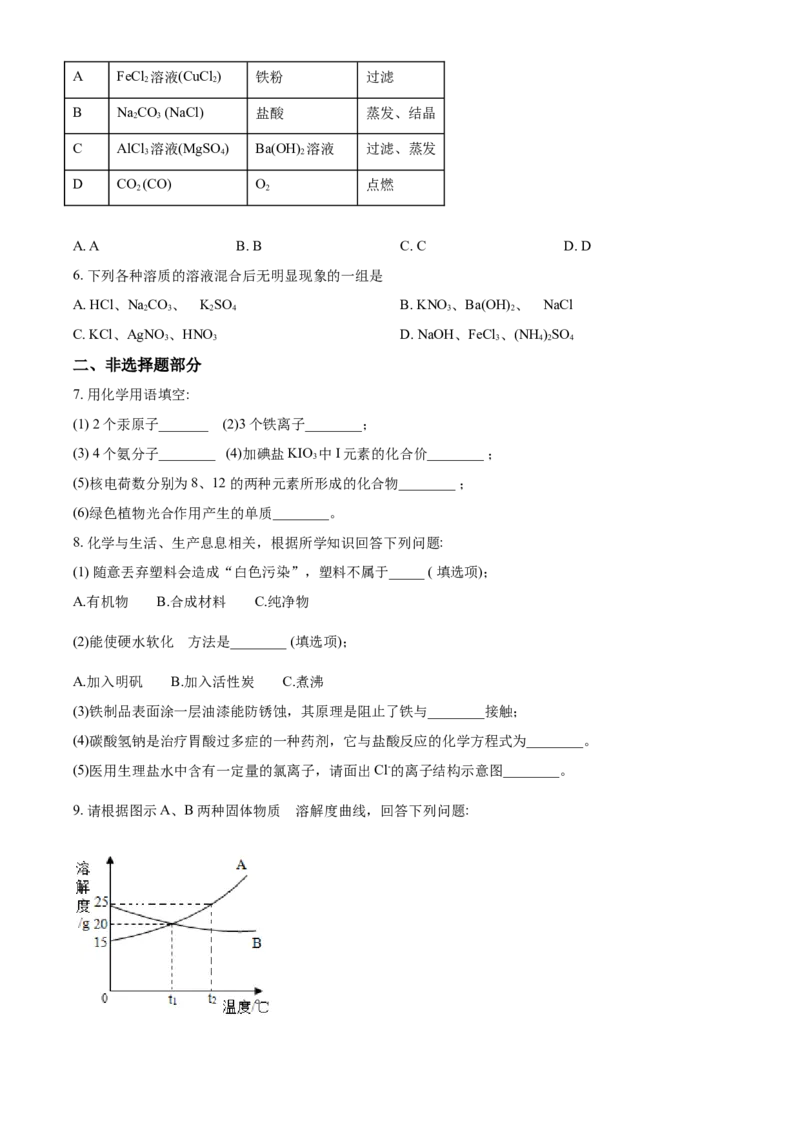
9. 请根据图示A、B两种固体物质 溶解度曲线,回答下列问题:(1)溶解度随温度升高而降低的物质是________;
(2)温度为______ (填“t℃”或“t℃”)时,A、B的溶解度相等;
1 2
(3) t ℃时,A的饱和溶液中溶质的质量分数为_______。
2
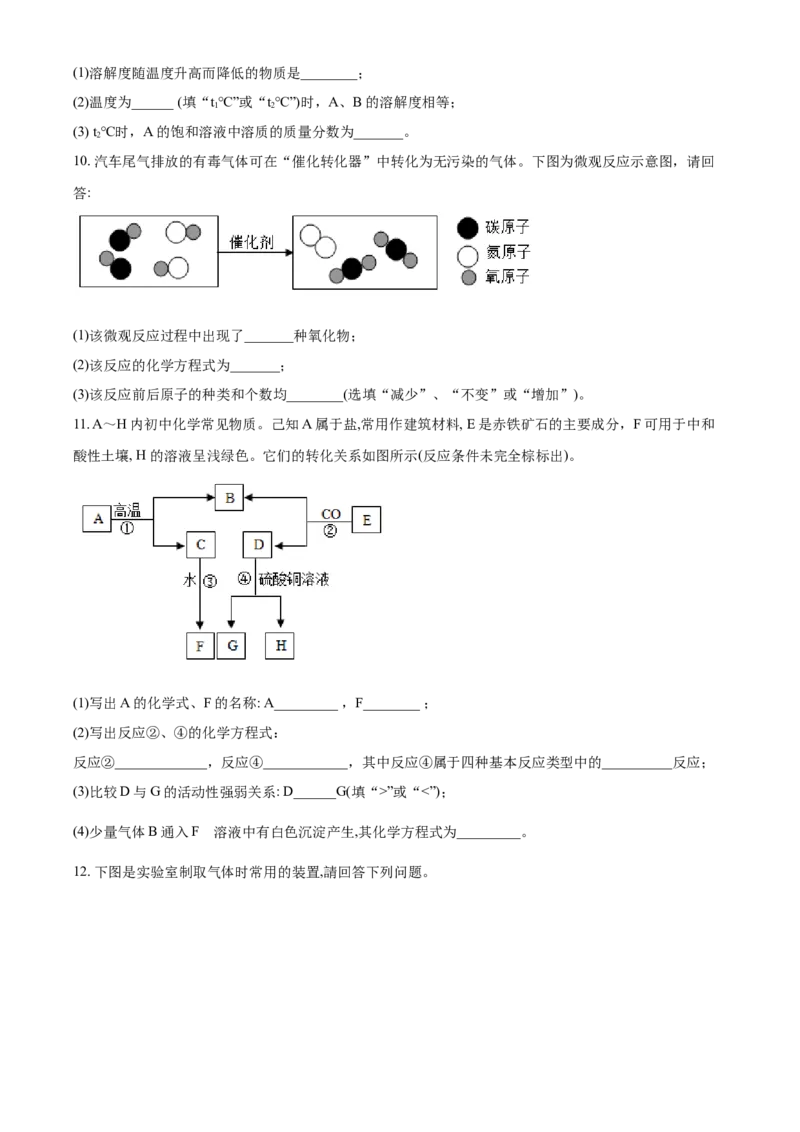
10. 汽车尾气排放的有毒气体可在“催化转化器”中转化为无污染的气体。下图为微观反应示意图,请回
答:
(1)该微观反应过程中出现了_______种氧化物;
(2)该反应的化学方程式为_______;
(3)该反应前后原子的种类和个数均________(选填“减少”、“不变”或“增加”)。
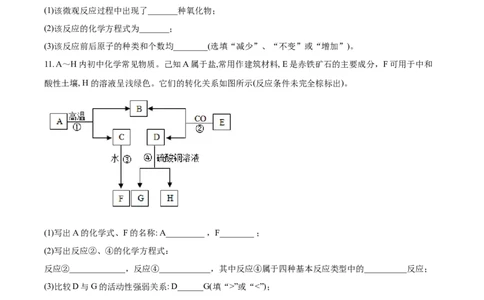
11. A~H内初中化学常见物质。己知A属于盐,常用作建筑材料, E是赤铁矿石的主要成分,F可用于中和
酸性土壤, H 的溶液呈浅绿色。它们的转化关系如图所示(反应条件未完全棕标出)。
(1)写出A的化学式、F的名称: A_________ ,F________ ;
(2)写出反应②、④的化学方程式:
反应②_____________,反应④____________,其中反应④属于四种基本反应类型中的__________反应;
(3)比较D与G的活动性强弱关系: D______G(填“>”或“<”);
的
(4)少量气体B通入F 溶液中有白色沉淀产生,其化学方程式为_________。
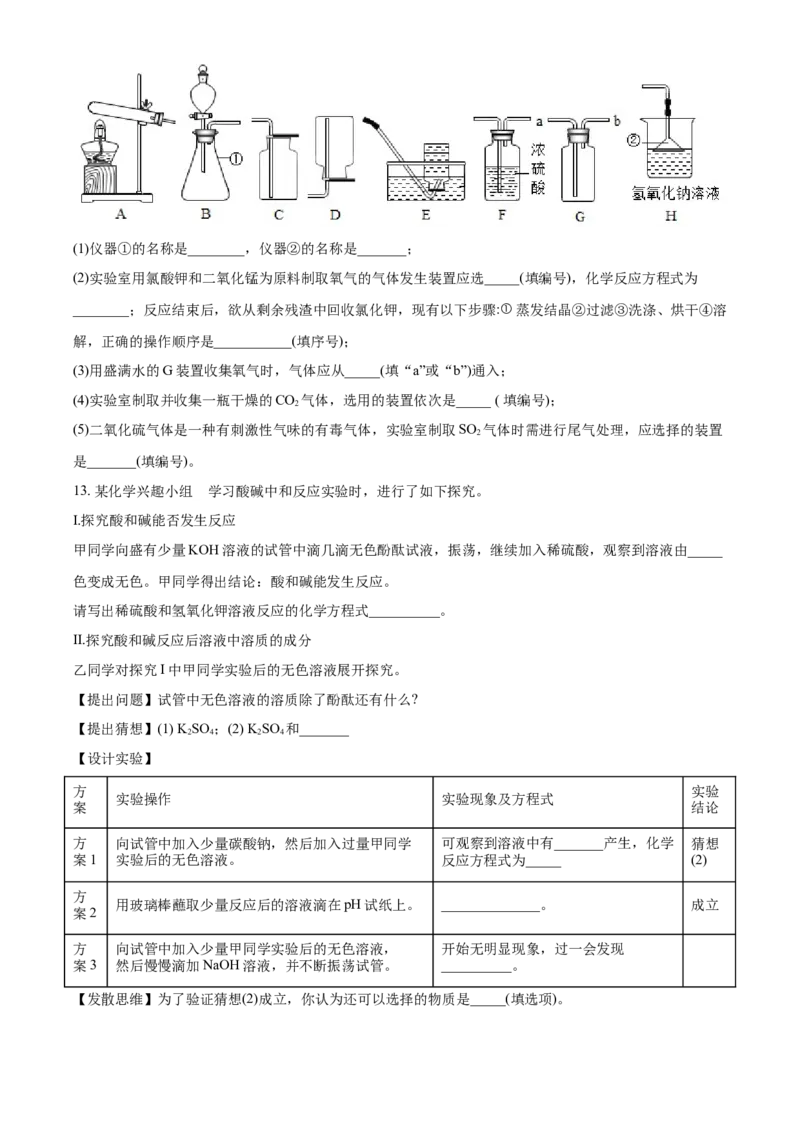
12. 下图是实验室制取气体时常用的装置,請回答下列问题。(1)仪器①的名称是________,仪器②的名称是_______;
(2)实验室用氯酸钾和二氧化锰为原料制取氧气的气体发生装置应选_____(填编号),化学反应方程式为
________;反应结束后,欲从剩余残渣中回收氯化钾,现有以下步骤:①蒸发结晶②过滤③洗涤、烘干④溶
解,正确的操作顺序是___________(填序号);
(3)用盛满水的G装置收集氧气时,气体应从_____(填“a”或“b”)通入;
(4)实验室制取并收集一瓶干燥的CO 气体,选用的装置依次是_____ ( 填编号);
2
(5)二氧化硫气体是一种有刺激性气味的有毒气体,实验室制取SO 气体时需进行尾气处理,应选择的装置
2
是_______(填编号)。
13. 某化学兴趣小组 在学习酸碱中和反应实验时,进行了如下探究。
I.探究酸和碱能否发生反应
甲同学向盛有少量KOH溶液的试管中滴几滴无色酚酞试液,振荡,继续加入稀硫酸,观察到溶液由_____
色变成无色。甲同学得出结论:酸和碱能发生反应。
请写出稀硫酸和氢氧化钾溶液反应的化学方程式__________。
II.探究酸和碱反应后溶液中溶质的成分
乙同学对探究I中甲同学实验后的无色溶液展开探究。
【提出问题】试管中无色溶液的溶质除了酚酞还有什么?
【提出猜想】(1) KSO ;(2) KSO 和_______
2 4 2 4
【设计实验】
方 实验
实验操作 实验现象及方程式
案 结论
方 向试管中加入少量碳酸钠,然后加入过量甲同学 可观察到溶液中有_______产生,化学 猜想
案1 实验后的无色溶液。 反应方程式为_____ (2)
方
用玻璃棒蘸取少量反应后的溶液滴在pH试纸上。 ______________。 成立
案2
方 向试管中加入少量甲同学实验后的无色溶液, 开始无明显现象,过一会发现
案3 然后慢慢滴加NaOH溶液,并不断振荡试管。 __________。
【发散思维】为了验证猜想(2)成立,你认为还可以选择的物质是_____(填选项)。A.Ba(NO ) B.锌粒 C.Cu D.盐酸
3 2
14. 化学实验小组同学为研究某公共场所铁制护栏锈蚀的程度,将12.8g已生锈的铁片,放入一定浓度的稀
盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如下图所示(假设铁片除有Fe O 外,不含其他
2 3
杂质)。
(1)生成氢气的质量为________g;
(2)所用稀盐酸中溶质的质量分数为________;
(3)计算该铁片中Fe O 的质量分数为? (写出计算过程)。
2 3