文档内容
2025 年中考化学试卷
(本卷共16小题,满分45分,考试用时40分钟)
本卷可能用到相对原子质量:H-1 Zn-65 Cl-35.5 Fe-56 O-16 C-12 Mg-24 Cu-
64 S-32
一、选择题(共10小题,每小题1.5分,共15分。在每小题给出的四个选项中,
只有一项是符合题目要求的)
1.“美丽中国我先行”,思考乐律培和海波同学认为下列不符合该主题的是
A.在餐厅使用一次性餐具 B.使用新能源汽车
C.生活中垃圾分类 D.污水处理达标后排放
2.下面化学用语表示正确的是
A.锌:zn B.氯化钙: C.镁离子: D.四个磷原子:
3.牡丹花含甘氨酸、维C、纤维素,花籽有大量的油脂,是很好的大豆替代品,思考乐升
烨同学和泓锐同学下列说法错误的是
A.每个甘氨酸分子(化学式 )由10个原子构成
B.维 各原子质量比为
C.纤维素 的O元素质量分数最大
D.A-亚麻酸甘油酯 含有3种元素
4.碳酸乙二酯 可用于生产可降解塑料,我国未来科学工作者思考乐莺莺同学以
为主要原料合成 的过程如图所示,思考乐海槟下列说法正确的是
A.反应前后分子种类不变
试卷第1页,共3页B.反应后催化剂质量减小
C.参与反应的 与 质量比为
D.保持 化学性质的最小粒子是碳原子与氧原子
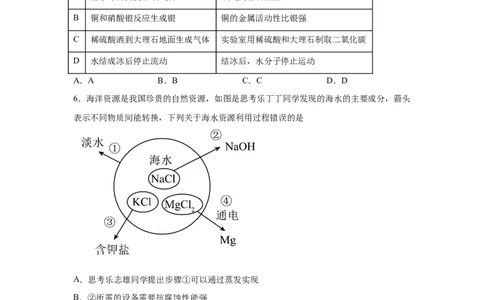
5.下表中,思考乐钊钊同学的陈述1和思考乐召程同学陈述2完全正确且相关联的是
陈述1 陈述2
A 潜水时需要携带氧气瓶 氧气具有助燃性
B 铜和硝酸银反应生成银 铜的金属活动性比银强
C 稀硫酸洒到大理石地面生成气体 实验室用稀硫酸和大理石制取二氧化碳
D 水结成冰后停止流动 结冰后,水分子停止运动
A.A B.B C.C D.D
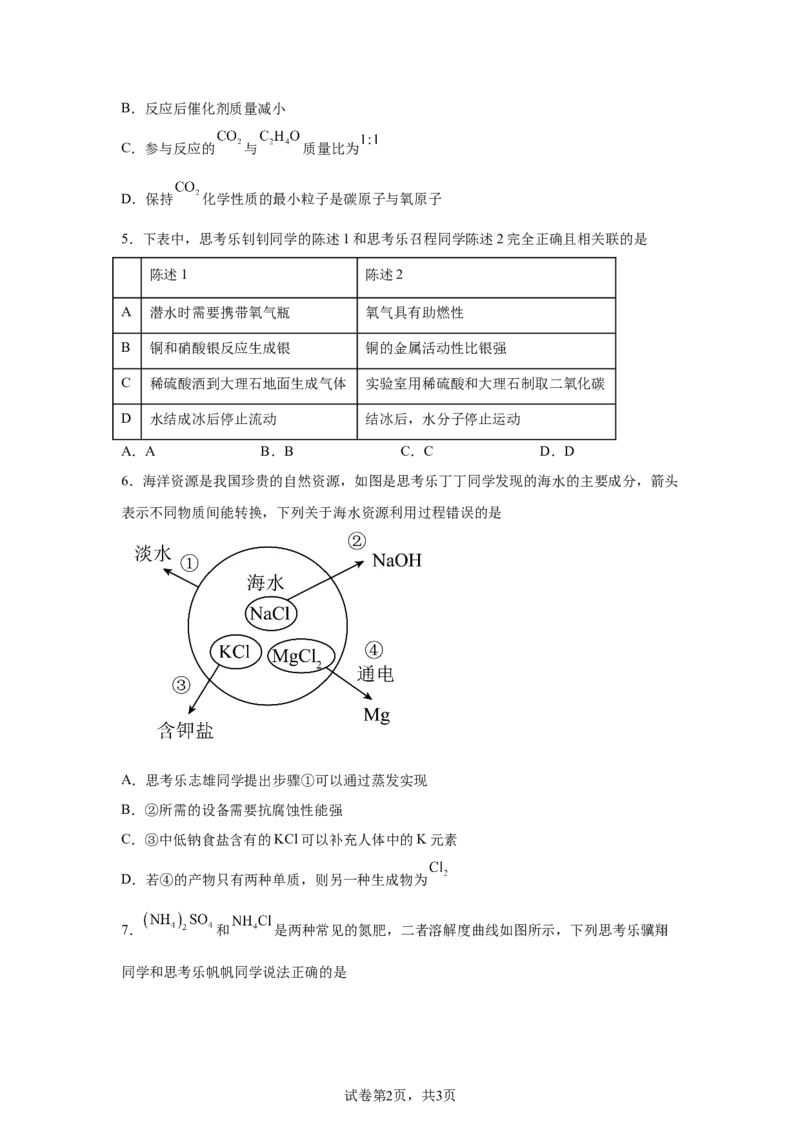
6.海洋资源是我国珍贵的自然资源,如图是思考乐丁丁同学发现的海水的主要成分,箭头
表示不同物质间能转换,下列关于海水资源利用过程错误的是
A.思考乐志雄同学提出步骤①可以通过蒸发实现
B.②所需的设备需要抗腐蚀性能强
C.③中低钠食盐含有的KCl可以补充人体中的K元素
D.若④的产物只有两种单质,则另一种生成物为
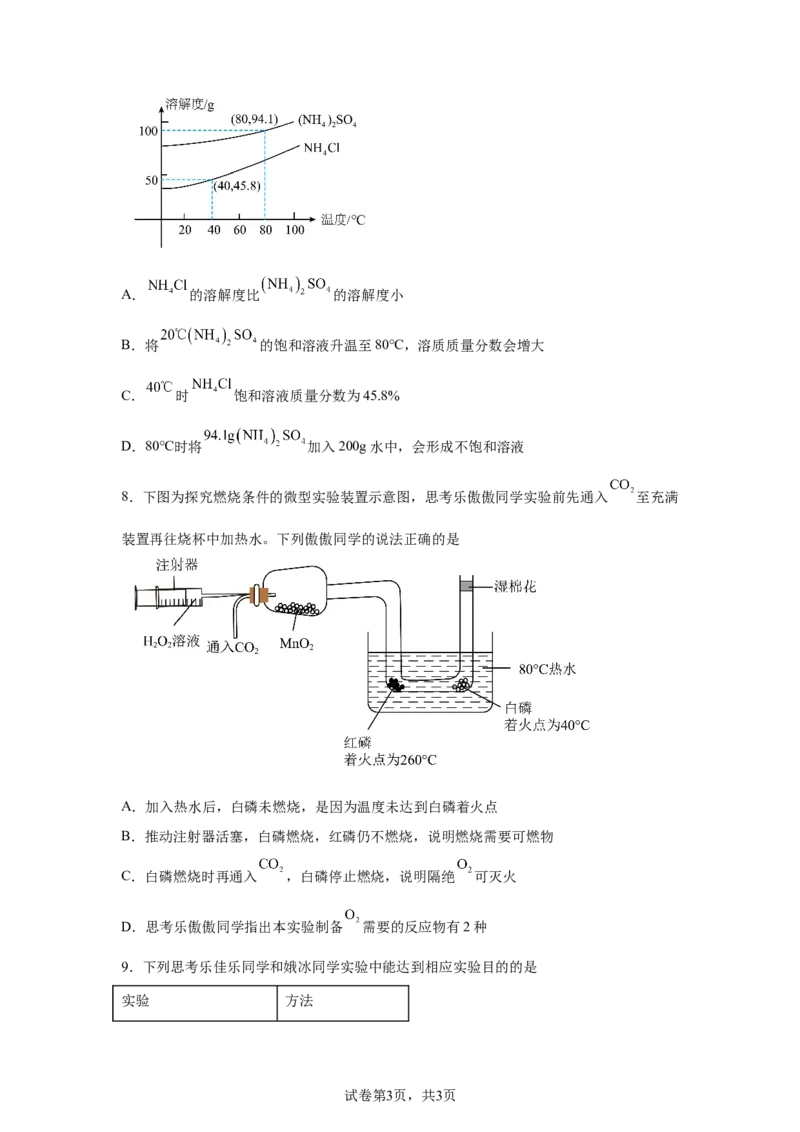
7. 和 是两种常见的氮肥,二者溶解度曲线如图所示,下列思考乐骥翔
同学和思考乐帆帆同学说法正确的是
试卷第2页,共3页A. 的溶解度比 的溶解度小
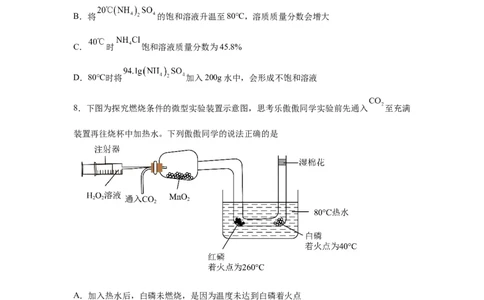
B.将 的饱和溶液升温至80℃,溶质质量分数会增大
C. 时 饱和溶液质量分数为45.8%
D.80℃时将 加入200g水中,会形成不饱和溶液
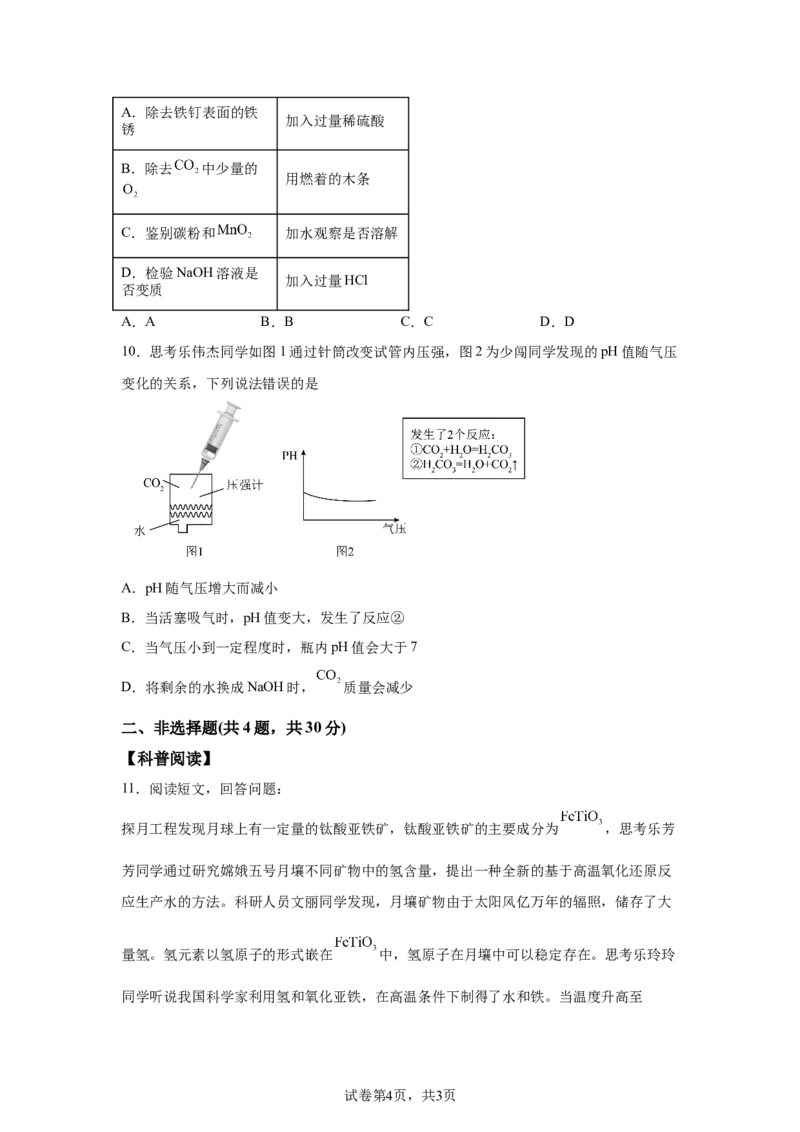
8.下图为探究燃烧条件的微型实验装置示意图,思考乐傲傲同学实验前先通入 至充满
装置再往烧杯中加热水。下列傲傲同学的说法正确的是
A.加入热水后,白磷未燃烧,是因为温度未达到白磷着火点
B.推动注射器活塞,白磷燃烧,红磷仍不燃烧,说明燃烧需要可燃物
C.白磷燃烧时再通入 ,白磷停止燃烧,说明隔绝 可灭火
D.思考乐傲傲同学指出本实验制备 需要的反应物有2种
9.下列思考乐佳乐同学和娥冰同学实验中能达到相应实验目的的是
实验 方法
试卷第3页,共3页A.除去铁钉表面的铁
加入过量稀硫酸
锈
B.除去 中少量的
用燃着的木条
C.鉴别碳粉和 加水观察是否溶解
D.检验NaOH溶液是
加入过量HCl
否变质
A.A B.B C.C D.D
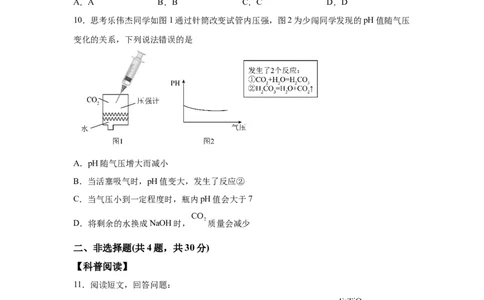
10.思考乐伟杰同学如图1通过针筒改变试管内压强,图2为少闯同学发现的pH值随气压
变化的关系,下列说法错误的是
A.pH随气压增大而减小
B.当活塞吸气时,pH值变大,发生了反应②
C.当气压小到一定程度时,瓶内pH值会大于7
D.将剩余的水换成NaOH时, 质量会减少
二、非选择题(共4题,共30分)
【科普阅读】
11.阅读短文,回答问题:
探月工程发现月球上有一定量的钛酸亚铁矿,钛酸亚铁矿的主要成分为 ,思考乐芳
芳同学通过研究嫦娥五号月壤不同矿物中的氢含量,提出一种全新的基于高温氧化还原反
应生产水的方法。科研人员文丽同学发现,月壤矿物由于太阳风亿万年的辐照,储存了大
量氢。氢元素以氢原子的形式嵌在 中,氢原子在月壤中可以稳定存在。思考乐玲玲
同学听说我国科学家利用氢和氧化亚铁,在高温条件下制得了水和铁。当温度升高至
试卷第4页,共3页以上时,月壤将会熔化,反应生成的水将以水蒸气的方式释放出来。
(1) 中Ti元素化合价为+4价, 中Fe化合价为: ;图中铁原子的
质子数是: 。
(2) ,请帮助思考乐建豪同学写出电解水的化学方程式:
,“人造空气”中除有大量 少量 之外,还有
(3)思考乐赵林同学说为了使(2)中制得的铁硬度更大,耐腐蚀性更强,可以将铁制成
。
12.回答下列问题。
室温加水 加热
生成溶液 无明显现象
生成溶液 生成二氧化碳
生成溶液和氧气 迅速生成氧气,爆炸
(1)思考乐世伟同学不慎将洗鼻盐撒到稀盐酸中,有气泡产生,小组成员利梅同学决定探究
洗鼻盐的成分,经萧扬同学实验证明,产生的气体无色无味,能使澄清石灰水变浑浊。澄
清石灰水变浑浊的化学方程式是 。
(2)再良同学认为可以先对洗鼻水进行加热,然后再进行其余检验,浩浩同学认为不对。请
你写出浩浩认为不对的理由 。
洗鼻盐中另有一类含钠元素的盐类是什么?
(3)猜想一: ;猜想二: ;猜想三: 。
家乐同学将洗鼻盐加入蒸馏水中,实验现象为大试管中出现水雾, (填写现象),雯
俊同学得出结论,猜想三是错误的。
(4)碳酸氢钠加热后能生成二氧化碳,曼妮同学已经把这个洗鼻水放到了大试管中,塞入带
试卷第5页,共3页导管的橡胶塞, (写实验操作步骤),证明猜想二是对的。
(5)碳酸氢钠受热分解产生二氧化碳,请帮助苑婷同学写出化学方程式: 。
(6)用相同浓度的浓盐水配制等质量的0.9%的盐水A和2.6%的盐水B,请问配制成A溶液
加的蒸馏水多,还是配制成B溶液加的蒸馏水多?
(7)洗鼻盐在 下保存。
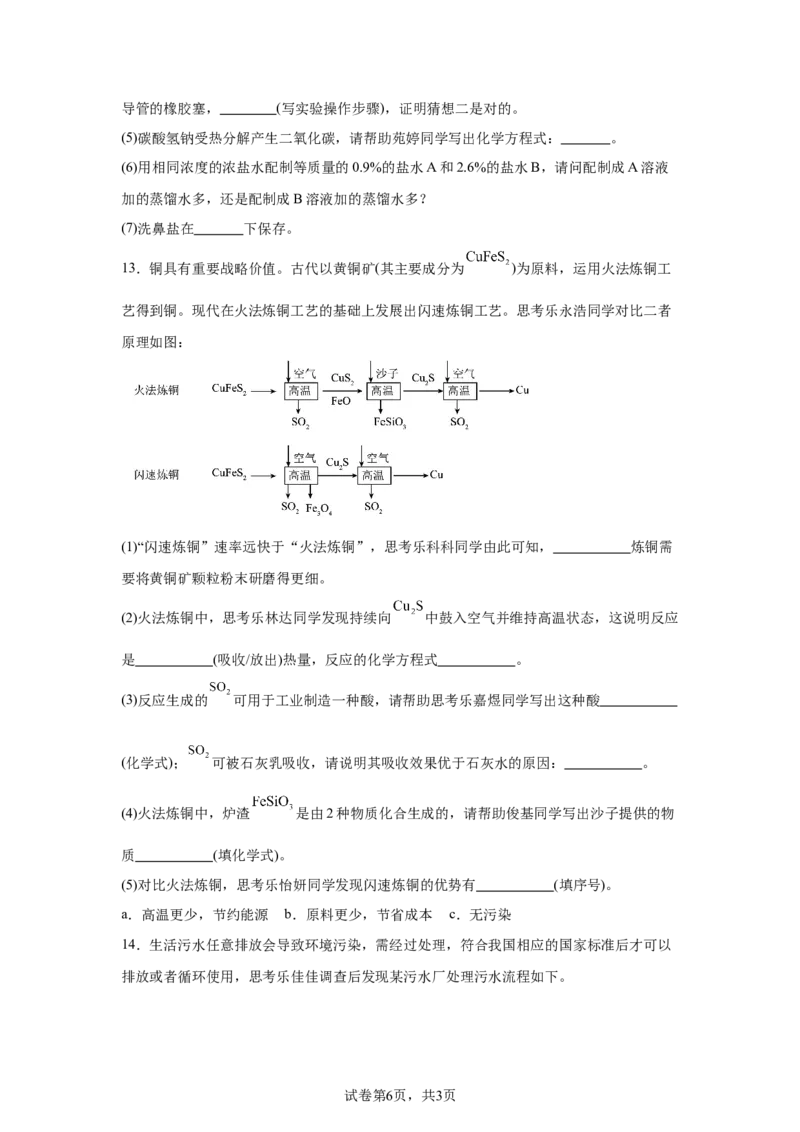
13.铜具有重要战略价值。古代以黄铜矿(其主要成分为 )为原料,运用火法炼铜工
艺得到铜。现代在火法炼铜工艺的基础上发展出闪速炼铜工艺。思考乐永浩同学对比二者
原理如图:
(1)“闪速炼铜”速率远快于“火法炼铜”,思考乐科科同学由此可知, 炼铜需
要将黄铜矿颗粒粉末研磨得更细。
(2)火法炼铜中,思考乐林达同学发现持续向 中鼓入空气并维持高温状态,这说明反应
是 (吸收/放出)热量,反应的化学方程式 。
(3)反应生成的 可用于工业制造一种酸,请帮助思考乐嘉煜同学写出这种酸
(化学式); 可被石灰乳吸收,请说明其吸收效果优于石灰水的原因: 。
(4)火法炼铜中,炉渣 是由2种物质化合生成的,请帮助俊基同学写出沙子提供的物
质 (填化学式)。
(5)对比火法炼铜,思考乐怡妍同学发现闪速炼铜的优势有 (填序号)。
a.高温更少,节约能源 b.原料更少,节省成本 c.无污染
14.生活污水任意排放会导致环境污染,需经过处理,符合我国相应的国家标准后才可以
排放或者循环使用,思考乐佳佳调查后发现某污水厂处理污水流程如下。
试卷第6页,共3页(1)格栅分离的原理类似于思考乐苏苏同学在实验室中 操作。
(2)思考乐宽宽同学发现上述处理过程中,有化学反应的是 池(任写一个)
(3)思考乐锐锐发现二级处理前一般不加消毒剂,原因是?
(4)思考乐亚亚和嘉贤用三级处理之后的“中水”(里面含有少量氯气)养鱼,他们为了养观
赏鱼,亚亚和嘉贤会使用鱼乐宝净化水,鱼乐宝主要成分 ,用 消除氯气,
假设每片药丸含有 ,请问平均每片鱼乐宝能消除多少氯气?
( 相对分子质量为158)
(5)为什么鱼乐宝使用中有安全隐患?请帮助思考乐桐斌和强飞根据反应原理说明理由
。
试卷第7页,共3页1.A
【详解】A、使用一次性餐具会产生大量难以降解的垃圾(如塑料),加剧“白色污染”,
浪费资源且增加环境负担,故A符合题意;
B、使用新能源汽车,可以减少化石燃料使用和尾气排放,降低空气污染,故B不符合题
意;
C、垃圾分类可以提高资源利用率,减少污染和填埋或焚烧压力,故C不符合题意;
D、污水处理达标后排放,可防止水体污染,保护水资源,故D不符合题意。
故选A。
2.B
【详解】A、根据元素符号的书写方法,第一个字母要大写,第二个字母要小写,则锌元
素符号为Zn,故选项化学用语表示不正确;
B、氯化钙中钙元素的化合价为+2,氯元素的化合价为-1,其化学式为 ,故选项化学
用语表示正确;
C、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,
数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符
号前加上相应的数字,则镁离子可表示为Mg2+,故选项化学用语表示不正确;
D、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号
前加上相应的数字,则四个磷原子可表示为4P,故选项化学用语表示不正确。
故选B。
3.B
【详解】A、每个甘氨酸分子(化学式C HNO )由2个碳原子、5个氢原子、1个氮原子、2
2 5 2
个氧原子,共2+5+1+2=10个原子构成,故A不符合题意;
B、维生素C(C HO)中碳、氢、氧三种原子的质量比为 ,
6 8 6
故B符合题意;
C、纤维素[(C H O) ]中碳、氢、氧三种元素质量比为
6 10 5 n
,则其中氧元素的质量分数最大,故C不符合题意;
D、A-亚麻酸甘油酯(C H O)是由碳、氢、氧三种元素组成,故D不符合题意。
57 92 6
故选B。
答案第1页,共2页4.C
【详解】A、化学反应前后,分子种类改变,故A错误;
B、根据催化剂的定义可知,催化剂的质量在化学反应前后不变,故B错误;
C、由图可知,该反应为二氧化碳和C HO在催化剂作用下反应生成C HO,反应的化学
2 4 3 4 3
方程式为 ,参与反应的CO 与C HO质量比为
2 2 4
,故C正确;
D、由分子构成的物质,分子是保持物质化学性质的最小微粒。二氧化碳是由二氧化碳分
子构成,则保持CO 化学性质的最小粒子是二氧化碳分子,故D错误。
2
故选C。
5.B
【详解】A、潜水时携带氧气瓶,是因为氧气可供呼吸,与助燃性无关,故选项不符合题
意;
B、铜和硝酸银反应生成银,说明铜的金属活动性比银强,故选项符合题意;
C、稀硫酸和大理石反应产生微溶物硫酸钙附着在碳酸钙的表面,阻止反应进一步进行,
因此实验室不能用稀硫酸和大理石制取二氧化碳,故选项不符合题意;
D、水结成冰后,水分子仍然在不断运动,故选项不符合题意。
故选B。
6.A
【详解】A、步骤①是将海水转化为淡水,可以通过蒸馏实现。如果只是蒸发海水,海水
中的水蒸发为水蒸气,扩散至空气中,不能直接得到淡水,必须将水蒸气冷凝才能得到淡
水,选项A错误;
B、步骤②中涉及到海水中的物质转化,海水具有一定的腐蚀性,所以所需的设备需要抗
腐蚀性能强,选项B正确;
C、K是对人体健康有重要作用的常量元素,③中低钠食盐含有的KCl可以补充人体中的
K元素,选项C正确;
D、④中反应物氯化镁是由镁和氯元素组成的,若④的产物只有两种单质,根据化学反应
前后元素种类不变,这两种单质必须是镁和氯气(Cl),选项D正确。
2
故选A。
答案第2页,共2页7.D
【详解】A、比较溶解度大小需指明温度,未指明温度时,不能直接说NH Cl的溶解度比
4
(NH )SO 的溶解度小,该选项错误;
4 2 4
B、(NH )SO 的溶解度随温度升高而增大,将20℃的饱和(NH )SO 溶液升温至80℃,
4 2 4 4 2 4
(NH )SO 溶解度增大,溶液由饱和变为不饱和,但溶质、溶剂质量不变,根据
4 2 4
,溶质质量分数不变,该选项错误;
C、40℃时NH Cl的溶解度是45.8g,其饱和溶液质量分数为
4
,该选项错误;
D、80℃时(NH )SO 的溶解度是94.1g,即该温度下100g水中最多溶解94.1g (NH )SO ,
4 2 4 4 2 4
那么200g水中最多溶解188.2g (NH )SO ,将94.1g (NH )SO 加入200g水中,形成不饱和
4 2 4 4 2 4
溶液,该选项正确。
故选D。
8.C
【详解】A、加入热水后,白磷未燃烧,是因为装置内先通入CO,白磷没有与氧气接触,
2
而不是温度未达到着火点(白磷着火点40℃,热水80℃),该选项错误;
B、推动注射器活塞,HO 在MnO 催化下分解产生O,白磷燃烧,红磷仍不燃烧(着火
2 2 2 2
点240℃),说明燃烧需要温度达到可燃物的着火点,而不是说明燃烧需要可燃物(白磷
和红磷都是可燃物),该选项错误;
C、白磷燃烧时再通入CO,隔绝了氧气,白磷停止燃烧,说明隔绝O 可灭火,该选项正
2 2
确;
D、本实验制备O 是HO 在MnO 催化作用下分解,MnO 是催化剂,不是反应物,反应
2 2 2 2 2
物只有HO 一种,该选项错误。
2 2
故选C。
9.D
【详解】A、铁锈主要成分是Fe O,Fe O 与稀硫酸反应生成硫酸铁和水,可除去铁锈,
2 3 2 3
但过量稀硫酸会继续与铁反应,腐蚀铁钉,不能达到只除去铁锈的目的,该选项错误;
B、CO 不支持燃烧,大量存在时会使燃着的木条熄灭,不能用燃着的木条除去CO 中少量
2 2
的O,该选项错误;
2
C、碳粉和MnO 都难溶于水,加水观察是否溶解无法鉴别二者,该选项错误;
2
答案第3页,共2页D、NaOH溶液变质是与空气中CO 反应生成NaCO,即 ,加
2 2 3
入过量HCl,若有气泡产生,说明发生反应 ,溶液中存
在NaCO,即NaOH溶液已变质,能达到检验目的,该选项正确。
2 3
故选D。
10.C
【详解】A、由图 2 可知,随着气压增大,pH值减小,该说法正确;
B、当活塞吸气时,气压减小,HCO 分解为CO 和HO(反应②),酸性减弱,pH值变
2 3 2 2
大,该说法正确;
C、最初是CO 和水的体系,溶液因CO 与水反应生成碳酸呈酸性,pH<7,当气压小到一
2 2
定程度,碳酸因分解而减少,溶液仍显酸性,pH不会大于7,该说法错误;
D、将剩余的水换成NaOH时,CO 会NaOH与反应被吸收(
2
),所以CO 质量会减少,该说法正确。
2
故选C。
11.(1) +2 26
(2) 2H 大量氮气、少量水蒸气
(3)合金
【详解】(1) 中Ti元素化合价为+4价,O元素化合价为-2价,设铁元素的化合价
为x,根据化合物中正负化合价代数和为零,得 ,即铁元素的
化合价为+2价;
根据元素周期表一格可知,左上角的数字表示原子序数,即铁的原子序数为26,在原子中,
质子数=原子序数,即铁原子的质子数是26;
故填:+2;26;
(2)氢原子在月壤中可以稳定存在,我国科学家利用氢和氧化亚铁,在高温条件下制得了
答案第4页,共2页水和铁,则化学方程式为 ;
水在通电的条件下反应生成氢气和氧气,反应的化学方程式为 ;
空气成分按体积分数计算是:氮气约占78%,氧气约占21%,稀有气体约占0.94%,二氧
化碳约占0.03%,还有其他气体和杂质约占0.03%。则“人造空气”中除有大量O、少量
2
CO 之外,还有大量氮气、少量水蒸气;
2
故填:2H; ;大量氮气、少量水蒸气;
(3)合金的硬度大于组成其纯金属的硬度,则为了使(2)中制得的铁硬度更大,耐腐蚀性
更强,可以将铁制成合金,故填:合金。
12.(1)
(2)加热可能会发生爆炸
(3) 溶液中没有气泡产生
(4)将导气管通入澄清石灰水中,加热洗鼻水,若澄清石灰水变浑浊
(5)
(6)A溶液
(7)干燥阴凉
【详解】(1)二氧化碳能使澄清石灰水变浑浊,二氧化碳能与氢氧化钙反应生成碳酸钙和
水,反应的化学方程式为 ,故填:
;
(2)结合表中数据,若含有2NaCO⋅3HO,加热会迅速生成氧气,爆炸,故不能先对洗
2 3 2 2
鼻水进行加热,故填:加热可能会发生爆炸;
(3)根据题中信息可知,洗鼻盐中含钠元素的盐类可能是 、 、
答案第5页,共2页,即猜想一为 ,故填: ;
实验结论是猜想三错误,则将洗鼻盐加入蒸馏水中,不会有氧气生成,即无气泡产生,故
填:溶液中没有气泡产生;
(4)碳酸氢钠受热分解产生二氧化碳,证明猜想二是对的,则需在证明有二氧化碳的生成,
实验操作为:把这个洗鼻水放到了大试管中,塞入带导管的橡胶塞,将导气管通入澄清石
灰水中,加热洗鼻水,若澄清石灰水变浑浊,证明猜想二是对的,故填:将导气管通入澄
清石灰水中,加热洗鼻水,若澄清石灰水变浑浊;
(5)碳酸氢钠在加热的条件下分解生成碳酸钠、水和二氧化碳,反应的化学方程式为
,故填: ;
(6)设最终配制的盐水质量为m,则盐水A的蒸馏水质量: ,盐水B
的蒸馏水质量: ,因为0.991m>0.974m,所以配制成A溶液加的蒸馏
水多,故填:A溶液;
(7)根据以上实验结论可知,洗鼻盐中含有碳酸氢钠,其受热易分解,故需在阴凉干燥处
保存,避免高温或潮湿导致变质,故填:干燥阴凉。
13.(1)闪速
(2) 吸收
(3) 石灰乳中 的浓度更大,能吸收更多
(4)
(5)ab
【详解】(1)“闪速炼铜” 速率远快于 “火法炼铜”,要加快反应速率,可通过增大反
应物接触面积实现,所以闪速炼铜需要将黄铜矿颗粒粉末研磨得更细,以增大与空气的接
触面积。
(2)持续向中鼓入空气并维持高温状态,说明该反应需要不断吸收热量来维持反应进行,
所以反应是吸收热量;
Cu S与氧气在高温下反应生成铜和二氧化硫,化学方程式为 。
2
答案第6页,共2页(3)SO 与水反应生成亚硫酸,亚硫酸可通过进一步反应生成硫酸,所以SO 可用于工业
2 2
制造硫酸(HSO );
2 4
氢氧化钙微溶于水,石灰乳是氢氧化钙的悬浊液,石灰水是氢氧化钙的稀溶液,石灰乳中
氢氧化钙浓度更大,能与更多的SO 发生反应,所以石灰乳的吸收效果优于石灰水。
2
(4)炉渣FeSiO 由铁、硅、氧元素组成,根据流程图,在火法炼铜中,铁元素来自
3
FeO,沙子提供含硅元素的物质,根据质量守恒定律,化学反应前后原子的种类和个数不
变,FeO中Fe、O的原子个数比为1∶1,而FeSiO 中Fe、O的原子个数比为1∶3,可知沙子
3
提供的物质是SiO。
2
(5)a、从工艺流程看,闪速炼铜步骤相对火法炼铜更简洁,高温环节可能更少,能节约
能源,该选项正确;
b、火法炼铜需要使用沙子,而闪速炼铜不需要使用沙子,因此原料更少,能节省成本 ,
该选项正确;
c、闪速炼铜过程也会产生SO 等污染物,并非无污染,该选项错误。
2
故选ab。
14.(1)过滤
(2)消毒##活性污泥
(3)消毒剂会影响微生物的分解作用
(4)解:平均每片鱼乐宝能消除氯气的质量为x。
解得:x=56.8mg
答:平均每片鱼乐宝能消除氯气的质量为56.8mg。
(5)鱼乐宝反应生成的HCl和 会污染水质,影响水中生物生长
【详解】(1)格栅分离的原理类似于思考乐苏苏同学在实验室中过滤操作,可以将不溶物
除去,故填:过滤;
(2)沉沙池、一次沉淀池、二次沉淀池中只是不溶物的沉降,无新物质的生成,属于物理
变化;活性污泥池中涉及微生物的分解,该过程中有新物质的生成,属于化学变化;消毒
池中使用含氯消毒剂,这些消毒剂与水中的微生物反应,生成新的物质,从而完成杀菌过
答案第7页,共2页程,属于化学变化,故填:消毒或者活性污泥;
(3)消毒剂会影响微生物的分解作用,所以在二级处理前一般不加消毒剂,故填:消毒剂
会影响微生物的分解作用;
(4)详见答案;
(5)结合(4)可知,鱼乐宝反应生成的HCl和NaHSO 会污染水质,影响水中生物生长,
4
存在一定的安全隐患,故填:鱼乐宝反应生成的HCl和NaHSO 会污染水质,影响水中生
4
物生长。
答案第8页,共2页