文档内容
2019年云南省昆明市初中学业水平考试化学试题卷
(全卷四个大题,共28个小题;满分100分,考试时间90分钟)
可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 Sr—88
第Ⅰ卷(共45分)
一、选择题(本大题共20个小题,其中第1~15小题,每小题2分,第16~20小题,每小题3分,共45分。每小
题只有一个选项符合题意,多选、错选或不选均不得分)
1.下列属于物理变化的是
A.西瓜榨汁 B.粮食酿酒 C.铜锅生锈 D.面包变质
2.下列属于纯净物的是
A.加碘食盐 B.豆浆 C.酱油 D.冰
3.NHHCO 属于
4 3
A.氮肥 B.钾肥 C.磷肥 D.复合肥
4.把少量下列物质分别放入水中,充分搅拌,不能得到溶液的是
A.冰糖 B.味精 C.芝麻油 D.葡萄糖
5.下列属于合成有机高分子材料的是
A.羊毛 B.涤纶 C.不锈钢 D.混凝土
6.下列有关广告词说法正确的是
A.某美容仪广告词——我们能将水分子变小
B.某食品广告词——纯绿色,无化学物质,不含化学添加剂
C.某化妆品广告词——我们专注自然护肤,不含任何化学成分
D.某矿泉水广告词——呈弱碱性,含钾、钙、钠、镁等多种人体所需的元素
7.云南盛产野生菌,我们能闻到某些野生菌散发出的特殊香味,是因为
A.分子之间有间隔 B.分子在不断运动
C.分子的体积和质量都很小 D.分子可以再分
8.氟元素与硅元素最本质的区别是
A.相对原子质量不同 B.中子数不同
C.中子数与核外电子数之和不同 D.质子数不同
9.小林同学某天中午的食谱:红烧肉、米饭、炸鸡块、牛奶,从营养均衡的角度分析,还需要补充的食物是
A.烤鸭 B.白菜汤 C.馒头 D.荷包蛋
10.稀土是储量较少的一类金属的统称,有“工业的维生素”的美誉。铕(Eu)是稀土元素中化学性质最活
泼的元素,EuO 中铕元素的化合价为
2 3
A.+1 B.+2 C.+3 D.+4
11.2019年是门捷列夫发表元素周期表150周年。为纪念门捷列夫,将在1955年发现的一种新元素命名为
“钔”,其在元素周期表中的有关信息如图所示,有关钔的说法错误的是
A.属于金属元素
B.元素符号是Md 101 Md
钔
C.原子序数是101
258
D.相对原子质量是258g
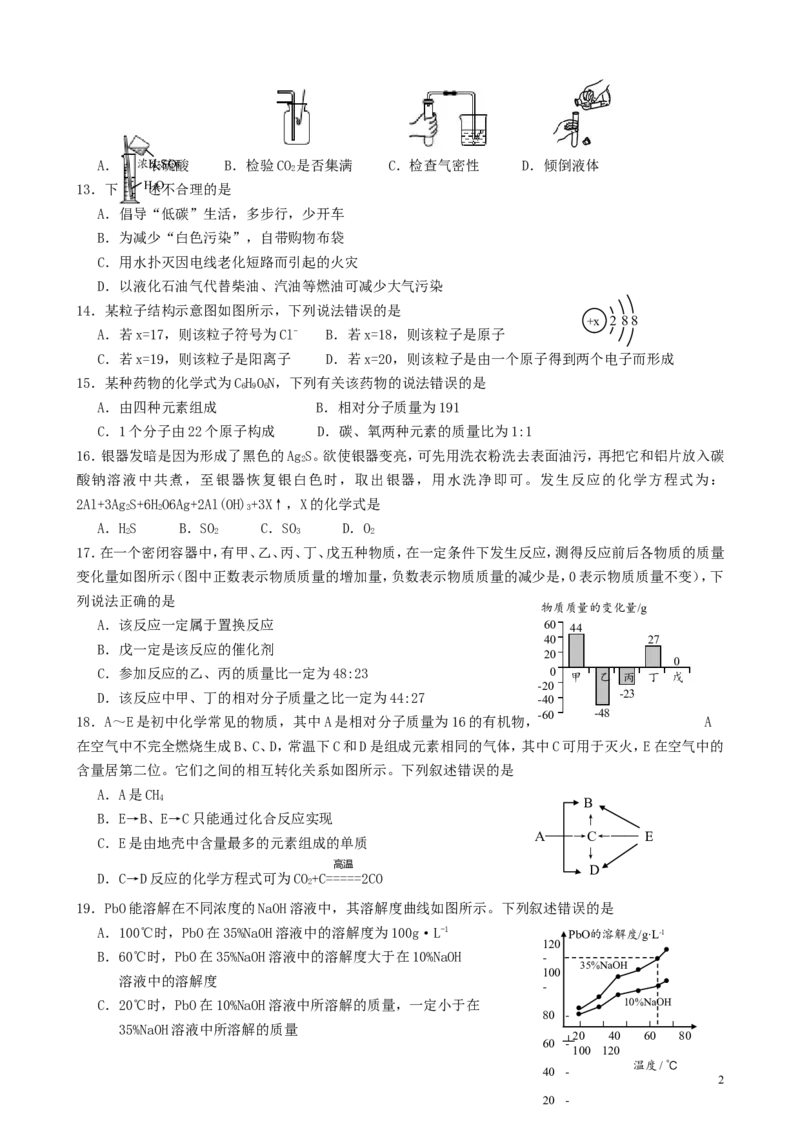
12.下列图示的实验操作中正确的是
1A.稀释浓浓HS硫O酸 B.检验CO 是否集满 C.检查气密性 D.倾倒液体
2 4 2
13.下列叙H述2 O不合理的是
A.倡导“低碳”生活,多步行,少开车
B.为减少“白色污染”,自带购物布袋
C.用水扑灭因电线老化短路而引起的火灾
D.以液化石油气代替柴油、汽油等燃油可减少大气污染
14.某粒子结构示意图如图所示,下列说法错误的是
+x 288
A.若x=17,则该粒子符号为Cl- B.若x=18,则该粒子是原子
C.若x=19,则该粒子是阳离子 D.若x=20,则该粒子是由一个原子得到两个电子而形成
15.某种药物的化学式为CHON,下列有关该药物的说法错误的是
6 9 6
A.由四种元素组成 B.相对分子质量为191
C.1个分子由22个原子构成 D.碳、氧两种元素的质量比为1:1
16.银器发暗是因为形成了黑色的AgS。欲使银器变亮,可先用洗衣粉洗去表面油污,再把它和铝片放入碳
2
酸钠溶液中共煮,至银器恢复银白色时,取出银器,用水洗净即可。发生反应的化学方程式为:
2Al+3AgS+6HO6Ag+2Al(OH)+3X↑,X的化学式是
2 2 3
A.HS B.SO C.SO D.O
2 2 3 2
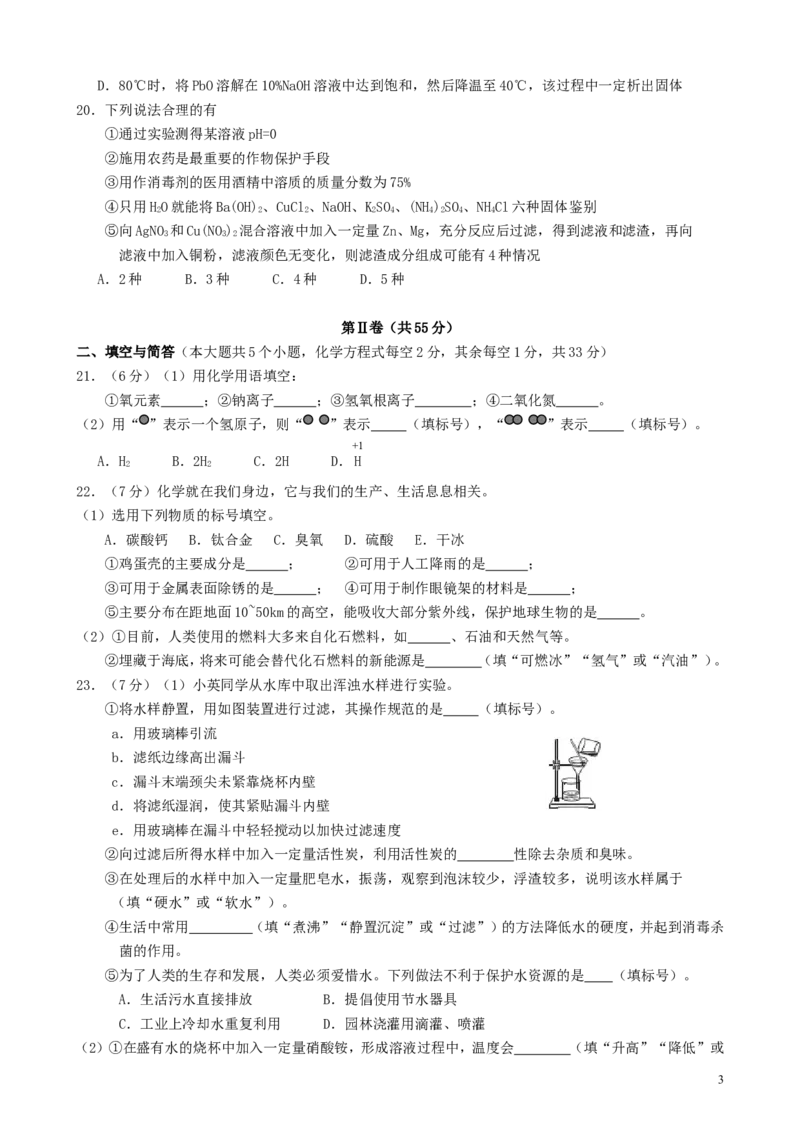
17.在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量
变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少是,0表示物质质量不变),下
列说法正确的是
物质质量的变化量/g
A.该反应一定属于置换反应 60 44
40 27
B.戊一定是该反应的催化剂
20
0
C.参加反应的乙、丙的质量比一定为48:23 0
甲 乙 丙 丁 戊
-20
D.该反应中甲、丁的相对分子质量之比一定为44:27 -40 -23
-60 -48
18.A~E是初中化学常见的物质,其中A是相对分子质量为16的有机物, A
在空气中不完全燃烧生成B、C、D,常温下C和D是组成元素相同的气体,其中C可用于灭火,E在空气中的
含量居第二位。它们之间的相互转化关系如图所示。下列叙述错误的是
A.A是CH
4 B
B.E→B、E→C只能通过化合反应实现 ↑
A——→C←—— E
C.E是由地壳中含量最多的元素组成的单质
↓
高温 D
D.C→D反应的化学方程式可为CO+C=====2CO
2
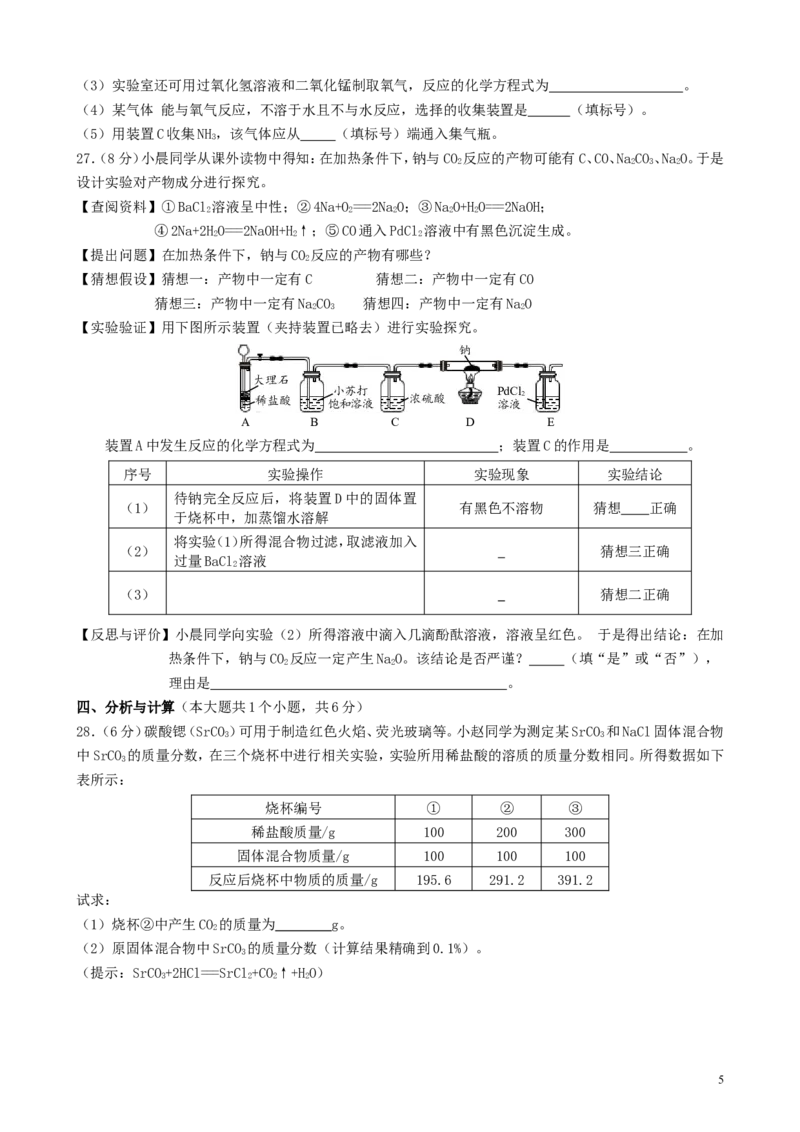
19.PbO能溶解在不同浓度的NaOH溶液中,其溶解度曲线如图所示。下列叙述错误的是
A.100℃时,PbO在35%NaOH溶液中的溶解度为100g·L-1 PbO的溶解度/g·L-1
120
B.60℃时,PbO在35%NaOH溶液中的溶解度大于在10%NaOH -
35%NaOH
100
溶液中的溶解度
-
C.20℃时,PbO在10%NaOH溶液中所溶解的质量,一定小于在 10%NaOH
80 -
35%NaOH溶液中所溶解的质量 ─┴─┴─┴─┴─┴─
20 40 60 80
60 ┴-
100 120
温度/℃
40 -
2
20 -D.80℃时,将PbO溶解在10%NaOH溶液中达到饱和,然后降温至40℃,该过程中一定析出固体
20.下列说法合理的有
①通过实验测得某溶液pH=0
②施用农药是最重要的作物保护手段
③用作消毒剂的医用酒精中溶质的质量分数为75%
④只用HO就能将Ba(OH)、CuCl、NaOH、KSO、(NH)SO、NHCl六种固体鉴别
2 2 2 2 4 4 2 4 4
⑤向AgNO 和Cu(NO) 混合溶液中加入一定量Zn、Mg,充分反应后过滤,得到滤液和滤渣,再向
3 3 2
滤液中加入铜粉,滤液颜色无变化,则滤渣成分组成可能有4种情况
A.2种 B.3种 C.4种 D.5种
第Ⅱ卷(共55分)
二、填空与简答(本大题共5个小题,化学方程式每空2分,其余每空1分,共33分)
21.(6分)(1)用化学用语填空:
①氧元素 ;②钠离子 ;③氢氧根离子 ;④二氧化氮 。
(2)用“ ”表示一个氢原子,则“ ”表示 (填标号),“ ”表示 (填标号)。
+1
A.H B.2H C.2H D.H
2 2
22.(7分)化学就在我们身边,它与我们的生产、生活息息相关。
(1)选用下列物质的标号填空。
A.碳酸钙 B.钛合金 C.臭氧 D.硫酸 E.干冰
①鸡蛋壳的主要成分是 ; ②可用于人工降雨的是 ;
③可用于金属表面除锈的是 ; ④可用于制作眼镜架的材料是 ;
⑤主要分布在距地面10~50km的高空,能吸收大部分紫外线,保护地球生物的是 。
(2)①目前,人类使用的燃料大多来自化石燃料,如 、石油和天然气等。
②埋藏于海底,将来可能会替代化石燃料的新能源是 (填“可燃冰”“氢气”或“汽油”)。
23.(7分)(1)小英同学从水库中取出浑浊水样进行实验。
①将水样静置,用如图装置进行过滤,其操作规范的是 (填标号)。
a.用玻璃棒引流
b.滤纸边缘高出漏斗
c.漏斗末端颈尖未紧靠烧杯内壁
d.将滤纸湿润,使其紧贴漏斗内壁
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
②向过滤后所得水样中加入一定量活性炭,利用活性炭的 性除去杂质和臭味。
③在处理后的水样中加入一定量肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该水样属 于
(填“硬水”或“软水”)。
④生活中常用 (填“煮沸”“静置沉淀”或“过滤”)的方法降低水的硬度,并起到消毒杀
菌的作用。
⑤为了人类的生存和发展,人类必须爱惜水。下列做法不利于保护水资源的是 (填标号)。
A.生活污水直接排放 B.提倡使用节水器具
C.工业上冷却水重复利用 D.园林浇灌用滴灌、喷灌
(2)①在盛有水的烧杯中加入一定量硝酸铵,形成溶液过程中,温度会 (填“升高”“降低”或
3“不变”)。
②用加了洗涤剂的水能洗掉餐具上的油污,这是利用了洗涤剂的 作用。
24.(7分)阅读下列材料。
美丽富饶的云南被誉为“有色金属王国”,其中铝、锌、锡的保有储量居全国第一位,铜、镍的保有储
量居全国第三位,是国家重要的锡、铜生产基地。
我国古代曾用“湿法炼铜”“火法炼铜”。“湿法炼铜”的原理是“曾青(硫酸铜溶液)得铁则化为
铜”;“火法炼铜”中用辉铜矿(主要成分CuS)炼铜的原理是:CuS与氧气在高温条件下反应生成铜和一
2 2
种会导致酸雨的气体(其相对分子质量为64)。
在河南安阳、湖北荆州、湖南宁乡、云南江川等地分别出土了后(司)母戊鼎、越王勾践剑、四羊方尊、牛
虎铜案等青铜文物,充分反映出我国古代青铜器的高超熔铸技艺。青铜是铜锡合金,锡的加入明显提高了铜
的强度,抗腐蚀性增强,因此锡青铜常用于制造齿轮等耐磨零部件和耐蚀配件。
虽然云南有色金属资源丰富,但是矿物的储量有限,而且不能再生,所以保护金属资源刻不容缓。
回答下列问题:
(1)下列在云南出土的文物是 (填标号)。
A.四羊方尊 B.牛虎铜案 C.越王勾践剑 D.后(司)母戊鼎
(2)可用来冶炼锡的矿石是 (填标号)。
A.菱铁矿(主要成分FeCO) B.铝土矿(主要成分AlO)
3 2 3
C.锡石(主要成分SnO) D.黄铜矿(主要成分CuFeS)
2 2
(3)青铜的抗腐蚀性比纯铜的 (填“强”或“弱”)。
(4)本材料中,“湿法炼铜”的化学方程式是 ,“火法炼铜”的化学方程式
是 。
25.(6分)碲(Te)广泛用于彩色玻璃和陶瓷工艺。用某工业废渣(主要含有TeO、少量Ag、Au)为原料制备碲
2
的一种工艺流程如下:
废渣→ → → → →TeO→ → →
\x( 碱浸 ) \x(过滤) \x( 沉碲 ) \x(过滤) \x(酸溶) \x(还原) \x(过滤)
2
→碲
回答下列问题:
(1)类比CO 与NaOH的反应,写出“碱浸”时发生反应的化学方程式: 。
2
(2)滤液1中的两种溶质是HSO 和 (填化学式)。
2 4
(3)上述工艺流程中设计“废渣→……→TeO”的目的是 。
2
(4)“酸溶”后,在TeCl 溶液中通入SO,反应生成碲和初中化学中两种常见的酸,则该反应的化学方
4 2
程式是 。
三、实验与探究(本大题共2个小题,化学方程式每空2分,其余每空1分,共16分)
26.(8分)根据下列装置图回答问题:
a
A B C D
(1)仪器a的名称是 。 c b
(2)实验室用高锰酸钾制取氧气,选择的发生装置是 (填标号),反应的化学方程式为 。
4(3)实验室还可用过氧化氢溶液和二氧化锰制取氧气,反应的化学方程式为 。
(4)某气体 能与氧气反应,不溶于水且不与水反应,选择的收集装置是 (填标号)。
(5)用装置C收集NH,该气体应从 (填标号)端通入集气瓶。
3
27.(8分)小晨同学从课外读物中得知:在加热条件下,钠与CO 反应的产物可能有C、CO、NaCO、NaO。于是
2 2 3 2
设计实验对产物成分进行探究。
【查阅资料】①BaCl 溶液呈中性;②4Na+O===2NaO;③NaO+HO===2NaOH;
2 2 2 2 2
④2Na+2HO===2NaOH+H↑;⑤CO通入PdCl 溶液中有黑色沉淀生成。
2 2 2
【提出问题】在加热条件下,钠与CO 反应的产物有哪些?
2
【猜想假设】猜想一:产物中一定有C 猜想二:产物中一定有CO
猜想三:产物中一定有NaCO 猜想四:产物中一定有NaO
2 3 2
【实验验证】用下图所示装置(夹持装置已略去)进行实验探究。
钠
大理石
小苏打 PdCl
稀盐酸 饱和溶液 浓硫酸 溶液 2
A B C D E
装置A中发生反应的化学方程式为 ;装置C的作用是 。
序号 实验操作 实验现象 实验结论
待钠完全反应后,将装置D中的固体置
(1) 有黑色不溶物 猜想 正确
于烧杯中,加蒸馏水溶解
将实验(1)所得混合物过滤,取滤液加入
(2) 猜想三正确
过量BaCl 溶液
2
(3) 猜想二正确
【反思与评价】小晨同学向实验(2)所得溶液中滴入几滴酚酞溶液,溶液呈红色。 于是得出结论:在加
热条件下,钠与CO 反应一定产生NaO。该结论是否严谨? (填“是”或“否”),
2 2
理由是 。
四、分析与计算(本大题共1个小题,共6分)
28.(6分)碳酸锶(SrCO)可用于制造红色火焰、荧光玻璃等。小赵同学为测定某SrCO 和NaCl固体混合物
3 3
中SrCO 的质量分数,在三个烧杯中进行相关实验,实验所用稀盐酸的溶质的质量分数相同。所得数据如下
3
表所示:
烧杯编号 ① ② ③
稀盐酸质量/g 100 200 300
固体混合物质量/g 100 100 100
反应后烧杯中物质的质量/g 195.6 291.2 391.2
试求:
(1)烧杯②中产生CO 的质量为 g。
2
(2)原固体混合物中SrCO 的质量分数(计算结果精确到0.1%)。
3
(提示:SrCO+2HCl===SrCl+CO↑+HO)
3 2 2 2
52019年云南省昆明市初中学业水平考试
化学试题卷参考答案及评分标准
一、选择题(本大题共20个小题,1~15小题每小题2分,16~20小题每小题3分,共45分)
1~5:ADACB 6~10:DBDBC 11~15:DCCDD 16~20:ACBCC
二、填空与简答(本大题共5个小题,化学方程式每空2分,其余每空1分,共33分)
21.(6分)(1)①O ②Na+ ③OH- ④NO (2)C B
2
22.(7分)(1)①A ②E ③D ④B ⑤C (2)①煤 ②可燃冰
23.(7分)(1)①ad(多选、少选、错选不得分) ②吸附 ③硬水 ④煮沸 ⑤A
(2)①降低 ②乳化
高温
24.(7分)(1)B (2)C (3)强 (4)Fe+CuSO===FeSO+Cu CuS+O=====2Cu+SO
4 4 2 2 2
25.(6分)(1)TeO+2NaOH===NaTeO+HO (2)NaSO
2 2 3 2 2 4
(3)提纯TeO 或除去Ag、Au(合理即可) (4)2SO+TeCl+4HO===4HCl+2HSO+Te↓
2 2 4 2 2 4
三、实验与探究(本大题共2个小题,化学方程式每空2分,其余每空1分,共16分)
26.(8分)(1)试管 (2)A 2KMnOKMnO+MnO+O↑
4 2 4 2 2
(3)2HO2HO+O↑ (4)D (5)c
2 2 2 2
27.(8分)【实验验证】CaCO+2HCl=== CaCl+CO↑+HO 吸收水蒸气(合理即可)
3 2 2 2
(1)一 (2)产生白色沉淀 (3)E中产生黑色沉淀
【反思与评价】否 实验装置中可能有空气,钠与空气中的氧气反应也产生NaO(合理即可)
2
四、分析与计算(本大题共1个小题,共6分)
28.(6分)(1)8.8 1分
(2)解:设SrCO 的质量为x。 与答共1分
3
SrCO + 2HCl=== SrCl + CO↑ + HO
3 2 2 2
148 44
x 8.8g 1分
== x=29.6g 各1分,共2分
混合物中SrCO 的质量分数为:×100%=29.6% 1分
3
6答:原固体混合物中SrCO 的质量分数为29.6%。
3
7