文档内容
期末总复习考点必杀 200 题
选择专练 02(压轴提升 45 题)
一、图像专题
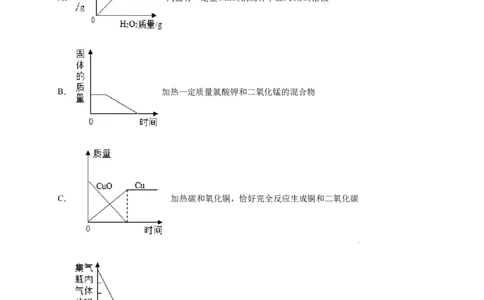
1.下列四个图像,分别对应四种操作,其中正确的是
A. 向盛有一定量MnO 的烧杯中加入HO 溶液
2 2 2
B. 加热一定质量氯酸钾和二氧化锰的混合物
C. 加热碳和氧化铜,恰好完全反应生成铜和二氧化碳
D. 用红磷测定空气中氧气含量
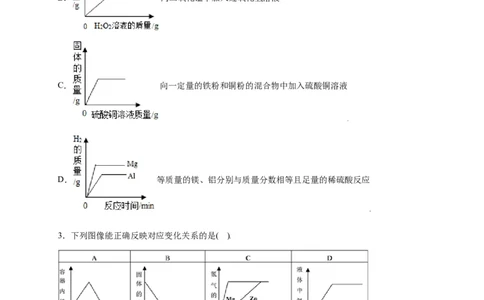
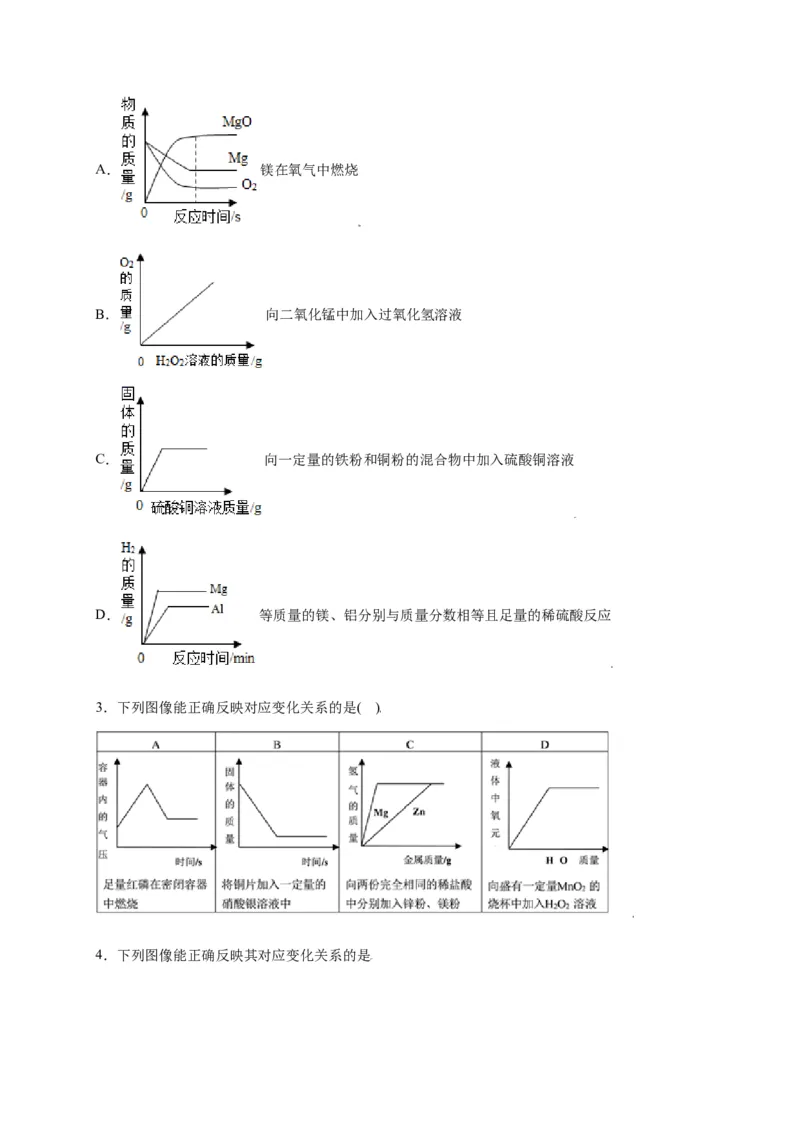
2.下面所示的四个图像,能正确反映对应变化关系的是A. 镁在氧气中燃烧
B. 向二氧化锰中加入过氧化氢溶液
C. 向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液
D. 等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
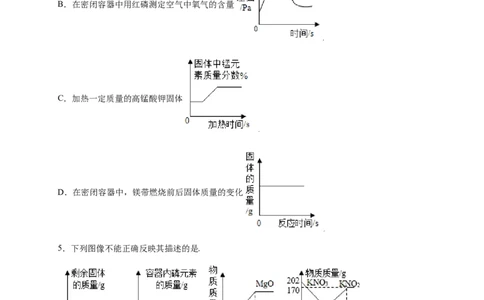
3.下列图像能正确反映对应变化关系的是( )
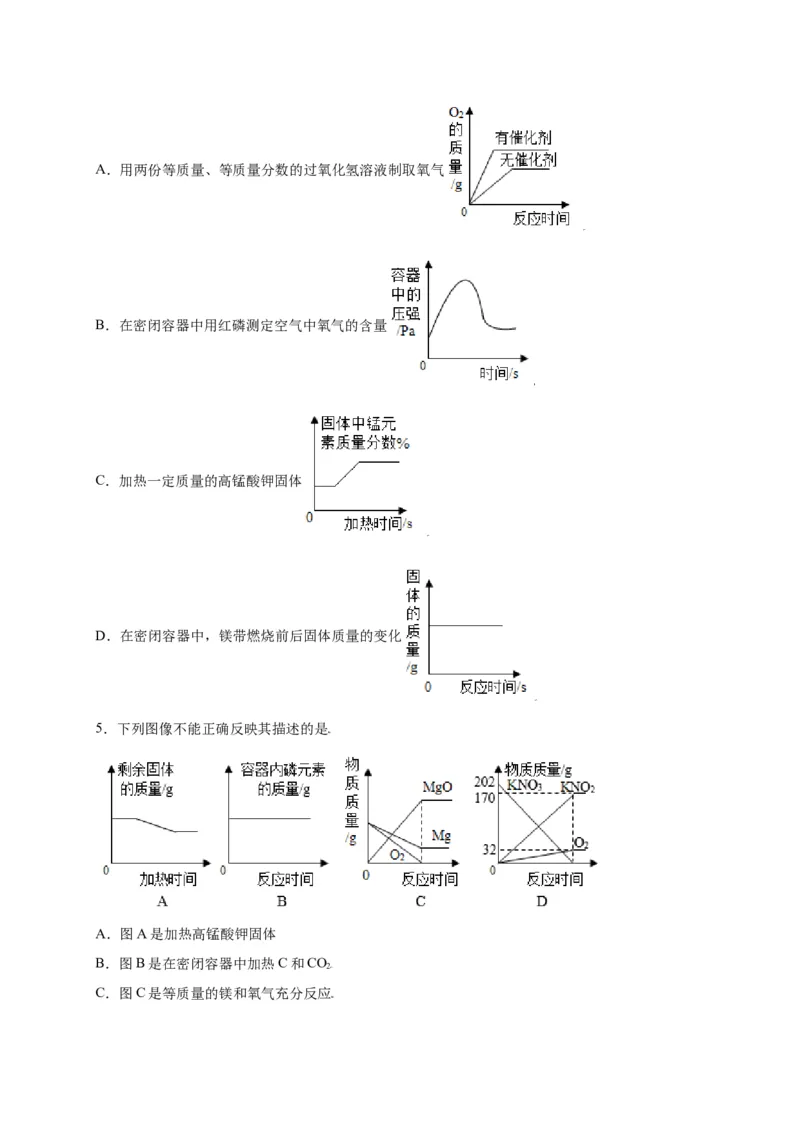
4.下列图像能正确反映其对应变化关系的是A.用两份等质量、等质量分数的过氧化氢溶液制取氧气
B.在密闭容器中用红磷测定空气中氧气的含量
C.加热一定质量的高锰酸钾固体
D.在密闭容器中,镁带燃烧前后固体质量的变化
5.下列图像不能正确反映其描述的是
A.图A是加热高锰酸钾固体
B.图B是在密闭容器中加热C和CO
2
C.图C是等质量的镁和氧气充分反应D.图D是发生的反应
6.下列图像能正确反映对应变化关系的是
D. 等质量的块状石
A.木炭在密闭的容 B.加热一定量的氯酸 灰石和粉末状石灰石分
C.电解水
器内燃烧 钾和二氧化锰固体 别与质量分数相同的足
量的稀盐酸反应
7.将质量相等的铝粉和铁粉分别与同体积、同浓度的稀硫酸反应。反应情况如下图所示。有关叙
述中正确的是
A.铝粉、铁粉和硫酸均有剩余
B.铝粉、铁粉均反应完,硫酸有剩余
C.硫酸、铝粉均反应完,铁粉有剩余
D.硫酸、铁粉均反应完,铝粉有剩余
8.现有等质量甲、乙、丙三种金属,同时放入三份溶质质量分数相同、体积相同的足量稀硫酸中,
产生氢气的质量如下图所示(已知甲、乙、丙在生成物中均为+2价)。下列说法中不正确的是A.生成氢气的质量:甲>乙>丙 B.相对原子质量:乙>丙>甲
C.金属活动性:乙>甲>丙 D.生成溶液的质量:丙>乙>甲
9.两个烧杯中装有等质量的金属锌和镁,分别逐滴滴加同浓度的稀硫酸,产生氢气的质量与加 入
硫酸的质量关系如图所示。下列说法正确的是
A.该图说明镁比锌的金属活动性强
B.a 点时,两个烧杯中的酸都恰好完全反应
C.b 点时,镁烧杯中产生的氢气多
D.c 点时,两个烧杯中都有酸剩余
10.等质量的Mg、Zn、Fe与足量的硫酸充分反应。产生氢气的质量(m)与时间(t)的关系如下
图,正确的是( )
A. B.
C. D.
二、计算专题
11.某元素原子A的质子数为z,已知B3﹣和A2+具有相同的核外电子数,则B元素的质子数为
A.z﹣2+3 B.z﹣2﹣3 C.z+2+3 D.z+2﹣3
12.已知一个SO 分子的质量为n kg,一个SO 分子的质量为m kg(设两分子中的硫原子和氧原子分
2 3
别相同),若以一个氧原子质量的1/16作为相对原子质量的标准,则SO 的相对分子质量为( )
2A.16m/(m-n) B.16n/(m-n) C.16n/(n-m) D.32n/(m-n)
13.将乙酸(CHCOOH)和葡萄糖(C H O)溶于水得到混合溶液,测得溶液中氢元素的质量分
3 6 12 6
数为8%,则溶液中碳元素的质量分数为
A.8% B.28% C.38% D.48%
14.某化肥 NH NO 中含有一种杂质,经测定化肥中氮元素的质量分数为 38%。则含有的杂质可能
4 3
是
A.NH HCO B.(NH )SO C.NH Cl D.CO(NH)
4 3 4 2 4 4 2 2
15.某气体由CH、C H、C H 中的一种或几种组成,取气体样品在氧气中完全燃烧,测得生成的
4 2 4 2 2
二氧化碳和水的质量比为22:9,下列对该气体组成的判断正确的是
A.该气体一定含有C H B.该气体中可能含有CH
2 4 4
C.该气体可能是由C H 和C H 组成 D.该气体不可能同时含有CH、C H、C H
2 4 2 2 4 2 4 2 2
16.由FeSO 和Fe (SO )、Ag SO 组成的混合物,测得该混合物中硫元素的质量分数为16%,则
4 2 4 3 2 4
金属元素的质量分数为( )
A.16% B.32% C.64% D.52%
17.工业上煅烧石灰石可制得生石灰。现有CaCO 和CaO的固体混合物,其中Ca与C的质量比为
3
10:1,则该混合物中Ca与O的质量比为
A.2:3 B.3:2 C.1:2 D.3:1
18.6.4g某物质在氧气中燃烧,恰好生成2.8g一氧化碳,4.4g二氧化碳和7.2g水,关于该物质有下
列判断:①一定含碳元素和氢元素;②一定不含氧元素;③可能含氧元素;④一定含氧元素;⑤分
子中C、H原子个数比为1:8;⑥分子中C、H、O原子个数比为1:4:1,其中正确的是
A.①②⑤ B.①②⑥ C.①③⑥ D.①④⑥
19.已知某过氧化氢溶液中氢、氧元素质量比为1:10,现取44g该溶液加入适量MnO ,充分反应
2
后,生成氧气的质量为
A.2 g B.4 g C.6 g D.8 g
20.某同学取ZnO、Al O、Cu的混合固体8g,加入20%的稀盐酸至恰好完全反应,共用去73g稀
2 3
盐酸。关于该实验的下列说法中正确的是
A.反应结束后,溶液最终呈蓝色 B.实验过程中一定有置换反应发生
C.反应后得到溶液中水的总质量为62g D.原混合固体中金属元素的质量分数为58%
21.取一定质量的碳酸钙高温加热一段时间后,冷却,测得剩余固体的质量为4.4g剩余固体中钙元
素的质量分数为50%,则反应生成CO 的质量为
2
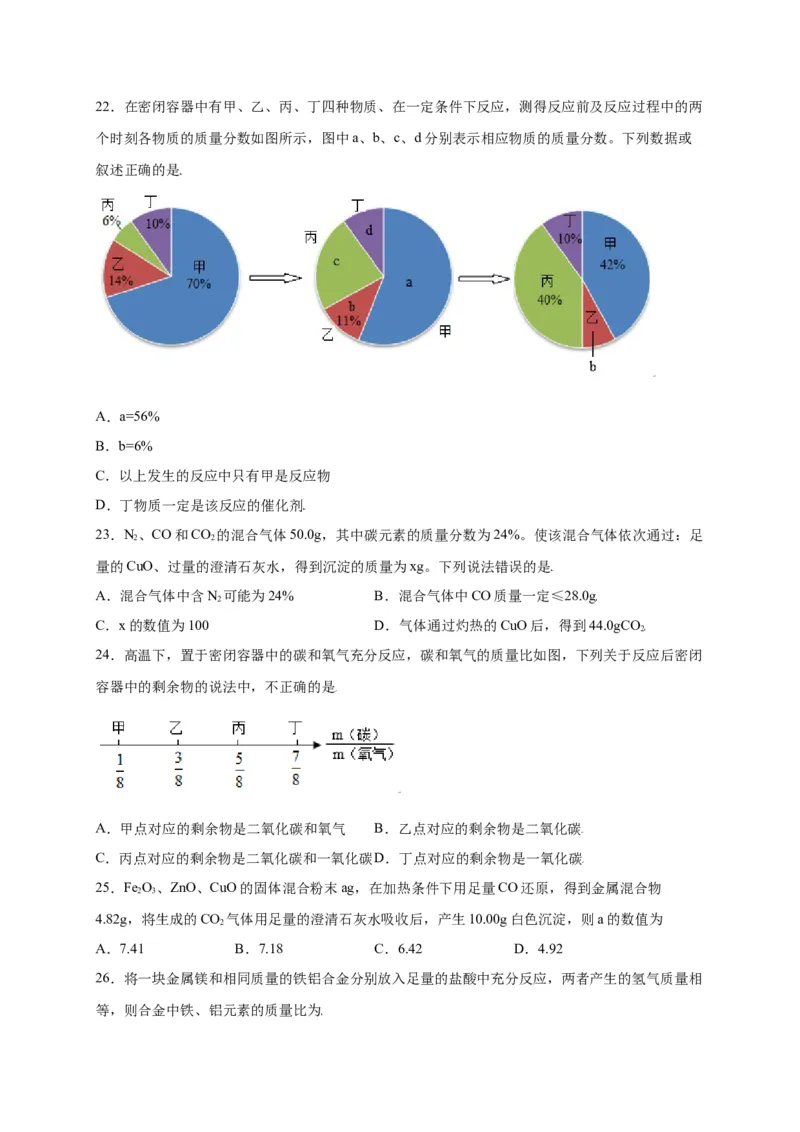
A.2.2g B.1.1g C.4.4g D.5g22.在密闭容器中有甲、乙、丙、丁四种物质、在一定条件下反应,测得反应前及反应过程中的两
个时刻各物质的质量分数如图所示,图中a、b、c、d分别表示相应物质的质量分数。下列数据或
叙述正确的是
A.a=56%
B.b=6%
C.以上发生的反应中只有甲是反应物
D.丁物质一定是该反应的催化剂
23.N、CO和CO 的混合气体50.0g,其中碳元素的质量分数为24%。使该混合气体依次通过:足
2 2
量的CuO、过量的澄清石灰水,得到沉淀的质量为xg。下列说法错误的是
A.混合气体中含N 可能为24% B.混合气体中CO质量一定≤28.0g
2
C.x的数值为100 D.气体通过灼热的CuO后,得到44.0gCO
2
24.高温下,置于密闭容器中的碳和氧气充分反应,碳和氧气的质量比如图,下列关于反应后密闭
容器中的剩余物的说法中,不正确的是
A.甲点对应的剩余物是二氧化碳和氧气 B.乙点对应的剩余物是二氧化碳
C.丙点对应的剩余物是二氧化碳和一氧化碳D.丁点对应的剩余物是一氧化碳
25.Fe O、ZnO、CuO的固体混合粉末ag,在加热条件下用足量CO还原,得到金属混合物
2 3
4.82g,将生成的CO 气体用足量的澄清石灰水吸收后,产生10.00g白色沉淀,则a的数值为
2
A.7.41 B.7.18 C.6.42 D.4.92
26.将一块金属镁和相同质量的铁铝合金分别放入足量的盐酸中充分反应,两者产生的氢气质量相
等,则合金中铁、铝元素的质量比为A.7:12 B.28:9 C.3:16 D.56:27
27.将不纯的锌6克(含杂质金属M)和不纯的铁6克(含杂质金属N),分别与足量的稀硫酸反
应到不再有氢气产生,得到的氢气都是0.2克,则M、N可能是
A.Mg和Cu B.Fe和A 1 C.A1和Mg D.Cu和Mg
28.将一定质量的铁和氧化铜的混合物粉末放入足量稀盐酸中,充分反应后产生气体0.2g,并得到
残留固体6.4g。则原混合物粉末的质量是
A.8.0g B.11.2g C.16.0g D.19.2g
29.Mg、Zn的混合物共10g,与一定质量的稀硫酸恰好完全反应,经测定反应后溶液质量增加了
9.6g,将反应后的溶液蒸发水分则得到的固体混合物的质量为
A.24.8g B.9.2g C.29.2g D.50g
30.蚀刻印刷电路的溶液后的溶液为FeCl 、FeCl 、CuCl 的混合溶液,如图向200g该溶液中加入
3 2 2
铁粉的质量与溶液质量的变化关系。下列说法正确的是( )
(查阅资料:2FeCl +Fe=3FeCl )
3 2
①200~a段发生的反应为2FeCl +Fe=3FeCl
3 2
②m点的溶液中溶质成分为:FeCl 和FeCl
3 2
③x=16.8
④原溶液中FeCl 与CuCl 的质量之比为65:81
3 2
A.①④ B.①③ C.②③ D.②④
31.现有锌粉和另一种金属组成的混合物,在6.5g该混合物中加入100g一定溶质质量分数的稀盐
酸后,混合物与稀盐酸恰好完全反应,产生氢气的质量为m,下列说法正确的是
A.若混合物为Zn、Mg,m可能是0.2g
B.若混合物为Zn、Fe,m等于0.2g
C.若混合物为Zn、Mg,则稀盐酸中溶质质量分数一定大于7.3%
D.若混合物为Zn、Fe,m等于0.1g,混合物中铁的质量分数为50%
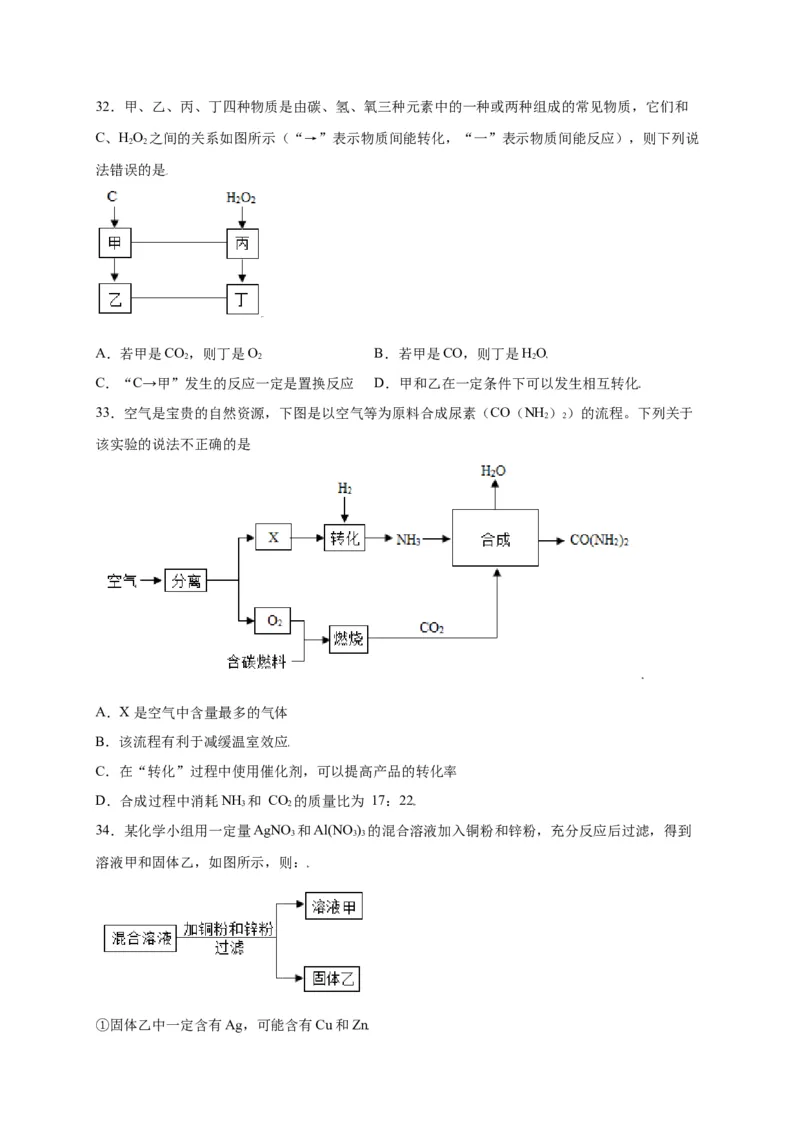
三、分析推断32.甲、乙、丙、丁四种物质是由碳、氢、氧三种元素中的一种或两种组成的常见物质,它们和
C、HO 之间的关系如图所示(“→”表示物质间能转化,“一”表示物质间能反应),则下列说
2 2
法错误的是
A.若甲是CO,则丁是O B.若甲是CO,则丁是HO
2 2 2
C.“C→甲”发生的反应一定是置换反应 D.甲和乙在一定条件下可以发生相互转化
33.空气是宝贵的自然资源,下图是以空气等为原料合成尿素(CO(NH ))的流程。下列关于
2 2
该实验的说法不正确的是
A.X 是空气中含量最多的气体
B.该流程有利于减缓温室效应
C.在“转化”过程中使用催化剂,可以提高产品的转化率
D.合成过程中消耗NH 和 CO 的质量比为 17:22
3 2
34.某化学小组用一定量AgNO 和Al(NO ) 的混合溶液加入铜粉和锌粉,充分反应后过滤,得到
3 3 3
溶液甲和固体乙,如图所示,则:
①固体乙中一定含有Ag,可能含有Cu和Zn②溶液甲中一定含有Al(NO ) 和Zn(NO )
3 3 3 2
③若溶液甲是蓝色,则溶液甲一定只含有Al(NO ) 和Cu(NO )
3 3 3 2
④若溶液甲是无色,则溶液甲一定含有Al(NO )、可能有Zn(NO ) 一定没有Cu(NO )
3 3 3 2 3 2
⑤向固体乙上滴加盐酸有气泡产生,则溶液甲中一定没有AgNO 和Cu(NO ) 上述四种说法正确的
3 3 2
个数为
A.2个 B.3个 C.4个 D.5个
35.现有一包由铜、锌和碳组成的粉末,放到一定量的AgNO 溶液中,完全反应后得到的固体有m
3
种,溶液中溶质有n种。下列说法中不正确的是
A.若m=2,则n=2或3
B.若m=3,则n=2或3
C.当m=2时,溶液一定呈蓝色
D.当m=3时,溶液可能呈蓝色
36.向AgNO、Cu(NO )、Fe(NO ) 的混合溶液中,加入一定量的锌粉,充分反应后过滤。
3 3 2 3 2
下列判断不正确的是
A.向滤渣中加入稀盐酸,有气泡产生,如果滤渣含有Zn,则一定有Fe
B.若滤液是蓝色,滤液中一定存在的物质是Zn(NO )、 Fe(NO ) 和Cu(NO )
3 2 3 2 3 2
C.与原溶液相比,滤液的质量可能增大,可能减小,可能不变
D.若滤渣中有红色固体,滤渣一定有Cu、Ag,可能有Fe、一定无Zn
37.在已经调平的托盘天平两边各放一只等质量的烧杯,向烧杯中各加入质量相等、溶质质量分数
相同的稀盐酸,然后在左烧杯中放入镁,在右烧杯中放入与镁质量相等的铝。等充分反应后,下列
分析错误的是
A.天平保持平衡,左边烧杯中酸没有剩余,镁可能有剩余
B.天平保持平衡,右边烧杯中,酸没有剩余,铝一定有剩余
C.天平失去平衡,左边烧杯中,酸一定有剩余,镁一定没剩余
D.天平失去平衡,右边烧杯中,酸可能有剩余,铝一定没剩余
38.能一次性验证Cu、Ag、Zn三种金属活动性顺序的一组试剂是
A.Cu、Ag、ZnCI 溶液 B.Ag、Zn、Cu(NO )
2 3 2
C.Cu、Ag、Zn、稀盐酸 D.Ag、ZnSO 溶液、CuSO 溶液
4 4
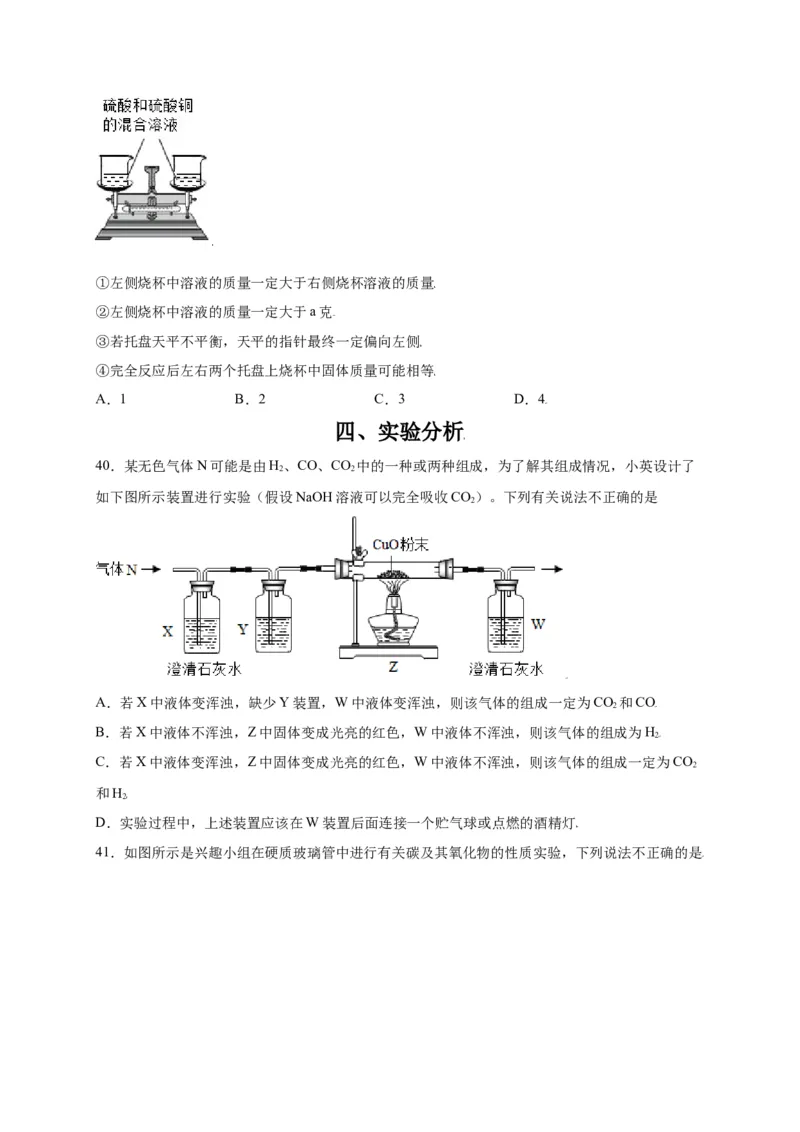
39.在已经调平衡的托盘天平两边各放一只质量相等的烧杯。将某硫酸和硫酸铜的混合溶液2a克
分为两等份,分别装入两只烧杯中,然后向左侧烧杯中放入氧化铜粉末、锌粉中的一种或两种,右
侧烧杯中放入等质量铁粉。充分反应后﹐下列说法中正确的个数是①左侧烧杯中溶液的质量一定大于右侧烧杯溶液的质量
②左侧烧杯中溶液的质量一定大于a克
③若托盘天平不平衡,天平的指针最终一定偏向左侧
④完全反应后左右两个托盘上烧杯中固体质量可能相等
A.1 B.2 C.3 D.4
四、实验分析
40.某无色气体N可能是由H、CO、CO 中的一种或两种组成,为了解其组成情况,小英设计了
2 2
如下图所示装置进行实验(假设NaOH溶液可以完全吸收CO)。下列有关说法不正确的是
2
A.若X中液体变浑浊,缺少Y装置,W中液体变浑浊,则该气体的组成一定为CO 和CO
2
B.若X中液体不浑浊,Z中固体变成光亮的红色,W中液体不浑浊,则该气体的组成为H
2
C.若X中液体变浑浊,Z中固体变成光亮的红色,W中液体不浑浊,则该气体的组成一定为CO
2
和H
2
D.实验过程中,上述装置应该在W装置后面连接一个贮气球或点燃的酒精灯
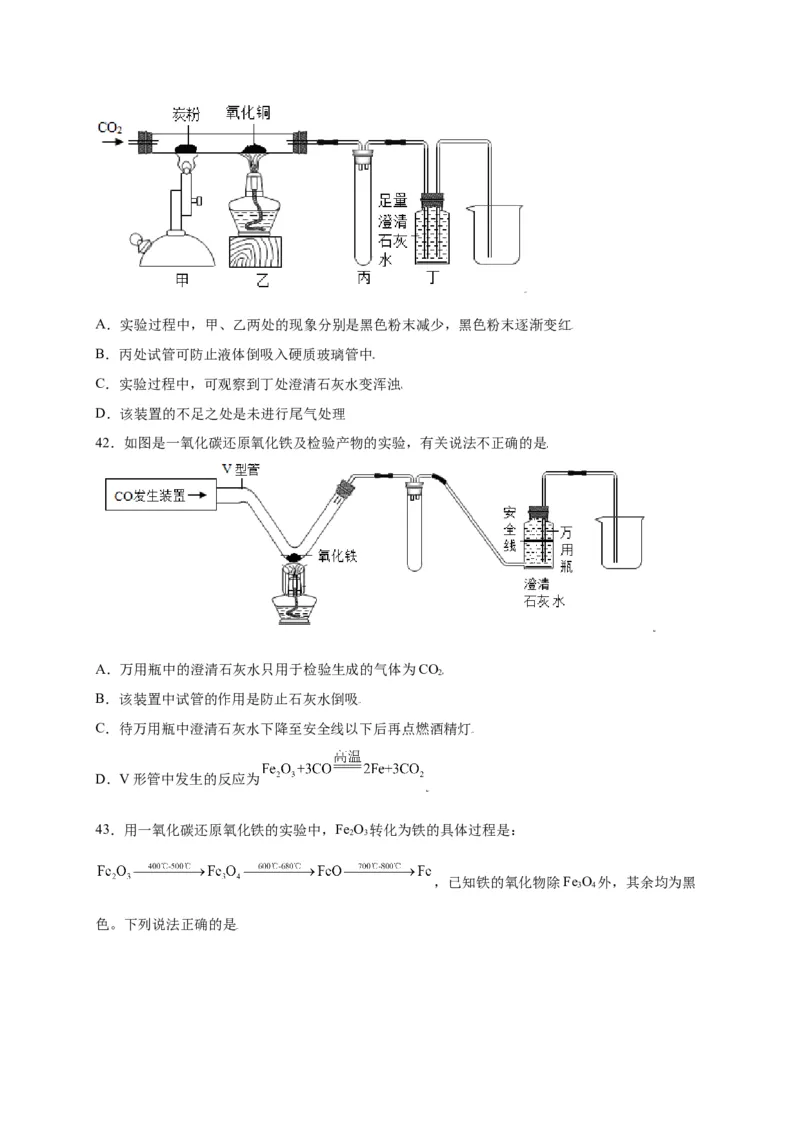
41.如图所示是兴趣小组在硬质玻璃管中进行有关碳及其氧化物的性质实验,下列说法不正确的是A.实验过程中,甲、乙两处的现象分别是黑色粉末减少,黑色粉末逐渐变红
B.丙处试管可防止液体倒吸入硬质玻璃管中
C.实验过程中,可观察到丁处澄清石灰水变浑浊
D.该装置的不足之处是未进行尾气处理
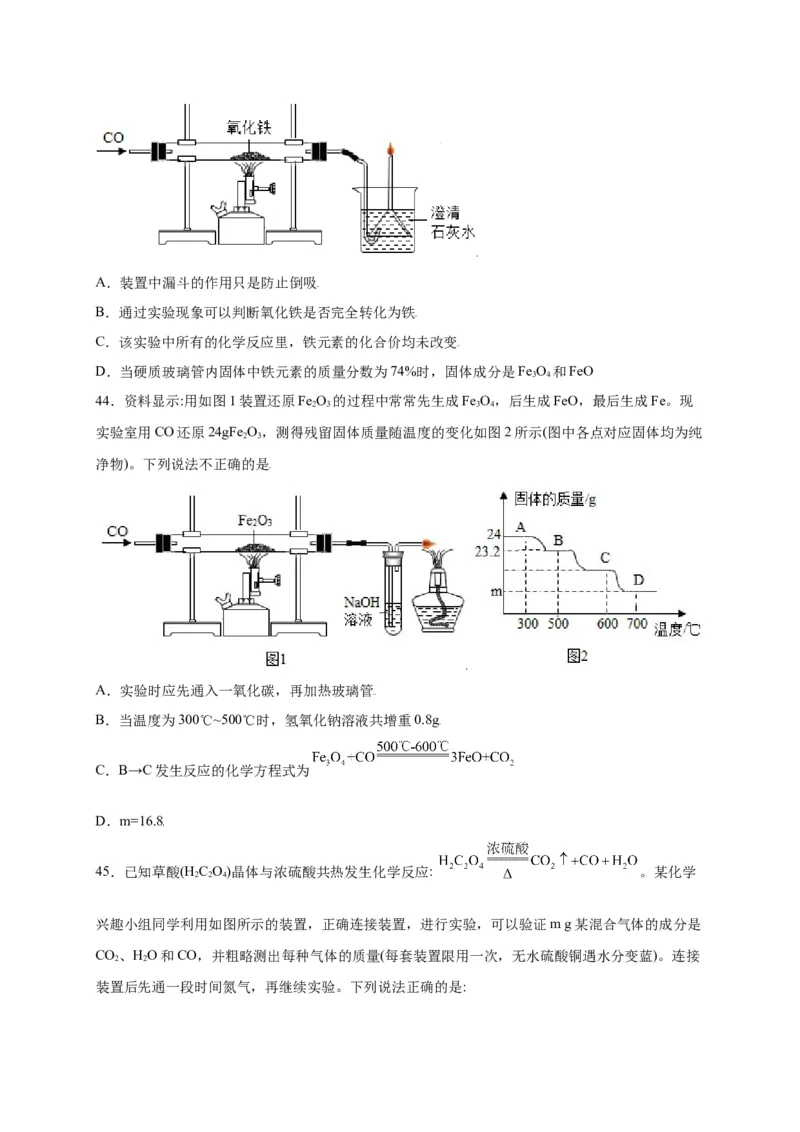
42.如图是一氧化碳还原氧化铁及检验产物的实验,有关说法不正确的是
A.万用瓶中的澄清石灰水只用于检验生成的气体为CO
2
B.该装置中试管的作用是防止石灰水倒吸
C.待万用瓶中澄清石灰水下降至安全线以下后再点燃酒精灯
D.V形管中发生的反应为
43.用一氧化碳还原氧化铁的实验中,Fe O 转化为铁的具体过程是:
2 3
,已知铁的氧化物除Fe O 外,其余均为黑
3 4
色。下列说法正确的是A.装置中漏斗的作用只是防止倒吸
B.通过实验现象可以判断氧化铁是否完全转化为铁
C.该实验中所有的化学反应里,铁元素的化合价均未改变
D.当硬质玻璃管内固体中铁元素的质量分数为74%时,固体成分是Fe O 和FeO
3 4
44.资料显示:用如图1装置还原Fe O 的过程中常常先生成Fe O,后生成FeO,最后生成Fe。现
2 3 3 4
实验室用CO还原24gFe O,测得残留固体质量随温度的变化如图2所示(图中各点对应固体均为纯
2 3
净物)。下列说法不正确的是
A.实验时应先通入一氧化碳,再加热玻璃管
B.当温度为300℃~500℃时,氢氧化钠溶液共增重0.8g
C.B→C发生反应的化学方程式为
D.m=16.8
45.已知草酸(H C O)晶体与浓硫酸共热发生化学反应: 。某化学
2 2 4
兴趣小组同学利用如图所示的装置,正确连接装置,进行实验,可以验证m g某混合气体的成分是
CO、HO和CO,并粗略测出每种气体的质量(每套装置限用一次,无水硫酸铜遇水分变蓝)。连接
2 2
装置后先通一段时间氮气,再继续实验。下列说法正确的是:A.装置的连接顺序依次为混合气体→E→C→B→D →A→尾气处理
B.实验时应先通混合气体后点燃酒精喷灯
C.计算CO的质量时,既能根据A中燃烧管内固体减少的质量计算,也可根据A中澄清石灰水增
加的质量计算,二种方法均准确
D.通过装置B、C、D在反应前后增加的总质量可以得出CO 的质量
2