文档内容
期末总复习考点必杀 200 题
专练 05(流程推断 15 题)
一、推断题
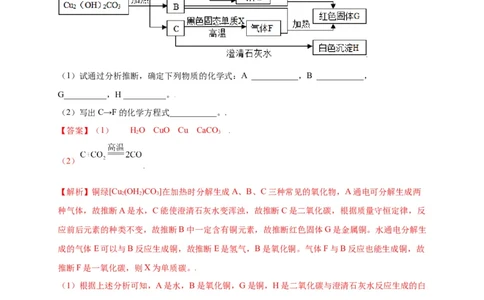
1.已知铜绿[Cu (OH )CO]在加热时分解生成A、B、C三种常见的氧化物。如图是有关物质之间的
2 2 3
转化关系(部分生成物未标出)。
(1)试通过分析推断,确定下列物质的化学式:A ___________,B ___________,
G__________,H __________。
(2)写出C→F的化学方程式___________。
【答案】(1) HO CuO Cu CaCO
2 3
(2)
【解析】铜绿[Cu (OH )CO]在加热时分解生成A、B、C三种常见的氧化物,A通电可分解生成两
2 2 3
种气体,故推断A是水,C能使澄清石灰水变浑浊,故推断C是二氧化碳,根据质量守恒定律,反
应前后元素的种类不变,故推断B中一定含有铜元素,故推断红色固体G是金属铜。水通电分解生
成的气体E可以与B反应生成铜,故推断E是氢气,B是氧化铜。气体F与B反应也能生成铜,故
推断F是一氧化碳,则X为单质碳。
(1)根据上述分析可知,A是水,B是氧化铜,G是铜,H是二氧化碳与澄清石灰水反应生成的白
色碳酸钙沉淀,故其化学式分别为HO、CuO、Cu、CaCO 。(2)根据上述分析可知C是二氧化
2 3
碳,X是单质碳,高温条件下反应生成具有还原性的一氧化碳,反应的化学方程式为:
。
2.A、B、D、N、W、Y、Z是初中常见物质,分别由C、H、O中的一种或两种元素组成,N完
全燃烧生成A和W,A能使澄清石灰水变浑浊,B、Y为单质。它们之间关系如图所示,图中“→”并表示由某一物质可生成另一物质(部分反应物、生成物及反应条件略去)
(1)N一定含有的元素是___________。
(2)D的化学式___________。
(3)①A使澄清石灰水变浑浊的化学方程式:___________;
②Z→Y的化学方程式:___________。
【答案】(1)C、H (2)CO (3)
【解析】A、B、D、N、W、Y、Z是初中常见物质,分别由C、H、O中的一种或两种元素组成,
N完全燃烧生成A和W,A能使澄清石灰水变浑浊,可推出A为二氧化碳,N可能为甲烷,W为
水,B、Y为单质,Z能转化为W和Y,W能转化为Y,可推出Y为氧气,Z为过氧化氢,B能转
化为D、A,D能转化为A,可推出B为碳,D为一氧化碳,代入验证,符合题意。
(1)由分析可知,N完全燃烧生成二氧化碳和水,根据质量守恒定律,化学反应前后,元素的种
类不变,生成物中含C、H、O,反应物中含氧元素,反应物中还应含C、H元素,故N一定含有
的元素是C、H;(2)D为一氧化碳,化学式为CO;(3)①A使澄清石灰水变浑浊的反应为二
氧化碳和氢氧化钙反应生成碳酸钙和水,该反应的化学方程式为: ;
②Z→Y的反应为过氧化氢在二氧化锰的催化下分解为水和氧气,该反应的化学方程式为:
。
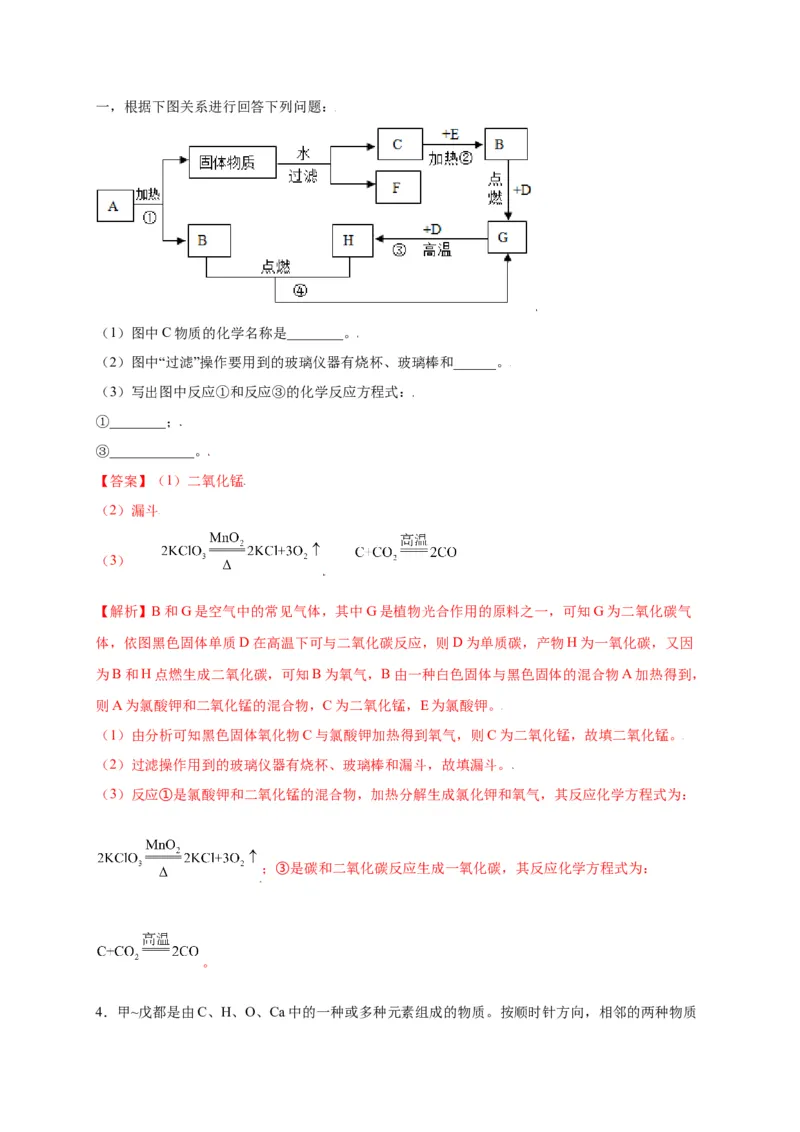
3.A-H是初中常见化学物质,已知A是一种白色固体与黑色固体的混合物,C是黑色固体氧化物,
D是黑色固体单质,E是白色固体,B和G是空气中的常见气体,其中G是植物光合作用的原料之一,根据下图关系进行回答下列问题:
(1)图中C物质的化学名称是________。
(2)图中“过滤”操作要用到的玻璃仪器有烧杯、玻璃棒和______。
(3)写出图中反应①和反应③的化学反应方程式:
①________;
③____________。
【答案】(1)二氧化锰
(2)漏斗
(3)
【解析】B和G是空气中的常见气体,其中G是植物光合作用的原料之一,可知G为二氧化碳气
体,依图黑色固体单质D在高温下可与二氧化碳反应,则D为单质碳,产物H为一氧化碳,又因
为B和H点燃生成二氧化碳,可知B为氧气,B由一种白色固体与黑色固体的混合物A加热得到,
则A为氯酸钾和二氧化锰的混合物,C为二氧化锰,E为氯酸钾。
(1)由分析可知黑色固体氧化物C与氯酸钾加热得到氧气,则C为二氧化锰,故填二氧化锰。
(2)过滤操作用到的玻璃仪器有烧杯、玻璃棒和漏斗,故填漏斗。
(3)反应①是氯酸钾和二氧化锰的混合物,加热分解生成氯化钾和氧气,其反应化学方程式为:
;③是碳和二氧化碳反应生成一氧化碳,其反应化学方程式为:
。
4.甲~戊都是由C、H、O、Ca中的一种或多种元素组成的物质。按顺时针方向,相邻的两种物质之间存在转化关系。已知:甲常温下是无色无味的液体,在通电条件下可以制得乙,丙和丁是组成
元素相同的气体,戊是石灰石的主要成分。
(1)推测物质的化学式:乙_______,丙_______;写出丙物质的一种用途:_______。
(2)丁转化为戊的化学方程式为_________。
(3)这五种物质中,属于氧化物的有__________种。
(4)戊转化为甲的同时也生成丁写出该反应的化学方程式:________。
【答案】(1) O CO 冶炼金属(合理即可)
2
(2)
(3)3
(4)
【解析】根据甲~戊都是由C、H、O、Ca中的一种或多种元素组成的物质,按顺时针方向,相邻的
两种物质之间存在转化关系,甲常温下是无色无味的液体,在通电条件下可以制得乙,所以甲是水,
丙和丁是组成元素相同的气体,戊是石灰石的主要成分,所以戊是碳酸钙,丁能转化成碳酸钙,所
以丁是二氧化碳,丙是一氧化碳,乙能转化成一氧化碳,所以乙是氧气,代入检验,验证合理。
(1)由分析可知,乙是氧气,其化学式为O,丙是一氧化碳,其化学式为CO,一氧化碳具有还
2
原性,可用于冶炼金属;
(2)丁转化为戊,即二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为
CO+Ca(OH) =CaCO ↓+H O;
2 2 3 2
(3)氧化物是由两种元素组成,其中一种元素是氧元素,所以这五种物质中,属于氧化物的有一
氧化碳、水、二氧化碳,共3种;
(4)戊转化为甲的同时也生成丁,该反应可以是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,
反应的化学方程式为CaCO +2HCl=CaCl +H O+CO↑。
3 2 2 25.A、B、C、D、E是初中化学中常见的五种无色气体,其中两种是单质,三种是化合物,E是天
然气的主要成分,它们之间的转化关系如图所示。请写出你的推断:
(1)B的化学式为______,D的化学式为______,E的化学式为______。
(2)写出A + E → H O + B的化学方程式:______。
2
(3)写出C的一种用途______。
【答案】(1) CO H CH
2 2 4
(2)
(3)做燃料或还原剂(其他合理答案均可)
【解析】根据信息“气体E为天然气的主要成分”,则可知E为甲烷。氧化铜和无色的气体D反应
会生成水,可以推测出D就是氢气,氧化铜和气体C反应会生成B,可以推测出C是一氧化碳,B
是二氧化碳;气体A和一氧化碳反应会生成二氧化碳,可以知道A就是氧气,氧气和氢气反应生
成水,氧气和气体E反应生成水和二氧化碳,则E是甲烷也符合。各物质代入题目中,进行验证,
符合题意。(1)B是CO,D是H,E是CH。
2 2 4
(2)甲烷和氧气在点燃的条件下反应产生水和二氧化碳: 。
(3)C是CO,CO可以用作做燃料或还原剂(其他合理答案均可)。
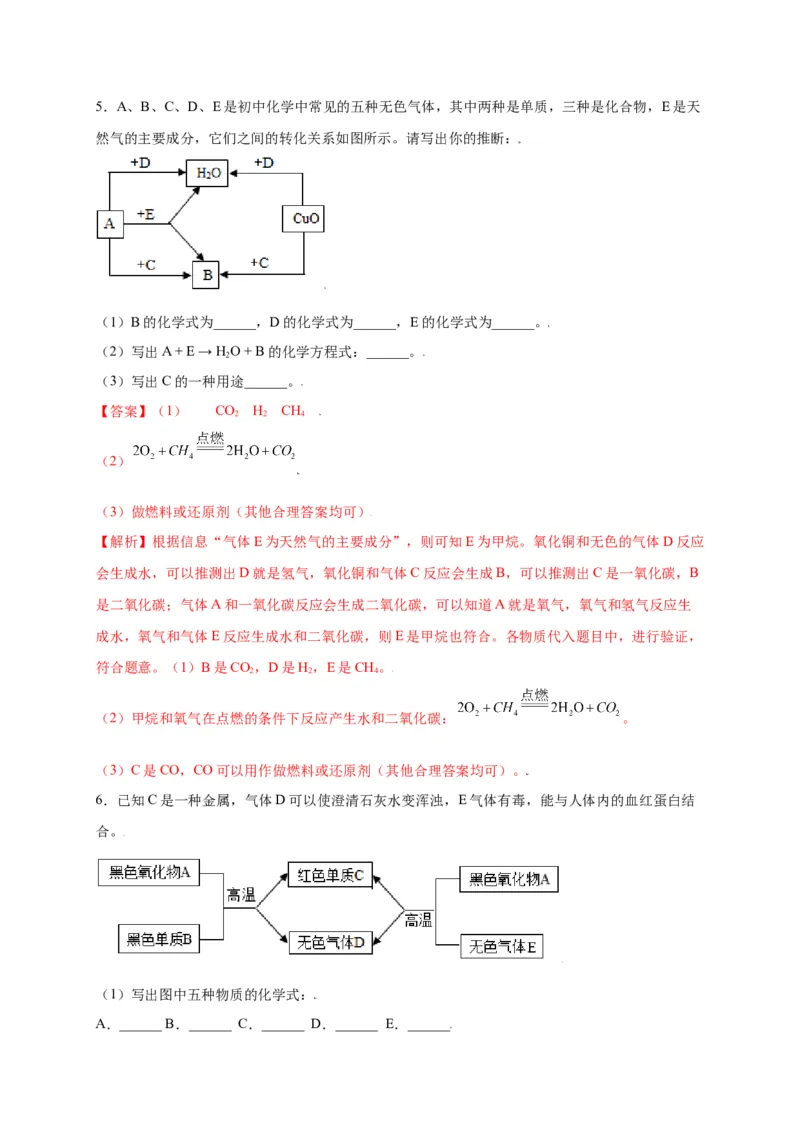
6.已知C是一种金属,气体D可以使澄清石灰水变浑浊,E气体有毒,能与人体内的血红蛋白结
合。
(1)写出图中五种物质的化学式:
A.______ B.______ C.______ D.______ E.______(2)写出图中所示两个反应的化学方程式:______; __________。
【答案】(1) CuO C Cu CO H
2 2
(2) C + 2CuO 2Cu + CO ↑ H + CuO Cu + H O
2 2 2
【解析】对于框图推断题,首先要做的就是抓住突破点,比如题目已知条件、物质的颜色、类别、
状态,化学反应的现象、类型等,进而对物质进行判断处理。在本题中,题目中最有用的信息是
“气体D可以使澄清石灰水变浑浊,E气体有毒,能与人体内的血红蛋白结合”,由此就可以推断出
D是二氧化碳、E是一氧化碳。
(1)从框图中各物质的颜色和类别我们可以作以下推断,从左到右,A是黑色氧化物、B 是黑色
单质,在高温下反应生成红色单质C和无色气体D,从黑色固体这个突破点,我们就可以推断该反
应是木炭还原氧化铜的反应,即A为氧化铜、B为木炭、C为单质铜、D为二氧化碳。而从右到左,
氧化铜和一种无色气体E高温下发生反应生成铜和二氧化碳,那么E即为一氧化碳。即答案为:A-
CuO;B-C;C-Cu;D-CO ;E-CO。
2
(2)本题涉及到的两个方程式为:①C + 2CuO 2Cu + CO ↑;②H + CuO Cu + HO。
2 2 2
7.2019年是祖国母亲的70华诞!这是一道以“青春‘心’向党,献礼七十年”为主题的推断题。图
中数字“7”中相连的物质可以发生反应;数字“0”中相连的物质可以发生转化,箭头指向生成物。
M物质既可以和B物质反应,也可以和F物质反应。
已知下列信息:①A在空气中燃烧生成最常见的液体E;
②B、M均为黑色固体,且B的相对分子质量为80;
③C、F的组成元素完全相同;
④D是可由高粱、玉米等发酵、蒸馏而得到的液体。
(1)写出下列物质的化学式
A.___________B.___________C.___________D.___________。(2)B和M反应的现象为___________。
(3)D同时转化为E和F的化学方程式为___________。
【答案】(1) H CuO CO C HOH
2 2 5
(2)黑色固体中逐渐有紫红色固体生成
(3)
【解析】①A在空气中燃烧生成最常见的液体E,则A是氢气,E是水;
②B、M均为黑色固体,且B的相对分子质量为80,则B是氧化铜,M是木炭;
③C、F的组成元素完全相同;
④D是可由高粱、玉米等发酵、蒸馏而得到的液体,则D是乙醇,乙醇燃烧生成水和二氧化碳,则
F为二氧化碳,结合③可知C为一氧化碳。
(1)A为氢气,化学式为H;B为氧化铜,化学式为CuO;C为一氧化碳,化学式为CO;D为乙
2
醇,化学式为C HOH;
2 5
(2)B和M反应为木炭还原氧化铜,实验现象为黑色固体中逐渐有紫红色固体生成;
(3)D同时转化为E和F为乙醇燃烧生成水和二氧化碳,方程式为:
8.如图中A、B、C、D、E是初中化学中常见的五种物质,在通常情况下,A为黑色固体,B、
C、E均为无色无味的气体,D为不溶于水的白色固体,在实验室常用含D的物质与稀盐酸反应制
取C,单质E是组成空气的主要成分之一。它们之间的关系如图所示,请回答下列问题:
(1)A的化学式是____________。
(2)写出B→C的化学方程式____________。
(3)写出C→D的化学方程式____________。
【答案】(1)C (2) (3)
【解析】A、B、C、D、E是初中化学中常见的五种物质,在通常情况下,A为黑色固体,B、C、E均为无色无味的气体,D为不溶于水的白色固体,在实验室常用含D的物质与稀盐酸反应制取
C,可推出C为二氧化碳,D为碳酸钙,A能转化为B、C,B、C能相互转化,可推出A为碳,B
为一氧化碳,A能与E反应生成B、C,单质E是组成空气的主要成分之一,可推出E为氧气,代
入验证,符合题意。
(1)由分析可知,A为碳,化学式为C;
(2)B→C为一氧化碳燃烧生成二氧化碳,该反应的化学方程式为: ;
(3)C→D为二氧化碳和氢氧化钙反应生成碳酸钙和水,该反应的化学方程式为:
。
9.A~G表示初中化学常见物质,其中A、B、C、D都是氧化物,E、F、G都是金属单质,F是导
电性导热性最好的金属,A和G均为红色,他们之间的转化关系如图所示(反应条件,部分反应物
及生成物已略去),请回答下列问题:
(1)F的化学式为________;G的化学式为_______。
(2)B的一种用途是___________;
(3)反应②的化学方程式为:_______;
(4)E、F、G三种金属的活动性由强到弱的顺序为__________。(用E、F、G表示)
(5)从微观角度解释B和D两种物质化学性质不同的原因_______。
【答案】(1) Ag Cu
(2)冶炼金属(作燃料)
(3)
(4)EGF
(5)两者的分子构成不同
【解析】A~G表示初中化学常见物质,F是导电性导热性最好的金属,可推出F为银,A和G均为红色,G能转化为F,G为金属单质,可推出G为铜,A能与B反应生成D和E,A、B、D均为
氧化物,E为金属单质,可推出A为氧化铁、B为一氧化碳,E为铁,D为二氧化碳;B能与C反
应转化为D和G,C为氧化物,可推出C为氧化铜,代入验证,符合题意。
(1)由分析可知,F为银,化学式为:Ag;G为铜,化学式为:Cu;
(2)B为一氧化碳,一氧化碳具有还原性,可用于冶炼金属;
(3)反应②为一氧化碳与氧化铜在加热的条件下反应生成铜和二氧化碳,该反应的化学方程式为:
;
(4)E能转化为F、G,即E能将F、G从其盐溶液中置换出来,说明E比F、G活泼,G能将F从
其盐溶液中置换出来,说明G比F活泼,故E、F、G三种金属的活动性由强到弱的顺序为:E>G
>F;
(5)B为一氧化碳,D为二氧化碳,一氧化碳和二氧化碳分子构成不同,故化学性质不同。
10.2020年6月23日,“北斗”卫星导航系统全面建成。现有“化学北斗七星”分别为碳、铁、氧气、
一氧化碳、氧化铁、氧化铜、稀盐酸等七种物质中的一种,已知相连的两颗星所代表的物质在一定
条件下可以发生化学反应。其中A可用于实验室制取二氧化碳,F是红棕色固体,G是一种单质。
请回答下列问题(部分反应物、生成物和反应条件已省略):
(1)F的化学式为______________;
(2)B与C反应的化学方程式为________;
(3)E与G反应的基本类型是________反应;
(4)下列物质中能替代D物质的是_________(填序号)。
①氢气 ②二氧化碳 ③水 ④硫酸
【答案】(1)Fe O (2) (3)置换 (4)①
2 3【解析】A可用于实验室制取二氧化碳,所以A为稀盐酸;F是红棕色固体,所以F是氧化铁;G
是一种单质且可以和氧化铁反应,所以G是碳;B可以和稀盐酸反应,所以B是铁;C可以和铁反
应,所以C是氧气; C可以和D反应,所以D是一氧化碳;E可以和一氧化碳反应,所以E是氧
化铜,代入验证,推断正确。
(1)F是氧化铁,化学式为:Fe O
2 3;
(2)B是铁,C是氧气,铁与氧气在点燃的条件下反应生成四氧化三铁,故化学方程式为:
;
(3)E是氧化铜,G是碳,氧化铜和碳在高温的条件下反应生成铜和二氧化碳,符合“单换单”的特
征,属于置换反应;
(4)D既要能和氧气反应,还要能和氧化铁、氧化铜反应,所以可以代替D物质的有:
①氢气可以和氧气、氧化铁、氧化铜反应,故可以代替;②二氧化碳不和氧气、氧化铁、氧化铜反
应,故不可以代替;③水不和氧气、氧化铁、氧化铜反应,故不可以代替;④碳酸不和氧气、氧化
铁、氧化铜反应,故不可以代替;
故填:①。
11.A、B、C、D、E分别表示初中化学常见的五种物质,它们的部分反应和转化关系如图所示
(“一”表示两种物质能发生反应,“→”表示一种物质能转化成另一种物质,且省略部分反应物
或生成物及条件),已知A、E中含有三种元素,B、C、D都是单质,B是年产量最高的金属,C
为紫红色。请回答:
(1)写出A、D物质的化学式:A______。D______。
(2)D生成C的化学方程式为______。
(3)B生成C的现象______。
【答案】(1) AgNO H
3 2(2)H+CuO Cu+H O
2 2
(3)银白色金属表面覆盖一层红色物质,溶液由蓝色变成浅绿色
【解析】B、C都是单质,B是年产量最高的金属,C为紫红色,则B为铁,C为铜;D为单质,能
与B相互转化,E中含有三种元素,能与B反应,且能转化为D,则D可以为氢气,E为硫酸;A
中含有三种元素,与铜、铁都能反应,则A可以为硝酸银,代入检验,验证合理;
(1)A为硝酸银,其化学式为AgNO,D为氢气,其化学式为H;
3 2
(2)D生成C,即氢气与氧化铜在加热的条件下生成铜和水,反应的化学方程式为H+CuO
2
Cu+H O;
2
(3)B为铁,C为铜,铁与硫酸铜(或氯化铜)反应生成硫酸亚铁(或氯化亚铁)和铜,可观察
到银白色金属表面覆盖一层红色物质,溶液由蓝色变成浅绿色,故填:银白色金属表面覆盖一层红
色物质,溶液由蓝色变成浅绿色。
12.A、B、C、D、E为初中化学常见的五种物质(或溶质),其中A是一种常用作导线的物质,
D能被磁铁吸引,C分别能与A、D发生置换反应,E的溶液为浅绿色。用“一”表示两种物质间
能发生化学反应,用“→”表示一种物质可以转化成另一种物质(部分反应物或生成物及反应条件
已略去)。请回答:
(1)写出下列物质的化学式。
A______;E______。
(2)B转化为A的化学方程式为______。
(3)A和C溶液反应的现象为______。
【答案】(1) Cu Fe(NO )
3 2
(2)
(3)有银白色固体析出,溶液由无色变为蓝色【解析】A、B、C、D、E为初中化学常见的五种物质,其中A是一种常用作导线的物质,可推出
A为铜,D能被磁铁吸引,可推出D为铁,C分别能与A、D发生置换反应,可推出C为硝酸银,
E的溶液为浅绿色,D能与E相互转化,C能转化为E,可推出E为硝酸亚铁,B能与D相互转化,
B能转化为A,可推出B为氢气,代入验证,符合题意。
(1)A为铜,化学式为Cu;E为硝酸亚铁,化学式为:Fe(NO );
3 2
(2)B转化为A的反应为氢气和氧化铜在加热的条件下反应生成铜和水,该反应的化学方程式为:
;
(3)A和C溶液反应为铜和硝酸银反应生成硝酸铜和银,现象为:有银白色固体析出,溶液由无
色变为蓝色。
13.我国每年报废的手机超过1亿部。废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,
随意丢弃既会造成资源浪费,也会污染土壤和水体。化学兴趣小组为回收其中的铜,设计并进行了
如下实验。(已知: ;不考虑金、银发生类似反应。)
(1)将电路板粉碎成粉末的目的是_________。
(2)步骤①~④中均用到玻璃棒,其作用是________。
(3)步骤②中的实验现象是:固体部分溶解,________。步骤②得到的滤渣是_________。
(4)步骤①所得滤液中的物质除水外,还有________,写出步骤①的其中一个化学方程式
________。
【答案】(1)增大反应物接触面积,加快反应速率
(2)过滤
(3) 溶液由无色变成蓝色 金、银或Au、Ag
(4) HSO 、Al (SO )、FeSO 2Al+3H SO =Al(SO )+3H ↑或Fe+H SO =FeSO+H ↑
2 4 2 4 3 4 2 4 2 4 3 2 2 4 4 2
【解析】(1)将电路板粉碎成粉末的目的是增大反应物接触面积,加快反应速率;(2)步骤①~④中都通过过滤将固体与液体进行分离,该操作中玻璃棒的作用为引流,防止液体
洒出;
(3)步骤②中铜和过氧化氢、硫酸反应生成硫酸铜和水,能够观察到固体部分溶解,溶液由无色
变成蓝色;步骤②中金、银不参与反应,所以步骤②得到的滤渣是金、银;
(4)由于硫酸过量,步骤①所得滤液中的溶质除硫酸外,还有稀硫酸和铝、铁反应生成的硫酸铝
和硫酸亚铁;铝与硫酸反应生成硫酸铝和氢气,铁与硫酸反应生成硫酸亚铁和氢气,反应的化学方
程式分别为2Al+3H SO =Al(SO )+3H ↑、Fe+H SO =FeSO+H ↑;
2 4 2 4 3 2 2 4 4 2
14.氯化铁溶液能腐蚀铜,工业上常用此原理生产印刷线路板.以下是印刷线路板的生产及废液的
处理过程:
请回答下列问题:
(1)步骤②中发生了两个反应:2FeCl +Fe═3FeCl 和__________;
3 2
(2)滤渣的成份有_____,步骤③中发生反应的化学方程式是_________;
(3)该流程中可以循环利用的物质是_____。
(4)向氧化铜和铁粉的混合物中,加入一定量的稀硫酸,反应停止后,过滤,除去不溶物.向滤
液中加一铁片,未看到铁片有任何变化.则滤出的不溶物中一定含有_____,可能含有金属单质
_____,滤液中一定含有_____,不可能含有_____。
【答案】(1)
(2) Fe、Cu
(3)氯化亚铁##FeCl
2
(4) 铜##Cu 铁##Fe 硫酸亚铁 CuSO 和HSO
4 4 2 4
【解析】(1)步骤②中还发生的反应为铁与氯化铜反应生成氯化亚铁和铜,该反应的化学方程式
为: ;(2)铁与氯化铁反应生成氯化亚铁,铁与氯化铜反应生成氯化亚铁和
铜,铁过量,故滤渣为Fe、Cu;步骤③中发生反应为铁与稀盐酸反应生成氯化亚铁和氢气,该反应的化学方程式为: ;(3)由图可知,该流程中可以循环利用的物质是:
FeCl ;
2
(4)向氧化铜和铁粉的混合物中,加入一定量的稀硫酸,氧化铜先与稀硫酸反应生成硫酸铜和水,
由于金属活动性:Fe>H>Cu,故铁先与硫酸铜反应生成硫酸亚铁和铜,待硫酸铜完全反应后,铁
与稀硫酸反应生成硫酸亚铁和氢气,过滤,除去不溶物.向滤液中加一铁片,未看到铁片有任何变
化,说明硫酸铜和硫酸已经完全反应,故滤出的不溶物中一定含Cu,铁可能恰好完全反应,也可
能过量,故可能含有的金属单质是Fe';滤液中一定含有FeSO ;不可能含CuSO 、HSO 。
4 4 2 4
15.图是以空气和其他必要的原料合成硝酸铵(NH NO )的工业流程(变化中的反应物和生成物
4 3
均已全部给出)。请按要求回答下列问题:
(1)步骤I中发生的是______(填“物理”或“化学”)变化。
(2)写出步骤Ⅲ中发生反应的符号表达式______。
(3)从生产流程可看出,五个步骤中所涉及的化学反应,较易进行的是______(填步骤编号)。
(4)上述化学反应中属于化合反应的有______个。
【答案】(1)物理 (2) (3)步骤IV和步骤Ⅴ (4)3
【解析】(1)步骤I中是空气的分离过程,没有生成新物质,发生的是物理变化。
(2)步骤Ⅲ中发生反应为氨气和氧气在催化剂和加热条件下生成一氧化氮和水,
。
(3)从生产流程可看出,五个步骤中所涉及的化学反应中Ⅱ、Ⅲ都需要一定条件,IV、Ⅴ不需要
特殊条件就能发生,故较易进行的是步骤IV和步骤Ⅴ。
(4)化合反应是多种物质生成一种物质的反应;Ⅱ是氮气和氢气生成氨气的反应;Ⅲ是生成两种
物质的反应;IV是一氧化碳、氧气、水生成硝酸的反应;Ⅴ为硝酸和氨气生成硝酸铵的反应;
故属于化合反应的有3个。