文档内容
期末总复习考点必杀 200 题
专练 06(精选探究 10 题)
1.小峰同学腿部轻微擦伤,医务室的大夫在他伤口上涂了医用过氧化氢溶液,小峰看到伤口处产
生了小气泡,很好奇。
(提出问题)为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
请写出过氧化氢分解的化学方程式_____________;
(查阅资料)①人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是 37℃
(提出猜想)猜想一:过氧化氢分解加快是因为人体温比医用瓶的温度高
猜想二:过氧化氢分解加快是因为体温下伤口中有过氧化氢酶。
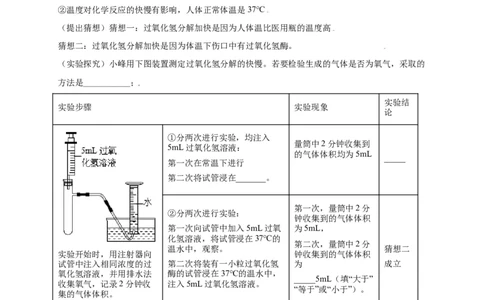
(实验探究)小峰用下图装置测定过氧化氢分解的快慢。若要检验生成的气体是否为氧气,采取的
方法是___________;
实验结
实验步骤 实验现象
论
①分两次进行实验,均注入
量筒中2分钟收集到
5mL过氧化氢溶液:
的气体体积均为5mL
_____
第一次在常温下进行
第二次将试管浸在_______。
第一次,量筒中2分
②分两次进行实验:
钟收集到的气体体积
第一次向试管中加入5mL 过氧 为5mL,
化氢溶液,将试管浸在37℃的
第二次,量筒中2分
温水中,观察。 猜想二
实验开始时,用注射器向 钟收集到的气体体积
试管中注入相同浓度的过 第二次将装有一小粒过氧化氢 为 成立
氧化氢溶液,并用排水法 酶的试管浸在 37℃的温水中,
_____5mL(填“大于”
收集氧气,记录2分钟收 注入5mL 过氧化氢溶液。
“等于”或“小于”)。
集的气体体积。
(提出质疑)小红认为小峰通过实验①和②得出“猜想二”成立的结论不严密,理由是________;
(得出结论) 猜想二成立
(反思交流) 除了上述因素会影响过氧化氢分解速度外,_____(写一种)也会影响过氧化氢分解
速度;
(拓展延伸)决定化学反应速率的主要因素有______(填字母)。
A.反应物的浓度 B.反应温度 C.使用催化剂 D.反应物的性质。
2.某研究小组同学发现,超市里有一种神奇的污渍爆炸盐(如图主要成分是:过碳酸钠(Na CO))能
2 4除去各种顽固污渍,溶于水,有许多气泡产生。该小组同学进行如下探究。
探究一:该气体的成分是什么?
(猜想与假设)
甲说:该气体可能是CO、O、CO、H、N
2 2 2 2.
乙说:不可能含有N,因为___________。
2
丙说:不可能含有CO和H,因为从药品安全角度考虑,H 易燃易爆,CO___________。
2 2
该小组同学认为:该气体可能含有CO、O 中的一种或两种。
2 2
(进行实验)
实验编号 实验操作 实验现象
① 将气体通入澄清石灰水中 澄清石灰水变浑浊
② 将带火星的木条深入该气体中 带火星木条没有复燃
(得出结论)
由实验①可知,该气体中肯定含有___________,请写出该反应的化学方程式___________。由实验
②___________(填“能”或“不能”)确定该气体中不含氧气。
3.在浓硫酸的催化作用下,固体草酸(HC O)受热分解生成碳的氧化物和水,某化学课外兴趣
2 2 4
小组对生成物中碳的氧化物种类进行了如下实验探究:
(提出问题)生成物中有哪种碳的氧化物?
(合理猜想)猜想1:只有CO 猜想2:只有CO 猜想3:_____
2
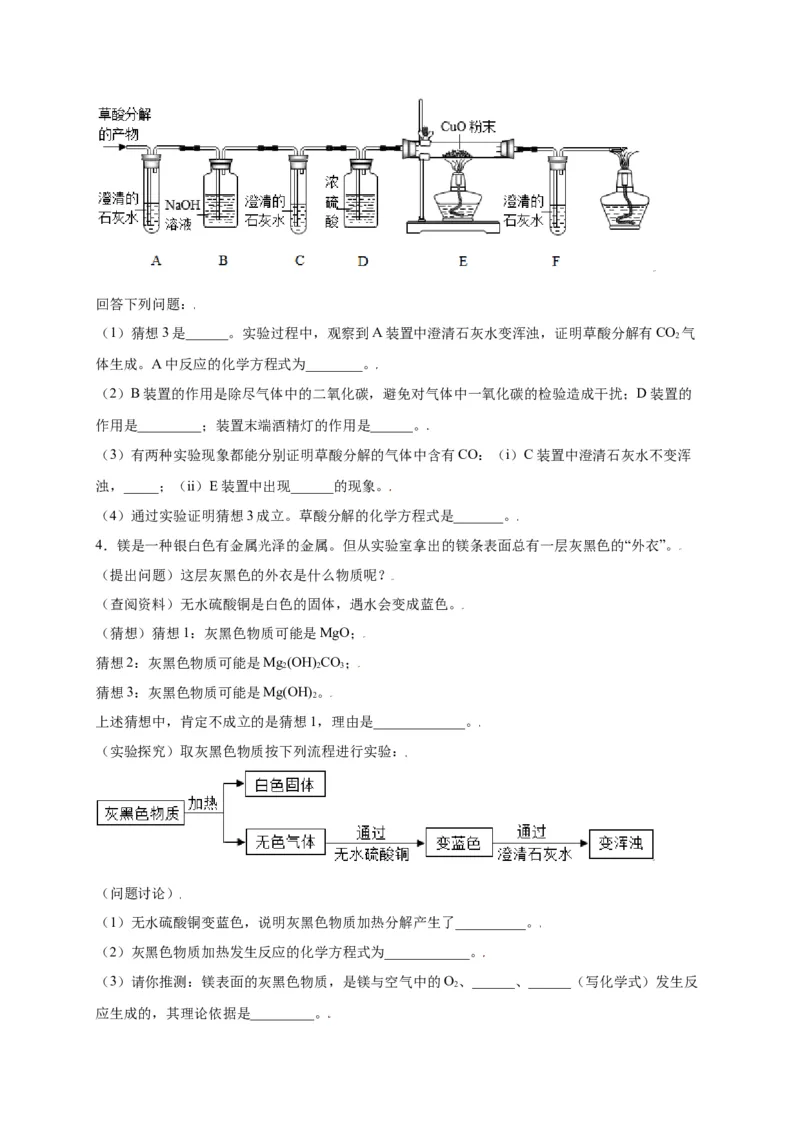
(设计实验)基于猜想3,依据CO和CO 的性质,兴趣小组的同学设计了如下实验:
2回答下列问题:
(1)猜想3是______。实验过程中,观察到A装置中澄清石灰水变浑浊,证明草酸分解有CO 气
2
体生成。A中反应的化学方程式为________。
(2)B装置的作用是除尽气体中的二氧化碳,避免对气体中一氧化碳的检验造成干扰;D装置的
作用是_________;装置末端酒精灯的作用是______。
(3)有两种实验现象都能分别证明草酸分解的气体中含有CO:(i)C装置中澄清石灰水不变浑
浊,_____;(ii)E装置中出现______的现象。
(4)通过实验证明猜想3成立。草酸分解的化学方程式是_______。
4.镁是一种银白色有金属光泽的金属。但从实验室拿出的镁条表面总有一层灰黑色的“外衣”。
(提出问题)这层灰黑色的外衣是什么物质呢?
(查阅资料)无水硫酸铜是白色的固体,遇水会变成蓝色。
(猜想)猜想1:灰黑色物质可能是MgO;
猜想2:灰黑色物质可能是Mg(OH) CO;
2 2 3
猜想3:灰黑色物质可能是Mg(OH) 。
2
上述猜想中,肯定不成立的是猜想1,理由是_____________。
(实验探究)取灰黑色物质按下列流程进行实验:
(问题讨论)
(1)无水硫酸铜变蓝色,说明灰黑色物质加热分解产生了__________。
(2)灰黑色物质加热发生反应的化学方程式为____________。
(3)请你推测:镁表面的灰黑色物质,是镁与空气中的O、______、______(写化学式)发生反
2
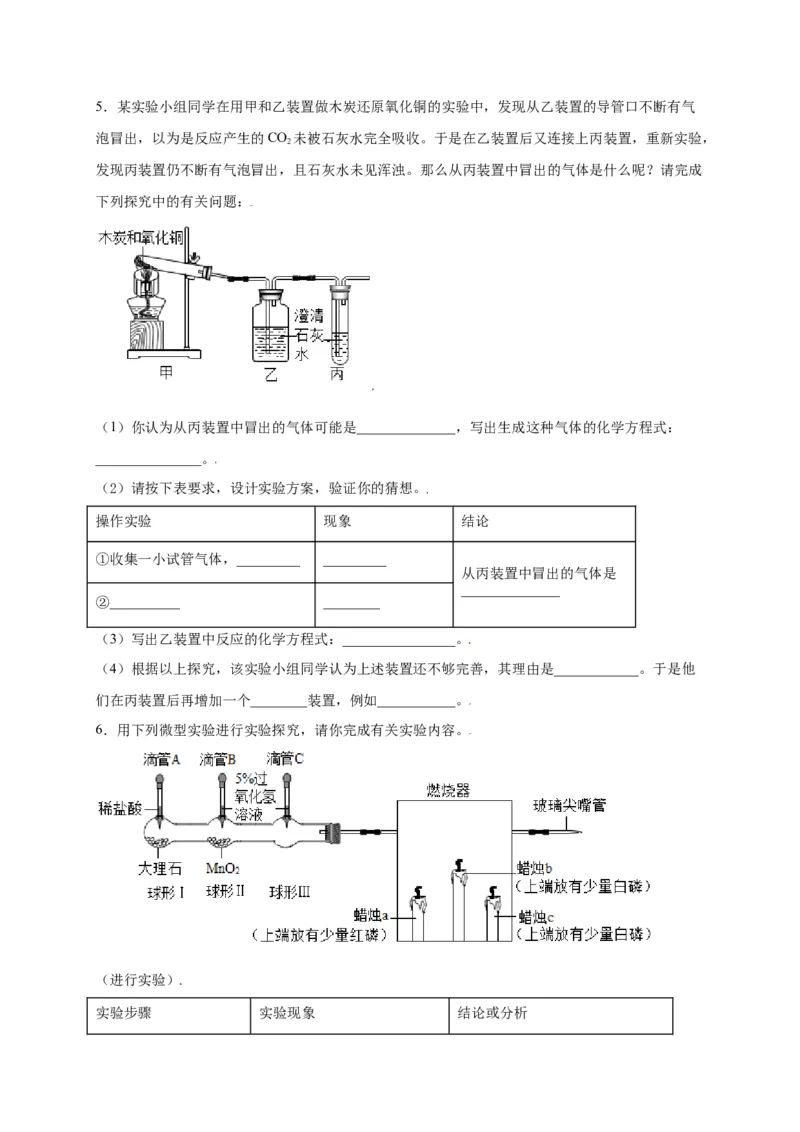
应生成的,其理论依据是_________。5.某实验小组同学在用甲和乙装置做木炭还原氧化铜的实验中,发现从乙装置的导管口不断有气
泡冒出,以为是反应产生的CO 未被石灰水完全吸收。于是在乙装置后又连接上丙装置,重新实验,
2
发现丙装置仍不断有气泡冒出,且石灰水未见浑浊。那么从丙装置中冒出的气体是什么呢?请完成
下列探究中的有关问题:
(1)你认为从丙装置中冒出的气体可能是______________,写出生成这种气体的化学方程式:
_______________。
(2)请按下表要求,设计实验方案,验证你的猜想。
操作实验 现象 结论
①收集一小试管气体,_________ _________
从丙装置中冒出的气体是
______________
②__________ ________
(3)写出乙装置中反应的化学方程式:________________。
(4)根据以上探究,该实验小组同学认为上述装置还不够完善,其理由是____________。于是他
们在丙装置后再增加一个________装置,例如___________。
6.用下列微型实验进行实验探究,请你完成有关实验内容。
(进行实验)
实验步骤 实验现象 结论或分析1.同时挤压滴管B和 ①球形Ⅱ__________,球形
球形Ⅱ反应的化学方程式是
Ⅲ有少量气泡缓慢放出。
C,控制相同量液体滴
___________。
于球形容器中。 ②蜡烛a、b、c都不燃烧。
a不燃烧的原因是_________,白
2.微热燃烧器至50℃。 蜡烛b、c燃烧,a不燃烧。 磷燃烧的化学方程式是
____________ 。
3.挤压滴管A,将足量 ①球形Ⅰ中有气泡放出。 球形Ⅰ产生的气体具有的化学性
稀盐酸滴于球形I中。 ②一段时间后,________。 质是______________。
4.熄灭蜡烛,将涂有澄
清石灰水的小烧杯罩住 烧杯内壁的石灰水变浑浊。 证明蜡烛一定含有碳元素。
玻璃尖嘴管。
(实验反思)
(1)对于步骤1,下列说法正确的是__________(选填编号)。
A.MnO 加快反应速率 B.MnO 质量和化学性质在反应前后没有改变
2 2
C.MnO 一定分解产生气体 D.反应过程中球形II比球形III内产生的气体多
2
(2)步骤4的结论不正确,你的理由是___________。
7.在浓硫酸的催化作用下,固体草酸(H C O)受热分解生成碳的氧化物和水。某化学课外兴趣小组
2 2 4
对生成物中碳的氧化物种类进行了如下实验探究:
查阅资料:
(1)氢氧化钠性质与氢氧化钙相似,且溶于水的能力比氢氧化钙强
(2)浓硫酸具有吸水性,可做某些气体的干燥剂
(提出问题)生成物中有哪几种碳的氧化物?
(猜想)
猜想1 猜想2 猜想3
只有CO 只有___________ 含有CO和CO
2
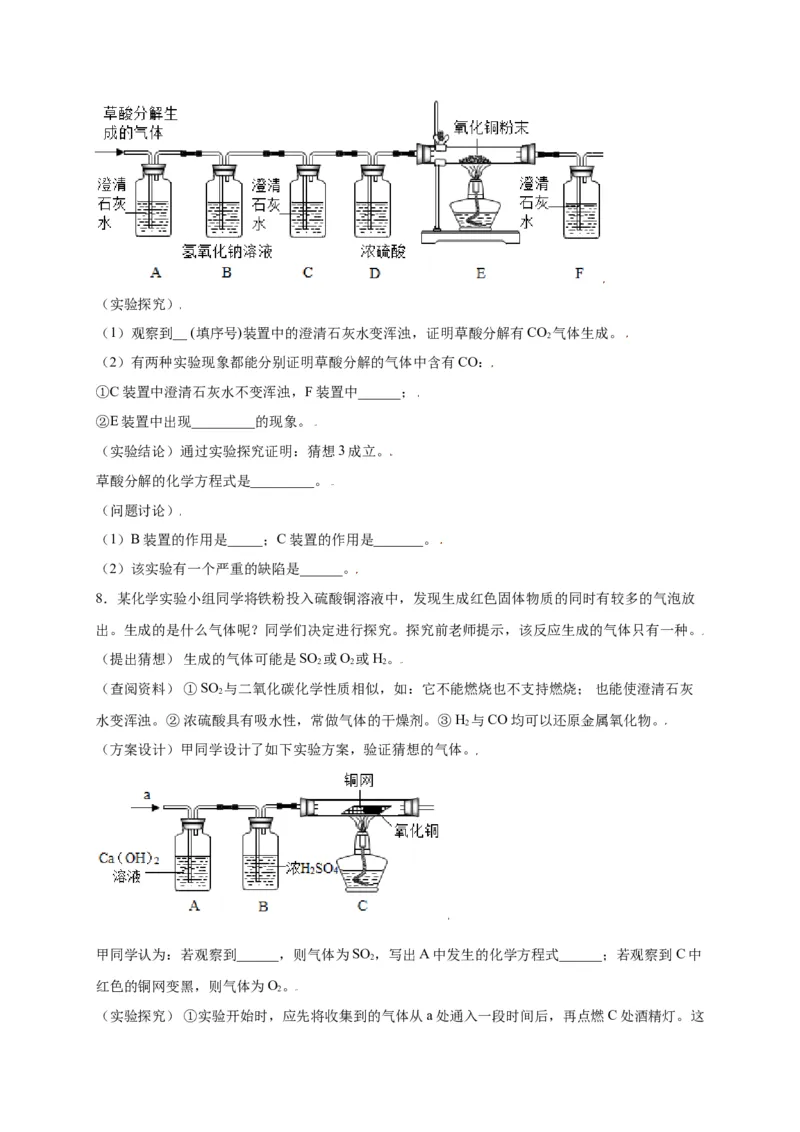
(设计实验)基于猜想3,依据CO和CO 的性质,兴趣小组同学设计了如下实验:
2(实验探究)
(1)观察到__ (填序号)装置中的澄清石灰水变浑浊,证明草酸分解有CO 气体生成。
2
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:
①C装置中澄清石灰水不变浑浊,F装置中______;
②E装置中出现_________的现象。
(实验结论)通过实验探究证明:猜想3成立。
草酸分解的化学方程式是_________。
(问题讨论)
(1)B装置的作用是_____;C装置的作用是_______。
(2)该实验有一个严重的缺陷是______。
8.某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放
出。生成的是什么气体呢?同学们决定进行探究。探究前老师提示,该反应生成的气体只有一种。
(提出猜想) 生成的气体可能是SO 或O 或H。
2 2 2
(查阅资料) ①SO 与二氧化碳化学性质相似,如:它不能燃烧也不支持燃烧; 也能使澄清石灰
2
水变浑浊。② 浓硫酸具有吸水性,常做气体的干燥剂。③ H 与CO均可以还原金属氧化物。
2
(方案设计)甲同学设计了如下实验方案,验证猜想的气体。
甲同学认为:若观察到______,则气体为SO ,写出A中发生的化学方程式______;若观察到 C中
2
红色的铜网变黑,则气体为O。
2
(实验探究) ①实验开始时,应先将收集到的气体从a处通入一段时间后,再点燃C处酒精灯。这样操作的目的是______。
②实验过程中发现 A 装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色,
试管壁上有水滴生成;
(实验结论)①铁粉与该硫酸铜溶液反应时,产生的气体是______。
②铁与硫酸铜溶液发生反应的化学方程式为______。
(实验反思)乙同学设计了一个简单的实验方案,他先收集一瓶气体,然后将燃着的木条伸入瓶中,
若______,则为SO ;若火柴燃烧更旺,则为______;若______,则为H。
2 2
9.目前,我区家庭普遍使用天然气(主要成分是甲烷CH),其燃烧后的产物可能有什么?同学
4
们开展了以下探究:
(提出问题)甲烷燃烧后生成哪些物质?
(猜想与假设)猜想一:CO、HO;
2 2
猜想二:CO、HO;
2
猜想三:CO、CO、HO
2 2
(查阅资料)白色无水CuSO 粉末遇水变蓝色
4
(设计并进行实验)将甲烷在一定量的纯净氧气中燃烧的产物依次通过下图装置,进行验证:
(1)请根据实验现象,填写实验结论。
实验现象 实验结论
A中白色粉末变为蓝色,B、E中石灰水变浑浊,D中红棕
猜想_______成立
色粉末变成黑色
(2)实验过程中C装置的作用是________;装置E的作用是________。
(3)D装置中发生反应的化学方程式是______;该反应中,发生氧化反应的物质是_____。
(4)实验过程中用纯净O 而不用空气的原因是_____。
2
(5)实验过程中A、B装置的顺序不能颠倒,原因是________。
(反思与交流)
(6)同学们一致认为:该装置存在安全缺陷,你的改正意见是________。(7)日常生活中,使用含碳燃料时,一定要加强通风,防止________中毒。
。
10.某活动小组根据如图所示进行模拟炼铁的实验,并对产物的成分进行探究。
(提出问题)黑色粉末A可能是什么呢?
(进行猜想)
(1)小明认为黑色粉末A全部是铁粉。请写出铁粉与CuSO 溶液反应的化学方程式_____。实验过
4
程中采取了过滤,该操作中用到的玻璃仪器有______、____和玻璃棒。
(2)小华认为小明的猜想是错误的,理由是___________。
(查阅资料)①铁的氧化物都能与稀盐酸,稀硫酸反应,其中氧化铁为红棕色,其余都为黑色,并
且只有四氧化三铁(该化合物中铁有+2、+3两种化合价)能被磁铁吸引。
②铁的氧化物都能与酸发生反应而溶解,生成氯化物和水,反应前后各元素化合价不变
③氯化铁溶液呈黄色。
(3)根据固体的颜色可知,黑色粉末A中肯定不含铁的氧化物中的____(写化学式);针对黑色
粉末A的成分,小华提出了猜想①和②,请结合所学知识补充余下的一个猜想。
猜想①:由铁粉和四氧化三铁(Fe O)组成;猜想②:由铁粉和氧化亚铁(FeO)组成;
3 4
猜想③:__________。
为了验证是哪一种猜想,设计了以下两个实验
(实验1)取少量黑色粉末A加入稀盐酸中,观察到有气泡,溶液颜色______,则可判断猜想②是
错误的。
(实验2)针对猜想①和猜想③,请你帮助小华完成以下实验设计
实验操作 可能的现象 结论
取少量黑色粉末A或B___________ ___________ 猜想①正确
(得出结论)在高温下,一氧化碳和氧化铁反应可生成铁或四氧化三铁。请写出生成的固体为四氧
化三铁的化学方程式___________。