文档内容
2024 年中考第一次模拟考试(武汉卷)
化 学
一、选择题(本题8小题,每小题只有一个选项符合题意。每小题3分,共24分)
1.下列物质的用途中,利用其化学性质的是( )
A.氧气用于气焊 B.浓硫酸用作干燥剂
C.铜用于制导线 D.用活性炭除去冰箱异味
【答案】A
【解析】物质的性质决定物质的用途,物质的化学性质是指在化学变化中表现出来的性质,物质的物理性
质是指不需要通过化学变化表现出来的性质,据此进行分析判断.
A、氧气用于气焊,是利用了氧气的氧化性,需要通过化学变化才表现出来,是利用了其化学性质,故选
项正确。
B、浓硫酸用作干燥剂,是利用了浓硫酸的吸水性,不需要发生化学变化就能表现出来,是利用了其物理
性质,故选项错误。
C、铜用于制导线,是利用了铜的导电性和延展性,不需要发生化学变化就能表现出来,是利用了其物理
性质,故选项错误。
D、用活性炭除去冰箱异味,是利用了活性炭的吸附性,不需要发生化学变化就能表现出来,是利用了其
物理性质,故选项错误。
故选:A。
2.正确规范的操作是实验成功和人身安全的重要保证。下列实验操作正确的是( )
A.测定溶液pH B.配制溶液
C.称量固体质量 D.稀释浓硫酸
【答案】A
【解析】A、测定溶液pH,用胶头滴管吸取液体滴到pH试纸上,将变色后的试纸与标准比色卡进行颜色
对比,A正确;B、量筒不能用于溶解,配制溶液,B错;C、托盘天平使用,左物右码,C错;D、在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水中,并不断搅拌。切不可将水倒进浓硫酸中。如果水倒进
浓硫酸中,由于水的密度小,浮在硫酸的上面,硫酸溶解时放出的热量不易散失,使水暴沸,带着酸向四
处飞溅,有可能发生意外,D错。
故选A。
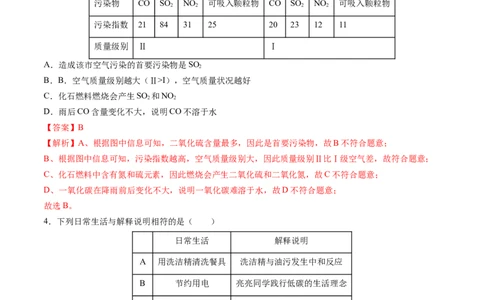
3.空气质量日报是通过新闻媒体向社会发布的环境信息,能及时准确地反映空气质量状况,增强人们对
环境的关注,提高环保意识。某市11月3日晚,下了一场大雨。下表是该市连续两天的空气质量日报。下
列说法错误的是( )
日期 2023年11月3日 2023年11月4日
污染物 CO SO NO 可吸入颗粒物 CO SO NO 可吸入颗粒物
2 2 2 2
污染指数 21 84 31 25 20 23 12 11
质量级别 Ⅱ Ⅰ
A.造成该市空气污染的首要污染物是SO
2
B.B.空气质量级别越大(Ⅱ>Ⅰ),空气质量状况越好
C.化石燃料燃烧会产生SO 和NO
2 2
D.雨后CO含量变化不大,说明CO不溶于水
【答案】B
【解析】A、根据图中信息可知,二氧化硫含量最多,因此是首要污染物,故B不符合题意;
B、根据图中信息可知,污染指数越高,空气质量级别大,因此质量级别Ⅱ比Ⅰ级空气差,故符合题意;
C、化石燃料中含有氮和硫元素,因此燃烧会产生二氧化硫和二氧化氮,故C不符合题意;
D、一氧化碳在降雨前后变化不大,说明一氧化碳难溶于水,故D不符合题意;
故选B。
4.下列日常生活与解释说明相符的是( )
日常生活 解释说明
A 用洗洁精清洗餐具 洗洁精与油污发生中和反应
B 节约用电 亮亮同学践行低碳的生活理念
C 用蜡烛照明 蜡烛燃烧生成CO 和HO
2 2
D 晾晒湿衣服 水分子的质量和体积都很小
【答案】B
【解析】A、洗洁精具有乳化作用,将油污分散为小油滴,可用于清洗餐具,日常生活与解释说明不相符,
选项不符合题意;
B、践行低碳生活理念,日常生活中可以节约用电等,日常生活与解释说明相符,符合题意;
C、用蜡烛照明,是因为蜡烛燃烧发光,日常生活与解释说明不相符,不符合题意;
D、晾晒湿衣服,是因为水分子在不断运动,运动到空气中,日常生活与解释说明不相符,不符合题意;故选B。
5.金鸡纳碱是一种抗疟药品,也是一种化学上常用的催化剂,其化学式为 ,下列关于该物质
的说法中,正确的是( )
A.该物质的相对分子质量为324g
B.该物质由20个碳原子、24个氢原子、2个氮原子和2个氧原子构成
C.该物质中碳元素质量分数为74.07%
D.该物质由碳、氢、氮、氧四种元素组成,且质量比为10∶12∶1∶1
【答案】C
【解析】
A、该物质的相对分子质量为324,不是324 g,故A不符合题意;
B、该物质的一个分子由20个碳原子、24个氢原子、2个氮原子和2个氧原子构成,故B不符合题意;
C、该物质中碳元素质量分数为 ,故C符合题意;
D、该物质由碳、氢、氮、氧四种元素组成,且质量比为(12×20)∶(1×24)∶(14×2)∶(16×2)=60∶6∶7∶8,
故D不符合题意;
故选C。
6.粗盐中含有泥沙及少量可溶性MgCl 、CaCl 、NaSO 等杂质,为获得精盐进行如图实验。叙述错误的
2 2 2 4
是:
A.根据NaCl的溶解度,可计算出溶解10g粗盐所需水的最少质量
B.只调换“过量的NaOH溶液”与“过量的BaCl 溶液”的顺序,也能达到实验目的
2
C.加入过量NaCO 溶液的目的是除尽BaCl 和CaCl
2 3 2 2
D.若称得精盐的质量为8.5g,则该粗盐样品中氯化钠的纯度是85%
【答案】D
【解析】
A、粗盐提纯的实验是在常温条件下进行的,所以可以依据氯化钠的溶解度,把粗盐看出全部是氯化钠,
可以计算出溶解10g粗盐所需水的最少质量,故A正确;
B、氢氧化钠的作用只是除去氯化镁,氯化钡可以除去硫酸钠,碳酸钠必须放在氯化钡的后面,除去过量
的氯化钡和溶液中的氯化钙,所以只调换“过量的NaOH溶液”与“过量的BaCl 溶液”的顺序,也能达
2
到实验目的,故B正确;
C、碳酸根离子和钡离子、钙离子会生成碳酸钡沉淀和碳酸钙沉淀,所以加入过量 NaCO 溶液的目的是除
2 3
尽BaCl 和CaCl ,故C正确;
2 2
D、在粗盐提纯过程中,反应生成了氯化钠,所以称得精盐的质量为 8.5g,该粗盐样品中氯化钠的纯度不
能说是85%,故D错误。故选:D。
7.氯代烃在内燃机中燃烧会生成氯化氢等气体。某氯代烃甲(化学式为C HCl)和氧气在密闭容器中反
x y z
应生成氯化氢和17.6g二氧化碳。反应前后物质的种类和分子数目如表所示。
物质 甲 氧气 氯化氢 二氧化碳
反应前分子数目 a 3a 0 0
反应后分子数目 0 a 3a 待测
下列说法错误 的是( )
A. x=2,y=3 B. 甲中氯元素的质量分数最大
C. 生成氯化氢的质量为21.9g D. 一个氧分子的质量为 g
【答案】D
【解析】
A、由表中数据可知,a个甲分子与3a-a=2a个氧分子反应生成3a个氯化氢分子,由于反应前后原子的种类
和个数不变,则1个甲分子中含有3个氢原子和3个氯原子,则y=z=3,又由于二氧化碳中的氧元素全部
来自氧气,则反应后二氧化碳分子个数为2a,再根据原子守恒,则1个甲分子中含有2个碳原子,则
x=2,该选项说法正确;
B、由前面分析可知,甲的化学式为C HCl,甲中碳元素、氢元素、氯元素的质量比为(12×2):
2 3 3
(1×3):(35.5×3)=8:1:35.5,则氯元素的质量分数最大,该选项说法正确;
C、由于反应的化学方程式为 ,且生成二氧化碳的质量为17.6g,设生
成的氯化氢的质量为x,则 , ,解得
x=21.9g,该选项说法正确;
D、设消耗的氧气的质量为y,则 , ,解得
y=12.8g,而消耗的氧分子的个数为2a,则一个氧分子的质量为 ,该选项说法不正确。
故选D。
8.小颖同学为比较Mg、Fe、Cu三种金属的活动性顺序进行了如图甲所示的实验,实验后把两试管中的
物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤,再向滤渣中加入适量稀盐酸, 产生无色气泡。根据上述信息,判断下列说法正确的是( )
A.原a、b试管中溶液都一定呈浅绿色
B.滤液中一定含有Mg2+、Fe2+,可能含有Cu2+
C.滤渣质量一定大于所加铁粉的总质量
D.滤渣含有三种固体物质
【答案】C
【解析】 三种金属的活动性顺序为 ,铁粉和硫酸镁不反应,铁粉和硫酸铜
反应生成铜和硫酸亚铁,发现烧杯内的红色固体明显增多,说明有铜生成,充分反应后过滤,若硫酸铜完
全反应,溶液中的阳离子是镁离子和亚铁离子,若硫酸铜没有完全反应,溶液中的阳离子是镁离子、亚铁
离子和铜离子。
A、原a试管中铁粉和硫酸镁不反应,溶液是无色的,b试管中铁粉和硫酸铜反应生成铜和硫酸亚铁,溶液
呈浅绿色,故A不正确;
B、充分反应后过滤再向滤渣中加入适量稀盐酸, 产生无色气泡,说明铁有剩余,则则滤液中一定含有
,不可能含有 ,故B不正确;
C、铁和硫酸铜反应生成硫酸亚铁和铜,56份铁置换出64份铜,质量增加,则滤渣质量一定大于所加铁粉
的总质量,故C正确;
D、滤渣含有铁和铜两种固体物质,故D不正确。
故选C。
二、非选择题(本题包括5小题,共26分)
9.(5分)请根据如图回答问题:
(1)实验A为测定白醋的酸碱度,若先用水润湿pH试纸,则测得结果与实际值相比 (选填“偏
大”或“偏小”)。
(2)实验B为验证质量守恒定律。实验时若取用红磷的量不足,对实验的结果 (选填“有”或“没有”)影响。
(3)实验C反应停止后溶液中的溶质一定有氯化钙,可能还有 ,反应后从溶液中要得到氯化
钙固体需要用到上述 装置(填编号)。
(4)实验C还可用于制取氧气,写出反应的化学方程式 。
【答案】(1)偏大 (2)没有 (3)氯化氢 E (4)2HO 2HO+O↑
2 2 2 2
【解答】解:(1)实验A为测定白醋的酸碱度,若先用水润湿pH试纸,则测得结果与实际值相比偏大;
故答案为:偏大;
(2)实验B为验证质量守恒定律。实验时若取用红磷的量不足,对实验的结果没有影响,因为反应是在
密闭装置中;故答案为:没有;
(3)实验C反应停止后溶液中的溶质一定有氯化钙,可能还有氯化氢,反应后从溶液中要得到氯化钙固
体需要用到蒸发操作;故答案为:氯化氢;E;
(4)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧
气,要注意配平;故答案为:2HO 2HO+O↑
2 2 2 2
10.(4分)室温20℃时,将129.0gNaOH固体加入到100g水中,搅拌后固体全部消失,放置到t 时刻开
1
始析出固体,到t 时刻析出10g固体。
2
已知:NaOH、Ca(OH) 在不同温度下的溶解度如下表所示。
2
温度℃ 0 10 20 30 50
NaOH溶解度/g 42.0 51.0 109.0 119.0 129.0
Ca(OH) 溶解度/g 0.18 0.17 0.16 0.15 0.13
2
(1)20℃时NaOH的溶解度为 g
(2)t 时刻所得溶液为 (填“饱和”或“不饱和”)溶液。
1
(3)20℃时,实验中常用NaOH溶液吸收CO 而不用Ca(OH) 溶液的原因: 。
2 2
(4)另称取11.55g氢氧化钠固体样品(含少量氢氧化钙)先将其全部溶于10g水中,再冷却到室温20℃
时,析出固体0.5g,下列说法正确的是______。
A.常温下NaOH易溶于水,Ca(OH) 微溶于水
2
B.t 时刻溶液的温度高于50℃,t 时刻溶液的温度为30℃
1 2
C.实验能证明NaOH固体溶于水放出热量
D.11.55g固体样品中氢氧化钙的质量为0.15g
【答案】(1)109.0 (2)饱和
(3)20℃时NaOH的溶解度远远大于Ca(OH) 的 溶解度,能吸收更多的CO 气体 (4)AC
2 2
【解析】(1)由表中数据知,20℃时NaOH的溶解度为109.0g。
(2)t 时刻析出固体,说明溶液中再不能溶解该固体,此时为饱和溶液。
1
(3)20℃时,NaOH的溶解度远远大于Ca(OH) 的溶解度,能吸收更多的CO 气体,故实验中常用NaOH
2 2溶液吸收CO
2。
(4)A、物质的溶解性是根据在20℃(室温)时的溶解度来划分的,溶解度大于10g,属于易溶物质;溶
解度大于1g,属于可溶物质;溶解度在0.01g~1g之间的,属于微溶物质;小于0.01g的,属于难溶物质。
根据表格数据知,常温下NaOH易溶于水,Ca(OH) 微溶于水,选项正确;
2
B、50℃时氢氧化钠的溶解度为129.0g,t 时129.0gNaOH固体完全溶解到100g水中,则溶液的温度
1
≥50℃,t 时析出10g固体,溶质质量为119.0g,即t 为30℃,选项错误;
2 2
C、室温20℃时,氢氧化钠溶解度为109.0g,将129.0gNaOH固体加入到100g水中,搅拌后固体全部消失,
说明氢氧化钠溶于水放热,温度升高,选项正确;
D、氢氧化钠溶解度随温度升高而增大,氢氧化钙溶解度随温度升高而减小,故冷却到室温20℃时,析出
的固体为氢氧化钠,此时溶液中氢氧化钠达到饱和,室温20℃时,氢氧化钠溶解度为109.0g,即10g水中
最多溶解10.9g的氢氧化钠,理论上则11.55g固体样品中氢氧化钙的质量为11.55g-0.5g-10.9g=0.15g,但是
该温度下氢氧化钙的溶解度只有0.16g,10g水中最多溶解0.016g氢氧化钙,故选项错误。
故选AC。
11.(5分)如图所示转化关系涉及的物质均为初中化学常见的物质。其中甲为单质,戊为绿色植物光合
作用的反应物。这些物质之间的反应与转化关系如图所示(“→”表示某一物质通过一步能转化为另一物
质,“—”表示连接的两种物质之间能反应,部分反应物、生成物及反应条件已略去)。
请回答下列问题。
(1)若乙是人体胃液中含有的酸:
①当丁是大理石的主要成分时,戊的名称是 。
②当丙是可做食品干燥剂的白色固体时,“乙—丁”反应的化学方程式是 。
(2)若乙是赤铁矿的主要成分:
①当丙为单质时,“乙—丁”反应的实验现象是 ;“丙→丁”反应 热量
(填序号:a.放出、b.吸收、c.既可能放出也可能吸收)。
②当丁为单质时,下列说法正确的是 。(填序号)
A.甲与丙能够反应生成丁 B.丁可以做燃料或冶炼金属
C.“丁→戊”反应属于化合反应 D.“戊→丁”反应中各元素的化合价均发生改变
【答案】(1) 二氧化碳
(2) 红棕色固体逐渐变黑 c ABD
【解析】(1) 若乙是人体胃液中含有的酸,则乙是盐酸;
①当丁是大理石的主要成分时,则丁是碳酸钙;戊为绿色植物光合作用的反应物,能和碳酸钙相互转化,
则戊的名称是二氧化碳;②当丙是可做食品干燥剂的白色固体时,则丙是氧化钙;氧化钙转化成的丁能和盐酸反应,则丁是氢氧化钙;
所以“乙—丁”的反应是盐酸和氢氧化钙反应生成氯化钙和水,反应的化学方程式是:
;
(2)若乙是赤铁矿的主要成分,则乙是氧化铁;
①当丙为单质时,丙能和氧化铁反应,丙转化成的丁也能和氧化铁反应,则丙是碳,丁是一氧化碳;所以
“乙一丁”的反应是氧化铁和一氧化碳在高温的条件下生成铁和二氧化碳,反应的实验现象是红棕色固体逐
渐变黑;
“丙- 丁”的反应可以是碳在氧气不足时燃烧生成一氧化碳,该反应放热,也可以是碳和二氧化碳在高温
的条件下生成一氧化碳,该反应吸热,所以该反应既可能放出也可能吸收热量,故选:c;
②当丁为单质时,丁能和氧化铁反应,丁能和氧化铁转化成的戊相互转化,则丁是氢气。戊是水;甲为单质,
氧化铁能转化成甲,则甲是铁;丙能和氧化铁反应,能转化成氢气,则丙可以是盐酸;
A、甲是铁,丙可以是盐酸,丁是氢气,铁与盐酸能够反应生成氢气,故选项说法正确;
B、丁是氢气,氢气可以做燃料或冶炼金属,故选项说法正确;
C、丁是氢气,戊是水,“丁→戊”的反应可以是氢气和氧气在点燃的条件下生成水,该反应属于化合反
应,也可以是氢气和氧化铜在加热的条件下生成铜和水,该反应属于置换反应,故选项说法不正确;
D、戊是水,丁是氢气,“戊→丁”反应是水在通电的条件下生成氢气和氧气,氢元素从+ 1价变为0价,
氧元素从- 2价变为0价,则各元素的化合价均发生改变,故选项说法正确;
故选:ABD。
12.(7分)烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中常含有杂质碳酸钠。某科学学习小
组同学围绕工业烧碱样品纯度测定问题,展开了讨论与探究。
(原理思路)利用NaCO 与稀HSO 反应产生CO,通过CO 质量的测定,确定样品中碳酸钠的质量,从
2 3 2 4 2 2
而计算样品纯度。
(实验方案)小华同学根据以上思路,设计了如图的实验方案(固定装置省略)。
(交流讨论)(1)小明认为上图实验方案的设计有缺陷,会导致难以避免的误差。你认为下列哪些因素
会导致实验结果偏高 (填序号)。
①加入的稀硫酸量不足 ②装置内空气中的CO 没有排出
2
③反应产生的CO 未被完全吸收 ④干燥管与空气直接相通
2
(方案改进)为减少误差,使CO 质量的测定更准确,该小组同学根据以上讨论,对上图方案进行改进,
2
设计了如下图的实验方案(固定装置省略)。(2)装置B中样品在与稀硫酸反应前和停止反应后,都要通过量的空气。反应前通空气时a、b、c三个弹
簧夹的控制方法是 。
(3)写出装置A中发生反应的化学方程式: 。
(数据分析)
(4)若反应过程中,装置B中滴加稀硫酸的速度太快,则烧碱的纯度将 (填“偏高”、“偏低”或“无
影响”)。
(5)若原样品共Ag,实验结束测得C装置增重Bg,D装置增重Cg,则原样品的纯度(质量分数)为
。
(拓展延伸)
(6)D装置用装有氢氧化钠固体的U形管,而不用装有澄清石灰水的洗气瓶的原因: ;
(7)实验结束后,小华、小明一起探讨时,发现按目前所学知识还有其它实验方案测定工业烧碱样品纯
度,方法是:取样品溶于水,滴加入过量的氯化钡溶液,过滤、洗涤、干燥、称量 的质量,再计算
出碳酸钠的质量,最后计算出其纯度。
【答案】(1)①③ (2)关闭c、打开a、b (3) 2NaOH+CO =Na CO+H O (4)偏高 (5)
2 2 3 2
(6)氢氧化钙微溶于水,所以石灰水可能无法将生成的二氧化碳完全吸收 (7)沉
淀
【解析】
(1)①加入的稀硫酸量不足、②装置内空气中的CO 没有排出、③反应产生的CO 未被完全吸收这三种
2 2
情况会导致二氧化碳质量偏低,计算出的碳酸钠质量偏小,而造成计算出的烧碱的纯度结果偏高;而④干
燥管与空气直接相通,氢氧化钠还会吸收空气中的二氧化碳和水蒸气,造成计算出的碳酸钠的质量偏大,
导致计算出的烧碱纯度结果偏低;故填:①②③;
(2)反应前通空气时,关闭c、打开a、b,可以把B、C装置中的二氧化碳排出,使实验结果更准确。
停止反应后,通过量的空气的目的是使生成的二氧化碳被氢氧化钠完全吸收;故填:关闭c、打开a、b;
使生成的二氧化碳被氢氧化钠完全吸收;
(3)空气通过氢氧化钠溶液时,空气中的二氧化碳与氢氧化钠反应生成碳酸钠和水;故填:
2NaOH+CO =Na CO+H O;
2 2 3 2
(4)若反应过程中,装置B中滴加稀硫酸的速度太快,在生成的二氧化碳就不能被氢氧化钠固体完全吸
收,造成计算出的碳酸钠的质量偏小,那么则烧碱的纯度将偏高;故填:偏高;
(5)D装置增重Cg,即生成了Cg的二氧化碳,设需要碳酸钠的质量为x,则:则原样品的纯度(质量分数)为: ;故填: 。
(6)氢氧化钙微溶于水,所以石灰水可能无法将生成的二氧化碳完全吸收,所以D装置用装有氢氧化钠
固体的U形管,而不用装有澄清石灰水的洗气瓶;故填:氢氧化钙微溶于水,所以石灰水可能无法将生成
的二氧化碳完全吸收;CO+Ca(OH)=CaCO ↓+H O;
2 2 3 2
(7)还可以采用沉淀法来测定样品的纯度,即取一定量的烧碱样品完全溶解于水中,然后向溶液中逐
滴加入氯化钡溶液,直到不再产生沉淀为止,过滤、洗涤、干燥、称量沉淀的质量,然后利用生成的碳酸
钡沉淀的质量,利用化学方程式NaCO+BaCl =BaCO ↓+2NaCl计算出碳酸钠的质量,最后根据烧碱样品
2 3 2 3
的质量即可计算出其纯度;故填:取一定量的烧碱样品完全溶解于水中,然后向溶液中逐滴加入氯化钡溶
液,直到不再产生沉淀为止,过滤、洗涤、干燥、称量沉淀的质量,然后利用生成的碳酸钡沉淀的质量,
利用化学方程式NaCO+BaCl =BaCO ↓+2NaCl计算出碳酸钠的质量,最后根据烧碱样品的质量即可计算
2 3 2 3
出其纯度。
13.(5分)2022年国产技术打造的氢燃料客车,服务于北京冬奥会和冬残奥会。工业上大规模生产 的
一种方法是利用天然气中的甲烷和水进行反应,其微观示意图如下:
请计算:
(1)甲烷中碳元素的质量分数是 ;
(2)理论上生产2t ,所消耗水的质量是多少t?
【答案】(1)75% (2)6t。
【解析】由反应的微观示意图可知,甲烷和水在催化剂和高温条件下生成CO和H,反应的化学方程式为
2
CH+H O CO+3H。
4 2 2
(1)甲烷中碳元素的质量分数为 ×100%=75%,故填:75%;
(2)解:设理论上生产2t ,所消耗水的质量为x答:理论上生产2t ,所消耗水的质量是6t。