文档内容
2024 年中考第三次模拟考试(武汉卷)
化 学
(考试时间:50分钟 试卷满分:50分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 S-32 Cl-35.5 Cu-64
第Ⅰ卷
一、选择题(本题8小题,每小题只有一个选项符合题意。每小题3分,共24分)
1.酒精常用作消毒剂、燃料和溶剂等。酒精的以下性质中,属于化学性质的是( )
A.挥发性 B.可燃性 C.易溶解 D.有香味
【答案】B
【解析】A、挥发性属于物理性质,故选项错误;
B、可燃性属于化学性质,故选项正确;
C、易溶解,溶解性属于物理性质,故选项错误;
D、有香味,气味属于物理性质,故选项错误。
故选:B。
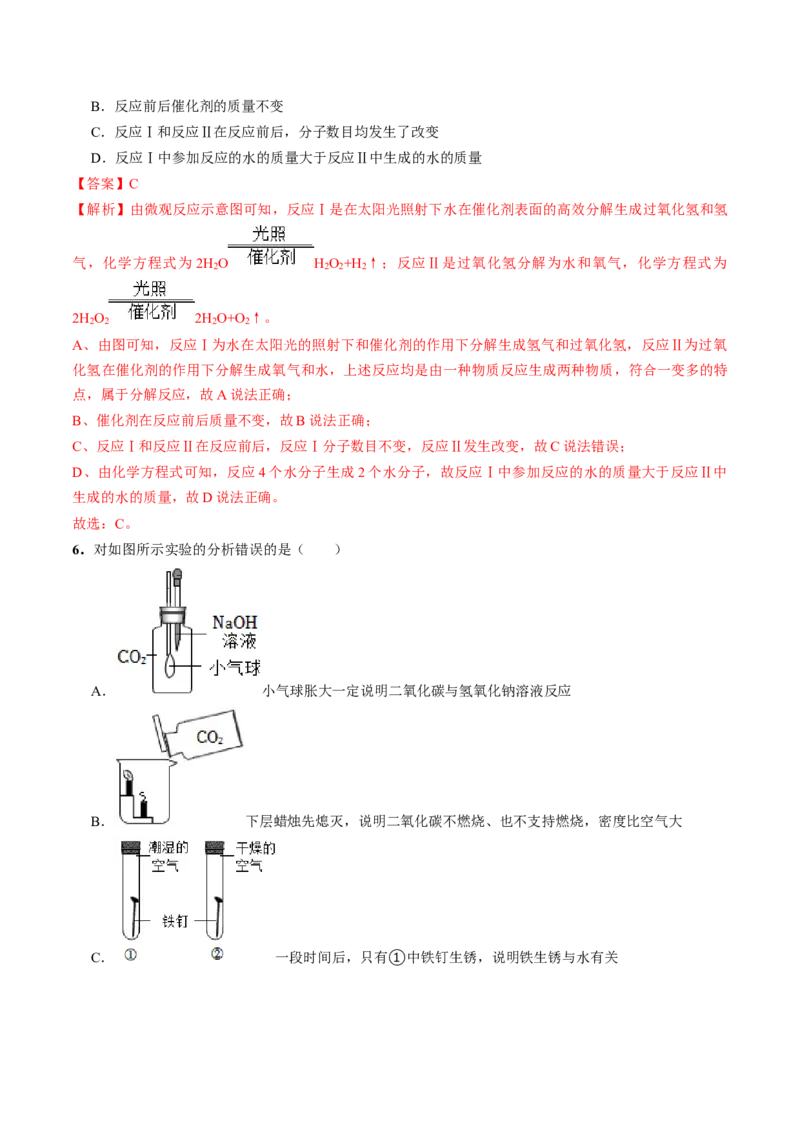
2.正确的实验操作是保证实验安全和顺利进行的前提,下列实验操作正确的是( )
A. 点燃酒精灯 B. 加热液体
C. 取用固体药品 D. 称量NaCl
【答案】B
【解析】A、禁止用燃着的酒精灯点燃另一只酒精,否则导致酒精外溢,引发火灾,该选项操作不正确;
B、加热液体时,液体体积不能超过试管容积的三分之一,且用酒精灯外焰加热,试管夹夹在据试管口的
三分之一处,该选项操作正确;
C、实验室中,不能用手直接拿药品,否则易导致手被腐蚀,该选项操作不正确;
D、用托盘天平称量药品时,应左物右码,而图中右物左码,该选项操作不正确。故选:B。
3.化学符号含义丰富,下列化学用语表示正确的是( )
A.4个磷原子:P4 B.3个氧分子:3O
2
C.碳酸根离子: D.氢氧化钡:BaOH
2
【答案】B
【解析】A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上
相应的数字,故4个磷原子表示为:4P,故A错误;
B、由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,
则三个氧分子可表示为:3O ,故B正确;
2
C、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负
符号在后,带1个电荷时,1要省略,则碳酸根离子可表示为 ,故C错误;
D、氢氧化钡中氢氧根显﹣1价,钡显+2价,则氢氧化钡的化学式是:Ba(OH) ,故D错误。
2
故选:B。
4.劳动创造美好生活。如表劳动项目所涉及的化学知识不正确的是( )
选项 劳动项目 化学知识
A 用食醋除去暖水瓶中的水垢 食醋的pH>7
B 给铁制楼梯扶手刷油漆防锈 油漆能隔绝水和氧气
C 用洗洁精清洗餐具上的油污 洗洁精有乳化功能
D 用熟石灰改良校园农场酸性土壤 熟石灰中含有OH﹣
【答案】A
【解析】A、食醋显酸性,食醋的pH<7,故说法错误;
B、给铁制楼梯扶手刷油漆防锈,油漆能隔绝水和氧气,利用的是隔绝氧气和水的原理,故说法正确;
C、用洗洁精清洗餐具上的油污,是因为洗洁精有乳化功能,能使植物油分散成无数细小的液滴,而不聚
成大的油珠,故说法正确;
D、用熟石灰改良校园农场酸性土壤,是因为熟石灰中含有OH﹣,故说法正确。
故选:A。
5.在太阳光的照射下,一种新型催化剂能帮助水高效分解获得氢气。该反应过程的微观示意图如图,下
列说法不正确的是( )
A.反应Ⅰ、Ⅱ均为分解反应B.反应前后催化剂的质量不变
C.反应Ⅰ和反应Ⅱ在反应前后,分子数目均发生了改变
D.反应Ⅰ中参加反应的水的质量大于反应Ⅱ中生成的水的质量
【答案】C
【解析】由微观反应示意图可知,反应Ⅰ是在太阳光照射下水在催化剂表面的高效分解生成过氧化氢和氢
气,化学方程式为 2H O H O +H ↑;反应Ⅱ是过氧化氢分解为水和氧气,化学方程式为
2 2 2 2
2H O 2H O+O ↑。
2 2 2 2
A、由图可知,反应Ⅰ为水在太阳光的照射下和催化剂的作用下分解生成氢气和过氧化氢,反应Ⅱ为过氧
化氢在催化剂的作用下分解生成氧气和水,上述反应均是由一种物质反应生成两种物质,符合一变多的特
点,属于分解反应,故A说法正确;
B、催化剂在反应前后质量不变,故B说法正确;
C、反应Ⅰ和反应Ⅱ在反应前后,反应Ⅰ分子数目不变,反应Ⅱ发生改变,故C说法错误;
D、由化学方程式可知,反应4个水分子生成2个水分子,故反应Ⅰ中参加反应的水的质量大于反应Ⅱ中
生成的水的质量,故D说法正确。
故选:C。
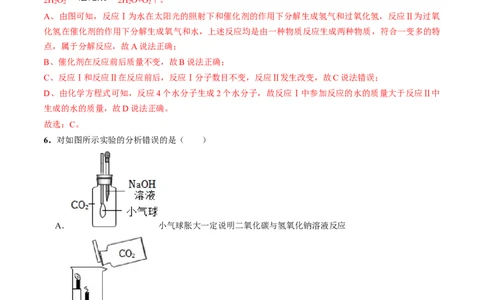
6.对如图所示实验的分析错误的是( )
A. 小气球胀大一定说明二氧化碳与氢氧化钠溶液反应
B. 下层蜡烛先熄灭,说明二氧化碳不燃烧、也不支持燃烧,密度比空气大
C. 一段时间后,只有①中铁钉生锈,说明铁生锈与水有关D. 干冷的烧杯内壁有水珠生成,说明蜡烛中含有氢元素
【答案】A
【解析】A、小气球胀大,不一定说明二氧化碳与氢氧化钠溶液反应,也可能是二氧化碳溶于水造成的,
故说法错误;
B、下层的蜡烛先熄灭,上层的蜡烛后熄灭,说明了CO 密度比空气的大;蜡烛熄灭,说明了二氧化碳不
2
能燃烧,也不能支持燃烧,故说法正确;
C、一段时间后,试管①中的铁钉能与氧气、水充分接触,试管②中的铁钉只能与干燥的空气接触,只有
①中铁钉生锈,说明铁生锈与水有关,故说法正确;
D、在火焰上方罩一个干冷的烧杯,烧杯内壁出现水雾,说明生成了水,水是由氢元素和氧元素组成的,
反应物氧气中只含有氧元素,说明蜡烛中一定含有氢元素,故说法正确。
故选:A。
7.已知下列物质的转化都是一步实现:① CaCO →Ca(NO ) ② Ca(OH) →Ca(NO )
3 3 2 2 3
③CaCl →Ca(NO ) ,下列相关说法不正确的是( )
2 2 3 2
A.转化①反应后溶液质量一定增大
B.转化②可以通过加入硝酸铜溶液来实现
C.三个转化中一定都有明显现象
D.三个转化中发生的反应一定都是复分解反应
【答案】C
【解析】A.①CaCO →Ca(NO ) ,只能通过碳酸钙和硝酸反应生成硝酸钙、二氧化碳和水来实现,根
3 3 2
据 CaCO +2HNO =Ca(NO ) +H O+CO ↑可知,每100份质量的碳酸钙参加反应就生成44份质量的二
3 3 3 2 2 2
氧化碳,根据质量守恒定律反应后溶液质量一定增大,故正确;
B.②Ca(OH) →Ca(NO ) ,可以是氢氧化钙和硝酸铜反应生成氢氧化铜沉淀和硝酸钙,故正确;
2 3 2
C.②Ca(OH) →Ca(NO ) 可以是氢氧化钙和硝酸反应生成硝酸钙和水,没有明显现象,故错误;
2 3 2
D.三个反应都是两种化合物相互交换成分生成两种新的化合物,都属于复分解反应,故正确。
故选:C。
8.某课题小组模拟工业海水提镁的流程,在实验室制取生产镁的原料——MgCl ,设计方案如图:
2
已知:①海水和苦卤中都含有NaCl、Na SO 、MgCl 、CaCl 、KCl等。
2 4 2 2②苦卤是海水晒盐后剩余的溶液。
③如表是某品牌不同碱的价格。
试剂 NaOH Ca(OH) Ba(OH) KOH
2 2
价格(元/吨) 2400 850 5300 5500
下列说法不正确的是( )
A.海水和苦卤都可以作为制取MgCl 的原料,选择苦卤更好
2
B.在工业生产中为了降低成本,试剂X最好选择表格中的Ca(OH)
2
C.该方案制取MgCl 时,要经历步骤Ⅰ和步骤Ⅱ两步转化,其主要目的是提纯、富集MgCl
2 2
D.小组同学最终制得19.0g干燥纯净的MgCl 固体。若步骤Ⅱ中稀盐酸与Mg(OH) 恰好完全反应,
2 2
且步骤Ⅲ中MgCl 没有损失,则步骤Ⅱ中消耗稀盐酸的质量为14.6g
2
【答案】D
【解析】A、海水中Mg2+的浓度很小,如果直接取海水加入碱使Mg2+转化成氢氧化镁沉淀,将消耗大量碱,
生产成本非常高,生产效率非常低,而苦卤是海水晒盐后剩余的溶液,由于水分的大量蒸发,苦卤中
Mg2+的浓度大大提高,使苦卤中的Mg2+转化成氢氧化镁沉淀所需要的碱将大大减少,降低了生产成本,提
高了生产效率,同时还实现了资源的综合利用,故A正确;
B、在工业生产中为了降低成本,必须选择既符合生产要求,又总价低的试剂;假设生产同样多的氢氧化
镁比如58吨,根据四种碱与氯化镁反应生成氢氧化镁的关系:2NaOH~Mg(OH) ,Ca(OH) ~Mg
2 2
(OH) ,Ba(OH) ~Mg(OH) ,2KOH~Mg(OH) ,计算可知,需要:氢氧化钠80吨,总价
2 2 2 2
192000元;氢氧化钙74吨,总价62900元;氢氧化钡171吨,总价906300元;氢氧化钾112吨,总价
616000元,因此试剂X最好选择表格中的Ca(OH) ,故B正确;
2
C、该方案制取氯化镁时,要经历步骤Ⅰ和步骤Ⅱ两步转化,步骤Ⅰ是加入足量的氢氧化钙,将苦卤中的
Mg2+转化为氢氧化镁沉淀(此时其他离子不能生成沉淀),经过过滤、洗涤得到纯净的氢氧化镁固体;步
骤Ⅱ向氢氧化镁中加入适量10%的稀盐酸,氢氧化镁与盐酸完全反应生成氯化镁,通过步骤Ⅰ和步骤Ⅱ两
步转化,除去了苦卤中原来跟Mg2+混杂在一起的其他离子,得到纯净的氯化镁溶液,因此经历步骤Ⅰ和步
骤Ⅱ两步转化的主要目的是:得到纯净的氯化镁溶液,故C正确;
D、设步骤Ⅱ中消耗稀盐酸的质量为x
Mg(OH) +2HCl=MgCl +2H O
2 2 2
73 95
x×10% 19.0g
解得x=146.0g
故步骤Ⅱ中消耗稀盐酸的质量为146.0g,故D错误。
故选:D。
第Ⅱ卷二、非选择题(本题包括5小题,共26分)
9.(4分)中华典籍中包含很多化学知识。
(1)《齐民要术》中记载古法酿醋是用粮食经过发酵而成,醋酸的化学式为C H O ,它由 种
2 4 2
元素组成的。
(2)《梦溪笔谈》中记载“熬胆矾铁釜,久之易化为铜”。叙述的是铁和硫酸铜的反应,说明铁的活
动性比铜 (选填“强”或“弱”)。
(3)《天工开物》中记载“凡石灰,经火焚炼为用”,描述的是煅烧石灰石的过程,反应的化学方程
式为 。
【答案】(1)3 (1分)
(2)强(1分)
(3)(3)CaCO CaO+CO ↑(2分)
3 2
【解析】(1)古法酿醋是用粮食经过发酵而成,发酵过程中生成了新物质醋酸等,属于化学变化;醋酸
的化学式为C H O ,醋酸是含有碳元素的化合物,属于有机物,0.5molC H O 中约含有1mol氧原子,约
2 4 2 2 4 2
含有6.02×1023个氧原子;
(2)“熬胆矾(硫酸铜)铁釜,久之亦化为铜”,其涉及的反应为铁和硫酸铜反应生成硫酸亚铁和铜,
铁能将铜盐溶液中的铜置换出来,说明铁的活动性比铜强,此反应是一种单质和一种化合物生成另一种单
质和另一种化合物,属于置换反应;
(3)煅烧石灰石生成氧化钙和二氧化碳,反应的化学方程式为:CaCO CaO+CO ↑。
3 2
10.(4分)请根据如图所示的a、b、c三种物质的溶解度曲线,回答下列问题:
(1)在t ℃时,向盛有50ga物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为 g。
2
(2)若a物质中混有少量b物质,最好采用 (填“降温结晶”或“蒸发结晶”)的方法
提纯a物质。
(3)t ℃时a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是 。
2
(4)下列说法正确的是 (填字母)。
A.将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
B.将t ℃时c物质的饱和溶液升温到t ℃,其溶液的质量一定减小
1 2
C.配制一定溶质质量分数的b物质溶液。若量取水时,仰视读数,其他操作均正确,则配制的b溶液中
溶质质量分数一定偏大【答案】(1)75(1分)
(2)降温结晶(1分)
(3)(3)c>b>a(1分)
(4)(4)B(1分)
【解析】(1)在t ℃时,a物质的溶解度是50g,所以向盛有50ga物质的烧杯中加入50g水,只能溶解
2
25g,所得溶液的质量为75g;
(2)a物质溶解度受温度影响大,b物质溶解度受温度影响不大,所以若a物质中混有少量b物质,最好
采用降温结晶的方法提纯a;
(3)t ℃时a、b、c三种物质的溶解度关系为a>b>c,所以 t ℃时a、b、c三种物质 的饱和溶液各
2 2
100g,所含溶剂的质量由大到小的顺序是 c>b>a;
(4)A、若采用升高温度将a物质的饱和溶液变为不饱和溶液,溶质的质量分数不变,故错误;
B、将t ℃时c物质的饱和溶液升温到t ℃,会析出晶体,所以其溶液的质量一定减小,故正确;
1 2
C、配制一定溶质质量分数的b物质溶液。若量取水时,视线与凹液面最低处保持水平,则操作正确,若
不是最低处,则操作错误,会影响正确读数,故错误。
故选:B。
11.(6分)钨(W)是一种重要的战略资源。如图是生产钨的一种工业流程。
已知:
①白钨矿的主要成分是钨酸钙(CaWO ),还含有CaO、SiO 等。
4 2
②碳在高温条件下会与金属钨反应生成碳化钨。
③浸出率是衡量在浸取过程中,固体中可溶性物质溶入浸出液中的百分率的指标。浸出率越高,金属
的提取率就越好。
请回答下列问题:
(1)操作1粉碎白钨矿的目的是 。( 2 ) “ 酸 浸 ” 时 适 当 升 高 温 度 会 提 高 浸 出 率 , 但 温 度 不 宜 太 高 , 原 因 是
。
(3)操作2所得滤液中一定含有的溶质是 (填化学式)。
(4)氨水(NH •H O)与钨酸发生反应的化学方程式为 。
3 2
(5)用氢气 还原 WO 可获得高纯度 的钨,此处不 宜用焦炭代替 氢气的原因是
3
。
【答案】(1)增大接触面积,使反应更加充分(1分)
(2)温度太高,盐酸挥发太快,降低浸出率(1分)
(3)CaC1 、HCl(1分)
2
(4)H WO +2NH •H O=(NH ) WO +2H O(2分)
2 4 3 2 4 2 4 2
(5)碳在高温条件下会与金属钨反应生成碳化钨(1分)
【解析】(1)操作1中粉碎白钨矿的目的是增大反应物的接触面积,使反应更快更充分;
(2)盐酸具有挥发性,“酸浸”时适当升高温度会提高浸出率,但温度不宜太高,原因为温度太高,加
速盐酸挥发,降低浸出率;
(3)操作2后,得到H WO 、SiO ,稀盐酸会与氧化钙,CaWO 反应,则操作2所得滤液中一定含有的
2 4 2 4
阳离子是Ca2+,因为加入过量盐酸,所以滤液中还含有H+,所得滤液中一 定含有的溶质是CaCl 、HCl;
2
(4)氨水(NH 3⋅H
2
O)与钨酸发生中和反应,生成(NH
4
)
2
WO
4
和的水,化学方程式为:
2NH 3⋅H
2
O+H
2
WO
4
=(NH
4
)
2
WO
4
+2H
2
O;
(5)根据题中提供的信息可知,用氢气还原 WO 可获得高纯度的钨,此处不宜用焦炭代替氢气的原因是
3
碳在高温条件下会与金属钨反应生成碳化钨。
12.(6分)中国在南海成功试采可燃冰,它将推动世界能源利用格局的改变。可燃冰是在高压低温环境
条件下,水分子笼中装有甲烷分子而成“冰块”。已知某种可燃冰的化学式为:CH •8H O。某校化学
4 2
兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与:
【提出问题】甲烷燃烧后生成哪些物质?
【查阅资料】①含碳元素的物质完全燃烧生成CO ,不完全燃烧生成CO;
2
②无水CuSO 遇水变蓝;
4
③氢氧化钠溶液与二氧化碳反应没有明显现象,常用于吸收二氧化碳气体。
【猜想与假设】
(1)甲:CO 、H O;乙:CO、H O;丙:NH 、H O;丁:CO 、CO、H O。
2 2 2 3 2 2 2
【实验探究】为了验证上述猜想与假设,将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置,
进行验证:【实验结论】
(1)B装置的作用是 ,装置中澄清石灰水变浑浊,其反应的化学方程
式为 ;
(2)红棕色氧化铁变成黑色,E装置中澄清石灰水也变浑浊,则证明甲烷燃烧产物中有 ;
(3)由此推断丁的猜想成立。
【交流反思】
(4)AB装置的顺序不能颠倒,理由是 ;
(5)为避免有毒的CO污染环境,所有含碳元素的物质燃烧必须满足的条件是 。
【答案】(1)检验产物中是否有二氧化碳气体(1分) Ca(OH) +CO =CaCO ↓+H O(2分)
2 2 3 2
(2)一氧化碳(1分)
(4)颠倒后无法确定水来自生成物还是澄清石灰水(1分)
(5)与充足的氧气(或空气)接触(1分)
【解析】(1)B中装有的是石灰水,二氧化碳能使石灰水变浑浊,因此装置B的作用是检验二氧化碳;
装置中澄清石灰水变浑浊,说明二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,其反应的化学方程式为:
Ca(OH) +CO =CaCO ↓+H O;
2 2 3 2
(2)红棕色氧化铁变成黑色,E装置中澄清石灰水也变浑浊,说明氧化铁被还原剂还原且生成物中有二氧
化碳,由此可推断是一氧化碳;因为一氧化碳能和氧化铁反应生成铁和二氧化碳,而二氧化碳能使石灰水
变浑浊;
(4)AB装置的顺序不能颠倒,颠倒后无法确定水来自生成物还是澄清石灰水;
(5)由于含碳元素的物质不充分燃烧会生成一氧化碳,因此要与充足的氧气(或空气)接触。
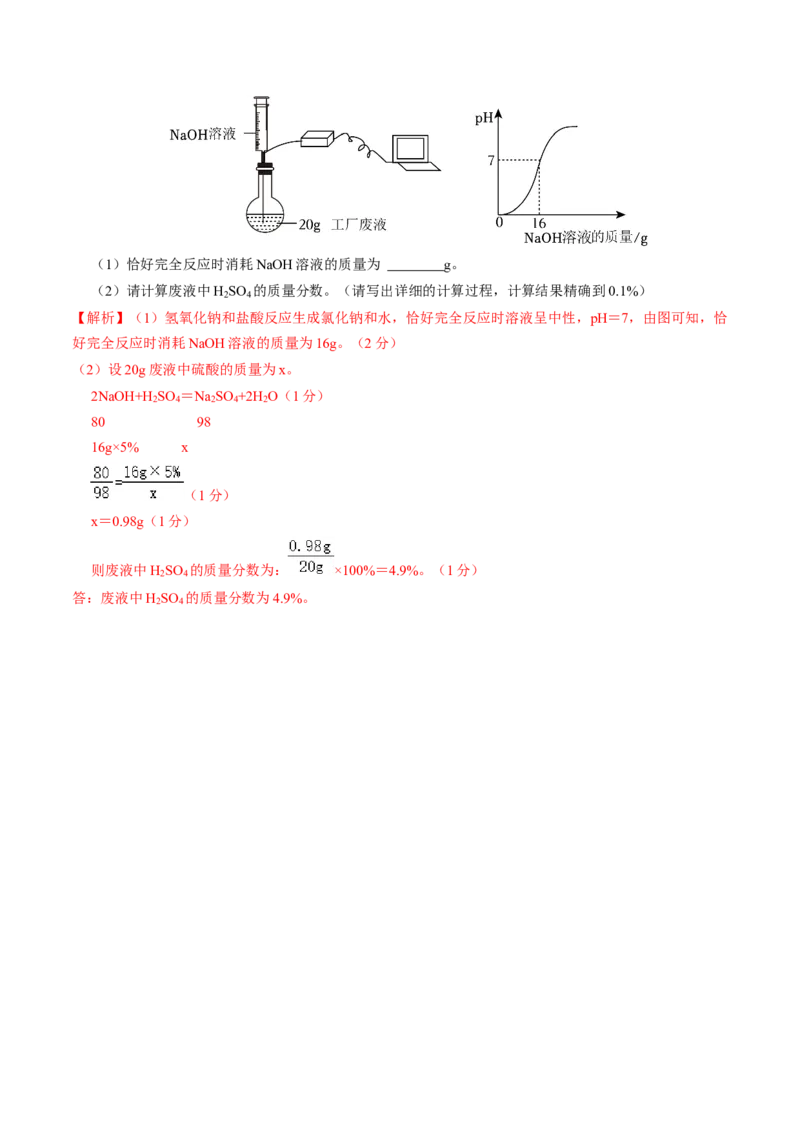
13.(6分)某硫酸厂的废液中含有H SO ,化学兴趣小组计划帮助其测定废液中H SO 的质量分数,实
2 4 2 4
验步骤;向烧瓶中倒入20g废液样品,插入pH计测定溶液的pH,向废液样品中逐滴加入5%的NaOH
溶液,实验过程中溶液pH变化如图所示。(1)恰好完全反应时消耗NaOH溶液的质量为 g。
(2)请计算废液中H SO 的质量分数。(请写出详细的计算过程,计算结果精确到0.1%)
2 4
【解析】(1)氢氧化钠和盐酸反应生成氯化钠和水,恰好完全反应时溶液呈中性,pH=7,由图可知,恰
好完全反应时消耗NaOH溶液的质量为16g。(2分)
(2)设20g废液中硫酸的质量为x。
2NaOH+H SO =Na SO +2H O(1分)
2 4 2 4 2
80 98
16g×5% x
(1分)
x=0.98g(1分)
则废液中H SO 的质量分数为: ×100%=4.9%。(1分)
2 4
答:废液中H SO 的质量分数为4.9%。
2 4