文档内容
2024 年中考第二次模拟考试(武汉卷)
化 学
(考试时间:50分钟 试卷满分:50分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Si-28 S-32 Cl-35.5 Cu-64 Ba-137
一、选择题(本题8小题,每小题只有一个选项符合题意。每小题3分,共24分)
1.2024年春晚节目《瓷影》,以舞绘型,展现青白瓷跨越千年的独特魅力,下列关于青白瓷的制作过程
中,属于化学变化的是( )
A.揉泥 B.烧窑
C.做坯 D.画坯
【答案】B
【解析】A、揉泥过程中没有新物质生成,属于物理变化,该选项不符合题意;
B、烧窑过程中有新物质生成,属于化学变化,该选项符合题意;
C、做坯过程中没有新物质生成,属于物理变化,该选项不符合题意;
D、画坯过程中没有新物质生成,属于物理变化,该选项不符合题意。
故选B。
2.规范的实验操作是完成实验的基本保障。下列基本实验操作正确的是( )
A.铁丝与氧气反应 B.组装发生装置
C.测定溶液的pH D.倾倒液体【答案】D
【解析】A、铁丝在氧气中燃烧时,为防止生成物熔化溅落下来使瓶底炸裂,集气瓶的底部应放少量的水
或铺一层细沙,图中集气瓶的底部没有放少量的水或铺一层细沙,图中所示操作错误;
B、发生装置中长颈漏斗的下方要在液面以下,而导管口应该刚露出橡皮塞,图中所示操作错误;
C、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸
上,与标准比色卡对比来确定pH.不能将pH试纸伸入待测液中,以免污染待测液,图中所示操作错误;
D、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,图中所示操作正确。
故选D。
3.反应 ,生成的次氯酸钠(NaClO)可用于疫情防控。下列叙述正确的是
( )
A.NaClO中氯的化合价为-1价 B.NaCl由离子构成
C.氯原子的结构示意图为 D.NaOH溶液可治疗胃酸过多
【答案】B
【解析】A、化合物中各元素的化合价的代数和为零;NaClO中钠元素显+1价,氧元素显-2价,设氯元素
的化合价为x,则+1+x+(-2)=0,解得x=+1,故A错误;
B、NaCl由钠离子和氯离子构成,故B正确;
C、氯原子的结构示意图为 ,故C错误;
D、氢氧化钠具有很强的腐蚀性,不能用于治疗胃酸过多,故D错误。
故选B。
4.劳动创造美好生活。下列与劳动项目相关的解释错误的是( )
选项 劳动项目 化学知识
A 用厨余垃圾自制花肥 物质发生缓慢氧化
B 清理家中鱼缸并通入空气 空气中的氧气易溶于水
C 往自制冲水器内放入活性炭 活性炭具有吸附作用
D 用食醋去除热水瓶内壁的水垢 食醋的pH<7
【答案】B
【解析】A、用厨余垃圾自制花肥,是因为厨余垃圾中某些物质与氧气发生了缓慢氧化,故A正确;
B、通入空气可以增加水中的含氧量,但空气中的氧气不易溶于水,故B错误;C、活性炭具有吸附性,可以吸附色素和异味,所以往自制冲水器内放入活性炭,可以净化水,故C正
确;
D、 用食醋去除热水瓶内壁的水垢,是因为食醋pH<7,呈酸性,能和水垢中的碳酸钙、氢氧化镁等反
应,故D正确。
故选B。
5.三氟化氮(NF )是一种优良的等离子蚀刻气体,用NF 蚀刻硅片时的产物均为气体,在芯片表面没有
3 3
任何残留物。该反应的微观示意图如下,下列有关说法正确的是( )
A.该反应四种物质中只有一种单质 B.该反应前后原子数目发生了改变
C.反应物甲与乙粒子个数比为4:3 D.物质丙与丁质量比为26:7
【答案】C
【解析】 由反应的示意图可知,反应物甲为NF 、乙为Si,生成物丙为SiF、丁为N,该反应为NF 和Si
3 4 2 3
在一定条件下反应生成SiF 和N,该反应方程式为: 。
4 2
A、该反应的四种物质中,硅和氮气均属于单质,故选项说法错误;
B、由质量守恒定律可知,化学反应前后原子的种类与数目不变,故选项说法错误;
C、由化学方程式可知,反应物甲与乙粒子个数比为4:3,故选项说法正确;
D、由化学方程式可知,物质丙与丁质量比为(3×104):(2×28)=39:7,故选项说法错误。
故选:C。
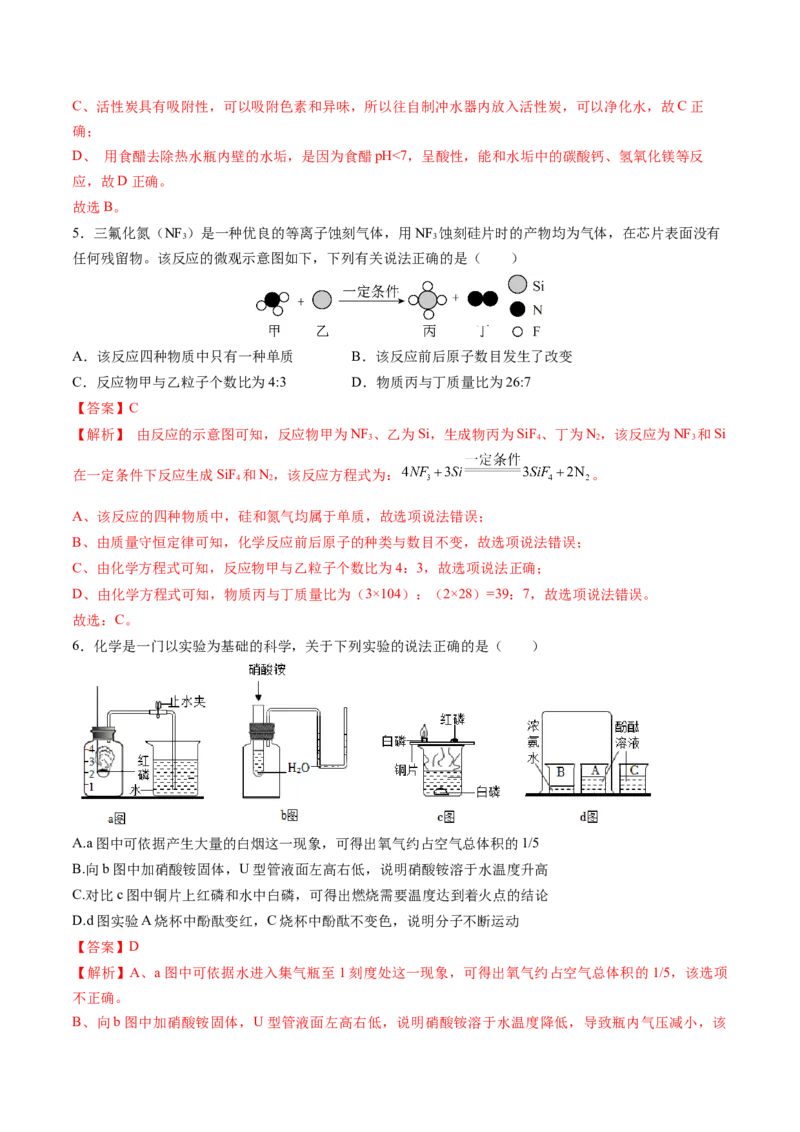
6.化学是一门以实验为基础的科学,关于下列实验的说法正确的是( )
A.a图中可依据产生大量的白烟这一现象,可得出氧气约占空气总体积的1/5
B.向b图中加硝酸铵固体,U型管液面左高右低,说明硝酸铵溶于水温度升高
C.对比c图中铜片上红磷和水中白磷,可得出燃烧需要温度达到着火点的结论
D.d图实验A烧杯中酚酞变红,C烧杯中酚酞不变色,说明分子不断运动
【答案】D
【解析】A、a图中可依据水进入集气瓶至1刻度处这一现象,可得出氧气约占空气总体积的1/5,该选项
不正确。
B、向b图中加硝酸铵固体,U型管液面左高右低,说明硝酸铵溶于水温度降低,导致瓶内气压减小,该选项错误。
C、对比c图中铜片上红磷和白磷,可得出燃烧需要温度达到着火点的结论,该选项不正确。
D、d图实验A烧杯中酚酞变红,C烧杯中酚酞不变色,是因为B中的氨分子是不断运动的,运动到 A中
时,与水结合生成氨水,氨水显碱性,能使酚酞变红色,可以说明分子不断运动,该选项正确。
故选:D。
7.甲、乙、丙是初中化学常见的三种物质, 他们之间的转化关系如图所示(“→”表示反应可一步实
现,部分物质和反应条件略去)。下列推断正确的是( )
A.若甲是HO,则乙可能是CaCl
2 2
B.若甲是CO,则丙可能是H
2 2
C.若甲转化为乙是置换反应,则乙转化为丙不可能也是置换反应
D.若甲转化为乙是复分解反应,则乙转化为丙不可能也是复分解反应
【答案】B
【解析】A、若甲是HO,乙是CaCl ,但HO不能一步转化为CaCl ,故选项推断不正确;
2 2 2 2
B、若甲是CO,乙是HO,二氧化碳与氢氧化钠反应生成碳酸钠和水,水通电分解生成氢气和氧气,则
2 2
丙可能是H,故选项推断正确;
2
C、若甲为铁,乙为铜,丙为银,铁与硫酸铜反应生成硫酸亚铁和铜,铜与硝酸银反应生成硝酸铜和银,
两者的转化都属于置换反应,故选项推断不正确;
D、若甲为碳酸钠,乙为氢氧化钠,丙为水,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化
钠与盐酸反应生成氯化钠和水,两者的转化都属于复分解反应,故选项推断不正确。
故选B。
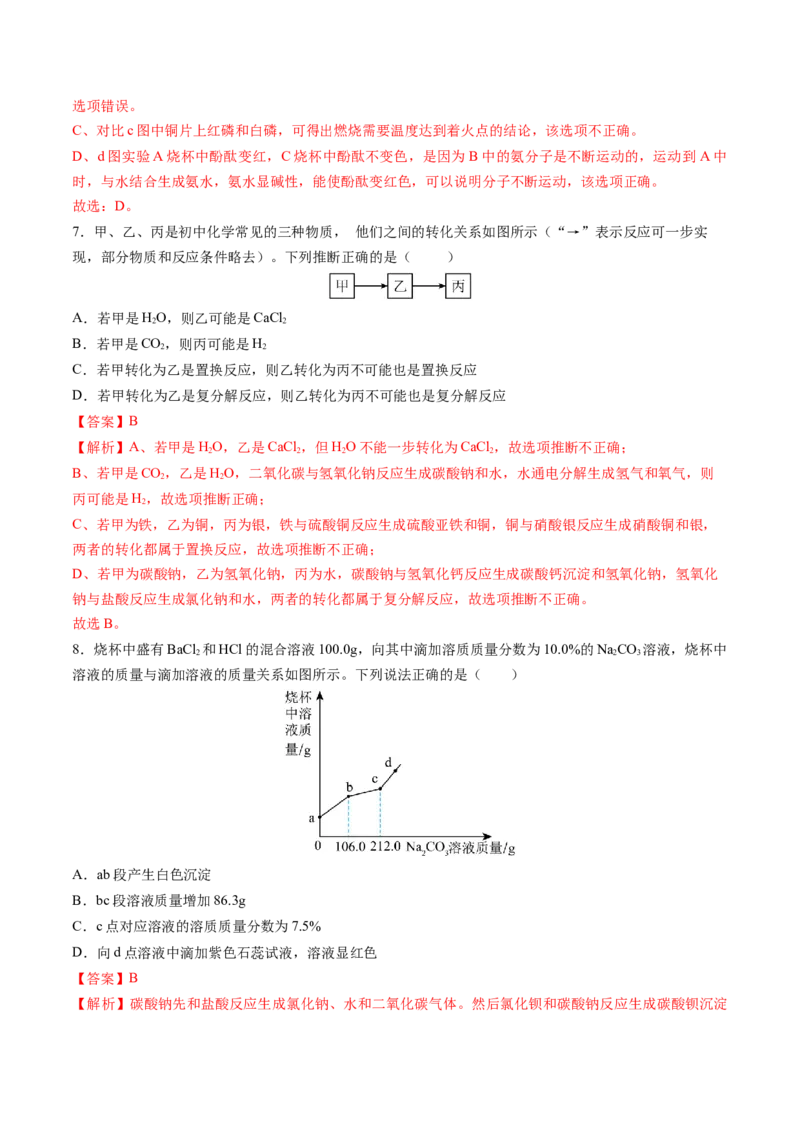
8.烧杯中盛有BaCl 和HCl的混合溶液100.0g,向其中滴加溶质质量分数为10.0%的NaCO 溶液,烧杯中
2 2 3
溶液的质量与滴加溶液的质量关系如图所示。下列说法正确的是( )
A.ab段产生白色沉淀
B.bc段溶液质量增加86.3g
C.c点对应溶液的溶质质量分数为7.5%
D.向d点溶液中滴加紫色石蕊试液,溶液显红色
【答案】B
【解析】碳酸钠先和盐酸反应生成氯化钠、水和二氧化碳气体。然后氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,之后无反应发生。所以 ab段为盐酸和碳酸钠反应,bc段为氯化钡和碳酸钠反应,cd段为碳酸
钠过量。
A. ab段产生气泡,无白色沉淀,错误。
B. 解:设生成碳酸钡的质量为x,生成氯化钠的质量为y
所以溶液增加质量为212g-106g-19.7g=86.3g
C. 设盐酸和碳酸钠反应生成氯化钠的质量为m,二氧化碳的质量为n。
所以c点对应溶液的溶质质量分数为 ,错误。
D. d碳酸钠过量,溶液为碱性,则滴加紫色石蕊试液,溶液显蓝色。错误。
故选:B。
二、非选择题(本题包括5小题,共26分)
9.(4分)星期天小明与同学们决定骑自行车郊外露营,请你根据所学的化学知识回答下列问题。
(1)他们到达了露营地,大家共同搭建好帐篷。下列用品中,由有机合成材料做成的是___________(填字
母序号)。
A.尼龙篷布 B.钢制撑杆 C.羊毛毯子
(2)小明在露营地被蚊虫叮咬(蚊虫分泌出蚁酸),他需要涂抹物质 (选填“食盐水”“肥皂
水”或“食醋”)以减轻痛痒。
(3)到了中午他们用自热米饭作为午餐,自热米饭是利用发热包中的生石灰与水反应放出热量来进行加
热,生石灰与水反应的产物的化学式为 。
(4)野营结束后,为防止引发火灾,大家用沙土将所有火源盖灭。他们利用的灭火原理是 。
【答案】(1)A
(2)肥皂水
(3)Ca(OH)
2
(4)隔绝氧气或空气
【解析】(1)A、尼龙属于合成纤维,属于有机合成材料,符合题意;B、钢是一种铁合金,属于金属材
料,不符合题意;C、羊毛属于天然纤维,属于天然材料,不符合题意。故选:A;
(2)若被蚊虫叮咬(蚊虫分泌出蚁酸),可选用碱性物质涂抹以减轻痛痒,其中食盐水显中性,肥皂水显碱
性,食醋显酸性,所以需要涂抹肥皂水以减轻痛痒;
(3)生石灰与水反应生成氢氧化钙,化学式为Ca(OH) ;
2
(4)野营结束后,为防止引发火灾,大家用沙土将所有火源盖灭,利用了隔绝氧气或空气达到灭火目
的。10.(4分)下表是 和 在不同温度时的溶解度,请回答下列问题。
温度/℃ 0 20 40 60
13.3 31.6 63.9 110
溶解度/g
0.19 0.17 0.14 0.12
(1)将接近饱和的 溶液变成饱和溶液,应 (填“升高”或“降低”)温度。
(2)60℃时,将50g硝酸钾固体溶解在50g水中,所得溶液的质量为 g。
(3)甲是60℃时含有120g水的 溶液,经过如下操作,得到 固体20g。
①乙溶液为 (填“饱和”或“不饱和”)溶液。
②对以上过程的分析,正确的是 (填字母)。
A.甲到乙的过程中溶质的质量不变 B.乙中溶质与溶剂的质量比为
C.乙到丙的过程中溶剂的质量不变 D.甲、乙、丙中溶质质量分数最大的是丙
【答案】(1)升高
(2)100
(3)不饱和 AC
【解析】(1)由图可知,氢氧化钙的溶解度随温度升高而减小,应升高温度,使氢氧化钙的溶解度减小
将接近饱和的氢氧化钙溶液变成饱和溶液,故填升高。
(2)由图可知,60℃时硝酸钾的溶解度为110g,60℃时,将50g硝酸钾固体溶解在50g水中,硝酸钾固
体完全溶解,所得溶液的质量=50g+50g=100g,故填100。
(3)①由图可知,甲是60℃时含有120g水的硝酸钾溶液,恒温蒸发20g水得到乙溶液,则乙、丙溶液中
水的质量为100g,20℃时硝酸钾的溶解度为31.6g,由图可知,乙溶液中水的质量为100g,硝酸钾的质量
=31.6g+20g=51.6g,60℃时硝酸钾的溶解度为110g,则乙溶液为硝酸钾的不饱和溶液,故填不饱和。
②A 由图可知,甲溶液恒温蒸发20g水得到乙溶液没有结晶,则甲到乙的过程中溶质的质量不变,选项正
确;
B 由①可知,乙溶液中水的质量为100g,硝酸钾的质量=31.6g+20g=51.6g,溶质与溶剂的质量比=51.6g:
100g=129:250,选项错误;
C 乙到丙的过程中,降低温度发生结晶,溶剂的质量不变,选项正确;
D、由①可知,乙溶液中水的质量为100g,硝酸钾的质量=31.6g+20g=51.6g,其中溶剂最少,溶质最多,
则甲、乙、丙中溶质质量分数最大的是乙,选项错误,故填AC。
11.(6分)钛和钛合金是21世纪的重要金属材料。工业上利用钛铁矿——钛酸亚铁( )制备金属钛( )的工艺流程如下。
【查阅资料】① 为固体,化学性质稳定,不与稀硫酸、稀盐酸反应。
② 沸点 、 沸点 。
(1)将钛铁矿粉碎的目的是 。
(2)“反应釜”中发生的反应是 ,X的化学式是 。
(3)“沸腾炉”中将 和 的混合物分离,该操作的名称是 。
(4)“合成器”中得到的产品中含有杂质镁,可加入足量稀硫酸除去,写出除杂原理反应 (写化
学方程式)。
(5)依据“绿色化学”理念,指出该生产过程中存在的不足之处是 。
【答案】(1)增大反应物的接触面积,加快反应速率
(2)CO
(3)蒸馏
(4)Mg+HSO =MgSO +H ↑
2 4 4 2
(5)能耗高,产生有毒气体污染环境
【解析】(1)将钛铁矿粉碎的目的是增大反应物的接触面积,加快反应速率,故填增大反应物的接触面
积,加快反应速率。
(2)由化学方程式可知,反应前出现了2个铁原子、2个钛原子、14个氯原子、6个氧原子和6个碳原
子,反应后出现了2个铁原子、2个钛原子、14个氯原子,根据质量守恒定律,反应后尚缺的6个氧原子
和6个碳原子存在于6X中,则X的化学式为CO,故填CO。
(3)由题文可知,氯化铁和四氯化钛的沸点不同,“沸腾炉”中将氯化铁和四氯化钛的混合物分离后得
到气态四氯化钛,该操作的名称是蒸馏,故填蒸馏。
(4)杂质镁和稀硫酸反应生成硫酸镁和氢气,故反应的化学方程式写为:Mg+HSO =MgSO +H ↑。
2 4 4 2
(5)由图可知,流程中需要维持高温的条件,能耗高,产生有毒气体污染环境,故填能耗高,产生有毒
气体污染环境。
12.(6分)某化学兴趣小组为制取CO并检验其化学性质,进行如下实验。回答有关问题:
(1)CO制取甲酸在浓硫酸作用下脱水,反应的化学方程式为:HCOOH CO↑+HO,该反应属于
2
基本反应类型中的 ;制得的CO在点燃前需 。
(2)CO性质将一定质量的CuO装入硬质玻璃管中,称量,总质量为mg。设计如下装置并完成实验。
1
步骤I:关闭K 打开K,缓缓通入氮气一段时间再关闭K;
2 1 1
步骤Ⅱ:点燃装置D两处的酒精灯;
步骤Ⅲ:打开K,通入纯净的一氧化碳,点燃装置B两处的酒精灯;
2
步骤Ⅳ:待装置B玻璃管中固体全部变色时,停止加热;
步骤Ⅴ:停止加热后,需继续通入CO直至装置冷却至室温,倒出固体,称量硬质玻璃管及固体剩余物共
mg
2
①步骤I 先通入一段时间氮气的目的是 。
②C中实验现象能够证明一氧化碳具有还原性,反应的化学方程式为 。
③假设生成物为纯铜,则生成Cu的质量为 g(用含m、m 的式子表示)。
1 2
【答案】(1)分解反应 验纯
(2)①排尽装置内空气,防止加热时发生爆炸
②
③4(m-m )
1 2
【解析】(1)由化学方程式可知,该反应是由一种物质反应生成两种物质,符合“一变多”的特点,属
于基本反应类型中的分解反应;
一氧化碳具有可燃性,点燃或加热一氧化碳与空气的混合物可能引起爆炸,所以制得的CO在点燃前需检
验纯度,防止点燃时发生爆炸;
(2)①一氧化碳具有可燃性,点燃或加热一氧化碳与空气的混合物可能引起爆炸,所以步骤I 先通入一
段时间氮气的目的是排尽装置内空气,防止加热时发生爆炸;
②C装置中在加热条件下,一氧化碳还原氧化铜生成铜和二氧化碳,则能够证明一氧化碳具有还原性的实
验现象是C中黑色粉末变成红色;反应的化学方程式为: ;
③假设生成物为纯铜,设生成Cu的质量为x,x=4(m-m )。
1 2
13.(6分)某化学实验室用稀硫酸处理含有氢氧化钠的废水。现取废水样品80g倒入烧杯中,加入几滴
无色酚酞溶液,然后逐滴加入9.8%的稀硫酸,反应过程中溶液的pH变化如图所示。回答下列问题:
(1)该实验是将 (选填“稀硫酸”或“氢氧化钠溶液”)滴加到另一种溶液中。
(2)废水中氢氧化钠的溶质质量分数(写出计算过程)。
【答案】(1)稀硫酸
(2)解:恰好反应时,加入的稀硫酸质量为100g,则其中溶质质量为100g×9.8%=9.8g。
设80g废水中氢氧化钠的质量为x,则
解得x=8g
则废水中氢氧化钠的溶质质量分数为
答:废水中氢氧化钠的溶质质量分数为10%。