文档内容
C.向酒精灯内添加酒精 D.除去水中的不溶性杂质
2024 年中考第二次模拟考试(济南卷)
3.创建全国文明城市,倡导人们讲文明话做文明事,节约能源、爱护环境从身边做起。下列做法不符合这
化 学
一主题的是
A.选择自行车和公交车作为出行工具 B.将废纸、汽水瓶等收集起来焚烧处理
(考试时间:60分钟 试卷满分:100分) C.不使用一次性塑料袋 D.垃圾分类处理,回收可再生资源
注意事项: 4.生活中处处有化学,化学与人体健康密切相关。下列说法不正确的是
A.不吃霉变或超过保质期的食物 B.青少年常喝碳酸饮料替代日常饮水
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
C.适当摄入水果蔬菜能补充维生素有助人体健康 D.合理使用食品添加剂
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
5.关于燃烧与灭火有很多成语,相关解释错误的是
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
A.火上浇油是补充可燃物,使燃烧更旺
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
B.釜底抽薪的目的是清除可燃物,从而灭火
4.考试结束后,将本试卷和答题卡一并交回。
C.钻木取火是利用钻木提升温度达到木材的着火点,实现燃烧的目的
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 Cl-35.5 Fe-56 S-32 D.杯水车薪指的是水太少,不能降低柴草的着火点,达不到灭火的目的
Cu-64 Zn-65 Ba-137 6.下列有关化学学科观念的说法中,不合理的是
A.能量观:化学变化的过程常伴随能量的变化
选择题部分 共 40 分
B.守恒观:1g氢气在16g氧气中充分燃烧,会生成17g水
一、单项选择题:本题共10小题,每小题2分,共20分。每小题四个选项中,只有一个选项 C.分类观:纯碱、烧碱、熟石灰不属于同一类物质
D.微粒观:酸溶液中都含有氢离子,因此酸具有相似的化学性质
最符合题目的要求。
7.2023年诺贝尔化学奖授予发现和合成量子点的三位科学家。量子点组成中常含镉等元素。下图是镉的结
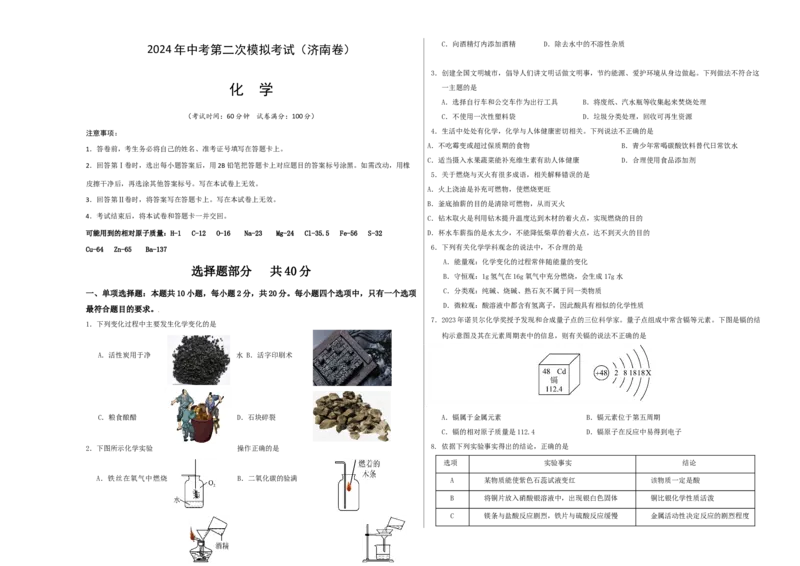
1.下列变化过程中主要发生化学变化的是
构示意图及其在元素周期表中的信息,则有关镉的说法不正确的是
A.活性炭用于净 水 B.活字印刷术
C.粮食酿醋 D.石块碎裂 A.镉属于金属元素 B.镉元素位于第五周期
C.镉的相对原子质量是112.4 D.镉原子在反应中易得到电子
2.下图所示化学实验 操作正确的是 8. 依据下列实验事实得出的结论,正确的是
选项 实验事实 结论
A.铁丝在氧气中燃烧 B.二氧化碳的验满 A 某物质能使紫色石蕊试液变红 该物质一定是酸
B 将铜片放入硝酸银溶液中,出现银白色固体 铜比银化学性质活泼
C 镁条与盐酸反应剧烈,铁片与硫酸反应缓慢 金属活动性决定反应的剧烈程度………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
D 向某水样中滴加肥皂水后振荡,产生大量泡沫 该水样属于硬水
A.A B.B C.C D.D
9.下列有关说法中,合理的是 此
A.通过化学变化,人们改造物质世界并实现物质与能量的相互转化
卷
B.中和反应生成盐和水,则生成盐和水的反应就是中和反应
C.催化剂可以改变化学反应速率,所以任何化学反应都需要催化剂 只
A.降温能使Y的不饱和溶液变成饱和溶液
D.碱的溶液能使紫色石蕊试液变蓝,则能使紫色石蕊试液变蓝的一定是碱的溶液 B.在t℃时,125gX的饱和溶液中水的质量为100g
1 装
10.己知某溶液X是下列四种物质中的一种,取三份等量的该物质,分别向其中滴加NaOH溶液,稀盐酸, C.在t℃时,X的饱和溶液的溶质质量分数为25%
1
D.t℃时,X、Y两种物质的饱和溶液升温到t℃,溶液中溶质的质量分数相等 订
AgNO 溶液中的各一种、产生的现象如表所示。则X是下列各项中的 1 2
3
14. 向MgCl 和CuCl 的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤渣和滤液。下列说法正
加入物质 稀盐酸 NaOH溶液 AgNO 溶液 2 2 不
3
确的是
现象 无明显现象 产生沉淀 产生沉淀 密
A.若滤液为蓝色,则滤渣中一定含有Cu和Zn
A.CuO B.Cu(NO) C.NaCO D.CuCl
3 2 2 3 2 B.若滤液不为蓝色,则滤液中一定不含CuCl
2 封
二、多项选择题:本题共5小题,每小题4分,共20分。每小题给出的四个选项中,至少有 C.若往滤渣中加入稀盐酸,有气泡产生,则滤渣中一定含有Mg
D.所得滤液中MgCl 的溶质质量分数比原溶液小
两个选项符合题目的要求,全部选对得4分,选对两个及以上但不全的得3分,选对一个得2 2
15.向Mg与MgCO 的混合粉末中加入200g9.8%的HSO 溶液,恰好完全反应后得到不饱和溶
3 2 4
分,有错选的得0分。
液甲和气体乙。将生成的气体乙通入足量NaOH溶液,溶液质量增加4.4g。以下说法正
11.杭州亚运会的火炬名为“薪火”,寓意着中华文明薪火相传。火炬以丙烷为燃料,丙烷燃烧的微观示
确的是
意图如下图所示。下列说法中正确的是
A.生成氢气的质量为0.2g
B.溶液甲中溶质的质量为12g
C.原固体粉末的质量为10.8g
D.与Mg粉反应的HSO 溶液的质量为100g
2 4
非选择题部分 共 60 分
A.该反应为氧化反应 B.参加反应的两种物质的分子个数比为1:1
C.反应前后共涉及两种氧化物 D.反应后生成的丙、丁两物质的质量比为11:6
三、填空题:本题共5小题,共60分。
12.为除去下列物质中混有的少量杂质,所采用的相应除杂质方案中,不正确的是
16. (13分)(1)按照要求从氮气、硝酸钾、碳酸、氧化钙中选取合适的物质,将其化学式填在横线上。
选项 物质 杂质 除杂质方案 ①食品包装袋中防腐的气体单质 。 ②一种能溶于水的盐 。
A O N 通过灼热的铜网 ③一种可作食品干燥剂的氧化物 。 ④一种不稳定的酸 。
2 2
(2)“人不负青山,青山定不负人。”坚持绿色发展,保护生态环境,已成为全社会共识。试回答下列
B KNO 溶液 KSO 加入适量BaCl 溶液,过滤
3 2 4 2
问题:
C NaCl固体 BaCl 加水溶解后,加入过量NaCO 溶液,过滤,蒸发结晶
2 2 3
①作为中学生我们应该养成生活垃圾分类投放的良好习惯。废弃塑料瓶、书、报纸应投入印有下列哪
D CaCl 溶液 HCl 加入过量CaCO,过滤
2 3 种标识的垃圾箱中 (填下列选项序号之一)。
A.A B.B C.C D.D
13.下图是 、 两种不含结晶水的固体物质的溶解度曲线。根据图示判断,下列有关说法中,错误的是
试题 第27页(共48页) 试题 第28页(共48页)(1)中国空间站采用柔性太阳翼为航天器的在轨运行提供动力,柔性太阳翼将 转化为电
能。空间站的建造使用了大量的钛合金,钛合金具有 (写一点)的特点。
(2)天宫空间站配置了再生式环控生保系统,实现了舱内大气成分控制、有害气体净化等,从而保障
A. B. C. D. 了航天员在轨长期驻留。航天员呼吸的氧气主要来自电解水,其反应的原理为
(填化学方程式)。此外,还有一部分氧气是储存在加压氧气罐中从地球上运送到空间站的,氧气加压
储存过程的微观实质是 。
②为响应“限塑令”,有些大型超市已经更换成可降解塑料袋,其中一种可降解塑料袋的主要成分是聚
(3)舱外航天服是太空行走关键保障,其躯干壳体为铝合金薄壁硬体结构,抗压能力强,经得起地面
乙烯醇,分子式为(CHO),聚乙烯醇是 (选填“混合物”、“化合物”、“氧化物”之一),属于
2 4 n
运输、火箭发射时的震动,其中铝合金属于 材料,写出铝的原子结构示意图 。
(选填“无机非金属材料”、“有机高分子材料”、“复合材料”之一)。在该物质中碳、
金属铝能与氢氧化钠溶液反应生成偏铝酸钠和物质X,化学方程式为2Al+2NaOH+2HO=2NaAlO+3X,X
氧两种元素的质量比为 (填最简整数比),在该物质中氢、氧两种元素的原子个数比为 (填 2 2
的化学式为 ,偏铝酸钠(NaAlO)中铝元素的化合价为 。
最简整数比),质量分数最小的元素是 (填元素符号)。 2
(4)航天飞行会导致航天员体内的钙流失,钙属于人体中的 (填“常量”或“微量”)元素,
③化石燃料的大量使用会影响生态环境。煤燃烧产生的二氧化硫和汽车尾气中的氮氧化物是导致酸雨
钙流失会引起的健康问题是 。为了补充钙元素,可以食用的食物是 (写一种)。
的主要物质。现在的汽车排气管上都安装了“催化转化器”(如图),使尾气中的一氧化碳和氮氧化物
18.(12分)下图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器(组装
(NO)转化为氮气和二氧化碳,该反应的化学方程式为 ,这样
x
实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列化学实验。
就能减少对空气的污染,其主要原因是 (填下列选项序号之一)。
A.生成的N 属于单质 B.生成的N 和CO 都不属于空气污染物
2 2 2
试回答下列问题:
C.生成的N 和CO 都不能燃烧 D.生成的CO 属于氧化物
2 2 2
(1)以石灰石和稀盐酸为原料,在实验室中制备并收集干燥、纯净的CO 气体,按照要求设计实验装置,
2
17.(12分)中国空间站的建成、神舟系列载人飞船的成功发射,标志着我国航天科技水平已处于世界领先
连接仪器。(提示:盐酸中挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)
地位。请分析图文信息,完成下面小题。
①所选仪器的连接顺序为 (从左到右填写装置序号字母)。
②上述装置A生成CO 的化学方程式为 。
2
(2)以过氧化氢溶液为原料(MnO 为催化剂)制备氧气,并对某种塑料的组成元素进行分析探究(资料
2
显示该塑料只含C、H、O三种元素),所选仪器按“A→B→E→B→D→碱石灰干燥管”的顺序连接(其
1 2………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
中B 、B 均为浓硫酸洗气瓶),实验前检验装置气密性,使该塑料试样在纯氧气中充分燃烧,观察现象,
1 2
收集有关实验数据(假设发生的化学反应都充分反应)。
①仪器A中所发生反应的化学方程式为 。
此
②仪器E的玻璃管中塑料试样充分燃烧后,测得装置B 质量增加3.6克,装置D质量增加8.8克,则在
2
卷
该塑料试样中碳、氢元素的质量比为 (写最简整数比);若没有装置B ,则上述计算出来的
1
碳、氢元素质量比会 (选填“偏小”“不受影响”“偏大”之一)。 只
(3)化学小组的同学测定某氧化铁样品(杂质为Fe)中FeO 的质量含量,设计了实验方案,所选仪器
2 3 装
按“CO(含有少量水蒸气和CO )→B→E→D→D”的顺序连接(D 、D 为氢氧化钠洗气瓶),检查装置 2 1 2 1 2
订
试根据实验过程和发生的现象做出判断,填写以下空白:
的气密性,称取该氧化铁样品20g,加入到E中玻璃管内,然后进行实验,经充分反应,测得玻璃管内
①气体D的名称为 ,白色沉淀H的化学式为 。 不
固体质量为16.4g。请根据上述信息,回答下列问题:
②白色沉淀G的成分是 (写化学式)。
①根据上述数据进行计算可知,该氧化铁样品中FeO 和单质Fe的质量之比为 (填最简整数
2 3 密
③溶液E中的溶质有 种,肯定存在的酸根离子有 (写出离子符号)。
比)。
④写出过程②中生成气体 F 的化学方程式 。 封
②若用D 装置反应前后的实验数据计算该氧化铁样品中FeO 的质量分数,结果会 (填“偏
1 2 3
⑤在混合物 B 里,上述四种物质中肯定不存在的物质是(写化学式) ,请简述 判断的理
大”、“偏小”或“基本一致”)。
由 。
③从环保角度考虑,该套实验装置还存在明显的不足之处,你的具体改进建议是 。
20.(11分)通过学习,我们认识了许多含钠元素的化合物,根据所学知识完成下面题目。
19.(12分)请回答下列问题。
(1)氢氧化钠固体俗称是 (写其中一个即可),氢氧化钠溶液有强烈的腐蚀性,不慎沾到皮肤
(1)实验室有两瓶没有标签的黑色粉末,已知是铁粉和碳粉中的各一种。甲、 乙两个小组的同学分别
上应立即用大量水冲洗,再涂上 溶液。长期敞口放置在空气中容易变质,请写出氢氧化钠变
用化学方法对两瓶药品进行了鉴别,其探究方法如下:
质的反应的化学方程式 。
①甲组同学取粉末少量分别加入两只试管,标记 A、B,分别滴加稀盐酸,振荡,观察到 A 试管有气泡
(2)现有NaCl和NaCO 的固体混合物10g,将其全部放入一洁净的烧杯中,然后加入足量蒸馏水,搅
2 3
冒出,溶液逐渐变为浅绿色,B试管无明显现象,则 A 试管中加入的黑色粉末是 。
拌,使固体完全溶解。再向烧杯中逐滴加入溶质质量分数为10%的BaC1 溶液,反应过程中产生沉淀的质
2
②乙组同学从下列四种试剂中选取了其中的一种,也成功将它们鉴别了出来。则乙组同学选取的是
量与所滴入BaC1 溶液的质量关系如下图所示。试回答:
2 。
A.水 B.食盐水
C.硫酸铜溶液 D.氢氧化钠溶液
(2)现有一固体混合物 A,其中可能含 NaCO 、Zn、Cu三种物质中的两种或多种,还有一固体混合物
2 3
B,其中可能含 MgCl 、Cu(NO) 、BaSO 、NHNO 四种物质中的两种或多种。按图所示进行实验,出现的
2 3 2 4 4 3
现象如图中所述(假设过程中所有发生的反应都恰好完全进行)。
①当滴入BaC1 溶液150g时(图中B点),烧杯中溶液里的溶质为 (写化学式)
2
②当滴入BaC1 溶液104g时(图中A点),恰好完全反应,试通过计算,求所得溶液中溶质的质量。(计
2
算结果精确到0.1g)
试题 第47页(共48页) 试题 第48页(共48页)