文档内容
第 5 单元 化学方程式知识清单
考点1 质量守恒定律的理解
1.质量守恒定律:参加化学反应的各物质质量总和,等于反应后生成的各物质的质量总和。
注意:
(1)适用范围:所有化学变化(物理变化不讨论质量守不守衡的关系)。
(2)守衡概念:质量守衡,不是体积、密度、分子个数等守衡。
(3)质量范围:所有参加反应的反应物质量(不包括没有反应完的部分和催化剂的质量)和所有生成物的质量。
尤其注意参加反应的气体或反应生成的气体、沉淀等不要忽略。
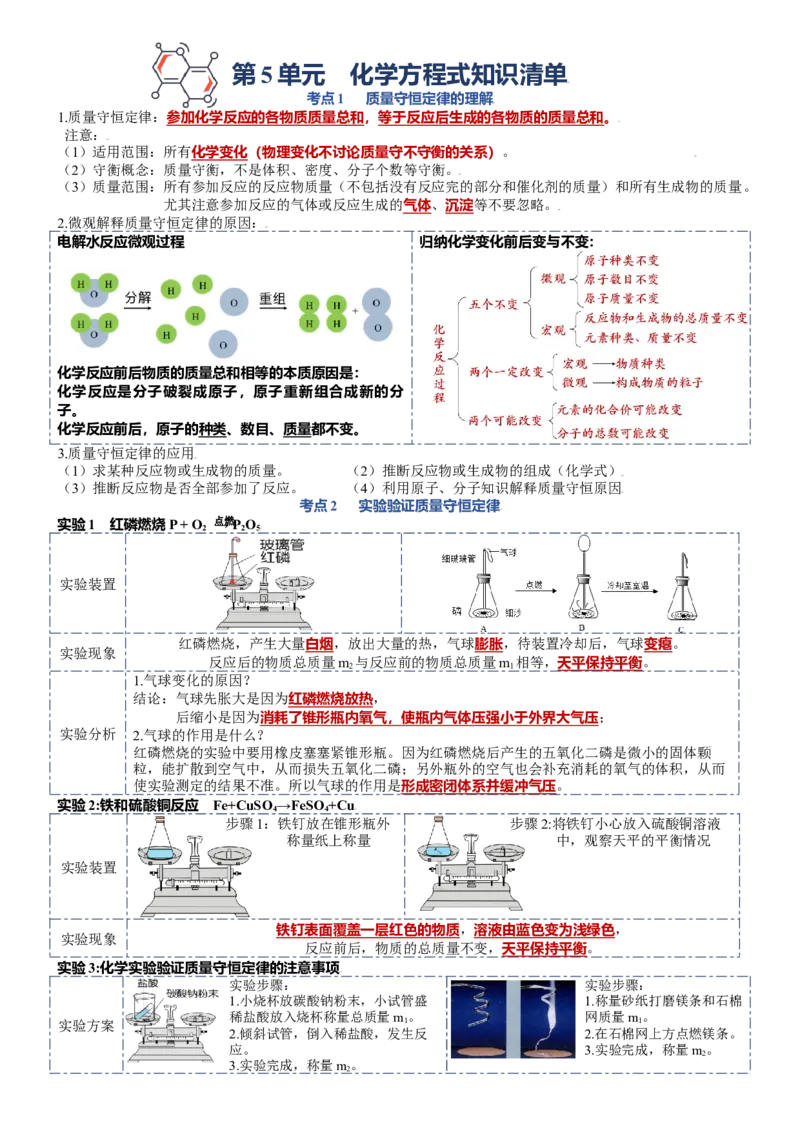
2.微观解释质量守恒定律的原因:
电解水反应微观过程 归纳化学变化前后变与不变:
化学反应前后物质的质量总和相等的本质原因是:
化学反应是分子破裂成原子,原子重新组合成新的分
子。
化学反应前后,原子的种类、数目、质量都不变。
3.质量守恒定律的应用
(1)求某种反应物或生成物的质量。 (2)推断反应物或生成物的组成(化学式)
(3)推断反应物是否全部参加了反应。 (4)利用原子、分子知识解释质量守恒原因
考点2 实验验证质量守恒定律
实验1 红磷燃烧P + O 点→燃 P O
2 2 5
实验装置
红磷燃烧,产生大量白烟,放出大量的热,气球膨胀,待装置冷却后,气球变瘪。
实验现象
反应后的物质总质量m 与反应前的物质总质量m 相等,天平保持平衡。
2 1
1.气球变化的原因?
结论:气球先胀大是因为红磷燃烧放热,
后缩小是因为消耗了锥形瓶内氧气,使瓶内气体压强小于外界大气压;
实验分析 2.气球的作用是什么?
红磷燃烧的实验中要用橡皮塞塞紧锥形瓶。因为红磷燃烧后产生的五氧化二磷是微小的固体颗
粒,能扩散到空气中,从而损失五氧化二磷;另外瓶外的空气也会补充消耗的氧气的体积,从而
使实验测定的结果不准。所以气球的作用是形成密闭体系并缓冲气压。
实验2:铁和硫酸铜反应 Fe+CuSO →FeSO+Cu
4 4
步骤1:铁钉放在锥形瓶外 步骤2:将铁钉小心放入硫酸铜溶液
称量纸上称量 中,观察天平的平衡情况
实验装置
铁钉表面覆盖一层红色的物质,溶液由蓝色变为浅绿色,
实验现象
反应前后,物质的总质量不变,天平保持平衡。
实验3:化学实验验证质量守恒定律的注意事项
实验步骤: 实验步骤:
1.小烧杯放碳酸钠粉末,小试管盛 1.称量砂纸打磨镁条和石棉
稀盐酸放入烧杯称量总质量m。 网质量m。
实验方案 1 1
2.倾斜试管,倒入稀盐酸,发生反 2.在石棉网上方点燃镁条。
应。 3.实验完成,称量m。
2
3.实验完成,称量m。
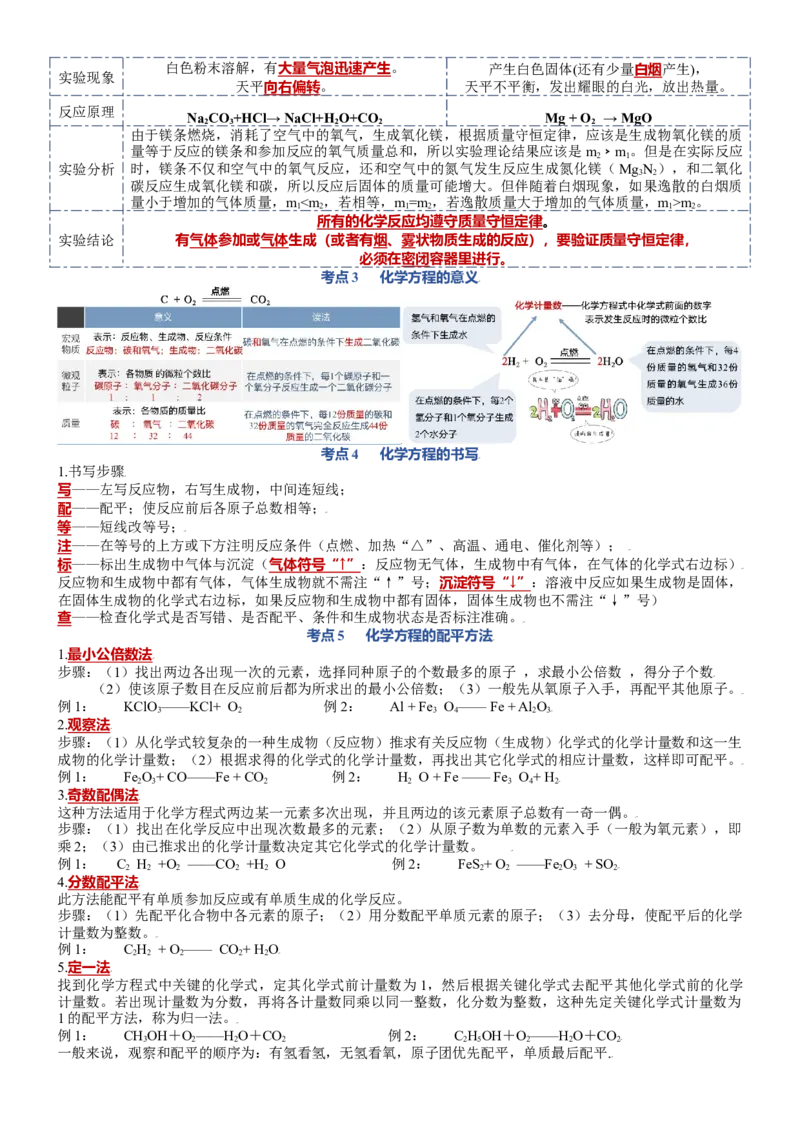
2白色粉末溶解,有大量气泡迅速产生。 产生白色固体(还有少量白烟产生),
实验现象
天平向右偏转。 天平不平衡,发出耀眼的白光,放出热量。
反应原理
Na CO +HCl→ NaCl+H O+CO Mg + O → MgO
2 3 2 2 2
由于镁条燃烧,消耗了空气中的氧气,生成氧化镁,根据质量守恒定律,应该是生成物氧化镁的质
量等于反应的镁条和参加反应的氧气质量总和,所以实验理论结果应该是m﹥m。但是在实际反应
2 1
实验分析 时,镁条不仅和空气中的氧气反应,还和空气中的氮气发生反应生成氮化镁(MgN ),和二氧化
3 2
碳反应生成氧化镁和碳,所以反应后固体的质量可能增大。但伴随着白烟现象,如果逸散的白烟质
量小于增加的气体质量,mm。
1 2 1 2 1 2
所有的化学反应均遵守质量守恒定律。
实验结论 有气体参加或气体生成(或者有烟、雾状物质生成的反应),要验证质量守恒定律,
必须在密闭容器里进行。
考点3 化学方程的意义
考点4 化学方程的书写
1.书写步骤
写——左写反应物,右写生成物,中间连短线;
配——配平;使反应前后各原子总数相等;
等——短线改等号;
注——在等号的上方或下方注明反应条件(点燃、加热“△”、高温、通电、催化剂等);
标——标出生成物中气体与沉淀(气体符号“↑”:反应物无气体,生成物中有气体,在气体的化学式右边标)
反应物和生成物中都有气体,气体生成物就不需注“↑”号;沉淀符号“↓”:溶液中反应如果生成物是固体,
在固体生成物的化学式右边标,如果反应物和生成物中都有固体,固体生成物也不需注“↓”号)
查——检查化学式是否写错、是否配平、条件和生成物状态是否标注准确。
考点5 化学方程的配平方法
1.最小公倍数法
步骤:(1)找出两边各出现一次的元素,选择同种原子的个数最多的原子 ,求最小公倍数 ,得分子个数
(2)使该原子数目在反应前后都为所求出的最小公倍数;(3)一般先从氧原子入手,再配平其他原子。
例1: KClO——KCl+ O 例2: Al + Fe O—— Fe + Al O
3 2 3 4 2 3
2.观察法
步骤:(1)从化学式较复杂的一种生成物(反应物)推求有关反应物(生成物)化学式的化学计量数和这一生
成物的化学计量数;(2)根据求得的化学式的化学计量数,再找出其它化学式的相应计量数,这样即可配平。
例1: Fe O+ CO——Fe + CO 例2: H O + Fe —— Fe O+ H
2 3 2 2 3 4 2
3.奇数配偶法
这种方法适用于化学方程式两边某一元素多次出现,并且两边的该元素原子总数有一奇一偶。
步骤:(1)找出在化学反应中出现次数最多的元素;(2)从原子数为单数的元素入手(一般为氧元素),即
乘2;(3)由已推求出的化学计量数决定其它化学式的化学计量数。
例1: C H +O ——CO +H O 例2: FeS+ O ——Fe O + SO
2 2 2 2 2 2 2 2 3 2
4.分数配平法
此方法能配平有单质参加反应或有单质生成的化学反应。
步骤:(1)先配平化合物中各元素的原子;(2)用分数配平单质元素的原子;(3)去分母,使配平后的化学
计量数为整数。
例1: C H + O —— CO+ H O
2 2 2 2 2
5.定一法
找到化学方程式中关键的化学式,定其化学式前计量数为1,然后根据关键化学式去配平其他化学式前的化学
计量数。若出现计量数为分数,再将各计量数同乘以同一整数,化分数为整数,这种先定关键化学式计量数为
1的配平方法,称为归一法。
例1: CHOH+O——HO+CO 例2: C HOH+O——HO+CO
3 2 2 2 2 5 2 2 2
一般来说,观察和配平的顺序为:有氢看氢,无氢看氧,原子团优先配平,单质最后配平.考点6 根据化学方程计算
1.计算依据:利用化学方程式能反映物质间的质量比,且质量比呈正比例关系。
2.计算步骤:①设未知数;②根据题意写出方程式;③根据化学方程式找出已知量与未知量的质量比;
④列出比例式,并求出未知数;⑤答
注意:①由于方程式只能反映物质间的质量比,因此代入方程式中的各个量必须是质量。
②由于方程式中各物质是纯净物,因此代入方程式中的量必须是纯净物的质量。
③单位必须统一。
3.计算中常用的关系式:
(1)m= ρv
(2)单位换算:1L=1000mL,1mL=1cm3
(3) 物质的纯度 = 纯物质的质量 / 不纯物质的质量 ×100%
变形: 纯物质的质量 = 不纯物质的质量 × 物质的纯度 不纯物质的质量 = 纯物质的质量 ÷ 物质的纯度
(4) 物质的纯度(纯物质的质量分数) =1- 杂质的质量分数