文档内容
陕西省西安中学高 2026 届高三第三次模拟考试
化学试题
(时间:75分钟 满分:100分 )
一、选择题(共 14 小题,每小题 3 分,共 42 分。在每小题给出的四个选项中,只有一项
是符合题目要求的)
1. 重庆市战略性新兴产业发展“十四五”规划(2021-2025年)涉及的下列物质中,属于金属材料的是
D.聚氨酯树
A.重组蛋白 B.高性能铜箔 C.氮化镓半导体
脂
A. A B. B C. C D. D
2. 下列化学用语或图示表示正确的是
A. NCl 的电子式:
3
B. HCO 的结构式:
2 3
C. P 的空间填充模型:
4
D. 用电子云轮廓图示意p-p σ键的形成:
3. 物质用途体现性质,下列两者对应关系不正确的是
A. 苯酚用于杀菌消毒,体现了苯酚的氧化性
B. 利用“杯酚”分离 和 ,体现了超分子分子识别的特征
C. 硫代硫酸钠用来除去自来水中的氯气,体现了硫代硫酸钠的还原性
的
D. 臭氧在四氯化碳中 溶解度高于在水中的溶解度,体现了臭氧的极性很弱
4. 分子结构修饰在药物设计与合成中有广泛的应用。布洛芬具有抗炎、镇痛、解热作用,但口服该药对胃、肠道有刺激性,可以对该分子进行如图所示的分子修饰。下列说法错误的是
A. 甲的分子式为C H O B. 甲分子中最多有8个碳原子共平面
13 18 2
C. 甲和乙都能与氢氧化钠溶液发生反应 D. 甲修饰成乙可降低对胃、肠道的刺激
5. 在2025年9·3阅兵式上,展示的多种先进武器装备涉及到众多物质结构相关知识。下列关于武器装备材
料的物质结构说法正确的是
A. 新型战斗机机身使用的是铝合金,其晶体结构中铝原子与合金元素原子形成混合型晶体
B. 用于制造导弹发动机耐高温部件的难熔合金(如钨合金),其高熔点特性主要源于原子半径小、价电子数
多,使得原子间形成的共价键强
C. 阅兵车辆轮胎使用的橡胶材料,属于体型高分子化合物,具有良好的弹性和可塑性
的
D. 激光武器中 核心光学材料,其内部微粒呈现规则有序排列,具有各向同性的特点,属于典型的离
子晶体
6. 化学研究应当注重宏观与微观相结合。下列宏观现象与微观解释不符的是
选
宏观现象 微观解释
项
邻羟基苯甲醛与对羟基苯甲
A 对羟基苯甲醛可形成分子内氢键,沸点更低一些
醛沸点不同
灼烧铜或铜的化合物火焰呈
B Cu原子电子跃迁时会吸收或释放特定波长的光
绿色
碳原子在三维空间无序排列,X射线衍射实验检验
C 炭黑是非晶体
看不到分立的斑点
氯化钠晶体熔点低于氧化镁 离子晶体中离子所带电荷数越少,离子半径越大,
D
晶体 离子晶体熔点越低
A. A B. B C. C D. D
7. 化学方程式是化学独有的学科语言,下列过程所对应的化学方程式或离子方程式错误的是
A. 用浓 溶液溶解 沉淀:
B. 使酸性 溶液褪色:C. 用新制 碱性悬浊液检验乙醛的醛基:CHCHO+2Cu(OH) +OH- → CHCOO-+Cu O↓+3HO
3 2 3 2 2
D. 工业上制备高铁酸钠的一种方法:
8. 科学家研究发现,利用CaF 晶体释放出的Ca2+和F-可脱除硅烷,这拓展了金属氟化物材料的生物医学
2
功能。CaF 晶胞结构如图1所示,该晶胞从A离子处沿体对角线的投影如图2所示。下列叙述错误的是
2
A. F-填充在以Ca2+构成的四面体空隙中
B. 若C离子的投影位置在⑩,则B离子的投影位置在⑦
C. 晶胞内Ca2+和F-的最短距离为 a nm
D. 若脱硅速率依赖于晶体提供自由氟离子的能力,则脱硅速率:BaF <CaF
2 2
9. 化合物XYZ W 为翡翠的主要成分,W、X、Y和Z为原子序数依次增大的短周期主族元素。基态W原
2 6
子的价层电子排布式为nsnnp2n,Y的基态原子核外电子共占据7个原子轨道,Z的最高正化合价和最低负
化合价的绝对值相等。下列说法中正确的是
.
A 简单离子半径:X>Y>W
B. ZW 的空间构型为直线型
2
C. X和Y的第一电离能均小于同周期相邻元素
D. YCl 分子中所有原子均满足8e-结构
3
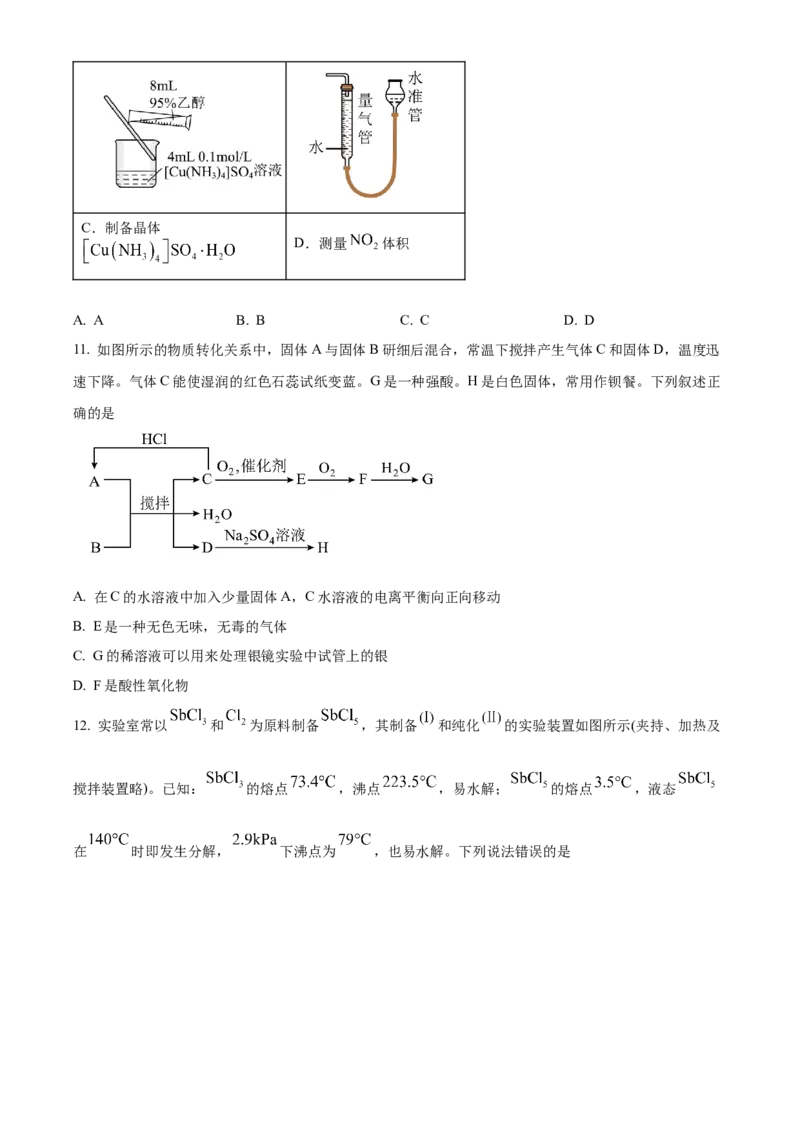
10. 下列实验设计,能达到实验目的的是
A.检验乙炔的还原性 B.除去 中的HClC.制备晶体
D.测量 体积
A. A B. B C. C D. D
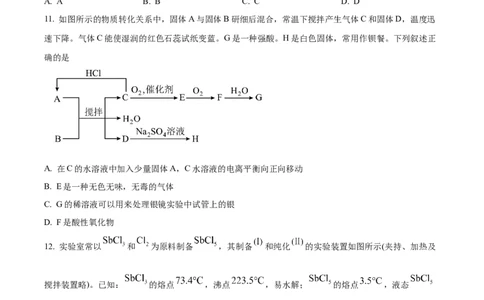
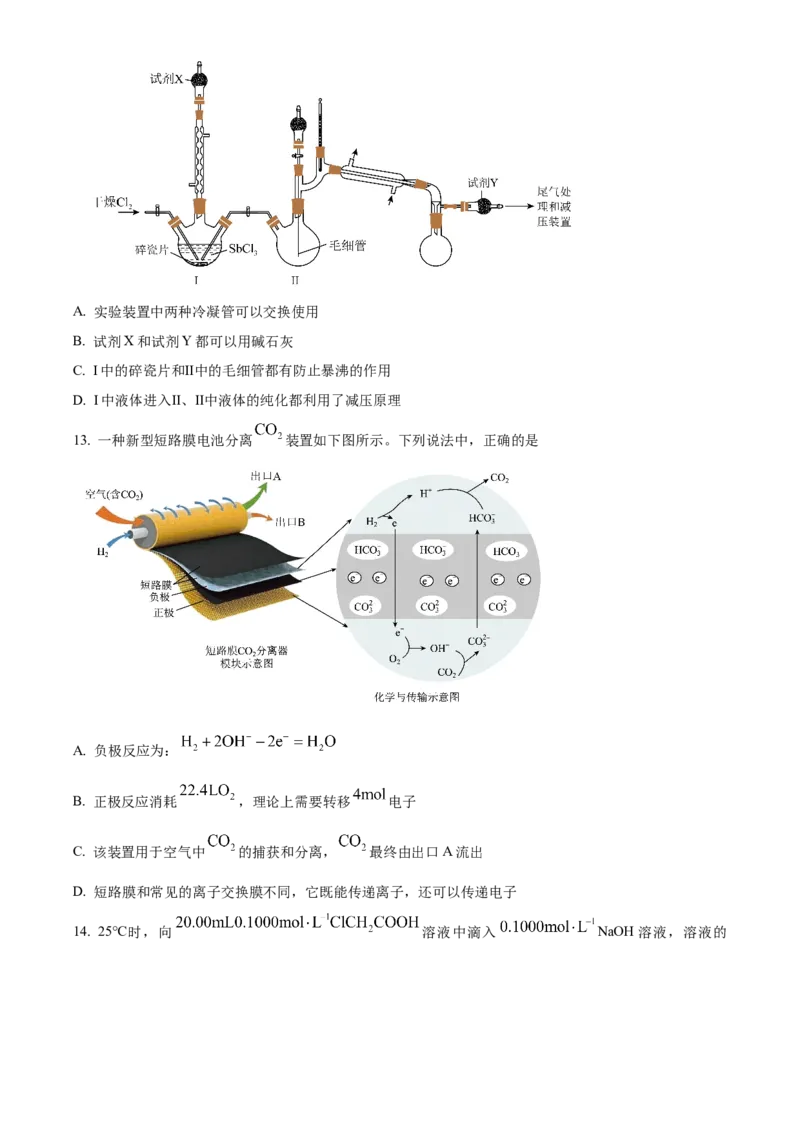
11. 如图所示的物质转化关系中,固体A与固体B研细后混合,常温下搅拌产生气体C和固体D,温度迅
速下降。气体C能使湿润的红色石蕊试纸变蓝。G是一种强酸。H是白色固体,常用作钡餐。下列叙述正
确的是
A. 在C的水溶液中加入少量固体A,C水溶液的电离平衡向正向移动
B. E是一种无色无味,无毒的气体
C. G的稀溶液可以用来处理银镜实验中试管上的银
D. F是酸性氧化物
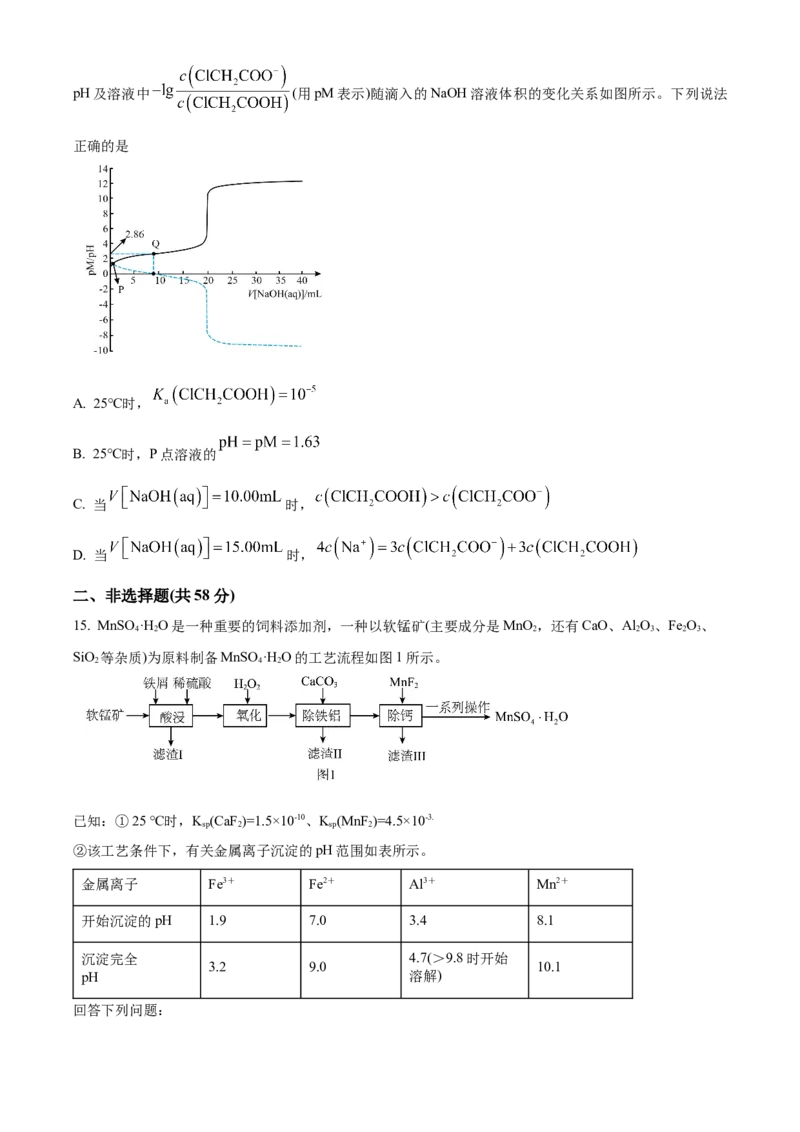
12. 实验室常以 和 为原料制备 ,其制备 和纯化 的实验装置如图所示(夹持、加热及
搅拌装置略)。已知: 的熔点 ,沸点 ,易水解; 的熔点 ,液态
在 时即发生分解, 下沸点为 ,也易水解。下列说法错误的是A. 实验装置中两种冷凝管可以交换使用
B. 试剂X和试剂Y都可以用碱石灰
C. I中的碎瓷片和Ⅱ中的毛细管都有防止暴沸的作用
D. I中液体进入Ⅱ、Ⅱ中液体的纯化都利用了减压原理
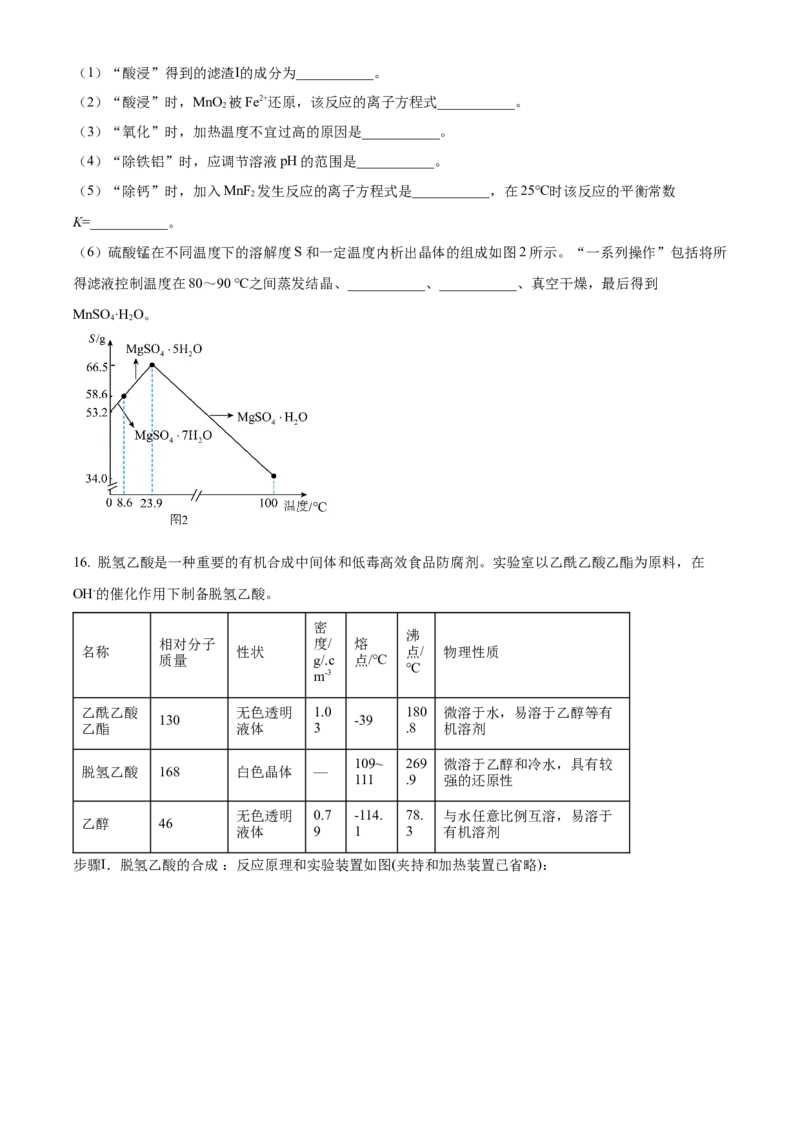
13. 一种新型短路膜电池分离 装置如下图所示。下列说法中,正确的是
A. 负极反应为:
B. 正极反应消耗 ,理论上需要转移 电子
C. 该装置用于空气中 的捕获和分离, 最终由出口A流出
D. 短路膜和常见的离子交换膜不同,它既能传递离子,还可以传递电子
14. 25℃时,向 溶液中滴入 NaOH溶液,溶液的pH及溶液中 (用pM表示)随滴入的NaOH溶液体积的变化关系如图所示。下列说法
正确的是
A. 25℃时,
B. 25℃时,P点溶液的
C. 当 时,
D. 当 时,
二、非选择题(共58分)
15. MnSO ·H O是一种重要的饲料添加剂,一种以软锰矿(主要成分是MnO ,还有CaO、Al O、Fe O、
4 2 2 2 3 2 3
SiO 等杂质)为原料制备MnSO ·H O的工艺流程如图1所示。
2 4 2
已知:①25 ℃时,K (CaF )=1.5×10-10、K (MnF )=4.5×10-3.
sp 2 sp 2
②该工艺条件下,有关金属离子沉淀的pH范围如表所示。
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀的pH 1.9 7.0 3.4 8.1
沉淀完全 的4.7(>9.8时开始
3.2 9.0 10.1
pH 溶解)
回答下列问题:(1)“酸浸”得到的滤渣Ⅰ的成分为___________。
(2)“酸浸”时,MnO 被Fe2+还原,该反应的离子方程式___________。
2
(3)“氧化”时,加热温度不宜过高的原因是___________。
(4)“除铁铝”时,应调节溶液pH的范围是___________。
(5)“除钙”时,加入MnF 发生反应的离子方程式是___________,在25℃时该反应的平衡常数
2
K=___________。
(6)硫酸锰在不同温度下的溶解度S和一定温度内析出晶体的组成如图2所示。“一系列操作”包括将所
得滤液控制温度在80~90 ℃之间蒸发结晶、___________、___________、真空干燥,最后得到
MnSO ·H O。
4 2
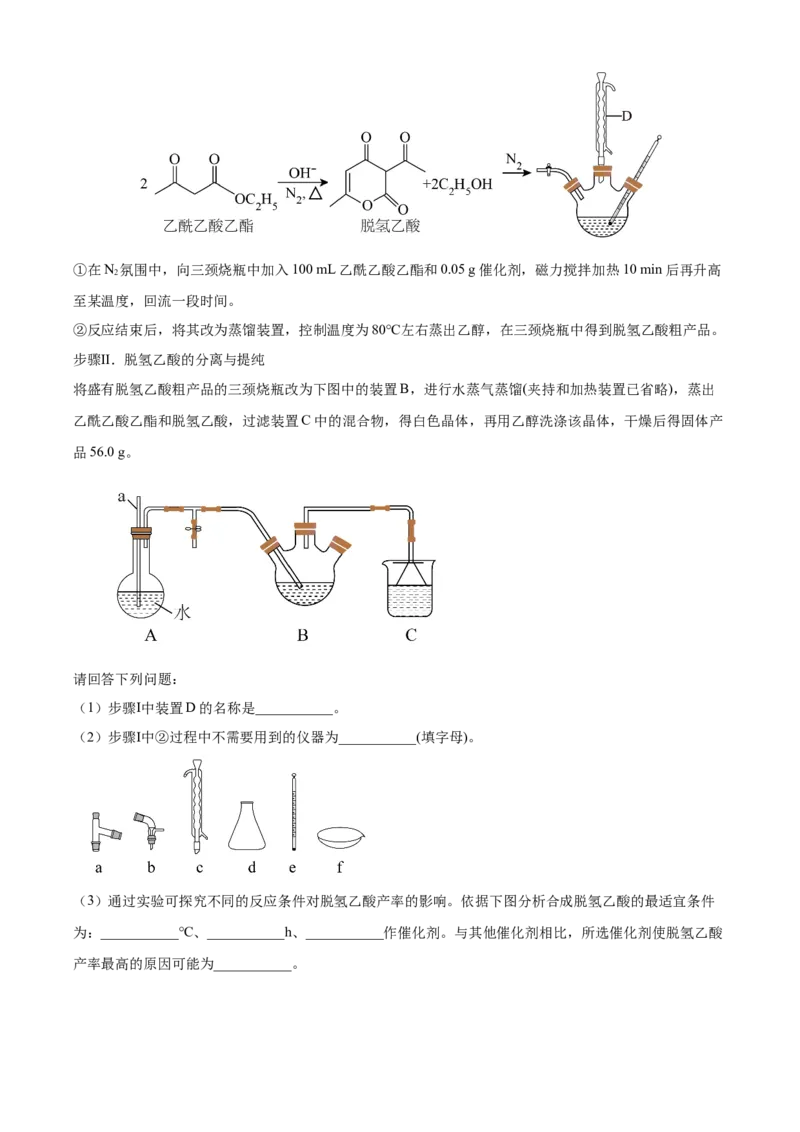
16. 脱氢乙酸是一种重要的有机合成中间体和低毒高效食品防腐剂。实验室以乙酰乙酸乙酯为原料,在
OH-的催化作用下制备脱氢乙酸。
密
沸
相对分子 度/ 熔
名称 性状 点/ 物理性质
质量 g/.c 点/℃
℃
m-3
乙酰乙酸 无色透明 1.0 180 微溶于水,易溶于乙醇等有
130 -39
乙酯 液体 3 .8 机溶剂
109~ 269 微溶于乙醇和冷水,具有较
脱氢乙酸 168 白色晶体 —
111 .9 强的还原性
无色透明 0.7 -114. 78. 与水任意比例互溶,易溶于
乙醇 46
液体 9 1 3 有机溶剂
步骤Ⅰ.脱氢乙酸的合成 :反应原理和实验装置如图(夹持和加热装置已省略):①在N 氛围中,向三颈烧瓶中加入100 mL乙酰乙酸乙酯和0.05 g催化剂,磁力搅拌加热10 min后再升高
2
至某温度,回流一段时间。
②反应结束后,将其改为蒸馏装置,控制温度为80℃左右蒸出乙醇,在三颈烧瓶中得到脱氢乙酸粗产品。
步骤Ⅱ.脱氢乙酸的分离与提纯
将盛有脱氢乙酸粗产品的三颈烧瓶改为下图中的装置B,进行水蒸气蒸馏(夹持和加热装置已省略),蒸出
乙酰乙酸乙酯和脱氢乙酸,过滤装置C中的混合物,得白色晶体,再用乙醇洗涤该晶体,干燥后得固体产
品56.0 g。
请回答下列问题:
(1)步骤Ⅰ中装置D的名称是___________。
(2)步骤Ⅰ中②过程中不需要用到的仪器为___________(填字母)。
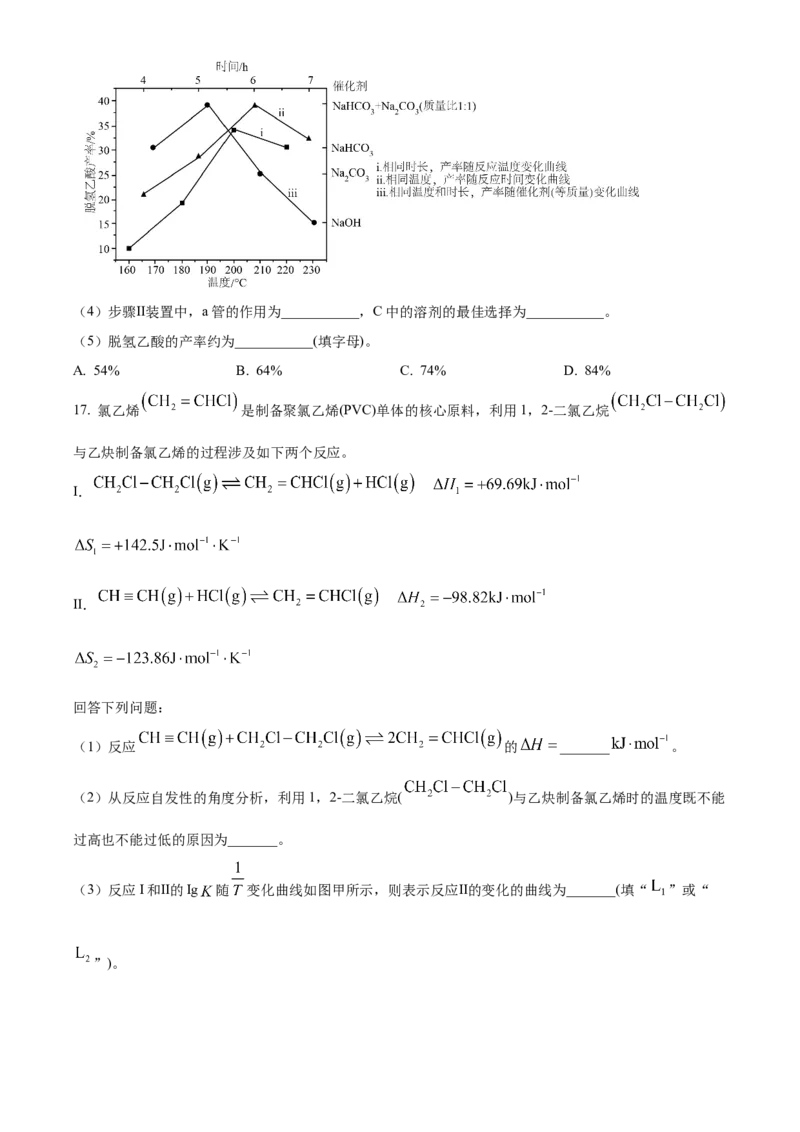
(3)通过实验可探究不同的反应条件对脱氢乙酸产率的影响。依据下图分析合成脱氢乙酸的最适宜条件
为:___________℃、___________h、___________作催化剂。与其他催化剂相比,所选催化剂使脱氢乙酸
产率最高的原因可能为___________。(4)步骤Ⅱ装置中,a管的作用为___________,C中的溶剂的最佳选择为___________。
(5)脱氢乙酸的产率约为___________(填字母)。
A. 54% B. 64% C. 74% D. 84%
17. 氯乙烯 是制备聚氯乙烯(PVC)单体的核心原料,利用1,2-二氯乙烷
与乙炔制备氯乙烯的过程涉及如下两个反应。
I.
Ⅱ.
回答下列问题:
(1)反应 的 _______ 。
(2)从反应自发性的角度分析,利用1,2-二氯乙烷( )与乙炔制备氯乙烯时的温度既不能
过高也不能过低的原因为_______。
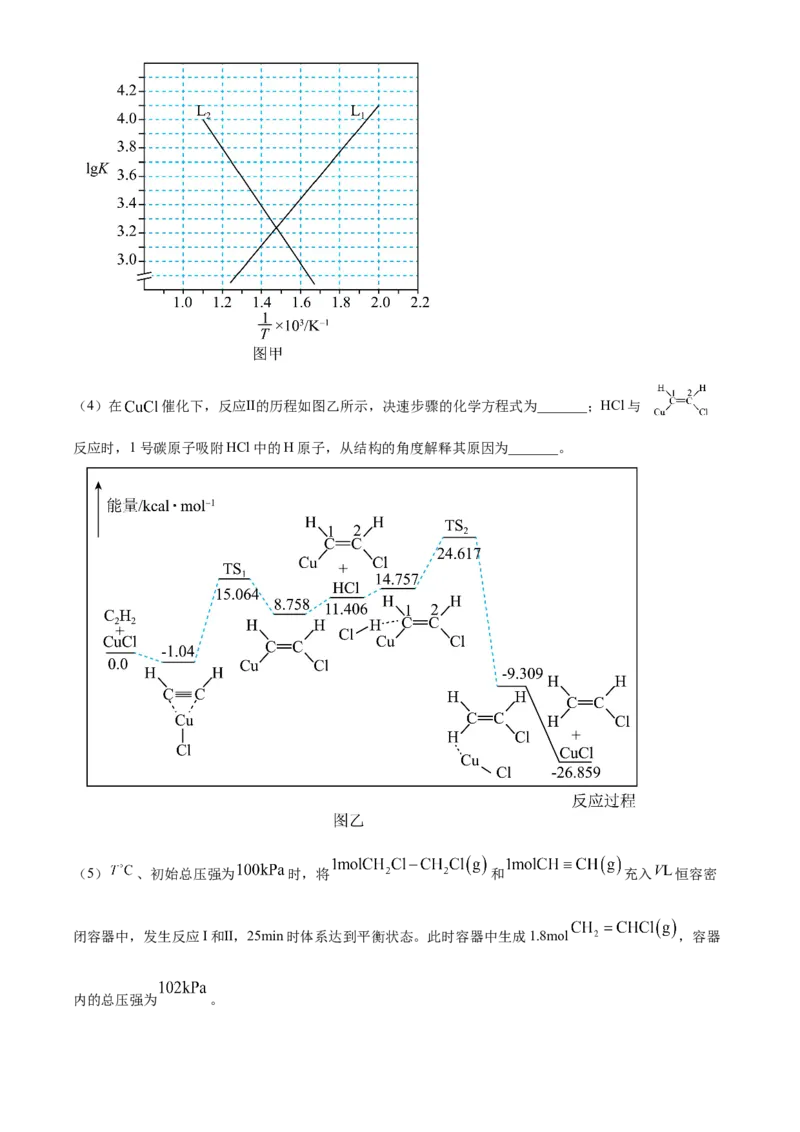
(3)反应I和Ⅱ的Ig 随 变化曲线如图甲所示,则表示反应Ⅱ的变化的曲线为_______(填“ ”或“
”)。(4)在 催化下,反应Ⅱ的历程如图乙所示,决速步骤的化学方程式为_______;HCl与
反应时,1号碳原子吸附HCl中的H原子,从结构的角度解释其原因为_______。
(5) 、初始总压强为 时,将 和 充入 恒容密
闭容器中,发生反应I和Ⅱ,25min时体系达到平衡状态。此时容器中生成1.8mol ,容器
内的总压强为 。①下列事实能判断体系达到平衡状态的是_______(填标号)。
a.相同时间内 生成的物质的量等于 消耗的物质的量
b.
c.容器中气体的平均摩尔质量不变
d.容器中混合气体的密度不变
② 内, _______ (用含 的代数式表示)。
③ 时,反应Ⅱ的压强平衡常数 _______ ( 为用分压表示的平衡常数,分压=总压×物质的
量分数)。
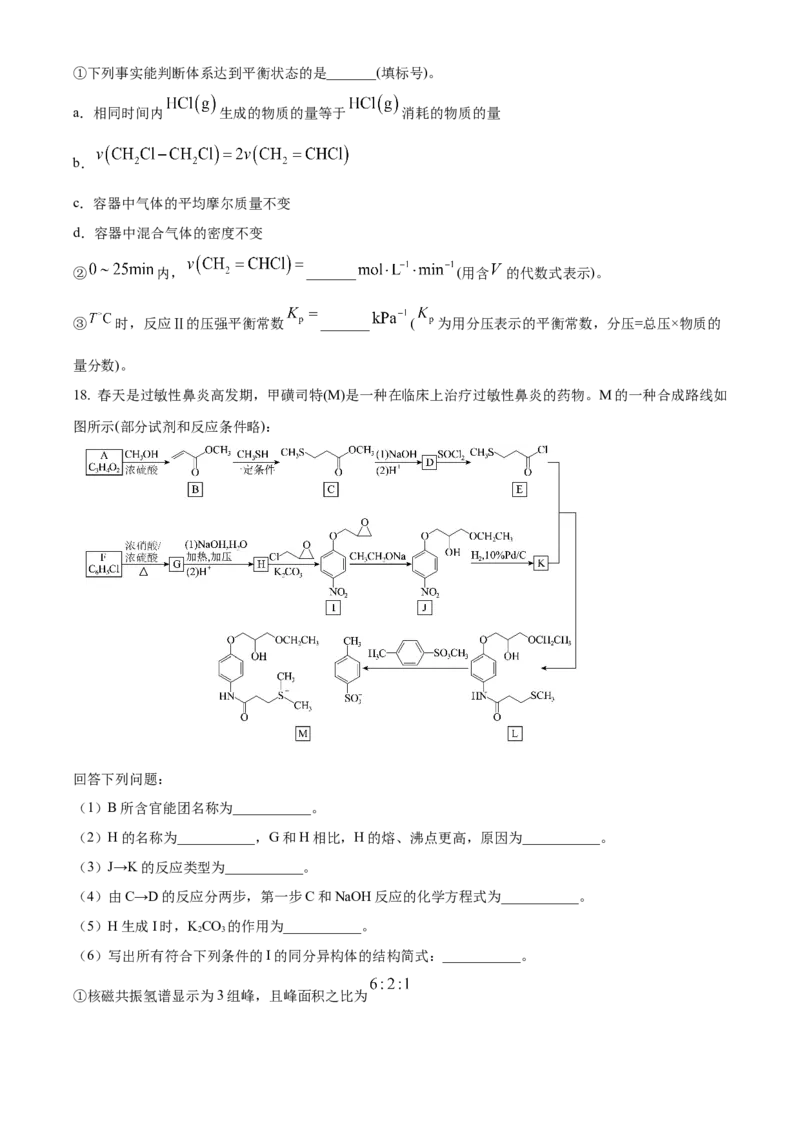
18. 春天是过敏性鼻炎高发期,甲磺司特(M)是一种在临床上治疗过敏性鼻炎的药物。M的一种合成路线如
图所示(部分试剂和反应条件略):
回答下列问题:
(1)B所含官能团名称为___________。
(2)H的名称为___________,G和H相比,H的熔、沸点更高,原因为___________。
(3)J→K的反应类型为___________。
(4)由C→D的反应分两步,第一步C和NaOH反应的化学方程式为___________。
(5)H生成I时,KCO 的作用为___________。
2 3
(6)写出所有符合下列条件的I的同分异构体的结构简式:___________。
①核磁共振氢谱显示为3组峰,且峰面积之比为②能发生水解反应
③能发生银镜反应
④存在 ,且直接与苯环相连
(7)环氧氯丙烷( )是一种用途较为广泛的基本有机化工原料,是合成甘油的中间体,也是
合成环氧树脂、氯醇橡胶等产品的主要原料。其一种工业合成路线如下: