文档内容
秘密★启用前 〔考试时间:2026年4月16日上午8∶30—9∶45〕
乐山市高中 2023级第二次调查研究考试
化 学
注意事项:
1.考生领到答题卡后,须在规定区域填写本人的姓名、准考证号和座位号,并在答题
卡背面用2B铅笔填涂座位号。
2.考生回答选择题时,选出每小题答案后,须用2B铅笔将答题卡上对应题目的答案标号涂
黑,如需改动,用橡皮擦干净后,再选涂其他答案标号。考生回答非选择题时,须用0.5mm黑色
字迹签字笔将答案写在答题卡上。选择题和非选择题的答案写在试卷或草稿纸上无效。
3.考生不得将答题卡和草稿纸带离考场,考试结束后由监考员统一回收。
可能用到的相对原子质量:C12
一、单项选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是最符合题目要求的。
1.化学与生产、生活和科技密切相关,下列说法正确的是
A.模仿壁虎足的结构制成的仿生胶带能与被黏着物之间形成化学键
B.药皂中加入少量苯酚来杀菌消毒,利用了苯酚的强氧化性
C.低密度聚乙烯比高密度聚乙烯支链多,软化温度低
D.烫发药水能使头发中的二硫键(-S-S-)发生断裂和重组,该过程不涉及氧化还原反应
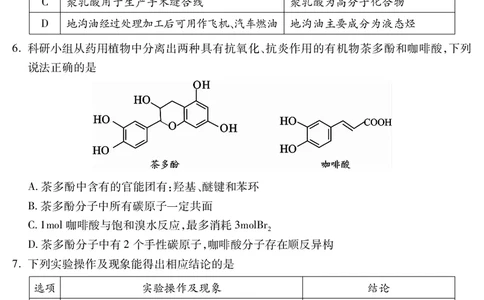
2.下列有关滴定管的使用或操作正确的是
A.甲:溶液润洗滴定管后,将液体从上口倒出
B.乙:盛装一定体积NaOH溶液
C.丙:从滴定管中放出一定体积盐酸溶液
D.丁:记录滴定管液面示数为7.1mL
3.CrO 是一种耐高温材料,用碳高温还原重铬酸钠(NaCrO)可以制备 CrO,反应的化学
2 3 2 2 7 2 3
方程式为:NaCrO +2C CrO +NaCO +CO↑,N 为阿伏加德罗常数的值,下列相关
2 2 7 2 3 2 3 A
说法正确的是
A.1mol基态Cr原子核外单电子的数目为5N
A
B.12g石墨中,含有的σ键的数目为1.5N
A
C.100mL0.1mol·L-1NaCO 溶液中CO2-的数目为0.01N
2 3 3 A
D.反应每生成22.4LCO,转移的电子数为6N
A
高三化学 第 1页(共8页)
书书书4.下列指定反应的离子方程式正确的是
A.乙酰胺在氢氧化钠溶液中水解:CHCONH +OH- CHCOO-+NH↑
3 2 3 3
B.CO 通入足量氨水中:CO +2OH- CO2-+HO
2 2 3 2
C.向Ca(ClO)溶液中通入少量SO:Ca2++ClO-+SO +HO Cl-+CaSO↓+2H+
2 2 2 2 4
D.用MnO 与浓盐酸共热制备Cl:MnO +4HCl(浓) Mn2++2Cl-+Cl↑+2HO
2 2 2 2 2
5.结构决定性质,性质决定用途,下列事实对应的解释正确的是
选项 事实 解释
A 热稳定性:HF>HCl HF分子间存在氢键
B 掺杂I的聚乙炔塑料能导电 材料中存在能自由移动的电子
2
C 聚乳酸用于生产手术缝合线 聚乳酸为高分子化合物
D 地沟油经过处理加工后可用作飞机、汽车燃油 地沟油主要成分为液态烃
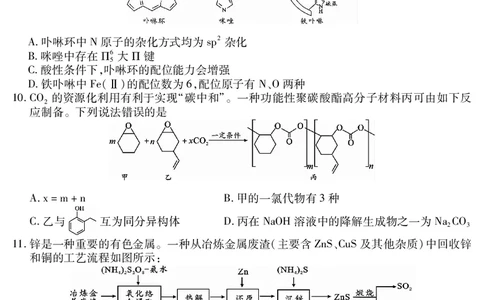
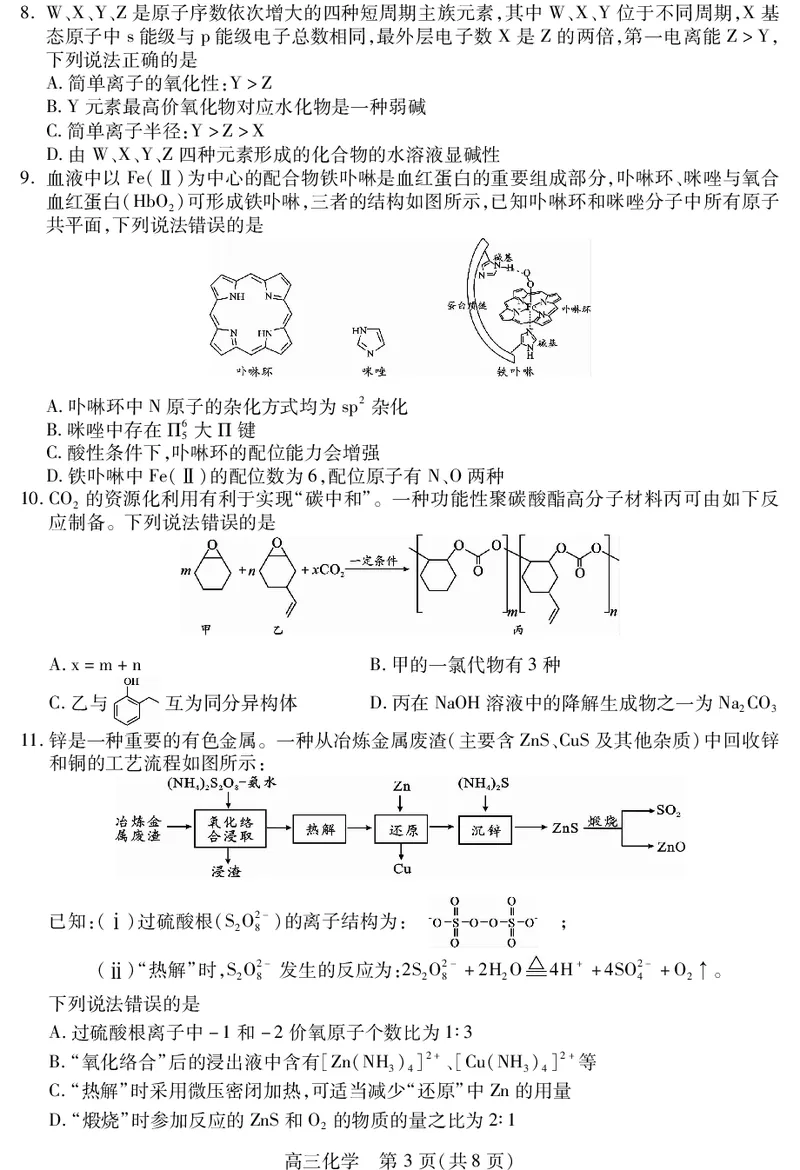
6.科研小组从药用植物中分离出两种具有抗氧化、抗炎作用的有机物茶多酚和咖啡酸,下列
说法正确的是
A.茶多酚中含有的官能团有:羟基、醚键和苯环
B.茶多酚分子中所有碳原子一定共面
C.1mol咖啡酸与饱和溴水反应,最多消耗3molBr
2
D.茶多酚分子中有2个手性碳原子,咖啡酸分子存在顺反异构
7.下列实验操作及现象能得出相应结论的是
选项 实验操作及现象 结论
将表面氧化的铜丝从酒精灯的外焰慢慢移向内 乙醇蒸气将CuO还原为单质
A
焰,黑色的铜丝变红色 Cu
向盛有 NHCl溶液的试管中滴加稀 NaOH溶 NHCl溶液与稀 NaOH溶液
4 4
B
液,用湿润的pH试纸靠近试管口,试纸不变蓝 不反应
取NaHSO 晶体加水充分溶解,滴加 BaCl溶
C 4 2 NaHSO 晶体中含有SO2-
4 4
液,产生白色沉淀
将木炭与热浓硫酸反应后产生的气体依次通过
D 酸性KMnO 溶液、品红溶液、澄清石灰水,品红 气体产物中不含SO
4 2
溶液不褪色,澄清石灰水变浑浊
高三化学 第 2页(共8页)8.W、X、Y、Z是原子序数依次增大的四种短周期主族元素,其中 W、X、Y位于不同周期,X基
态原子中s能级与p能级电子总数相同,最外层电子数 X是 Z的两倍,第一电离能 Z>Y,
下列说法正确的是
A.简单离子的氧化性:Y>Z
B.Y元素最高价氧化物对应水化物是一种弱碱
C.简单离子半径:Y>Z>X
D.由W、X、Y、Z四种元素形成的化合物的水溶液显碱性
9.血液中以Fe(Ⅱ)为中心的配合物铁卟啉是血红蛋白的重要组成部分,卟啉环、咪唑与氧合
血红蛋白(HbO)可形成铁卟啉,三者的结构如图所示,已知卟啉环和咪唑分子中所有原子
2
共平面,下列说法错误的是
A.卟啉环中N原子的杂化方式均为sp2杂化
B.咪唑中存在Π6大Π键
5
C.酸性条件下,卟啉环的配位能力会增强
D.铁卟啉中Fe(Ⅱ)的配位数为6,配位原子有N、O两种
10.CO 的资源化利用有利于实现“碳中和”。一种功能性聚碳酸酯高分子材料丙可由如下反
2
应制备。下列说法错误的是
A.x=m+n B.甲的一氯代物有3种
C.乙与 互为同分异构体 D.丙在NaOH溶液中的降解生成物之一为NaCO
2 3
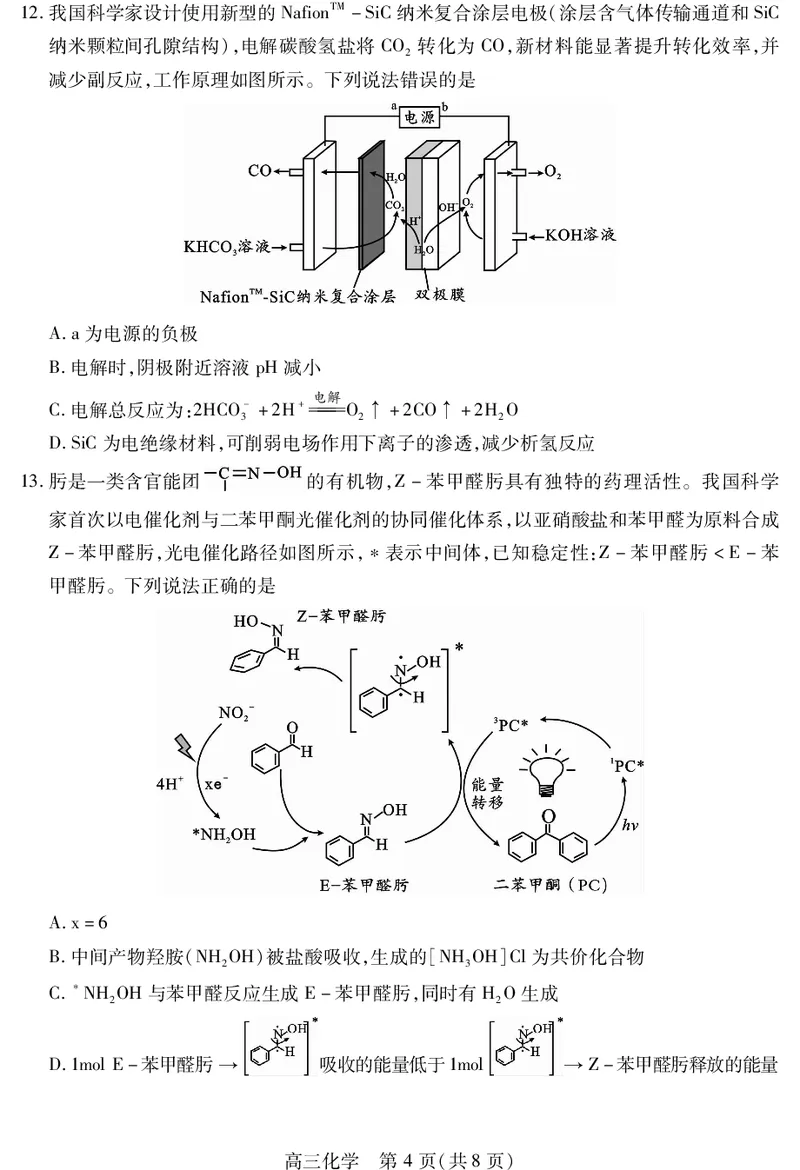
11.锌是一种重要的有色金属。一种从冶炼金属废渣(主要含ZnS、CuS及其他杂质)中回收锌
和铜的工艺流程如图所示:
已知:(ⅰ)过硫酸根(SO2-)的离子结构为: ;
2 8
(ⅱ)“热解”时,SO2-发生的反应为:2SO2-+2HO 4H++4SO2-+O↑。
2 8 2 8 2 4 2
下列说法错误的是
A.过硫酸根离子中-1和-2价氧原子个数比为1∶3
B.“氧化络合”后的浸出液中含有[Zn(NH)]2+、[Cu(NH)]2+等
3 4 3 4
C.“热解”时采用微压密闭加热,可适当减少“还原”中Zn的用量
D.“煅烧”时参加反应的ZnS和O 的物质的量之比为2∶1
2
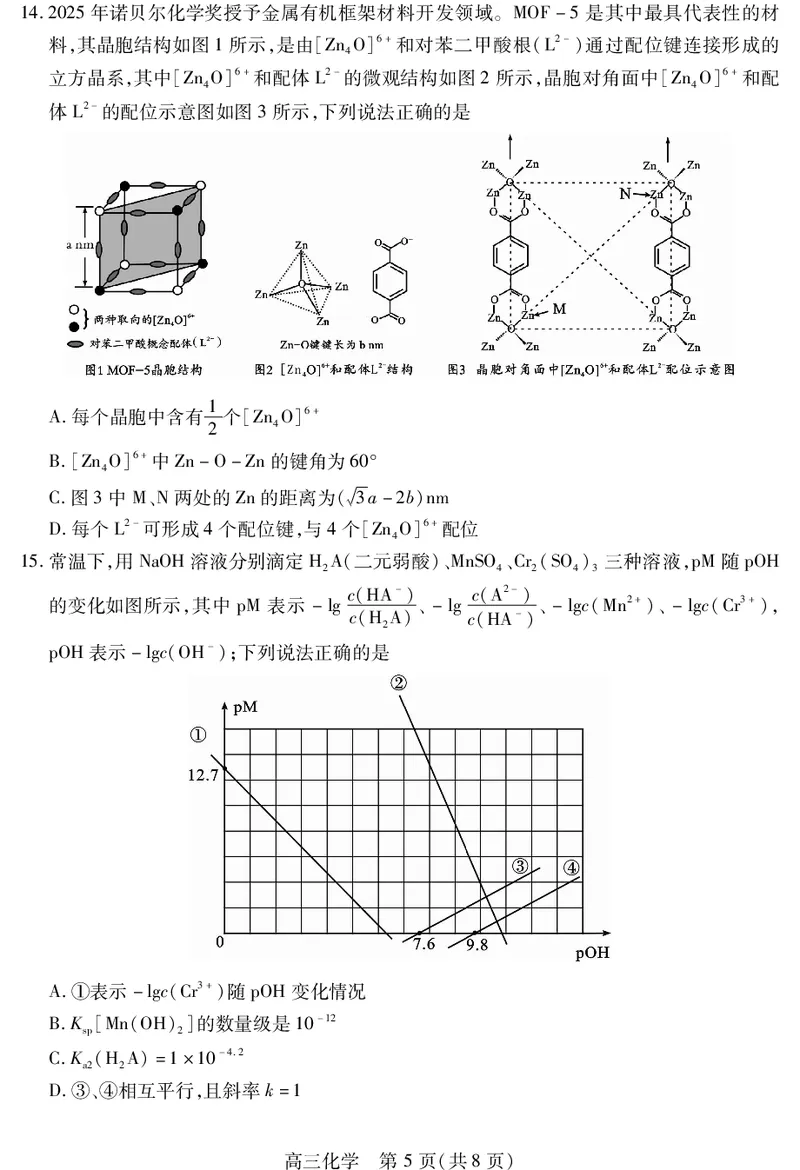
高三化学 第 3页(共8页)12.我国科学家设计使用新型的NafionTM-SiC纳米复合涂层电极(涂层含气体传输通道和SiC
纳米颗粒间孔隙结构),电解碳酸氢盐将 CO 转化为 CO,新材料能显著提升转化效率,并
2
减少副反应,工作原理如图所示。下列说法错误的是
A.a为电源的负极
B.电解时,阴极附近溶液pH减小
电解
C.电解总反应为:2HCO-+2H+O↑+2CO↑+2HO
3 2 2
D.SiC为电绝缘材料,可削弱电场作用下离子的渗透,减少析氢反应
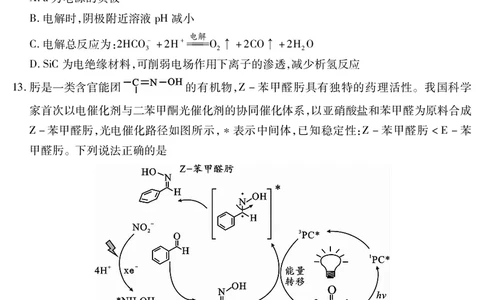
13.肟是一类含官能团 的有机物,Z-苯甲醛肟具有独特的药理活性。我国科学
家首次以电催化剂与二苯甲酮光催化剂的协同催化体系,以亚硝酸盐和苯甲醛为原料合成
Z-苯甲醛肟,光电催化路径如图所示,表示中间体,已知稳定性:Z-苯甲醛肟 <E-苯
甲醛肟。下列说法正确的是
A.x=6
B.中间产物羟胺(NHOH)被盐酸吸收,生成的[NHOH]Cl为共价化合物
2 3
C.NHOH与苯甲醛反应生成E-苯甲醛肟,同时有HO生成
2 2
D.1molE-苯甲醛肟 → 吸收的能量低于1mol → Z-苯甲醛肟释放的能量
高三化学 第 4页(共8页)14.2025年诺贝尔化学奖授予金属有机框架材料开发领域。MOF-5是其中最具代表性的材
料,其晶胞结构如图1所示,是由[ZnO]6+和对苯二甲酸根(L2-)通过配位键连接形成的
4
立方晶系,其中[ZnO]6+和配体L2-的微观结构如图2所示,晶胞对角面中[ZnO]6+和配
4 4
体L2-的配位示意图如图3所示,下列说法正确的是
1
A.每个晶胞中含有 个[ZnO]6+
2 4
B.[ZnO]6+中Zn-O-Zn的键角为60°
4
C.图3中M、N两处的Zn的距离为(槡3a-2b)nm
D.每个L2-可形成4个配位键,与4个[ZnO]6+配位
4
15.常温下,用NaOH溶液分别滴定HA(二元弱酸)、MnSO、Cr(SO)三种溶液,pM随 pOH
2 4 2 4 3
c(HA-) c(A2-)
的变化如图所示,其中 pM表示 -lg 、-lg 、-lgc(Mn2+)、-lgc(Cr3+),
c(HA) c(HA-)
2
pOH表示-lgc(OH-);下列说法正确的是
A.①表示-lgc(Cr3+)随pOH变化情况
B.K[Mn(OH)]的数量级是10-12
sp 2
C.K (HA)=1×10-4.2
a2 2
D.③、④相互平行,且斜率k=1
高三化学 第 5页(共8页)二、非选择题:本题共4小题,共55分。
16.(14分)
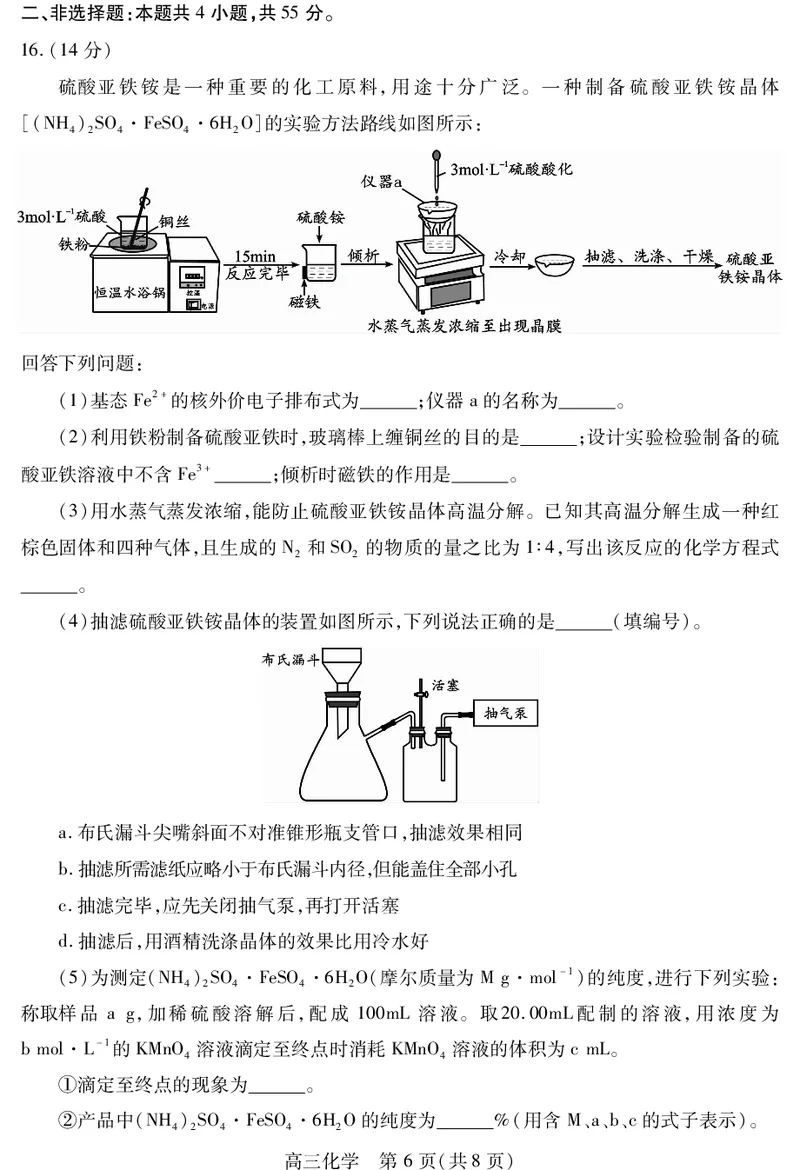
硫酸亚铁铵是一种重要的化工原料,用途十分广泛。一种制备硫酸亚铁铵晶体
[(NH)SO·FeSO·6HO]的实验方法路线如图所示:
4 2 4 4 2
回答下列问题:
(1)基态Fe2+的核外价电子排布式为 ;仪器a的名称为 。
(2)利用铁粉制备硫酸亚铁时,玻璃棒上缠铜丝的目的是 ;设计实验检验制备的硫
酸亚铁溶液中不含Fe3+ ;倾析时磁铁的作用是 。
(3)用水蒸气蒸发浓缩,能防止硫酸亚铁铵晶体高温分解。已知其高温分解生成一种红
棕色固体和四种气体,且生成的N 和SO 的物质的量之比为1∶4,写出该反应的化学方程式
2 2
。
(4)抽滤硫酸亚铁铵晶体的装置如图所示,下列说法正确的是 (填编号)。
a.布氏漏斗尖嘴斜面不对准锥形瓶支管口,抽滤效果相同
b.抽滤所需滤纸应略小于布氏漏斗内径,但能盖住全部小孔
c.抽滤完毕,应先关闭抽气泵,再打开活塞
d.抽滤后,用酒精洗涤晶体的效果比用冷水好
(5)为测定(NH)SO·FeSO·6HO(摩尔质量为Mg·mol-1)的纯度,进行下列实验:
4 2 4 4 2
称取样品 ag,加稀硫酸溶解后,配成 100mL溶液。取20.00mL配制的溶液,用浓度为
bmol·L-1的KMnO 溶液滴定至终点时消耗KMnO 溶液的体积为cmL。
4 4
①滴定至终点的现象为 。
②产品中(NH)SO·FeSO·6HO的纯度为 %(用含M、a、b、c的式子表示)。
4 2 4 4 2
高三化学 第 6页(共8页)17.(13分)
1-甲基萘在催化剂作用下发生选择性加氢反应,生成1-甲基四氢萘和5-甲基四氢萘,
同时伴有副反应,生成1-甲基十氢萘,反应原理如图所示:
回答下列问题:
(1)苯环的侧链烷基中,直接与苯环连接的碳原子上有 C-H,则该 C-H能被酸性高锰
酸钾溶液氧化成 -COOH,即 ,则5-甲基四氢萘被酸性
高锰酸钾溶液完全氧化后含苯环结构的产物的结构简式为 。
(2)ΔH = kJ·mol-1。
4
(3)为提高两种四氢萘产品中5-甲基四氢萘的选择性,可以改进的措施是 。
(4)四个反应的平衡常数K随温度变化的关系如图1所示,温度为 T时,反应1的平衡
1
常数与反应2、反应4的平衡常数之间的关系是 K = (用含 K、K 的式子表示),曲线
1 2 4
a、b中,表示反应2的平衡常数随温度变化的曲线为 (填编号)。
(5)在1×103kPa的高压H 氛围下(H 的压强近似等于总压),向体系中充入1mol1-甲
2 2
基萘,测得不同温度下达平衡时,各物质的物质的量分数 x(x表示某气体的物质的量与除 H
2
外气体总物质的量之比)随温度T的变化关系如图2所示。
①600K到675K时,升高温度,5-甲基四氢萘增多的原因可能是 。
②675K达平衡时1-甲基萘的转化率为 %,反应3的分压平衡常数 K =
p
(kPa)-2(结果保留两位小数)。
18.(14分)
某科研团队用绿柱石(主要成分为BeAlSiO ,含LiO等)生产 BeO和 Al(SO)的工
3 2 6 18 2 2 4 3
艺流程如下:
已知:CHCOOH熔点为122℃,微溶于冷水,易溶于热水。
6 5
高三化学 第 7页(共8页)回答下列问题:
(1)为了提升焙烧效率,可采取的措施有 (写一种即可);焙烧生成的SiF分子的空
4
间构型为 。
(2)“沉铝”时,滤饼的主要成分为苯甲酸铝[Al(CHCOO)],写出该反应的化学方程式 。
6 5 3
(3)“沉铍”时,发生反应的离子方程式为 ;已知常温下K[Be(OH)]=1.0×10-21,若
sp 2
溶液中c(Be2+)=0.1mol·L-1,则Be2+开始沉淀时溶液的pH= 。
(4)流程中“操作a”的名称为 ,实验室进一步提纯CHCOOH的方法是 。
6 5
(5)已知常见的 AB型离子晶体的离子半径比和配位数的关系如下表,已知:
r(Be2+)=45pm,r(O2-)=140pm。
r/r [0.225,0.414) [0.414,1.732) [1.732,1)
+ -
配位数 4 6 8
①则BeO中离子的配位数为 ,下列晶体的晶胞类型与BeO相似的是 (填编号)。
a.立方ZnS晶体(类似金刚石) b.NaCl晶体 c.CaF晶体 d.CsCl晶体
2
②BeO晶胞的边长为 pm(列出计算式)。
19.(14分)
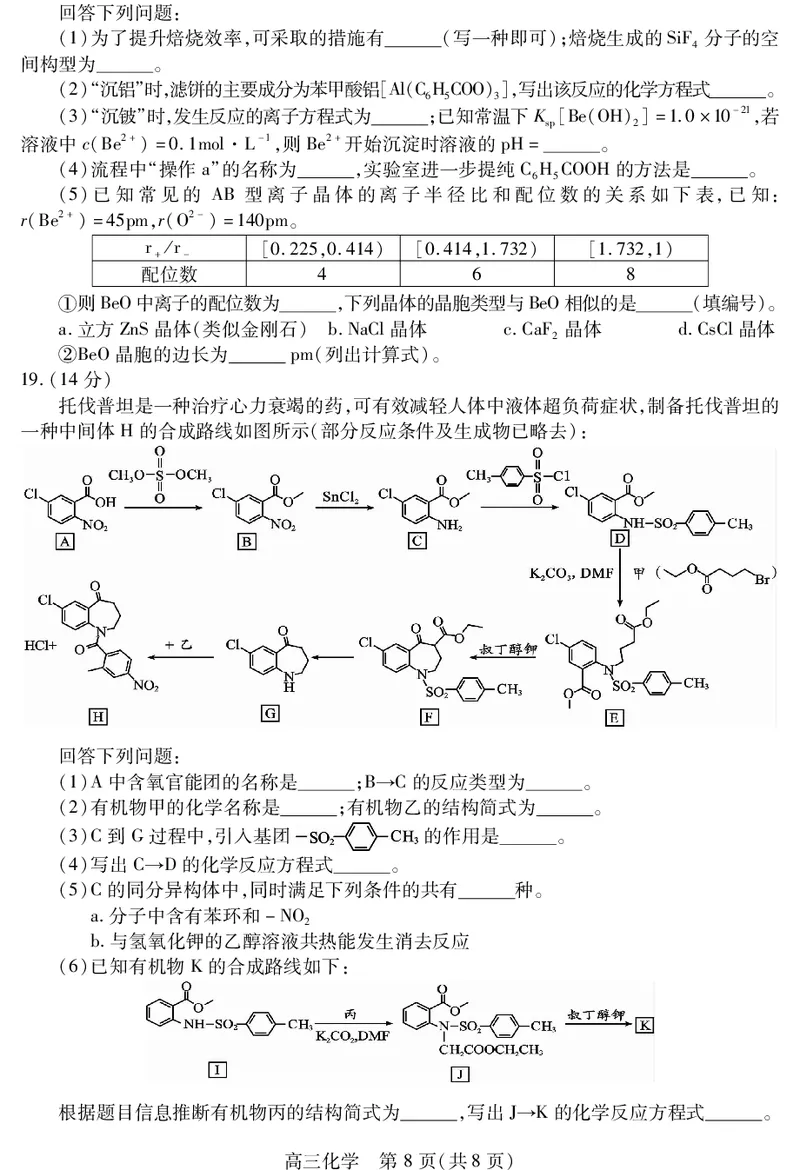
托伐普坦是一种治疗心力衰竭的药,可有效减轻人体中液体超负荷症状,制备托伐普坦的
一种中间体H的合成路线如图所示(部分反应条件及生成物已略去):
回答下列问题:
(1)A中含氧官能团的名称是 ;B→C的反应类型为 。
(2)有机物甲的化学名称是 ;有机物乙的结构简式为 。
(3)C到G过程中,引入基团 的作用是 。
(4)写出C→D的化学反应方程式 。
(5)C的同分异构体中,同时满足下列条件的共有 种。
a.分子中含有苯环和-NO
2
b.与氢氧化钾的乙醇溶液共热能发生消去反应
(6)已知有机物K的合成路线如下:
根据题目信息推断有机物丙的结构简式为 ,写出J→K的化学反应方程式 。
高三化学 第 8页(共8页)