文档内容
2024/2025学年度第一学期
联盟校第二次阶段性考试高一年级化学试题
(总分100分 考试时间75分钟)
本卷可能用到的相对原子质量 H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
一、选择题:(本大题共 28 小题,每小题 3 分,共计 84 分。
在每小题的四个选项中,只有一个选项最符合题目要求。)
1.下列行为不符合“绿色化学”这一主题的是
A.多使用公共交通工具出行 B.植物秸秆就地焚烧
C.发展太阳能和风力发电 D.对燃煤进行脱硫处理
2.发射神舟飞船的火箭箭体使用的是某种铝合金材料。下列不属于火箭箭体所
用铝合金材料特点的是
A.强度高 B.密度大 C.延展性好 D.耐腐蚀
3.萤石又称氟石,是一种矿物,其主要成分是氟化钙(CaF ),CaF 属于
2 2
A.盐 B.单质 C.碱 D.酸
4.许多化学物质在日常生活中有俗名。下列物质的俗名与化学式对应正确的是
A.双氧水—Na O B.胆矾—Cu SO
2 2 4
C.明矾—Al (SO ) D.干冰—CO
2 4 3 2
5.工业上可以利用氪的一种同位素 Kr 进行测井探矿、无损探伤、检查管道泄
85
36
漏等。这里的85是指
A.质子数 B.电子数 C.中子数 D.质量数
6.某物质在灼烧时透过蓝色钴玻璃看到火焰呈紫色,说明该物质中一定含有
A.钾元素 B.钾原子 C.钾离子 D.钾的化合物
7.下列图示表示过滤的是
A B C D
8.下列变化属于化学变化的是A.金属腐蚀 B.氨气液化 C.碘的升华 D.矿石粉碎
9.下列化学用语书写正确的是
A.水溶液中 的电离方程式:
37
B.中子数为18的氯原子: Cl
17
C. 的离子结构示意图为:
D.NaSO 的名称:硫酸钠
2 3
10.我国力争在2060年前实现“碳中和”。1mol CO 在标准状况下体积约为
2
A. 1L B. 11.2L C. 22.4L D. 33.6L
11.下列关于钠及其化合物的描述中,正确的是
A. 钠的硬度很大 B. 钠在O 中燃烧可生成NaO
2 2 2
C. 常温下,钠与O 不反应 D. 电解饱和食盐水可以制得钠
2
12. 有关海水中提取溴的说法错误的是
A.可以利用氯气氧化溴离子
B.海水晒盐后的卤水是提取溴的原料
C.可用高温水蒸气将溴从溶液中吹出
D.吹出的溴蒸气冷凝后得到纯溴
13.舍勒发现氯气是在1774年,他使用软锰矿与浓盐酸混合并加热产生了一种
黄绿色的气体。实验室常用高锰酸钾代替二氧化锰制取氯气,反应的化学方程式
为2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8HO,下列有关该反应的说法
4 2 2 2
正确的是
A.KMnO 是还原剂 B.HCl在反应中得电子
4
C.MnCl 是氧化产物 D.HCl体现还原性和酸性
2
14.下列反应的离子方程式正确的是
A.电解饱和NaCl溶液:
B. 与NaOH溶液反应制取漂白剂:C.向KI溶液中通 制取 :
D.实验室制Cl:MnO + 4H+ + 4Cl- = Mn2+ + Cl ↑+ 2H O
2 2 2 2
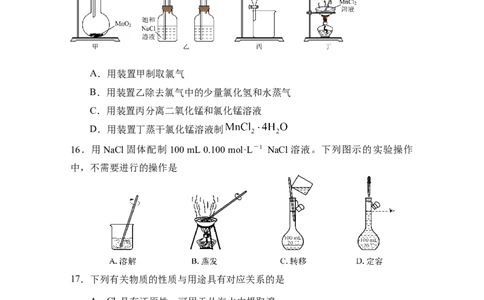
15.下列装置应用于实验室制氯气并回收氯化锰 的实验,能达
到实验目的的是
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢和水蒸气
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制
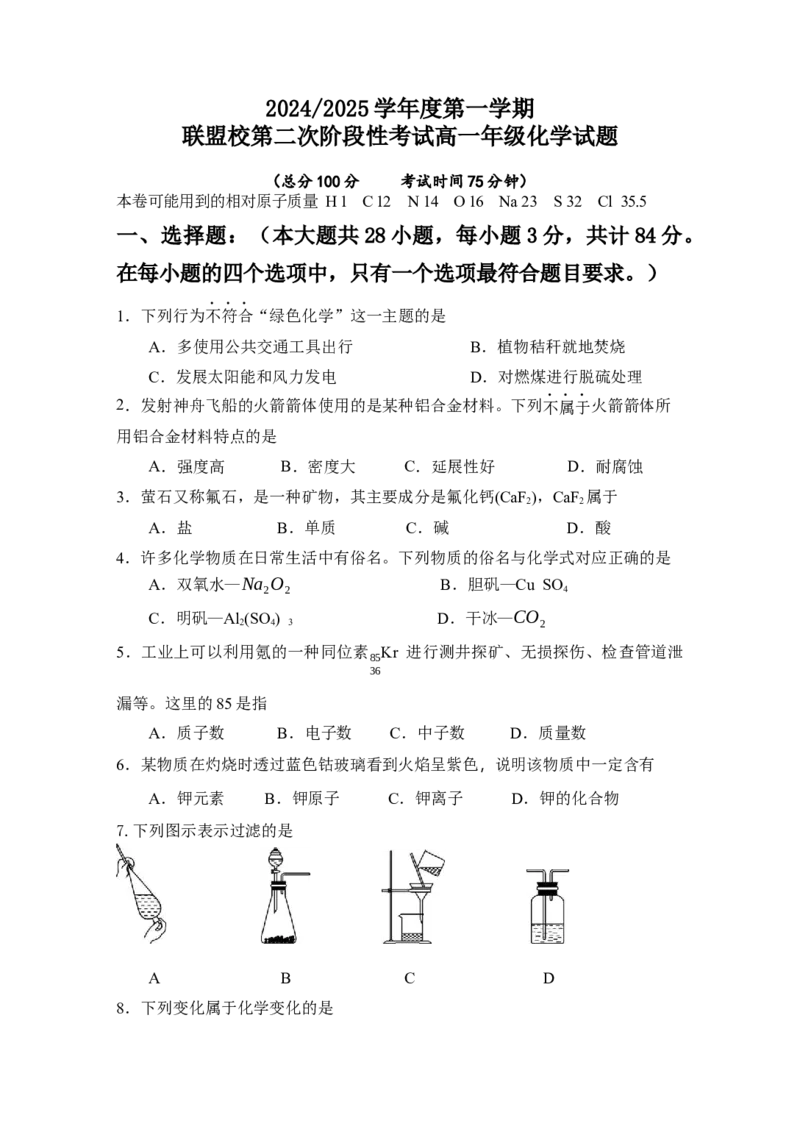
16.用NaCl固体配制100 mL 0.100 mol·L-1 NaCl溶液。下列图示的实验操作
中,不需要进行的操作是
17.下列有关物质的性质与用途具有对应关系的是
A.Cl 具有还原性,可用于从海水中提取溴
2
B.ClO 易溶于水,可用于自来水消毒
2
C.HClO不稳定,可用于棉、麻漂白
D.MnO 有氧化性,可用于实验室制氯气
2
18.适度饮水有益于健康,但过量饮水会使体内电解质浓度过低,导致生理紊乱
而引起“水中毒”。下列属于人体内常见的电解质的是
A.NaCl B.盐酸 C.葡萄糖 D.油脂19.在含有大量的Al3+、H+、SO 的溶液中,还可能大量存在的离子是
A.Fe2+ B.HCO C.OH- D.Ba2+
20. 当光束通过下列分散系时,能产生丁达尔效应的是
A.硫酸铜溶液 B.氢氧化铁胶体 C.医用酒精 D.饱和食盐
水
21.SiC可用作耐火材料。C和Si它们原子结构中相同的是
A.质子 B.电子 C.电子层数 D.最外层电子数
22.硫酸是重要化工产品,广泛用于冶金和石油工业,可通过以下反应生产硫酸:
S + O SO 、2SO + O 2SO 、SO + H O === H SO 。
2 2 2 2 3 3 2 2 4
上述三个反应都属于
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
23.下列有关二氧化硫的说法错误的是
A.SO 能使酸性高锰酸钾溶液褪色,说明SO 具有漂白性
2 2
B.SO 是一种无色刺激性气味且易溶于水的气体
2
C.食品中适量添加SO 可以起到漂白、杀菌、抗氧化的作用
2
D.SO 会引起酸雨
2
24.下列物质的变化,不能通过一步化学反应完成的是
A.Na→NaO B.S→SO
2 2 3
C.Cl→HClO D.HSO (浓)→SO
2 2 4 2
25.HSO 是重要的化工原料,下列说法正确的是
2 4
A.向稀硫酸中滴加酚酞溶液,溶液显红色
B.浓HSO 能跟炭反应,说明浓硫酸具有酸性
2 4
C.可由黄铁矿(FeS )为原料制取
2
D.可用浓硫酸与铁反应制备H
2
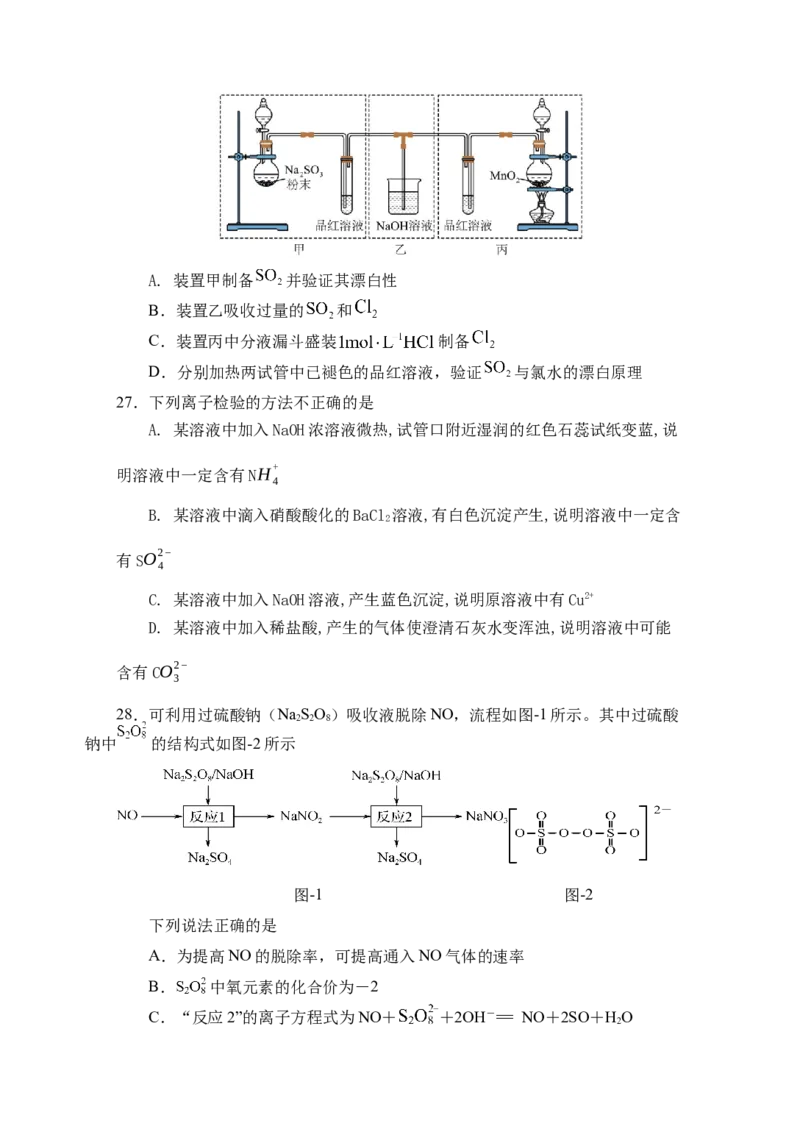
26.探究和比较 和氯水漂白性的实验装置如图所示,下列装置或操作不能实
现目的是A. 装置甲制备 并验证其漂白性
B.装置乙吸收过量的 和
C.装置丙中分液漏斗盛装 制备
D.分别加热两试管中已褪色的品红溶液,验证 与氯水的漂白原理
27.下列离子检验的方法不正确的是
A. 某溶液中加入NaOH浓溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说
明溶液中一定含有NH+
4
B. 某溶液中滴入硝酸酸化的BaCl 溶液,有白色沉淀产生,说明溶液中一定含
2
有SO2−
4
C. 某溶液中加入NaOH溶液,产生蓝色沉淀,说明原溶液中有Cu2+
D. 某溶液中加入稀盐酸,产生的气体使澄清石灰水变浑浊,说明溶液中可能
含有CO2−
3
28.可利用过硫酸钠(NaSO)吸收液脱除NO,流程如图-1所示。其中过硫酸
2 2 8
钠中 的结构式如图-2所示
图-1 图-2
下列说法正确的是
A.为提高NO的脱除率,可提高通入NO气体的速率
B. 中氧元素的化合价为-2
C.“反应2”的离子方程式为NO+ +2OH-= NO+2SO+HO
2D.理论上每脱除1 mol NO,整个流程中至少需加入1 mol Na SO
2 2 8
二、非选择题:本大题共2题,共计16分
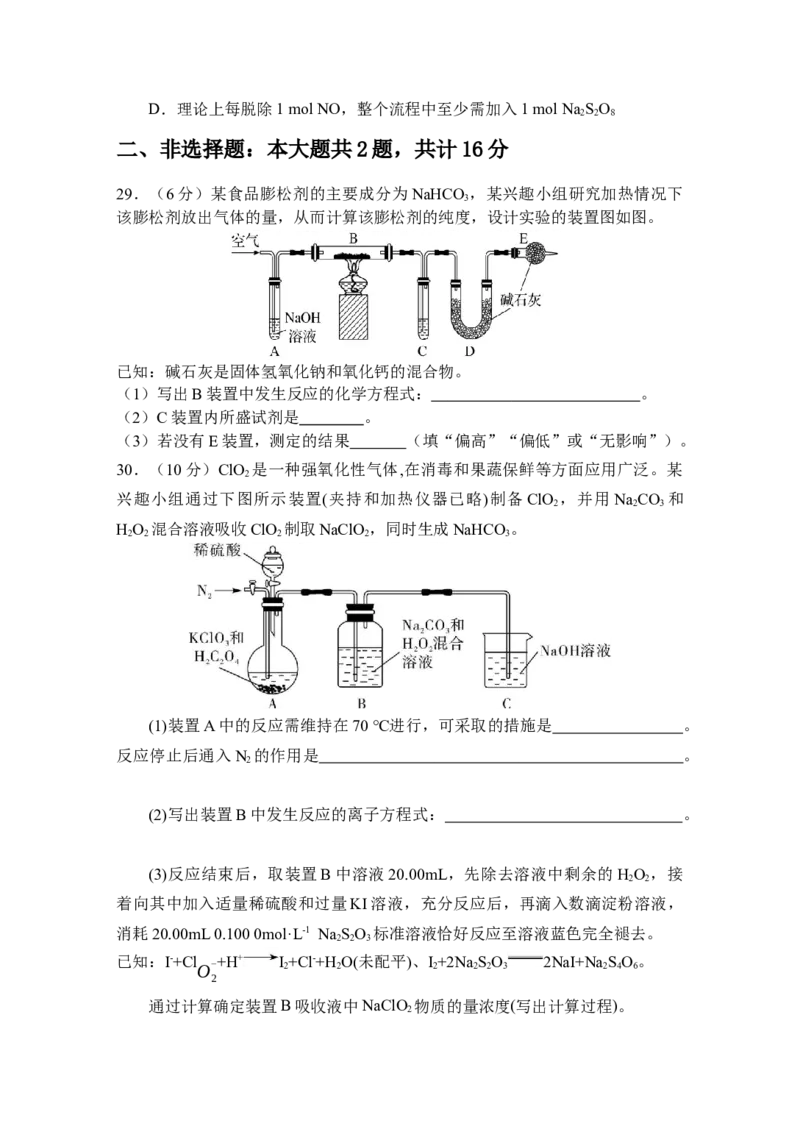
29.(6分)某食品膨松剂的主要成分为NaHCO ,某兴趣小组研究加热情况下
3
该膨松剂放出气体的量,从而计算该膨松剂的纯度,设计实验的装置图如图。
已知:碱石灰是固体氢氧化钠和氧化钙的混合物。
(1)写出B装置中发生反应的化学方程式: 。
(2)C装置内所盛试剂是 。
(3)若没有E装置,测定的结果 (填“偏高”“偏低”或“无影响”)。
30.(10分)ClO 是一种强氧化性气体,在消毒和果蔬保鲜等方面应用广泛。某
2
兴趣小组通过下图所示装置(夹持和加热仪器已略)制备ClO ,并用NaCO 和
2 2 3
HO 混合溶液吸收ClO 制取NaClO,同时生成NaHCO 。
2 2 2 2 3
(1)装置A中的反应需维持在70 ℃进行,可采取的措施是 。
反应停止后通入N 的作用是 。
2
(2)写出装置B中发生反应的离子方程式: 。
(3)反应结束后,取装置B中溶液20.00mL,先除去溶液中剩余的HO ,接
2 2
着向其中加入适量稀硫酸和过量KI溶液,充分反应后,再滴入数滴淀粉溶液,
消耗20.00mL 0.100 0mol·L-1 Na SO 标准溶液恰好反应至溶液蓝色完全褪去。
2 2 3
已知:I-+Cl O-+H+ I
2
+Cl-+H
2
O(未配平)、I
2
+2Na
2
S
2
O
3
2NaI+Na
2
S
4
O
6
。
2
通过计算确定装置B吸收液中NaClO 物质的量浓度(写出计算过程)。
2