文档内容
射洪中学高 2025 级高一上期强实班期中考试
化学试题
(考试时间:60分钟 满分:100分)
注意事项:
1.答卷前,考生务必将自己的班级、姓名、考号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用 2B铅笔把答题卡上对应题目的答案标号涂
黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡对应题号的位置上。写在本试卷上无效。
4.考试结束后,将答题卡交回。
可能用到的相对原子质量:
H—1 C—12 N—14 O—16 Na—23 Al—27 S—32 Cl—35.5
K—39 Fe—56
第 I 卷 选择题
一、选择题:本题共 14 小题, 每小题只有一个选项符合题目要求,每题 3 分, 共 42
分。
1. 下列说法错误的是
①金属钠失火可用干燥的沙土扑灭
②钠能从硫酸铜溶液中置换出金属铜
③Na O 为碱性氧化物,能与水反应生成NaOH
2 2
④NaHCO 可作胃酸中和剂和食用碱
3
⑤Fe O 俗称铁红,常作油漆、涂料、油墨和橡胶的红色颜料
2 3
⑥合金因加入其他原子改变了金属原子的层状排列而硬度变大
A. ①② B. ①④ C. ②③
D. ⑤⑥
2. 下列物质长期露置于空气中会变质,但不涉及氧化还原反应的是
A. Al B. Ca(OH) C. Fe(OH)
2 2
D. 氯水
3. 下列各项物质间的转化不能通过一步反应完成的是
A.
B.
C.D.
4. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 溶液:
B. 的溶液:
C. 能溶解 的溶液:
D. 的溶液:
5.设 NA 为阿伏伽德罗常数的值,下列说法正确的是
A. 2.3 g Na 与O2 反应得到Na2O 与Na2O2 的混合物,转移电子数为0.1NA
B. 2.67 g AlCl3 完全转化为Al(OH)3 胶体,生成的Al(OH)3 胶粒个数为0.02NA
C.标准状况下,11.2 L Cl2 通入足量水中充分反应,转移电子数为 0.5NA
D. 6.0 g NaHSO4 在熔融状态下电离出的阴阳离子总数为 0.15NA
6. 17gNH 溶解在1L水中(水的密度为1g/cm3),所得溶液的密度为ρg/cm3,质量分数为w,
3
物质的量浓度为c,下列叙述正确的是
A. 所得溶液的物质的量浓度c=1mol/L
B. 将该溶液加热蒸发浓缩至原来一半体积,则溶质的物质的量浓度变为原来的两倍
C. 17gNH 所占体积为22.4L
3
D. 所得溶液的溶质质量分数:
7. 等质量的O 和O 相比较,下列有关叙述中正确的是
2 3
①分子数目比为2:3 ②物质的量之比3:2 ③氧原子数之比为1:1
④氧元素质量之比为3:2 ⑤电子数比为2:3
A. ①④ B. ②③ C. ④⑤ D.
①②③④⑤
8. 关于①、②、③、④四套装置的说法正确的是
A. 图①不能证明过氧化钠与水反应放热
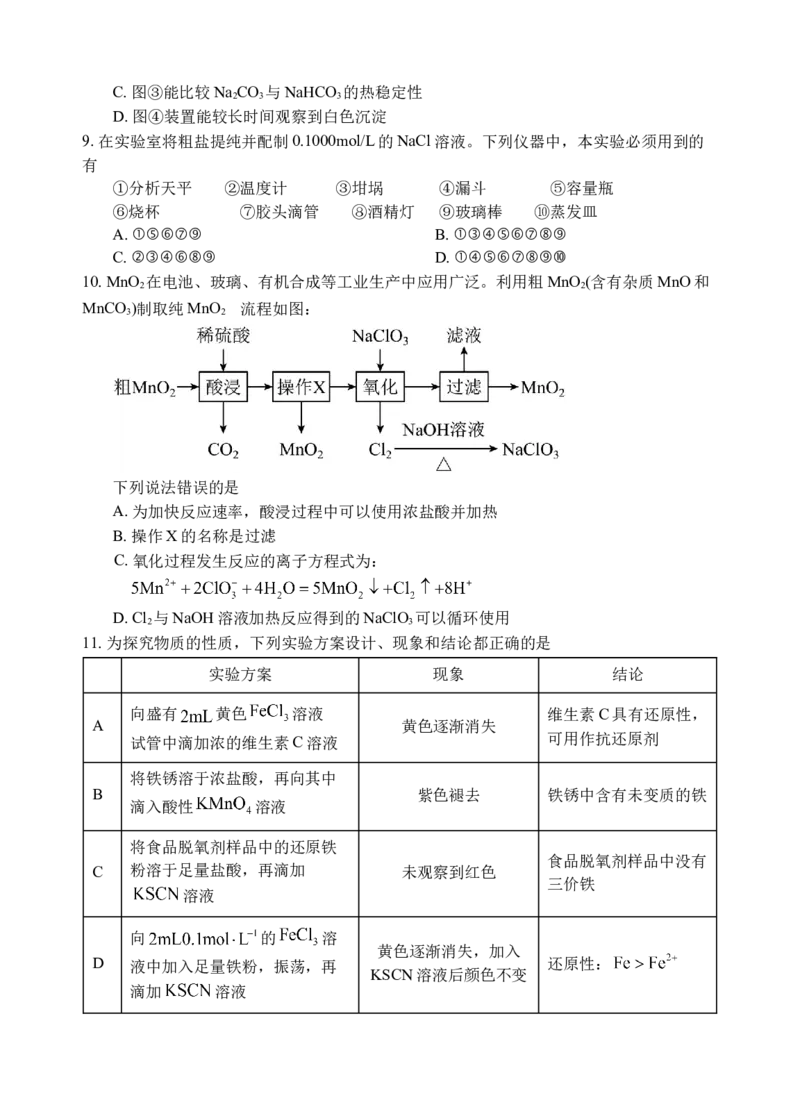
B. 实验室用图②进行固液加热反应C. 图③能比较Na CO 与NaHCO 的热稳定性
2 3 3
D. 图④装置能较长时间观察到白色沉淀
9. 在实验室将粗盐提纯并配制0.1000mol/L的NaCl溶液。下列仪器中,本实验必须用到的
有
①分析天平 ②温度计 ③坩埚 ④漏斗 ⑤容量瓶
⑥烧杯 ⑦胶头滴管 ⑧酒精灯 ⑨玻璃棒 ⑩蒸发皿
A. ①⑤⑥⑦⑨ B. ①③④⑤⑥⑦⑧⑨
C. ②③④⑥⑧⑨ D. ①④⑤⑥⑦⑧⑨⑩
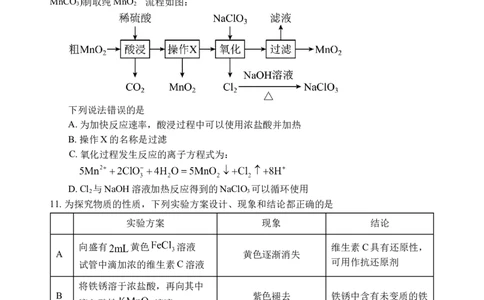
10. MnO 在电池、玻璃、有机合成等工业生产中应用广泛。利用粗MnO (含有杂质MnO和
2 2
MnCO )制取纯MnO 的流程如图:
3 2
下列说法错误的是
A. 为加快反应速率,酸浸过程中可以使用浓盐酸并加热
B. 操作X的名称是过滤
C. 氧化过程发生反应的离子方程式为:
D. Cl 与NaOH溶液加热反应得到的NaClO 可以循环使用
2 3
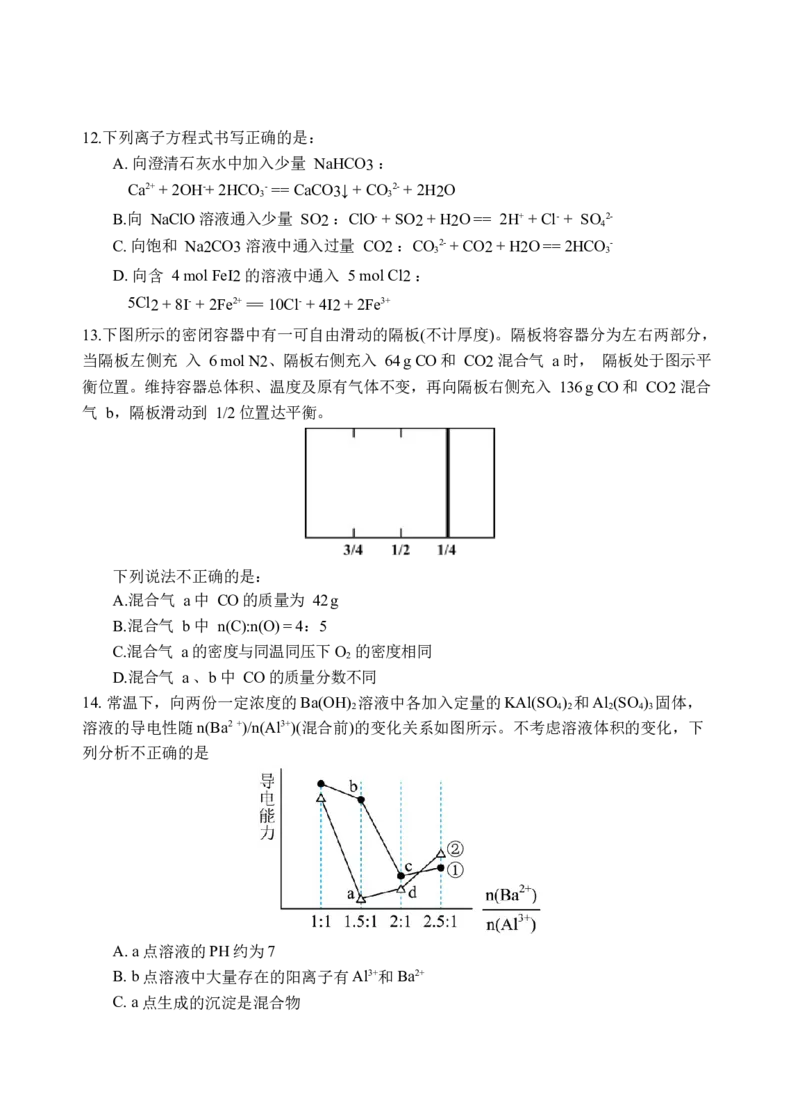
11. 为探究物质的性质,下列实验方案设计、现象和结论都正确的是
实验方案 现象 结论
向盛有 黄色 溶液 的维生素C具有还原性,
A 黄色逐渐消失
可用作抗还原剂
试管中滴加浓的维生素C溶液
将铁锈溶于浓盐酸,再向其中
B 紫色褪去 铁锈中含有未变质的铁
滴入酸性 溶液
将食品脱氧剂样品中的还原铁
食品脱氧剂样品中没有
C 粉溶于足量盐酸,再滴加 未观察到红色
三价铁
溶液
向 的 溶
黄色逐渐消失,加入
D 液中加入足量铁粉,振荡,再 还原性:
KSCN溶液后颜色不变
滴加 溶液12.下列离子方程式书写正确的是:
A. 向澄清石灰水中加入少量 NaHCO3 :
Ca2+ + 2OH-+ 2HCO - == CaCO3↓ + CO 2- + 2H2O
3 3
B.向 NaClO 溶液通入少量 SO2 :ClO- + SO2 + H2O == 2H+ + Cl- + SO 2-
4
C. 向饱和 Na2CO3 溶液中通入过量 CO2 :CO 2-+ CO2 + H2O == 2HCO -
3 3
D. 向含 4 mol FeI2 的溶液中通入 5 mol Cl2 :
5Cl2 + 8I- + 2Fe2+ == 10Cl- + 4I2 + 2Fe3+
13.下图所示的密闭容器中有一可自由滑动的隔板(不计厚度)。隔板将容器分为左右两部分,
当隔板左侧充 入 6 mol N2、隔板右侧充入 64 g CO 和 CO2 混合气 a 时, 隔板处于图示平
衡位置。维持容器总体积、温度及原有气体不变,再向隔板右侧充入 136 g CO 和 CO2 混合
气 b,隔板滑动到 1/2 位置达平衡。
下列说法不正确的是:
A.混合气 a 中 CO 的质量为 42 g
B.混合气 b 中 n(C):n(O) = 4:5
C.混合气 a 的密度与同温同压下O 的密度相同
2
D.混合气 a 、b 中 CO 的质量分数不同
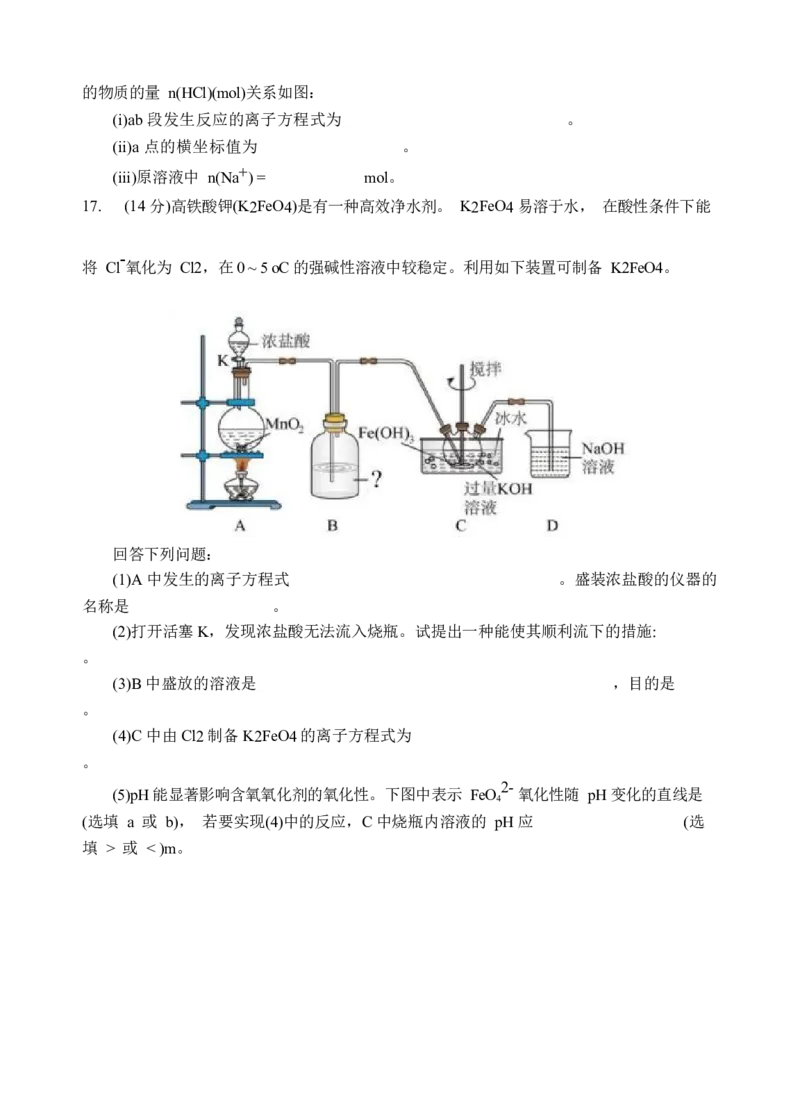
14. 常温下,向两份一定浓度的Ba(OH) 溶液中各加入定量的KAl(SO ) 和Al (SO ) 固体,
2 4 2 2 4 3
溶液的导电性随n(Ba2 +)/n(Al3+)(混合前)的变化关系如图所示。不考虑溶液体积的变化,下
列分析不正确的是
A. a点溶液的PH约为7
B. b点溶液中大量存在的阳离子有Al3+和Ba2+
C. a点生成的沉淀是混合物D. ②代表加入Al (SO ) 的变化曲线
2 4 3
第 II 卷(非选择题)
二、非选择题:本题共4小题,总计58分。
15. (14 分) 按要求完成下列有关问题。
(1) 钠与水反应的化学方程式:
。
(2)四氧化三铁溶于稀硝酸的离子方程式:
。
(3)0. 1 molCO 与6.4gNaOH 充分反应的总离子方程式 :
2
。
(4)当温度70℃,可发现KC1O 与浓盐酸反应的氧化产物及还原产物均为ClO 气
3 2
体,试写出该反应的化学方程式:
。此时参与反应的氧化剂与还原剂物质的量比为 。
(5)配平方程式:_____P4 + ______P2I4 + _______H2O= ______PH4I +_____H3PO4。
(6)0.5 mol 乙醇(C H OH)完全燃烧产生的CO2和水蒸气全部通入过量的Na2O2 完
2 5
全吸收,可使固体增重 g。
16. (14 分)某无色澄清溶液仅可能由下列离子中的几种组成:
阳离子 NH
4
+ 、K+ 、Na+ 、Ag+ 、Cu2+
阴离子 OH- 、CO 2- 、 Cl、HSO - 、SO 2-
3 3 4
现将该溶液平均分成三等份,进行如下实验:
① 取第一份试样滴入紫色石蕊试液,溶液呈深蓝色。
② 取第二份试样加入足量 Ba(NO3)2 溶液, 产生白色沉淀,过滤。
③ 向②的滤渣中加入过量稀盐酸, 沉淀部分溶解,再次过滤。
④ 将③的滤渣洗涤、干燥并称重, 得 2.33 g 白色固体。
⑤ 取②中滤液, ,未见白色沉淀生成。 回答下列问题:
(1)实验⑤的目的是检验 Cl- 。试补充空白处遗漏的操作:
。
(2)根据上述实验, 该溶液中一定不存在的离子有 ,一定存在的离子有
。
(3)蘸取少量试样进行焰色试验,观察到火焰呈 色,说明溶液中有 Na +存
在为确定 K +是否存在,透过 (填仪器名称)再次观察火焰,未见紫色。
(4)向第三份试样中逐滴加入稀盐酸, 最终有无色气
体产生。生成气体的标况下体积 V(气体)(mL)与加入盐酸的物质的量 n(HCl)(mol)关系如图:
(i)ab 段发生反应的离子方程式为 。
(ii)a 点的横坐标值为 。
(iii)原溶液中 n(Na + ) = mol。
17. (14 分)高铁酸钾(K2FeO4)是有一种高效净水剂。 K2FeO4 易溶于水, 在酸性条件下能
-
将 Cl 氧化为 Cl2,在0 ~ 5 oC 的强碱性溶液中较稳定。利用如下装置可制备 K2FeO4。
回答下列问题:
(1)A 中发生的离子方程式 。盛装浓盐酸的仪器的
名称是 。
(2)打开活塞K,发现浓盐酸无法流入烧瓶。试提出一种能使其顺利流下的措施:
。
(3)B 中盛放的溶液是 ,目的是
。
(4)C 中由Cl2制备K2FeO4的离子方程式为
。
2-
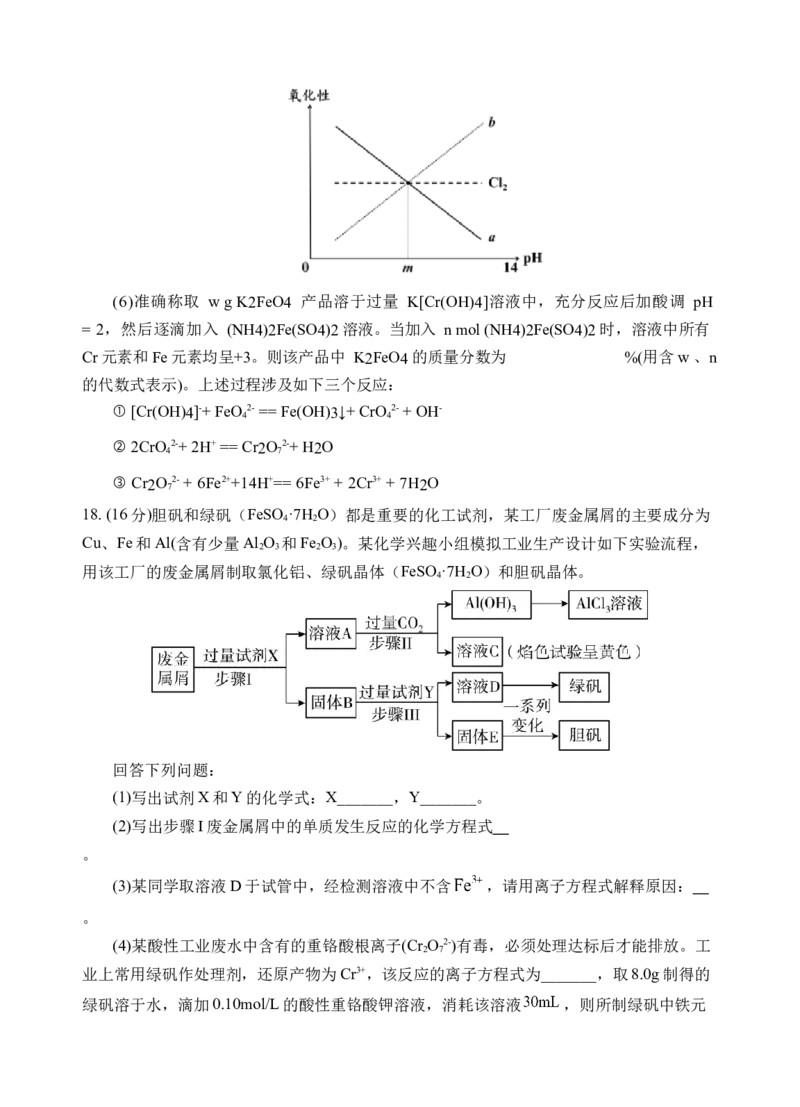
(5)pH 能显著影响含氧氧化剂的氧化性。下图中表示 FeO 氧化性随 pH 变化的直线是
4
(选填 a 或 b), 若要实现(4)中的反应,C 中烧瓶内溶液的 pH 应 (选
填 > 或 < )m。(6)准确称取 w g K2FeO4 产品溶于过量 K[Cr(OH)4]溶液中,充分反应后加酸调 pH
= 2,然后逐滴加入 (NH4)2Fe(SO4)2 溶液。当加入 n mol (NH4)2Fe(SO4)2 时,溶液中所有
Cr元素和Fe元素均呈+3。则该产品中 K2FeO4 的质量分数为 %(用含w 、n
的代数式表示)。上述过程涉及如下三个反应:
① [Cr(OH)4]-+ FeO 2- == Fe(OH)3↓+ CrO 2-+ OH-
4 4
② 2CrO 2-+ 2H+ == Cr2O 2-+ H2O
4 7
③ Cr2O 2- + 6Fe2++14H+== 6Fe3+ + 2Cr3+ + 7H2O
7
18. (16分)胆矾和绿矾(FeSO ·7H O)都是重要的化工试剂,某工厂废金属屑的主要成分为
4 2
Cu、Fe和Al(含有少量Al O 和Fe O )。某化学兴趣小组模拟工业生产设计如下实验流程,
2 3 2 3
用该工厂的废金属屑制取氯化铝、绿矾晶体(FeSO ·7H O)和胆矾晶体。
4 2
回答下列问题:
(1)写出试剂X和Y的化学式:X_______,Y_______。
(2)写出步骤I废金属屑中的单质发生反应的化学方程式
。
(3)某同学取溶液D于试管中,经检测溶液中不含 ,请用离子方程式解释原因:
。
(4)某酸性工业废水中含有的重铬酸根离子(Cr O 2-)有毒,必须处理达标后才能排放。工
2 7
业上常用绿矾作处理剂,还原产物为Cr3+,该反应的离子方程式为_______,取8.0g制得的
绿矾溶于水,滴加0.10mol/L的酸性重铬酸钾溶液,消耗该溶液 ,则所制绿矾中铁元素的质量分数为_______。
(5)实验室需使用200mL1.00mol/LFeSO 溶液。配制溶液时所需玻璃仪器除烧杯、量
4
筒、玻璃棒外还有 ,先计算所需绿矾固
体的质量: g并称量,然后配制溶液。定容时若俯视容量瓶刻度线,会导
致溶液浓度 (填偏大、偏小或无影响)。