文档内容
射洪中学高 2025 级高一上期第二次月考
化学试题
命题人:蒋函灵 黄芳 审题人:赖光贵
(考试时间:60分钟 满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用 2B铅笔把答题卡上对应题目的答案
标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无
效。
3.回答非选择题时,将答案写在答题卡对应题号的位置上。写在本试卷上无
效。
4.考试结束后,将答题卡交回。
第 I 卷(选择题,共 60 分)
一、选择题(单选题,共15题,每题4分,共60分。)
1.下列发生的变化与氧化还原反应无关的是
A.食物腐败 B.钟乳石的形成 C.铁的生锈 D.液化气的燃烧
2.下列化学用语或图示表达不正确的是
A.还原剂和氧化剂的关系:
B.NaCl溶液中的水合离子:
C. 在水中电离:
D. 的同素异形体:
3.BaS可通过BaSO +4H BaS+4H O反应制得。下列有关的说法正确的是
4 2 2
A.BaSO 中含有硫酸根,属于酸 B.反应类型为置换反应
4
C.BaSO 、BaS均属于盐 D.BaSO 中硫元素的化合价为+4
4 4
4.下列说法正确的是
A.分散系有的是纯净物,有的是混合物
B.溶液和胶体的本质区别为是否有丁达尔效应
C.直径在1~100nm的Al(OH) 颗粒属于胶体
3
高一化学 第 1 页 共 6 页D.泥水、食盐水、有色玻璃分别为浊液、溶液、胶体
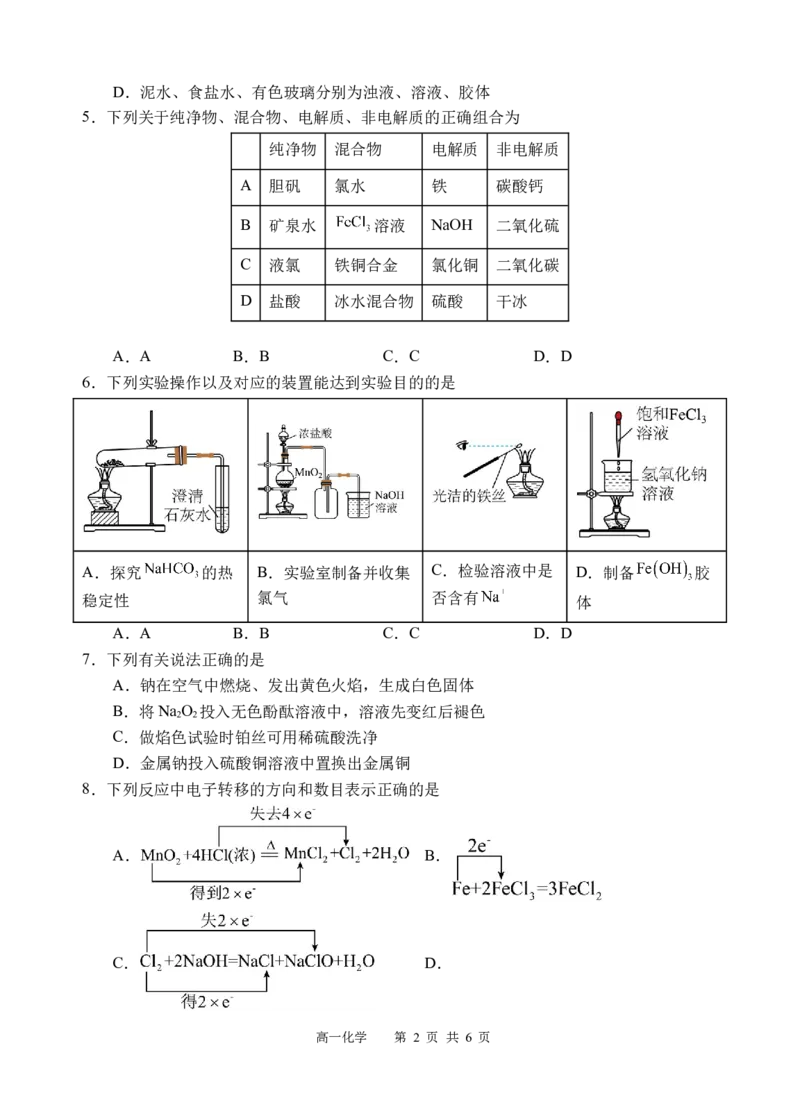
5.下列关于纯净物、混合物、电解质、非电解质的正确组合为
纯净物 混合物 电解质 非电解质
A 胆矾 氯水 铁 碳酸钙
B 矿泉水 溶液 NaOH 二氧化硫
C 液氯 铁铜合金 氯化铜 二氧化碳
D 盐酸 冰水混合物 硫酸 干冰
A.A B.B C.C D.D
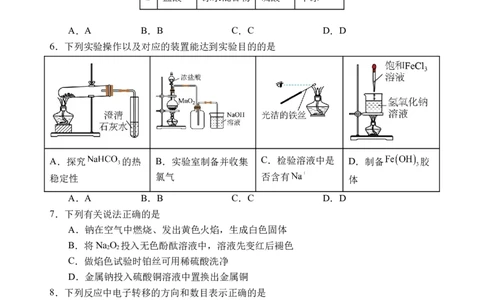
6.下列实验操作以及对应的装置能达到实验目的的是
A.探究 的热 B.实验室制备并收集 C.检验溶液中是 D.制备 胶
稳定性 氯气 否含有 体
A.A B.B C.C D.D
7.下列有关说法正确的是
A.钠在空气中燃烧、发出黄色火焰,生成白色固体
B.将Na O 投入无色酚酞溶液中,溶液先变红后褪色
2 2
C.做焰色试验时铂丝可用稀硫酸洗净
D.金属钠投入硫酸铜溶液中置换出金属铜
8.下列反应中电子转移的方向和数目表示正确的是
A. B.
C. D.
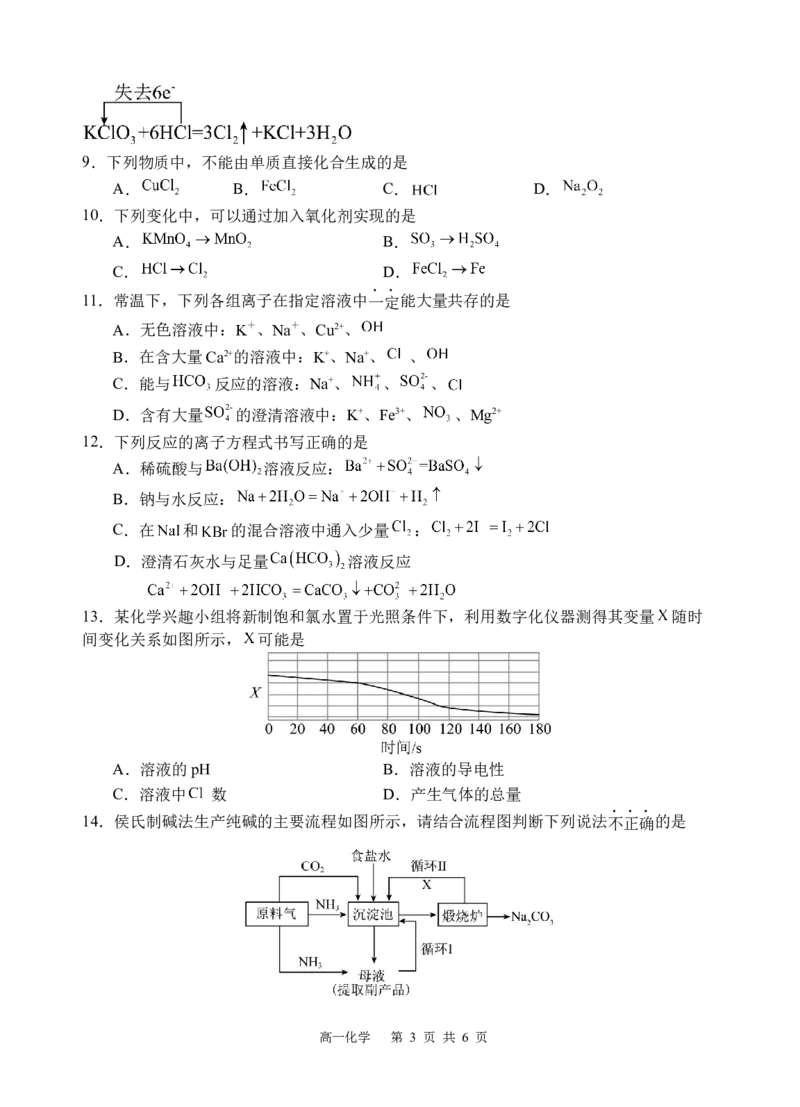
高一化学 第 2 页 共 6 页9.下列物质中,不能由单质直接化合生成的是
A. B. C. D.
10.下列变化中,可以通过加入氧化剂实现的是
A. B.
C. D.
11.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.无色溶液中:K+、Na+、Cu2+、
B.在含大量Ca2+的溶液中:K+、Na+、 、
C.能与 反应的溶液:Na+、 、 、
D.含有大量 的澄清溶液中:K+、Fe3+、 、Mg2+
12.下列反应的离子方程式书写正确的是
A.稀硫酸与 溶液反应:
B.钠与水反应:
C.在 和 的混合溶液中通入少量 :
D.澄清石灰水与足量 溶液反应
13.某化学兴趣小组将新制饱和氯水置于光照条件下,利用数字化仪器测得其变量 随时
间变化关系如图所示, 可能是
A.溶液的pH B.溶液的导电性
C.溶液中 数 D.产生气体的总量
14.侯氏制碱法生产纯碱的主要流程如图所示,请结合流程图判断下列说法不正确的是
高一化学 第 3 页 共 6 页A.该流程中未涉及氧化还原反应
B.该流程中 可循环使用,副产品可作肥料
C.该流程中向饱和食盐水中先通 至饱和,再通足量
D.沉淀池中发生反应的化学方程式为:
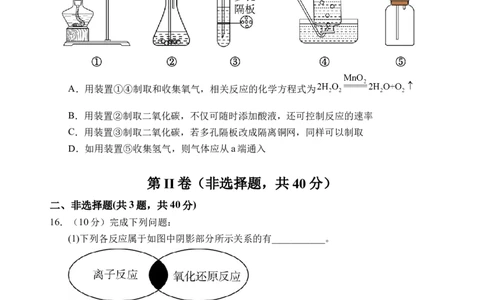
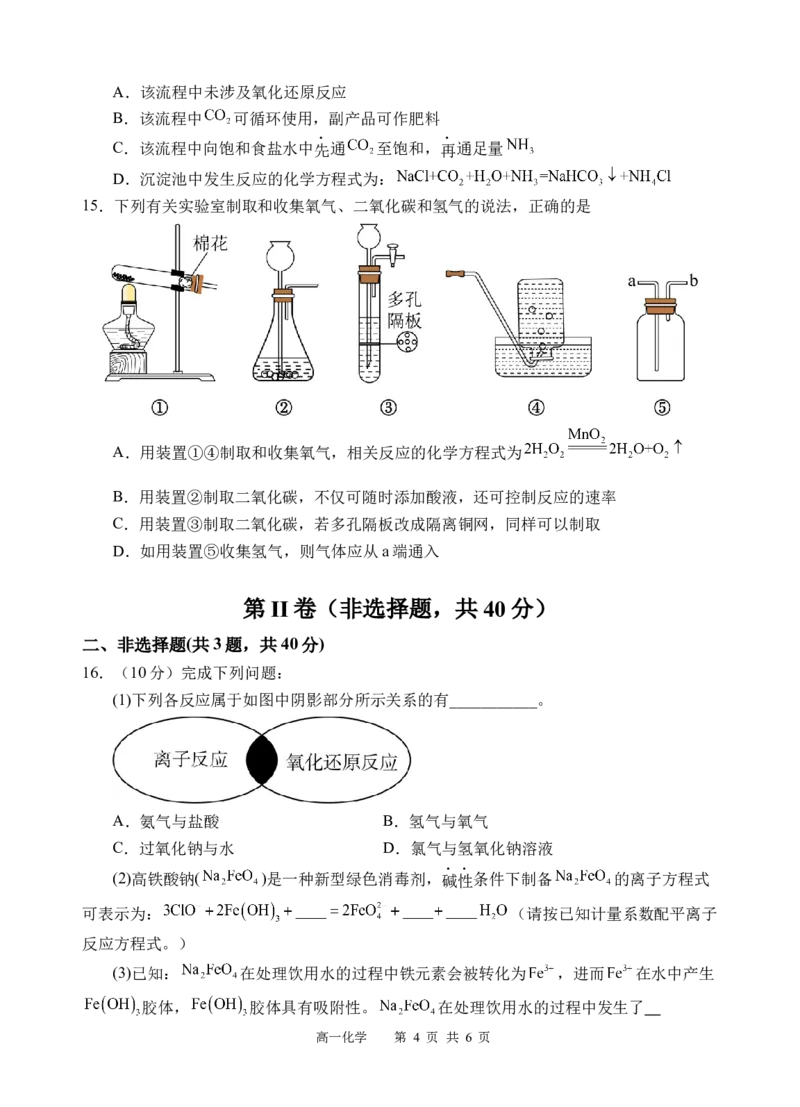
15.下列有关实验室制取和收集氧气、二氧化碳和氢气的说法,正确的是
A.用装置①④制取和收集氧气,相关反应的化学方程式为
B.用装置②制取二氧化碳,不仅可随时添加酸液,还可控制反应的速率
C.用装置③制取二氧化碳,若多孔隔板改成隔离铜网,同样可以制取
D.如用装置⑤收集氢气,则气体应从a端通入
第 II 卷(非选择题,共 40 分)
二、非选择题(共3题,共40分)
16.(10分)完成下列问题:
(1)下列各反应属于如图中阴影部分所示关系的有___________。
A.氨气与盐酸 B.氢气与氧气
C.过氧化钠与水 D.氯气与氢氧化钠溶液
(2)高铁酸钠( )是一种新型绿色消毒剂,碱性条件下制备 的离子方程式
可表示为: (请按已知计量系数配平离子
反应方程式。)
(3)已知: 在处理饮用水的过程中铁元素会被转化为 ,进而 在水中产生
胶体, 胶体具有吸附性。 在处理饮用水的过程中发生了
高一化学 第 4 页 共 6 页(填“氧化”、“还原”或“非氧化还原”)反应。 胶体为 色液体,写出
区分胶体与溶液的实验方法名称: 。
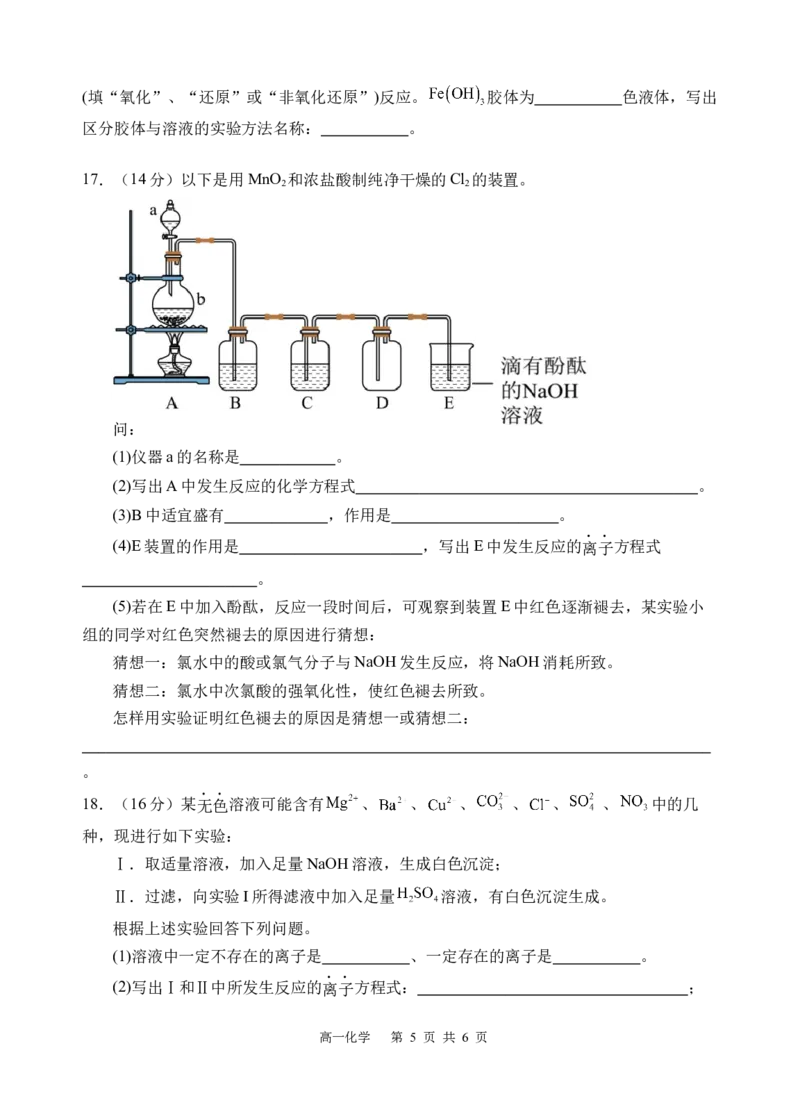
17.(14分)以下是用MnO 和浓盐酸制纯净干燥的Cl 的装置。
2 2
问:
(1)仪器a的名称是 。
(2)写出A中发生反应的化学方程式 。
(3)B中适宜盛有 ,作用是 。
(4)E装置的作用是 ,写出E中发生反应的离子方程式
。
(5)若在E中加入酚酞,反应一段时间后,可观察到装置E中红色逐渐褪去,某实验小
组的同学对红色突然褪去的原因进行猜想:
猜想一:氯水中的酸或氯气分子与NaOH发生反应,将NaOH消耗所致。
猜想二:氯水中次氯酸的强氧化性,使红色褪去所致。
怎样用实验证明红色褪去的原因是猜想一或猜想二:
。
18.(16分)某无色溶液可能含有 、 、 、 、 、 、 中的几
种,现进行如下实验:
Ⅰ.取适量溶液,加入足量NaOH溶液,生成白色沉淀;
Ⅱ.过滤,向实验I所得滤液中加入足量 溶液,有白色沉淀生成。
根据上述实验回答下列问题。
(1)溶液中一定不存在的离子是 、一定存在的离子是 。
(2)写出Ⅰ和Ⅱ中所发生反应的离子方程式: ;
高一化学 第 5 页 共 6 页; 。
(3)为了验证溶液中是否存在 、 ,某同学提出下列假设:
①只存在 ;② 、 同时存在;③只存在 。
已知实验提供的试剂只有稀盐酸、 溶液、稀硝酸、NaOH溶液和蒸馏水。
验证溶液中是否存在 的实验方法: 。
(4)若阳离子的数目均为a个,不管阴离子的种类是一种还是两种,阴离子的总数目可以
肯定的是 个。
(5)某化工厂排出的废液中含有 、 、 三种金属阳离子,欲用分别含 、
、 三种不同的阴离子的物质将上述金属阳离子逐一形成沉淀除去。正确加入阴离子
的先后顺序是: 。
高一化学 第 6 页 共 6 页