文档内容
2020年上海市中考化学试卷
一、选择题(共20分)下列各题均只有一个正确选项,请将正确选项的代号用 2B铅笔填
涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂。
1.(1分)空气中含量最多的物质是( )
A.氧气 B.氮气 C.氦气 D.水蒸气
2.(1分)镁的元素符号是( )
A.mg B.Mg C.Mn D.Ag
3.(1分)属于悬浊液的是( )
A.矿泉水 B.糖水 C.泥水 D.自来水
4.(1分)物质中氯元素以游离态形式存在的是( )
A.Cl B.FeCl C.NH Cl D.HCl
2 3 4
5.(1分)互为同素异形体的一组物质是( )
A.大理石与石灰石 B.氧气与液氧
C.石墨与金刚石 D.水与双氧水
6.(1分)下列可作氮肥的物质是( )
A.(NH ) SO B.K SO C.KCl D.Ca(H PO )
4 2 4 2 4 2 4 2
7.(1分)含有氧分子的物质是( )
A.过氧化氢 B.氧气 C.二氧化碳 D.氧化镁
8.(1分)下列属于有机物的是( )
A.氧气 B.水 C.蔗糖 D.氯化钾
9.(1分)具有良好发展前景的绿色能源是( )
A.氢气 B.煤 C.木炭 D.石油
10.(1分)一些食物的近似pH如下,其中呈碱性的是( )
选项 A B C D
食物 苹果汁 西红柿汁 菠菜汁 鸡蛋清
pH 2.9﹣3.3 4.0﹣4.4 5.1﹣5.7 7.6﹣8.0
A.A B.B C.C D.D
11.(1分)下列物质中,金属活动性最强的是( )
A.铝 B.铁 C.铜 D.银
12.(1分)玻璃棒不能用于( )A.蘸取液体 B.引流液体 C.捣碎石灰石 D.搅拌液体
13.(1分)物质的俗名和化学式对应正确的是( )
A.干冰 H O B.烧碱 NaOH C.纯碱 K CO D.熟石灰 CaO
2 2 3
14.(1分)自来水生产中通入氯气的作用是( )
A.杀菌消毒 B.沉降颗粒物
C.吸附有色物质 D.凝聚悬浮物
15.(1分)用氯化钠固体配制5%的氯化钠溶液100g,无需使用的仪器是( )
A.电子天平 B.烧杯 C.药匙 D.蒸发皿
16.(1分)酸的组成中一定含有( )
A.金属元素 B.氧元素 C.原子团 D.酸根
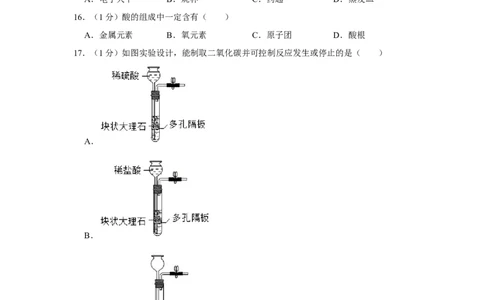
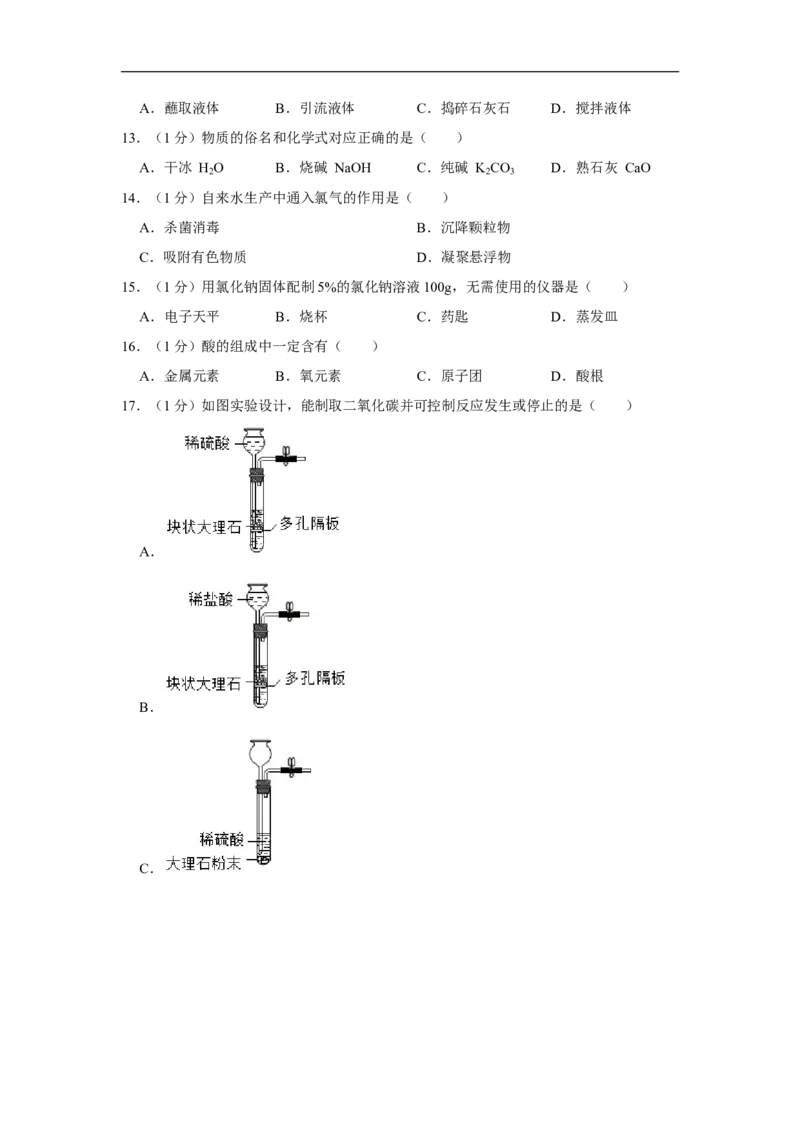
17.(1分)如图实验设计,能制取二氧化碳并可控制反应发生或停止的是( )
A.
B.
C.D.
18.(1分)有关中和反应的说法一定正确的是( )
A.反应物均须溶于水 B.有沉淀生成
C.有气体生成 D.有盐生成
19.(1分)关于粗盐提纯的实验,说法正确的是( )
A.粗盐不可以放在烧杯里称量
B.蒸发皿不可以直接加热
C.蒸发时发现有固体开始析出,即停止加热
D.涉及的分离操作有溶解、过滤和蒸发
20.(1分)在100mL 5%的硫酸中依次加入一定量的氧化铁和氢氧化钠溶液,有关说法
一定正确的是( )
A.有沉淀生成
B.溶液最终呈黄色
C.只发生两个反应
D.溶液中硫酸根的物质的量始终不变
二、填空题(共22分)请根据要求在答题纸的相应位置作答。
21.(7分)化学消毒剂主要用于杀灭病原微生物,在控制传染病的过程中发挥重要作用。
①75%的酒精常用于医疗消毒。75%的酒精溶液属于 (选填“纯净物”或
“混合物”),酒精挥发属于 (选填“物理”或“化学”)变化。
②84消毒液(主要成分NaClO)适用于一般物体表面消毒。NaClO由 种不同
元素组成,灼烧时火焰呈 色。
③二氧化氯(ClO )是一种高效消毒剂。ClO 中Cl、O原子个数比为 ,Cl
2 2
元素的化合价为 ;1mol ClO 中约含有 个Cl原子。
2
22 . ( 9 分 ) 实 验 室 制 取 氧 气 并 进 行 相 关 性 质 实 验 。①写出仪器甲的名称 。
②以氯酸钾和二氧化锰为原料制氧气的化学方程式是 ,应选
用的发生装置是 (选填编号),用向上排空气法收集氧气应选用的装置是
(选填编号)。
③用排水法收集氧气时,集气瓶内的水全部排出后,将导管移出集气瓶,再进行如下
操作:a.从水槽中取出集气瓶;b.瓶口向上放置;c.在集气瓶口盖好毛玻璃片。正
确的操作顺序是 (用编号排序)。
④硫在氧气中燃烧生成二氧化硫,火焰呈 色;二氧化硫若大量排放到空气中
造 成 的 后 果 是 。 铁 丝 在 氧 气 中 燃 烧 的 化 学 方 程 式 是
,实验时应预先在集气瓶底部放少量细沙,细沙的作用是 。
23.(6分)稀盐酸是实验室常用的试剂,有关稀盐酸的性质实验如下。
①若需检验某盐酸样品中是否含有硫酸,应选用的试剂是 。
②向放有锌粒的试管中滴加稀盐酸,有气泡产生,该反应的基本类型是 。
③向滴有酚酞的氢氧化钠溶液中滴加稀盐酸至过量,观察到的现象是
,反应的化学方程式是 。
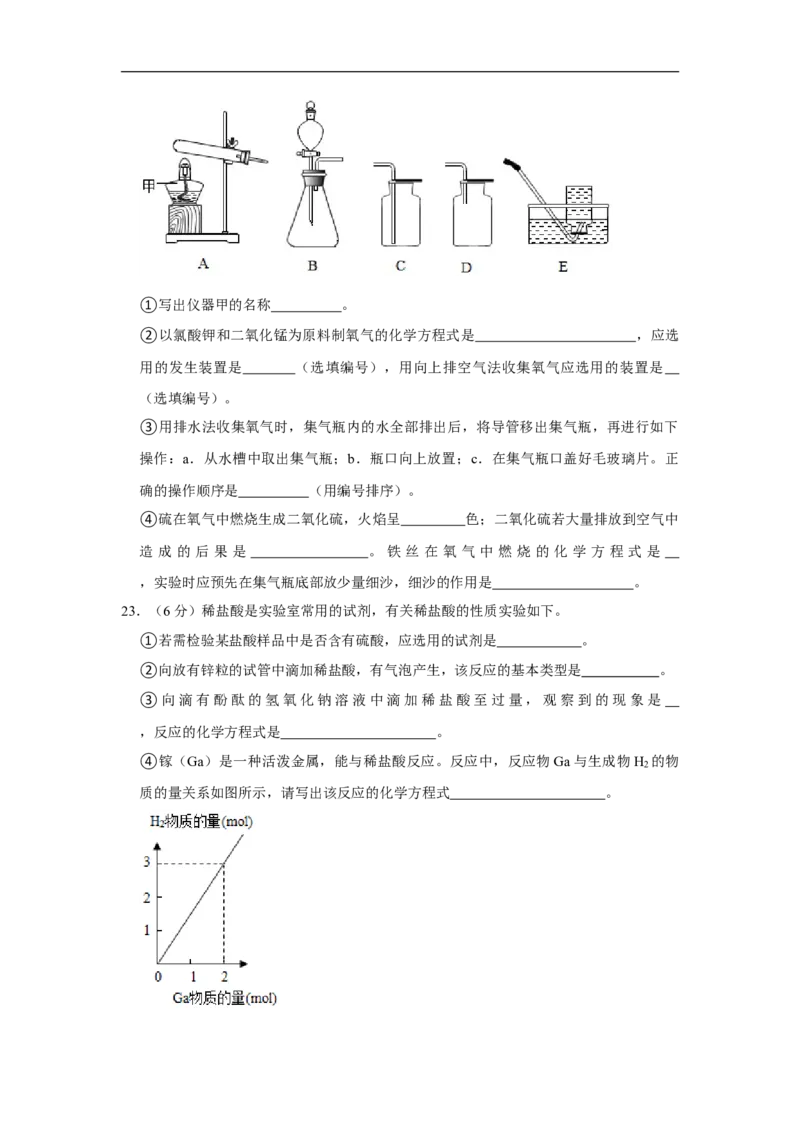
④镓(Ga)是一种活泼金属,能与稀盐酸反应。反应中,反应物Ga与生成物H 的物
2
质的量关系如图所示,请写出该反应的化学方程式 。八、简答题(共18分)请根据要求在答题纸的相应位置作答。
24.(9分)NaCl、CaCl 的部分溶解度数据见下表。
2
温度(℃) 20 40 60 80 100
溶解度 NaCl 36.0 36.6 37.1 38.0 39.2
(g/100g水)
CaCl 27.6 39.8 41.4 43.2 45.2
2
①由上表可知:20℃时,NaCl的溶解度是 g/100g水;60℃时,溶解度相
对较大的物质是 。
②某NaCl固体中含有CaCl 杂质,分别取样进行实验。
2
【测定杂质含量】
取10.0g样品溶于水,加入足量Na CO 溶液,与CaCl 反应生成NaCl和0.01mol CaCO
2 3 2 3
沉淀,计算样品中CaCl 的质量。(根据化学方程式列式计算) 。
2
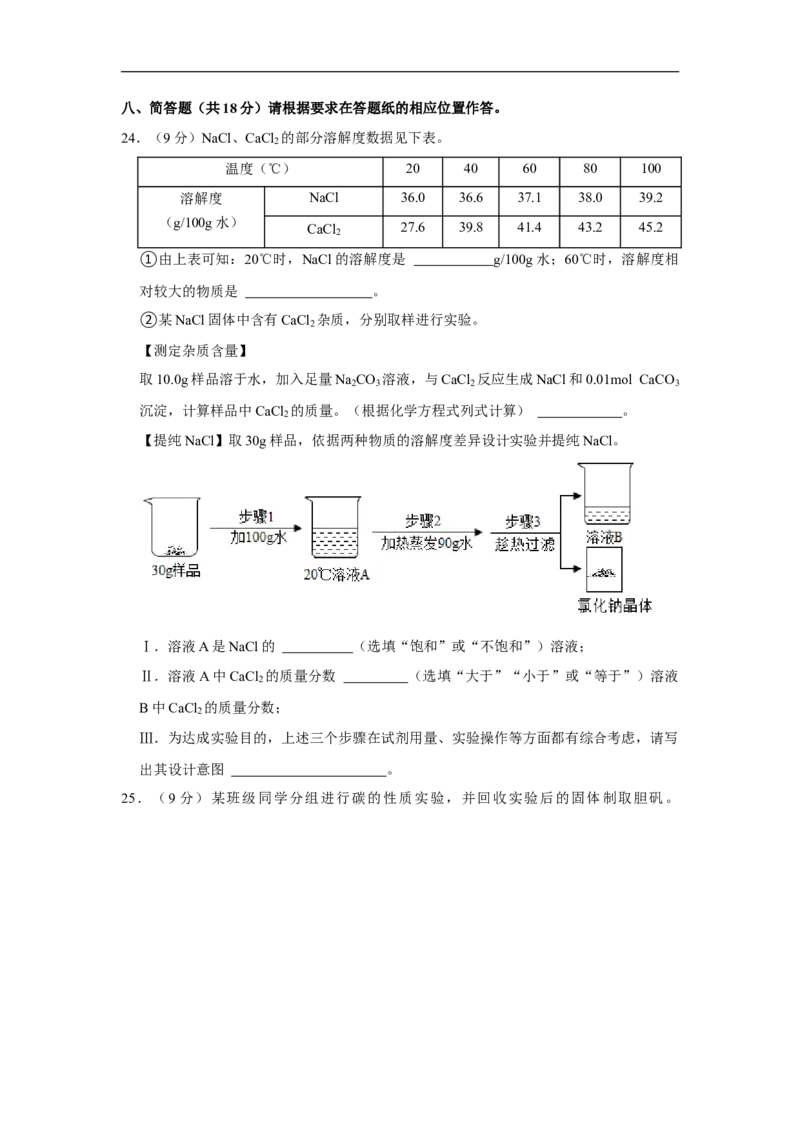
【提纯NaCl】取30g样品,依据两种物质的溶解度差异设计实验并提纯NaCl。
Ⅰ.溶液A是NaCl的 (选填“饱和”或“不饱和”)溶液;
Ⅱ.溶液A中CaCl 的质量分数 (选填“大于”“小于”或“等于”)溶液
2
B中CaCl 的质量分数;
2
Ⅲ.为达成实验目的,上述三个步骤在试剂用量、实验操作等方面都有综合考虑,请写
出其设计意图 。
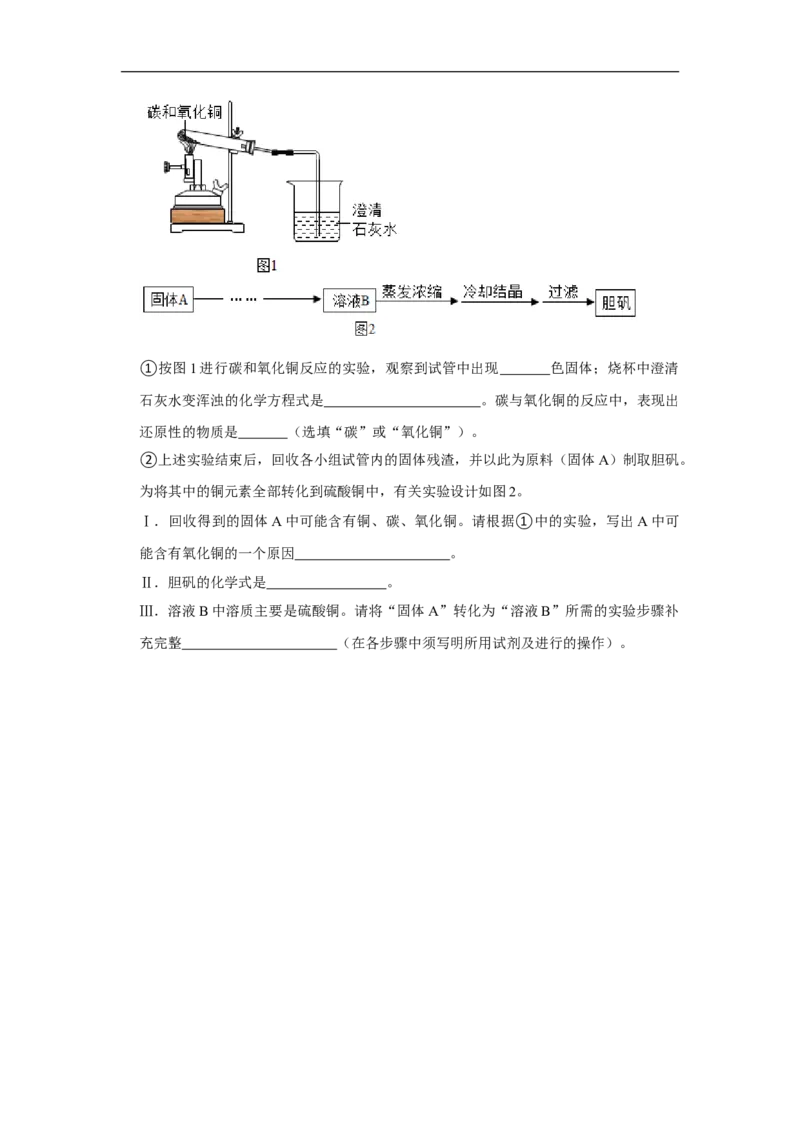
25.(9 分)某班级同学分组进行碳的性质实验,并回收实验后的固体制取胆矾。①按图1进行碳和氧化铜反应的实验,观察到试管中出现 色固体;烧杯中澄清
石灰水变浑浊的化学方程式是 。碳与氧化铜的反应中,表现出
还原性的物质是 (选填“碳”或“氧化铜”)。
②上述实验结束后,回收各小组试管内的固体残渣,并以此为原料(固体A)制取胆矾。
为将其中的铜元素全部转化到硫酸铜中,有关实验设计如图2。
Ⅰ.回收得到的固体A中可能含有铜、碳、氧化铜。请根据①中的实验,写出A中可
能含有氧化铜的一个原因 。
Ⅱ.胆矾的化学式是 。
Ⅲ.溶液B中溶质主要是硫酸铜。请将“固体A”转化为“溶液B”所需的实验步骤补
充完整 (在各步骤中须写明所用试剂及进行的操作)。