文档内容
威远中学校2025-2026学年高一上期第二次月考
化学试题
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 Ba-137
第Ⅰ卷(选择题 共45分)
一、选择题:本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
1. 下列我国古代的技术应用中,其工作原理不涉及氧化还原反应的是( )
A火药使用 B粮食酿酒 C转轮排字 D铁的冶炼
2.下列说法中,正确的是( )
A.MgCl 的摩尔质量是95 g
2
B.18 g HO在标准状况下的体积约为22.4 L
2
C.5.85 g NaCl溶于1 L水中,可配成0.1 mol·L-1的NaCl溶液
D.在一定温度和压强下,各种气态物质体积的大小主要由构成物质的分子数决定
3.常温下,在溶液中能发生如下反应:①2A2++B ===2A3++2B-; ②2B-+Z===B +2Z-;③16H+
2 2 2
+10Z-+2XO===2X2++5Z+8HO,由此判断下列说法错误的是( )
2 2
A.氧化性由强到弱的顺序是XO、Z、B 、A3+
2 2
B.还原性由强到弱的顺序是A2+、B-、Z-、X2+
C.反应Z+2A2+===2A3++2Z-可以进行
2
D.Z元素在反应②③中均被还原
4.下列化学用语错误的是( )
A.硫离子的结构示意图:
B.KAl(SO ) 的电离方程式:KAl(SO )===K++Al3++2SO
4 2 4 2
C.氧元素的同素异形体:O 与O
2 3
D.NaCl溶液中的水合离子:
5.下列转化中,需要加入氧化剂才能实现的是( )
A.Cl―→Cl- B.HCO―→CO C.MnO―→Mn2+ D.S2-―→S
2 2
6.下列关于钠及其化合物的说法中不正确的是( )
A.NaO 可在呼吸面具或潜水艇中作为氧气的来源
2 2
B.在自然界中,钠以化合物的形式存在
C.NaCO 溶液有碱性,可用于治疗胃酸过多
2 3
D.NaCO 可用于造纸和制皂工业
2 3
7.下列离子方程式书写正确的是( )
A.NaO 与HO反应制备O:NaO+HO===2Na++2OH-+O↑
2 2 2 2 2 2 2 2
B.少量的NaHCO 与Ca(OH) 溶液的反应:HCO+OH-+Ca2+===CaCO ↓+HO
3 2 3 2
C. 向NaHSO 溶液中加入Ba(OH) 溶液至SO刚好沉淀: 2H++SO+Ba2++2OH-===BaSO↓+2HO
4 2 4 2
D.氯气溶于水的反应:Cl+HO2H++Cl-+ClO-
2 2
8.下列实验操作、现象、结论均正确的是 ( )
选项 实验操作 现象 结论
用洁净铂丝蘸取某溶液,在酒精灯外焰上灼
A 火焰呈黄色 该溶液为NaOH溶液
烧
B 向某溶液中加入AgNO 溶液 溶液产生白色沉淀 原溶液中有Cl-存在
3
C 向包裹NaO 粉末的棉花滴入蒸馏水 棉花燃烧起来 NaO 与水反应为放热反应
2 2 2 2
D 向CuSO 溶液中加绿豆大的Na块 有红色沉淀产生 钠置换出了CuSO 中的Cu
4 4
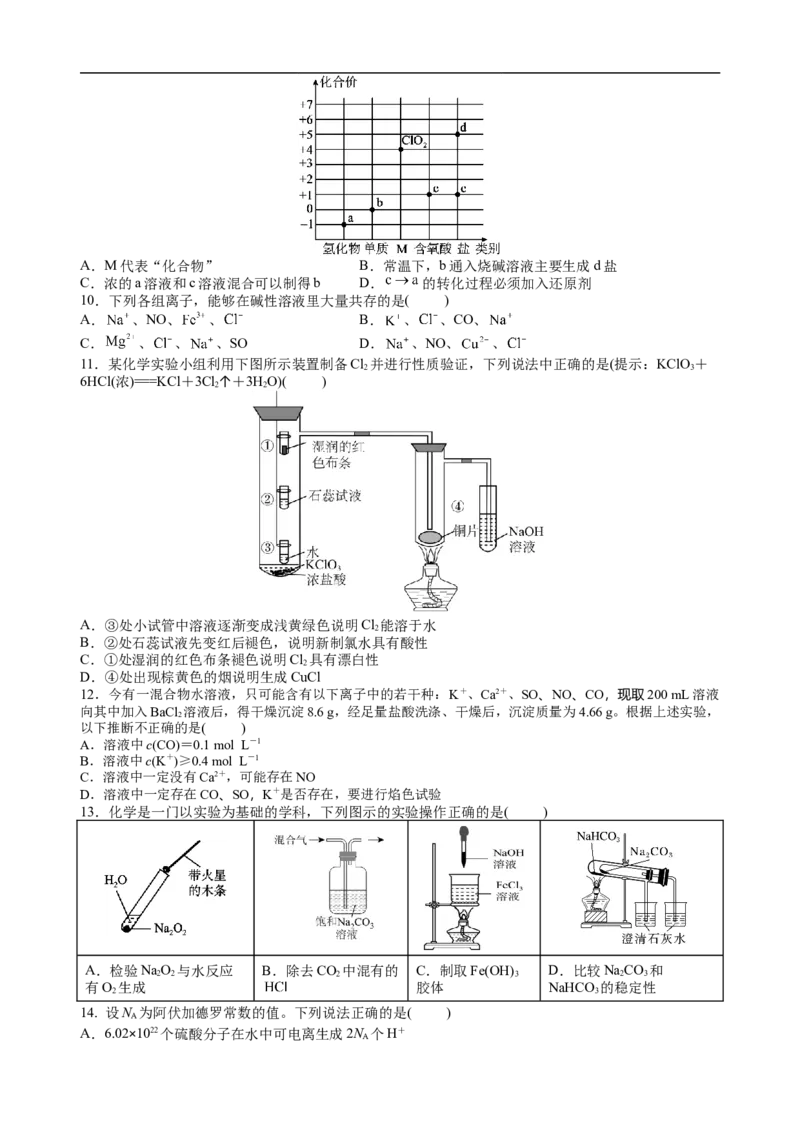
9.下图是氯元素的“价类”二维图。下列说法正确的是( )A.M代表“化合物” B.常温下,b通入烧碱溶液主要生成d盐
C.浓的a溶液和c溶液混合可以制得b D. 的转化过程必须加入还原剂
10.下列各组离子,能够在碱性溶液里大量共存的是( )
A. 、NO、 、 B. 、 、CO、
C. 、 、 、SO D. 、NO、 、
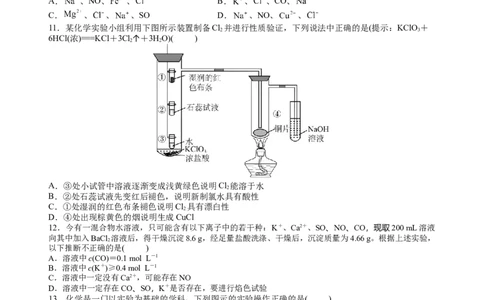
11.某化学实验小组利用下图所示装置制备Cl 并进行性质验证,下列说法中正确的是(提示:KClO+
2 3
6HCl(浓)===KCl+3Cl↑+3HO)( )
2 2
A.③处小试管中溶液逐渐变成浅黄绿色说明Cl 能溶于水
2
B.②处石蕊试液先变红后褪色,说明新制氯水具有酸性
C.①处湿润的红色布条褪色说明Cl 具有漂白性
2
D.④处出现棕黄色的烟说明生成CuCl
12.今有一混合物水溶液,只可能含有以下离子中的若干种:K+、Ca2+、SO、NO、CO,现取200 mL溶液
向其中加入BaCl 溶液后,得干燥沉淀8.6 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g。根据上述实验,
2
以下推断不正确的是( )
A.溶液中c(CO)=0.1 mol L-1
B.溶液中c(K+)≥0.4 mol L-1
C.溶液中一定没有Ca2+,可能存在NO
D.溶液中一定存在CO、SO,K+是否存在,要进行焰色试验
13.化学是一门以实验为基础的学科,下列图示的实验操作正确的是( )
A.检验NaO 与水反应 B.除去CO 中混有的 C.制取Fe(OH) D.比较NaCO 和
2 2 2 3 2 3
有O 生成 胶体 NaHCO 的稳定性
2 3
14. 设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.6.02×1022个硫酸分子在水中可电离生成2N 个H+
AB.在0 ℃、101 kPa时,22.4 L氢气中含有N 个氢原子
A
C.1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1N
A
D.标准状况下,22.4 L Cl 与足量的铁充分反应,转移的电子数为3N
2 A
15. 下列说法错误的是( )
A.酸性氧化物一定是非金属氧化物,碱性氧化物一定是金属氧化物
B.已知HPO (次磷酸)与足量的NaOH反应只生成一种盐NaH PO ,则HPO 为一元酸
3 2 2 2 3 2
C.在反应KHIO +9HI===2KI+4I+6HO中,还原剂与氧化剂的物质的量之比为7∶1
2 3 6 2 2
D.树状分类法各级之间存在包含关系,如氧化物属于化合物
第II卷(非选择题 共55分)
二、非选择题:本题共4个小题,共55分。
16.(14分)物质的分类、物质的量相关计算在化学中占有重要地位。
现有下列10种物质:①Cu;②淀粉溶液;③NaHCO ;④CO;⑤NH ;⑥Al (SO );⑦冰醋酸;
3 2 3 2 4 3
⑧Ca(ClO) 溶液;⑨熔融的KNO;⑩酒精。
2 3
根据所学知识回答下列问题:
(1)以上能发生丁达尔效应的是_____________。(填写序号,下同)能导电的是__________。
(2)属于电解质的是_____________。
(3)写出③溶于水的电离方程式___________________________________。
(4)等质量的CO和CO 在同温同压下体积比为___________(写最简整数比)。
2
(5)设N 为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积
A
约是 L(用含N 的式子表示)
A
(6)VmLAl (SO ) 溶液中含Al3+ag,则溶液中SO物质的量浓度为___________mol·L-1(用含a、V的式子
2 4 3
表示)。
17.(13分)研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)维生素C可以将Fe3+转化为Fe2+,说明维生素 具有___________(填“氧化性”或“还原性”)。
(2)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2HS+O===2X+2HO。
2 2 2
① 是___________(填化学式)。
②用单线桥标出上述方程式的电子转移方向和数目 。
(3)高铁酸盐是一种新型、高效、多功能绿色水处理剂。
①干法制备高铁酸钠(Na FeO)的主要反应为:2FeSO +6NaO===2NaFeO+2NaO+2NaSO +O↑,
2 4 4 2 2 2 4 2 2 4 2
该反应中NaO 是___________(填选项)
2 2
a.只作氧化剂 b.只作还原剂
c.既作氧化剂又作还原剂 d.既不作氧化剂又不作还原剂
②请写出NaO 与CO 反应的化学方程式________________________________________________。
2 2 2
③相同条件下,总质量为2.9g的 和H 的混合气体在足量的氧气中充分燃烧,然后立即通过足量的
2
NaO 固体,固体的质量增加___________g。
2 2
④湿法制备高铁酸钾(K FeO)的反应原理如下,请配平下列离子方程式:
2 4
Fe(OH) +ClO-+OH-===FeO+Cl-+HO。
3 2
18.(14分)I.物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角,CaO 与
2
NaO 都属于过氧化物。过氧化钙是一种难溶于水、可与水缓慢反应、能溶于酸的白色固体,广泛用于
2 2
果蔬保鲜、空气净化、污水处理等方面。以下是一种制备过氧化钙的实验方法:
已知:CaCl +HO+2NH +nHO===CaO·nHO↓+2NH Cl
2 2 2 3 2 2 2 4
回答下列问题:
(1)CaO 中氧元素化合价为________。
2
(2)操作Ⅰ、Ⅱ为________。
(3) CaO 可用于长途运输鱼苗,利用了CaO 的性质有________(填字母)。
2 2
A.能缓慢供氧 B.能潮解 C.能抑菌(4)检验“洗涤”是否合格的方法是:取最后一次洗涤液少许于试管中,先滴加稀硝酸酸化,然后滴入
________溶液,看是否产生白色沉淀。
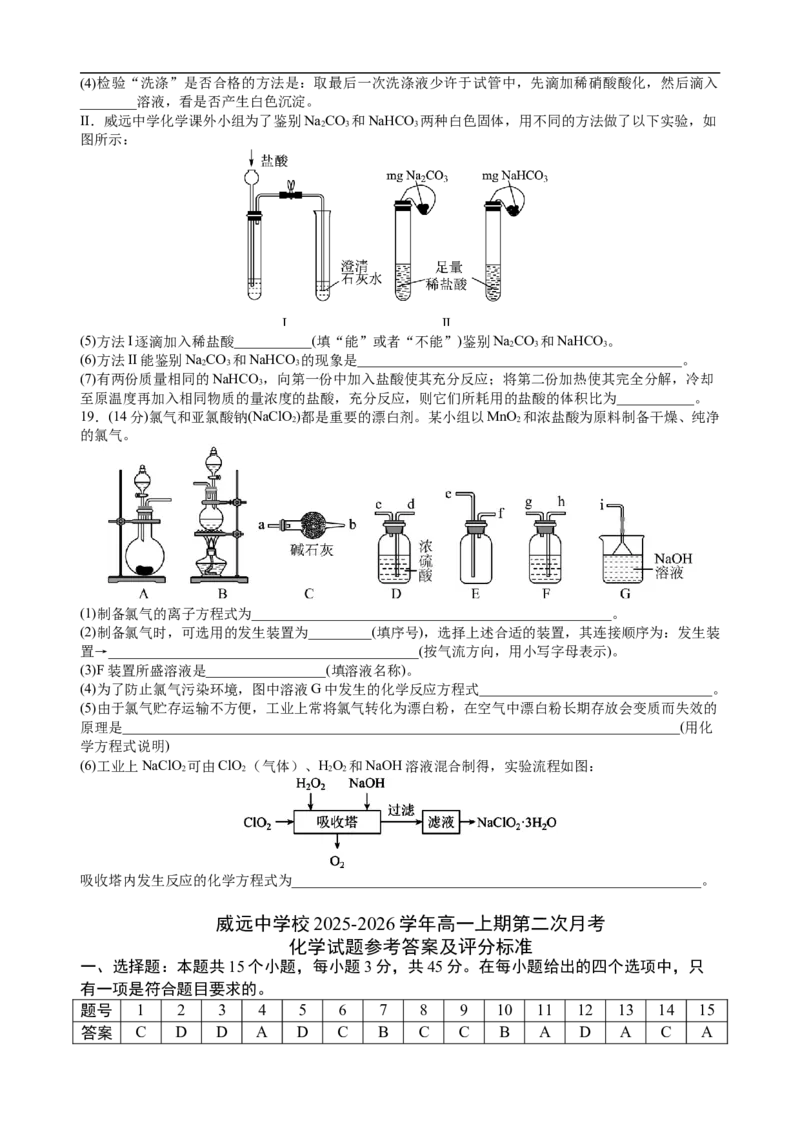
II.威远中学化学课外小组为了鉴别Na CO 和NaHCO 两种白色固体,用不同的方法做了以下实验,如
2 3 3
图所示:
(5)方法I逐滴加入稀盐酸___________(填“能”或者“不能”)鉴别Na CO 和NaHCO 。
2 3 3
(6)方法II能鉴别Na CO 和NaHCO 的现象是______________________________________________。
2 3 3
(7)有两份质量相同的NaHCO ,向第一份中加入盐酸使其充分反应;将第二份加热使其完全分解,冷却
3
至原温度再加入相同物质的量浓度的盐酸,充分反应,则它们所耗用的盐酸的体积比为___________。
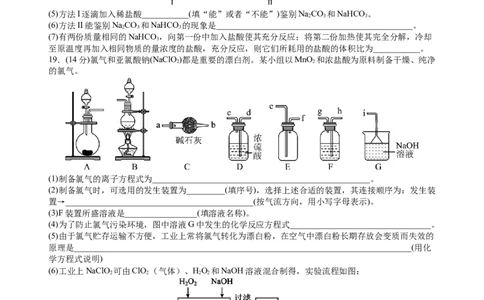
19.(14分)氯气和亚氯酸钠(NaClO)都是重要的漂白剂。某小组以MnO 和浓盐酸为原料制备干燥、纯净
2 2
的氯气。
(1)制备氯气的离子方程式为___________________________________________________。
(2)制备氯气时,可选用的发生装置为_________(填序号),选择上述合适的装置,其连接顺序为:发生装
置→____________________________________________(按气流方向,用小写字母表示)。
(3)F装置所盛溶液是_________________(填溶液名称)。
(4)为了防止氯气污染环境,图中溶液G中发生的化学反应方程式_________________________________。
(5)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的
原理是_______________________________________________________________________________(用化
学方程式说明)
(6)工业上NaClO 可由ClO (气体)、HO 和NaOH溶液混合制得,实验流程如图:
2 2 2 2
吸收塔内发生反应的化学方程式为__________________________________________________________。
威远中学校2025-2026学年高一上期第二次月考
化学试题参考答案及评分标准
一、选择题:本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C D D A D C B C C B A D A C A二、非选择题:本题共4个小题,共55分。
16.(14分)
(1) ② (2分) ①⑧⑨ (2分)
(2) ③⑥⑦⑨(2分)
(3)NaHCO ===Na++HCO (2分)
3
(4)11∶7 (2分)
(5) (2分)
(6)×103 或 ×103 (2分)
17.(13分)
(1)还原性 (1分)
4e-
(2)Ag S (2分) 4Ag+2H S+O ===2Ag S+2H O (2分)
2 2 2 2 2
(3)① c (2分) ②2Na O +2CO ===2Na CO +O (2分) ③2.9 (2分)
2 2 2 2 3 2
④Fe(OH) +ClO-+OH-===FeO+Cl-+HO(2分)
3 2
18.(14分)
(1)-1(2分)
(2)过滤(2分)
(3)AC(2分)
(4)AgNO (2分)
3
(5)能 (2分)
(6)盛NaHCO 的装置比盛Na CO 的装置反应剧烈且反应后的气球大 (2分)
3 2 3
(7)1∶1 (2分)
19.(14分)
(1)MnO +4H++2Cl-=====Cl +2H O+Mn2+ (2分)
2 2 2
(2)B (2分) h→g→d→c→e→f→i或h→g→d→c→e→f→a→b (2分)
(3)饱和食盐水(2分)
(4)Cl +2NaOH===NaCl+NaClO+H O (2分)
2 2
(5)Ca(ClO) +CO +H O===CaCO +2HClO 、2HClO=====2HCl+O ↑ (各1分,共2分)
2 2 2 3 2
(6)2ClO +H O +2NaOH===2NaClO +O ↑+2H O (2分)
2 2 2 2 2 2