文档内容
微信公众号:上海通优教案资料中心
学业水平参考样卷
综合测试 化学
2026.4
相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 Cu-64
一、氢能(8分)
人们不断探索各种制氢、储氢和用氢的方法,使氢气的生成和使用形成理想的循环体系。
1. 目前已经实现用可再生能源发电,再电解水生产 “绿氢”。
(1) 属于可再生能源的是________。
A. 煤 B. 石油 C. 天然气 D. 风能
(2) 写出电解水的化学方程式________________________。
(3) 电解时为了增加水的导电能力,要加入一种溶液。常温下,该溶液pH>7,它显________。
A. 酸性 B. 碱性 C. 中性
2. 用一种含锌元素的催化剂,可使水在阳光下直接分解生成氢气。元素周期表中锌元素的相关信息如图1
所示,据此可知________。
A. 一个锌原子的质量为65.38g B. 锌的相对原子质量为65.38g
C. 锌离子的核外电子数为30 D. 锌原子中的质子数为30
一定条件
3. 将氢气转化为金属氢化物是化学储氢的一种方式。用镁储存氢气的原理为Mg+H₂ MgH₂,该反
应属于________。
A. 分解反应 B. 置换反应 C. 化合反应 D. 复分解反应
4. 氢化镁释放氢气,主要有以下两种方法。
方法I:MgH₂+2H₂O=Mg(OH)₂+2H₂↑
△
方法II:MgH₂ Mg+H₂↑
(1) 消耗等量的 MgH₂,用方法 I 释放的氢气质量 (m) 与用方法 II 释放的氢气质量 (m ) 之间的关系是
I II
________。
A. m>m B. m10g
溶解性 难溶 微溶 可溶 易溶
A. 难溶物质 B. 微溶物质 C. 可溶物质 D. 易溶物质
(2) 配制200g溶质质量分数为2%的高锰酸钾溶液,需要高锰酸钾固体____g,水____mL。
用表2所示的四个实验进行探究
表2
实验 Ⅰ 实验 Ⅱ 实验 Ⅲ 实验 Ⅳ
加入20mL 加入 加入20mL 加入
2%的KMnO₄溶液 0.4g MnO₂固体 2%的KMnO₄溶液 0.4g KMnO₄固体
实验
操作
示意图
20mL 20mL 20mL 20mL
水 10%的H₂O₂溶液 10%的H₂O₂溶液 10%的H₂O₂溶液
反应较为剧烈,有大 剧烈放热,瞬间产生
实验 无色液体变为深紫红 有气泡生成,无色液
量气泡生成,无色液 大量气泡,无色液体
现象 色溶液 体变为黑色悬浊液
体变为黑色悬浊液 变为黑色悬浊液
6. 写出实验II中发生反应的化学方程式________________________________。
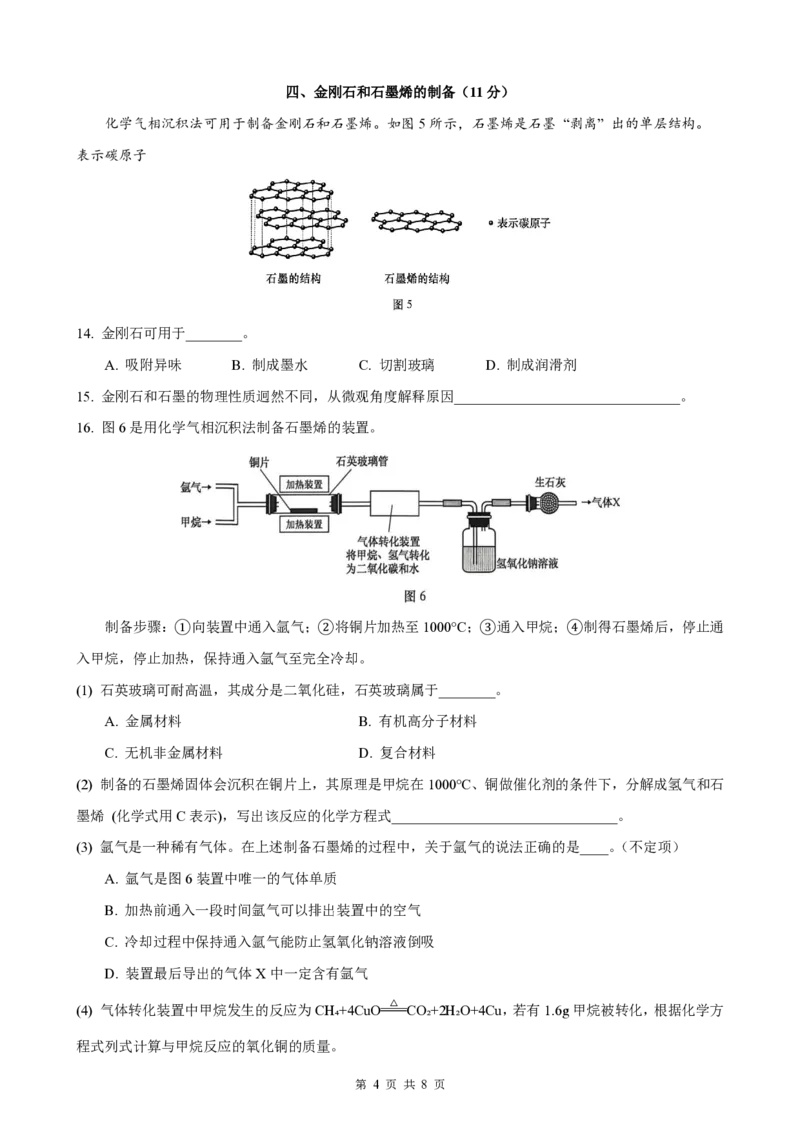
7. 将带火星的木条分别伸入实验III和实验IV的锥形瓶中,观察到木条复燃,说明有________生成。
8. 对实验III中的黑色悬浊液做如图3所示的探究。
(1) 为了观察黑色悬浊液中液体的颜色,除去其中难溶固体的操作X是________。
A. 蒸发 B. 过滤 C. 降温结晶 D. 蒸发结晶
第 2 页 共 8 页微信公众号:上海通优教案资料中心
(2) 根据上述探究,可以确定实验III中________。(不定项)
A. 黑色悬浊液是纯净物 B. 黑色固体是KMnO₄
C. H₂O₂完全消耗 D. KMnO₄完全消耗
9. 评估实验室中能否通过混合高锰酸钾固体和10%的过氧化氢溶液制备并用排水法收集氧气?理由是
______________________________________________________________________________________。
三、锅炉中的水垢(10分)
锅炉广泛应用于生活和工业中,图 4 所示的是一种热水锅炉的部分结构,其使用过程中会产生水垢,
若水垢过多会影响生产效率,甚至造成事故。
10. 煤在送入燃烧炉前需要粉碎处理。粉碎的目的是________。
A. 减少废气中CO₂的量 B. 使煤充分燃烧
C. 增加废气中CO的量 D. 使煤完全分解
11. 用铁做热水锅,主要利用了铁的________。
A. 导电性 B. 导热性 C. 金属光泽 D. 磁性
12. 锅炉水垢的主要成分是CaCO₃和Mg(OH)₂,它们是由水中溶解的少量Ca(HCO₃)₂、Mg(HCO₃)₂反应生成
的,化学方程式如下。
△
反应I:Ca(HCO₃)₂ CaCO₃↓+CO₂↑+H₂O
△
反应II:Mg(HCO₃)₂ Mg(OH)₂↓+2X
(1) CaCO₃中碳元素的化合价为________。
A. +1 B. +2 C. +3 D. +4
(2) 反应II中物质X的化学式为________。
(3) 相比进水管中,热水锅和出水管内更容易生成水垢,原因是________________________。
(4) 写出一条可减少锅炉中水垢生成的措施________________________________。
13. 锅炉需要定期清洗水垢,用稀盐酸可以除去水垢。
(1) Mg(OH)₂是一种碱,写出它与稀盐酸反应的化学方程式________________________________。
(2) 用足量稀盐酸除去铁质锅炉中的水垢时,需要把握好清洗时间的长短,原因是_____________________。
第 3 页 共 8 页微信公众号:上海通优教案资料中心
四、金刚石和石墨烯的制备(11分)
化学气相沉积法可用于制备金刚石和石墨烯。如图5所示,石墨烯是石墨 “剥离” 出的单层结构。
表示碳原子
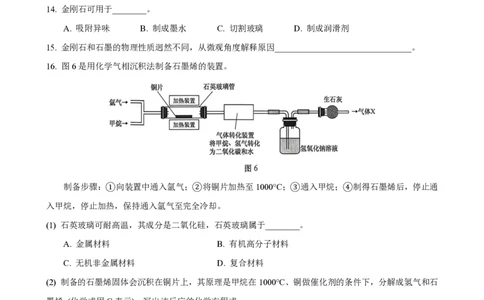
14. 金刚石可用于________。
A. 吸附异味 B. 制成墨水 C. 切割玻璃 D. 制成润滑剂
15. 金刚石和石墨的物理性质迥然不同,从微观角度解释原因________________________________。
16. 图6是用化学气相沉积法制备石墨烯的装置。
制备步骤:①向装置中通入氩气;②将铜片加热至1000°C;③通入甲烷;④制得石墨烯后,停止通
入甲烷,停止加热,保持通入氩气至完全冷却。
(1) 石英玻璃可耐高温,其成分是二氧化硅,石英玻璃属于________。
A. 金属材料 B. 有机高分子材料
C. 无机非金属材料 D. 复合材料
(2) 制备的石墨烯固体会沉积在铜片上,其原理是甲烷在1000°C、铜做催化剂的条件下,分解成氢气和石
墨烯 (化学式用C表示),写出该反应的化学方程式________________________________。
(3) 氩气是一种稀有气体。在上述制备石墨烯的过程中,关于氩气的说法正确的是____。(不定项)
A. 氩气是图6装置中唯一的气体单质
B. 加热前通入一段时间氩气可以排出装置中的空气
C. 冷却过程中保持通入氩气能防止氢氧化钠溶液倒吸
D. 装置最后导出的气体X中一定含有氩气
△
(4) 气体转化装置中甲烷发生的反应为CH₄+4CuO CO₂+2H₂O+4Cu,若有1.6g甲烷被转化,根据化学方
程式列式计算与甲烷反应的氧化铜的质量。
第 4 页 共 8 页微信公众号:上海通优教案资料中心
五、灭火器(11分)
二氧化碳灭火器和干粉灭火器是两种常见的灭火器,适合配备在学校、实验室等场所。
17. 二氧化碳灭火器里充装了液态的二氧化碳。打开阀门,灭火器内的二氧化碳液体转变为二氧化碳气体
喷射而出。下列相关说法正确的是________。(不定项)
A. 灭火器在不使用的状态下,其内部的二氧化碳分子静止不动
B. 二氧化碳液体气化属于物理变化
C. 二氧化碳液体气化的过程中,分子间距发生变化
D. 灭火器使用前后,其内部的二氧化碳分子个数不变
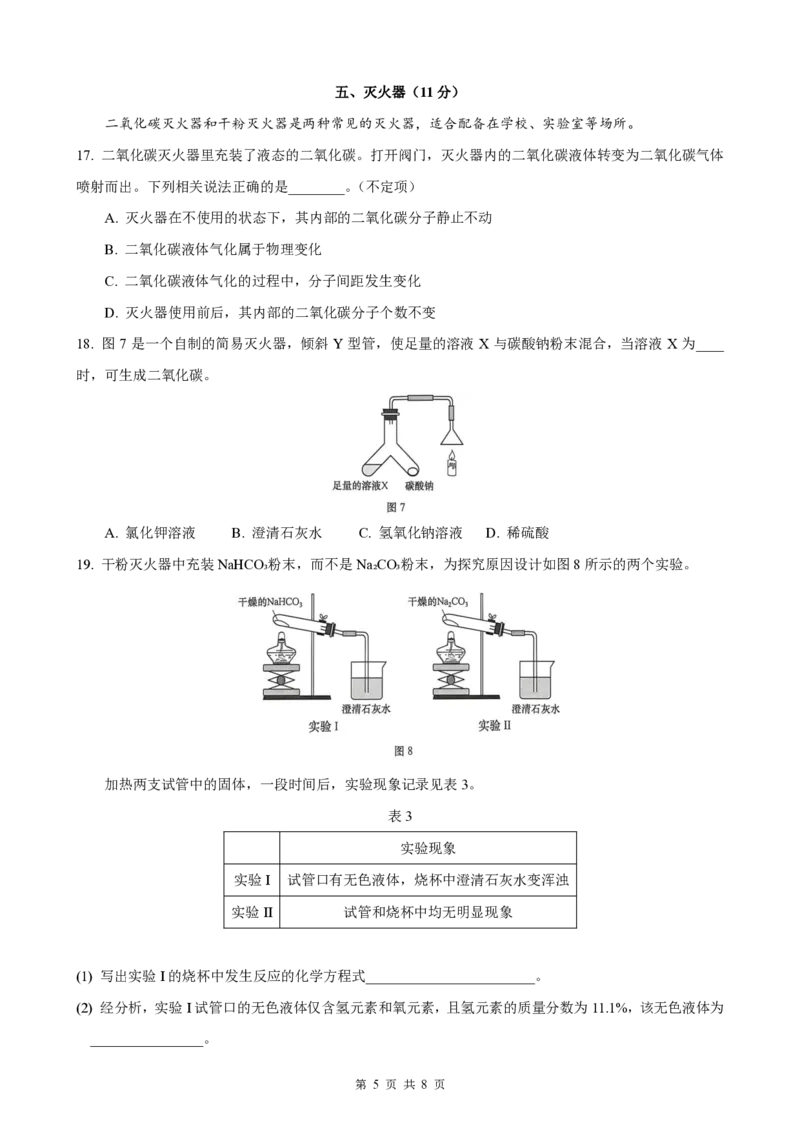
18. 图 7 是一个自制的简易灭火器,倾斜 Y 型管,使足量的溶液 X 与碳酸钠粉末混合,当溶液 X 为____
时,可生成二氧化碳。
A. 氯化钾溶液 B. 澄清石灰水 C. 氢氧化钠溶液 D. 稀硫酸
19. 干粉灭火器中充装NaHCO₃粉末,而不是Na₂CO₃粉末,为探究原因设计如图8所示的两个实验。
加热两支试管中的固体,一段时间后,实验现象记录见表3。
表3
实验现象
实验I 试管口有无色液体,烧杯中澄清石灰水变浑浊
实验II 试管和烧杯中均无明显现象
(1) 写出实验I的烧杯中发生反应的化学方程式________________________。
(2) 经分析,实验I试管口的无色液体仅含氢元素和氧元素,且氢元素的质量分数为11.1%,该无色液体为
________________。
第 5 页 共 8 页微信公众号:上海通优教案资料中心
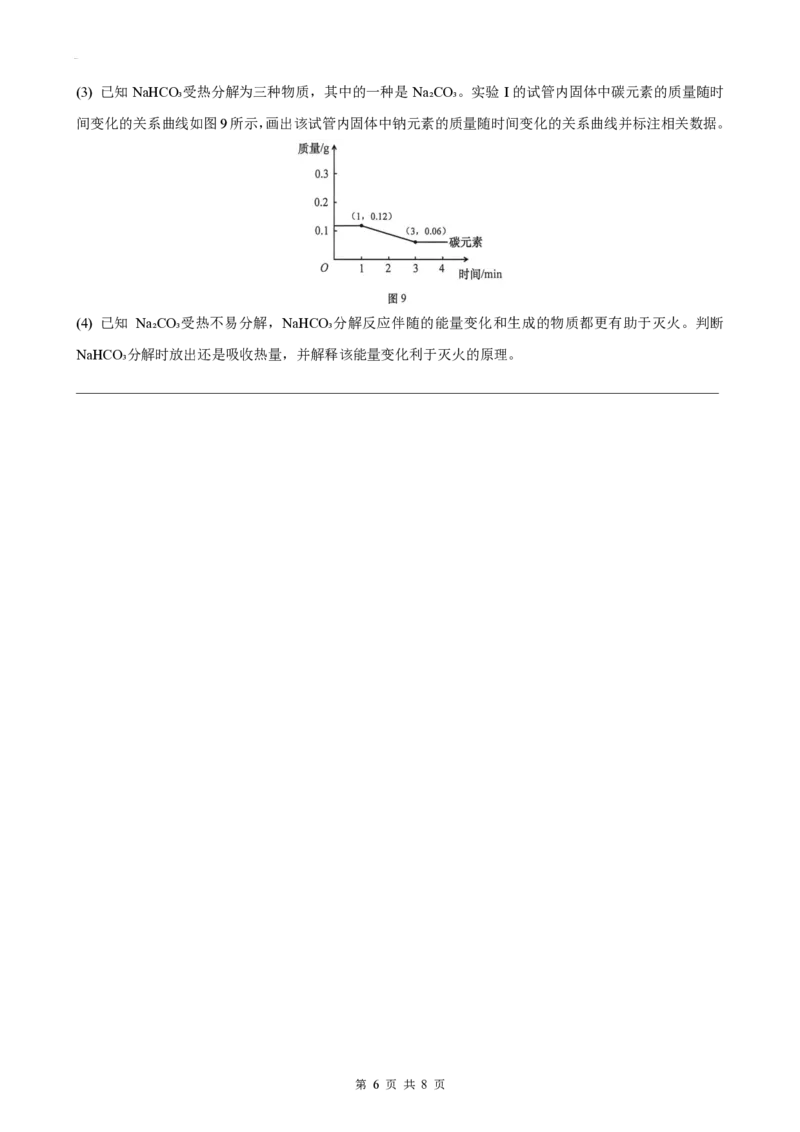
(3) 已知NaHCO₃受热分解为三种物质,其中的一种是 Na₂CO₃。实验I的试管内固体中碳元素的质量随时
间变化的关系曲线如图9所示,画出该试管内固体中钠元素的质量随时间变化的关系曲线并标注相关数据。
(4) 已知 Na₂CO₃受热不易分解,NaHCO₃分解反应伴随的能量变化和生成的物质都更有助于灭火。判断
NaHCO₃分解时放出还是吸收热量,并解释该能量变化利于灭火的原理。
___________________________________________________________________________________________
第 6 页 共 8 页微信公众号:上海通优教案资料中心
参考答案
一、氢能(8分)
1. (1) D
通电
(2) 2H₂O 2H₂↑+O₂↑
(3) B
2. D
3. C
4. (1) A
(2) Mg可以循环用于储氢,原料可重复利用
二、高锰酸钾和过氧化氢(10分)
5. (1) C
(2) 4;196
6. 2H₂O₂
MnO2
2H₂O+O₂↑
7. 氧气(O₂)
8. (1) B
(2) CD
9. 不能;反应剧烈放热、瞬间产生大量气体,易发生危险,不利于收集
三、锅炉中的水垢(10分)
10. B
11. B
12. (1) D
(2) CO₂
(3) 温度越高,碳酸氢盐越易分解生成水垢
(4) 使用软水(或先将水煮沸再使用)
13. (1) Mg(OH)₂+2HCl=MgCl₂+2H₂O
(2) 防止稀盐酸过量,与铁锅炉反应腐蚀锅炉
四、金刚石和石墨烯的制备(11分)
14. C
15. 碳原子的排列方式不同
16. (1) C
第 7 页 共 8 页微信公众号:上海通优教案资料中心
1000℃
(2) CH₄ C+2H₂
铜
(3) BCD
(4) 32g
五、灭火器(11分)
17. BC
18. D
19. (1) CO₂+Ca(OH)₂=CaCO₃↓+H₂O
(2) H₂O(水)
(3) 图略
(4) 吸收热量;吸热降低温度,使可燃物温度降至着火点以下,利于灭火
第 8 页 共 8 页