文档内容
九年级理化化学部分
相对原子质量:C-12 H-1 O-16 Ca-40
五、选择题(本大题共 17 题,共 20 分)
【21~34 每题只有 1 个正确选项,每题 1 分,共 14 分。】
1. “含碘食盐”中“碘”指的是
A. 原子 B. 分子 C. 元素 D. 单质
2. 空气中能供给动植物呼吸的气体是
A. 氮气 B. 氧气 C. 水蒸气 D. 二氧化碳
3. 氧化镁(MgO)中镁元素的化合价为
A. +1 B. +2 C. +3 D. +4
4. 硫元素以游离态存在的物质是
A. H SO B. Na SO C. S D. SO
2 4 2 3 2
5. 放入一定量水中,充分搅拌后能形成溶液的物质是
A. 泥沙 B. 淀粉 C. 豆油 D. 蔗糖
6. 下列物质在氧气里燃烧时,能生成有刺激性气味的气体的是
A. 铁丝 B. 硫 C. 镁条 D. 木炭
7. 下列为人体部分液体的pH范围,其中酸性最强的是
A. 唾液(6.6-7.1) B. 胃液(0.9-1.5) C. 胆汁(7.1-7.3) D. 血浆(7.3-7.4)
的
8. 物质用途主要由化学性质决定 是
A. 稀有气体作电光源 B. 氯化钠配制生理盐水
C. 干冰用于人工降雨 D. 生石灰用于食品加热
9. 有关化学用语的叙述,错误的是
A. H:表示 2 个氢原子 B. He:表示氦气
2
C. NH :表示铵根 D. BaCO :表示碳酸钡
4 3
10. 实验操作正确的是
A. 塞进橡皮塞 B. 处理废弃药品C. 蒸发食盐水 D. 量取液体
11. 手机使用的锂(Li)电池是新型高能电池,总反应可表示为Li+MnO =LiMnO ,相关说法正确的是
2 2
A. 该反应属于化合反应 B. 锂元素属于非金属元素
C. MnO 中含有氧分子 D. LiMnO 属于氧化物
2 2
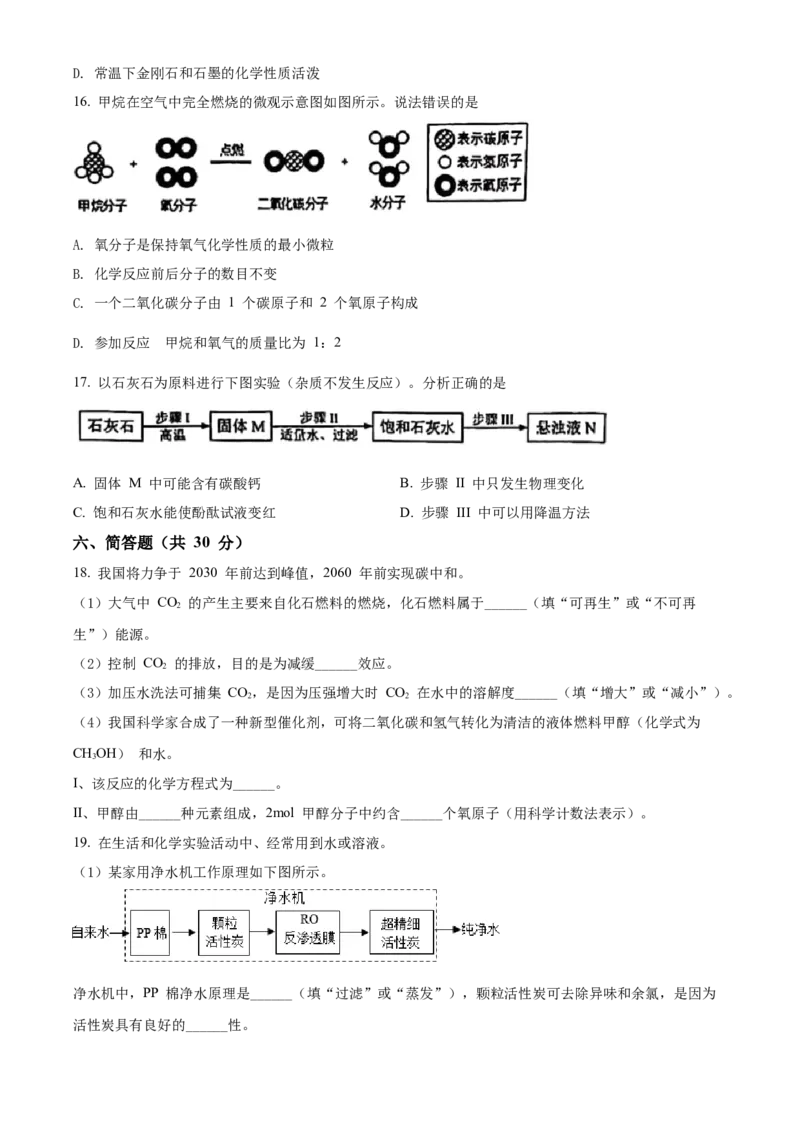
12. 关于测定空气中氧气含量的实验,下列说法正确的是
A. 实验前止水夹没有夹紧
B. 将红磷换成木炭进行实验
C. 待装置冷却至室温后,再打开止水夹
D. 点燃红磷缓慢伸入集气瓶中后,再塞紧瓶塞
13. 说法正确的是
A. 只含一种元素的物质一定是单质
B. 分子的质量一定大于原子的质量
C. 化学反应前后质量不变的物质一定是催化剂
D. 由不同种分子构成的物质一定是混合物
14. t℃时,将接近饱和的硝酸钾溶液变为该温度下的饱和溶液,分析正确的是
A. 溶质质量一定变大 B. 溶质质量分数一定变大
C. 溶剂质量一定变小 D. 溶液质量一定变大
【35~37 每题有 1~2 个正确选项,每题 2 分,共 6 分。有 2 个正确选项的,选对 1 个
得 1 分,多选或错选得 0 分。】
15. 金刚石和石墨是常见的碳单质。相关说法正确的是
A. 金刚石和石墨可以互称为同素异形体
.
B lg 金刚石和 1g 石墨含有原子数相同
C. 金刚石和石墨中原子的排列方式相同D. 常温下金刚石和石墨的化学性质活泼
16. 甲烷在空气中完全燃烧的微观示意图如图所示。说法错误的是
A. 氧分子是保持氧气化学性质的最小微粒
B. 化学反应前后分子的数目不变
C. 一个二氧化碳分子由 1 个碳原子和 2 个氧原子构成
的
D. 参加反应 甲烷和氧气的质量比为 1:2
17. 以石灰石为原料进行下图实验(杂质不发生反应)。分析正确的是
A. 固体 M 中可能含有碳酸钙 B. 步骤 II 中只发生物理变化
C. 饱和石灰水能使酚酞试液变红 D. 步骤 III 中可以用降温方法
六、简答题(共 30 分)
18. 我国将力争于 2030 年前达到峰值,2060 年前实现碳中和。
(1)大气中 CO 的产生主要来自化石燃料的燃烧,化石燃料属于______(填“可再生”或“不可再
2
生”)能源。
(2)控制 CO 的排放,目的是为减缓______效应。
2
(3)加压水洗法可捕集 CO,是因为压强增大时 CO 在水中的溶解度______(填“增大”或“减小”)。
2 2
(4)我国科学家合成了一种新型催化剂,可将二氧化碳和氢气转化为清洁的液体燃料甲醇(化学式为
CHOH) 和水。
3
I、该反应的化学方程式为______。
II、甲醇由______种元素组成,2mol 甲醇分子中约含______个氧原子(用科学计数法表示)。
19. 在生活和化学实验活动中、经常用到水或溶液。
(1)某家用净水机工作原理如下图所示。
净水机中,PP 棉净水原理是______(填“过滤”或“蒸发”),颗粒活性炭可去除异味和余氯,是因为
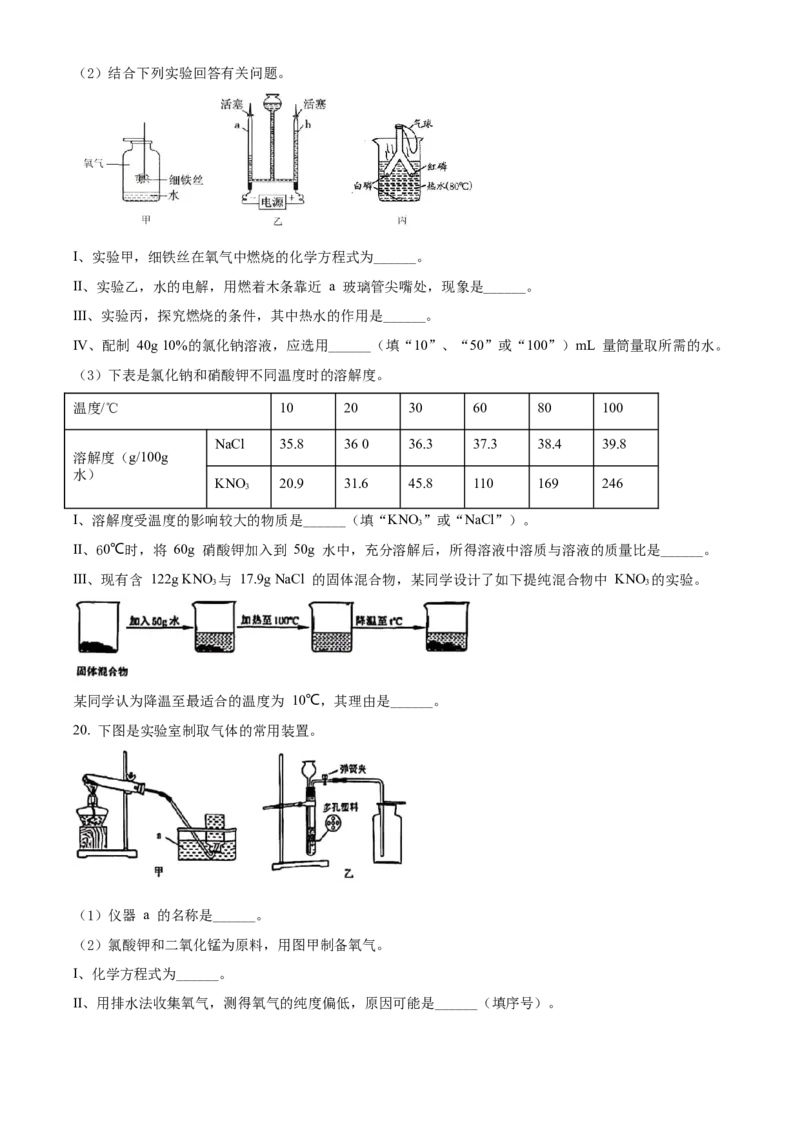
活性炭具有良好的______性。(2)结合下列实验回答有关问题。
I、实验甲,细铁丝在氧气中燃烧的化学方程式为______。
II、实验乙,水的电解,用燃着木条靠近 a 玻璃管尖嘴处,现象是______。
III、实验丙,探究燃烧的条件,其中热水的作用是______。
IV、配制 40g 10%的氯化钠溶液,应选用______(填“10”、“50”或“100”)mL 量筒量取所需的水。
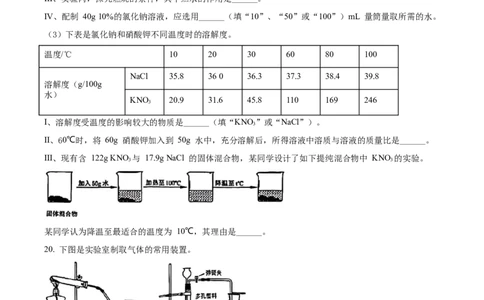
(3)下表是氯化钠和硝酸钾不同温度时的溶解度。
温度/℃ 10 20 30 60 80 100
.
NaCl 35.8 360 36.3 37.3 38.4 39.8
溶解度(g/100g
水)
KNO 20.9 31.6 45.8 110 169 246
3
I、溶解度受温度的影响较大的物质是______(填“KNO”或“NaCl”)。
3
II、60℃时,将 60g 硝酸钾加入到 50g 水中,充分溶解后,所得溶液中溶质与溶液的质量比是______。
III、现有含 122g KNO 与 17.9g NaCl 的固体混合物,某同学设计了如下提纯混合物中 KNO 的实验。
3 3
某同学认为降温至最适合的温度为 10℃,其理由是______。
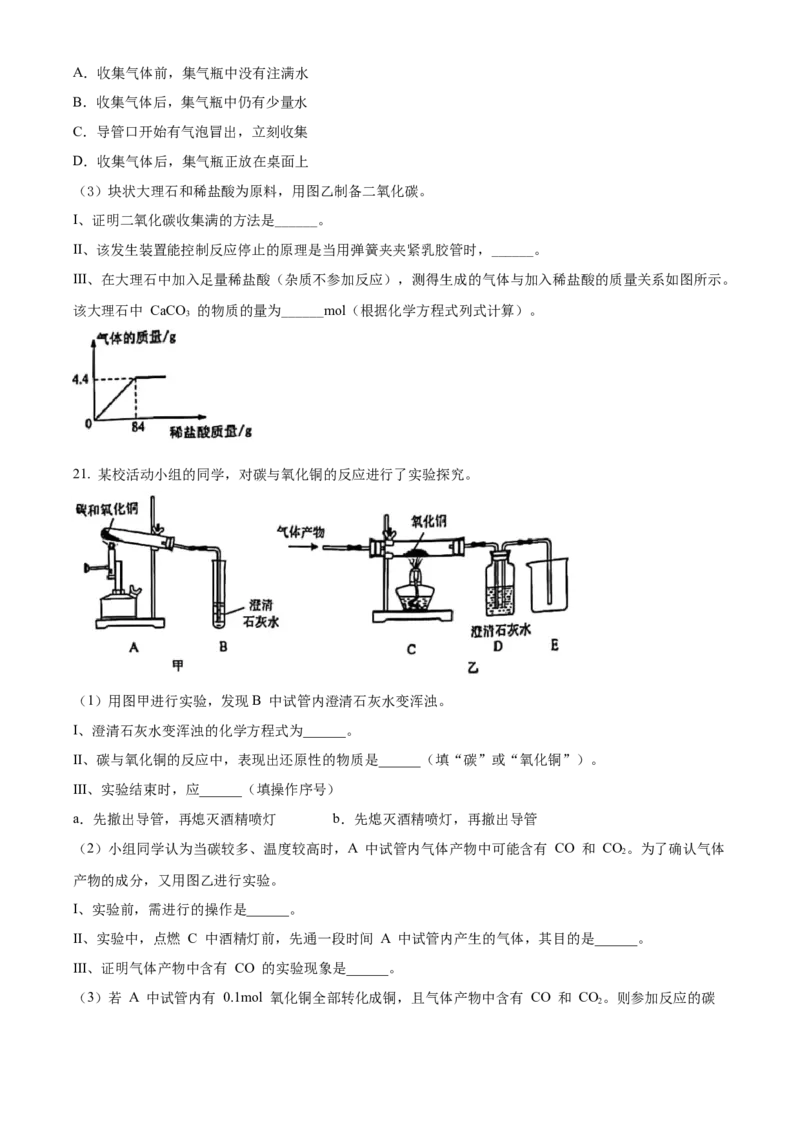
20. 下图是实验室制取气体的常用装置。
(1)仪器 a 的名称是______。
(2)氯酸钾和二氧化锰为原料,用图甲制备氧气。
I、化学方程式为______。
II、用排水法收集氧气,测得氧气的纯度偏低,原因可能是______(填序号)。A.收集气体前,集气瓶中没有注满水
B.收集气体后,集气瓶中仍有少量水
C.导管口开始有气泡冒出,立刻收集
D.收集气体后,集气瓶正放在桌面上
(3)块状大理石和稀盐酸为原料,用图乙制备二氧化碳。
I、证明二氧化碳收集满的方法是______。
II、该发生装置能控制反应停止的原理是当用弹簧夹夹紧乳胶管时,______。
III、在大理石中加入足量稀盐酸(杂质不参加反应),测得生成的气体与加入稀盐酸的质量关系如图所示。
该大理石中 CaCO 的物质的量为______mol(根据化学方程式列式计算)。
3
21. 某校活动小组的同学,对碳与氧化铜的反应进行了实验探究。
(1)用图甲进行实验,发现B 中试管内澄清石灰水变浑浊。
I、澄清石灰水变浑浊的化学方程式为______。
II、碳与氧化铜的反应中,表现出还原性的物质是______(填“碳”或“氧化铜”)。
。
III、实验结束时,应______(填操作序号)
a.先撤出导管,再熄灭酒精喷灯 b.先熄灭酒精喷灯,再撤出导管
(2)小组同学认为当碳较多、温度较高时,A 中试管内气体产物中可能含有 CO 和 CO。为了确认气体
2
产物的成分,又用图乙进行实验。
I、实验前,需进行的操作是______。
II、实验中,点燃 C 中酒精灯前,先通一段时间 A 中试管内产生的气体,其目的是______。
III、证明气体产物中含有 CO 的实验现象是______。
(3)若 A 中试管内有 0.1mol 氧化铜全部转化成铜,且气体产物中含有 CO 和 CO。则参加反应的碳
2的物质的量(n)的取值范围是。