文档内容
化学部分
相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 Fe-56 Cu-64 Zn-65 Ag-108
一、选择题(共20分)第21-34题,每题均只有一个正确选项
1. 空气中含量最多的气体是
A. HO B. O C. N D. He
2 2 2
2. 做饭时,食盐不小心溅在火焰上,火焰呈
A. 紫色 B. 黄色 C. 红色 D. 蓝色
3. 室温时人体中一些体液的pH如下,其中酸性最强的是
A. 尿液:5.00-7.00 B. 唾液:6.50-7.50 C. 胃液:0.80-1.50 D. 血液:7.35-7.45
4. 与C 互为同素异形体的是
60
A. 金刚石 B. 木炭 C. 活性炭 D. 一氧化碳
5. 下列可为植物生长提供营养元素且属于磷肥的物质是
A. Ca(HPO ) B. KCO C. KNO D. NH HCO
2 4 2 2 3 3 4 3
6. 物质的用途利用其化学性质的是
A. 石墨—制作电极 B. 干冰—制冷剂
C. 稀有气体—制作电光源 D. 盐酸—除铁锈
的
7. 物质在氧气中燃烧现象描述错误 是
A. 木炭:发出白光 B. 硫磺:生成无色无味气体
C. 白磷:生成白色固体 D. 铁丝:生成黑色固体
8. 下列物质属于纯净物的是
A. 盐酸 B. 矿泉水 C. 胆矾 D. 石灰石
9. 在水中不能形成溶液的物质是
A. 氯化氢 B. 氯化钠 C. 氯化银 D. 氯化钙
10. 关于过氧化氢(H O)的说法正确的是
2 2
A. 过氧化氢是由氢分子和氧分子构成的
B. 保持过氧化氢化学性质的微粒是氢原子和氧原子
C. 一个过氧化氢分子由4个原子构成
D. 过氧化氢是由2个氢元素和2个氧元素构成的
11. 属于酸性氧化物的是
.
A HSO B. HO C. CO D. CO
2 4 2 2
12. 下列化学方程式书写正确的是A. B.
C. D.
13. 关于二氧化硫和三氧化硫的说法错误的是
A. 组成元素相同 B. 元素存在状态相同
C. 物质类别相同 D. 分子结构相同
14. 下列探究氢氧化钙固体是否变质的方法合理的是
A. 加水溶解 B. 滴加过量稀盐酸
C. 高温煅烧 D. 滴加无色酚酞试液
第15-17题,每题均有1、2个正确选项,每题2分,选对1个得1分,多选或错选得0分。
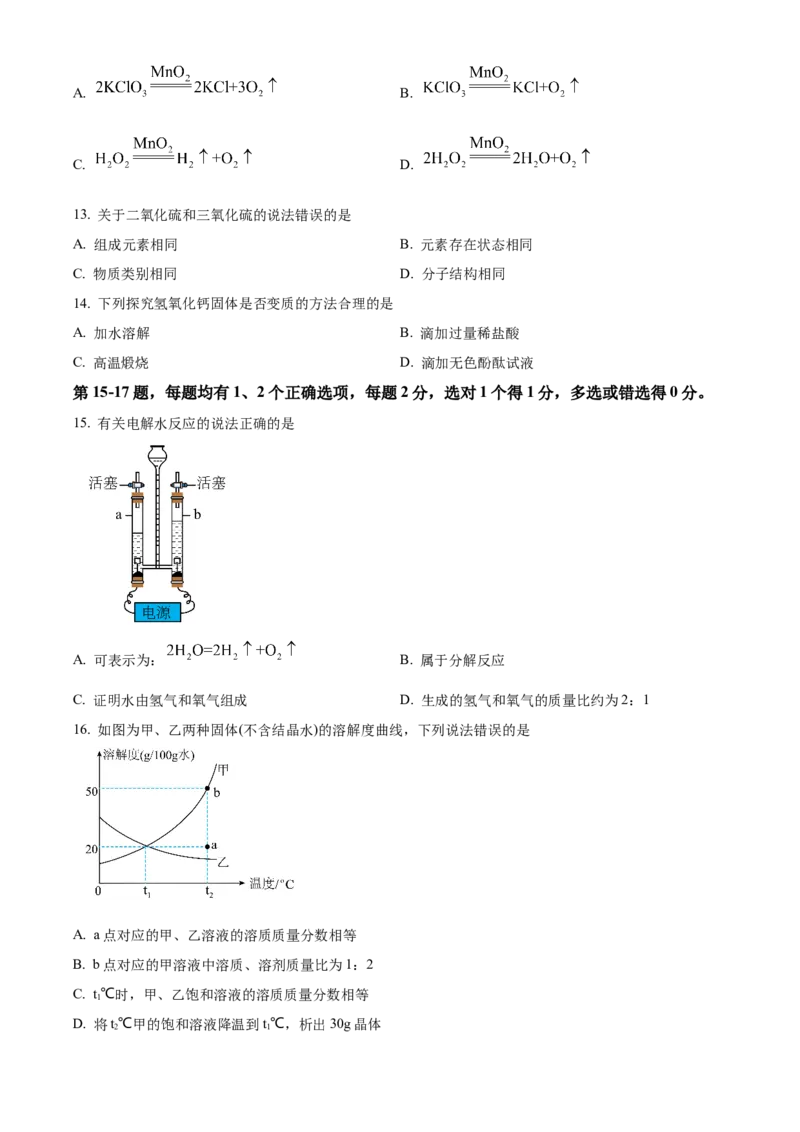
15. 有关电解水反应的说法正确的是
A. 可表示为: B. 属于分解反应
C. 证明水由氢气和氧气组成 D. 生成的氢气和氧气的质量比约为2:1
16. 如图为甲、乙两种固体(不含结晶水)的溶解度曲线,下列说法错误的是
A. a点对应的甲、乙溶液的溶质质量分数相等
B. b点对应的甲溶液中溶质、溶剂质量比为1:2
C. t℃时,甲、乙饱和溶液的溶质质量分数相等
1
D. 将t℃甲的饱和溶液降温到t℃,析出30g晶体
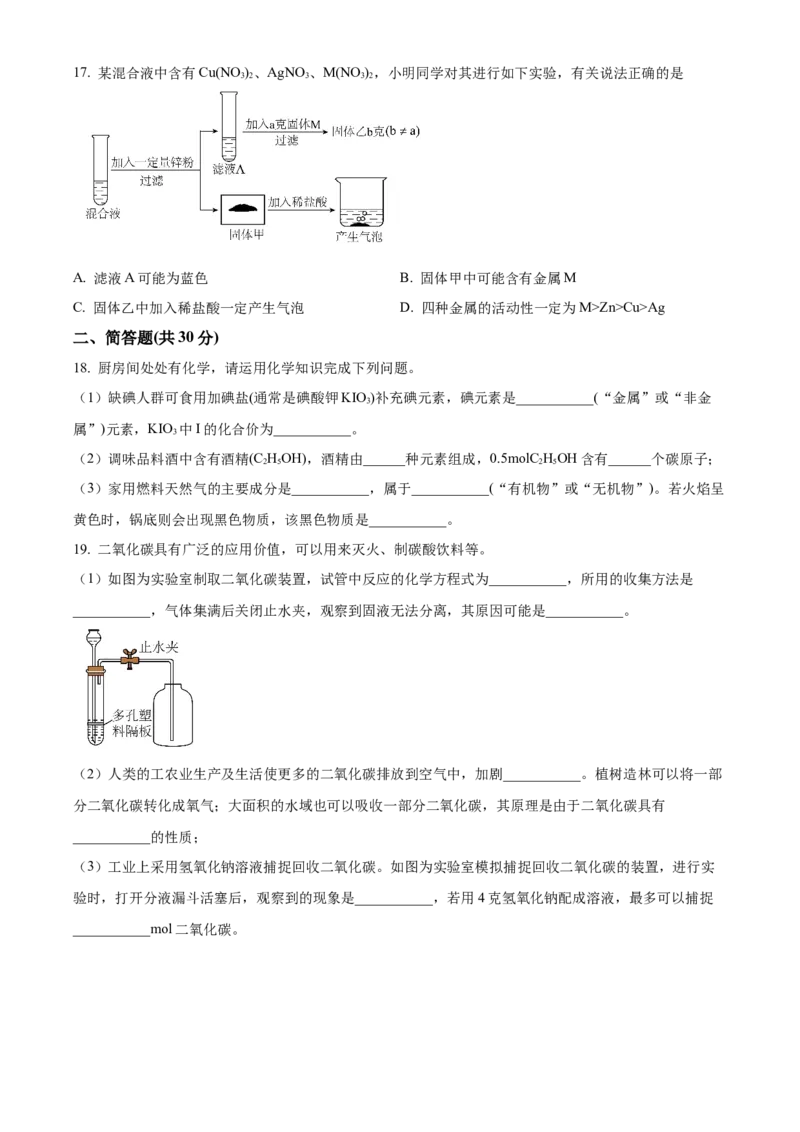
2 117. 某混合液中含有Cu(NO )、AgNO、M(NO),小明同学对其进行如下实验,有关说法正确的是
3 2 3 3 2
A. 滤液A可能为蓝色 B. 固体甲中可能含有金属M
C. 固体乙中加入稀盐酸一定产生气泡 D. 四种金属的活动性一定为M>Zn>Cu>Ag
二、简答题(共30分)
18. 厨房间处处有化学,请运用化学知识完成下列问题。
(1)缺碘人群可食用加碘盐(通常是碘酸钾KIO )补充碘元素,碘元素是___________(“金属”或“非金
3
属”)元素,KIO 中I的化合价为___________。
3
(2)调味品料酒中含有酒精(C HOH),酒精由______种元素组成,0.5molC HOH含有______个碳原子;
2 5 2 5
(3)家用燃料天然气的主要成分是___________,属于___________(“有机物”或“无机物”)。若火焰呈
黄色时,锅底则会出现黑色物质,该黑色物质是___________。
19. 二氧化碳具有广泛的应用价值,可以用来灭火、制碳酸饮料等。
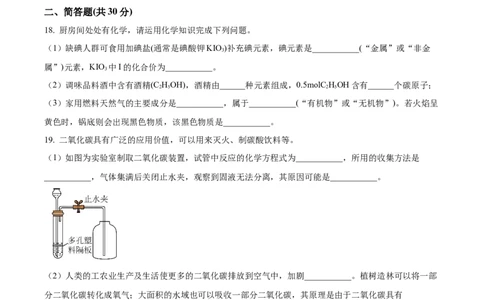
(1)如图为实验室制取二氧化碳装置,试管中反应的化学方程式为___________,所用的收集方法是
___________,气体集满后关闭止水夹,观察到固液无法分离,其原因可能是___________。
(2)人类的工农业生产及生活使更多的二氧化碳排放到空气中,加剧___________。植树造林可以将一部
分二氧化碳转化成氧气;大面积的水域也可以吸收一部分二氧化碳,其原理是由于二氧化碳具有
___________的性质;
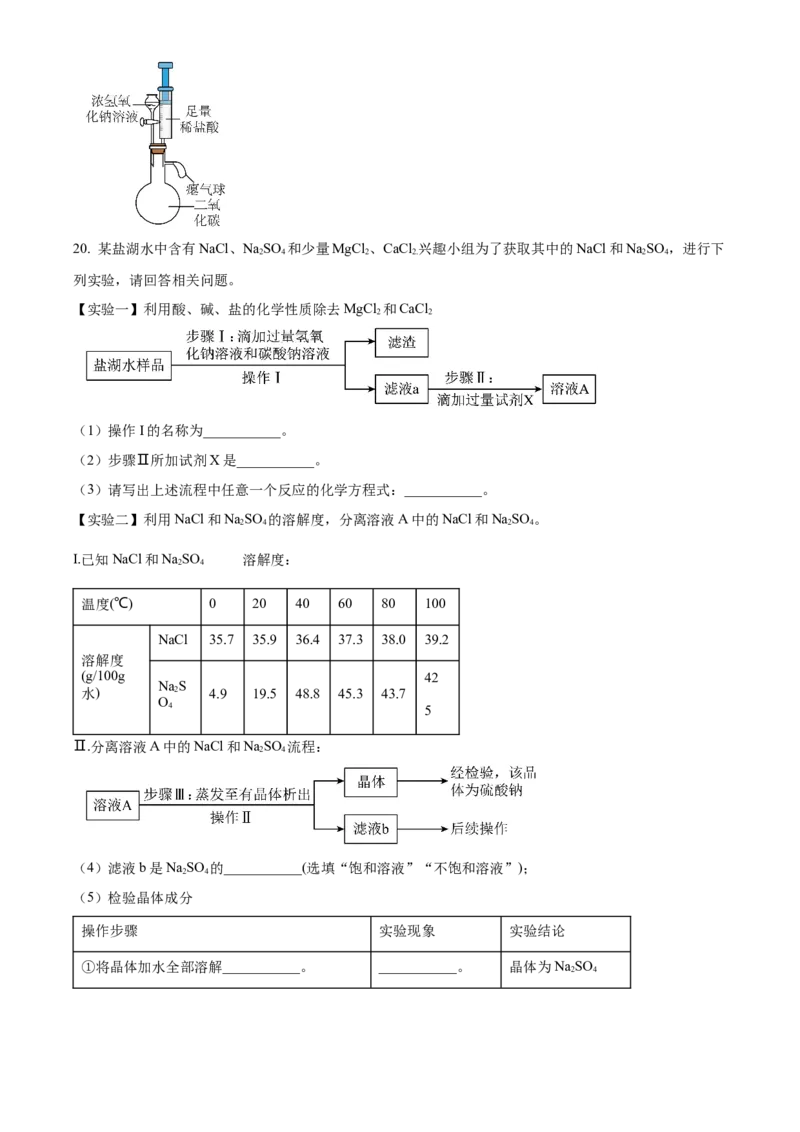
(3)工业上采用氢氧化钠溶液捕捉回收二氧化碳。如图为实验室模拟捕捉回收二氧化碳的装置,进行实
验时,打开分液漏斗活塞后,观察到的现象是___________,若用4克氢氧化钠配成溶液,最多可以捕捉
___________mol二氧化碳。20. 某盐湖水中含有NaCl、NaSO 和少量MgCl 、CaCl 兴趣小组为了获取其中的NaCl和NaSO ,进行下
2 4 2 2. 2 4
列实验,请回答相关问题。
【实验一】利用酸、碱、盐的化学性质除去MgCl 和CaCl
2 2
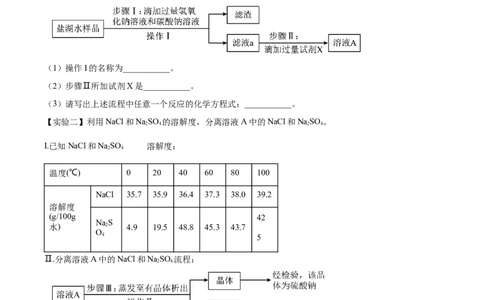
(1)操作I的名称为___________。
(2)步骤Ⅱ所加试剂X是___________。
(3)请写出上述流程中任意一个反应的化学方程式:___________。
【实验二】利用NaCl和NaSO 的溶解度,分离溶液A中的NaCl和NaSO 。
2 4 2 4
的
I.已知NaCl和NaSO 溶解度:
2 4
温度(℃) 0 20 40 60 80 100
NaCl 35.7 35.9 36.4 37.3 38.0 39.2
溶解度
(g/100g 42 .
NaS
水) 2 4.9 19.5 48.8 45.3 43.7
O
4 5
Ⅱ.分离溶液A中的NaCl和NaSO 流程:
2 4
(4)滤液b是NaSO 的___________(选填“饱和溶液”“不饱和溶液”);
2 4
(5)检验晶体成分
操作步骤 实验现象 实验结论
①将晶体加水全部溶解___________。 ___________。 晶体为NaSO
2 4(6)为了尽可能分离得到较纯且较多的NaCl和NaSO ,你的“后续操作”是___________。
2 4
21. 硫酸铜在农业、水处理、工艺美术等领域都有重要的用途。下述方案均可制得硫酸铜。
【方案一】用铜和浓硫酸共热制取硫酸铜
原理:
【方案二】用铜通过下列流程制取硫酸铜:Cu CuO CuSO
4
完成下列问题:
(1)制得的硫酸铜为________色;
(2)方案一中的生成物X是________。
(3)方案二中生成CuSO 反应的化学方程式为________,观察到的现象是_________。
4
(4)方案二中把铜全部转化成硫酸铜的操作是________。
(5)现要制取一定量硫酸铜,请你选择较优方案并说明理由________ 。