文档内容
高一化学
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cu 64
一、选择题:共 16 题,每题 3 分,共 48 分。每题只有一个选项符合题意。
1.科技兴国,材料的研究与应用在众多领域做出巨大的贡献。下列有关说法不正确的是
A.计算机芯片的主要材料是晶体硅
B.碳纳米管与石墨烯互为同位素
C.碳化硅陶瓷是一种新型无机非金属材料
D.镍钛合金属于金属材料
2.氟利昂(CCl F)是一种制冷剂,是 CH 的一种衍生物。下列说法正确的是
3 4
A.Cl-的结构示意图: B.甲烷分子空间构型:
C.碳元素在周期表中的位置是:第二周期第ⅥA 族 D.中子数为 10 的氟原子:
3.下列物质的性质和用途或保存方法相对应的是
A.氨易液化,汽化时要吸收大量的热,可用作制冷剂
B.浓硫酸具有脱水性,可做干燥剂
C.SiO 属于酸性氧化物,可用于制光导纤维
2
D.无水氯化钙和生石灰都具有吸水性,可用于干燥氨气
4.下列实验装置图能达到实验目的的是
A B C D
制取收集氨气 收集 NO 气体 除去 CO 中的 SO 测量氯水的 pH 值
2 2 2
阅读下列资料,完成 5~7 题:
海洋是一个十分巨大的资源宝库,Na、Cl、Mg、Br、Ca、S 等元素储量很高。海水资源
的利用主要包括海水淡化、海水晒盐,从海水中制取镁、钾、溴等化工产品。从海水中提取
镁的步骤是将石灰乳加入海水沉淀池中,得到氢氧化镁沉淀,再将氢氧化镁与盐酸反应,得到
的溶液然后获得六水合氯化镁晶体(MgCl ·6H O),进一步操作得到无水氯化镁。
2 2
5.下列关于海水中提取物质的说法正确的是
A.电解 MgCl 溶液可以得到金属镁
2
B.海水中获取淡水和氯化钠都用到蒸馏操作
C.在空气中加热蒸干氯化镁溶液可得到 MgCl ·6H O
2 2
D.向粗盐水中先后加入 BaCl 和 NaCO 溶液以除去其中的 SO 2-和 Ca2+
2 2 3 4
16.“吹出法”是工业上常用的一种海水提溴技术,该技术主要流程如下:
下列有关说法正确的是
A.流程图中“海水”一般采用的是提取粗盐后的母液
B.通入热空气主要是利用氧气将 Br-完全氧化
C.吹出后剩余溶液中可以大量共存的离子有 SO 2-、Cl-、Br-
3
D.流程图中“分离”所用的仪器包括烧杯、漏斗、玻璃棒
7.下列有关反应方程式书写符合要求的是
电解
A.表示“氧化 1”所用氯气来源的离子方程式:HO+2Cl- 2OH-+Cl↑+H↑
2 2 2
B.海水中得到 Mg(OH) 沉淀的化学反应方程式:2NaOH+MgCl =Mg(OH) ↓+2NaCl
2 2 2
C.流程图中“吸收”过程反应的离子方程式:SO 2 +Br 2 +H 2 O=2H++2Br-+ SO 32-
D. 将 Cl 通 入 含 等 物 质 的 量 FeBr 的 溶 液 中 反 应 离 子 方 程 式 : 2Fe2
2 2
++2Cl
2
+2Br-=Br
2
+2Fe2++4Cl-
8.化学反应中的能量变化,通常主要表现为热量的变化——吸热或者放热。下列有关说法
不正确的是
A.已知 C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定
B.中和反应反应热测定实验中,将 NaOH 溶液快速一次性倒入量热计内筒
C.放热反应的反应物的总能量高于生成物的总能量
D.对于反应 C+CO 高温2CO,反应物总键能高于生成物总键能
2
9.在指定条件下,下列选项所示的物质间转化能实现的是
A. B.
C. D.
10.设 N 为阿伏加德罗常数的值。下列说法正确的是
A
A.常温下,18g 水中含有 O-H 键数为 2N
A
B.7.8gNa O 固体中含离子总数为 0.4N
2 2 A
C.标准状况下,11.2L 水中含有分子的数目为 0.5N
A
D.1molFe 与 1molCl 充分反应,转移电子数为 3N
2 A
11.短周期主族元素 X、Y、Z、W 的原子序数依次增大。X、Y、Z、W 最外层电子数之和
为 18,Y 和 Z 形成的稳定结构的离子 Y2-与 Z2+具有相同的电子层结构,W 与 Y 同主族。下
列说法正确的是
A.非金属性:Y 小于 X
B.Y 的简单氢化物比 W 的稳定
C.X 的最高价氧化物对应的水化物的酸性比 W 的强
2D.Y 分别与 Z、W 形成的化合物中化学键类型相同
12.下列实验操作及现象所得结论正确的是
实验操作 现象 结论
取少量 Fe(NO ) 溶液,滴入硫酸酸化 溶液变黄色 HO 氧化性比 Fe3+强
3 2 2 2
A
的 HO 溶液
2 2
B 中产生白色胶状
B N 的非金属比 Si 强
沉淀
C 蘸有浓氨水的玻璃棒靠近溶液 有白烟产生 溶液 不可能是浓硫酸
D 将红热的炭放入浓硝酸中 产生红棕色气体 浓硝酸可以将碳氧化
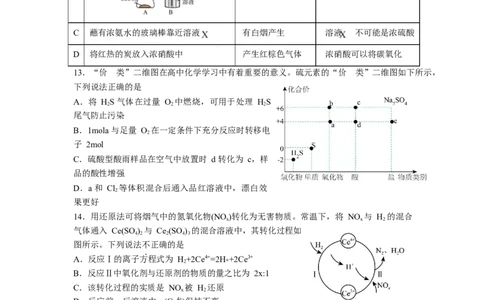
13.“价—类”二维图在高中化学学习中有着重要的意义。硫元素的“价—类”二维图如下所示,
下列说法正确的是
A.将 HS 气体在过量 O 中燃烧,可用于处理 HS
2 2 2
尾气防止污染
B.1mola 与足量 O 在一定条件下充分反应时转移电
2
子 2mol
C.硫酸型酸雨样品在空气中放置时 d 转化为 c,样
品的酸性增强
D.a 和 Cl 等体积混合后通入品红溶液中,漂白效
2
果更好
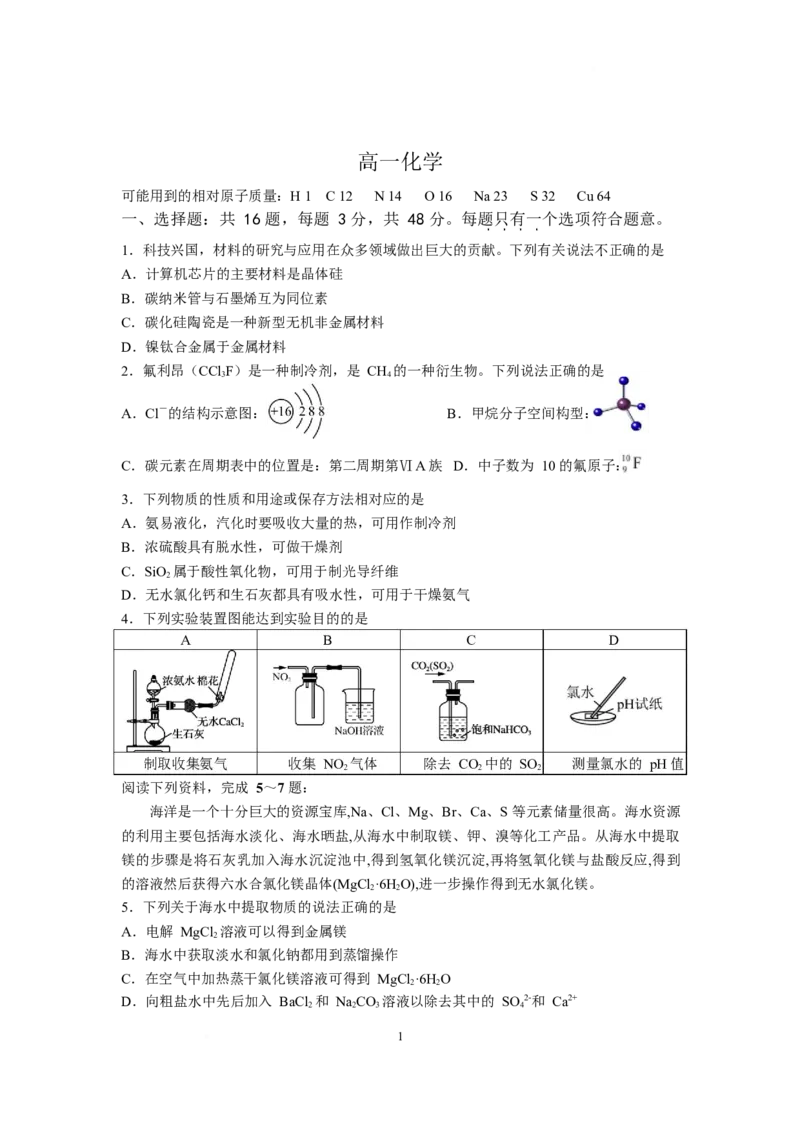
14.用还原法可将烟气中的氮氧化物(NO )转化为无害物质。常温下,将 NO 与 H 的混合
x x 2
气体通入 Ce(SO) 与 Ce (SO ) 的混合溶液中,其转化过程如
4 2 2 4 3
图所示。下列说法不正确的是
A.反应Ⅰ的离子方程式为 H
2
+2Ce4+=2H++2Ce3+
B.反应Ⅱ中氧化剂与还原剂的物质的量之比为 2x:1
C.该转化过程的实质是 NO 被 H 还原
x 2
D.反应前、后溶液中 c(Ce4+)保持不变
15.某废催化剂含 SiO、ZnS 和 CuS。某实验小组以该废催化剂为原料, 回收锌和铜,设
2
计实验流程如图:
下列说法不正确的是
A.步骤①中产生的气体可用 NaOH 溶液进行吸收
B.步骤②中所加试剂可以用浓硫酸代替
3C.滤渣 1 成分是 SiO 和 CuS,滤渣 2 成分可能为 SiO 和 S
2 2
D.步骤④制得蓝矾表面滴加浓硫酸变白色,体现浓硫酸吸水性
16.38.4gCu 与一定量浓硝酸恰好完全反应生成氮的氧化物,这些氧化物恰好溶解在 NaOH
溶液中得到 NaNO 和 NaNO 的混合溶液,反应过程及有关数据如图所示,下列有关判断
3 2
不正确的是
A.硝酸在反应中体现氧化性和酸性
B.混合气体中 NO 的物质的量是 0.1mol
2 4
C.该浓硝酸物质的量浓度为 11mol/L
D.氮的氧化物和 NaOH 溶液反应时,NO 作还原剂
二、非选择题:共 3 题,共 52 分。
17.硝酸是一种重要的基础化工原料。历史上先后出现多种不同的制备硝酸的方法。
方法一:17 世纪,人们以硝石(主要成分 NaNO )为氮源制备硝酸,化学方程式为:HSO
3 2 4
△
(浓)+ NaNO NaHSO + HNO↑。
3 4 3
(1)该反应中,浓硫酸体现了酸性和 ▲ 性。
(2)该反应加热温度不能过高,原因是 ▲ (用化学方程式表示)。
方法二:20 世纪初,挪威出现了电弧法生产硝酸,是历史上最早的硝酸工业化尝试。
(3)该方法是科学家通过高压电弧使空气中的氮气与氧气反应,生成氮氧化物,进一步氧
化吸收合成硝酸。该过程属于 ▲ 。
A.人工固氮 B.自然固氮 C.生物固氮
(4)评价电弧法的优、劣势(各列举一点)。①优势: ▲ ;②劣势: ▲ 。
方法三:合成氨问世后,氨氧化法进入工业化阶段,这种方法至今依然是世界上生产硝酸的
主要方法。以氨气为氮源催化氧化制备硝酸,反应原理分以下三步进行:
(5)第 III 步反应的化 学方程式为 ▲ 。
(6)研究发现,第Ⅱ步反应按如下两步反应进行:
①2NO(g) === NO(g) ΔH<0(快反应)
2 2 1
②NO(g) + O (g) === 2NO (g) ΔH<0(慢反应)
2 2 2 2 2
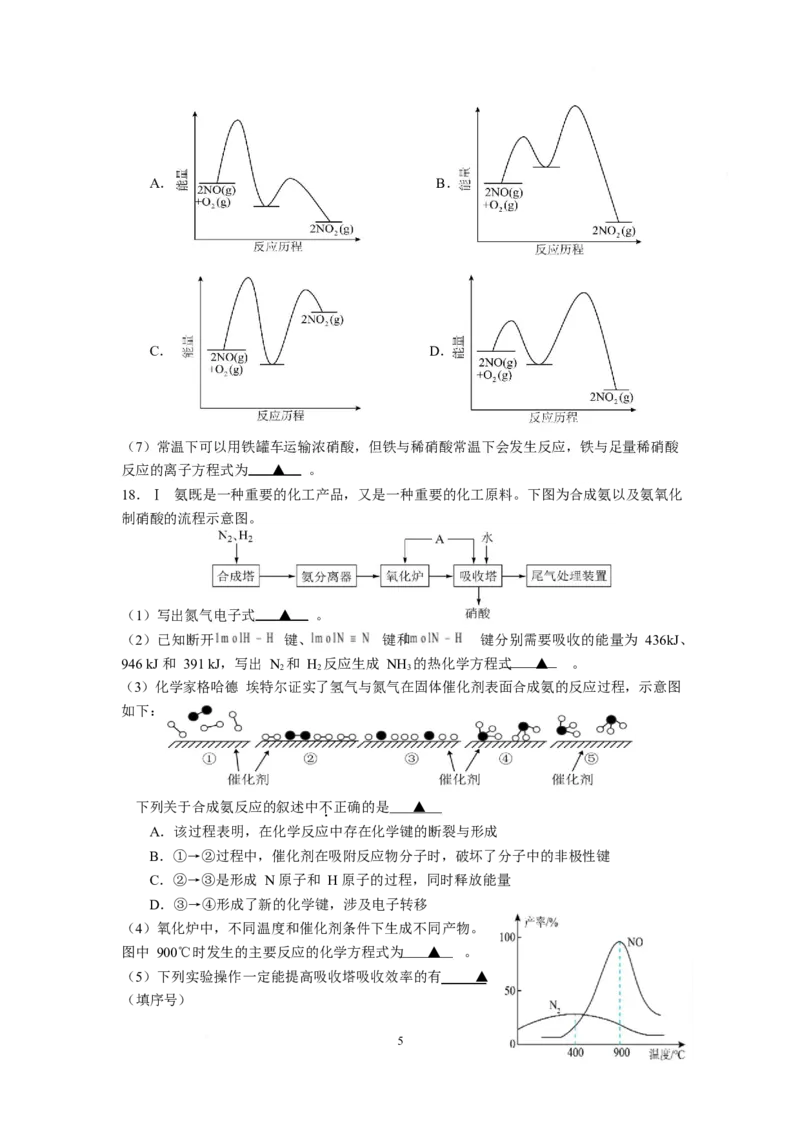
NO 是该反应的 ▲ (选填“催化剂”或“中间产物”)。已知反应物分子必须具有
2 2
足够的能量成为活化分子后才能发生化学反应,二者的平均能量之差叫做“活化能”,“活化
能”越大反应越慢。能正确表示该反应历程能量变化的示意图是 ▲ 。
4A. B.
C. D.
(7)常温下可以用铁罐车运输浓硝酸,但铁与稀硝酸常温下会发生反应,铁与足量稀硝酸
反应的离子方程式为 ▲ 。
18.Ⅰ 氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化
制硝酸的流程示意图。
(1)写出氮气电子式 ▲ 。
(2)已知断开 键、 键和 键分别需要吸收的能量为 436kJ、
946 kJ 和 391 kJ,写出 N 和 H 反应生成 NH 的热化学方程式 ▲ 。
2 2 3
(3)化学家格哈德•埃特尔证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图
如下:
下列关于合成氨反应的叙述中不正确的是 ▲
A.该过程表明,在化学反应中存在化学键的断裂与形成
B.①→②过程中,催化剂在吸附反应物分子时,破坏了分子中的非极性键
C.②→③是形成 N 原子和 H 原子的过程,同时释放能量
D.③→④形成了新的化学键,涉及电子转移
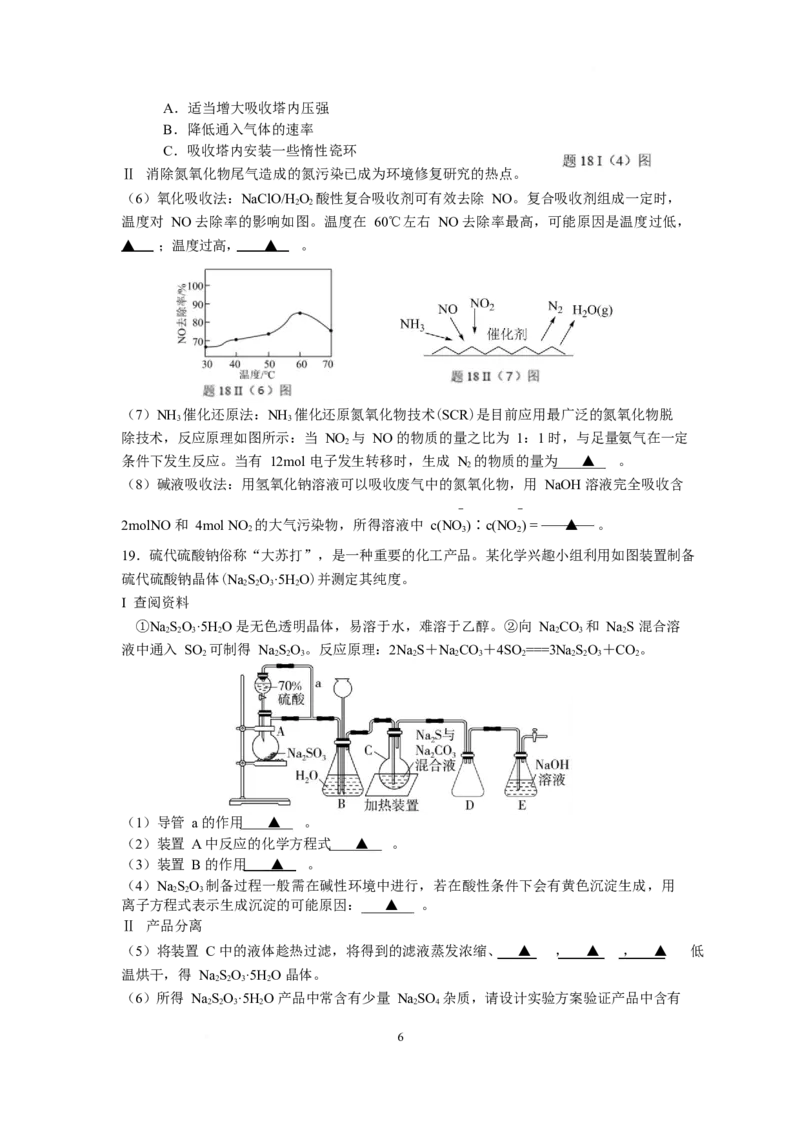
(4)氧化炉中,不同温度和催化剂条件下生成不同产物。
图中 900℃时发生的主要反应的化学方程式为 ▲ 。
(5)下列实验操作一定能提高吸收塔吸收效率的有 ▲
(填序号)
5A.适当增大吸收塔内压强
B.降低通入气体的速率
C.吸收塔内安装一些惰性瓷环
Ⅱ 消除氮氧化物尾气造成的氮污染已成为环境修复研究的热点。
(6)氧化吸收法:NaClO/HO 酸性复合吸收剂可有效去除 NO。复合吸收剂组成一定时,
2 2
温度对 NO 去除率的影响如图。温度在 60℃左右 NO 去除率最高,可能原因是温度过低,
▲ ;温度过高, ▲ 。
(7)NH 催化还原法:NH 催化还原氮氧化物技术(SCR)是目前应用最广泛的氮氧化物脱
3 3
除技术,反应原理如图所示:当 NO 与 NO 的物质的量之比为 1:1 时,与足量氨气在一定
2
条件下发生反应。当有 12mol 电子发生转移时,生成 N 的物质的量为 ▲ 。
2
(8)碱液吸收法:用氢氧化钠溶液可以吸收废气中的氮氧化物,用 NaOH 溶液完全吸收含
− −
2molNO 和 4mol NO 的大气污染物,所得溶液中 c(NO )∶c(NO ) = ▲ 。
2 3 2
19.硫代硫酸钠俗称“大苏打”,是一种重要的化工产品。某化学兴趣小组利用如图装置制备
硫代硫酸钠晶体(NaSO·5H O)并测定其纯度。
2 2 3 2
I 查阅资料
①NaSO·5H O 是无色透明晶体,易溶于水,难溶于乙醇。②向 NaCO 和 NaS 混合溶
2 2 3 2 2 3 2
液中通入 SO 可制得 NaSO。反应原理:2NaS+NaCO+4SO ===3Na SO+CO。
2 2 2 3 2 2 3 2 2 2 3 2
(1)导管 a 的作用 ▲ 。
(2)装置 A 中反应的化学方程式 ▲ 。
(3)装置 B 的作用 ▲ 。
(4)NaSO 制备过程一般需在碱性环境中进行,若在酸性条件下会有黄色沉淀生成,用
2 2 3
离子方程式表示生成沉淀的可能原因: ▲ 。
Ⅱ 产品分离
(5)将装置 C 中的液体趁热过滤,将得到的滤液蒸发浓缩、 ▲ , ▲ , ▲ 低
温烘干,得 NaSO·5H O 晶体。
2 2 3 2
(6)所得 NaSO·5H O 产品中常含有少量 NaSO 杂质,请设计实验方案验证产品中含有
2 2 3 2 2 4
6NaSO : ▲ 。
2 4
Ⅲ NaSO·5H O 产品纯度测定
2 2 3 2
(7)为了测定粗产品中 NaSO·5H O(M=248g/mol)的纯度,一般采用在酸性条件下用
2 2 3 2
KMnO 标准液滴定的方法(假定粗产品中杂质与酸性 KMnO 溶液不反应)。称取 1.5g 的粗
4 4
样品溶于水,用 0.40mol/L 酸性 KMnO 4 溶液滴定,KMnO 4 被还原为 Mn2+,当溶液中 S 2 O 32
-全部被氧化成 时,消耗酸性 KMnO 溶液的体积为 20.00 mL。计算产品中 NaSO·
4 2 2 3
5HO 的纯度 ▲ (写出计算过程,结果保留三位有效数字)。
2
7