文档内容
福建省 2022 年高考化学试题
C Cu
1. 福建多个科研机构经过长期联合研究发现,使用 60和改性的 基催化剂,可打通从合成气经草酸二
甲酯常压催化加氢制备乙二醇的技术难关。下列说法正确的是
A. 草酸属于无机物 B. C 与石墨互为同分异构体
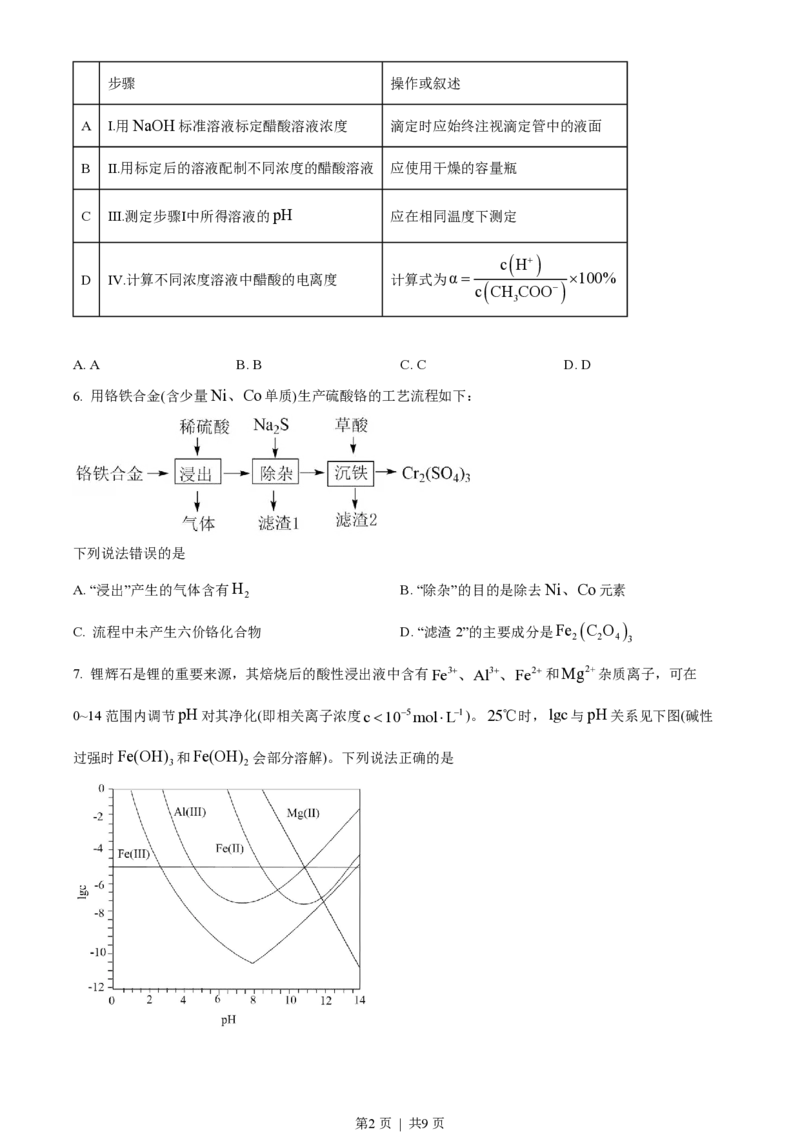
60
C. Cu属于过渡元素 D. 催化剂通过降低焓变加快反应速率
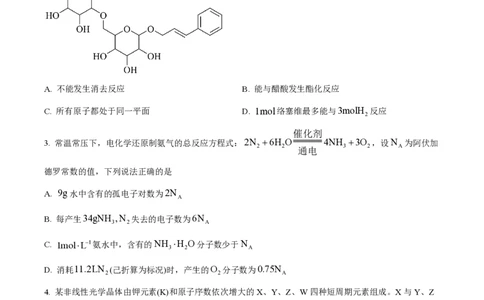
2. 络塞维是中药玫瑰红景天中含有的一种天然产物,分子结构见下图。关于该化合物下列说法正确的是
A. 不能发生消去反应 B. 能与醋酸发生酯化反应
C. 所有原子都处于同一平面 D. 1mol络塞维最多能与3molH 反应
2
催化剂
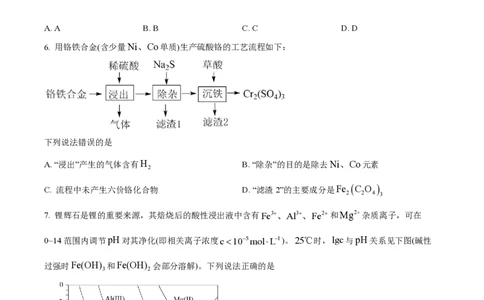
3. 常温常压下,电化学还原制氨气的总反应方程式:2N +6H O 4NH +3O ,设N 为阿伏加
2 2 3 2 A
通电
德罗常数的值,下列说法正确的是
A. 9g水中含有的孤电子对数为2N
A
B. 每产生34gNH ,N 失去的电子数为6N
3 2 A
C. 1mol×L-1氨水中,含有的NH ×H O分子数少于N
3 2 A
D. 消耗11.2LN (己折算为标况)时,产生的O 分子数为0.75N
2 2 A
4. 某非线性光学晶体由钾元素(K)和原子序数依次增大的X、Y、Z、W四种短周期元素组成。X与Y、Z
与W均为同周期相邻元素,X的核外电子总数为最外层电子数的2倍,Z为地壳中含量最多的元素。下列
说法正确的是
A. 简单氢化物沸点:Z>W B. YW 分子的空间构型为三角锥形
3
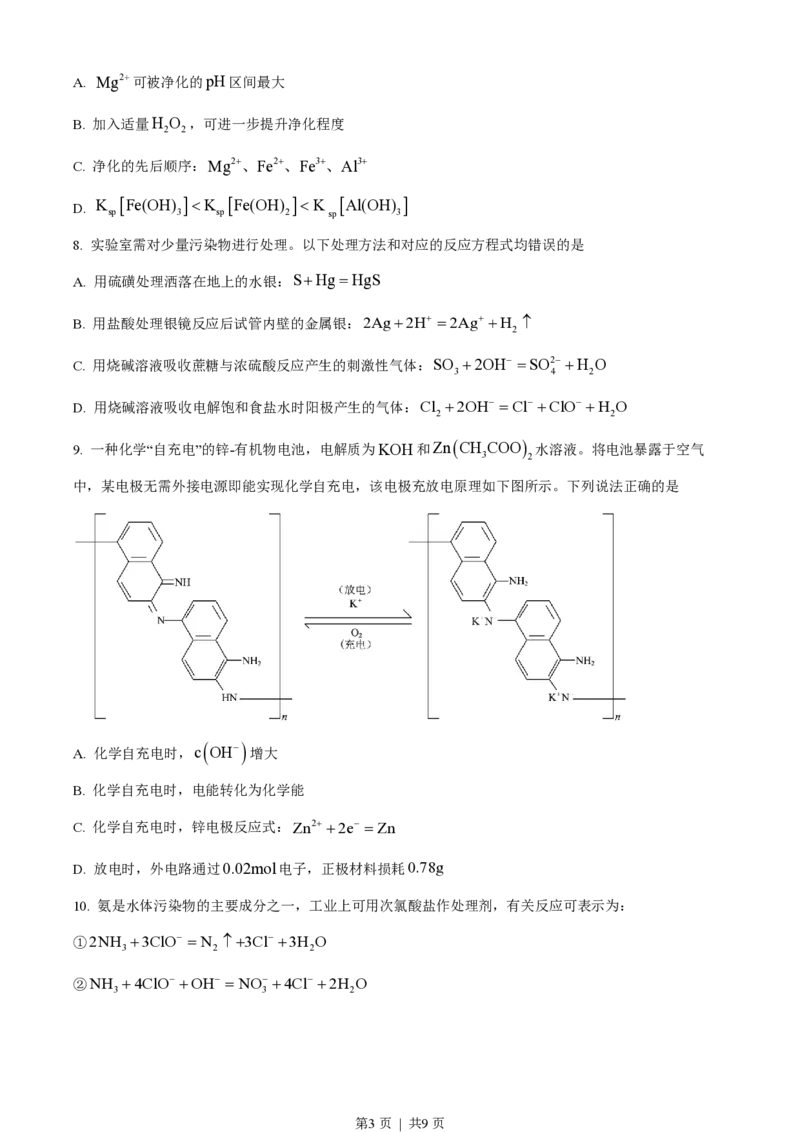
C. 原子半径:Yx 时,c
Cl-
=4c
NO-
1 3
C. x >x 时,x越大,生成N 的量越少
1 2
D. x=x 时,c
Na+
+c
H+
+c
NH+
=c
Cl-
+c
OH-
+c
ClO-
1 4
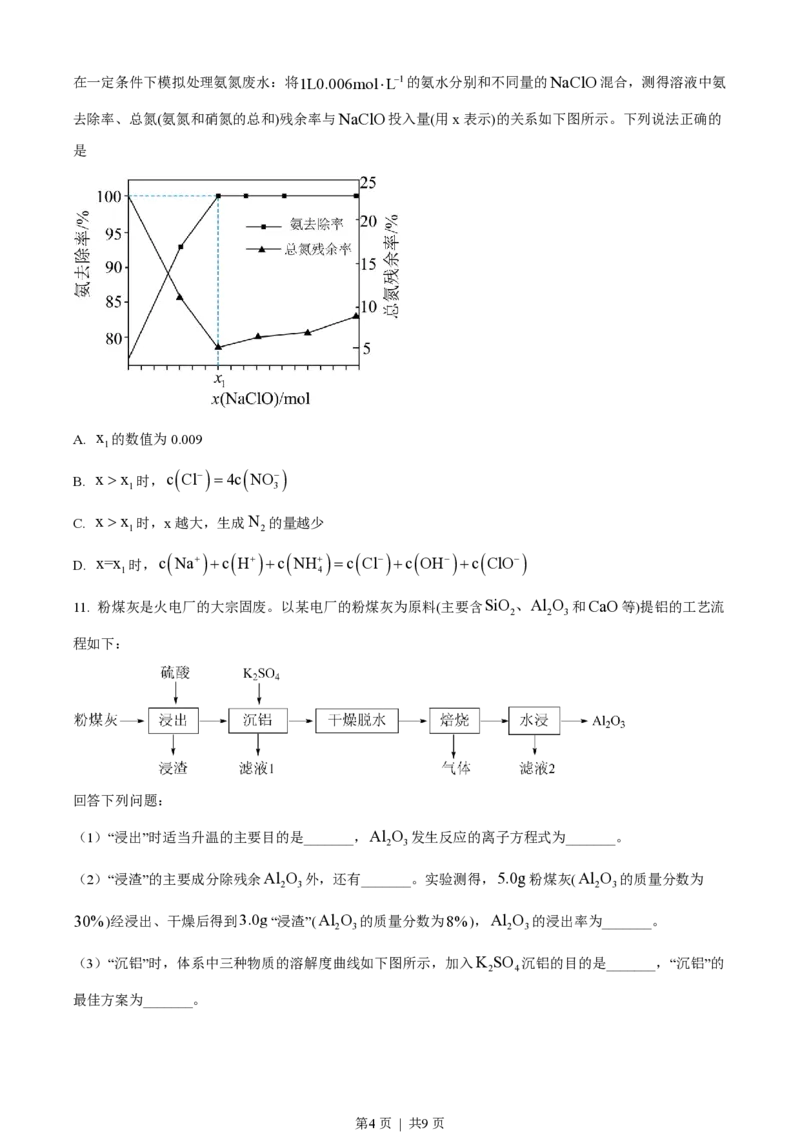
11. 粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰为原料(主要含SiO 、Al O 和CaO等)提铝的工艺流
2 2 3
程如下:
回答下列问题:
(1)“浸出”时适当升温的主要目的是_______,Al O 发生反应的离子方程式为_______。
2 3
(2)“浸渣”的主要成分除残余Al O 外,还有_______。实验测得,5.0g粉煤灰(Al O 的质量分数为
2 3 2 3
30%)经浸出、干燥后得到3.0g“浸渣”(Al O 的质量分数为8%),Al O 的浸出率为_______。
2 3 2 3
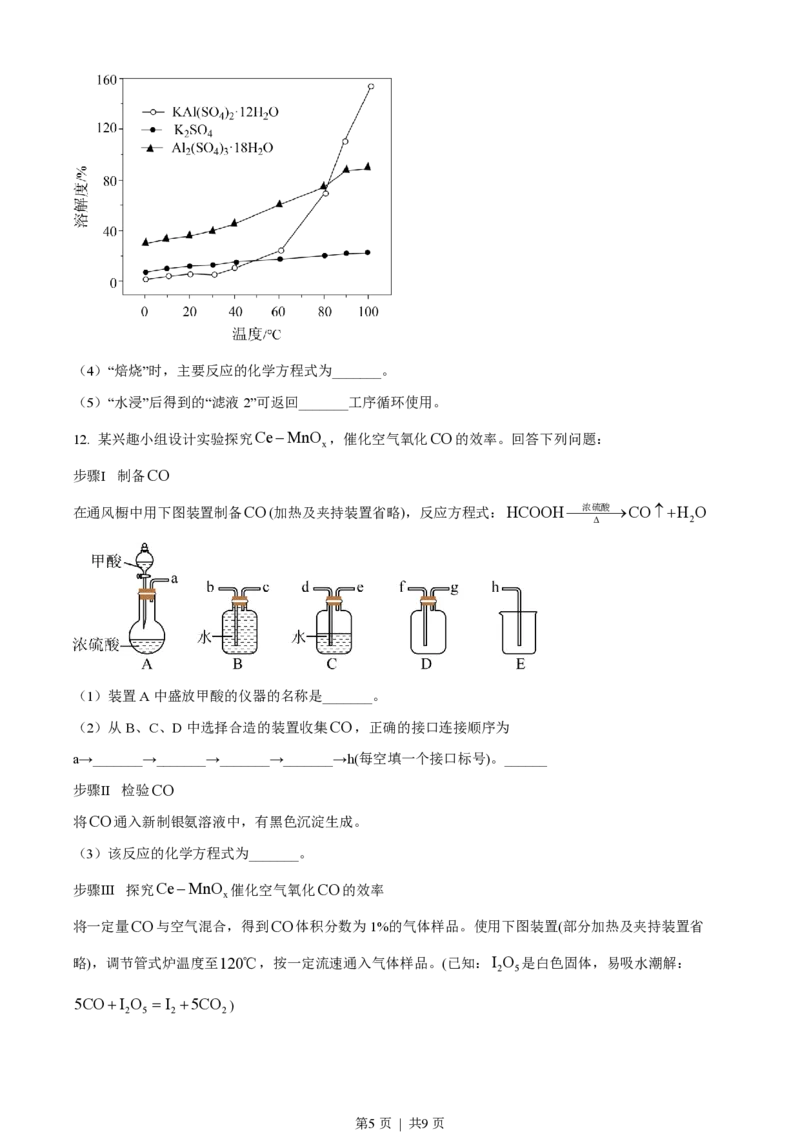
(3)“沉铝”时,体系中三种物质的溶解度曲线如下图所示,加入K SO 沉铝的目的是_______,“沉铝”的
2 4
最佳方案为_______。
第4页 | 共9页(4)“焙烧”时,主要反应的化学方程式为_______。
(5)“水浸”后得到的“滤液2”可返回_______工序循环使用。
12. 某兴趣小组设计实验探究Ce-MnO ,催化空气氧化CO的效率。回答下列问题:
x
步骤Ⅰ 制备CO
在通风橱中用下图装置制备CO(加热及夹持装置省略),反应方程式:HCOOH¾浓¾硫¾酸®CO+H O
D 2
(1)装置A中盛放甲酸的仪器的名称是_______。
(2)从B、C、D中选择合造的装置收集CO,正确的接口连接顺序为
a→_______→_______→_______→_______→h(每空填一个接口标号)。______
步骤Ⅱ 检验CO
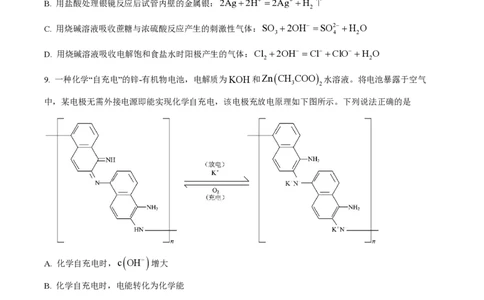
将CO通入新制银氨溶液中,有黑色沉淀生成。
(3)该反应的化学方程式为_______。
步骤Ⅲ 探究Ce-MnO 催化空气氧化CO的效率
x
将一定量CO与空气混合,得到CO体积分数为1%的气体样品。使用下图装置(部分加热及夹持装置省
略),调节管式炉温度至120℃,按一定流速通入气体样品。(已知:I O 是白色固体,易吸水潮解:
2 5
5CO+I O =I +5CO )
2 5 2 2
第5页 | 共9页(4)通入11.2L(已折算为标况)的气体样品后,继续向装置内通入一段时间氮气,最终测得U形管内生成
了0.1016gI 。
2
①能证明CO被空气氧化的现象是_______;
②CO被催化氧化的百分率为_______;
③若未通入氮气,②的结果将_______(填“偏大”“偏小”或“无影响”)。
(5)探究气体与催化剂接触时长对催化氧化效率的影响时,采用_______方法可以缩短接触时长。
(6)步骤Ⅲ装置存在的不足之处是_______。
13. 异丙醇 C H O 可由生物质转化得到,催化异丙醇脱水制取高值化学品丙烯 C H 的工业化技术已
3 8 3 6
引起人们的关注,其主要反应如下:
Ⅰ.C H O(g)ˆˆ†C H (g)+H O(g) ΔH =+52kJ×mol-1
3 8 ‡ˆˆ 3 6 2 1
Ⅱ 2C H (g)ˆˆ†C H (g) ΔH =-97kJ×mol-1
. 3 6 ‡ˆˆ 6 12 2
回答下列问题:
(1)已知2C H O(g)+9O (g)=6CO (g)+8H O(g) ΔH=-3750kJ×mol-1,则C H (g)燃烧生成
3 8 2 2 2 3 6
CO (g)和H O(g)的热化学方程式为_______。
2 2
(2)在1350℃下,刚性密闭容器中的反应体系内水蒸气浓度与反应时间关系如下表:
反应时间/μs 0 4 8 12 t 20
H O浓度/ppm 0 2440 3200 3600 4000 4100
2
①4~8μs内,vC H O=_______ppm×μs-1;
3 8
②t_______16(填“>”“<”或“=”)。
(3)在恒温刚性密闭容器中,反应Ⅰ、Ⅱ均达到平衡的判据是_______(填标号)。
a.H O(g)的分压不变 b.混合气体密度不变
2
c.nC H =2nC H d.v H O=v C H O
3 6 6 12 正 2 逆 3 8
第6页 | 共9页(4)在一定条件下,若反应Ⅰ、Ⅱ的转化率分别为98%和40%,则丙烯的产率为_______。
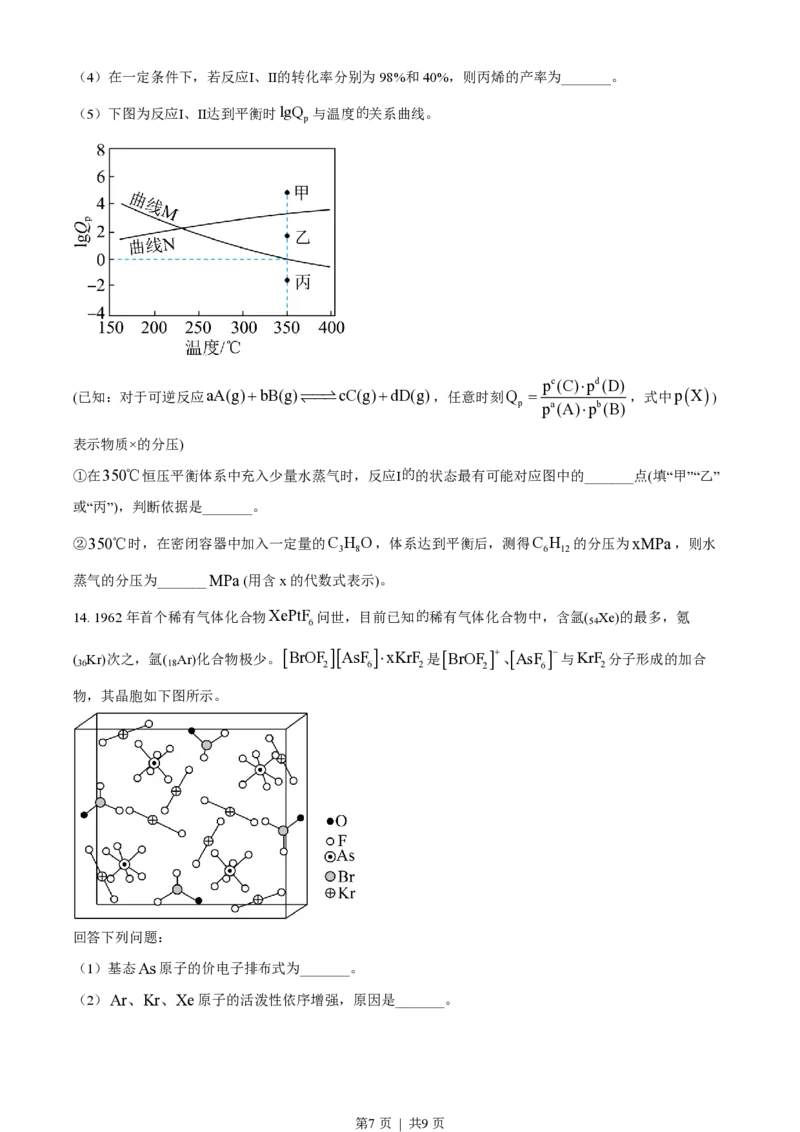
(5)下图为反应Ⅰ、Ⅱ达到平衡时lgQ 与温度的关系曲线。
p
pc(C)×pd(D)
(已知:对于可逆反应aA(g)+bB(g)ˆˆ†cC(g)+dD(g),任意时刻Q = ,式中pX )
‡ˆˆ p pa(A)×pb(B)
表示物质×的分压)
①在350℃恒压平衡体系中充入少量水蒸气时,反应Ⅰ的的状态最有可能对应图中的_______点(填“甲”“乙”
或“丙”),判断依据是_______。
②350℃时,在密闭容器中加入一定量的C H O,体系达到平衡后,测得C H 的分压为xMPa,则水
3 8 6 12
蒸气的分压为_______MPa(用含x的代数式表示)。
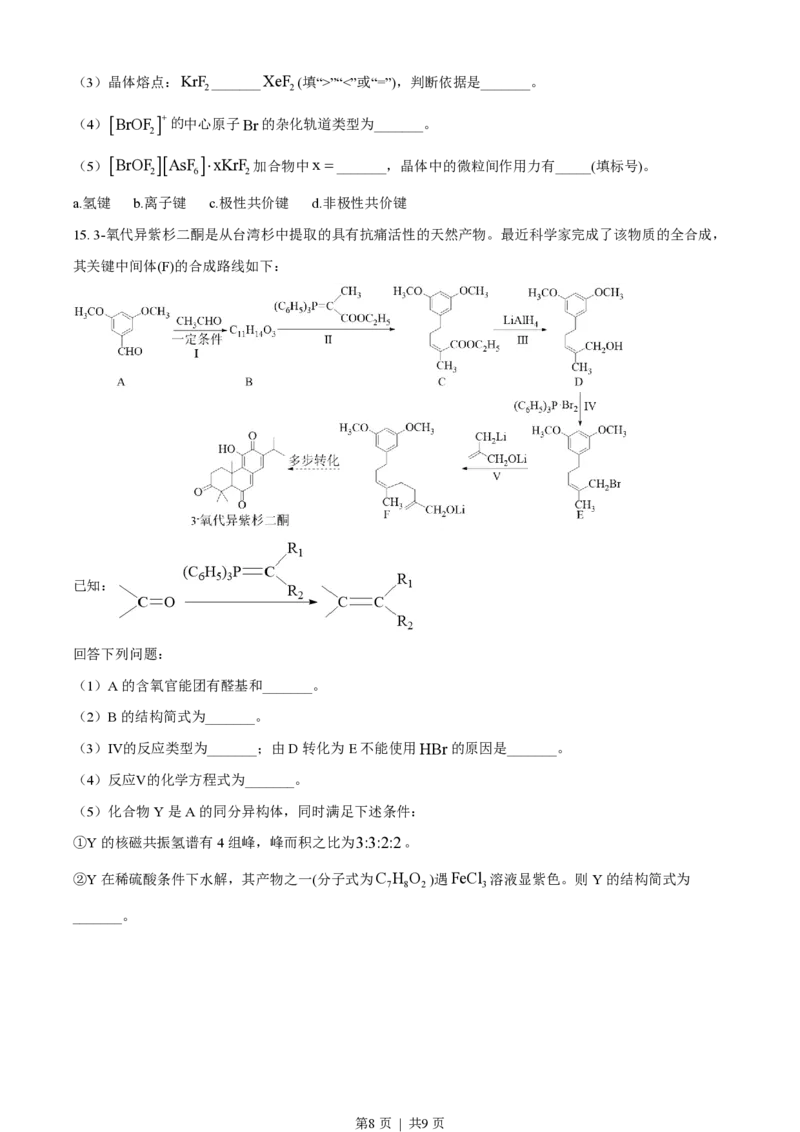
14. 1962年首个稀有气体化合物XePtF 问世,目前已知的稀有气体化合物中,含氩( Xe)的最多,氪
6 54
( Kr)次之,氩( Ar)化合物极少。 BrOF AsF ×xKrF 是BrOF +、AsF - 与KrF 分子形成的加合
36 18 2 6 2 2 6 2
物,其晶胞如下图所示。
回答下列问题:
(1)基态As原子的价电子排布式为_______。
(2)Ar、Kr、Xe原子的活泼性依序增强,原因是_______。
第7页 | 共9页(3)晶体熔点:KrF _______XeF (填“>”“<”或“=”),判断依据是_______。
2 2
(4)BrOF +的中心原子Br的杂化轨道类型为_______。
2
(5) BrOF AsF ×xKrF 加合物中x =_______,晶体中的微粒间作用力有_____(填标号)。
2 6 2
a.氢键 b.离子键 c.极性共价键 d.非极性共价键
15. 3-氧代异紫杉二酮是从台湾杉中提取的具有抗痛活性的天然产物。最近科学家完成了该物质的全合成,
其关键中间体(F)的合成路线如下:
已知:
回答下列问题:
(1)A的含氧官能团有醛基和_______。
(2)B的结构简式为_______。
(3)Ⅳ的反应类型为_______;由D转化为E不能使用HBr的原因是_______。
(4)反应Ⅴ的化学方程式为_______。
(5)化合物Y是A的同分异构体,同时满足下述条件:
①Y的核磁共振氢谱有4组峰,峰而积之比为3:3:2:2。
②Y在稀硫酸条件下水解,其产物之一(分子式为C H O )遇FeCl 溶液显紫色。则Y的结构简式为
7 8 2 3
_______。
第8页 | 共9页第9页 | 共9页