文档内容
机密★启用前
河南省 2025 年普通高中学业水平选择性考试
化学
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在试卷、答题卡上。
2.回答选择题时,选出每小题答案后,用 2B铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写
在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 Li7 C12 N14 O16 Na23 S32 Cl35.5 Fe56 Br80
一、选择题:本题共 14小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一
项是符合题目要求。
1. 活字印刷术极大地促进了世界文化的交流,推动了人类文明的进步。下列“活字”字坯的主要成分为硅
酸盐的是
A.泥活字 B.木活字 C.铜活字 D.铅活字
A. A B. B C. C D. D
2. 下列化学用语或图示正确的是
A. 反-1,2-二氟乙烯的结构式:
B. 二氯甲烷分子的球棍模型:
C. 基态S原子的价电子轨道表示式:
第1页/共11页
学科网(北京)股份有限公司D. 用电子式表示CsCl的形成过程:
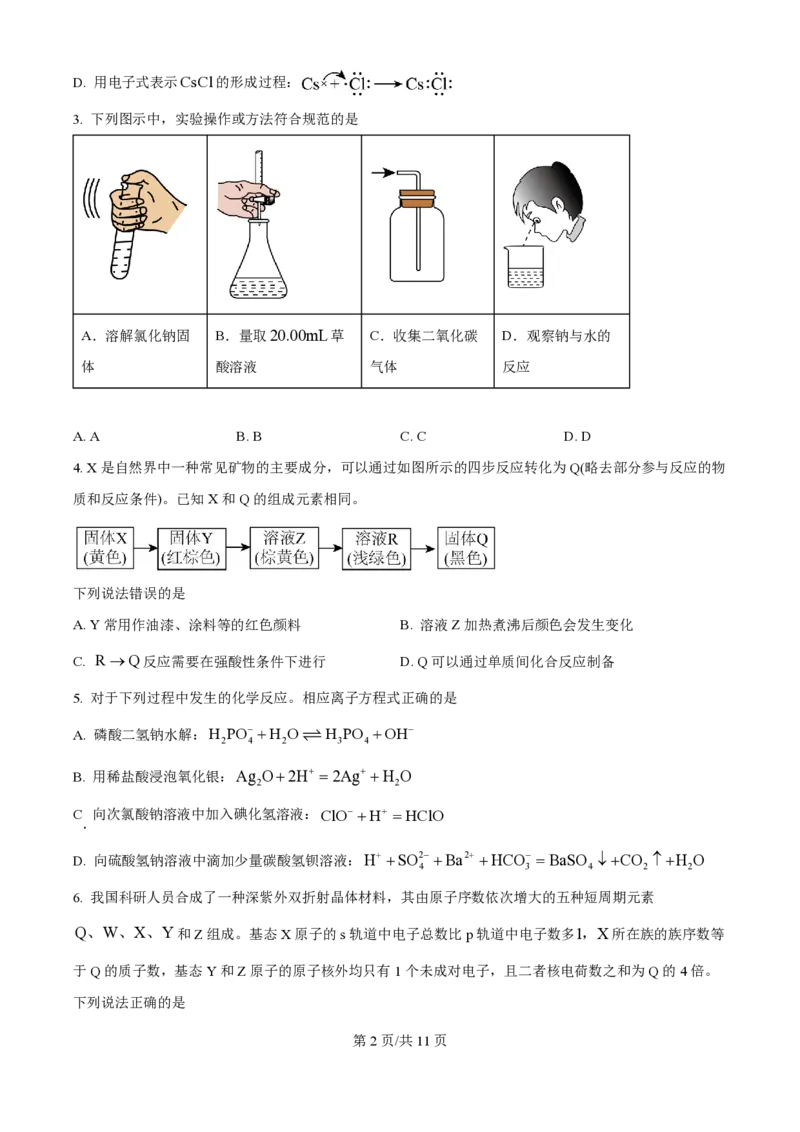
3. 下列图示中,实验操作或方法符合规范的是
A.溶解氯化钠固 B.量取20.00mL草 C.收集二氧化碳 D.观察钠与水的
体 酸溶液 气体 反应
A. A B. B C. C D. D
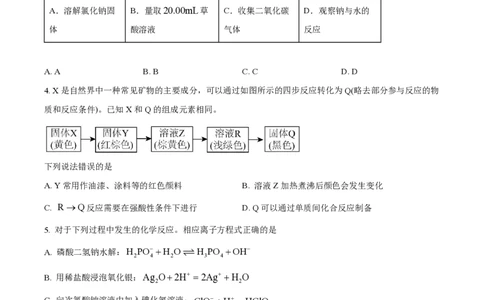
4. X是自然界中一种常见矿物的主要成分,可以通过如图所示的四步反应转化为Q(略去部分参与反应的物
质和反应条件)。已知X和Q的组成元素相同。
下列说法错误的是
A. Y常用作油漆、涂料等的红色颜料 B. 溶液Z加热煮沸后颜色会发生变化
C. R ®Q反应需要在强酸性条件下进行 D. Q可以通过单质间化合反应制备
5. 对于下列过程中发生的化学反应。相应离子方程式正确的是
A. 磷酸二氢钠水解:H 2 PO 4 - +H 2 O ƒ H 3 PO 4 +OH-
B. 用稀盐酸浸泡氧化银:Ag O+2H+ =2Ag+ +H O
2 2
C 向次氯酸钠溶液中加入碘化氢溶液:ClO- +H+ =HClO
.
D. 向硫酸氢钠溶液中滴加少量碳酸氢钡溶液:H+ +SO2- +Ba2+ +HCO- =BaSO ¯+CO +H O
4 3 4 2 2
6. 我国科研人员合成了一种深紫外双折射晶体材料,其由原子序数依次增大的五种短周期元素
Q、W、X、Y和Z组成。基态X原子的s轨道中电子总数比p轨道中电子数多1,X所在族的族序数等
于Q的质子数,基态Y和Z原子的原子核外均只有1个未成对电子,且二者核电荷数之和为Q的4倍。
下列说法正确的是
第2页/共11页
学科网(北京)股份有限公司A. QY 为极性分子 B. ZY 为共价晶体
3
C 原子半径:W>Z D. 1个X 分子中有2个p键
. 2
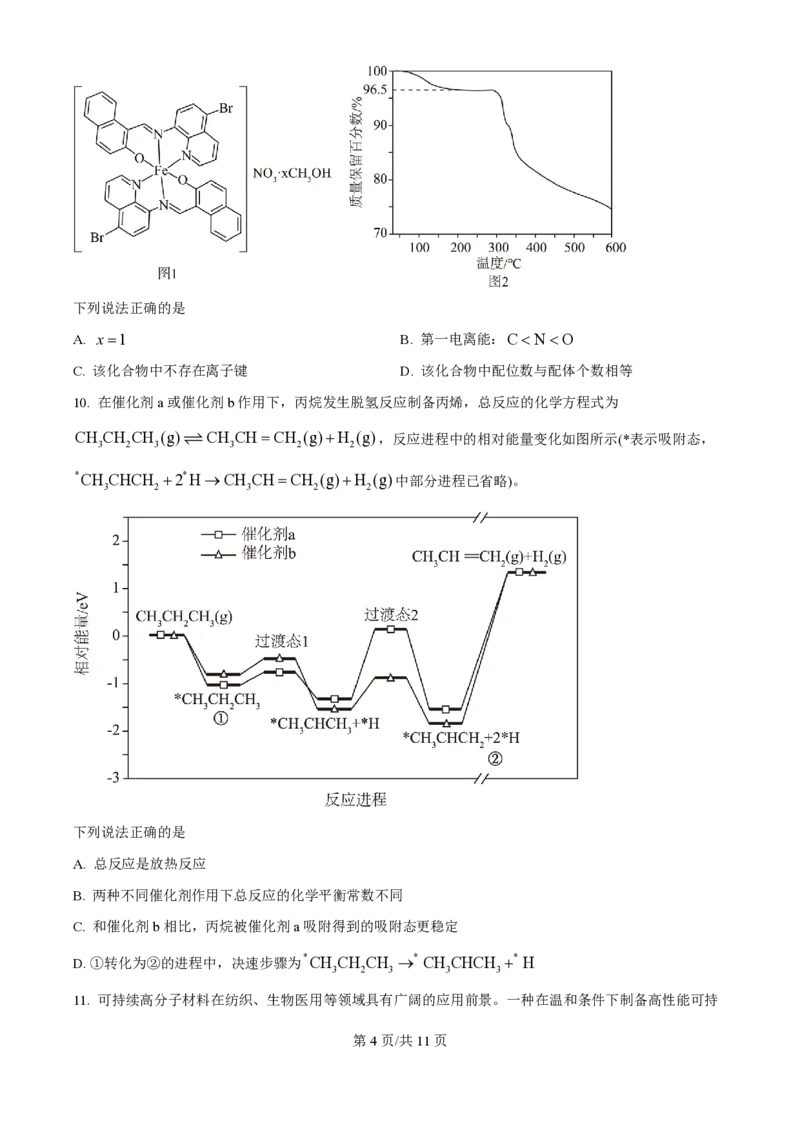
7. 化合物M是从红树林真菌代谢物中分离得到的一种天然产物,其结构如图所示。下列有关M的说法正
确的是
A. 分子中所有的原子可能共平面
B. 1molM 最多能消耗4molNaOH
C. 既能发生取代反应,又能发生加成反应
D. 能形成分子间氢键,但不能形成分子内氢键
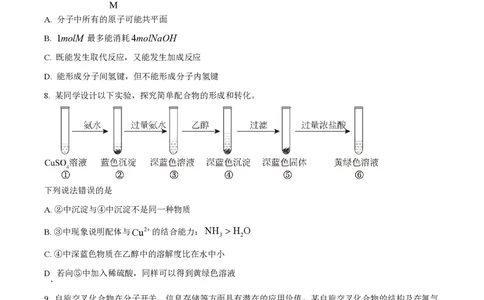
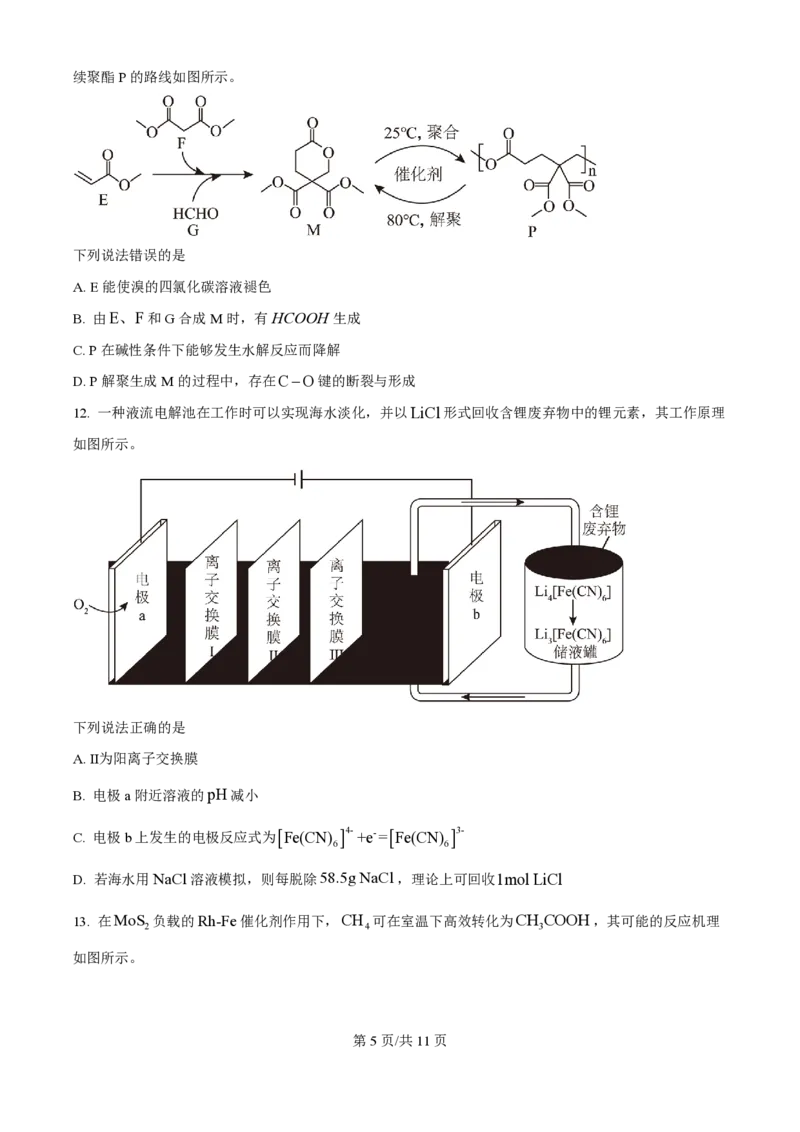
8. 某同学设计以下实验,探究简单配合物的形成和转化。
下列说法错误的是
A. ②中沉淀与④中沉淀不是同一种物质
B. ③中现象说明配体与Cu2+的结合能力:NH >H O
3 2
C. ④中深蓝色物质在乙醇中的溶解度比在水中小
D 若向⑤中加入稀硫酸,同样可以得到黄绿色溶液
.
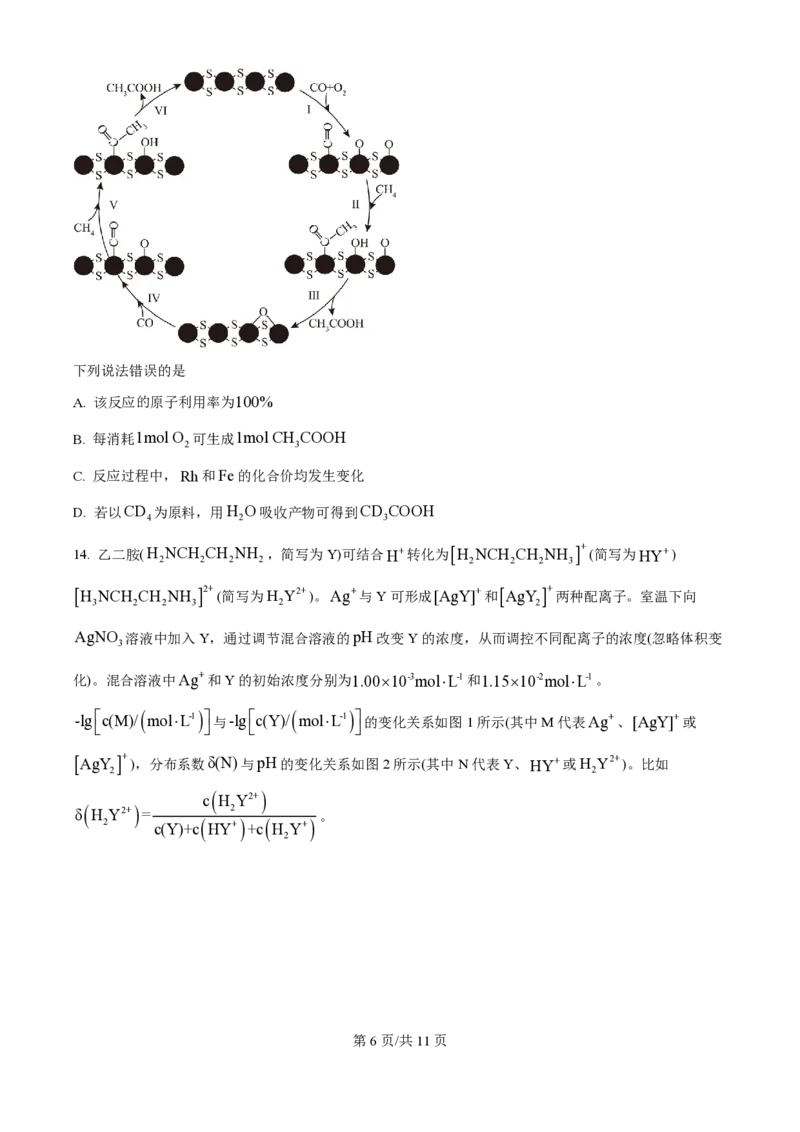
9. 自旋交叉化合物在分子开关、信息存储等方面具有潜在的应用价值。某自旋交叉化合物的结构及在氯气
气氛下的热重曲线分别如图1和图2所示。该化合物的相对分子质量M =870+32x(x为整数)。
r
第3页/共11页
学科网(北京)股份有限公司下列说法正确的是
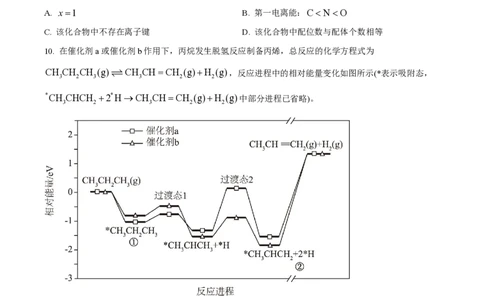
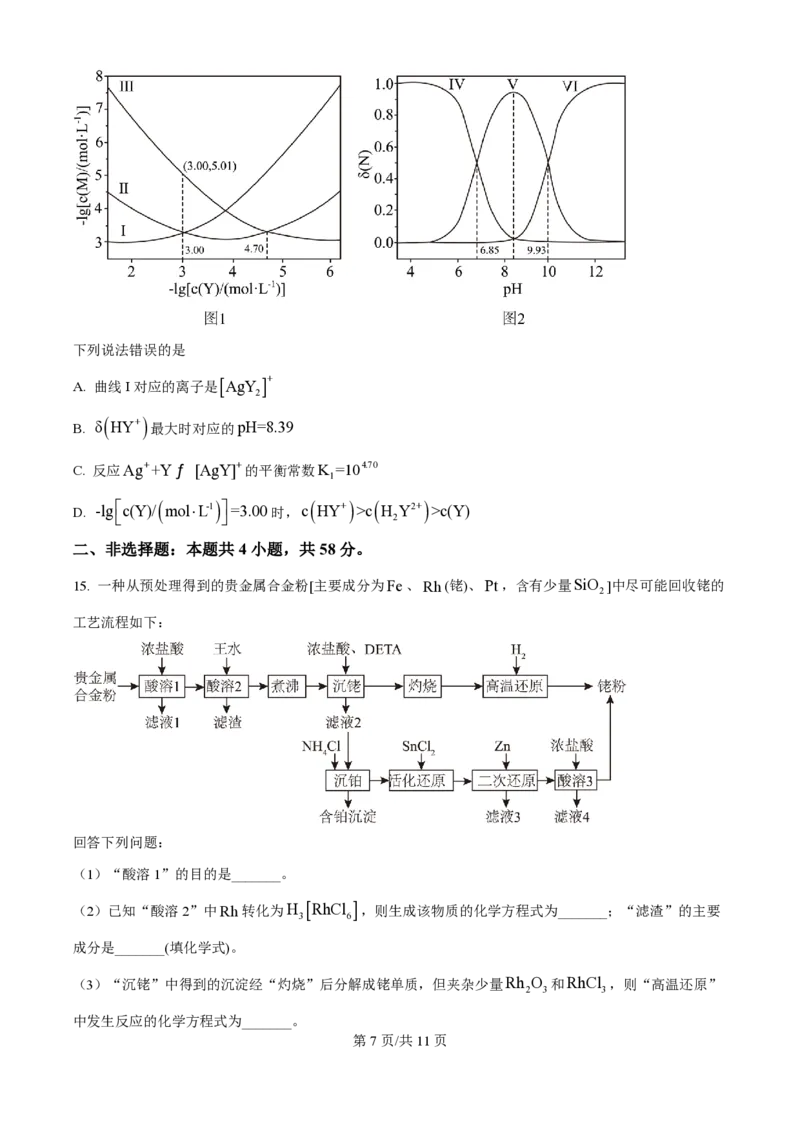
A. x=1 B. 第一电离能:C< Nc H Y2+ >c(Y)
ë û 2
二、非选择题:本题共 4小题,共 58分。
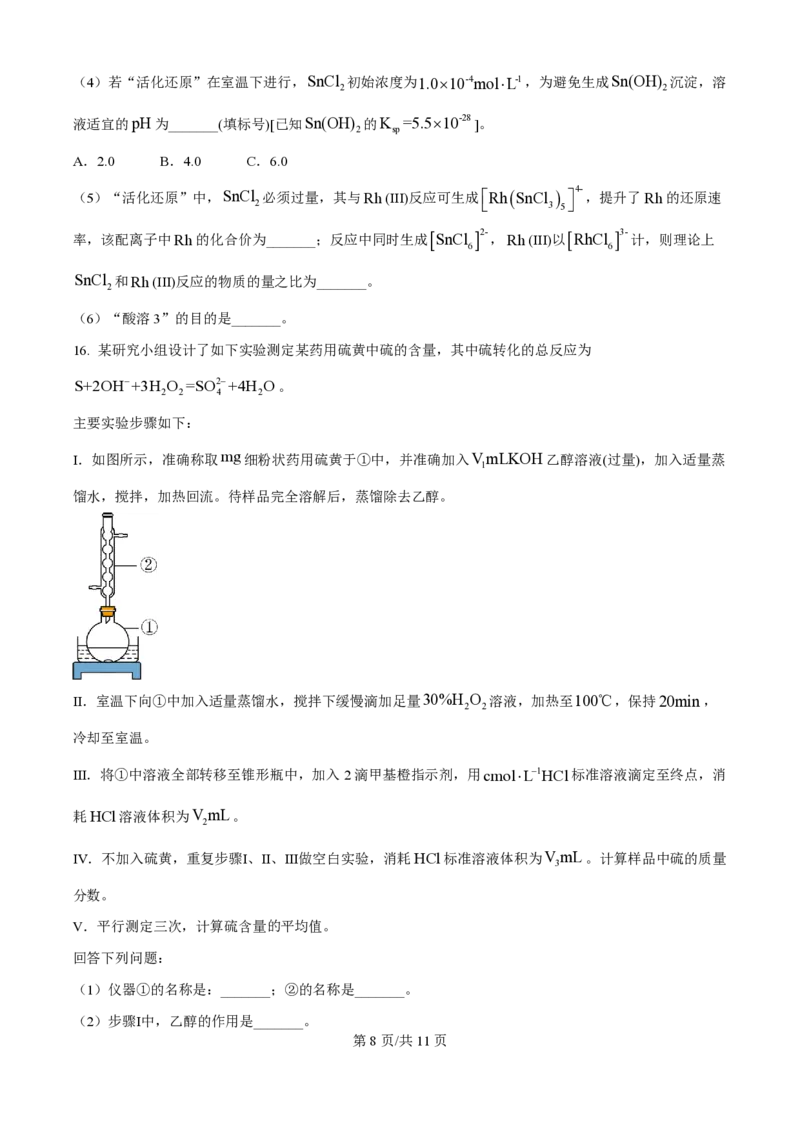
15. 一种从预处理得到的贵金属合金粉[主要成分为Fe、Rh(铑)、Pt,含有少量SiO ]中尽可能回收铑的
2
工艺流程如下:
回答下列问题:
(1)“酸溶1”的目的是_______。
(2)已知“酸溶2”中Rh转化为H RhCl ,则生成该物质的化学方程式为_______;“滤渣”的主要
3 6
成分是_______(填化学式)。
(3)“沉铑”中得到的沉淀经“灼烧”后分解成铑单质,但夹杂少量Rh O 和RhCl ,则“高温还原”
2 3 3
中发生反应的化学方程式为_______。
第7页/共11页
学科网(北京)股份有限公司(4)若“活化还原”在室温下进行,SnCl 初始浓度为1.0´10-4mol×L-1,为避免生成Sn(OH) 沉淀,溶
2 2
液适宜的pH为_______(填标号)[已知Sn(OH) 的K =5.5´10-28 ]。
2 sp
A.2.0 B.4.0 C.6.0
(5)“活化还原”中,SnCl 必须过量,其与Rh(III)反应可生成éRhSnCl ù 4- ,提升了Rh的还原速
2 ë 3 5 û
率,该配离子中Rh的化合价为_______;反应中同时生成SnCl 2- ,Rh(III)以RhCl 3- 计,则理论上
6 6
SnCl 和Rh(III)反应的物质的量之比为_______。
2
(6)“酸溶3”的目的是_______。
16. 某研究小组设计了如下实验测定某药用硫黄中硫的含量,其中硫转化的总反应为
S+2OH-+3H O =SO2-+4H O。
2 2 4 2
主要实验步骤如下:
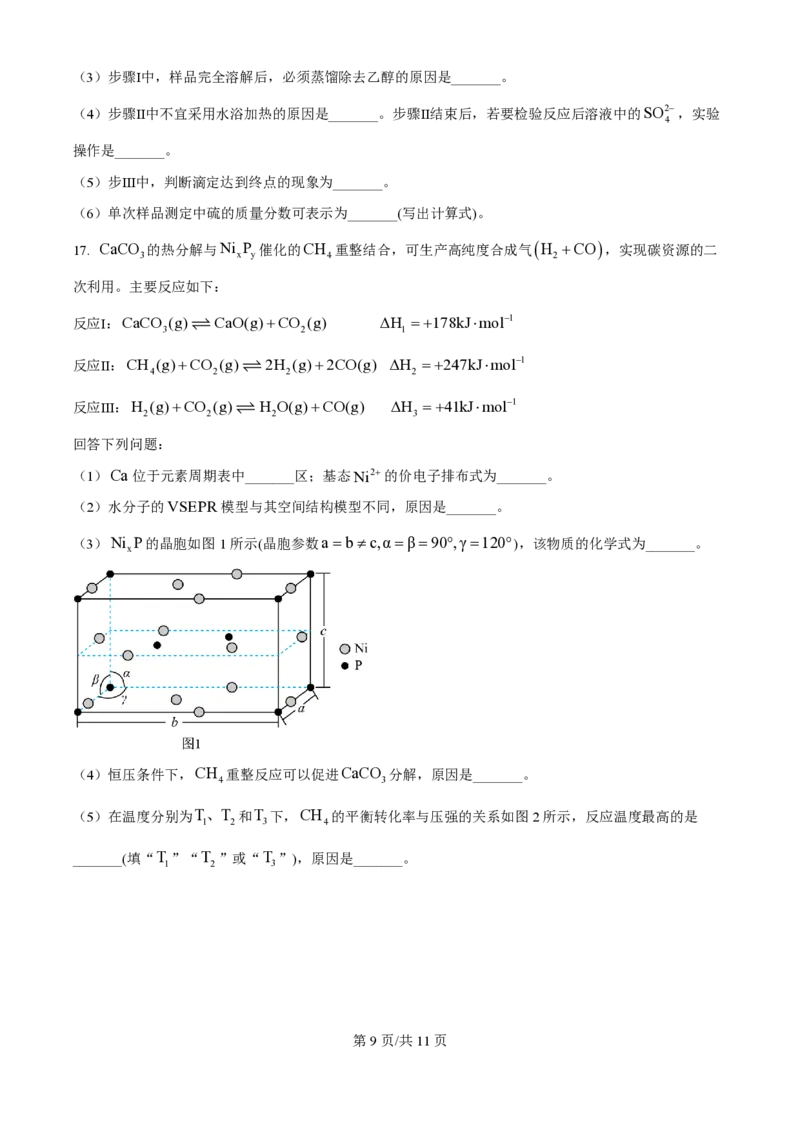
Ⅰ.如图所示,准确称取mg细粉状药用硫黄于①中,并准确加入VmLKOH乙醇溶液(过量),加入适量蒸
1
馏水,搅拌,加热回流。待样品完全溶解后,蒸馏除去乙醇。
Ⅱ.室温下向①中加入适量蒸馏水,搅拌下缓慢滴加足量30%H O 溶液,加热至100℃,保持20min,
2 2
冷却至室温。
Ⅲ.将①中溶液全部转移至锥形瓶中,加入2滴甲基橙指示剂,用cmol×L-1HCl标准溶液滴定至终点,消
耗HCl溶液体积为V mL。
2
Ⅳ.不加入硫黄,重复步骤Ⅰ、Ⅱ、Ⅲ做空白实验,消耗HCl标准溶液体积为VmL。计算样品中硫的质量
3
分数。
Ⅴ.平行测定三次,计算硫含量的平均值。
回答下列问题:
(1)仪器①的名称是:_______;②的名称是_______。
(2)步骤Ⅰ中,乙醇的作用是_______。
第8页/共11页
学科网(北京)股份有限公司(3)步骤Ⅰ中,样品完全溶解后,必须蒸馏除去乙醇的原因是_______。
(4)步骤Ⅱ中不宜采用水浴加热的原因是_______。步骤Ⅱ结束后,若要检验反应后溶液中的SO2-,实验
4
操作是_______。
(5)步Ⅲ中,判断滴定达到终点的现象为_______。
(6)单次样品测定中硫的质量分数可表示为_______(写出计算式)。
17. CaCO 的热分解与Ni P 催化的CH 重整结合,可生产高纯度合成气 H +CO ,实现碳资源的二
3 x y 4 2
次利用。主要反应如下:
反应Ⅰ:CaCO
3
(g)
ƒ
CaO(g)+CO
2
(g) DH
1
=+178kJ×mol-1
反应Ⅱ:CH
4
(g)+CO
2
(g)
ƒ
2H
2
(g)+2CO(g) DH
2
=+247kJ×mol-1
反应Ⅲ:H
2
(g)+CO
2
(g)
ƒ
H
2
O(g)+CO(g) DH
3
=+41kJ×mol-1
回答下列问题:
(1)Ca位于元素周期表中_______区;基态Ni2+的价电子排布式为_______。
(2)水分子的VSEPR模型与其空间结构模型不同,原因是_______。
(3)Ni P的晶胞如图1所示(晶胞参数a =b¹c,α=β=90°,γ=120°),该物质的化学式为_______。
x
(4)恒压条件下,CH 重整反应可以促进CaCO 分解,原因是_______。
4 3
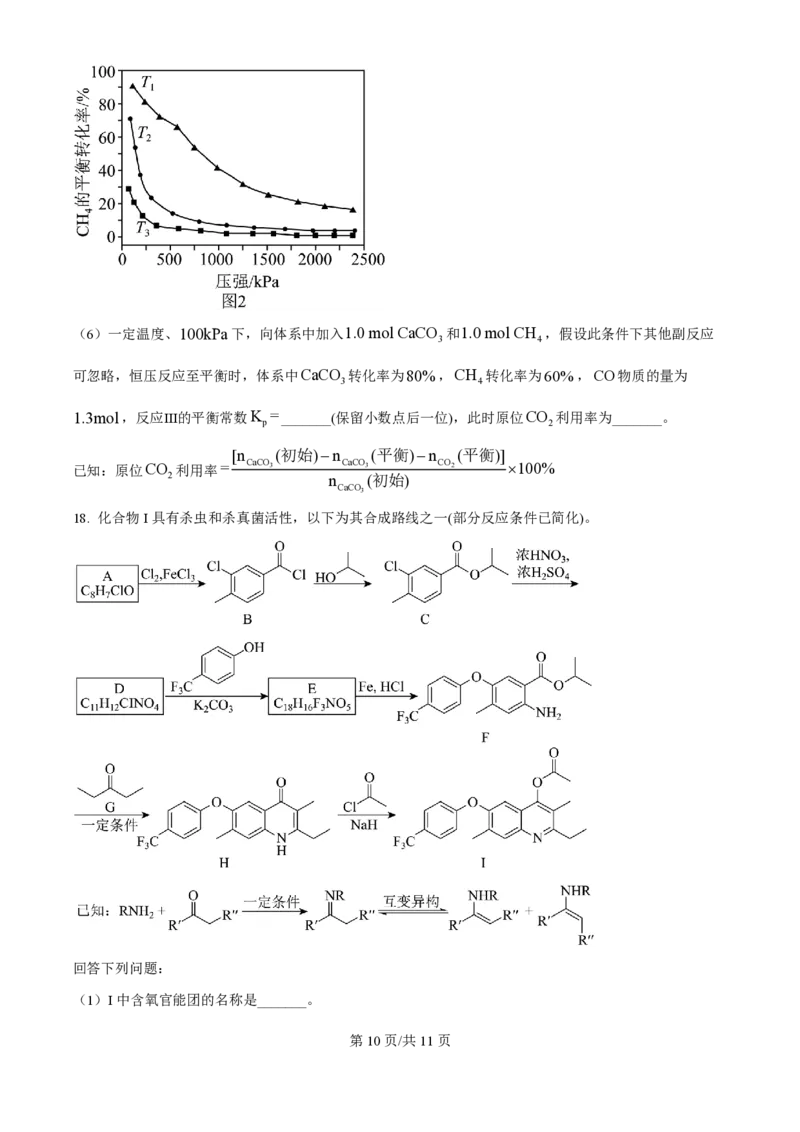
(5)在温度分别为T、T 和T 下,CH 的平衡转化率与压强的关系如图2所示,反应温度最高的是
1 2 3 4
_______(填“T ”“T ”或“T ”),原因是_______。
1 2 3
第9页/共11页
学科网(北京)股份有限公司(6)一定温度、100kPa下,向体系中加入1.0 mol CaCO 和1.0 mol CH ,假设此条件下其他副反应
3 4
可忽略,恒压反应至平衡时,体系中CaCO 转化率为80%,CH 转化率为60%,CO物质的量为
3 4
1.3mol,反应Ⅲ的平衡常数K =_______(保留小数点后一位),此时原位CO 利用率为_______。
p 2
[n (初始)-n (平衡)-n (平衡)]
已知:原位CO 利用率= CaCO 3 CaCO 3 CO 2 ´100%
2 n (初始)
CaCO
3
18. 化合物I具有杀虫和杀真菌活性,以下为其合成路线之一(部分反应条件已简化)。
回答下列问题:
(1)I中含氧官能团的名称是_______。
第10页/共11页
学科网(北京)股份有限公司(2)A的结构简式为_______。
(3)由B生成C的化学方程式为_______。反应时,在加热搅拌下向液体B中滴加异丙醇;若改为向异
丙醇中滴加B则会导致更多副产物的生成,副产物可能的结构简式为_______(写出一种即可)。
(4)由D生成E的反应类型为_______。
(5)由F生成H的反应中可能生成中间体J,已知J的分子式为C H FNO ,则J的结构简式为
23 26 3 3
_______(写出一种即可)。
(6)G的同分异构体中,含有碳氧双键的还有_______种(不考虑立体异构);其中,能发生银镜反应,且
核磁共振氢谱显示为两组峰的同分异构体的结构简式为_______。
第11页/共11页
学科网(北京)股份有限公司