文档内容
第一章 原子结构与性质
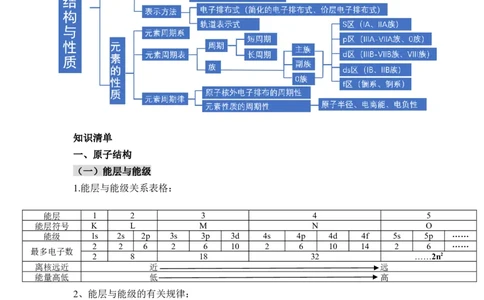
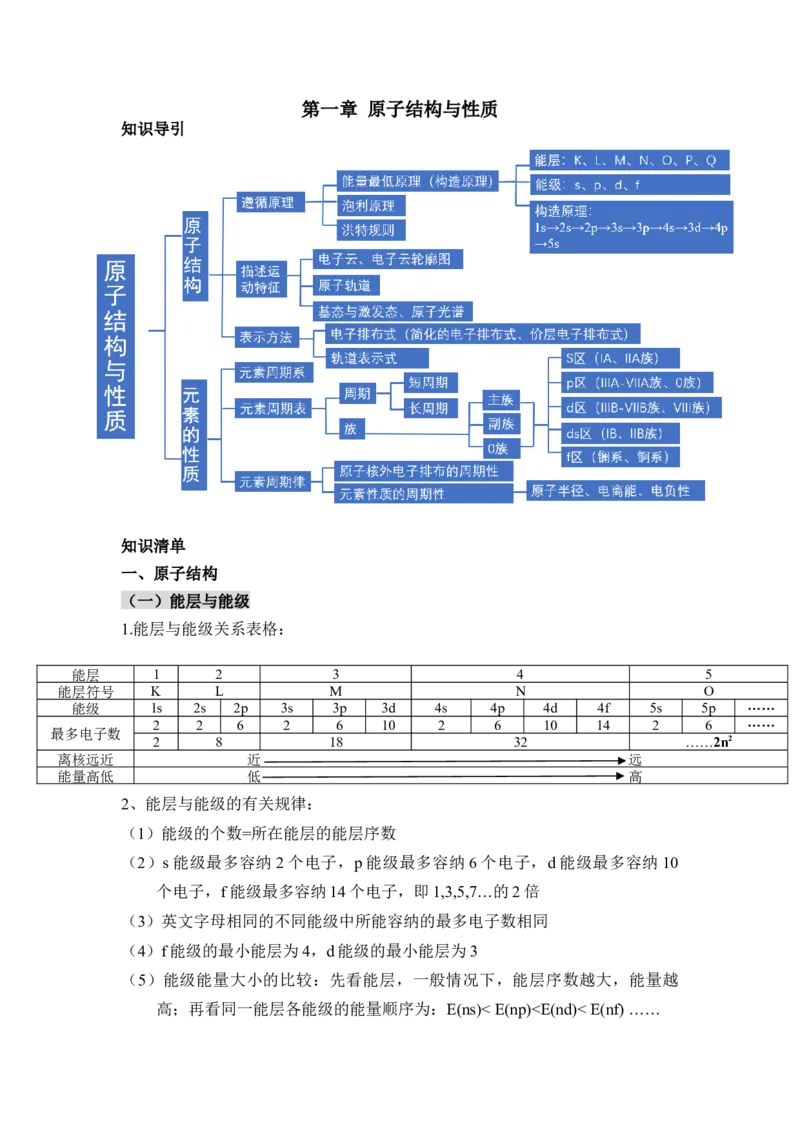
知识导引
知识清单
一、原子结构
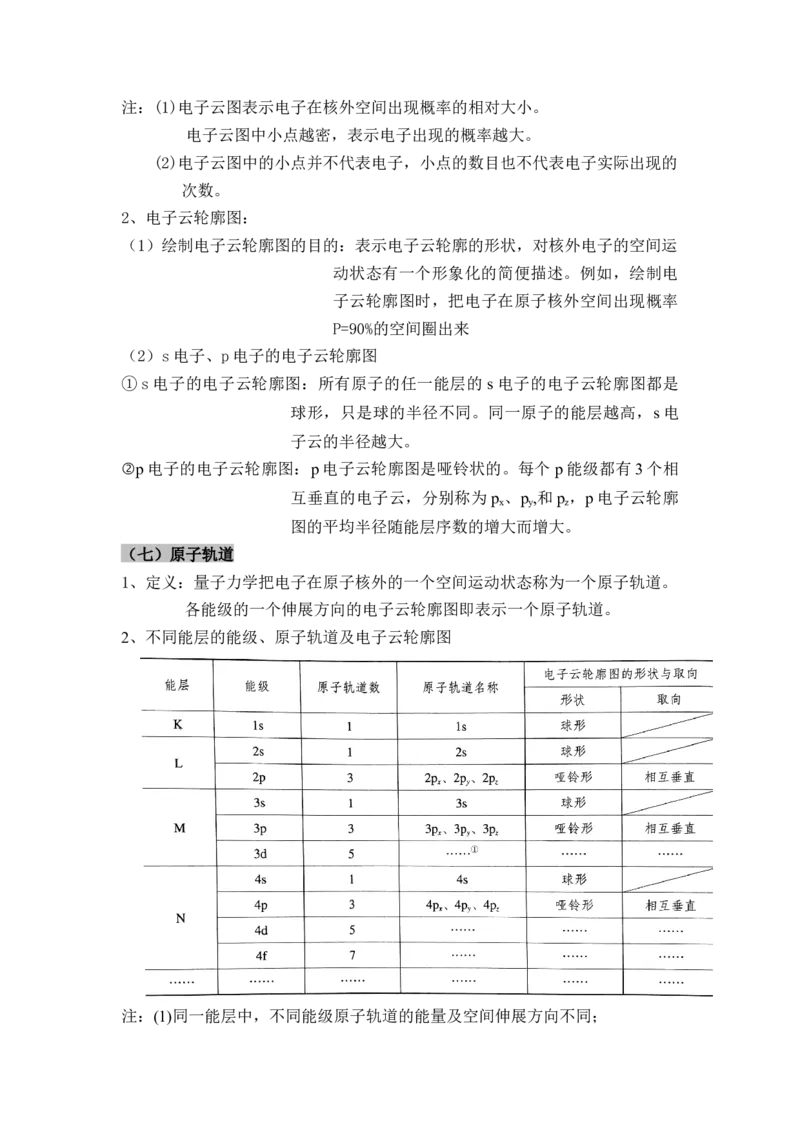
(一)能层与能级
1.能层与能级关系表格:
能层 1 2 3 4 5
能层符号 K L M N O
能级 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p ……
2 2 6 2 6 10 2 6 10 14 2 6 ……
最多电子数
2 8 18 32 ……2n2
离核远近 近 远
能量高低 低 高
2、能层与能级的有关规律:
(1)能级的个数=所在能层的能层序数
(2)s能级最多容纳 2个电子,p能级最多容纳 6个电子,d能级最多容纳 10
个电子,f能级最多容纳14个电子,即1,3,5,7…的2倍
(3)英文字母相同的不同能级中所能容纳的最多电子数相同
(4)f能级的最小能层为4,d能级的最小能层为3
(5)能级能量大小的比较:先看能层,一般情况下,能层序数越大,能量越
高;再看同一能层各能级的能量顺序为:E(ns)< E(np)1) 2或8 为原子轨道全充满的稳定结构
(三)元素周期表的分区
1.按电子排布分区:各区元素原子的价层电子排布、元素的位置及类别
分
元素位置 价层电子排布式 元素种类及性质特点
区
原子的核外电子最后排布在 ns 能级
s区 IA族、ⅡA族 ns1-2 上,属于活泼金属元素(H除外),为碱金
属元素和碱土金属元素
原子的核外电子最后排布在 np 能级
ⅢA~ⅦA族及0
p区 ns2np1-6(He除外) (He为s能级)上,为非金属元素和少数
族
金属元素
ⅢB~ⅦB族(镧 为过渡金属元素,原子的核外电子最
d区 系、锕系除外) (n-1)d1-9ns1-2(Pd除外) 后排布在(n-1)d能级上,d轨道可以不
以及Ⅷ族 同程度地参与化学键的形成
为过渡金属元素,核外电子先填满
ds (n-1)d能级而后再填充ns能级,由于d
IB族、ⅡB族 (n-1)d10ns1-2
区 轨道已填满电子,因此d轨道一般不
参与化学键的形成
镧系元素化学性质相似;锕系元素化
f区 镧系和锕系 (n-2)f0-14(n-1)d0-2ns2
学性质相似
2.按金属元素与非金属元素分区
(1)金属元素、非金属元素在元素周期表中的位置
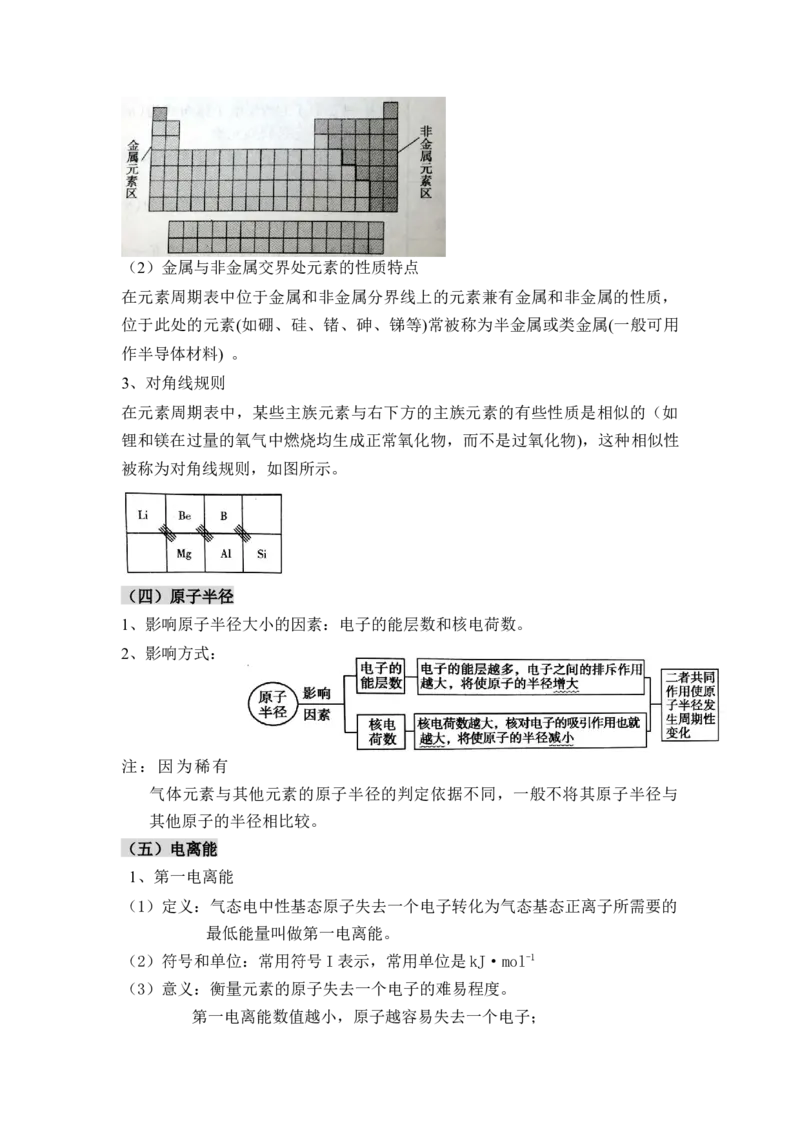
沿着周期表中硼、硅、砷、碲、砹、与铝、锗、锑、钋、之间画一条线,线的
左边是金属元素(氢除外),线的右边是非金属元素。非金属元素要集中在元素周
期表右上角的三角区内(如图)。(2)金属与非金属交界处元素的性质特点
在元素周期表中位于金属和非金属分界线上的元素兼有金属和非金属的性质,
位于此处的元素(如硼、硅、锗、砷、锑等)常被称为半金属或类金属(一般可用
作半导体材料) 。
3、对角线规则
在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的(如
锂和镁在过量的氧气中燃烧均生成正常氧化物,而不是过氧化物),这种相似性
被称为对角线规则,如图所示。
(四)原子半径
1、影响原子半径大小的因素:电子的能层数和核电荷数。
2、影响方式:
注:因为稀有
气体元素与其他元素的原子半径的判定依据不同,一般不将其原子半径与
其他原子的半径相比较。
(五)电离能
1、第一电离能
(1)定义:气态电中性基态原子失去一个电子转化为气态基态正离子所需要的
最低能量叫做第一电离能。
(2)符号和单位:常用符号I表示,常用单位是kJ·mol-1
(3)意义:衡量元素的原子失去一个电子的难易程度。
第一电离能数值越小,原子越容易失去一个电子;第一电离能数值越大,原子越难失去一个电子。
(4)变化规律
①一般规律:同周期:随原子序数的递增而增大;
同周期中,第一电离能最小的是第一主族的元素,
最大的是稀有气体元素;
第一电离能最大的元素是氦。
同主族:随原子序数的递增而减小。
②特例:具有全充满、半充满及全空的电子构型的原子稳定性较高,其电离能
数值较大。
例如:第IIA族>第IIIA族; 第VA族>第VIA族
③过渡元素的第一电离能的变化不太规则,同周期元素中随着元素原子核电荷
数的增加,第一电离能略有增加。
2、逐级电离能
(1)含义:原子的+1价气态基态离子再失去1个电子所需要的最低能量叫做第
二电离能,依次类推。
(2)变化规律
①同一元素的逐级电离能是逐渐增大的,即I < I < I <…
1 2 3
②当相邻逐级电离能突然变大时,说明失去的电子所在电子层发生了变化
3、电离能的应用
(1)推断元素原子的核外电子排布
例如:Li的逐级电离能I 《 I < I ,表明Li原子核外的三个电子排布在两个能
1 2 3
层(K、L能层)上,且最外层上只有一个电子。
(2)判断主族元素的最高正化合价或最外层电子数
如果电离能在I 与I 之间发生突变,则元素的原子易形成+n价离子而不易形
n n+1
成+(n+1)价离。如果是主族元素,则其最外层有 n 个电子,最高正化合价为
+n(O、F除外)。
(3)判断元素的金属性、非金属性强弱
I 越大,元素的非金属性越强(稀有气体元素除外); I 越小,元素的金属性越
1 1
强。
(六)电负性
1、键合电子: 元素相互化合时,原子中用于形成化学键的电子称为键合电子
2、电负性
(1)定义:用来描述不同元素的原子对键合电子吸引力的大小
(2)意义:电负性越大的原子,对键合电子的吸引力越大。(3)大小的标准:以氟的电负性为4.0和锂的电负性为1.0作为相对标准,得
出各元素的电负性。
(4)变化规律:一般来说,同周期元素从左到右,元素的电负性逐渐变大;
同族元素从上到下,元素的电负性逐渐变小。
金属元素的电负性较小,非金属元素的电负性较大。
电负性最大的是氟,最小的是铯
(5)应用
①判断元素的金属性或非金属性强弱
I、金属元素的电负性一般小于1.8,非金属元素的电负性一般大1.8,而位于非
金属三角区边界的“类金属”(如锗、锑等)的电负性则在1.8左右,它们既有
金属性,又有非金属性。
注:不能把电负性1.8作为划分金属元素和非金属元素的绝对标准
II、金属元素的电负性越小,金属元素越活泼;非金属元素的电负性越大,非
金属元素越活泼。
②判断化学键的类型
I、如果两种成键元素的电负性差值大于 1.7,它们之间通常形成离子键,但也
有特例(如HF)。
II、如果两种成键元素的电负性差值小于1.7,它们之间通常形成共价键, 但也
有特例(如NaH)。
③判断元素的化合价
I、电负性小的元素易呈现正价
II、电负性大的元素易呈现负价
④解释对角线规则
利用电负性可以解释对角线规则,如 Li-Mg、Be-Al、B-Si,由于它们的电负性
分别接近,对键合电子的吸引力相当,故表现出相似的性质。
(6)电负性与第一电离能的关系
电负性用于衡量原子吸引键合电子的能力,电负性大的原子吸引电子的能力
强,所以一般来说,电负性大的原子对应元素的第一电离能也大。
例题1:依诺沙星具有广谱的抗菌作用,尤其是对需氧的革兰氏阴性杆菌的抗
菌活性比较好,可用于敏感细菌引起的感染。下列关于依诺沙星涉及的元素
C、N、O、F的说法错误的是( )
A.第一电离能:F>O>N>C
B.电负性:F>O>N>C
C.稳定性:HF>H O>NH >CH
2 3 4D.原子半径:C>N>O>F
【答案】A
【解析】第VA族元素原子的最外层电子排布式为ns2np3,为半充满的稳定结
构,第一电离能大于同周期相邻元素,故第一电离能:F>N>O>C,A项错误;电
负性:F>O>N>C,B项正确;电负性越大,元素的非金属性越强,其简单氢化物
越稳定,C项正确;同周期主族元素从左到右,原子半径逐渐减小,故原子半
径:C>N>O>F,D项正确。。
例题2:如图为元素周期表中短周期的一部分,下列关于Y、Z、M的说法正确
的是( )
A.电负性:Y>Z>M
B.半径:M->Z2->Y-
C.原子半径:ZM>Z
【答案】D
【解析】由图示关系可知,X为He元素,Y为F元素,M为Cl元素,Z为硫元
素。A项,一般来说,同周期主族元素从左到右,电负性逐渐增大,同主族元
素从上到下,电负性逐渐减小,元素的电负性:F>C1>S,错误;B项,核外电子
排布相同的离子,核电荷数越大,离子半径越小,离子半径:S2->Cl->F-,错误;
C项,同周期主族元素从左到右,原子半径逐渐减小,原子半径:S>Cl,错误;
D项,第一电离能:F>Cl>S,正确。
例题3:根据表中所列五种9元素的第一至第四电离能数据(单位:kJ·mol-1),回
答下列问题。
(1)在元素周期表中,最可能处于同一族的是 (填字母,下同)。
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)下列离子的氧化性最弱的是 。
A.S2+ B.R+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是 。A.硼 B.铍 C.氦 D.氢
4)上述元素会出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧
面说明: 。如果U
元
素是第四周期元素,请估计它的第2次电离能突跃将发生在失去第 个电子时
(5)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺
序是 ,其中S的第一电离能异常高的原因是
。
【答案】(1)E (2)D (3)C (4)电子分层排布,各能层能量不同 10
(5)R