文档内容
专练 10 氧化还原反应规律及应用
授课提示:对应学生用书19页
1.[2024·江苏淮安期中]室温下进行下列实验,根据实验操作和现象所得到的结论不正
确的是( )
选项 实验操作和现象 实验结论
A 向PbO 中滴加浓盐酸,出现黄绿色气体 PbO 具有氧化性
2 2
向KI溶液中滴加几滴NaNO 溶液,再滴加淀粉溶
B 2 NO的氧化性比I 的强
液后变蓝色 2
向FeSO 溶液中先滴加KSCN溶液,无明显现象,
C 4 Fe2+既有氧化性又有还原性
再滴加HO 溶液,溶液变成血红色
2 2
向KI溶液中滴入少量新制氯水和四氯化碳,振
D I-的还原性强于Cl-
荡、静置,溶液下层呈紫红色
答案:C
解析:Cl从-1价升高到0价,被氧化,PbO 具有氧化性,A项正确;滴加淀粉溶液
2
后变蓝色,说明有I 生成,可证明NO的氧化性比I 的强,B项正确;Fe2+遇KSCN溶液不
2 2
变红,Fe3+遇KSCN溶液变红,由此说明加入的HO 能使Fe2+氧化为Fe3+,则Fe2+是该反
2 2
应中的还原剂,只表现出还原性,不表现出氧化性,C项错误;新制氯水与KI反应生成
I,I 易溶于四氯化碳,则溶液下层呈紫红色,可知I-的还原性强于Cl-,D项正确。
2 2
2.[2024·辽宁朝阳期中]关于反应:KClO +6HCl===KCl+3HO+3Cl↑,用同位素
3 2 2
示踪法进行研究,反应前将KClO 标记为K37ClO ,HCl标记为H35Cl,下列说法正确的是(
3 3
)
A.反应后,37Cl全部存在于氯化钾中
B.产物氯气的摩尔质量为72 g·mol-1
C.在氯气和氯化钾中都含有37Cl
D.产物氯气中37Cl与35Cl的原子个数比为1∶5
答案:D
解析:反应KClO +6HCl===KCl+3HO+3Cl↑中,只有Cl元素化合价发生了变化,
3 2 2
根据氧化还原反应中“化合价只靠近不交叉”的原则可知,用双线桥法表示该反应中转移
电子的情况为
将KClO 标记为K37ClO ,37Cl应全部存在于氯气中,A、C错误;根据得失电子守恒
3 3
可知,产物氯气中37Cl与35Cl的原子个数比为1∶5,因此产物氯气的摩尔质量为 g·mol-
1≈70.67 g·mol-1,B错误、D正确。
3.[2024·哈尔滨师大附中高三考试]在混合体系中,确认化学反应先后顺序有利于问题
的解决,下列反应先后顺序判断正确的是( )
A.等物质的量的FeBr 、FeI 的溶液中缓慢通入Cl:I-、Fe2+、Br-
2 2 2B.等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:H+、Fe3+、Cu2+、Fe2+
C.等物质的量的 Ba(OH) 、KOH 的溶液中通入 CO :Ba(OH) 、KOH、BaCO 、
2 2 2 3
KCO
2 3
D.等物质的量的 AlO、OH-、CO 溶液中,逐滴加入盐酸:OH-、CO、AlO、
Al(OH)
3
答案:A
解析:在含等物质的量的FeBr 、FeI 的溶液中缓慢通入Cl ,氯气具有氧化性,先和
2 2 2
还原性强的离子反应,离子的还原性顺序:I->Fe2+>Br-,故A正确;在含等物质的量的
Fe3+、Cu2+、H+的溶液中加入Zn,金属锌先是和氧化性强的离子发生反应,离子的氧化性
顺序是:Fe3+>Cu2+>H+>Fe2+,故B错误;在含等物质的量的Ba(OH) 、KOH的溶液中
2
通入CO ,反应顺序为:Ba(OH) 、KOH、KCO 、BaCO ,故C错误;若H+先与CO反应,
2 2 2 3 3
生成二氧化碳,而二氧化碳与溶液中 AlO反应生成Al(OH) ,反应顺序为OH-、AlO、
3
CO、Al(OH) ,故D错误。
3
4.[情境创新]白金(Pt)性质稳定,难以参与一些反应,但白金能够溶解在王水(浓盐酸
与浓硝酸的混合物)中,生成HPtCl 、HO和NO。下列有关上述反应的说法正确的是(
2 6 2
)
A.该反应过程中,HNO 与HCl体现氧化性
3
B.每减少22 mol H+,有16 mol H—O键形成
C.转移3 mol电子时,可以生成22.4 L NO
D.氧化剂与氧化产物的物质的量之比为4∶3
答案:D
解析:根据题意,可以得出 Pt 和王水反应的化学方程式为 3Pt+4HNO +
3
18HCl===3H PtCl +4NO↑+8HO,HCl中各元素的化合价没有改变,所以 HCl没有体现
2 6 2
氧化性,A选项错误;每消耗4 mol HNO 和18 mol HCl,同时生成3 mol H PtCl 、4 mol
3 2 6
NO和8 mol H O,即有16 mol H—O键生成,因反应中有HPtCl 生成,故H+实际减少量
2 2 6
小于22 mol,B选项错误;转移3 mol电子时,可以生成标准状况下22.4 L NO,C选项错
误;氧化剂为HNO,氧化产物为HPtCl ,根据化学方程式可以得出D选项正确。
3 2 6
5.[情境创新]国家生态环境部召开新闻发布会,指出空气污染天数增加的重要原因是
全国臭氧浓度同比上升。测定空气中 O 含量的方法之一是:将含O 的空气通入足量的KI
3 3
溶液,O 与KI反应生成两种单质,然后将所得溶液用NaSO 标准溶液滴定,计算得出空
3 2 2 3
气中O 含量,滴定过程涉及的反应是2NaSO +I===Na SO +2NaI。下列判断不正确的
3 2 2 3 2 2 4 6
是( )
A.上述方法中涉及2个氧化还原反应
B.KI与O 反应生成O、I 两种氧化产物
3 2 2
C.加NaSO 标准溶液进行滴定时,可以淀粉为指示剂
2 2 3
D.滴定反应中转移0.5 mol电子,则吸收5.6 L(标准状况)O
3
答案:B
解析:该测定O 的方法中涉及2个反应:HO+O +2KI===O +I +2KOH,2NaSO
3 2 3 2 2 2 2 3
+I===Na SO+2NaI,通过反应前后元素化合价变化,可知上述反应均为氧化还原反应,
2 2 4 6
A项正确;上述第1个反应中O 既不是氧化产物,也不是还原产物,I 是氧化产物,KOH
2 2
是还原产物,B项错误;I 遇淀粉变蓝,可用淀粉作该滴定反应的指示剂,C项正确;由上
2
述两个反应的化学方程式可知,存在关系式 O ~I ~2NaI,故转移2 mol电子,则吸收了1
3 2
mol O,即转移0.5 mol电子,则吸收了0.25 mol(标准状况下5.6 L) O ,D项正确。
3 3
6.[2024·皖中名校联盟高三第一次联考]现有下列三个氧化还原反应:① 2B-+Z===B +2Z-②2A2++B ===2A3++2B- ③2XO+10Z-+16H+===2X2++5Z +8HO,
2 2 2 2 2
根据上述反应,判断下列结论中正确的是( )
A.要除去含有A2+、Z-和B-混合溶液中的A2+,而不氧化Z-和B-,应加入B
2
B.氧化性强弱顺序为:XO>Z >A3+>B
2 2
C.X2+是XO的氧化产物,B 是B-的还原产物
2
D.在溶液中不可能发生反应:XO+5A2++8H+===X2++5A3++4HO
2
答案:A
解析:根据①知,氧化性:Z>B ,根据②知,氧化性:B >A3+,根据③知,氧化性:
2 2 2
XO>Z ,所以氧化性关系为:XO>Z >B >A3+,所以要除去含有A2+、Z-和B-混合溶液中
2 2 2
的A2+,而不氧化Z-和B-,应加入B ,A正确,B错误;X2+是XO的还原产物,B 是B-
2 2
的氧化产物,C错误;因为氧化性关系为:XO>Z >B >A3+,在溶液中可能发生反应:XO
2 2
+5A2++8H+===X2++5A3++4HO,D错误。
2
7.已知酸性:HCO >HClO>HCO,氧化性:HClO>Cl >Br >Fe3+>I ,下列有关
2 3 2 2 2
离子反应或离子方程式的叙述中,正确的是( )
A.能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、I-能大量共存
B.向溴水中加入足量氯化亚铁溶液能使溶液变成无色
C.向NaClO溶液中通入少量二氧化碳的离子方程式:ClO-+CO +HO===HClO+
2 2
HCO
D.向FeI 溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl===2Fe3++2Cl-
2 2
答案:C
解析:因氧化性:Fe3+>I ,则Fe3+能将I-氧化生成I ,故A错误;溴水能将亚铁离
2 2
子氧化成铁离子,溶液呈黄色,故B错误;因酸性:HCO>HClO>HCO,则向NaClO溶
2 3
液中通入少量二氧化碳生成的盐为NaHCO ,离子方程式为:ClO-+CO +HO===HClO+
3 2 2
HCO,故C正确;因还原性:I->Fe2+,则向FeI 溶液中滴加少量氯水时,I-先被氧化,
2
故D错误。
8.氯酸是一种强酸,浓度超过40%时会发生分解,该反应可表示为aHClO―→bO↑
3 2
+cCl↑+dHClO+eHO,下列有关说法不正确的是( )
2 4 2
A.由反应可确定氧化性:HClO>O
3 2
B.由非金属性:Cl>S,可推知酸性:HClO>H SO
3 2 4
C.若氯酸分解所得 1 mol混合气体的质量为 45 g,则反应的化学方程式可表示为
3HClO===2O ↑+Cl↑+HClO+HO
3 2 2 4 2
D.若化学计量数a=8,b=3,则生成3 mol O 时该反应转移20 mol电子
2
答案:B
解析:根据非金属性只能比较最高价含氧酸的酸性强弱,故B错误。
9.[情境创新]当今环境保护越来越受重视,某化工集团为减少环境污染,提高资源的
利用率,将钛厂、氯碱厂、甲醇厂进行联合生产。其主要生产工艺如下:
下列叙述正确的是( )
A.该流程中的“电解”“氯化”“合成”均涉及氧化还原反应B.“氯化”时每消耗12 g焦炭,则转移2 mol电子
C.“合成”反应中氧化剂与还原剂的物质的量之比为2∶1
D.上述流程中“Mg,Ar”可用“Mg,CO”代替
2
答案:A
解析:分析流程图中的物质转化,“电解”“氯化”“合成”中均有单质参与反应或
生成,故均涉及氧化还原反应,A项正确;“氯化”时还原剂包括焦炭和FeTiO ,故B项
3
错误;“合成”反应的化学方程式为CO+2H―→CHOH,故氧化剂与还原剂的物质的量
2 3
之比为1∶2,C项错误;800 ℃条件下,CO 与Mg反应,D项错误。
2
10.已知2Fe3++2I-===I +2Fe2+、2Fe2++Br ===2Br-+2Fe3+。现向含FeBr 、FeI 的
2 2 2 2
溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的 KSCN溶液,结果溶液变为红
色,则下列叙述中正确的是( )
①氧化性:Br >Fe3+>I ②原溶液中Br-一定被氧化 ③通入氯气后,原溶液中的Fe2
2 2
+一定被氧化 ④不能确定通入氯气后的溶液中是否还存在Fe2+ ⑤若取少量所得溶液,
加入CCl 后静置,向上层溶液中加入足量的AgNO 溶液,只产生白色沉淀,说明原溶液中
4 3
Fe2+、Br-均被完全氧化
A.①②③④ B.①③④⑤
C.②④⑤ D.①②③④⑤
答案:B
解析:由已知的两个化学方程式及同一个反应中氧化剂的氧化性大于氧化产物的氧化
性可知,氧化性Fe3+>I 、Br >Fe3+,故①正确;向溶液中滴加KSCN溶液变为红色说明溶
2 2
液中含有Fe3+,则说明溶液中无I-存在,又氧化性Cl>Br >Fe3+>I ,氯气的量不确定,则
2 2 2
Br-不一定被氧化,故②错误,③正确;由上述分析可知溶液中存在Fe3+,但不能确定是
否所有的Fe2+均被氧化为Fe3+,故④正确;上层溶液中若含Br-,则产生淡黄色沉淀,若
含I-,则产生黄色沉淀,由题知只产生白色沉淀,则说明溶液中含 Cl-,即溶液中的Fe2
+、Br-均被完全氧化,故⑤正确。
11.已知:
下列说法中正确的是( )
A.上述转化说明还原性:I->NaSO>Br-
2 2 3
B.每生成1 mol IO,同时消耗2.5 mol Br
2
C.生成I 的反应中氧化剂与还原剂的物质的量之比为1∶5
2
D.有氧化产物Br-生成
答案:C
解析:由①I-(样品)――→IO可得还原性:I->Br-,再由②I――→I-可得还原性:
2
NaSO>I-,则还原性:NaSO>I->Br-,A错误;由得失电子守恒可知,每生成1 mol
2 2 3 2 2 3
IO,消耗3 mol Br ,B错误;生成I 的反应为IO+5I-+6H+===3I +3HO,则氧化剂与还
2 2 2 2
原剂的物质的量之比为1∶5,C正确;Br-是还原产物,D错误。
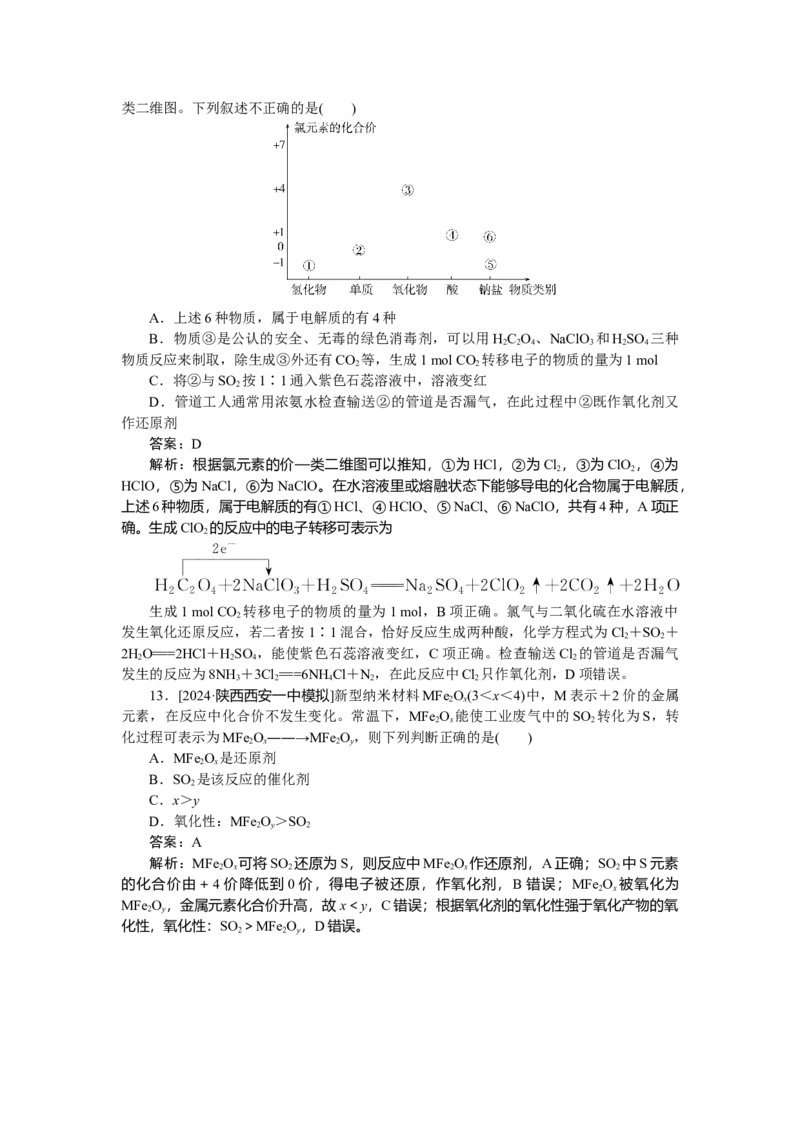
12.[2024·辽宁名校联盟联考]价—类二维图是学习元素及其化合物知识的重要模型。
它是以元素化合价为纵坐标,以物质类别为横坐标的二维平面图像。如图为氯元素的价—类二维图。下列叙述不正确的是( )
A.上述6种物质,属于电解质的有4种
B.物质③是公认的安全、无毒的绿色消毒剂,可以用HC O 、NaClO 和HSO 三种
2 2 4 3 2 4
物质反应来制取,除生成③外还有CO 等,生成1 mol CO 转移电子的物质的量为1 mol
2 2
C.将②与SO 按1∶1通入紫色石蕊溶液中,溶液变红
2
D.管道工人通常用浓氨水检查输送②的管道是否漏气,在此过程中②既作氧化剂又
作还原剂
答案:D
解析:根据氯元素的价—类二维图可以推知,①为HCl,②为Cl ,③为ClO ,④为
2 2
HClO,⑤为NaCl,⑥为NaClO。在水溶液里或熔融状态下能够导电的化合物属于电解质,
上述6种物质,属于电解质的有①HCl、④HClO、⑤NaCl、⑥NaClO,共有4种,A项正
确。生成ClO 的反应中的电子转移可表示为
2
生成1 mol CO 转移电子的物质的量为1 mol,B项正确。氯气与二氧化硫在水溶液中
2
发生氧化还原反应,若二者按1∶1混合,恰好反应生成两种酸,化学方程式为Cl+SO +
2 2
2HO===2HCl+HSO ,能使紫色石蕊溶液变红,C项正确。检查输送Cl 的管道是否漏气
2 2 4 2
发生的反应为8NH +3Cl===6NHCl+N,在此反应中Cl 只作氧化剂,D项错误。
3 2 4 2 2
13.[2024·陕西西安一中模拟]新型纳米材料MFe O(3<x<4)中,M表示+2价的金属
2 x
元素,在反应中化合价不发生变化。常温下,MFe O 能使工业废气中的SO 转化为S,转
2 x 2
化过程可表示为MFe O――→MFe O,则下列判断正确的是( )
2 x 2 y
A.MFe O 是还原剂
2 x
B.SO 是该反应的催化剂
2
C.x>y
D.氧化性:MFe O>SO
2 y 2
答案:A
解析:MFe O 可将SO 还原为S,则反应中MFe O 作还原剂,A正确;SO 中S元素
2 x 2 2 x 2
的化合价由+4价降低到 0价,得电子被还原,作氧化剂,B错误;MFe O 被氧化为
2 x
MFe O,金属元素化合价升高,故x<y,C错误;根据氧化剂的氧化性强于氧化产物的氧
2 y
化性,氧化性:SO >MFe O,D错误。
2 2 y