文档内容
专练 16 碳、硅及其化合物新型无机非金属材料
授课提示:对应学生用书31页
一、选择题
1.[2022·辽宁卷]北京冬奥会备受世界瞩目。下列说法错误的是( )
A.冰壶主材料花岗岩属于无机非金属材料
B.火炬“飞扬”使用的碳纤维属于有机高分子材料
C.冬奥会“同心”金属奖牌属于合金材料
D.短道速滑服使用的超高分子量聚乙烯属于有机高分子材料
答案:B
解析:花岗岩的主要成分是石英、云母、长石等矿物,属于无机非金属材料,A正确;
碳纤维指的是含碳量在90%以上的高强度高模量纤维,属于无机非金属材料,B错误;金
属奖牌属于合金材料,C正确;聚乙烯属于有机高分子材料,D正确。
2.[2022·广东卷]广东一直是我国对外交流的重要窗口,馆藏文物是其历史见证。下列
文物主要由硅酸盐制成的是( )
文物
选项 A.南宋鎏金饰品 B.蒜头纹银盒
文物
选项 C.广彩瓷咖啡杯 D.铜镀金钟座
答案:C
解析:鎏金饰品属于金属材料,A项错误;纹银盒的主要成分是银,B项错误;瓷质
咖啡杯的主要成分是陶瓷,属于硅酸盐材料,C项正确;铜镀金钟座的主要成分是合金,
D项错误。
3.[2024·吉林东北师大附中一模]“中国名片”有中国航天、军事、天文等,这些领域
的发展受到全世界瞩目,而这些领域与化学有着密切的联系。下列说法不正确的是
( )A.“天宫二号”空间实验室的硅电池板将光能直接转化为电能
B.“蛟龙”号潜水器所使用的钛合金材料具有强度大、密度小、耐腐蚀等特性
C.5G技术的应用离不开光缆,我国光缆线路总长度超过了三千万千米,光缆的主要成
分是晶体硅
D.港珠澳大桥设计使用寿命120年,水下钢柱镶锌块是利用牺牲阳极的阴极保护法防
腐蚀
答案:C
解析:“天宫二号”空间实验室的硅电池板是为空间实验室提供电能的装置,可以将
光能转化为电能,A正确;“蛟龙”号潜水器所使用的钛合金是合金材料,具有强度大、
密度小、耐腐蚀、耐热等特性,B正确;光缆的主要成分是二氧化硅,C错误;水下钢柱
镶锌块,铁和锌在水中形成原电池,锌作负极被腐蚀,铁作正极被保护,利用的是牺牲阳
极的阴极保护法,D正确。
4.[2022·河北卷]定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的
是( )
A.传统陶瓷是典型的绝缘材料
B.陶瓷主要成分为SiO 和MgO
2
C.陶瓷烧制的过程为物理变化
D.白瓷的白色是因铁含量较高
答案:A
解析:传统陶瓷是典型的绝缘材料,常用于高压变压器的开关外包装和器件,A正确;
陶瓷的主要成分为硅酸盐,而不是SiO 和MgO,B错误;陶瓷烧制过程发生复杂的化学反
2
应,有新物质生成,属于化学变化,C错误;由于Fe2+、Fe3+和铁的氧化物均有颜色,白
瓷的白色是因为铁含量较低甚至几乎不含,D错误。
5.[2024·云南昆明摸底]在海洋碳循环中,通过如图所示的途径固定碳。下列说法错误
的是( )
A.该循环过程中未涉及氧化还原反应
B.光合作用能将太阳能转化为化学能
C.钙化作用涉及的离子方程式之一为
Ca2++2HCO===CaCO ↓+CO↑+HO
3 2 2
D.吸收作用中产生HCO的途径为CO
2
+H
2
O⇌H
2
CO
3
,H
2
CO 3⇌HCO+H+
答案:A
解析:光合作用中,利用太阳能将二氧化碳、水转化为(CHO) 和O ,发生的是氧
2 n 2
化还原反应,A项错误;由图可知,光合作用将太阳能转化为化学能,B项正确;NaHCO
3
和NaCO 与CaCl 发生的离子反应分别为Ca2++2HCO===CaCO ↓+CO↑+HO、Ca2+
2 3 2 3 2 2
+CO===CaCO
3
↓,C 项正确;二氧化碳溶于水,发生反应:CO
2
+H
2
O⇌H
2
CO
3
,
H
2
CO 3⇌H++HCO,D项正确。
6.工业上利用无机矿物资源生产部分材料的流程示意图如下。下列说法正确的是 (
)A.在铝土矿制备较高纯度Al的过程中只用到NaOH溶液、CO 气体、冰晶石
2
B.石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C.在制粗硅时,氧化剂与还原剂的物质的量之比为1∶2
D.黄铜矿(CuFeS)与O 反应产生的Cu S、SO 均是还原产物
2 2 2 2
答案:C
解析:在铝土矿制备较高纯度Al的过程中除用到NaOH溶液、CO 气体、冰晶石,还
2
用到盐酸,A 错误;石英不属于盐,不能与盐酸反应,B 错误;由方程式 SiO +
2
2C=====Si+2CO↑可知在制粗硅时,氧化剂与还原剂的物质的量之比为1∶2,C正确;
SO 是氧化产物,D错误。
2
7.下列说法正确的是( )
①N95口罩对新型冠状病毒有明显阻隔作用,其主要生产原料聚丙烯属于新型无机非
金属材料
②硅酸可用于制备硅胶,硅胶可用作袋装食品、瓶装药品的干燥剂
③Mg2+、H+、SiO、SO在水溶液中能大量共存
④向含有K+、Na+、Br-、SiO的溶液中通入CO 后各离子仍能大量存在
2
⑤SiO 不与任何酸反应,可用石英制造耐酸容器
2
⑥硅酸钠可制备木材防火剂,也可用于制备硅酸胶体
⑦Si→SiO→HSiO 均能一步转化
2 2 3
A.①⑤⑥ B.①②⑥⑦
C.②⑥ D.③④⑥
答案:C
解析:聚丙烯是有机高分子材料,①错误;硅胶具有较强的吸水性,且无毒,可作干
燥剂,②正确;H+与SiO会生成HSiO 沉淀,不能大量共存,③错误;向含有K+、Na
2 3
+、Br-、SiO的溶液中通入CO ,会生成HSiO 沉淀,④错误;SiO 可与氢氟酸反应,⑤
2 2 3 2
错误;硅酸钠具有较好的耐热性,可制备木材防火剂,也可用于制备硅酸胶体,⑥正确;
SiO→HSiO 不能一步实现转化,⑦错误。
2 2 3
8.[2023·湖北卷]工业制备高纯硅的主要过程如下:
石英砂――→粗硅――→SiHCl ――→高纯硅
3
下列说法错误的是( )
A.制备粗硅的反应方程式为
SiO+2C=====Si+2CO↑
2
B.1 mol Si含Si—Si键的数目约为4×6.02×1023C.原料气HCl和H 应充分去除水和氧气
2
D.生成SiHCl 的反应为熵减过程
3
答案:B
解析:SiO 和C在高温下发生反应生成 Si和CO,因此,制备粗硅的反应方程式为
2
SiO +2C=====Si+2CO↑,A说法正确;在晶体硅中,每个Si与其周围的4个Si形成共
2
价键并形成立体空间网状结构,因此,平均每个Si形成2个共价键,1 mol Si含Si—Si键
的数目约为2×6.02×1023,B说法错误;HCl易与水形成盐酸,在一定的条件下氧气可以
将HCl氧化;H 在高温下遇到氧气能发生反应生成水,且其易燃易爆,其与SiHCl 在高温
2 3
下反应生成硅和HCl,因此,原料气HCl和H 应充分去除水和氧气 ,C说法正确;Si+
2
3HCl(g)=====SiHCl (g)+H (g),该反应是气体分子数减少的反应,因此,生成
3 2
SiHCl 的反应为熵减过程,D说法正确;综上所述,本题选B。
3
9.[2024·广州市综合测试]化学推动科技进步。下列说法不正确的是( )
A.祝融号探测器发现火星上存在橄榄石(MgFe SiO),其成分属于无机化合物
x 2-x 4
B.天和核心舱电推进系统中使用的氮化硼陶瓷,其属于新型无机非金属材料
C.奋斗者号载人潜水器球壳,其原料中的46Ti与47Ti互为同位素
D.月壤样品中发现天然玻璃纤维,该纤维中的SiO 属于分子晶体
2
答案:D
解析:SiO 属于共价晶体,D项错误。
2
10.多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池等的主要原料。已知多
晶硅第三代工业制取流程如图所示:
下列说法错误的是( )
A.Y、Z分别为H、Cl
2 2
B.制取粗硅时焦炭与石英发生副反应生成碳化硅,该副反应中,氧化剂与还原剂的物
质的量之比为1∶2
C.SiHCl 极易水解,产物为HSiO、H、HCl,据此推测SiHCl 中硅为+2价
3 2 3 2 3
D.多晶硅是硅的一种同素异形体
答案:C
解析:电解饱和食盐水得到NaOH、H 、Cl ,Y和Z点燃下能够发生反应,即X为
2 2
NaOH,根据流程中,SiHCl 被还原成Si,即Y为H ,Z为Cl ,故A说法正确;焦炭和石
3 2 2
英发生的副反应:SiO +3C=====SiC+2CO↑,焦炭既是氧化剂又是还原剂,氧化剂与还
2
原剂物质的量之比为1∶2,故B说法正确;SiHCl 水解的产物是HSiO 、H 、HCl,推出
3 2 3 2
SiHCl 中H应为-1价,即Si的化合价为+4价,故C说法错误;多晶硅为单质,是硅的
3
一种同素异形体,故D说法正确。
二、非选择题
11.Ⅰ.在工业中加热条件下利用镁制取硅:2Mg+SiO=====2MgO+Si,同时有副反应
2
发生:2Mg+Si=====MgSi,MgSi遇盐酸迅速反应生成SiH (硅烷),SiH 在常温下是
2 2 4 4
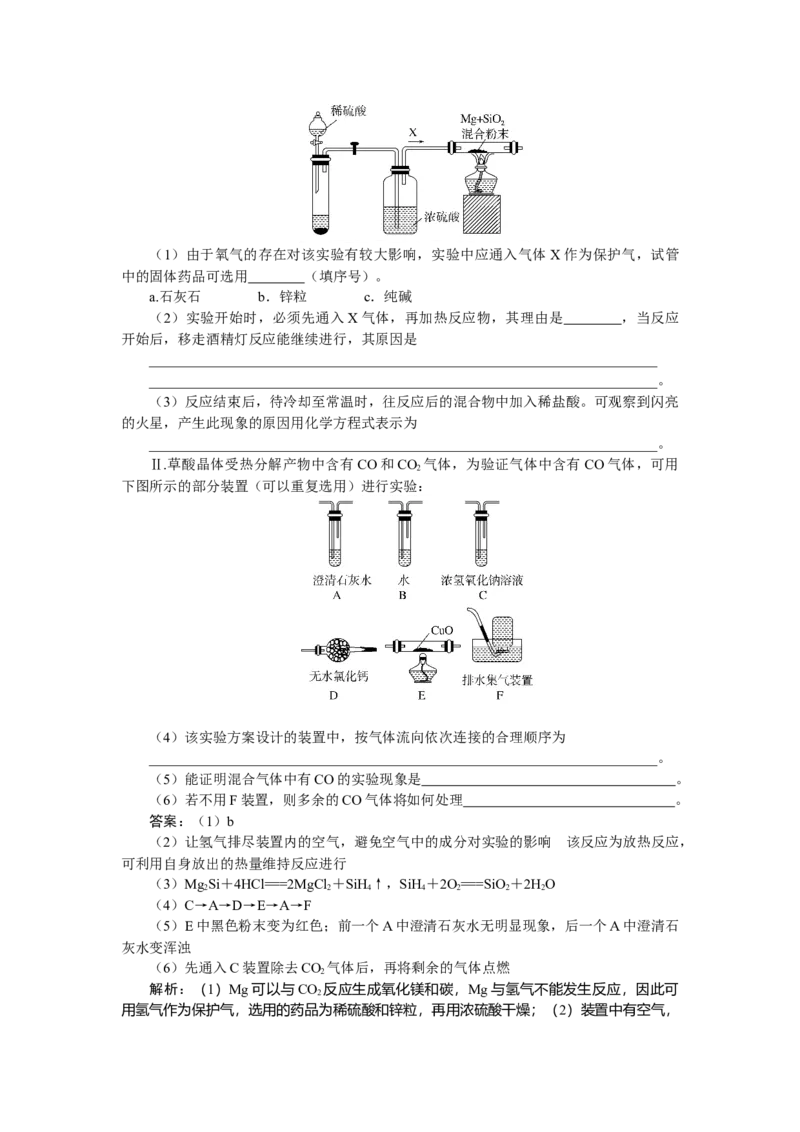
一种不稳定、易分解的气体。如图是进行Mg与SiO 反应的实验装置:
2(1)由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管
中的固体药品可选用 (填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通入X气体,再加热反应物,其理由是 ,当反应
开始后,移走酒精灯反应能继续进行,其原因是
________________________________________________________________________
________________________________________________________________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸。可观察到闪亮
的火星,产生此现象的原因用化学方程式表示为
________________________________________________________________________。
Ⅱ.草酸晶体受热分解产物中含有CO和CO 气体,为验证气体中含有CO气体,可用
2
下图所示的部分装置(可以重复选用)进行实验:
(4)该实验方案设计的装置中,按气体流向依次连接的合理顺序为
________________________________________________________________________。
(5)能证明混合气体中有CO的实验现象是 。
(6)若不用F装置,则多余的CO气体将如何处理 。
答案:(1)b
(2)让氢气排尽装置内的空气,避免空气中的成分对实验的影响 该反应为放热反应,
可利用自身放出的热量维持反应进行
(3)MgSi+4HCl===2MgCl +SiH↑,SiH+2O===SiO +2HO
2 2 4 4 2 2 2
(4)C→A→D→E→A→F
(5)E中黑色粉末变为红色;前一个A中澄清石灰水无明显现象,后一个A中澄清石
灰水变浑浊
(6)先通入C装置除去CO 气体后,再将剩余的气体点燃
2
解析:(1)Mg可以与CO 反应生成氧化镁和碳,Mg与氢气不能发生反应,因此可
2
用氢气作为保护气,选用的药品为稀硫酸和锌粒,再用浓硫酸干燥;(2)装置中有空气,若不用氢气排空装置中的空气,氢气和空气的混合气体燃烧会发生爆炸,所以反应开始前
应该先通氢气排尽装置中的空气;Mg与SiO 反应的条件是加热,停止加热后,反应能继
2
续进行,说明该反应为放热反应,可利用自身放出的热量维持反应进行;
(3)MgSi 遇盐酸迅速反应生成 SiH (硅烷),其反应的方程式为:MgSi+
2 4 2
4HCl===2MgCl +SiH↑,SiH 常温下是一种不稳定、易自燃的气体,反应的方程式为
2 4 4
SiH +2O===SiO +2HO,所以往反应后的混合物中加入稀盐酸,可观察到闪亮的火星。
4 2 2 2
(4)要验证草酸晶体分解产物中有CO,只能通过检验CO与CuO反应的产物CO 的存在
2
来达到这一目的。因为草酸晶体的分解产物本身含有CO ,会对CO的检验造成干扰,所
2
以在检验CO前应将分解产物中的CO 除尽,可选用C装置来除去CO ,A装置用来检验
2 2
CO 是否除尽.将除去CO 的气体通过盛有无水氯化钙的装置D干燥,然后通过盛有CuO
2 2
的装置E,CuO将CO氧化为CO,再将气体通过盛有澄清石灰水的A装置,用来检验CO
2 2
的存在。因CO有毒,最后可将尾气通过排水法收集。(5)若前一个装置A中澄清石灰水
不变浑浊,说明草酸晶体分解的产物CO 已除尽;E中黑色CuO变红,同时其后的装置A
2
中澄清石灰水变浑浊,说明草酸晶体分解产物中含有CO。(6)F装置的作用是收集CO
气体,以防污染环境,更换的方法是将气体先通入C装置除去CO 气体后,将CO点燃。
2