文档内容
专练 33 盖斯定律及应用 反应热的比较和计算
授课提示:对应学生用书65页
1.Mn2+催化HO 分解:2HO (l)===2H O(l)+O (g) ΔH ,其反应机理如下
2 2 2 2 2 2 1
图。
若反应Ⅱ的焓变为ΔH ,则反应Ⅰ的焓变ΔH为(反应Ⅰ、Ⅱ的计量数均为最简整数
2
比)( )
A.ΔH-ΔH B.ΔH+ΔH
1 2 1 2
C.2ΔH-ΔH D.ΔH-2ΔH
1 2 1 2
答案:A
解析:由图可知反应过程为HO +Mn2+===2H++MnO (Ⅰ),MnO +HO +2H+
2 2 2 2 2 2
===Mn2++2HO+O↑(Ⅱ),题中给出的反应可由两个反应相加获得,有ΔH =ΔH+
2 2 1
ΔH,ΔH=ΔH-ΔH。
2 1 2
2.[2024·湖南博雅中学月考]下列说法或表示法正确的是( )
A.氢气与氧气反应生成等量的水蒸气和液态水,前者放出热量多
B.需要加热的反应说明它是吸热反应
C.在稀溶液中:H+(aq)+OH-(aq)===H O(l)
2
ΔH=-57.3 kJ·mol-1,若将含0.5 mol H SO 的浓硫酸与含1 mol NaOH的溶液混合,
2 4
放出的热量大于57.3 kJ
D.1 mol S 完全燃烧放热 297.3 kJ,其热化学方程式:S+O===SO ΔH=-297.3
2 2
kJ·mol-1
答案:C
解析:水蒸气变为液态水放热,氢气与氧气反应生成等量的水蒸气和液态水,后者放
出热量多,故A错误;反应吸、放热与反应条件无关,故B错误;浓硫酸溶于水放热,若
将含0.5 mol H SO 的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ,故C
2 4
正确;热化学方程式要标注物质的聚集状态,故D错误。
3.已知共价键的键能与热化学方程式信息如下表:
共价键 H—H H—O
键能/(kJ·mol-1) 436 463
2H(g)+O(g)===2H O(g)
热化学方程式 2 2 2
ΔH=-482 kJ·mol-1
则2O(g)===O (g)的ΔH为 ( )
2
A.428 kJ·mol-1 B.-428 kJ·mol-1
C.498 kJ·mol-1 D.-498 kJ·mol-1
答案:D
解析:2O(g)===O (g)的过程形成O===O共价键,是放热过程,其ΔH等于负的
2
O===O共价键的键能,A、C错误;对于热化学方程式2H (g)+O (g)===2H O(g)
2 2 2
ΔH=-482 kJ·mol-1,根据键能与焓变的关系ΔH=2E(H—H)+E(O===O)-4E(O—
H),可计算得E(O===O)=-482 kJ·mol-1+4×463 kJ·mol-1-2×436 kJ·mol-1=498
kJ·mol-1,B错误,D正确。
4.已知:
C(s)+O(g)===CO (g) ΔH
2 2 1
CO(g)+C(s)===2CO(g) ΔH
2 22CO(g)+O(g)===2CO (g) ΔH
2 2 3
4Fe(s)+3O(g)===2Fe O(s) ΔH
2 2 3 4
3CO(g)+Fe O(s)===3CO (g)+2Fe(s) ΔH
2 3 2 5
下列关于上述反应焓变的判断正确的是( )
A.ΔH>0,ΔH<0
1 3
B.ΔH>0,ΔH>0
2 4
C.ΔH=ΔH+ΔH
1 2 3
D.ΔH=ΔH+ΔH
3 4 5
答案:C
解析:发光放热的剧烈的氧化还原反应为燃烧,故煤炭的燃烧为放热反应,即ΔH <
1
0,ΔH <0,A错误;以碳、CO或H 为还原剂的氧化还原反应为吸热反应,故ΔH >0;
3 2 2
燃烧均为放热反应,故铁在氧气中燃烧是放热的,即 ΔH <0,B错误;一个反应无论是一
4
步完成还是分为几步完成,其热效应是相同的,已知②CO (g)+C(s)===2CO(g)
2
ΔH
2
③2CO(g)+O (g)===2CO (g) ΔH 根据盖斯定律可知将②+③相加可得:C
2 2 3
(s)+O (g)===CO (g) ΔH =ΔH +ΔH ,C正确;已知:④4Fe(s)+3O (g)
2 2 1 2 3 2
===2Fe O(s)ΔH ⑤3CO(g)+Fe O(s)===3CO (g)+2Fe(s) ΔH
2 3 4 2 3 2 5
根据盖斯定律可知将(④÷2+⑤)×2/3可得:2CO(g)+O (g)===2CO (g)ΔH
2 2 3
=,D错误。
5.下列说法正确的是( )
A.甲烷的燃烧热为ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH
4
(g)+2O(g)===CO (g)+2HO(g) ΔH=-890.3 kJ·mol-1
2 2 2
B.已知HO(l)===H O(g) ΔH=+44 kJ·mol-1,则2 g H (g)完全燃烧生成液
2 2 2
态水比生成气态水多释放22 kJ的能量
C.常温下,反应C(s)+CO(g)===2CO(g)不能自发进行,则该反应的ΔH<0
2
D.同温同压下,H(g)+Cl(g)===2HCl(g)在光照和点燃条件的ΔH相同
2 2
答案:D
解析:水的状态应该是液态,即甲烷燃烧的热化学方程式可表示为CH (g)+2O
4 2
(g)===CO (g)+2HO(l) ΔH=-890.3 kJ·mol-1,A错误;已知HO(l)===H O
2 2 2 2
(g) ΔH=+44 kJ·mol-1,则2 g H (g)即1 mol氢气完全燃烧生成液态水比生成气态
2
水多释放44 kJ的热量,B错误;常温下,反应C(s)+CO (g)===2CO(g)的ΔH>
2
0,C错误;反应热只与反应物和生成物总能量的相对大小有关系,则同温同压下,H
2
(g)+Cl(g)===2HCl(g)在光照和点燃条件下反应的ΔH相同,D正确。
2
6.不管化学反应过程是一步完成还是分为数步完成,这个过程的热效应是相同的。
已知:HO(g)===H O(l)
2 2
ΔH=-Q kJ·mol-1 ①
1 1
C HOH(g)===C HOH(l)
2 5 2 5
ΔH=-Q kJ·mol-1 ②
2 2
C HOH(g)+3O(g)===2CO (g)+3HO(g)
2 5 2 2 2
ΔH=-Q kJ·mol-1 ③
3
若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为( )
A.(Q+Q+Q)kJ
1 2 3
B.[0.5(Q+Q+Q)] kJ
1 2 3
C.(0.5Q-1.5Q+0.5Q) kJ
1 2 3
D.(1.5Q-0.5Q+0.5Q) kJ
1 2 3
答案:D
解析:根据盖斯定律可以知道①×3-②+③得C HOH(l)+3O (g)===2CO
2 5 2 2
(g)+3HO(l) ΔH=(-3Q +Q -Q ) kJ·mol-1,即1 mol液态酒精完全燃烧并恢
2 1 2 3
复至室温,则放出的热量为(3Q -Q +Q ) kJ,则23 g液态酒精完全燃烧并恢复至室温,
1 2 3
则放出的热量为0.5×(3Q-Q+Q) kJ=(1.5Q-0.5Q+0.5Q) kJ,D正确。
1 2 3 1 2 3
7.已知:①H+(aq)+OH-(aq)===H O(l) ΔH =-57.3 kJ·mol-1, ②H (g)
2 1 2
+O(g)===H O(g) ΔH=-241.8 kJ·mol-1,下列有关说法正确的是( )
2 2 2
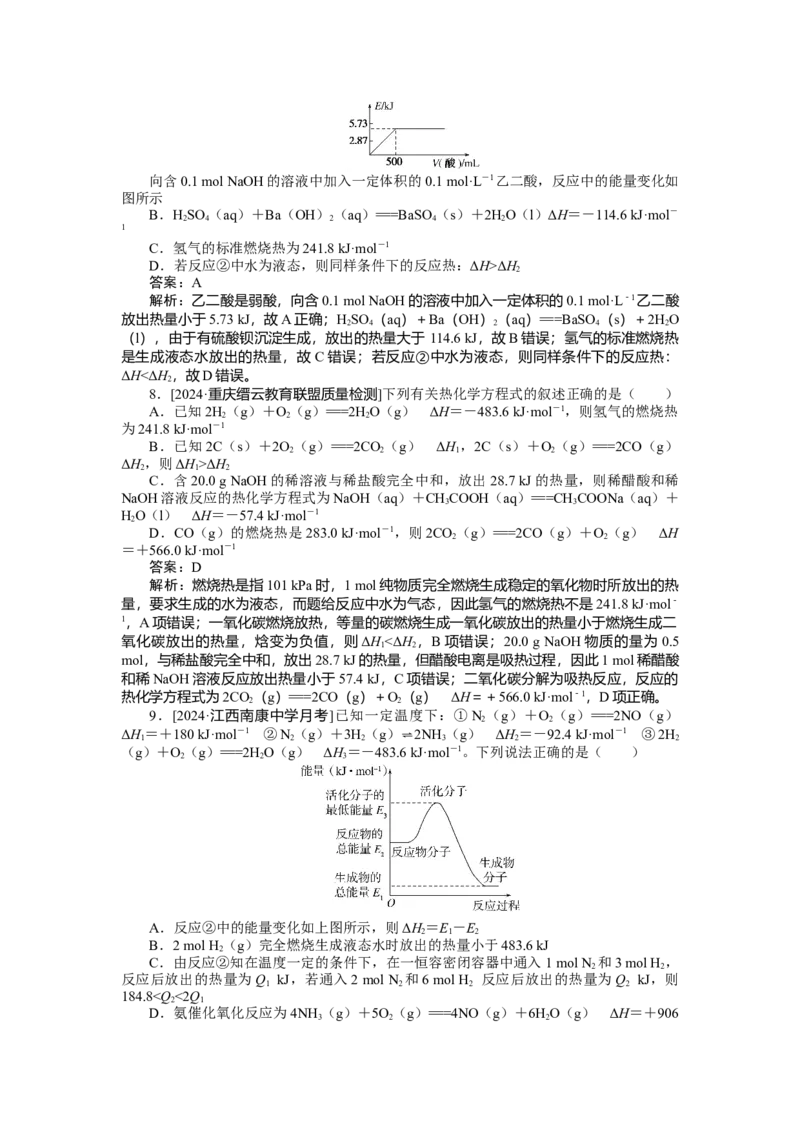
A.向含0.1 mol NaOH的溶液中加入一定体积的0.1 mol·L-1乙二酸,反应中的能量变化如
图所示
B.HSO (aq)+Ba(OH) (aq)===BaSO (s)+2HO(l)ΔH=-114.6 kJ·mol-
2 4 2 4 2
1
C.氢气的标准燃烧热为241.8 kJ·mol-1
D.若反应②中水为液态,则同样条件下的反应热:ΔH>ΔH
2
答案:A
解析:乙二酸是弱酸,向含0.1 mol NaOH的溶液中加入一定体积的0.1 mol·L-1乙二酸
放出热量小于5.73 kJ,故A正确;HSO (aq)+Ba(OH) (aq)===BaSO (s)+2HO
2 4 2 4 2
(l),由于有硫酸钡沉淀生成,放出的热量大于 114.6 kJ,故B错误;氢气的标准燃烧热
是生成液态水放出的热量,故C错误;若反应②中水为液态,则同样条件下的反应热:
ΔH<ΔH,故D错误。
2
8.[2024·重庆缙云教育联盟质量检测]下列有关热化学方程式的叙述正确的是( )
A.已知2H (g)+O (g)===2H O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热
2 2 2
为241.8 kJ·mol-1
B.已知2C(s)+2O (g)===2CO (g) ΔH ,2C(s)+O (g)===2CO(g)
2 2 1 2
ΔH,则ΔH>ΔH
2 1 2
C.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀
NaOH溶液反应的热化学方程式为NaOH(aq)+CHCOOH(aq)===CH COONa(aq)+
3 3
HO(l) ΔH=-57.4 kJ·mol-1
2
D.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO (g)===2CO(g)+O (g) ΔH
2 2
=+566.0 kJ·mol-1
答案:D
解析:燃烧热是指101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热
量,要求生成的水为液态,而题给反应中水为气态,因此氢气的燃烧热不是241.8 kJ·mol-
1,A项错误;一氧化碳燃烧放热,等量的碳燃烧生成一氧化碳放出的热量小于燃烧生成二
氧化碳放出的热量,焓变为负值,则ΔH<ΔH ,B项错误;20.0 g NaOH物质的量为0.5
1 2
mol,与稀盐酸完全中和,放出28.7 kJ的热量,但醋酸电离是吸热过程,因此1 mol稀醋酸
和稀NaOH溶液反应放出热量小于57.4 kJ,C项错误;二氧化碳分解为吸热反应,反应的
热化学方程式为2CO(g)===2CO(g)+O(g) ΔH=+566.0 kJ·mol-1,D项正确。
2 2
9.[2024·江西南康中学月考]已知一定温度下:①N (g)+O (g)===2NO(g)
2 2
ΔH
1
=+180 kJ·mol-1 ②N
2
(g)+3H
2
(g) ⇌2NH
3
(g) ΔH
2
=-92.4 kJ·mol-1 ③2H
2
(g)+O(g)===2H O(g) ΔH=-483.6 kJ·mol-1。下列说法正确的是( )
2 2 3
A.反应②中的能量变化如上图所示,则ΔH=E-E
2 1 2
B.2 mol H (g)完全燃烧生成液态水时放出的热量小于483.6 kJ
2
C.由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N 和3 mol H ,
2 2
反应后放出的热量为Q kJ,若通入2 mol N 和6 mol H 反应后放出的热量为Q kJ,则
1 2 2 2
184.80)
1
(Ⅱ)Br
2
(l)+H
2
(g) ⇌2HBr(g) ΔH=-Q
2
kJ·mol-1(Q
2
>0)
(Ⅲ)Cl
2
(g)+H
2
(g) ⇌2HCl(g) ΔH=-Q
3
kJ·mol-1(Q
3
>0)
下列叙述正确的是( )
A.Q>Q
1 3
B.将1 mol Br (g)和1 mol H (g)混合后充分反应,放出热量Q kJ
2 2 1
C.Br
2
(l) ⇌Br
2
(g) ΔH=(Q
2
-Q
1
) kJ·mol-1
D.1 mol HBr(g)具有的能量大于1 mol HBr(l)具有的能量
答案:D
解析:A项,由于氯的非金属性比溴强,所以等物质的量的Cl (g)、Br (g)分别
2 2
与H (g)反应时,Cl (g)与H (g)反应放出的热量更多,即Q>Q ,错误;B项,Br
2 2 2 3 1 2
(g)+H
2
(g)⇌2HBr(g)是可逆反应,所以1 mol Br
2
(g)与1 mol H
2
(g)混合后充分
反应,放出热量小于Q
1
kJ,错误;C项,由(Ⅱ)-(Ⅰ)得,Br
2
(l)⇌Br
2
(g) ΔH
=-(Q -Q ) kJ·mol-1,错误;D项,物质从气态转化为液态要释放出能量,所以1
2 1
mol HBr(g)具有的能量大于1 mol HBr(l)具有的能量,正确。
11.室温下,CuSO (s)和 CuSO ·5H O(s)溶于水及CuSO ·5H O受热分解的能量
4 4 2 4 2
变化如图所示,下列说法不正确的是( )
A.将CuSO ·5H O(s)溶于水会使溶液温度降低
4 2
B.将CuSO (s)溶于水会使溶液温度升高
4
C.ΔH>ΔH
3 2
D.ΔH=ΔH+ΔH
1 2 3
答案:D
解析:胆矾溶于水时,溶液温度降低,反应为 CuSO ·5H O(s)===Cu2+(aq)+SO
4 2
(aq)+5HO ΔH>0,故A正确;硫酸铜溶于水,溶液温度升高,该反应为放热反应,
2 3
则:CuSO (s)===Cu2+(aq)+SO(aq) ΔH <0;故B正确;由图像分析:ΔH <0,
4 2 2
ΔH>0,ΔH>ΔH,故C正确;由图像分析可知:ΔH=ΔH-ΔH,故D错误。
3 3 2 1 3 2
12.[2024·山西部分学校联考]将1 L 0.1 mol·L-1 BaCl 溶液与足量稀硫酸充分反应放
2
出a kJ热量,将1 L 0.5 mol·L-1 HCl溶液与足量CHCOONa溶液充分反应放出b kJ热量
3
(不考虑醋酸钠水解);将0.5 L 1 mol·L-1硫酸溶液与足量(CHCOO) Ba(可溶性强电
3 2
解质)溶液反应放出的热量为( )
A.(5a-2b) kJ B.(5a+2b) kJ
C.(2b-5a) kJ D.(10a+4b) kJ
答案:B解析:根据题意,可得:①Ba2+(aq)+SO(aq)===BaSO (s) ΔH=-10a
4
kJ·mol-1,②H+(aq)+CHCOO-(aq)===CH COOH(aq) ΔH=-2b kJ·mol-1。根据
3 3
盖斯定律,由①+②×2可得硫酸和(CHCOO) Ba的反应为2H+(aq)+SO(aq)+
3 2
Ba2+(aq)+2CHCOO-(aq)===2CH COOH(aq)+BaSO (s) ΔH=-(10a+4b)
3 3 4
kJ·mol-1,故0.5 mol HSO 参加反应,放出热量为(10a+4b) kJ·mol-1×0.5 mol=(5a+
2 4
2b) kJ。
13.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO(s)+3C(s)===K S(s)+N(g)+3CO(g)ΔH=x kJ·mol-1
3 2 2 2
已知:碳的标准燃烧热 ΔH =a kJ·mol-1,S(s)+2K(s)===K S(s) ΔH =b
1 2 2
kJ·mol-1,2K(s)+N(g)+3O(g)===2KNO (s)
2 2 3
ΔH=c kJ·mol-1则x为( )
3
A.3a+b-c B.c-3a-b
C.a+b-c D.c-a-b
答案:A
解析:碳燃烧的热化学方程式为①C(s)+O (g)===CO (g) ΔH =a kJ·mol-
2 2 1
1,将另外两个热化学方程式进行编号,②S(s)+2K(s)===K S(s) ΔH =b kJ·mol
2 2
-1,③2K(s)+N (g)+3O (g)===2KNO (s) ΔH =c kJ·mol-1,运用盖斯定律,
2 2 3 3
①×3+②-③得S(s)+2KNO (s)+3C(s)===K S(s)+N (g)+3CO (g)
3 2 2 2
ΔH=(3a+b-c) kJ·mol-1,则x=3a+b-c,故A正确。