文档内容
专练 5 物质的量浓度溶液的配制与计算
一、选择题
1.[2024·福建师大附中期中]下列说法正确的是( )
A.现需配制480 mL 0.1 mol·L-1硫酸铜溶液,则需要称量7.68 g硫酸铜固体
B.100 g物质的量浓度为18.4 mol·L-1的硫酸溶液,用水稀释到物质的量浓度为 9.2
mol·L-1,需要水100 g
C.将10 g CuSO 溶解在90 g水中,可配制质量分数为10%的CuSO 溶液
4 4
D.使用量筒量取一定体积的浓硫酸配制一定物质的量浓度的稀硫酸,将浓硫酸转移
至烧杯后须用蒸馏水洗涤量筒,并将洗涤液一并转移至烧杯
答案:C
解析:配制480 mL溶液应选择500 mL容量瓶,则m=cVM=0.1 mol·L-1×0.5 L×160
g·mol-1=8.0 g,A项错误;由c×=c×、ρ≠ρ 及c =2c 可知,m≠2m ,B项错误;ω
1 2 1 2 1 2 2 1
=×100%=×100%=10%,C项正确;用量筒量取一定体积的浓硫酸配制一定物质的量浓度
的稀硫酸,将浓硫酸完全转移至烧杯后无需用蒸馏水洗涤量筒,D项错误。
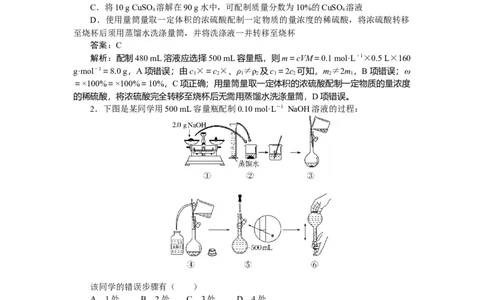
2.下图是某同学用500 mL容量瓶配制0.10 mol·L-1 NaOH溶液的过程:
该同学的错误步骤有( )
A.1处 B.2处 C.3处 D.4处
答案:C
解析:第①步不能把NaOH放在称量纸上称量;第④步玻璃棒应接触容量瓶内壁刻度
线以下的部分;第⑤步定容时应平视刻度线。
3.[2024·甘肃兰州一中月考]下图是病人输液用的氯化钠注射液标签的部分内容,下列
说法不正确的是( )A.该注射液的质量为2.25 g
B.0.9%是氯化钠的质量分数
C.该注射液的密度为1 g·mL-1
D.氯化钠的物质的量浓度约为0.15 mol·L-1
答案:A
解析:由标签可知,该注射液含NaCl的质量为2.25 g,A项错误;标签中的0.9%指氯
化钠的质量分数,B项正确;该注射液的密度为=1 g·mL-1,C项正确;氯化钠的物质的
量浓度为≈0.15 mol·L-1,D项正确。
4.[2023·全国甲卷]实验室将粗盐提纯并配制0.100 0 mol·L-1的NaCl溶液。下列仪器
中,本实验必须用到的有( )
①天平 ②温度计 ③坩埚 ④分液漏斗
⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥ B.①④⑤⑥
C.②③⑦⑧ D.①⑤⑥⑧
答案:D
解析:实验室将粗盐提纯时,需要将其溶于一定量的水中,然后将其中的硫酸根离子、
钙离子、镁离子依次用稍过量的氯化钡溶液、碳酸钠溶液和氢氧化钠溶液除去,该过程中
有过滤操作,需要用到烧杯、漏斗和玻璃棒;将所得滤液加适量盐酸酸化后蒸发结晶得到
较纯的食盐,该过程要用到蒸发皿和酒精灯;用提纯后得到的精盐配制溶液的基本步骤有
称量、溶解、转移、洗涤、定容、摇匀等操作,需要用到天平、容量瓶、烧杯、玻璃棒、
胶头滴管等。综上所述,本实验必须用到的有①天平、⑤容量瓶、⑥烧杯、⑧酒精灯,因
此本题选D。
5.浓度为2 mol·L-1 的盐酸V L,欲使其浓度变为4 mol·L-1,以下列出的方法中可行
的是( )
A.通入标准状况下的HCl气体44.8 L
B.将溶液加热蒸发浓缩至0.5V L
C.蒸发掉0.5V L水
D.加入10 mol·L-1盐酸0.6V L,再将溶液稀释至2V L
答案:D
解析:浓度为2 mol·L-1的盐酸V L含溶质HCl 2V mol。A项,加入2 mol HCl,体积
会发生改变,不可行;B项,加热浓缩时HCl和水都要蒸发出去,不可行;C项,蒸发掉
0.5V L水后溶液体积无法求出,不可行;D项,属于混合溶液的有关计算,加入10 mol·L
-1盐酸0.6V L后,溶质HCl的物质的量为8V mol,再将溶液稀释至2V L,浓度变为4
mol·L-1,可行。
6.有9.7 g Cu和Zn的合金与足量的稀HNO 反应,还原产物只有NO气体,其体积在
3
标准状况下为2.24 L。将溶液稀释为1 L,测得溶液的pH=1,此时溶液中NO的浓度为(
)A.0.3 mol·L-1 B.0.4 mol·L-1
C.0.5 mol·L-1 D.0.6 mol·L-1
答案:B
解析:NO气体是Cu和Zn的合金还原HNO 得到的,在这个过程中,金属失去的电子
3
跟HNO 得到电子数相等,生成0.1 mol的NO气体,HNO 得到0.3 mol的电子,在这个过
3 3
程中金属失去0.3 mol的电子,又由于都是二价金属,所以跟Cu2+和Zn2+结合的NO的物
质的量也为0.3 mol。再加上溶液中的0.1 mol的硝酸,总共是0.4 mol的NO,又因为溶液
的体积为1 L,即B正确。
7.[2024·山西省怀仁县高三月考]下列有关实验原理或操作正确的是( )
A.用20 mL量筒量取15 mL酒精,加水5 mL,配制质量分数为75%的酒精溶液
B.在200 mL某硫酸盐溶液中,含有1.5N 个硫酸根离子,同时含有N 个金属离子,
A A
则该硫酸盐的物质的量浓度为2.5 mol·L-1
C.实验中需用2.0 mol·L-1的NaCO 溶液950 mL,配制时应选用的容量瓶的规格和称
2 3
取NaCO 的质量分数分别为950 mL、201.4 g
2 3
D.实验室配制500 mL 0.2 mol·L-1的硫酸亚铁溶液,其操作是:用天平称15.2 g绿矾
(FeSO ·7H O),放入小烧杯中加水溶解,转移到500 mL容量瓶,稀释、定容、摇匀
4 2
答案:B
解析:用20 mL量筒量取15 mL酒精,加水5 mL,配制的酒精溶液质量分数小于
75%,故A错误;硫酸根离子与金属离子的个数比是3∶2,该盐的化学式是R (SO ) ,
2 4 3
该硫酸盐的物质的量0.5 mol,浓度为2.5 mol·L-1,故B正确;实验中需用2.0 mol·L-1的
NaCO 溶液950 mL,配制时应选用的容量瓶的规格和称取NaCO 的质量分数分别为1 000
2 3 2 3
mL、212.0 g,故C错误;实验室配制500 mL 0.2 mol·L-1的硫酸亚铁溶液,其操作是:用
天平称27.8 g绿矾(FeSO ·7H O),放入小烧杯中加水溶解,转移到 500 mL容量瓶,稀
4 2
释、定容、摇匀,故D错误。
8.[2024·全国百强校江西省上高县高三月考]在溶液的配制过程中会引起浓度偏高的是
( )
①用1 g 98%的浓硫酸加4 g水配制成19.6%的硫酸
②配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇匀后,发现液面低
于刻度线
③10%的硫酸和90%的硫酸等体积混合配制50%的硫酸溶液
④向80 mL水中加入18.4 mol·L-1硫酸20 mL,配制3.68 mol·L-1的硫酸溶液
⑤质量分数为5x%和x%的两种氨水等体积混合配制成3x%的氨水
A.①③⑤ B.②④⑤
C.③④ D.④⑤
答案:C
解析:①用1 g 98%的浓硫酸加4 g水,所得溶液中硫酸的质量分数为:×100%=
19.6%,该操作合理;②配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇
匀后,因为容量瓶刻度线上方有残留的溶液,所以液面会低于刻度线,不会影响配制结果
③硫酸的密度大于1,10%的硫酸和90%的硫酸等体积混合,所得溶液的质量分数大于
50%;④在80 mL水中加入18.4 mol·L-1的硫酸20 mL,所得溶液体积小于100 mL,配制
的溶液浓度大于3.68 mol·L-1;⑤氨水密度小于1,质量分数为5x%和x%的两种氨水等体
积混合所得溶液质量分数小于3x%。所以C选项是正确的。
9.[2024·北京和平一中月考]在a L Al (SO ) 和(NH ) SO 的混合溶液中加入b
2 4 3 4 2 4
mol BaCl ,恰好使溶液中的SO完全沉淀;如加入足量强碱并加热可得到c mol NH ,则原
2 3溶液中Al3+的浓度(mol·L-1)为( )
A. B.
C. D.
答案:C
解析:由于产生c mol NH ,则必定有NHc mol,使SO完全沉淀需Ba2+b mol,因此
3
SO有b mol。根据电荷守恒:2c(SO)=c(NH)+3c(Al3+),则3c(Al3+)= mol·L
-1,c(Al3+)= mol·L-1。
10.[2024·大庆中学高三月考]N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.100 mL 12 mol·L-1的浓硝酸与过量Cu反应转移电子数目为0.6N
A
B.将1 mol Cl 通入水中,HClO、Cl-、ClO-粒子数之和等于2N
2 A
C.同温同压下,两个等体积的干燥圆底烧瓶中分别充满①HCl ②NO ,进行喷泉实
2
验。经充分反应后烧瓶内溶质的物质的量浓度之比为3∶2
D.实验室里要用480 mL 0.1 mol·L-1的硫酸铜溶液,需称取12.5克胆矾配制成溶液
答案:D
解析:100 mL 12 mol·L-1的浓硝酸与过量Cu反应,还原产物为NO 、NO的混合物,
2
转移电子数目大于 0.6N ,故 A 错误;氯水中含有氯分子,将 1 mol Cl 通入水中,
A 2
HClO、Cl-、ClO-粒子数之和小于2N ,故B错误;设容器体积是V L,则气体的物质的
A
量是mol;①HCl进行喷泉实验得到溶液的体积是V L,盐酸的浓度是mol÷V L=mol·L-
1;②NO 进行喷泉实验后发生反应3NO +HO===2HNO +NO, 得到硝酸溶液的体积是V
2 2 2 3
L,生成硝酸的物质的量为mol×,硝酸的浓度是mol×÷V L=mol·L-1,溶质的物质的量
浓度之比为1∶1,故C错误;实验室里要用480 mL 0.1 mol·L-1的硫酸铜溶液,需用500
mL容量瓶,需胆矾0.5 L×0.1 mol·L-1×250 g·mol-1=12.5 g,故D正确。
11.标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·m L-1),所得溶液的
密度为ρ g·mL-1,质量分数为W。物质的量浓度为c mol·L-1,则下列关系中不正确的是
( )
A.ρ=(17V+22 400)/(22.4+22.4V)
B.W=17c/(1 000ρ)
C.W=17V/(17V+22 400)
D.c=1 000ρV/(17V+22 400)
答案:A
解析:由于溶液的体积既不是水的体积也不是二者体积之和,溶液的体积不能直接确
定,仅利用V无法确定ρ, A错误;由c==,可得:W=, B正确;氨水的质量分数=
=,C正确;氨水的物质的量浓度===,D正确。
12.某氯化镁溶液的密度为1.18 g·cm-3,其中镁离子的质量分数为5.1%,则300 mL
该溶液中Cl-的物质的量等于( )
A.0.37 mol B.0.63 mol
C.0.74 mol D.1.50 mol
答案:D
解析:300 mL该氯化镁溶液的质量为1.18 g·cm-3×300 mL=354 g,镁离子的物质的
量为≈0.75 mol,氯化镁溶液中n(Cl-)=2n(Mg2+)=2×0.75 mol=1.50 mol,故选D。
二、非选择题
13.在一定温度下,某饱和氢氧化钠溶液体积为V mL,溶液密度为d g·cm-3,质量
分数为w,物质的量浓度为c mol·L-1,溶液中含氢氧化钠的质量为m g。
(1)用m、V表示溶液中溶质的物质的量浓度(c)为 。(2)用w、d表示溶液中溶质的物质的量浓度(c)为 。
(3)用c、d表示溶液中溶质的质量分数(w)为 。
答案:(1) mol·L-1 (2)25dw mol·L-1 (3)%
解析:(1)c== mol·L-1
(2)c==25dw mol·L-1
(3)w=×100%=%
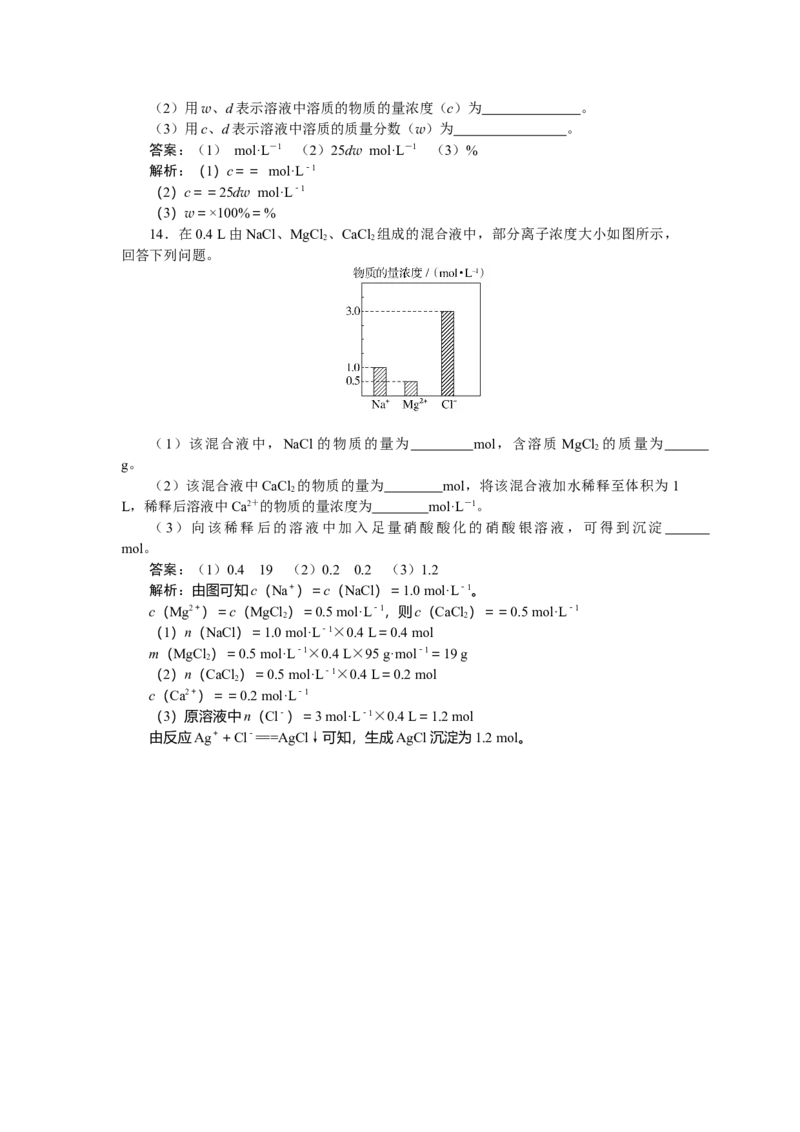
14.在0.4 L由NaCl、MgCl 、CaCl 组成的混合液中,部分离子浓度大小如图所示,
2 2
回答下列问题。
(1)该混合液中,NaCl 的物质的量为 mol,含溶质 MgCl 的质量为
2
g。
(2)该混合液中CaCl 的物质的量为 mol,将该混合液加水稀释至体积为1
2
L,稀释后溶液中Ca2+的物质的量浓度为 mol·L-1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀
mol。
答案:(1)0.4 19 (2)0.2 0.2 (3)1.2
解析:由图可知c(Na+)=c(NaCl)=1.0 mol·L-1。
c(Mg2+)=c(MgCl )=0.5 mol·L-1,则c(CaCl )==0.5 mol·L-1
2 2
(1)n(NaCl)=1.0 mol·L-1×0.4 L=0.4 mol
m(MgCl )=0.5 mol·L-1×0.4 L×95 g·mol-1=19 g
2
(2)n(CaCl )=0.5 mol·L-1×0.4 L=0.2 mol
2
c(Ca2+)==0.2 mol·L-1
(3)原溶液中n(Cl-)=3 mol·L-1×0.4 L=1.2 mol
由反应Ag++Cl-===AgCl↓可知,生成AgCl沉淀为1.2 mol。