文档内容
2008年湖南省娄底市中考化学试卷
一、选择题(共20小题,每小题2分,满分40分)
1.(2分)2008年8月8日到24日,第二十九届奥运会将在北京举行,下列与此会相关
的事项中,属于化学反应的是( )
A.将金属银打造成银牌 B.使水凝固成冰
C.奥运圣火“祥云”的燃烧 D.生石灰干燥食品
2.(2分)臭氧(O )主要分布在距离地面10km﹣50km的高空,形成臭氧层.臭氧层吸
3
收了太阳光中大部分紫外线,使地球上的生物免受紫外线伤害.臭氧属于( )
A.非金属单质 B.金属单质 C.化合物 D.混合物
3.(2分)能保持氢气化学性质的最小粒子是( )
A.H B.2H C.H D.H+
2
4.(2分)“减少污染,净化空气,还我一片蓝天”,已成为世界各国人民的共同心声.
下列气体中,对空气会产生污染的是( )
A.O B.N C.CO D.SO
2 2 2 2
5.(2分)“安全生产,人命关天”.国家对易燃、易爆物的生产、贮存、运输,使用有
严格规定,绝不允许违章操作.下列物质与空气混合后,遇火不会发生爆炸的是
( )
A.液化石油气 B.二氧化碳 C.汽油 D.面粉
6.(2分)大理石是一种重要的建筑材料,它的主要成分是( )
A.CaO B.Ca(OH) C.CaCO D.CaCl
2 3 2
7.(2分)下列家庭中常见的调味与水混合后,不能形成溶液的是( )
A.食盐 B.白醋 C.白糖 D.花生油
8.(2分)下列物质中,由地壳中含量最多的金属元素、非金属元素和空气中含量最多的
元素组成的是( )
A.CaCO B.Al (SO ) C.Al(NO ) D.Fe(OH)
3 2 4 3 3 3 3
9.(2分)物质的化学式书写正确的是( )
A.氧化镁MgO B.氯化锌ZnCl
2
C.氧化铁Fe O D.碳酸钾KCO
2 3 3
10.(2分)宇宙飞船内用含氢氧化锂过滤网除去宇航员呼出的二氧化碳,该反应的化学
方程式为2LiOH+CO ═Li CO +X.则X的化学式为( )
2 2 3A.H B.H O C.H O D.O
2 2 2 2 2
11.(2分)钾肥能促进作物茎秆粗壮,增强对病虫害和倒伏的抵抗能力.下列物质中能
用作钾肥的是( )
A.尿素[CO(NH ) ] B.硝酸铵(NH NO )
2 2 4 3
C.磷酸二氢钙[Ca(H PO ) ] D.碳酸钾(K CO )
2 4 2 2 3
12.(2分)在下列溶液中分别滴加NaOH溶液,会产生蓝色沉淀的是( )
A.FeCl B.CuSO C.MgCl D.KNO
2 4 2 3
13.(2分)在日常生活中,下列做法中不符合科学的是( )
A.用干冰人工降雨
B.用食醋除去开水瓶中的水垢
C.用水冲洗自行车防锈
D.用熟石灰给养鸡场消毒
14.(2分)具备基本的化学实验技能是进行科学探究活动的基础和保证.下列实验操作
中,正确的是( )
A.用药匙取用粉末状药品
B.将实验剩余的药品带出实验室
C.用嘴吹灭酒精灯
D.将称量物放在天平的右盘进行称量
15.(2分)在CuCl 和AlCl 的混合溶液中,加入过量的锌粉,充分反应后过滤,留在滤
2 3
纸上的物质是( )
A.Cu B.Cu和Al C.Zn和Cu D.Cu、Al和Zn
16.(2分)某些含氟(F)牙膏中含有一种化学式为Na FPO 的物质.已知其中的氟元素
2 3
化合价为﹣1价,则其中的磷元素的化合价为( )
A.﹣5 B.+1 C.+3 D.+5
17.(2分)下列各组物质在水溶液中能大量共存的是( )
A.NaOH MgCl
2
NaCl B.NaCl Na
2
SO
4
NaOH
C.BaCl
2
KCl H
2
SO
4
D.HCl KOH NaCl
18.(2分)欲配制一定质量分数的盐酸溶液,需使用的一组仪器是( )
A.酒精灯、玻璃棒、量筒、烧杯
B.托盘天平、烧杯、试管、量筒
C.胶头滴管、烧杯、玻璃棒、药匙D.烧杯、量筒、玻璃棒、胶头滴管
19.(2分)5.6克不纯的铁粉与足量的稀盐酸完全反应放出0.24克氢气,则此铁粉中含有
的另一种金属可能是( )
A.Zn B.Cu C.Mg D.Ag
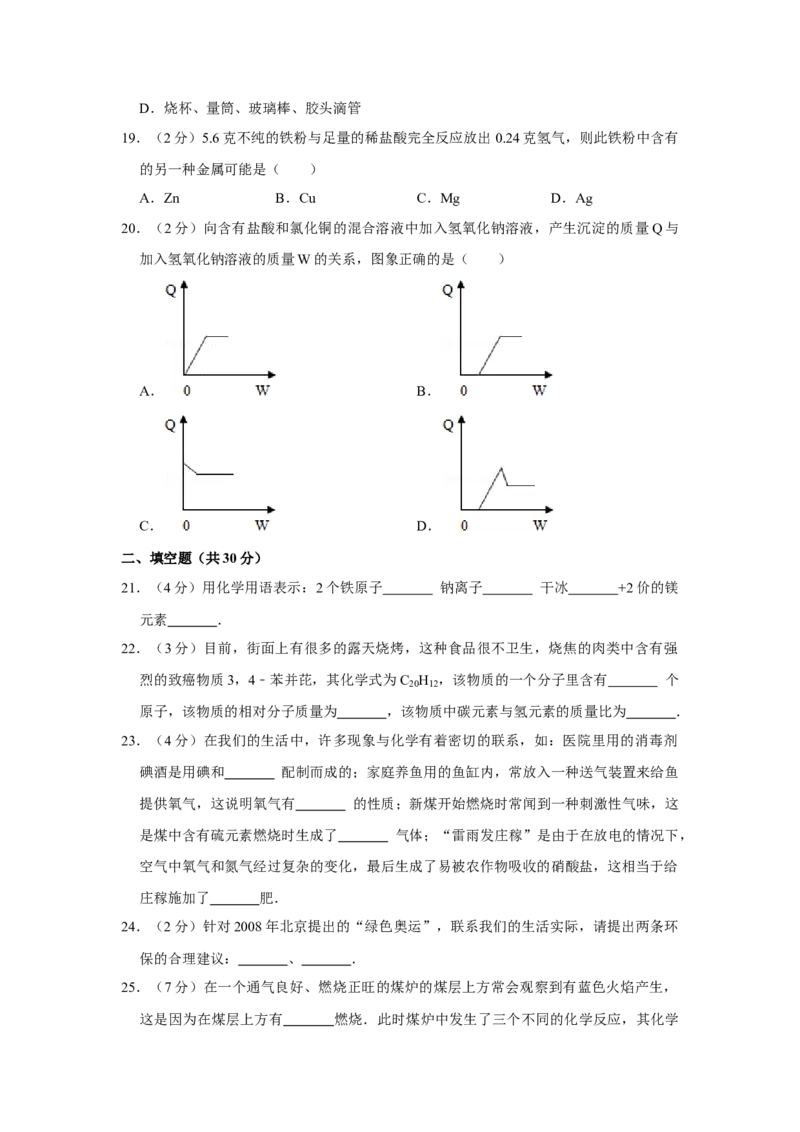
20.(2分)向含有盐酸和氯化铜的混合溶液中加入氢氧化钠溶液,产生沉淀的质量Q与
加入氢氧化钠溶液的质量W的关系,图象正确的是( )
A. B.
C. D.
二、填空题(共30分)
21.(4分)用化学用语表示:2个铁原子 钠离子 干冰 +2价的镁
元素 .
22.(3分)目前,街面上有很多的露天烧烤,这种食品很不卫生,烧焦的肉类中含有强
烈的致癌物质3,4﹣苯并芘,其化学式为C H ,该物质的一个分子里含有 个
20 12
原子,该物质的相对分子质量为 ,该物质中碳元素与氢元素的质量比为 .
23.(4分)在我们的生活中,许多现象与化学有着密切的联系,如:医院里用的消毒剂
碘酒是用碘和 配制而成的;家庭养鱼用的鱼缸内,常放入一种送气装置来给鱼
提供氧气,这说明氧气有 的性质;新煤开始燃烧时常闻到一种刺激性气味,这
是煤中含有硫元素燃烧时生成了 气体;“雷雨发庄稼”是由于在放电的情况下,
空气中氧气和氮气经过复杂的变化,最后生成了易被农作物吸收的硝酸盐,这相当于给
庄稼施加了 肥.
24.(2分)针对2008年北京提出的“绿色奥运”,联系我们的生活实际,请提出两条环
保的合理建议: 、 .
25.(7分)在一个通气良好、燃烧正旺的煤炉的煤层上方常会观察到有蓝色火焰产生,
这是因为在煤层上方有 燃烧.此时煤炉中发生了三个不同的化学反应,其化学方程式是:
.
① .
② .
26.③(5分)下面是有关硫化氢气体(H
2
S)的信息,请仔细阅读:
鸡蛋腐败时会产生一种无色、有臭鸡蛋气味的硫化氢气体.
①硫化氢气体是一种大气污染物,它在空气中点燃完全燃烧时,生成二氧化硫和水.
②氢硫化氢气体通入浓硫酸中,会发生化学反应:H
2
S+H
2
SO
4
═SO
2
+S↓+2H
2
O
③根据以上信息,回答下列问题:
(1)硫化氢的物理性质是 ;
(2)写出硫化氢在空气中燃烧的化学方程式: ;
(3)若实验过程中尾气内含有硫化氢, (填“能”或“不能”)用浓硫酸来
吸收,理由是 .
27.(3分)根据如图单质和化合物(或化合物的水溶液)间的转化关系推断出各有关物
质,将其化学式填入空白处.
(1)若Y是无色气体,乙的溶液是呈浅绿色,则X是 ;
(2)若Y是红色固体,乙的溶液呈浅绿色,由甲可以是 ;
(3)若X是无色气体,甲是黑色粉末,则乙是 .
28.(2分)有一种混合气体,可能由H 、CO、CO 和HCl中的一种或几种组成,将此混
2 2
合气体通入澄清的石灰水中,未见浑浊,但气体总体积明显减小;再将剩余的气体在氧
气中燃烧,燃烧产物不能使无水硫酸铜变蓝.则原混合气体中一定含有 ,可能
含有 .
三、实验题(共14分)
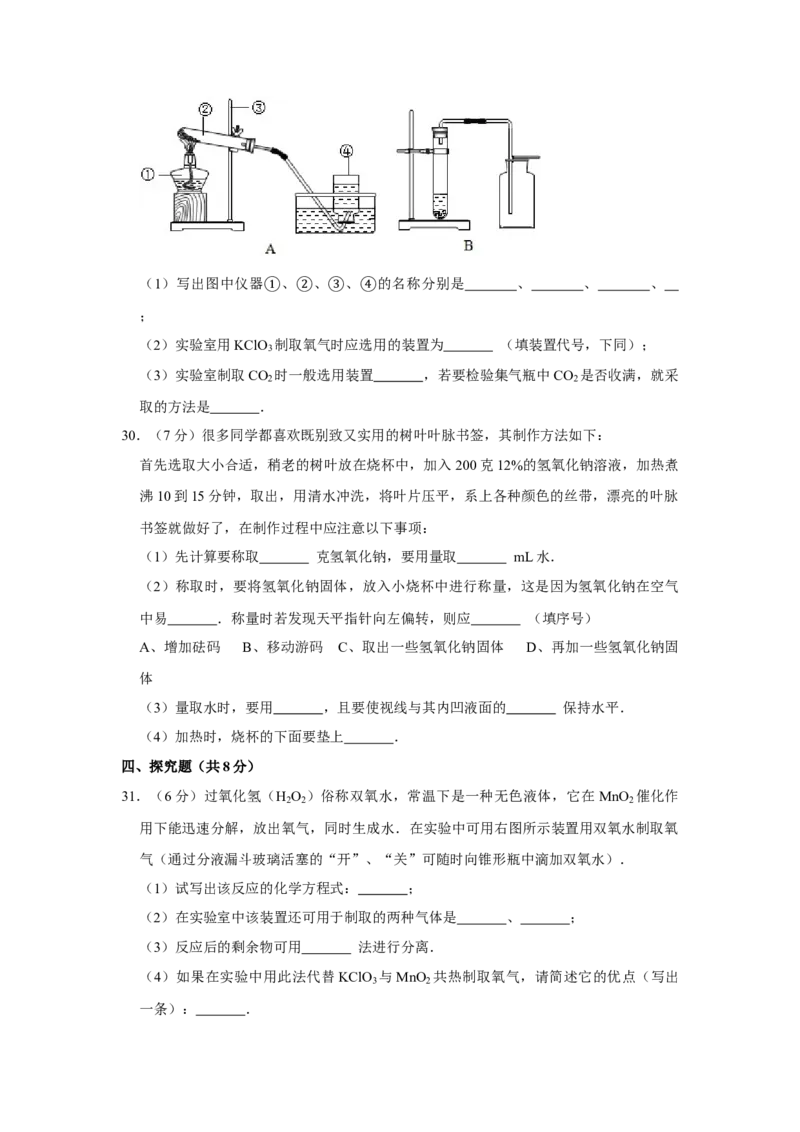
29.(7分)根据下列装置图回答问题:(1)写出图中仪器 、 、 、 的名称分别是 、 、 、
; ① ② ③ ④
(2)实验室用KClO 制取氧气时应选用的装置为 (填装置代号,下同);
3
(3)实验室制取CO 时一般选用装置 ,若要检验集气瓶中CO 是否收满,就采
2 2
取的方法是 .
30.(7分)很多同学都喜欢既别致又实用的树叶叶脉书签,其制作方法如下:
首先选取大小合适,稍老的树叶放在烧杯中,加入 200克12%的氢氧化钠溶液,加热煮
沸10到15分钟,取出,用清水冲洗,将叶片压平,系上各种颜色的丝带,漂亮的叶脉
书签就做好了,在制作过程中应注意以下事项:
(1)先计算要称取 克氢氧化钠,要用量取 mL水.
(2)称取时,要将氢氧化钠固体,放入小烧杯中进行称量,这是因为氢氧化钠在空气
中易 .称量时若发现天平指针向左偏转,则应 (填序号)
A、增加砝码 B、移动游码 C、取出一些氢氧化钠固体 D、再加一些氢氧化钠固
体
(3)量取水时,要用 ,且要使视线与其内凹液面的 保持水平.
(4)加热时,烧杯的下面要垫上 .
四、探究题(共8分)
31.(6分)过氧化氢(H O )俗称双氧水,常温下是一种无色液体,它在 MnO 催化作
2 2 2
用下能迅速分解,放出氧气,同时生成水.在实验中可用右图所示装置用双氧水制取氧
气(通过分液漏斗玻璃活塞的“开”、“关”可随时向锥形瓶中滴加双氧水).
(1)试写出该反应的化学方程式: ;
(2)在实验室中该装置还可用于制取的两种气体是 、 ;
(3)反应后的剩余物可用 法进行分离.
(4)如果在实验中用此法代替KClO 与MnO 共热制取氧气,请简述它的优点(写出
3 2
一条): .32.(2分)纯金首饰金光闪闪不易生锈,深受人们喜.有一种外形与纯金相似的黄铜是
由铜和锌组成的合金(各自保持单质的化学性质).有人用黄铜制成首饰冒充黄金制品
高价出售,欺骗消费者.请根据你所学过的化学知识,试设计鉴别黄金与黄铜的方法:
(1)根据俗语“真金不怕火练”,你能想到的一种方法是: ;
(2)根据常见金属的活动性顺序,你能想到的另外一种方法是: .
五、计算题(共8分)
33.(3分)某校化学课外研究小组为了测定石灰石的纯度,采用了以下的方法:取8克
这种石灰石样品,把40克稀盐酸分四次加入,测量过程得数据见下表(已知石灰石样
品中含有杂质不溶于水,且不与盐酸反应):
序号 加入稀盐酸的质量(克) 剩余固体质量(克)
第1次 10 5.5
第2次 10 m
第3次 10 1.2
第4次 10 1.2
(1)表中m的数值应该为 .
(2)试计算该石灰石样品的纯度.(即样品中CaCO 的质量分数.)
3
34.(5分)取碳酸钠和氯化钠的固体混合物14.6克,与质量为73克的稀盐酸恰好完全反
应,产生二氧化碳气体的质量为4.4克.试计算:
(1)固体混合物中碳酸钠的质量.
(2)反应所得的溶液中溶质的质量分数(最后结果保留一位小数).