文档内容
2009年湖南省株洲市中考化学试卷
一、选择题(共20小题,每小题分,满分40分)
1.(2分)下列现象属于化学变化的是( )
A.碘溶于酒精制成碘酒 B.瓷碗破碎
C.汽油挥发 D.蜡烛燃烧
2.(2分)下列说法中叙述错误的是( )
A.硫酸铜可用于游泳池水消毒,也可用于自来水消毒
B.黄曲霉毒素能损害人的肝脏,诱发肝癌等疾病.因此,霉变食物绝对不能食用
C.有些青少年不爱吃蔬菜、水果,这会引起维生素摄入不足而影响生长发育
D.氢气燃烧时放出的热量约为同质量汽油的三倍,燃烧后的产物是水,是理想的可再
生能源
3.(2分)小贝对柠檬汁、肥皂水、食盐水、草木灰水的pH分别进行了测定,其中pH最
小的是( )
A.柠檬汁 B.肥皂水 C.食盐水 D.草木灰水
4.(2分)下列说法错误的是( )
A.纯碱不是碱 B.酱油不是油
C.淀粉不属于糖类 D.碳酸不属于有机物
5.(2分)关于化学方程式3Fe+2O Fe O ,四位同学有如下所示的四种说法,其
2 3 4
中错误的是( )
A. B.C. D.
6.(2分)火星大气中95%是二氧化碳,其余为少量的氮气、氢气,还找到了有液态水存
在的证据.根据以上信息,下列推断错误的是( )
火星大气是纯净物;
①火星与地球大气成分相似;
②火星上钢铁容易生锈;
③火星上一定存在生命;
④火星上温室效应显著.
⑤A. B. C. D.
7.(2①分④)小⑤明从冰箱冷藏室②(③温⑤度为4℃)取出一①杯②4③℃④的澄清石灰水①,盖②上③杯④盖⑤,在
室温(温度为20℃)下放置一段时间后,发现杯底有少量晶体析出。下列说法错误的是
( )
A.室温时该石灰水溶液一定是饱和溶液
B.4℃时该石灰水溶液可能是不饱和溶液
C.氢氧化钙的溶解度随温度升高而增大
D.该石灰水4℃时溶液中溶质的质量分数大于室温时溶液中溶质的质量分数
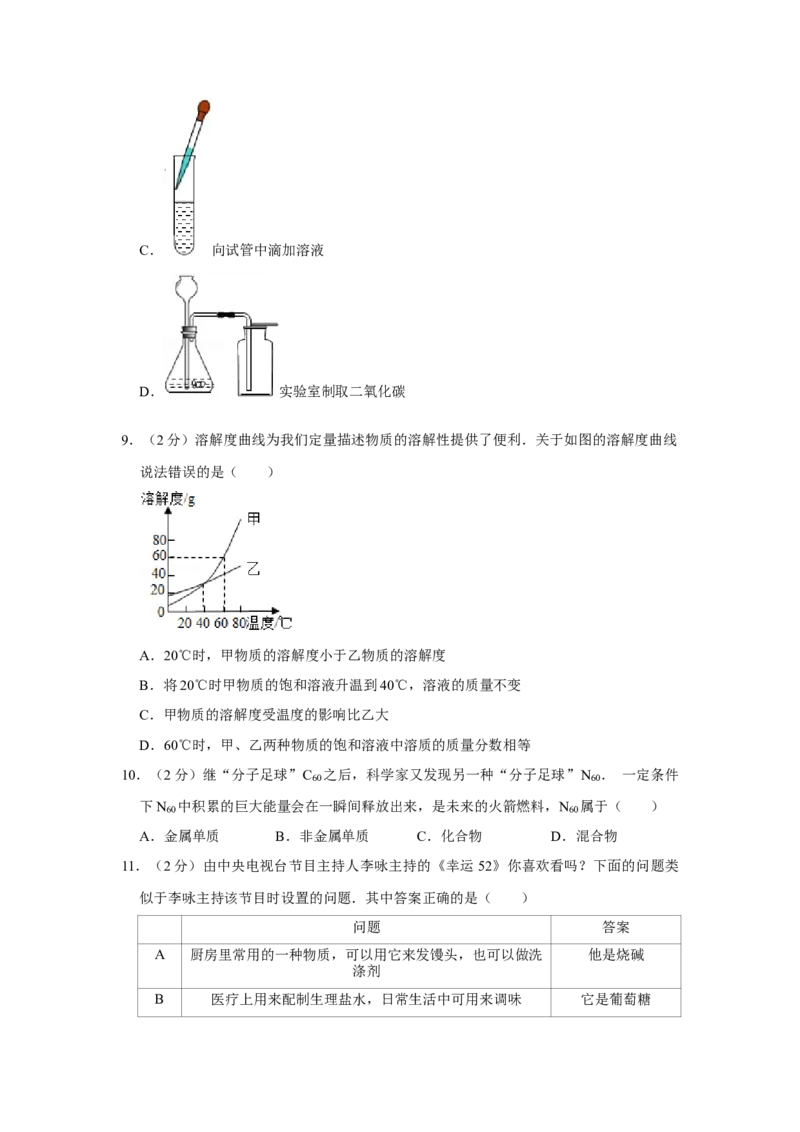
8.(2分)下列实验操作或装置错误的是( )
A. 实验室制取氧气
B. 检查装置的气密性C. 向试管中滴加溶液
D. 实验室制取二氧化碳
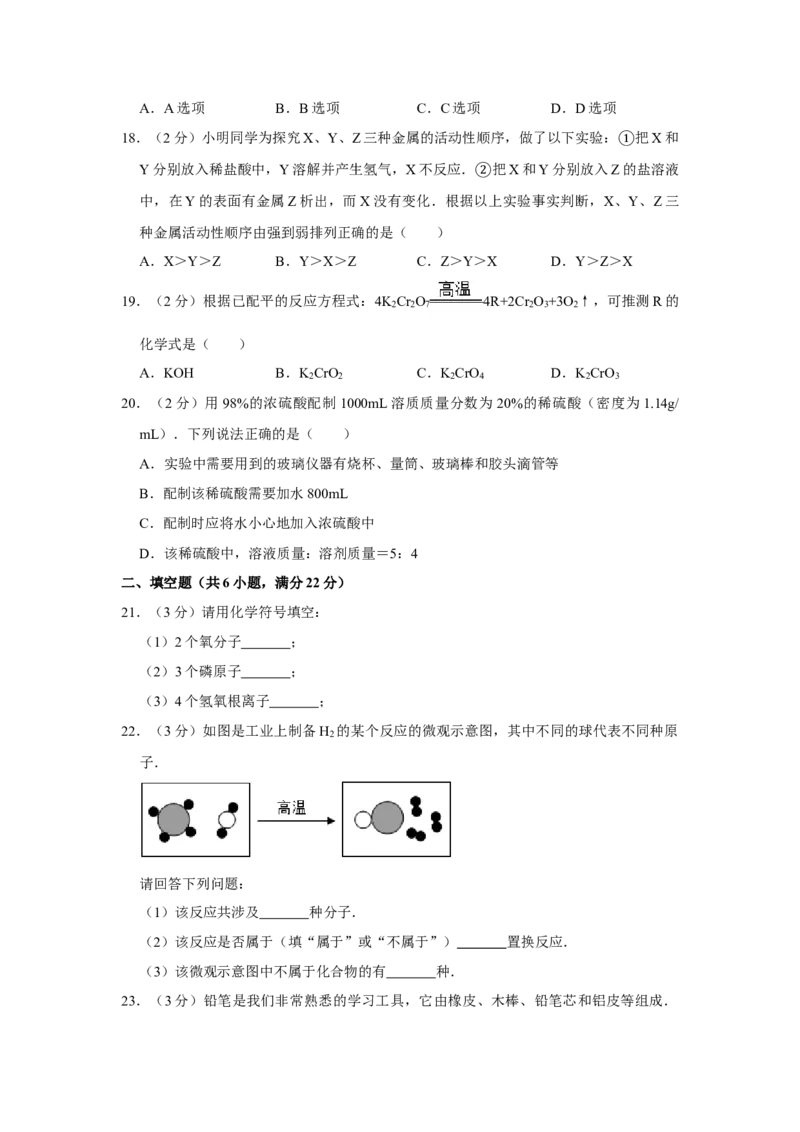
9.(2分)溶解度曲线为我们定量描述物质的溶解性提供了便利.关于如图的溶解度曲线
说法错误的是( )
A.20℃时,甲物质的溶解度小于乙物质的溶解度
B.将20℃时甲物质的饱和溶液升温到40℃,溶液的质量不变
C.甲物质的溶解度受温度的影响比乙大
D.60℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等
10.(2分)继“分子足球”C 之后,科学家又发现另一种“分子足球”N . 一定条件
60 60
下N 中积累的巨大能量会在一瞬间释放出来,是未来的火箭燃料,N 属于( )
60 60
A.金属单质 B.非金属单质 C.化合物 D.混合物
11.(2分)由中央电视台节目主持人李咏主持的《幸运 52》你喜欢看吗?下面的问题类
似于李咏主持该节目时设置的问题.其中答案正确的是( )
问题 答案
A 厨房里常用的一种物质,可以用它来发馒头,也可以做洗 他是烧碱
涤剂
B 医疗上用来配制生理盐水,日常生活中可用来调味 它是葡萄糖C 由碳和氢两种元素组成的气态化合物,也是农村沼气池中 它是甲烷
有植物残体分解产生的可燃性气体,容易充分燃烧,是清
洁能源
D 一种氧化物,它既能与酸性氧化物反应,又能与碱性氧化 无这样的氧化物
物反应,但都不生成盐
A.A正确 B.B正确 C.C正确 D.D正确
12.(2分)对下列事故处理的方法错误的是( )
A.如果不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液
B.当酒精洒在桌面上并着火燃烧时,不要惊慌,应立刻用湿抹布扑盖
C.浓H SO 沾在皮肤上,立即用NaOH溶液处理
2 4
D.发现人员一氧化碳中毒时,立即转移到通风的地方救治
13.(2分)高锰酸钾分解得到的产物除了氧气外,还有锰酸钾﹙K MnO ﹚、二氧化锰
2 4
﹙MnO ﹚,这两种含锰化合物中锰元素的化合价分别为( )
2
A.+6、+4 B.+6、﹣4 C.+7、+4 D.+7、﹣4
14.(2分)下列做法对人类的生存环境会造成危害的是( )
A.工业废水、生活污水经污水处理厂集中处理后再排放
B.农业上为了提高粮食产量,解决粮食危机而大量使用农药和化肥
C.不随意丢弃废旧电池
D.大力植树造林,严禁乱砍滥伐森林
15.(2分)下列试剂中不能鉴别稀硫酸和氢氧化钠溶液两种溶液的是( )
A.氯化钡溶液 B.氯化钾溶液 C.硫酸铜溶液 D.碳酸钠溶液
16.(2分)在化学学习过程中,常常要用到分类的方法.下列各组物质的分类正确的是
( )
A.混合物:空气、粗盐、牛奶
B.盐:氯化钙、硫酸、硝酸钾
C.氧化物:MgO、P O 、KClO
2 5 3
D.单质:铝、金刚石、氯化氢
17.(2分)下列对一些事实的微观解释错误的是( )
事实 解释
A 春天来了,百花盛开,花香四溢 分子在不断运动
B 炎热的夏天自行车胎容易爆裂 分子运动加快
C 水电解产生氢气和氧气 分子是可以再分的
D 架在高处的电线夏季变得比冬季长 原子的体积热胀冷缩A.A选项 B.B选项 C.C选项 D.D选项
18.(2分)小明同学为探究X、Y、Z三种金属的活动性顺序,做了以下实验: 把X和
Y分别放入稀盐酸中,Y溶解并产生氢气,X不反应. 把X和Y分别放入Z①的盐溶液
中,在Y的表面有金属Z析出,而X没有变化.根据以②上实验事实判断,X、Y、Z三
种金属活动性顺序由强到弱排列正确的是( )
A.X>Y>Z B.Y>X>Z C.Z>Y>X D.Y>Z>X
19.(2分)根据已配平的反应方程式:4K Cr O 4R+2Cr O +3O ↑,可推测R的
2 2 7 2 3 2
化学式是( )
A.KOH B.K CrO C.K CrO D.K CrO
2 2 2 4 2 3
20.(2分)用98%的浓硫酸配制1000mL溶质质量分数为20%的稀硫酸(密度为1.14g/
mL).下列说法正确的是( )
A.实验中需要用到的玻璃仪器有烧杯、量筒、玻璃棒和胶头滴管等
B.配制该稀硫酸需要加水800mL
C.配制时应将水小心地加入浓硫酸中
D.该稀硫酸中,溶液质量:溶剂质量=5:4
二、填空题(共6小题,满分22分)
21.(3分)请用化学符号填空:
(1)2个氧分子 ;
(2)3个磷原子 ;
(3)4个氢氧根离子 ;
22.(3分)如图是工业上制备H 的某个反应的微观示意图,其中不同的球代表不同种原
2
子.
请回答下列问题:
(1)该反应共涉及 种分子.
(2)该反应是否属于(填“属于”或“不属于”) 置换反应.
(3)该微观示意图中不属于化合物的有 种.
23.(3分)铅笔是我们非常熟悉的学习工具,它由橡皮、木棒、铅笔芯和铝皮等组成.在这些物质中:(1)能导电的是铝皮和 .(2)属于有机物的是木棒和 .
(3)燃烧不能生成二氧化碳的是 .
24.(5分)请从“ 二氧化碳; 熟石灰; 生石灰; 硝酸; 尿素; 聚乙烯塑
料; 碳酸氢钠”①中选择适当的②物质填空(③填序号):④ ⑤ ⑥
(1)⑦固态时可用于人工降雨的物质是 ;(2)可直接用作农作物氮肥的物质是
;
(3)可治疗胃酸过多症的物质是 ;(4)常用作袋装食品干燥剂的是 ;
(5)可以制成食品包装袋的是 .
25.(5分)元素周期表是我们学习化学的重要工具.如图是元素周期表的部分信息(其
中省略了氦、锂、铍、硼、氖、氩等6种元素的元素符号)
1H 2
氢 氦
3 4 5 6C 7N 8O 9F 10
锂 铍 硼 碳 氮 氧 氟 氖
11Na 12Mg 13AL 14Si 15P 16S 17Cl 18
钠 镁 铝 硅 磷 硫 氯 氩
19K 20Ca …
钾 钙
请你认真分析信息,回答:
(1)空气中含量最多的元素的原子序数是 .
(2)认真阅读上表,可以发现原子序数为 的元素符号错误,应该写成 .
(3)请你写出由原子序数为1、8、20的三种元素组成的化合物的化学式 .
(4)原子序数为16的元素的原子得到电子后形成的﹣2价离子是(写粒子符号)
.
26.(3分)镁是一种常见的金属,中学化学中经常使用镁的单质及其化合物进行实验.
(1)在试管中放入一小块镁条,加入5mL稀盐酸,我们除了观察到反应剧烈、产生大
量气泡外,还能观察到的现象是 .
(2)向MgO与过量的盐酸反应生成的MgCl 溶液中滴加浓度比较大的NaOH溶液时,
2
刚开始没有出现白色沉淀〔Mg (OH) 〕,随着氢氧化钠溶液的加入,逐渐出现白色
2
沉淀.请回答下列问题:
刚开始没有出现白色沉淀的原因是 (用化学方程式表示).
①生成白色沉淀〔Mg (OH)
2
〕的化学方程式为: .
②三、解答题(共6小题,满分38分)
27.(6分)水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要关心水、
爱护水、节约用水.
(1)我国规定生活饮用水的水质必须达到下述四项指标:a.不得呈现异色b.不得有
异味c.应澄清透明d.不得含有细菌和病毒.其中“c指标”可以通过 操作达
到.
(2)生活中可以采用 区分硬水和软水,可以通过 的方法降低水的硬度.
(3)水的用途广泛,许多化学实验中用到水,请你列举一例:
(4)下列各种水中属于纯净物的是 (填序号).
矿泉水 自来水 蒸馏水 汽水 糖水
①(5)小明②家长期饮③用“××牌④纯净水”⑤,专家认为这是不科学的,理由是 .
28.(6分)已知:A、B、C、D、E、F是六种常见的物质,其中A是黑色固体,B是无
色无味的剧毒气体,C是紫红色金属单质.它们之间的转化关系如图:
请回答:
(1)写出下列物质的化学式:B 、C 、E .
(2)写出反应 的化学反应方程式: .
(3)写出反应① 的化学反应方程式: ;该反应属于基本反应类型中的
反应. ②
29.(7分)氨气是一种无色有刺激性气味、极易溶于水、密度比空气小的气体.某学习
小组在探究活动中要制取一定量的氨气,该小组查阅资料后,得知以下两种方法可以制
取氨气:
第一种方法:氮气与氢气在高温、高压、催化剂的条件下生成氨气;
第二种方法:氯化铵固体和熟石灰粉末在加热条件下生成氨气.
(1)该小组同学没有选择第一种方法制取氨气的原因是 .
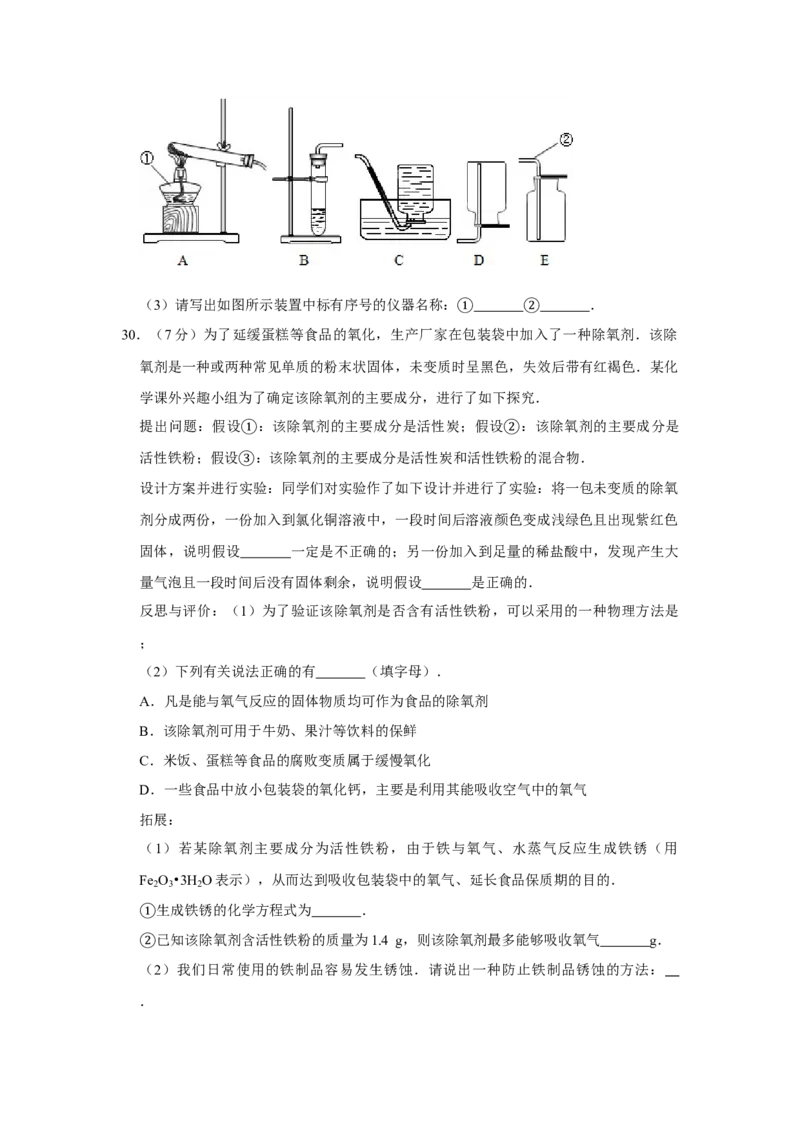
(2)在如图所示装置中,制取氨气的装置是 ,理由是 ;收集氨气的装
置是 ,理由是 .(3)请写出如图所示装置中标有序号的仪器名称: .
30.(7分)为了延缓蛋糕等食品的氧化,生产厂家在①包装袋中加②入了一种除氧剂.该除
氧剂是一种或两种常见单质的粉末状固体,未变质时呈黑色,失效后带有红褐色.某化
学课外兴趣小组为了确定该除氧剂的主要成分,进行了如下探究.
提出问题:假设 :该除氧剂的主要成分是活性炭;假设 :该除氧剂的主要成分是
活性铁粉;假设①:该除氧剂的主要成分是活性炭和活性铁②粉的混合物.
设计方案并进行③实验:同学们对实验作了如下设计并进行了实验:将一包未变质的除氧
剂分成两份,一份加入到氯化铜溶液中,一段时间后溶液颜色变成浅绿色且出现紫红色
固体,说明假设 一定是不正确的;另一份加入到足量的稀盐酸中,发现产生大
量气泡且一段时间后没有固体剩余,说明假设 是正确的.
反思与评价:(1)为了验证该除氧剂是否含有活性铁粉,可以采用的一种物理方法是
;
(2)下列有关说法正确的有 (填字母).
A.凡是能与氧气反应的固体物质均可作为食品的除氧剂
B.该除氧剂可用于牛奶、果汁等饮料的保鲜
C.米饭、蛋糕等食品的腐败变质属于缓慢氧化
D.一些食品中放小包装袋的氧化钙,主要是利用其能吸收空气中的氧气
拓展:
(1)若某除氧剂主要成分为活性铁粉,由于铁与氧气、水蒸气反应生成铁锈(用
Fe O •3H O表示),从而达到吸收包装袋中的氧气、延长食品保质期的目的.
2 3 2
生成铁锈的化学方程式为 .
①已知该除氧剂含活性铁粉的质量为1.4 g,则该除氧剂最多能够吸收氧气 g.
②(2)我们日常使用的铁制品容易发生锈蚀.请说出一种防止铁制品锈蚀的方法:
.31.(6分)据有关专家介绍,用醋酸蒸气对空气进行消毒可以有效地预防流感.某学校
在每间教室用120g 10%的醋酸(CH COOH)水溶液加热制取蒸气进行空气消毒处理.
3
请计算:
(1)醋酸的相对分子质量为 .
(2)120g 10%的醋酸溶液中含水 g.
(3)120g 10%醋酸溶液中氧元素的质量是多少?(要求写出计算过程)
32.(6分)在一次化学课外活动中,化学老师给小亮同学 30g NaCl固体样品(含有
CuCl 杂质),要求用所提供的试剂:一定质量分数的氢氧化钠溶液、氢氧化钾溶液、
2
稀盐酸各100g,通过实验将CuCl 除去(不引进其它杂质)并测出其中所含氯化铜的质
2
量分数.小亮同学通过思考并查阅有关溶解度数据以后,很快完成了老师交给的任务.
他的方法是:将30g NaCl样品加入100g水中,固体全部溶解后再逐渐加入所选试剂,
当加入的试剂质量为56g时,恰好完全反应,测得生成的沉淀为4.9g.请回答:
(1)该同学所选用的试剂是 .
(2)该30g NaCl样品中所含氯化铜的质量分数是多少?(要求写出计算过程)
(3)当恰好完全反应时,所得溶液的质量是多少?(要求写出计算过程)