文档内容
2012年湖南省怀化市中考化学试卷
一、我能选择(每小题只有一个正确选项,每小题2分,共40分)
1.(2分)下列过程一定包含化学变化的是( )
A.轮胎爆炸 B.清洗蔬菜 C.榨甘蔗汁 D.蜡烛燃烧
2.(2分)下列粒子中不能直接构成物质的是( )
A.核外电子 B.原子 C.分子 D.离子
3.(2分)下列物质中,属于氧化物的是( )
A.NaCl B.CaO C.NaOH D.H SO
2 4
4.(2分)下列做法不会对环境造成危害的是( )
A.使用后的塑料袋随意丢弃
B.大量使用化肥农药
C.工业废水、生活污水处理达标后排放
D.废旧电池已无用处,不需要回收
5.(2分)造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
A.分子很小 B.分子之间有间隙
C.分子在不断运动 D.分子由原子构成
6.(2分)下列化学符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是(
)
A.Cu B.O C.H D.C
2 60
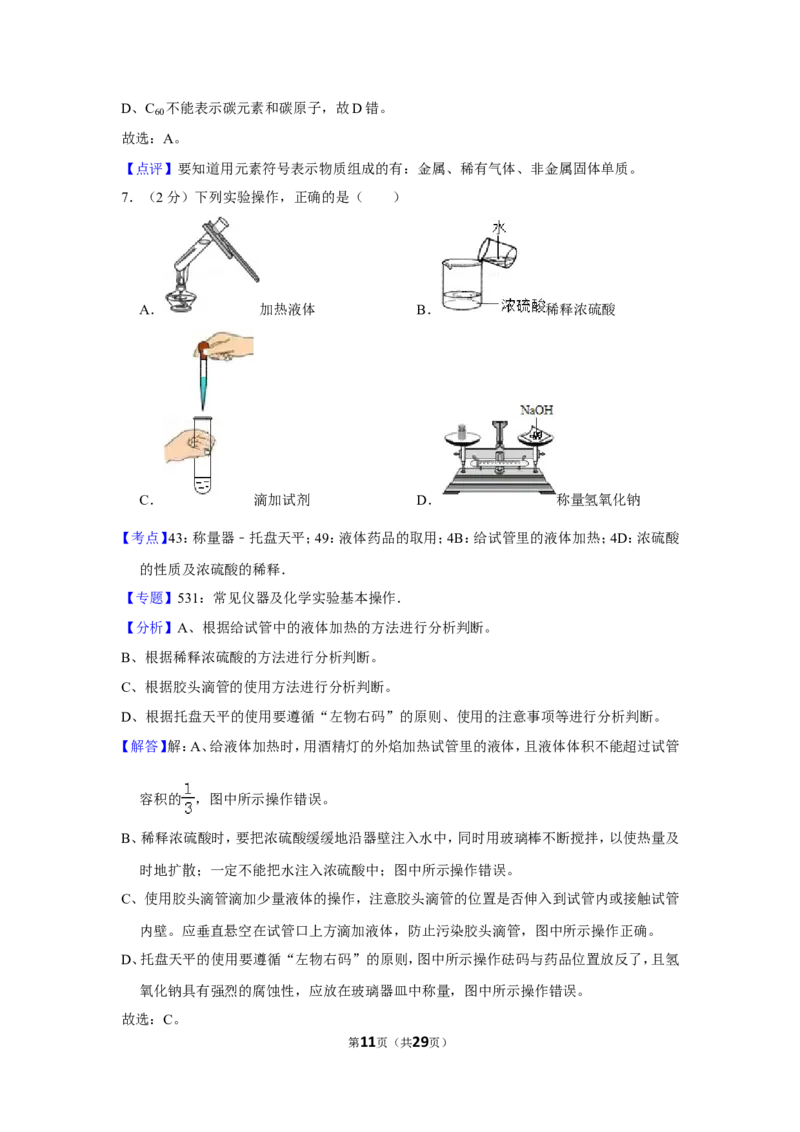
7.(2分)下列实验操作,正确的是( )
A. 加热液体 B. 稀释浓硫酸
C. 滴加试剂 D. 称量氢氧化钠
第1页(共29页)8.(2分)食品安全与人体健康密切相关,下列做法不会损害人体健康的是( )
A.用含小苏打的发酵粉焙制糕点
B.用废弃皮革制成的工业明胶添加到果冻、酸奶、冰淇淋等食品中
C.用霉变花生制成的花生油烹调食品
D.用“淋巴肉”制水饺肉馅
9.(2分)氮肥、磷肥和钾肥是最主要的化学肥料,下列物质中属于复合肥的是( )
A.NH HCO B.Ca (PO ) C.KCl D.KNO
4 3 3 4 2 3
10.(2分)市场上有“加碘食盐”、“富哂酱油”、“高钙牛奶”等商品,这里的“碘、哂、
钙”指的是( )
A.原子 B.分子 C.单质 D.元素
11.(2分)形成酸雨的主要气体是( )
A.CO B.SO C.CO D.O
2 2 3
12.(2分)下列说法不正确的是( )
A.利用木炭的还原性由CuO冶炼铜
B.天然金刚石是最硬的非金属单质,可制成钻石
C.利用活性炭的稳定性来吸附冰箱中的异味
D.利用石墨的导电性制造石墨电极
13.(2分)下列溶液中,能使酚酞试液变红的是( )
A.烧碱溶液 B.稀硫酸 C.稀盐酸 D.醋酸溶液
14.(2分)下列叙述正确的是( )
A.木炭在充足的氧气中燃烧生成一氧化碳
B.硫在氧气中燃烧发出蓝紫色火焰
C.铁丝在氧气中燃烧火星四射,生成三氧化二铁
D.红磷在空气中燃烧产生大量的白雾
15.(2分)第16界世界气候大会于2011年12月在南非德班召开,会议的主题是“促进低碳
经济,减少二氧化碳的排放”。下列做法不符合这一主题的是( )
A.开发新能源(太阳能、潮汐能、风能等),减少化石燃料的使用
B.限制化工发展,关停化工企业,消除污染源头
C.用第四代LED绿色光源代替白炽灯
D.加快研发利用二氧化碳合成聚碳酸酯类可降解塑料
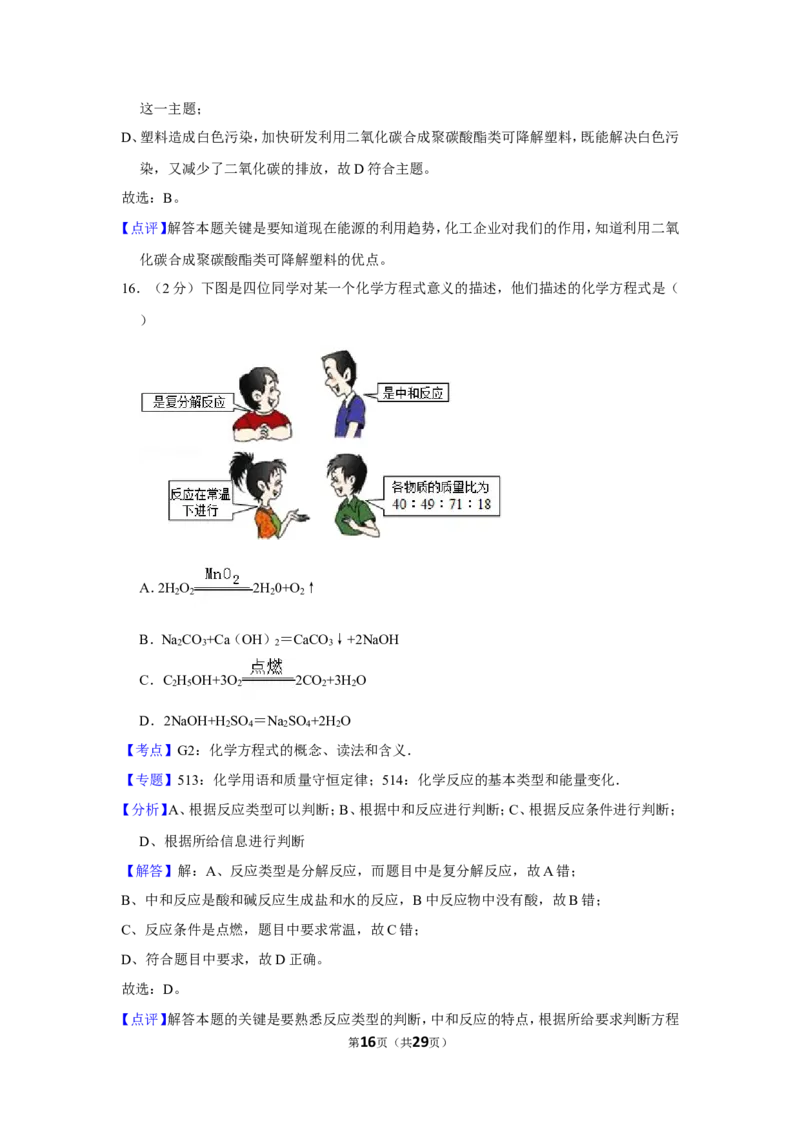
16.(2分)下图是四位同学对某一个化学方程式意义的描述,他们描述的化学方程式是(
第2页(共29页))
A.2H O 2H 0+O ↑
2 2 2 2
B.Na CO +Ca(OH)=CaCO ↓+2NaOH
2 3 2 3
C.C H OH+3O 2CO +3H O
2 5 2 2 2
D.2NaOH+H SO =Na SO +2H O
2 4 2 4 2
17.(2分)下列说法正确的是( )
A.电解水产生氢气和氧气,说明水是由氢分子和氧分子构成的
B.用洗洁精洗涤油腻的碗碟,是利用了溶解的原理
C.蒸馏是净化程度最高的净水方法
D.我国金属资源丰富,废旧金属根本不用回收
18.(2分)2011年9月12日,中国科学家屠呦呦荣获拉克斯﹣﹣狄蓓吉临床医学研究奖,以
表彰她发现的一种药物﹣﹣青蒿素,它是治疗疟疾的特效药,化学式是C H O .下列有
15 22 5
关青蒿素的说法正确的是( )
A.“青蒿素”是混合物
B.“青蒿素”含42个原子
C.“青蒿素”中碳元素的质量分数是6.38%
D.“青蒿素”中碳、氢、氧三种元素的质量比是90:11:40
19.(2分)下列物质不能区分氧气和二氧化碳的是( )
A.澄清石灰水 B.稀硫酸
C.燃烧的火柴 D.紫色石蕊试液
20.(2分)在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质
的质量如下表:
第3页(共29页)物质 甲 乙 丙 丁
反应前质量/g 3 5 20 7
反应后质量/g 10 5 8 待测
通过分析,判断下列说法正确的是( )
A.测得反应后丁物质的质量为12g
B.乙物质一定是催化剂
C.该反应是化合反应
D.该反应是复分解反应
二、我会填空(每空1分,共20分)
21.(3分)请从氢气、浓硫酸、蛋白质、淀粉几种物质中选择适当的物质,按要求填空:
(1)可做高能清洁燃料的是 。(写化学式)
(2)具有强烈腐蚀性的是 。(写名称)
(3) (写名称)是构成细胞的基本物质,是重要的营养物质,处在生长发育期的青少年
每天至少需摄取70克。
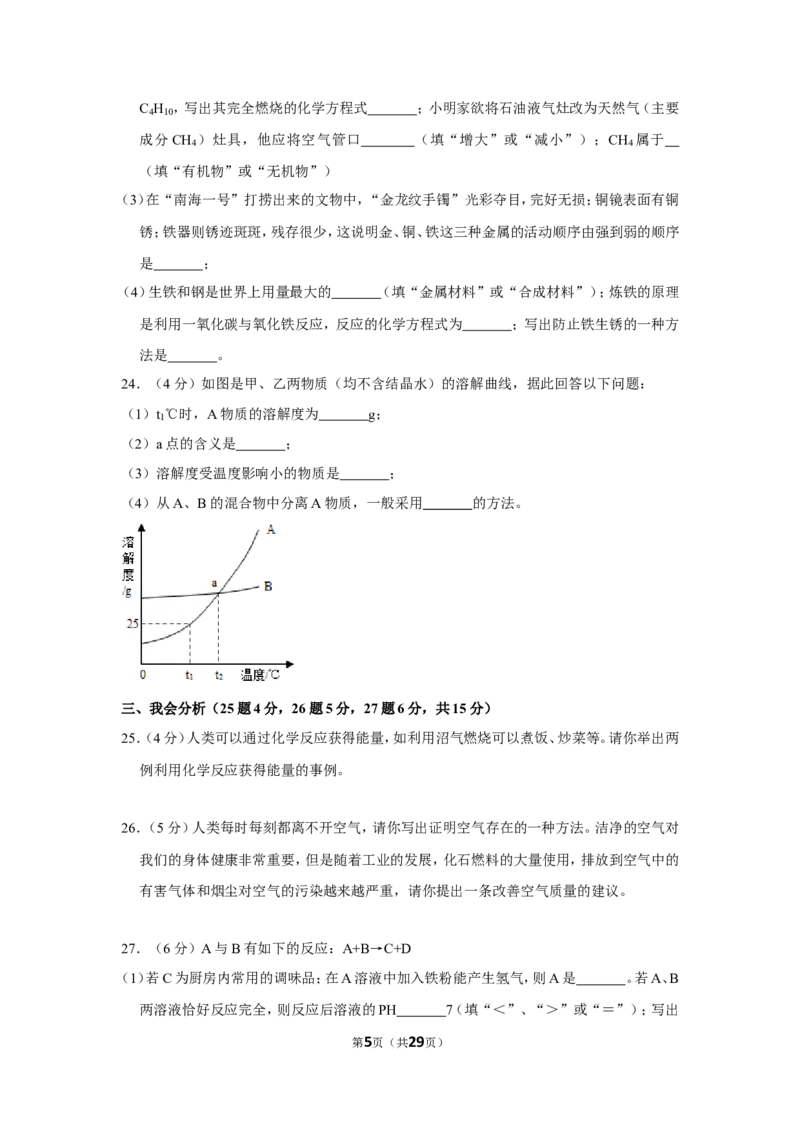
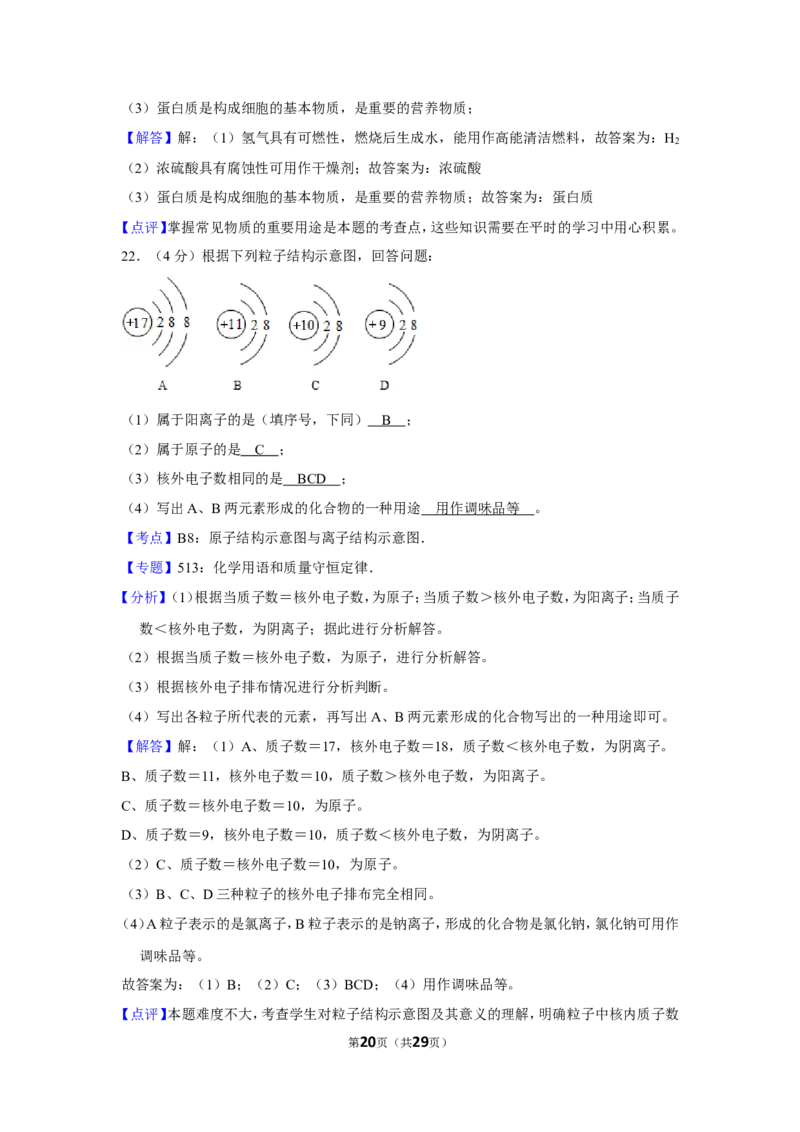
22.(4分)根据下列粒子结构示意图,回答问题:
(1)属于阳离子的是(填序号,下同) ;
(2)属于原子的是 ;
(3)核外电子数相同的是 ;
(4)写出A、B两元素形成的化合物的一种用途 。
23.(9分)南海是中国四大海域中最大、最深、自然资源最为丰富的海域,南海不但资源丰富,
还是亚太地区海运的“咽喉要道”,这里有世界上最繁忙的航线,因此引起周边国家的窥
视。
(1)海水属于 (填“纯净物”或“混合物”);海水晒盐属于混合物分离操作的是
。(填序号)
A、蒸馏 B、蒸发 C、过滤 D、沉淀
(2)南海油气资源丰富,石油加工可得到石油液化气,假设某石油液化气的主要成分为
第4页(共29页)C H ,写出其完全燃烧的化学方程式 ;小明家欲将石油液气灶改为天然气(主要
4 10
成分CH )灶具,他应将空气管口 (填“增大”或“减小”);CH 属于
4 4
(填“有机物”或“无机物”)
(3)在“南海一号”打捞出来的文物中,“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜
锈;铁器则锈迹斑斑,残存很少,这说明金、铜、铁这三种金属的活动顺序由强到弱的顺序
是 ;
(4)生铁和钢是世界上用量最大的 (填“金属材料”或“合成材料”);炼铁的原理
是利用一氧化碳与氧化铁反应,反应的化学方程式为 ;写出防止铁生锈的一种方
法是 。
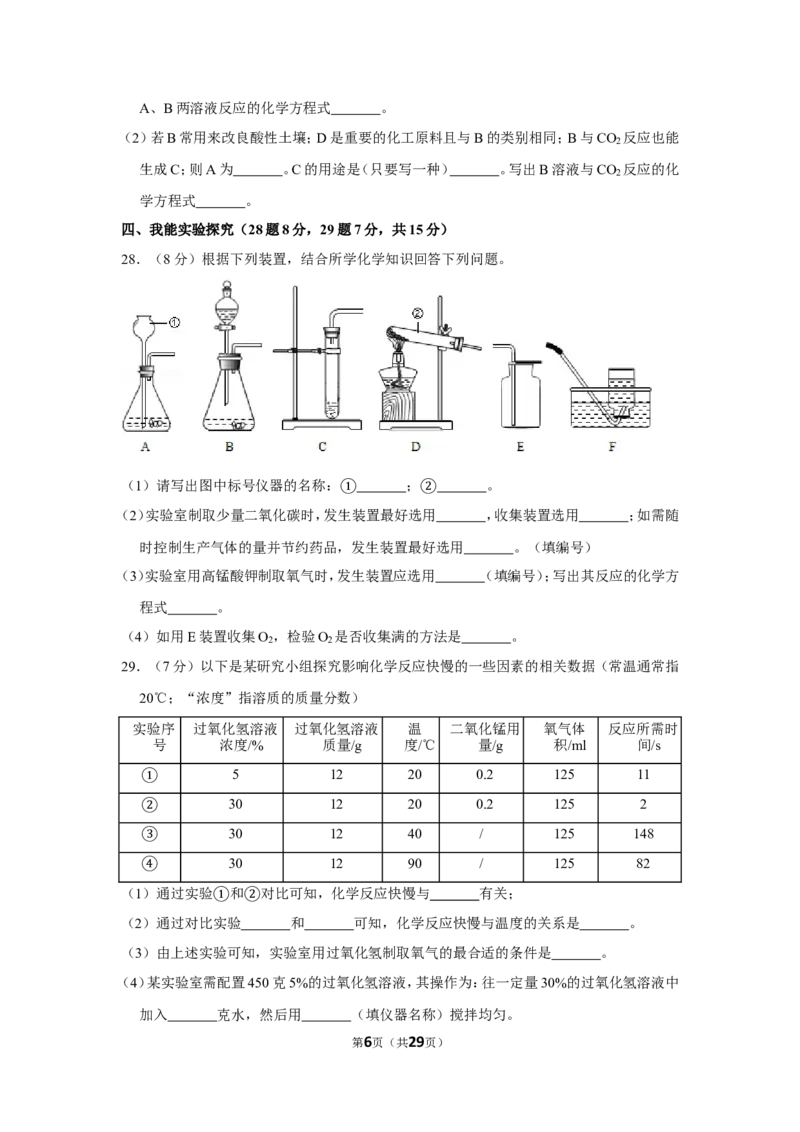
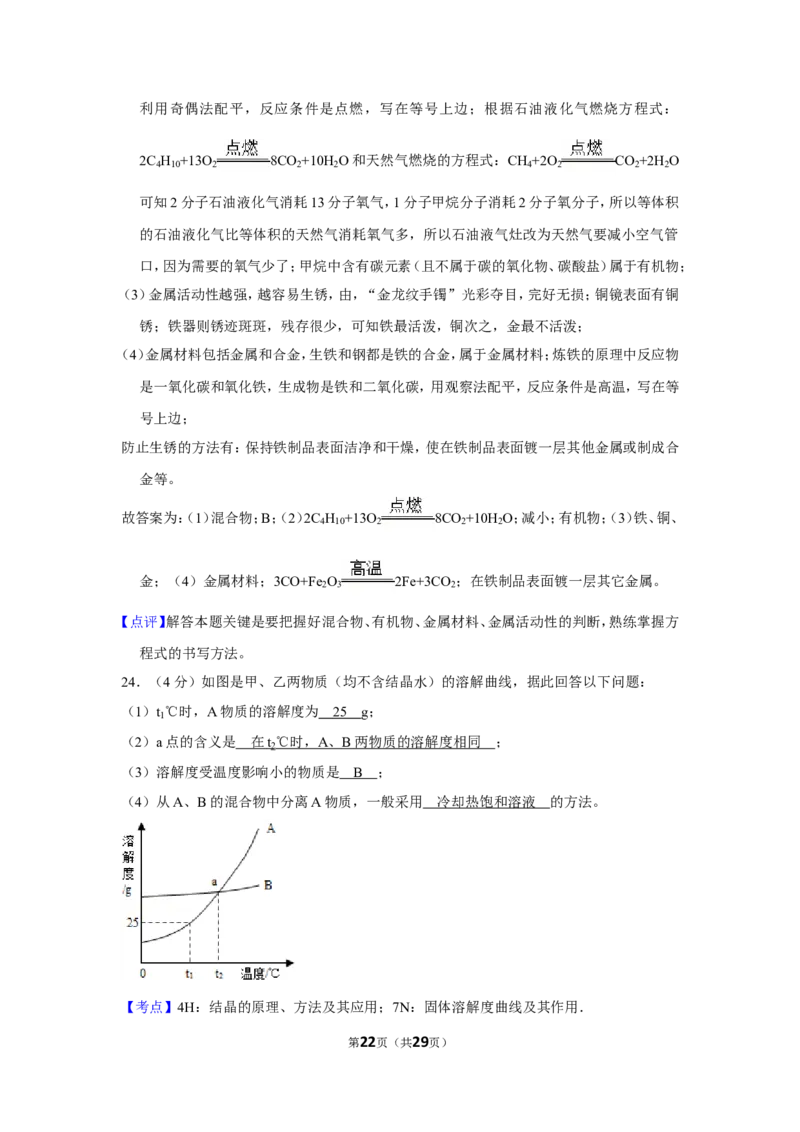
24.(4分)如图是甲、乙两物质(均不含结晶水)的溶解曲线,据此回答以下问题:
(1)t ℃时,A物质的溶解度为 g;
1
(2)a点的含义是 ;
(3)溶解度受温度影响小的物质是 ;
(4)从A、B的混合物中分离A物质,一般采用 的方法。
三、我会分析(25题4分,26题5分,27题6分,共15分)
25.(4分)人类可以通过化学反应获得能量,如利用沼气燃烧可以煮饭、炒菜等。请你举出两
例利用化学反应获得能量的事例。
26.(5分)人类每时每刻都离不开空气,请你写出证明空气存在的一种方法。洁净的空气对
我们的身体健康非常重要,但是随着工业的发展,化石燃料的大量使用,排放到空气中的
有害气体和烟尘对空气的污染越来越严重,请你提出一条改善空气质量的建议。
27.(6分)A与B有如下的反应:A+B→C+D
(1)若C为厨房内常用的调味品;在A溶液中加入铁粉能产生氢气,则A是 。若A、B
两溶液恰好反应完全,则反应后溶液的PH 7(填“<”、“>”或“=”);写出
第5页(共29页)A、B两溶液反应的化学方程式 。
(2)若B常用来改良酸性土壤;D是重要的化工原料且与B的类别相同;B与CO 反应也能
2
生成C;则A为 。C的用途是(只要写一种) 。写出B溶液与CO 反应的化
2
学方程式 。
四、我能实验探究(28题8分,29题7分,共15分)
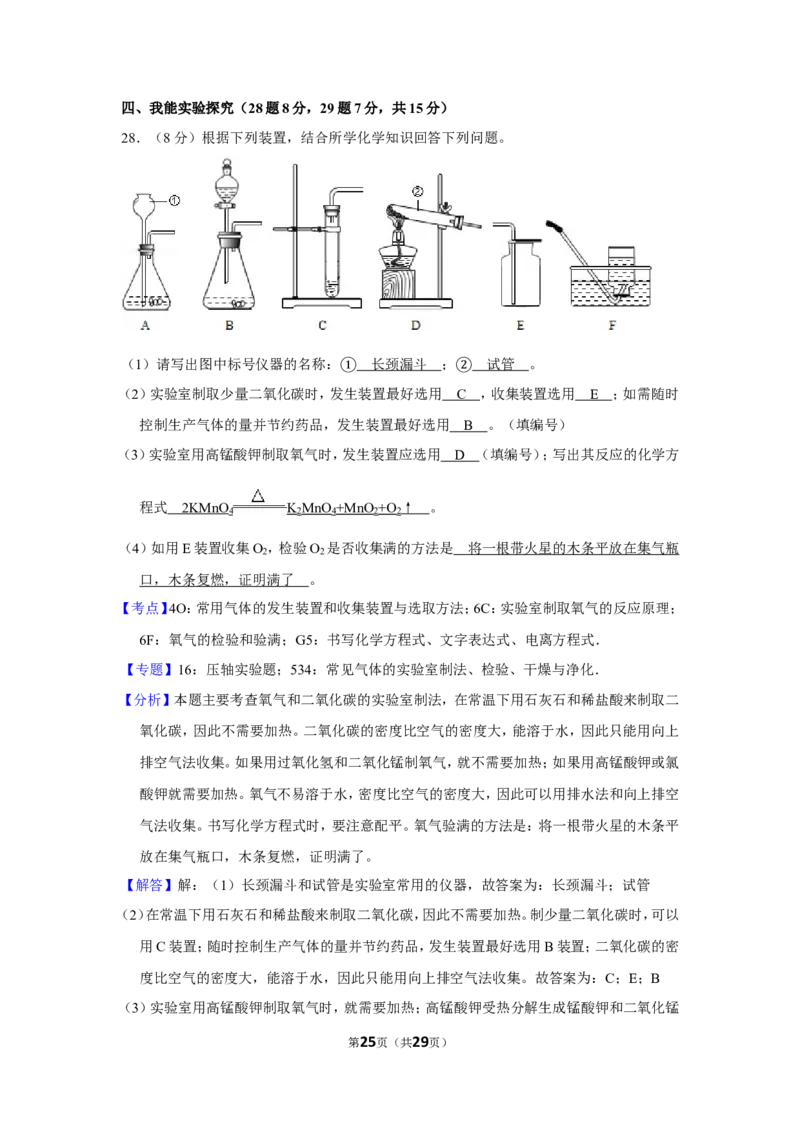
28.(8分)根据下列装置,结合所学化学知识回答下列问题。
(1)请写出图中标号仪器的名称: ; 。
(2)实验室制取少量二氧化碳时,发生①装置最好选②用 ,收集装置选用 ;如需随
时控制生产气体的量并节约药品,发生装置最好选用 。(填编号)
(3)实验室用高锰酸钾制取氧气时,发生装置应选用 (填编号);写出其反应的化学方
程式 。
(4)如用E装置收集O ,检验O 是否收集满的方法是 。
2 2
29.(7分)以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指
20℃;“浓度”指溶质的质量分数)
实验序 过氧化氢溶液 过氧化氢溶液 温 二氧化锰用 氧气体 反应所需时
号 浓度/% 质量/g 度/℃ 量/g 积/ml 间/s
5 12 20 0.2 125 11
① 30 12 20 0.2 125 2
② 30 12 40 / 125 148
③ 30 12 90 / 125 82
(1④)通过实验 和 对比可知,化学反应快慢与 有关;
(2)通过对比①实验 ② 和 可知,化学反应快慢与温度的关系是 。
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是 。
(4)某实验室需配置450克5%的过氧化氢溶液,其操作为:往一定量30%的过氧化氢溶液中
加入 克水,然后用 (填仪器名称)搅拌均匀。
第6页(共29页)五、我会计算(30题4分,31题6分,共10分)
30.(4分)已知R+H SO =RSO +H ↑,若13克金属R与足量稀硫酸完全反应可制得0.4克
2 4 4 2
氢气。试分析:
(1)RSO 中R的化合价为 。
4
(2)通过计算确定R的相对原子质量。
31.(6分)未成年人和老年人是需要补钙的主要人群,目前市面上有许多补钙的钙片出售,
如图是盖中盖高钙片的部分说明,某课外兴趣小组欲检验说明的真伪,进行了入下的实验:
盖中盖高钙片
【主要原料】碳酸钙、维生素D
【功效成分】每片含:钙500mg、维生素D100IU
【用法用量】每日1片,嚼食。
【适宜人群】需要补钙者。
【注意事项】
1、本品不能代替药物。
2、不宜超过推荐量或与同类营养素补充剂同时食用。
【规格】2.5g×36片
取1片片剂研碎
①将其加入足量稀盐酸中
②完全反应后收集到0.55g二氧化碳
③试分析:
(1)未成年人缺钙会得 。(填序号)
A、坏血症 B、贫血 C、佝偻病 D、甲状腺肿大
(2)通过计算判断此钙片中钙含量与标注是否属实。(假定钙片中其他成份不与盐酸反应,1g
=1000mg)
第7页(共29页)2012 年湖南省怀化市中考化学试卷
参考答案与试题解析
一、我能选择(每小题只有一个正确选项,每小题2分,共40分)
1.(2分)下列过程一定包含化学变化的是( )
A.轮胎爆炸 B.清洗蔬菜 C.榨甘蔗汁 D.蜡烛燃烧
【考点】E3:化学变化和物理变化的判别.
【专题】512:物质的变化与性质.
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化
和物理变化的本质区别是否有新物质生成;据此分析判断。
【解答】解:A、轮胎爆炸的过程中只是轮胎的形状发生改变,没有新物质生成,属于物理变化。
B、清洗蔬菜的过程中只是将泥沙等蔬菜表面的杂质与蔬菜分离,没有新物质生成,属于物理
变化。
C、榨甘蔗汁的过程中只是从甘蔗中分离出甘蔗汁,没有新物质生成,属于物理变化。
D、蜡烛燃烧的过程中有新物质二氧化碳和水生成,属于化学变化。
故选:D。
【点评】本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于
物理变化,若有新物质生成属于化学变化。
2.(2分)下列粒子中不能直接构成物质的是( )
A.核外电子 B.原子 C.分子 D.离子
【考点】B2:分子、原子、离子、元素与物质之间的关系.
【专题】511:物质的微观构成与物质的宏观组成.
【分析】构成物质的基本粒子有分子、原子和离子,据此进行分析判断即可。
【解答】解:A、核外电子是构成原子的一种粒子,不能直接构成物质。
B、原子是构成物质的一种粒子,有些物质是由原子直接构成的,金属和固态非金属单质等是
由原子直接构成的。
C、分子是构成物质的一种粒子,有些物质是由分子直接构成的,如水是由水分子构成的,氧
气是由氧分子构成的。
D、离子是构成物质的一种粒子,有些物质是由离子直接构成的,如氯化钠是由钠离子和氯离
子构成的。
第8页(共29页)故选:A。
【点评】本题难度不大,主要考查了构成物质的微观粒子方面的知识,掌握常见物质的粒子构
成是正确解答本题的关键。
3.(2分)下列物质中,属于氧化物的是( )
A.NaCl B.CaO C.NaOH D.H SO
2 4
【考点】A3:从组成上识别氧化物.
【专题】516:物质的分类.
【分析】根据氧化物的概念:氧化物是只含有两种元素且其中一种元素是氧元素的化合物,据
此进行分析解答。
【解答】解:A、NaCl是由钠、氯两种元素组成的化合物,不含氧元素,不属于氧化物,故选项
错误。
B、CaO是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,故选项正确。
C、NaOH是由钠、氧、氢三种元素组成的化合物,不属于氧化物,故选项错误。
D、H SO 是由氢、硫、氧三种元素组成的化合物,不属于氧化物,故选项错误。
2 4
故选:B。
【点评】本题难度不大,考查氧化物的判断,抓住氧化物的特征、熟悉常见的物质的组成是正
确解答本题的关键。
4.(2分)下列做法不会对环境造成危害的是( )
A.使用后的塑料袋随意丢弃
B.大量使用化肥农药
C.工业废水、生活污水处理达标后排放
D.废旧电池已无用处,不需要回收
【考点】79:水资源的污染与防治;8J:废弃金属对环境的污染;I6:白色污染与防治;K6:合理
使用化肥、农药对保护环境的重要意义.
【专题】212:化学与环境保护.
【分析】A、使用后的塑料袋随意丢弃会造成白色污染;
B、大量使用化肥农药会污染环境;
C、工业废水、生活污水处理达标后排放,可以保护水体;
D、废旧电池随意乱扔会污染环境。
【解答】解:A、使用后的塑料袋随意丢弃会造成白色污染,故A不符合题意;
B、大量使用化肥农药会污染土壤和水体,造成环境污染,故B不符合题意;
第9页(共29页)C、工业废水、生活污水处理达标后排放,可以保护水体,不会造成环境污染,故C符合题意;
D、废旧电池随意乱扔会污染水体和土壤,所以应该回收,故D不符合题意。
故选:C。
【点评】本题主要考查人们的环保意识,要树立保护环境的意识,保护环境人人有责。
5.(2分)造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
A.分子很小 B.分子之间有间隙
C.分子在不断运动 D.分子由原子构成
【考点】B9:利用分子与原子的性质分析和解决问题.
【专题】511:物质的微观构成与物质的宏观组成.
【分析】根据分子的性质进行分析,烟草在燃烧的过程中会产生如CO、尼古丁、焦油等对人体
有害的物质。构成这些有害物质的微粒会不断运动,从而造成他人被动吸烟,也就是常说
的“二手烟”。
【解答】解:由于烟草在燃烧的过程中会产生如CO、尼古丁、焦油等对人体有害的物质。构成
这些有害物质的微粒会不断运动,从而造成他人被动吸烟,也就是常说的“二手烟”。因
此在公共场所应禁止吸烟。
A、由分子的性质可知,吸食“二手烟”的主要原因与分子的大小无关,故A错误;
B、由分子的性质可知,吸食“二手烟”的主要原因与分子之间有间隙无关,故B 错误;
C、由于分子在不断运动,这是造成吸食“二手烟”的主要原因,故C正确;
D、吸食“二手烟”的主要原因与分子的构成没有关系,故D错误。
故选:C。
【点评】准确理解分子的性质,会应用微粒的基本性质解释某些生活中的现象。
6.(2分)下列化学符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是(
)
A.Cu B.O C.H D.C
2 60
【考点】C3:元素的符号及其意义;D1:化学式的书写及意义.
【专题】513:化学用语和质量守恒定律.
【分析】既能表示一个原子,又能表示一种元素说明是元素符号,还能表示一种物质说明该物
质是用元素符号直接表示的,有金属、稀有气体、非金属固体单质。
【解答】解:A、Cu表示铜元素、一个铜原子、铜这种物质,故A正确;
B、O能表示一个原子,又能表示一种元素,不能表示物质,需在右下角放上数字2,故B错;
C、H 不能表示氢元素和氢原子,故C错;
2
第10页(共29页)D、C 不能表示碳元素和碳原子,故D错。
60
故选:A。
【点评】要知道用元素符号表示物质组成的有:金属、稀有气体、非金属固体单质。
7.(2分)下列实验操作,正确的是( )
A. 加热液体 B. 稀释浓硫酸
C. 滴加试剂 D. 称量氢氧化钠
【考点】43:称量器﹣托盘天平;49:液体药品的取用;4B:给试管里的液体加热;4D:浓硫酸
的性质及浓硫酸的稀释.
【专题】531:常见仪器及化学实验基本操作.
【分析】A、根据给试管中的液体加热的方法进行分析判断。
B、根据稀释浓硫酸的方法进行分析判断。
C、根据胶头滴管的使用方法进行分析判断。
D、根据托盘天平的使用要遵循“左物右码”的原则、使用的注意事项等进行分析判断。
【解答】解:A、给液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管
容积的 ,图中所示操作错误。
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及
时地扩散;一定不能把水注入浓硫酸中;图中所示操作错误。
C、使用胶头滴管滴加少量液体的操作,注意胶头滴管的位置是否伸入到试管内或接触试管
内壁。应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作正确。
D、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,且氢
氧化钠具有强烈的腐蚀性,应放在玻璃器皿中称量,图中所示操作错误。
故选:C。
第11页(共29页)【点评】本题难度不大,掌握常见仪器的名称、用途、使用注意事项及常见化学实验操作的注
意事项等是正确解题的关键。
8.(2分)食品安全与人体健康密切相关,下列做法不会损害人体健康的是( )
A.用含小苏打的发酵粉焙制糕点
B.用废弃皮革制成的工业明胶添加到果冻、酸奶、冰淇淋等食品中
C.用霉变花生制成的花生油烹调食品
D.用“淋巴肉”制水饺肉馅
【考点】9G:常用盐的用途;J3:亚硝酸钠、甲醛等化学品的性质与人体健康.
【专题】211:化学与生活健康.
【分析】A、根据小苏打的用途考虑;B、根据废弃皮革制成的工业明胶的危害考虑;C、根据霉
变花生米的危害考虑;D、根据淋巴肉的危害考虑。
【解答】解:A、小苏打是碳酸氢钠的俗称,常用的用途是作发酵粉焙制糕点,故A正确;
B、由废皮革制成的明胶,其中往往含有重铬酸钾和重铬酸钠。用这种原料生产水解蛋白,过
程中会产生大量重金属六价铬等有毒化合物。故B错;
C、霉变花生中含有致癌物,故C错;
D、所谓淋巴肉,是指未摘除腺体的猪、牛、羊血脖肉和喉气管肉。由于淋巴是动物的免疫器
官,含有大量吞噬细胞,吞噬各种细菌和病毒,而且还有大量致癌物质,人一旦食用,很可
能引起人体免疫功能低下,尤其是没有经过检疫的猪淋巴,危害更大,故D错。
故选:A。
【点评】解答本题关键是要知道小苏打的用途,由废皮革制成的明胶的危害,霉变花生、淋巴
肉的危害。
9.(2分)氮肥、磷肥和钾肥是最主要的化学肥料,下列物质中属于复合肥的是( )
A.NH HCO B.Ca (PO ) C.KCl D.KNO
4 3 3 4 2 3
【考点】9J:常见化肥的种类和作用.
【专题】527:常见的盐 化学肥料.
【分析】含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾
肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥。
【解答】解:A、NH HCO 中含有氮元素,属于氮肥。
4 3
B、Ca (PO ) 中含有磷元素,属于磷肥。
3 4 2
C、KCl中含有钾元素,属于钾肥。
D、KNO 中含有钾元素和氮元素,属于复合肥。
3
第12页(共29页)故选:D。
【点评】本题主要考查化肥的分类方面的知识,解答时要分析化肥中含有哪些营养元素,然后
再根据化肥的分类方法确定化肥的种类。
10.(2分)市场上有“加碘食盐”、“富哂酱油”、“高钙牛奶”等商品,这里的“碘、哂、
钙”指的是( )
A.原子 B.分子 C.单质 D.元素
【考点】C1:元素的概念.
【专题】511:物质的微观构成与物质的宏观组成.
【分析】“加碘食盐”、“富哂酱油”、“高钙牛奶”等商品中的“碘、哂、钙”不是以单质、
分子、原子等形式存在,而是指元素。
【解答】解:“加碘食盐”、“富哂酱油”、“高钙牛奶”等商品中的“碘、哂、钙”不是以单
质、分子、原子等形式存在,这里所指的“碘、哂、钙”是强调存在的元素,与具体形态无
关。
故选:D。
【点评】本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正
确解答此类试题的关键。
11.(2分)形成酸雨的主要气体是( )
A.CO B.SO C.CO D.O
2 2 3
【考点】9C:酸雨的产生、危害及防治.
【专题】212:化学与环境保护.
【分析】酸雨主要由化石燃料燃烧产生的二氧化硫、氮氧化物等酸性气体,经过复杂的大气化
学反应,被雨水吸收溶解而成,据此分析解答即可;
【解答】解:A、二氧化碳是大气的成分之一,含量过多会形成温室效应,与水反应生成的碳酸
酸性很弱不会形成酸雨,故错误;
B、二氧化硫能和水反应生成亚硫酸,当雨水的pH<5.6时就形成酸雨。故正确;
C、一氧化碳虽有毒,但不与水反应,不会形成酸雨,故错误;
D、臭氧是一种氧的单质,能阻挡紫外线,但不是形成酸雨的气体,故错误。
故选:B。
【点评】解答本题要掌握各种物质的性质方面的知识,只有这样才能对相关方面的问题做出
正确的判断。
12.(2分)下列说法不正确的是( )
第13页(共29页)A.利用木炭的还原性由CuO冶炼铜
B.天然金刚石是最硬的非金属单质,可制成钻石
C.利用活性炭的稳定性来吸附冰箱中的异味
D.利用石墨的导电性制造石墨电极
【考点】C6:碳单质的物理性质及用途;C7:碳的化学性质.
【专题】523:碳单质与含碳化合物的性质与用途.
【分析】碳元素组成的单质包括它们都是由碳元素组成的,碳的单质由于其结构不同物理性
质不同,但化学性质相同,主要有在常温下不活泼,碳的可燃性及还原性,据此分析解答
即可;
【解答】解:A、木炭具有还原性,所以可以利用木炭还原氧化铜而得到单质的铜;
B、金刚石是天然物质中最硬的非金属单质,所以可以制成钻石,作为装饰品耐磨且恒久;
C、利用活性炭吸附冰箱中的异味,是根据活性炭具有吸附性;
D、石墨可以导电,所以可用来制造石墨电极;
故选:C。
【点评】本题主要考查碳单质的性质,解答的关键是要掌握各种物质的性质,只有掌握了物质
的性质才能确定物质的用途。
13.(2分)下列溶液中,能使酚酞试液变红的是( )
A.烧碱溶液 B.稀硫酸 C.稀盐酸 D.醋酸溶液
【考点】91:酸碱指示剂及其性质.
【专题】151:课本知识同类信息.
【分析】能使酚酞试液变红的溶液呈碱性,据此对选项中的溶液酸碱性进行判断分析即可。
【解答】解:A、烧碱溶液即氢氧化钠溶液呈碱性,能使酚酞试液变红;
B、稀硫酸溶液呈酸性,不能使酚酞变色;
C、稀盐酸溶液呈酸性,不能使酚酞变色;
D、醋酸即乙酸溶液呈酸性,不能使酚酞变色;
故选:A。
【点评】本题考查了指示剂酚酞在酸碱性溶液中的变色情况,利用了碱性溶液能使酚酞变红
的知识,属基础性知识考查题。
14.(2分)下列叙述正确的是( )
A.木炭在充足的氧气中燃烧生成一氧化碳
B.硫在氧气中燃烧发出蓝紫色火焰
第14页(共29页)C.铁丝在氧气中燃烧火星四射,生成三氧化二铁
D.红磷在空气中燃烧产生大量的白雾
【考点】6A:氧气与碳、磷、硫、铁等物质的反应现象.
【专题】532:实验现象的观察和记录.
【分析】A、根据木炭的化学性质进行分析判断。
B、根据硫在氧气中燃烧的现象进行分析判断。
C、根据铁丝在氧气中燃烧的现象进行分析判断。
D、根据红磷在空气中燃烧的现象进行分析判断。
【解答】解:A、木炭在充足的氧气中燃烧生成二氧化碳,故选项说法错误。
B、硫在氧气中燃烧,发出明亮的蓝紫色火焰,故选项说法正确。
C、铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁而不是三氧化二铁,故选项说法错误。
D、红磷在空气中燃烧,产生大量的白烟,而不是白雾,故选项说法错误。
故选:B。
【点评】本题难度不大,掌握氧气的化学性质、常见物质燃烧的现象即可正确解答;在描述物
质燃烧的现象时,需要注意光和火焰、烟和雾的区别。
15.(2分)第16界世界气候大会于2011年12月在南非德班召开,会议的主题是“促进低碳
经济,减少二氧化碳的排放”。下列做法不符合这一主题的是( )
A.开发新能源(太阳能、潮汐能、风能等),减少化石燃料的使用
B.限制化工发展,关停化工企业,消除污染源头
C.用第四代LED绿色光源代替白炽灯
D.加快研发利用二氧化碳合成聚碳酸酯类可降解塑料
【考点】6I:自然界中的碳循环.
【专题】212:化学与环境保护.
【分析】A、根据化石燃料的缺点考虑;B、根据化工企业的作用考虑;C、根据第四代LED绿色
光源的优点考虑;D、根据塑料造成白色污染考虑。
【解答】解:A、化石燃料中含有大量的碳元素,化石燃料使用时会产生大量的二氧化碳,所以
要开发新能源(太阳能、潮汐能、风能等),减少化石燃料的使用,就能减少二氧化碳的释
放,故A符合主题;
B、化工企业对人类经济的发展起决定作用,所以不能关停,而应该减少污染,工业三废经处
理后再排放,故B不符合这一主题;
C、第四代LED绿色光源既节能又环保,所以用第四代LED绿色光源代替白炽灯,故C符合
第15页(共29页)这一主题;
D、塑料造成白色污染,加快研发利用二氧化碳合成聚碳酸酯类可降解塑料,既能解决白色污
染,又减少了二氧化碳的排放,故D符合主题。
故选:B。
【点评】解答本题关键是要知道现在能源的利用趋势,化工企业对我们的作用,知道利用二氧
化碳合成聚碳酸酯类可降解塑料的优点。
16.(2分)下图是四位同学对某一个化学方程式意义的描述,他们描述的化学方程式是(
)
A.2H O 2H 0+O ↑
2 2 2 2
B.Na CO +Ca(OH)=CaCO ↓+2NaOH
2 3 2 3
C.C H OH+3O 2CO +3H O
2 5 2 2 2
D.2NaOH+H SO =Na SO +2H O
2 4 2 4 2
【考点】G2:化学方程式的概念、读法和含义.
【专题】513:化学用语和质量守恒定律;514:化学反应的基本类型和能量变化.
【分析】A、根据反应类型可以判断;B、根据中和反应进行判断;C、根据反应条件进行判断;
D、根据所给信息进行判断
【解答】解:A、反应类型是分解反应,而题目中是复分解反应,故A错;
B、中和反应是酸和碱反应生成盐和水的反应,B中反应物中没有酸,故B错;
C、反应条件是点燃,题目中要求常温,故C错;
D、符合题目中要求,故D正确。
故选:D。
【点评】解答本题的关键是要熟悉反应类型的判断,中和反应的特点,根据所给要求判断方程
第16页(共29页)式正误的方法。
17.(2分)下列说法正确的是( )
A.电解水产生氢气和氧气,说明水是由氢分子和氧分子构成的
B.用洗洁精洗涤油腻的碗碟,是利用了溶解的原理
C.蒸馏是净化程度最高的净水方法
D.我国金属资源丰富,废旧金属根本不用回收
【考点】71:电解水实验;75:水的净化;7H:乳化现象与乳化作用;8K:金属的回收利用及其
重要性.
【专题】521:空气与水;524:金属与金属材料.
【分析】A、利用电解水能证明的结论解决即可;
B、依据洗洁精洗涤油污的原理进行分析判断;
C、从蒸馏的除杂原理分析判断;
D、从废旧金属的回收利用分析解决;
【解答】解:A、电解水是生成了氢气与氧气能证明水是由氢氧两种元素组成,水是由水分子
构成的,所以不可能存在氢分子与氧分子;
B、洗洁精洗涤油污的原理利用了洗洁净的乳化作用,不是利用了溶解的原理;
C、蒸馏的操作可以得到纯水,所以它是对水净化程度最高的方法;
D、废旧金属的回收利用可以节约资源,是人类可持续发展的要求,所以废旧金属不回收是资
源的巨大浪费;
故选:C。
【点评】此题是与水及金属相关的问题考查题,题型较基础,只要对相关的基础知识有一个较
清晰的认识即可顺利解题。
18.(2分)2011年9月12日,中国科学家屠呦呦荣获拉克斯﹣﹣狄蓓吉临床医学研究奖,以
表彰她发现的一种药物﹣﹣青蒿素,它是治疗疟疾的特效药,化学式是C H O .下列有
15 22 5
关青蒿素的说法正确的是( )
A.“青蒿素”是混合物
B.“青蒿素”含42个原子
C.“青蒿素”中碳元素的质量分数是6.38%
D.“青蒿素”中碳、氢、氧三种元素的质量比是90:11:40
【考点】A5:纯净物和混合物的判别;D9:元素质量比的计算;DA:元素的质量分数计算.
菁
【专题】152:结合课本知识的信息.
第17页(共29页)【分析】A、根据纯净物有固定的组成考虑;B、根据分子的原子构成考虑;C、根据碳元素的质
量分数计算考虑;D、根据元素质量比的计算考虑。
【解答】解:A、纯净物有固定的组成和性质,混合物没有固定的组成,能写出化学式来,说明
该物质属于纯净物,故A错误;
B、一个“青蒿素”分子中含42个原子,故B错误;
C、“青蒿素”中碳元素的质量分数是: ×100%=63.8%,故C错误;
D、“青蒿素”中碳、氢、氧三种元素的质量比是:12×15:1×22:16×5=90:11:40,故D正确。
故选:D。
【点评】解答本题关键是要知道纯净物有固定的组成,分子的原子构成,熟悉元素质量及质量
分数的计算方法。
19.(2分)下列物质不能区分氧气和二氧化碳的是( )
A.澄清石灰水 B.稀硫酸
C.燃烧的火柴 D.紫色石蕊试液
【考点】4Q:常见气体的检验与除杂方法.
【专题】16:压轴实验题;182:物质的鉴别题.
【分析】A、根据二氧化碳的性质考虑;B、根据二氧化碳与氧气是否能与硫酸反应考虑;C、根
据氧气的助燃性和二氧化碳的不支持燃烧考虑;D、根据二氧化碳与水反应考虑。
【解答】解:A、使澄清石灰水变浑浊的原气体是二氧化碳氧气则不能,所以A能区分,故A错;
B、二氧化碳与氧气都不能与硫酸反应,所以不能区分,故B正确;
C、氧气具有助燃性,能使燃烧的火柴燃烧的更旺的原气体是氧气,二氧化碳不支持燃烧,能
使燃烧的火柴熄灭的原气体是二氧化碳,所以能区别,故C错;
D、二氧化碳能与水反应生成碳酸,使紫色石蕊试液变红,所以能使紫色石蕊试液变红的原气
体是二氧化碳,氧气不能,所以能区别,故D错。
故选:B。
【点评】鉴别两种物质就要根据两种物质性的不同点考虑,加入试剂后呈现的现象不同就行。
20.(2分)在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质
的质量如下表:
物质 甲 乙 丙 丁
反应前质量/g 3 5 20 7
反应后质量/g 10 5 8 待测
第18页(共29页)通过分析,判断下列说法正确的是( )
A.测得反应后丁物质的质量为12g
B.乙物质一定是催化剂
C.该反应是化合反应
D.该反应是复分解反应
【考点】FA:反应类型的判定;G1:质量守恒定律及其应用.
【专题】16:压轴实验题;513:化学用语和质量守恒定律.
【分析】本题可分析先甲、乙、丙三种物质反应前后的质量变化情况,确定是反应物还是生成
物;然后根据质量守恒定律确定丁是反应物还是生成物,进而可以确定反应类型。
【解答】解:A、由表中数据分析可知,反应前后,甲的质量增加了7g,故甲是生成物,参加反
应的甲的质量为7g;乙的质量不变,乙可能作该反应的催化剂,也可能没有参加反应;同
理可以确定丙是反应物,参加反应的丙的质量为12g;由质量守恒定律,丁应是生成物,且
生成的丁的质量为12g﹣7g=5g,故反应后丁物质的质量为7g+5g=12g;故选项说法正确。
B、乙的质量不变,乙可能作该反应的催化剂,也可能没有参加反应,故选项说法错误。
C、该反应的反应物是丙,生成物是甲和丁,反应符合“一变多”的特征,属于分解反应,故
选项说法错误。
D、根据C选项的分析,该反应属于分解反应,不是复分解反应,故选项说法错误。
故选:A。
【点评】本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运
用质量守恒定律。
二、我会填空(每空1分,共20分)
21.(3分)请从氢气、浓硫酸、蛋白质、淀粉几种物质中选择适当的物质,按要求填空:
(1)可做高能清洁燃料的是 H 。(写化学式)
2
(2)具有强烈腐蚀性的是 浓硫酸 。(写名称)
(3) 蛋白质 (写名称)是构成细胞的基本物质,是重要的营养物质,处在生长发育期的青
少年每天至少需摄取70克。
【考点】92:酸的物理性质及用途;HN:氢气的用途和氢能的优缺点;J2:生命活动与六大营养
素.
【专题】151:课本知识同类信息.
【分析】(1)氢气具有可燃性,能用作高能燃料;
(2)浓硫酸具有腐蚀性可用作干燥剂;
第19页(共29页)(3)蛋白质是构成细胞的基本物质,是重要的营养物质;
【解答】解:(1)氢气具有可燃性,燃烧后生成水,能用作高能清洁燃料,故答案为:H
2
(2)浓硫酸具有腐蚀性可用作干燥剂;故答案为:浓硫酸
(3)蛋白质是构成细胞的基本物质,是重要的营养物质;故答案为:蛋白质
【点评】掌握常见物质的重要用途是本题的考查点,这些知识需要在平时的学习中用心积累。
22.(4分)根据下列粒子结构示意图,回答问题:
(1)属于阳离子的是(填序号,下同) B ;
(2)属于原子的是 C ;
(3)核外电子数相同的是 BCD ;
(4)写出A、B两元素形成的化合物的一种用途 用作调味品等 。
【考点】B8:原子结构示意图与离子结构示意图.
【专题】513:化学用语和质量守恒定律.
【分析】(1)根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子
数<核外电子数,为阴离子;据此进行分析解答。
(2)根据当质子数=核外电子数,为原子,进行分析解答。
(3)根据核外电子排布情况进行分析判断。
(4)写出各粒子所代表的元素,再写出A、B两元素形成的化合物写出的一种用途即可。
【解答】解:(1)A、质子数=17,核外电子数=18,质子数<核外电子数,为阴离子。
B、质子数=11,核外电子数=10,质子数>核外电子数,为阳离子。
C、质子数=核外电子数=10,为原子。
D、质子数=9,核外电子数=10,质子数<核外电子数,为阴离子。
(2)C、质子数=核外电子数=10,为原子。
(3)B、C、D三种粒子的核外电子排布完全相同。
(4)A粒子表示的是氯离子,B粒子表示的是钠离子,形成的化合物是氯化钠,氯化钠可用作
调味品等。
故答案为:(1)B;(2)C;(3)BCD;(4)用作调味品等。
【点评】本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数
第20页(共29页)和核外电子数之间的关系是解题的关键。
23.(9分)南海是中国四大海域中最大、最深、自然资源最为丰富的海域,南海不但资源丰富,
还是亚太地区海运的“咽喉要道”,这里有世界上最繁忙的航线,因此引起周边国家的窥
视。
(1)海水属于 混合物 (填“纯净物”或“混合物”);海水晒盐属于混合物分离操作的是
B 。(填序号)
A、蒸馏 B、蒸发 C、过滤 D、沉淀
(2)南海油气资源丰富,石油加工可得到石油液化气,假设某石油液化气的主要成分为
C H ,写出其完全燃烧的化学方程式 2C H +13O 8CO +10H O ;小明家欲
4 10 4 10 2 2 2
将石油液气灶改为天然气(主要成分CH )灶具,他应将空气管口 减小 (填“增大”或
4
“减小”);CH 属于 有机物 (填“有机物”或“无机物”)
4
(3)在“南海一号”打捞出来的文物中,“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜
锈;铁器则锈迹斑斑,残存很少,这说明金、铜、铁这三种金属的活动顺序由强到弱的顺序
是 铁、铜、金 ;
(4)生铁和钢是世界上用量最大的 金属材料 (填“金属材料”或“合成材料”);炼铁的
原理是利用一氧化碳与氧化铁反应,反应的化学方程式为 3CO+F e O
2 3
2Fe+3CO ;写出防止铁生锈的一种方法是 在铁制品表面镀一层其它金属 。
2
【考点】4H:结晶的原理、方法及其应用;86:金属活动性顺序及其应用;89:金属材料及其应
用;8A:一氧化碳还原氧化铁;8G:金属锈蚀的条件及其防护;A5:纯净物和混合物的判别;
AC:有机物与无机物的区别;G5:书写化学方程式、文字表达式、电离方程式;H3:常用燃
料的使用与其对环境的影响;HC:海洋中的资源.
【专题】152:结合课本知识的信息;16:压轴实验题.
【分析】(1)根据海水的成分结合海水晒盐过程考虑混何物分离操作;(2)根据方程式的写法
和天然气消耗氧气的比较,有机物的判断考虑本体;(3)根据金属是否容易生锈考虑本题;
(4)根据金属材料的分类、方程式的写法和防止生锈的方法考虑本题。
【解答】解:(1)海水中含有水、氯化钠、氯化镁等物质属于混合物;海水晒盐主要是通过阳光
和风力使水分蒸发,使晶体结晶析出的过程,所以蒸发就是混合物的分离;
(2)根据C H 的成分可知燃烧后产物是:碳与氧结合生成的二氧化碳,氢和氧结合生成的水,
4 10
第21页(共29页)利用奇偶法配平,反应条件是点燃,写在等号上边;根据石油液化气燃烧方程式:
2C H +13O 8CO +10H O和天然气燃烧的方程式:CH +2O CO +2H O
4 10 2 2 2 4 2 2 2
可知2分子石油液化气消耗13分子氧气,1分子甲烷分子消耗2分子氧分子,所以等体积
的石油液化气比等体积的天然气消耗氧气多,所以石油液气灶改为天然气要减小空气管
口,因为需要的氧气少了;甲烷中含有碳元素(且不属于碳的氧化物、碳酸盐)属于有机物;
(3)金属活动性越强,越容易生锈,由,“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜
锈;铁器则锈迹斑斑,残存很少,可知铁最活泼,铜次之,金最不活泼;
(4)金属材料包括金属和合金,生铁和钢都是铁的合金,属于金属材料;炼铁的原理中反应物
是一氧化碳和氧化铁,生成物是铁和二氧化碳,用观察法配平,反应条件是高温,写在等
号上边;
防止生锈的方法有:保持铁制品表面洁净和干燥,使在铁制品表面镀一层其他金属或制成合
金等。
故答案为:(1)混合物;B;(2)2C H +13O 8CO +10H O;减小;有机物;(3)铁、铜、
4 10 2 2 2
金;(4)金属材料;3CO+Fe O 2Fe+3CO ;在铁制品表面镀一层其它金属。
2 3 2
【点评】解答本题关键是要把握好混合物、有机物、金属材料、金属活动性的判断,熟练掌握方
程式的书写方法。
24.(4分)如图是甲、乙两物质(均不含结晶水)的溶解曲线,据此回答以下问题:
(1)t ℃时,A物质的溶解度为 2 5 g;
1
(2)a点的含义是 在 t ℃时, A 、 B 两物质的溶解度相同 ;
2
(3)溶解度受温度影响小的物质是 B ;
(4)从A、B的混合物中分离A物质,一般采用 冷却热饱和溶液 的方法。
【考点】4H:结晶的原理、方法及其应用;7N:固体溶解度曲线及其作用.
第22页(共29页)【专题】515:溶液、浊液与溶解度.
【分析】根据物质的溶解度曲线,分析确定:t ℃时,A物质的溶解度;溶解度曲线角交点的意
1
义;物质的溶解度受温度影响的情况及分离混合物物的方法。
【解答】解:(1)由A物质的溶解度曲线可知,t ℃时,A物质的溶解度为25g;
1
(2)由A、B物质的溶解度曲线可知:a点的是A、B两物质的溶解度曲线的交点,a定的含义
是:在t ℃时,A、B两物质的溶解度相同;
2
(3)由溶解度曲线可知,溶解度受温度影响小的物质是B;
(4)由A、B物质的溶解度曲线可知:A物质的溶解度受温度的影响较大,B物质的溶解度受
温度的影响不大。所以,从A、B的混合物中分离A物质,一般采用冷却热饱和溶液的方法。
故答为:(1)25;(2)在t ℃时,A、B两物质的溶解度相同;(3)B;(4)冷却热饱和溶液。
2
【点评】本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对
固体溶解度的理解,培养学生应用知识解决问题的能力。
三、我会分析(25题4分,26题5分,27题6分,共15分)
25.(4分)人类可以通过化学反应获得能量,如利用沼气燃烧可以煮饭、炒菜等。请你举出两
例利用化学反应获得能量的事例。
【考点】E5:物质发生化学变化时的能量变化.
【专题】514:化学反应的基本类型和能量变化.
【分析】化学反应不但生成新物质而且还会伴随着能量的变化,这种能量变化经常表现为热
能、光能和电能的放出或吸收,结合生活常识和所学知识举出两例利用化学反应获得能量
的事例即可。
【解答】解:蜡烛照明是将化学能转化为光能;火力发电是利用煤、石油、天然气等燃料燃烧时
产生的热能,通过发电动力装置转换成电能。
故答案为:蜡烛照明;火力发电等。
【点评】本题难度不大,了解常见的化学反应的能量变化即可正确解答本题。
26.(5分)人类每时每刻都离不开空气,请你写出证明空气存在的一种方法。洁净的空气对
我们的身体健康非常重要,但是随着工业的发展,化石燃料的大量使用,排放到空气中的
有害气体和烟尘对空气的污染越来越严重,请你提出一条改善空气质量的建议。
【考点】65:防治空气污染的措施.
【专题】16:压轴实验题;212:化学与环境保护.
【分析】利用侧立在水中的集气瓶会有气泡冒出,证明空气的存在;为了保护大气成分的相对
稳定,减少硫氧化物、氮氧化物,则应减少化石燃料的使用。
第23页(共29页)【解答】解:空集气瓶在盛满水的水槽中侧立,有气泡冒出,说明有空气存在;
化石燃料的大量使用,排放到空气中的有害气体和烟尘对空气的污染越来越严重,为保护我
们的环境,就要开发新能源,减少化石燃料的使用。
【点评】环境、能源已经成为社会关注的焦点问题,与之相关的问题就成为中考的热点之一。
27.(6分)A与B有如下的反应:A+B→C+D
(1)若C为厨房内常用的调味品;在A溶液中加入铁粉能产生氢气,则A是 稀盐酸 。若
A、B两溶液恰好反应完全,则反应后溶液的PH = 7(填“<”、“>”或“=”);写
出A、B两溶液反应的化学方程式 HCl+NaOH ═ NaCl+H O 。
2
(2)若B常用来改良酸性土壤;D是重要的化工原料且与B的类别相同;B与CO 反应也能
2
生成C;则A为 N a CO 。C的用途是(只要写一种) 建筑材料(合理即可) 。写出B
2 3
溶液与CO 反应的化学方程式 CO +Ca ( OH ) = CaCO ↓ +H O 。
2 2 2 3 2
【考点】AE:物质的鉴别、推断.
【专题】112:常见物质的推断题;16:压轴实验题.
【分析】(1)根据若C为厨房内常用的调味品可猜测C是食盐,在A溶液中加入铁粉能产生
氢气说明A是一种酸,据此分析解答即可;
(2)若B常用来改良酸性土壤,可知B是氢氧化钙,D是重要的化工原料且与B的类别相同,
说明D是一种碱,据此结合相关的信息分析即可;
【解答】解:(1)C为厨房内常用的调味品可猜测C是食盐,在A溶液中加入铁粉能产生氢气
说明是一种酸,依据C可能是食盐,所以该酸可能是稀盐酸,此时B应该是氢氧化钠,因
为盐酸和氢氧化钠反应能生成氯化钠,且符合A+B→C+D的形式,故猜测正确,当盐酸和
氢氧化钠恰好反应时会生成氯化钠和水,此时溶液呈中性 pH=7,方程式为:
HCl+NaOH═NaCl+H O;
2
(2)B常用来改良酸性土壤,可知B是氢氧化钙,D是重要的化工原料且与B的类别相同,说
明D是一种碱,氢氧化钙与二氧化碳反应可生成碳酸钙和水,所以C是碳酸钙,则A是碳
酸钠,D是氢氧化钠,符合A+B→C+D且与叙述情况相符,碳酸钙是重要的建筑材料(合
理即可),氢氧化钙与二氧化碳反应方程式为:CO +Ca(OH) =CaCO ↓+H O;
2 2 3 2
故答案为:(1)稀盐酸;=;HCl+NaOH═NaCl+H O;
2
(2)Na CO ;建筑材料(合理即可);CO +Ca(OH) =CaCO ↓+H O;
2 3 2 2 3 2
【点评】此题是一道推断分析题,解题的关键是利用题内的叙述确定相关的结论,而后大胆进
行猜测,最后依据要求进行验证即可。
第24页(共29页)四、我能实验探究(28题8分,29题7分,共15分)
28.(8分)根据下列装置,结合所学化学知识回答下列问题。
(1)请写出图中标号仪器的名称: 长颈漏斗 ; 试管 。
(2)实验室制取少量二氧化碳时,发①生装置最好选用 ② C ,收集装置选用 E ;如需随时
控制生产气体的量并节约药品,发生装置最好选用 B 。(填编号)
(3)实验室用高锰酸钾制取氧气时,发生装置应选用 D (填编号);写出其反应的化学方
程式 2KMnO K MnO +MnO +O ↑ 。
4 2 4 2 2
(4)如用E装置收集O ,检验O 是否收集满的方法是 将一根带火星的木条平放在集气瓶
2 2
口,木条复燃,证明满了 。
【考点】4O:常用气体的发生装置和收集装置与选取方法;6C:实验室制取氧气的反应原理;
6F:氧气的检验和验满;G5:书写化学方程式、文字表达式、电离方程式.
【专题】16:压轴实验题;534:常见气体的实验室制法、检验、干燥与净化.
【分析】本题主要考查氧气和二氧化碳的实验室制法,在常温下用石灰石和稀盐酸来制取二
氧化碳,因此不需要加热。二氧化碳的密度比空气的密度大,能溶于水,因此只能用向上
排空气法收集。如果用过氧化氢和二氧化锰制氧气,就不需要加热;如果用高锰酸钾或氯
酸钾就需要加热。氧气不易溶于水,密度比空气的密度大,因此可以用排水法和向上排空
气法收集。书写化学方程式时,要注意配平。氧气验满的方法是:将一根带火星的木条平
放在集气瓶口,木条复燃,证明满了。
【解答】解:(1)长颈漏斗和试管是实验室常用的仪器,故答案为:长颈漏斗;试管
(2)在常温下用石灰石和稀盐酸来制取二氧化碳,因此不需要加热。制少量二氧化碳时,可以
用C装置;随时控制生产气体的量并节约药品,发生装置最好选用B装置;二氧化碳的密
度比空气的密度大,能溶于水,因此只能用向上排空气法收集。故答案为:C;E;B
(3)实验室用高锰酸钾制取氧气时,就需要加热;高锰酸钾受热分解生成锰酸钾和二氧化锰
第25页(共29页)和氧气,配平即可,故答案为:D;2KMnO K MnO +MnO +O ↑
4 2 4 2 2
(4)氧气验满的方法是:将一根带火星的木条平放在集气瓶口,木条复燃,证明满了。故答案
为:将一根带火星的木条平放在集气瓶口,木条复燃,证明满了。
【点评】本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书
写和仪器的名称,综合性比较强。气体的制取装置的选择与反应物的状态和反应的条件有
关;气体的收集装置的选择与气体的密度和溶解性有关。本考点是中考的重要考点之一,
主要出现在实验题中。
29.(7分)以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指
20℃;“浓度”指溶质的质量分数)
实验序 过氧化氢溶液 过氧化氢溶液 温 二氧化锰用 氧气体 反应所需时
号 浓度/% 质量/g 度/℃ 量/g 积/ml 间/s
5 12 20 0.2 125 11
① 30 12 20 0.2 125 2
② 30 12 40 / 125 148
③ 30 12 90 / 125 82
(1④)通过实验 和 对比可知,化学反应快慢与 过氧化氢的浓度 有关;
(2)通过对比实①验 ② 和 可知,化学反应快慢与温度的关系是 温度越高反应速
度越快,温度越低③反应速度越④慢 。
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是 2 0 ℃时 5% 过氧化氢
溶液中加入少量二氧化锰 。
(4)某实验室需配置450克5%的过氧化氢溶液,其操作为:往一定量30%的过氧化氢溶液中
加入 37 5 克水,然后用 玻璃棒 (填仪器名称)搅拌均匀。
【考点】2B:影响化学反应速率的因素探究;6C:实验室制取氧气的反应原理.
【专题】16:压轴实验题;537:科学探究.
【分析】(1)比较表格中的 数据在其他条件都相同时,可以看出过氧化氢的浓度对反应
速率的影响。 ①②
(2)比较表格中的 数据在其他条件都相同时,可以看出温度对反应速率的影响。
(3)根据实验室操③作简④便且制取气体易收集的原则分析选择即可。
(4)依据溶液稀释的方法,根据稀释前后溶质的质量不变完成。
【解答】解:(1)从表中分析可知: 是过氧化氢浓度不同而其他的反应时各种量均相同,
①②
第26页(共29页)可知这一过程是考查反应物的浓度与反应速度的关系;
(2) 则是温度不同其他条件相同,明显是对温度影响化学反应速度的探究;从结果看温
度③高④时反应所用的时间较短,既反应的速度较快,温度低时反应的速度慢适合收集气体;
(3)实验室用过氧化氢制取氧气要求反应简便易操作,所以采用不加热而加催化剂的方法进
行较合适,从易于收集的角度反应的速度不能太快也不能太慢,所以最合适的条件是
20℃时5%过氧化氢溶液中加入少量二氧化锰;
(4)设利用配置450克5%的过氧化氢溶液所需的30%的过氧化氢溶液质量是x。
450g×5%=x×30%
x=75g
所以加水的质量是450g﹣75g=375g
配置的过程是往一定量30%的过氧化氢溶液中加入375g克水,然后用玻璃棒搅拌均匀即可;
故答案为:(1)过氧化氢的浓度;(2) ; ;温度越高反应速度越快,温度越低反应速度越
慢;(3)20℃时5%过氧化氢溶液③中加④入少量二氧化锰;(4)375;玻璃棒;
【点评】本题主要考查了能够影响化学反应的因素,解答这类题时要注意尽可能的把题中的
能够影响化学反应的因素找出,然后再利用控制变量法来进行判断,最后得出答案。
五、我会计算(30题4分,31题6分,共10分)
30.(4分)已知R+H SO =RSO +H ↑,若13克金属R与足量稀硫酸完全反应可制得0.4克
2 4 4 2
氢气。试分析:
(1)RSO 中R的化合价为 + 2 价 。
4
(2)通过计算确定R的相对原子质量。
【考点】D6:有关元素化合价的计算;G6:根据化学反应方程式的计算.
【专题】16:压轴实验题;191:化学式的计算;193:有关化学方程式的计算.
【分析】根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查。在本题中,根据
整个物质对外不显电性,正负化合价的代数和为零的原则,硫酸根是﹣2价,那么R是+2
价;然后根据化学方程式的计算,求R的相对原子质量。
【解答】解:(1)根据化合物中正负化合价的代数和为零的原则,硫酸根是﹣2价,那么R是+2
价,故答案为:+2价
(2)设R的相对原子质量为x
R+H SO =RSO +H ↑
2 4 4 2
x 2
13g 0.4g
第27页(共29页)x=65 答:R的相对原子质量为65
故答案为:65
【点评】本考点考查了根据化学方程式的计算和在化合物中,正负化合价的代数和为零的原
则,是中考计算题中经常出现的题型。做题时要注意:化学方程式要写正确,计算要准确,
相对原子质量的单位是一,省略不写。本考点主要出现在计算题中。
31.(6分)未成年人和老年人是需要补钙的主要人群,目前市面上有许多补钙的钙片出售,
如图是盖中盖高钙片的部分说明,某课外兴趣小组欲检验说明的真伪,进行了入下的实验:
盖中盖高钙片
【主要原料】碳酸钙、维生素D
【功效成分】每片含:钙500mg、维生素D100IU
【用法用量】每日1片,嚼食。
【适宜人群】需要补钙者。
【注意事项】
1、本品不能代替药物。
2、不宜超过推荐量或与同类营养素补充剂同时食用。
【规格】2.5g×36片
取1片片剂研碎
①将其加入足量稀盐酸中
②完全反应后收集到0.55g二氧化碳
③试分析:
(1)未成年人缺钙会得 C 。(填序号)
A、坏血症 B、贫血 C、佝偻病 D、甲状腺肿大
(2)通过计算判断此钙片中钙含量与标注是否属实。(假定钙片中其他成份不与盐酸反应,1g
=1000mg)
【考点】DE:标签上标示的物质成分及其含量;G6:根据化学反应方程式的计算;J1:人体的元
素组成与元素对人体健康的重要作用.
【专题】136:标签图示型;16:压轴实验题.
【分析】(1)人体缺钙会患多种疾病,未成年人缺钙会得佝偻病,老年人缺钙会得骨质疏松症;
(2)根据碳酸钙与盐酸反应的方程式,将二氧化碳的质量代入计算可判断碳酸钙的质量,然
后乘以钙在碳酸钙中所占有的质量分数,求出钙元素的质量与补钙剂的说明比较判定是
否属实。
第28页(共29页)【解答】解:(1)体缺钙会患多种疾病,未成年人缺钙会得佝偻病,老年人缺钙会得骨质疏松
症;故答案为:C
(2)因盐酸足量,则碳酸钙完全反应;
设片钙片中碳酸钙的质量为x
CaCO +2HCl═CaCl +CO ↑+H O
3 2 2 2
100 44
x 0.55g
解得x=1.25g,
则1.25g碳酸钙中含钙元素的质量为:1.25g× ×100%=0.5g
0.5g×1000mg/g=500mg
与说明中每片含钙500mg、一致,则说明属实,
答:此钙片中钙含量与标注属实
【点评】本题考查利用化学式和化学反应方程式的计算,学生明确常化学式计算的方法、化学
反应中何种物质的质量可代入方程式计算是解答的关键。
第29页(共29页)