文档内容
2014 年武汉中考化学试题
一、选择题(本题包括8小题,每小题只有一个选项符合题意,每小题3分,共24分)
1.下列变化属于化学变化的是( )
A.将木头锯断 B.铁生锈 C.将弯曲的弹簧拉直 D.水受热变成水蒸气
2.下列有关原子、分子的说法错误的是( )
A.原子、分子都是构成物质的微粒 B.原子、分子总在不断运动
C.分子可以再分,原子不能再分 D.分子间有一定的间隔
3.下列有关物质组成的说法正确的是( )
A.煤气是由一氧化碳、甲烷、氢气等组成的混合物
B.葡萄糖不属于有机物
C.造成酸雨的主要物质是一氧化碳和二氧化碳
D.氢气和天然气都含有碳元素,都可以作燃料
4.化学在生活中用途广泛。下列有关说法错误的是( )
A.使用农药、化肥对人类有利也有弊
B.合理食用加碘盐有利于碘缺乏病人健康
C.食用甲醛水溶液浸泡过的海产品对人体无害
D.香烟的烟气中含有很多对人体有害的物质
5.二氧化钛(TiO)是一种用途广泛的化工原料,用四氯化钛(TiCl )与某常见物质X反应可
2 4
制得二氧化钛,反应的化学方程式为:TiCl +□X=TiO+4HCl
4 2
关于物质X下列说法正确的是( ) (H-1 O-16)
A.该物质由碳、氢、氧三种元素组成 B.该物质的化学式为HO
2 2
C.该物质中氢、氧元素的质量比1:8 D.该物质中氢元素的质量分数为5%
6.下列有关说法正确的是( )
A.实现CO CO 的相互转化都只有一种途径
2
+O +H O
B.铝可以实验单质 2 氧化物 2 碱
+O
C.实现C 2 CO 转化都利用了碳的可燃性
2
+CuO
通电
D.实现HO O 的相互转化,化学反应的基本类型不同
2 2
7.某化学兴趣小组的同学在教师的指导下,正确完成如下图所示的两实验。已知所用实验装
置气密性良好。
实验一 实验二
关于该实验有如下说法:①红磷熄灭并冷却后才能打开弹簧夹;②点燃酒精灯加热
铜丝,可观察到铜丝由红色变成黑色;③停止加热后即可读出注射器内气体体积约为
24mL;④实验取用铜丝的多少不会影响实验结果;⑤两个实验均能证明空气是混合物;⑥
两个实验均能证明空气中约含1/5体积的氧气。
其中正确说法的个数有( )
A.2个 B.3个 C.4个 D.5个8.某化学兴趣小组的同学将一枚洁净的铁钉放入硫酸铜溶液中,观察到铁钉表面有红色物
质析出,且产生少量的气体,于是他们重新配制硫酸铜溶液,再次实验,又观察到相同的
现象。
关于该实验有如下说法:①产生的气体可能是氢气;②完全反应后溶液呈黄色;③实
验中一定发生了置换反应;④由实验可以得出金属活动性顺序:Cu>Fe;⑤硫酸铜溶液可
能显酸性;⑥重做实验没有任何意义。
其中正确说法的个数有( )
A.2个 B.3个 C.4个 D.5个
二、非选择题(本题包括5小题,共26分)
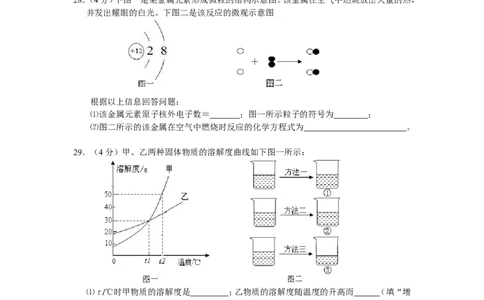
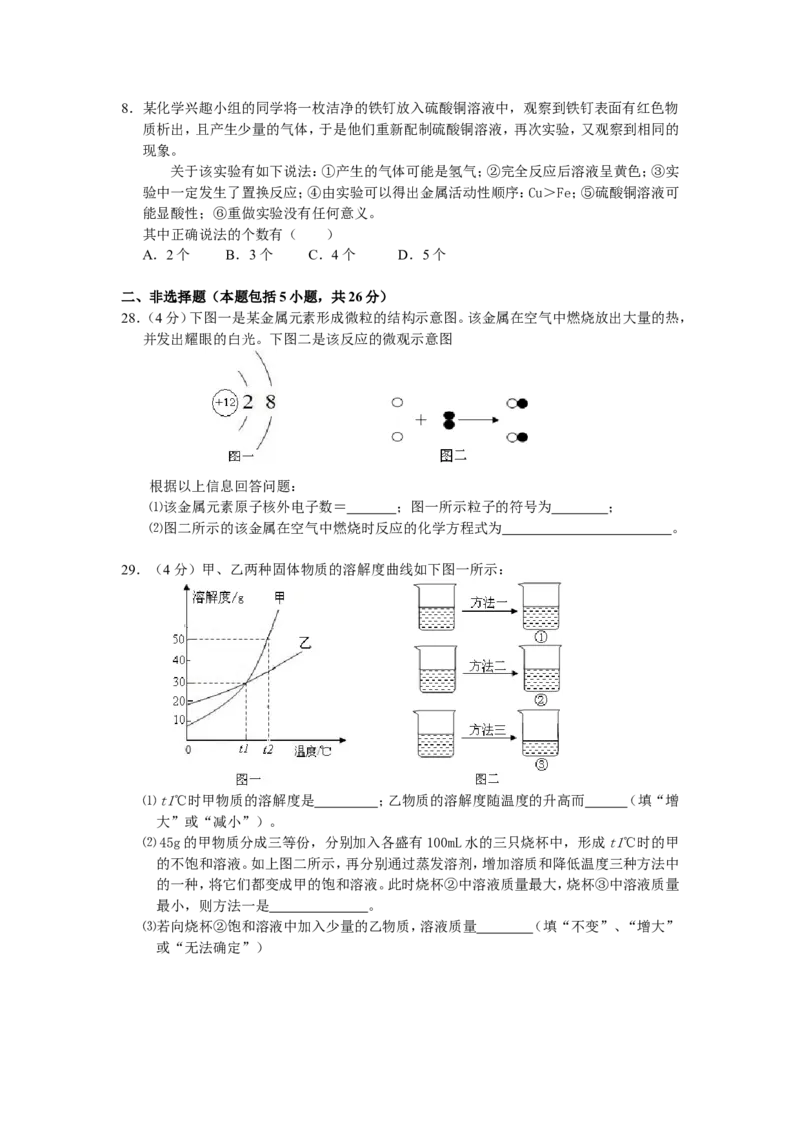
28.(4分)下图一是某金属元素形成微粒的结构示意图。该金属在空气中燃烧放出大量的热,
并发出耀眼的白光。下图二是该反应的微观示意图
根据以上信息回答问题:
⑴该金属元素原子核外电子数= ;图一所示粒子的符号为 ;
⑵图二所示的该金属在空气中燃烧时反应的化学方程式为 。
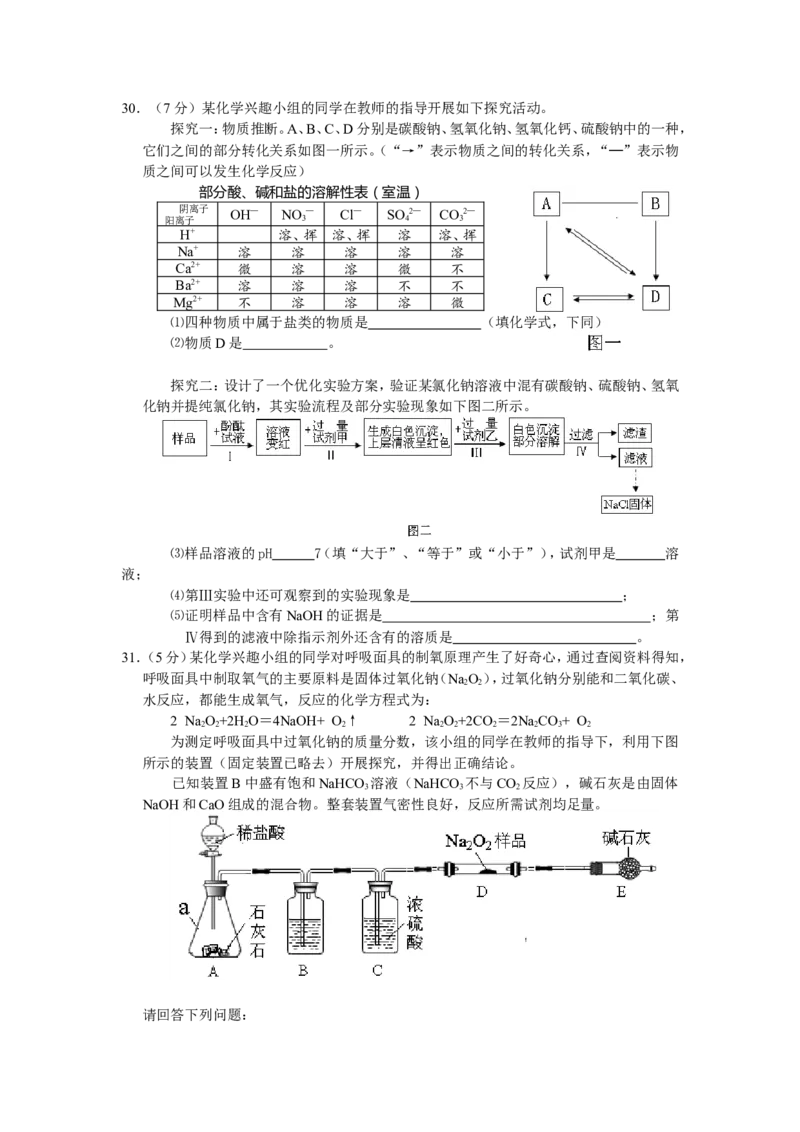
29.(4分)甲、乙两种固体物质的溶解度曲线如下图一所示:
⑴t1℃时甲物质的溶解度是 ;乙物质的溶解度随温度的升高而 (填“增
大”或“减小”)。
⑵45g的甲物质分成三等份,分别加入各盛有100mL水的三只烧杯中,形成t1℃时的甲
的不饱和溶液。如上图二所示,再分别通过蒸发溶剂,增加溶质和降低温度三种方法中
的一种,将它们都变成甲的饱和溶液。此时烧杯②中溶液质量最大,烧杯③中溶液质量
最小,则方法一是 。
⑶若向烧杯②饱和溶液中加入少量的乙物质,溶液质量 (填“不变”、“增大”
或“无法确定”)30.(7分)某化学兴趣小组的同学在教师的指导开展如下探究活动。
探究一:物质推断。A、B、C、D分别是碳酸钠、氢氧化钠、氢氧化钙、硫酸钠中的一种,
它们之间的部分转化关系如图一所示。(“→”表示物质之间的转化关系,“─”表示物
质之间可以发生化学反应)
部分酸、碱和盐的溶解性表(室温)
阴离子 OH— NO — Cl— SO 2— CO2—
阳离子 3 4 3
H+ 溶、挥 溶、挥 溶 溶、挥
Na+ 溶 溶 溶 溶 溶
Ca2+ 微 溶 溶 微 不
Ba2+ 溶 溶 溶 不 不
Mg2+ 不 溶 溶 溶 微
⑴四种物质中属于盐类的物质是 (填化学式,下同)
⑵物质D是 。
探究二:设计了一个优化实验方案,验证某氯化钠溶液中混有碳酸钠、硫酸钠、氢氧
化钠并提纯氯化钠,其实验流程及部分实验现象如下图二所示。
⑶样品溶液的pH 7(填“大于”、“等于”或“小于”),试剂甲是 溶
液;
⑷第Ⅲ实验中还可观察到的实验现象是 ;
⑸证明样品中含有NaOH的证据是 ;第
Ⅳ得到的滤液中除指示剂外还含有的溶质是 。
31.(5分)某化学兴趣小组的同学对呼吸面具的制氧原理产生了好奇心,通过查阅资料得知,
呼吸面具中制取氧气的主要原料是固体过氧化钠(NaO),过氧化钠分别能和二氧化碳、
2 2
水反应,都能生成氧气,反应的化学方程式为:
2 NaO+2H O=4NaOH+ O↑ 2 NaO+2CO =2NaCO+ O
2 2 2 2 2 2 2 2 3 2
为测定呼吸面具中过氧化钠的质量分数,该小组的同学在教师的指导下,利用下图
所示的装置(固定装置已略去)开展探究,并得出正确结论。
已知装置B中盛有饱和NaHCO 溶液(NaHCO 不与CO 反应),碱石灰是由固体
3 3 2
NaOH和CaO组成的混合物。整套装置气密性良好,反应所需试剂均足量。
请回答下列问题:⑴仪器a的名称是 ,装置A的作用是 ;
⑵不用装置E取代装置C的理由是 ;
⑶装置D中过氧化钠样品的质量为m g,装置D在反应前后质量分别为n g和n g,若样
1 2
品中所含杂质既不溶于水,也不参加化学反应,则样品中过氧化钠的质量分数=
。(Na-23 O-16 C-12 H-1)
32.(6分)将4.0g Cu—Zn合金粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应。过滤,称
量滤液的质量,相关实验数据如下:
反应前物质质量/g 反应后物质质量/g
Cu—Zn合金 稀硫酸 滤液质量
4.0 10 11.26
⑴Cu—Zn合金属于 材料(填“金属”或“有机合成”)。
⑵若不考虑该合金中除Cu、Zn以外的其它成分,请计算原Cu—Zn合金中Zn的质量。写
出必要的计算过程。(Zn-65 Cu-63.5 H-1 O-16 S-32)
参考答案一、选择题
1 2 3 4 5 6 7 8
B C A C C D C B
二、非选择题
28、⑴12 Mg2+
点燃
⑵ 2Mg+O==2MgO
2
29、⑴30g;增大
⑵降低温度 ⑶增大
30、⑴NaCO Na SO
2 3 2 4
⑵NaOH
⑶大于 氯化钡
⑷有气泡产生,溶液由红色变为无色
⑸加入过量的试剂甲(氯化钡)后溶液仍为红色;
氯化钠、氯化钡、氯化氢(或NaCl、BaCl 、HCl)
2
31、⑴锥形瓶,制备CO
2
⑵碱石灰会吸收CO(碱石灰能同时吸收水和CO)
2 2
⑶ (或 39(n2-n1)/14m×100%)
32、⑴金属
⑵设合金中Zn的质量为X
Zn + H SO =ZnSO +H ↑
2 4 4 2
65 2
X 2X/65
10g+X-2X/65=11.26g
X=1.3g
答:略