文档内容
2016年湖北省黄石市中考化学试卷
一、选择题(共10小题,每小题2分,满分20分)
1.(2分)空气中含量最多的气体是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
2.(2分)下列物质中,不属于化石燃料的是( )
A.煤 B.石油 C.天然气 D.乙醇
3.(2分)下列过程属于化学变化的是( )
A.碘升华 B.铝放置于空气中,表面生成一层致密的薄膜
C.风能发电 D.蒸发蔗糖水溶液得到蔗糖晶体
4.(2分)一些食物就得近似pH如下:
食物 葡萄汁 苹果汁 牛奶 玉米粥 鸡蛋清
pH 3.5~4.5 2.9~3.3 6.3~6.6 7.0~8.0 7.6~8.0
下列说法不正确的是( )
A.鸡蛋清显碱性 B.苹果汁和葡萄汁显酸性
C.葡萄汁比苹果汁的酸性强 D.胃酸过多的人适宜吃玉米粥
5.(2分)下列关于催化剂的说法正确的是( )
A.催化剂必定加快反应速率
B.反应前后催化剂的化学性质通常会发生改变
C.在酿造工业和制药工业,一般都要用酶作催化剂
D.用氯酸钾制取氧气时,加入催化剂可使生成氧气的质量增加
6.(2分)下列各组物质中的分类正确的是( )
A.氧化物:H O、NO 、Fe O
2 2 3 4
B.碱:Ca(OH)、Ba(OH)、Na CO
2 2 2 3
C.酸:CH COOH、CH 、H SO
3 4 2 4
D.盐:NH NO 、MgCl 、CuO
4 3 2
7.(2分)下列关于二氧化碳与一氧化碳的性质比较不正确的是( )
A.组成:均由碳元素和氧元素组成
B.性质:CO 、CO都可以使澄清石灰水变浑浊
2
C.用途:干冰可用于人工降雨;一氧化碳气体可作燃料
第1页(共22页)D.危害:二氧化碳会导致“温室效应”;一氧化碳会引起中毒
8.(2分)下列除杂,分离提纯的方法或选用的试剂不正确的是( )
选项 物质 所含杂质 除去杂质的方法
A 硝酸钾 少量氯化钠 重结晶
B N O 通过灼热的铜网
2 2
C CaCl 溶液 稀盐酸 加入过量碳酸钙,过滤
2
D Fe 铁锈 稀硫酸
A.A B.B C.C D.D
9.(2分)验证Zn、Fe、Cu金属的活动性强弱,下列的实际组合实验方案不能达到
实验目的是( )
A.FeSO 溶液、Zn、Cu
4
B.ZnSO 溶液、稀盐酸溶液、Fe、Cu
4
C.ZnSO 溶液、FeSO 溶液、Cu
4 4
D.ZnCl 溶液、CuCl 溶液、Fe
2 2
10.(2分)类推是化学学习中常用的思维方法,以下类推结果中正确的是( )
A.铝与盐酸反应生成AlCl 和H ,则金属铁与盐酸反应生成FeCl 和H
3 2 3 2
B.碱的水溶液显碱性,所以NaOH的水溶液一定是碱性溶液
C.酸溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的一定是酸的
溶液
D.燃烧一般都伴随着发光、放热现象,所以有发光、放热现象的变化就是燃烧
二、解答题(共7小题,满分39分)
11.(5分)请从下面五种物质中选择恰当的物质,将其字母代码填入空格中。
A.涤纶 B.硝酸钾 C.苛性钠 D.生铁 E.油脂
(1)可做复合肥的是 。
(2)属于基本营养物质的是 。
(3)用于铸造农具的是 。
(4)属于有机合成材料的是 。
(5)能使酚酞溶液变为红色的碱类物质是 。
第2页(共22页)12.(6分)(1)下列是与水有关的几个描述,请根据所学知识填写完整:
①自然界中的水大多是 (选填“混合物”或“纯净物”);
② (填物质名称)具有吸附性,可用于水的净化;
③电解H O时,与直流电源的 (选填“正”或“负”)极相连的电极附近
2
得到H .
2
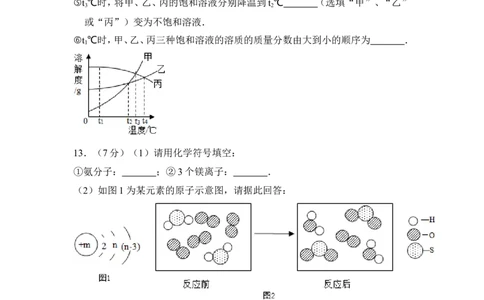
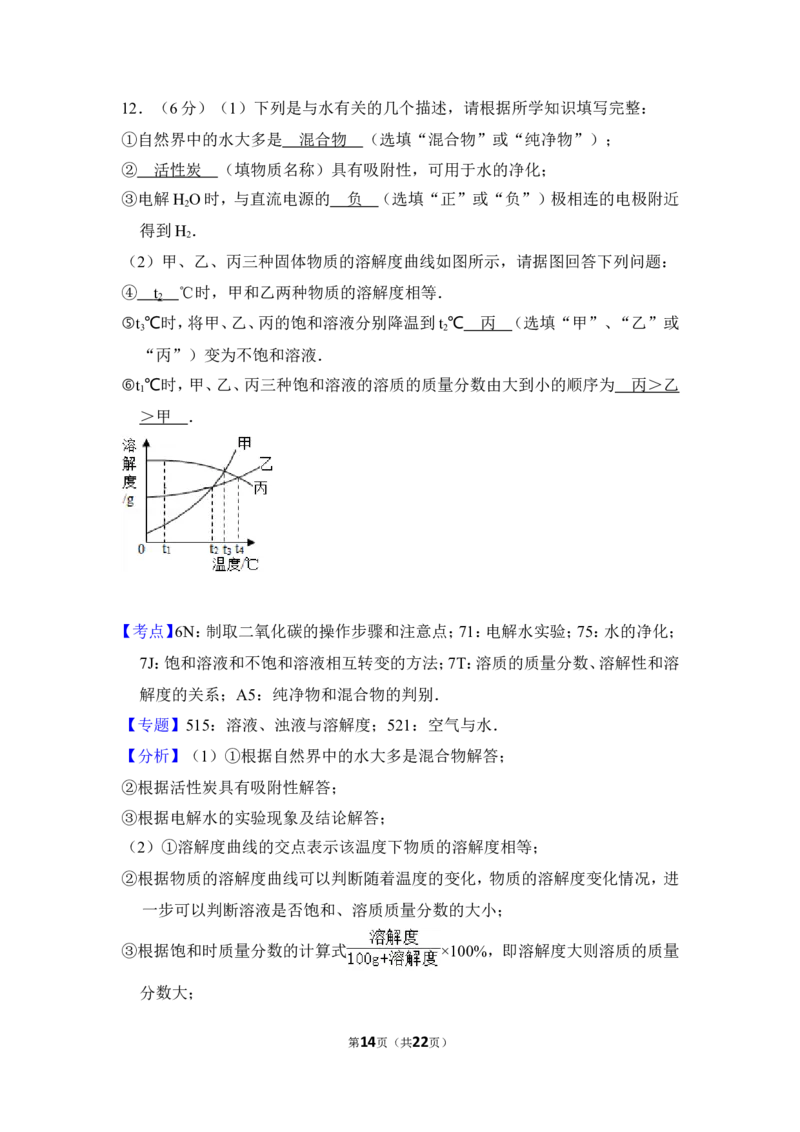
(2)甲、乙、丙三种固体物质的溶解度曲线如图所示,请据图回答下列问题:
④ ℃时,甲和乙两种物质的溶解度相等.
⑤t ℃时,将甲、乙、丙的饱和溶液分别降温到t ℃ (选填“甲”、“乙”
3 2
或“丙”)变为不饱和溶液.
⑥t ℃时,甲、乙、丙三种饱和溶液的溶质的质量分数由大到小的顺序为 .
1
13.(7分)(1)请用化学符号填空:
①氨分子: ;②3个镁离子: .
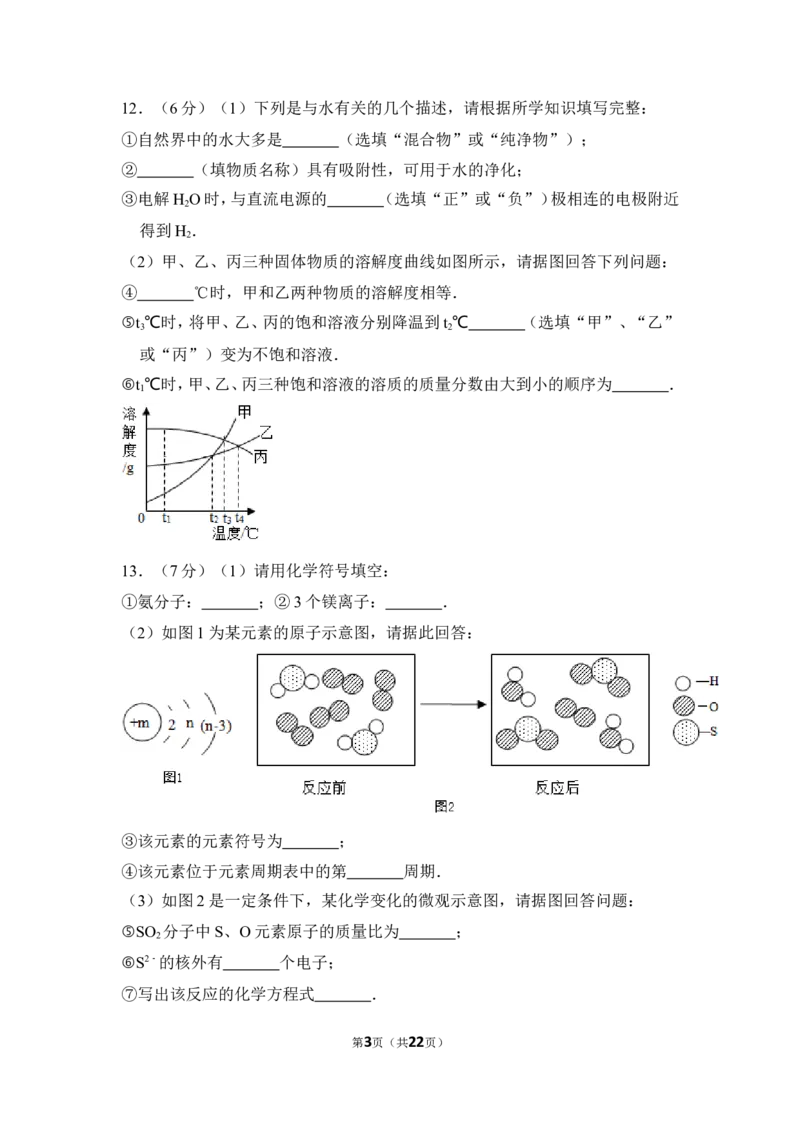
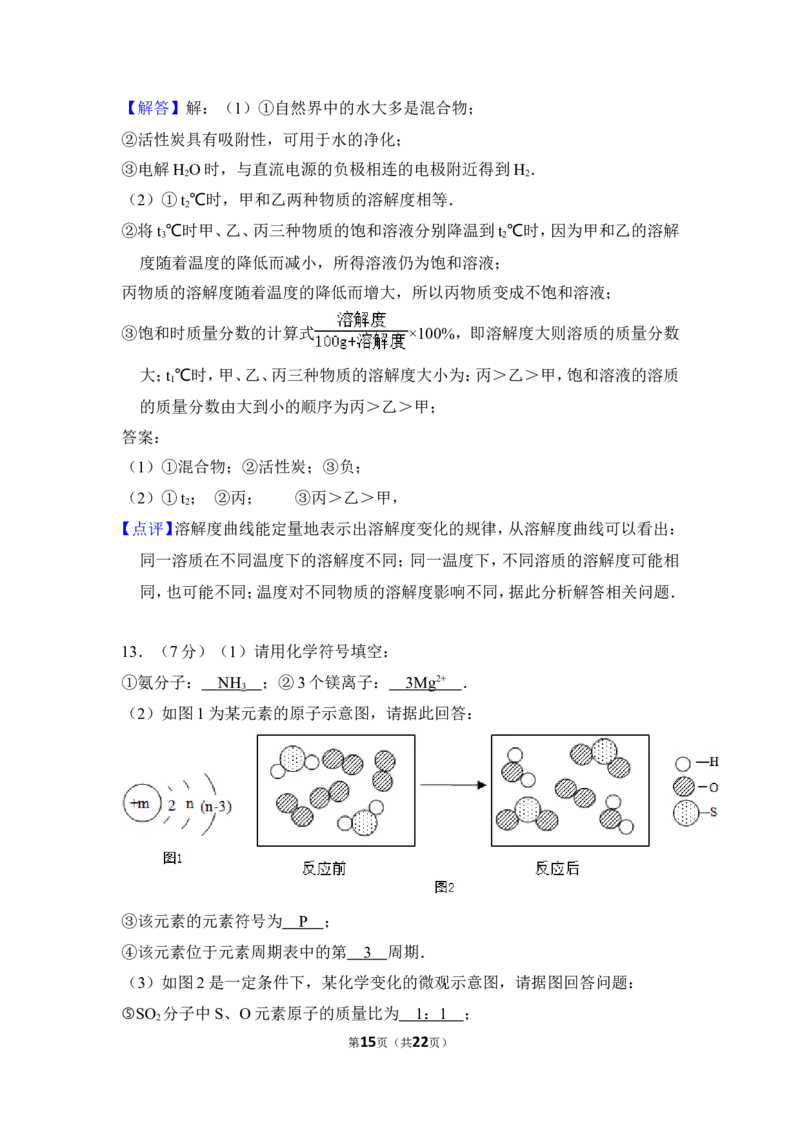
(2)如图1为某元素的原子示意图,请据此回答:
③该元素的元素符号为 ;
④该元素位于元素周期表中的第 周期.
(3)如图2是一定条件下,某化学变化的微观示意图,请据图回答问题:
⑤SO 分子中S、O元素原子的质量比为 ;
2
⑥S2﹣的核外有 个电子;
⑦写出该反应的化学方程式 .
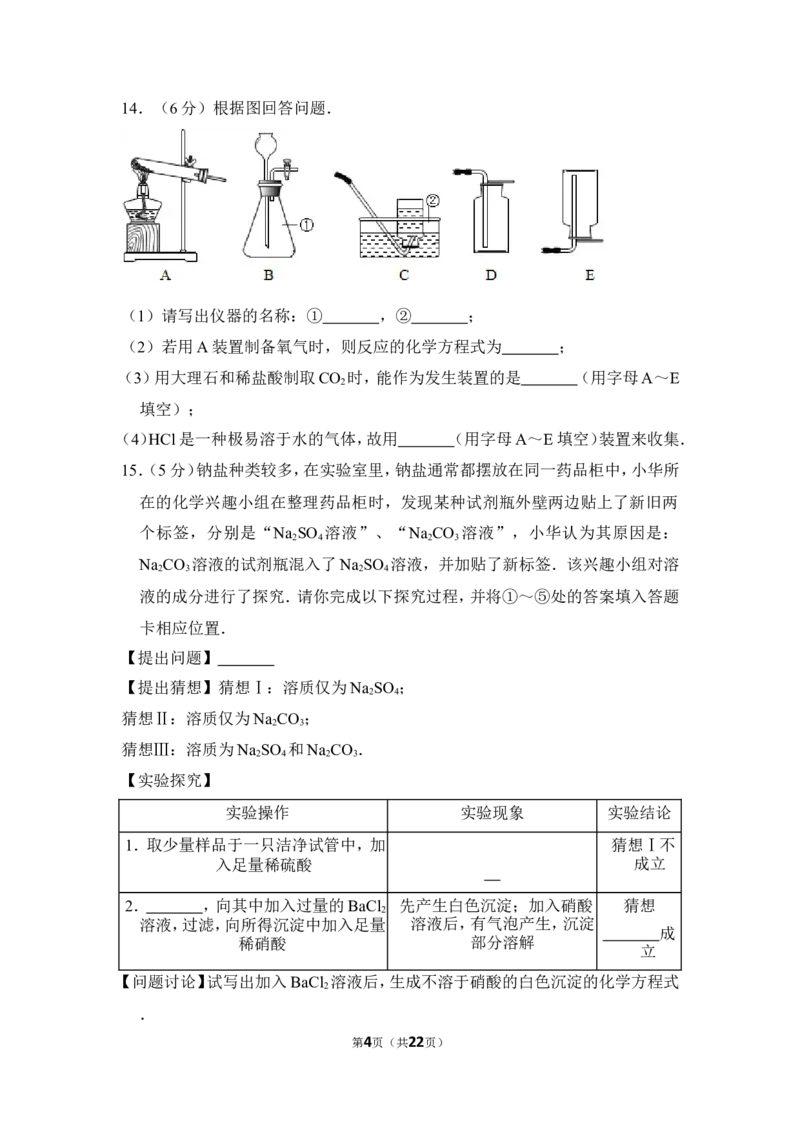
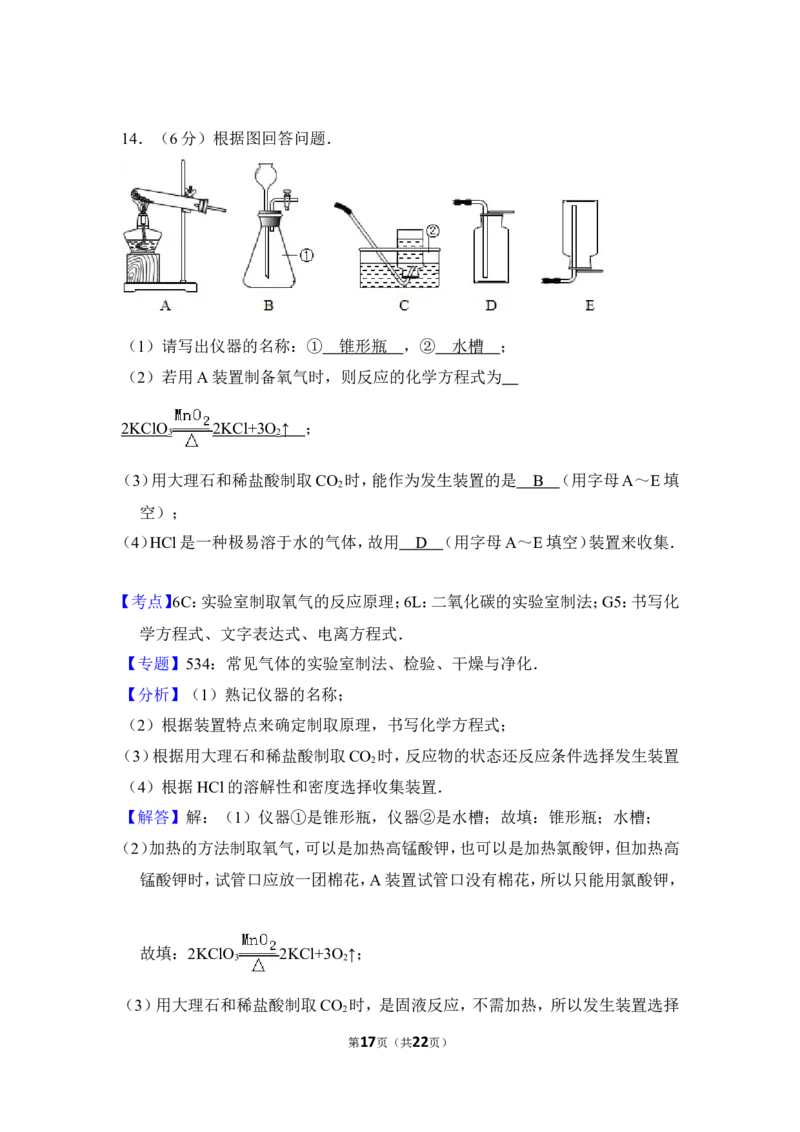
第3页(共22页)14.(6分)根据图回答问题.
(1)请写出仪器的名称:① ,② ;
(2)若用A装置制备氧气时,则反应的化学方程式为 ;
(3)用大理石和稀盐酸制取CO 时,能作为发生装置的是 (用字母A~E
2
填空);
(4)HCl是一种极易溶于水的气体,故用 (用字母A~E填空)装置来收集.
15.(5分)钠盐种类较多,在实验室里,钠盐通常都摆放在同一药品柜中,小华所
在的化学兴趣小组在整理药品柜时,发现某种试剂瓶外壁两边贴上了新旧两
个标签,分别是“Na SO 溶液”、“Na CO 溶液”,小华认为其原因是:
2 4 2 3
Na CO 溶液的试剂瓶混入了Na SO 溶液,并加贴了新标签.该兴趣小组对溶
2 3 2 4
液的成分进行了探究.请你完成以下探究过程,并将①~⑤处的答案填入答题
卡相应位置.
【提出问题】
【提出猜想】猜想Ⅰ:溶质仅为Na SO ;
2 4
猜想Ⅱ:溶质仅为Na CO ;
2 3
猜想Ⅲ:溶质为Na SO 和Na CO .
2 4 2 3
【实验探究】
实验操作 实验现象 实验结论
1.取少量样品于一只洁净试管中,加 猜想Ⅰ不
入足量稀硫酸 成立
2. ,向其中加入过量的BaCl 先产生白色沉淀;加入硝酸 猜想
2
溶液,过滤,向所得沉淀中加入足量 溶液后,有气泡产生,沉淀
成
稀硝酸 部分溶解
立
【问题讨论】试写出加入BaCl 溶液后,生成不溶于硝酸的白色沉淀的化学方程式
2
.
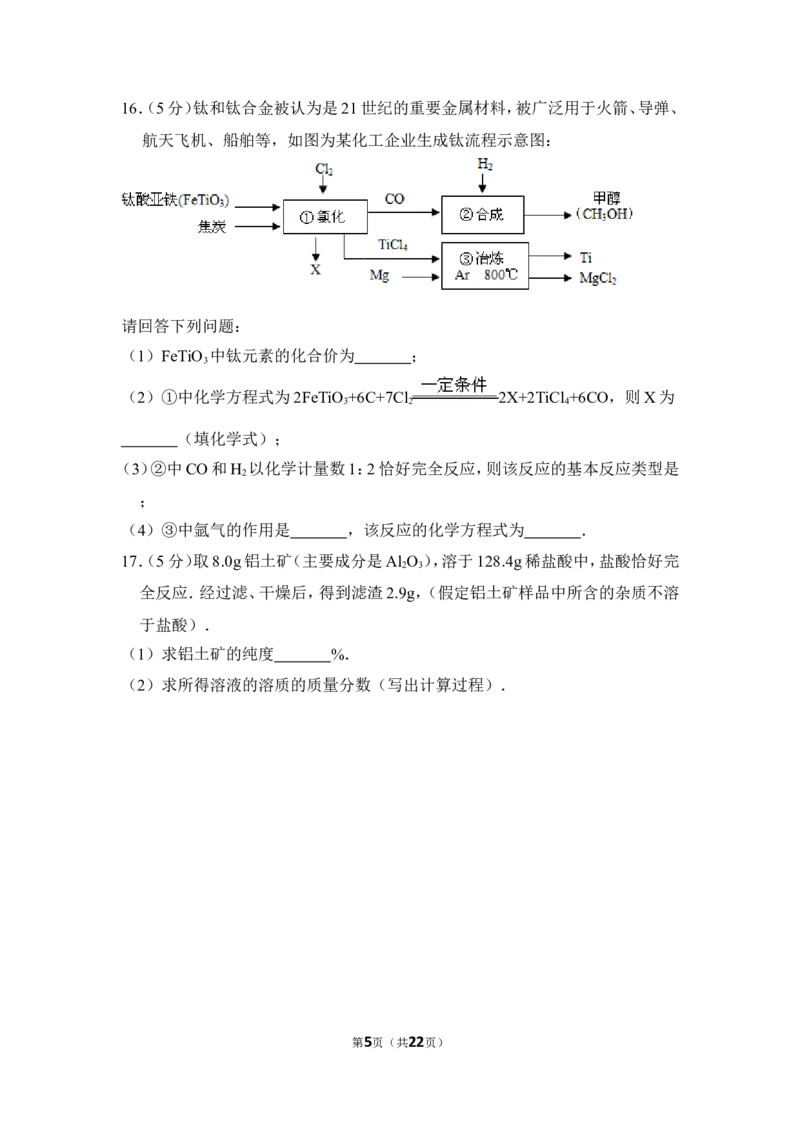
第4页(共22页)16.(5分)钛和钛合金被认为是21世纪的重要金属材料,被广泛用于火箭、导弹、
航天飞机、船舶等,如图为某化工企业生成钛流程示意图:
请回答下列问题:
(1)FeTiO 中钛元素的化合价为 ;
3
(2)①中化学方程式为2FeTiO +6C+7Cl 2X+2TiCl +6CO,则X为
3 2 4
(填化学式);
(3)②中CO和H 以化学计量数1:2恰好完全反应,则该反应的基本反应类型是
2
;
(4)③中氩气的作用是 ,该反应的化学方程式为 .
17.(5分)取8.0g铝土矿(主要成分是Al O ),溶于128.4g稀盐酸中,盐酸恰好完
2 3
全反应.经过滤、干燥后,得到滤渣2.9g,(假定铝土矿样品中所含的杂质不溶
于盐酸).
(1)求铝土矿的纯度 %.
(2)求所得溶液的溶质的质量分数(写出计算过程).
第5页(共22页)2016 年湖北省黄石市中考化学试卷
参考答案与试题解析
一、选择题(共10小题,每小题2分,满分20分)
1.(2分)空气中含量最多的气体是( )
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
【考点】61:空气的成分及各成分的体积分数.
【专题】521:空气与水.
【分析】根据空气中各成分及体积分数来回答本题,并能灵活运用它们解释一些
生活中常见的现象。
【解答】解:空气中各成分及体积分数为:氮气:78%、氧气:21%、稀有气体:
0.94%、二氧化碳0.03%、水蒸气和杂质:0.03%。
故选:A。
【点评】熟记空气中各成分及体积分数,知道空气中的主要气体,哪种气体最多,
哪种气体最少。
2.(2分)下列物质中,不属于化石燃料的是( )
A.煤 B.石油 C.天然气 D.乙醇
【考点】H7:化石燃料及其综合利用.
【专题】152:结合课本知识的信息.
【分析】天然气、煤、石油属于化石燃料.在我国能源领域占有重要的地位.
【解答】解:煤、石油和天然气是三大化石燃料。乙醇不属于化石燃料,属于可再生
能源。
故选:D。
【点评】解答本题要充分理解化石燃料包括哪些物质,只有这样才能对问题做出
正确的判断.
第6页(共22页)3.(2分)下列过程属于化学变化的是( )
A.碘升华 B.铝放置于空气中,表面生成一层致密的薄膜
C.风能发电 D.蒸发蔗糖水溶液得到蔗糖晶体
【考点】E3:化学变化和物理变化的判别.
【专题】332:化学反应的分类思想;512:物质的变化与性质.
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变
化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
【解答】解:A、碘升华的过程中没有新物质生成,属于物理变化。
B、铝放置于空气中,表面生成一层致密的薄膜,是由于Al被空气中氧气氧化为
氧化铝的原因,此过程中有新物质氧化铝生成,属于化学变化。
C、风能发电的过程中没有新物质生成,属于物理变化。
D、蒸发蔗糖水溶液得到蔗糖晶体的过程中没有新物质生成,属于物理变化。
故选:B。
【点评】本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物
质生成属于物理变化,若有新物质生成属于化学变化.
4.(2分)一些食物就得近似pH如下:
食物 葡萄汁 苹果汁 牛奶 玉米粥 鸡蛋清
pH 3.5~4.5 2.9~3.3 6.3~6.6 7.0~8.0 7.6~8.0
下列说法不正确的是( )
A.鸡蛋清显碱性 B.苹果汁和葡萄汁显酸性
C.葡萄汁比苹果汁的酸性强 D.胃酸过多的人适宜吃玉米粥
【考点】99:溶液的酸碱性与pH值的关系.
【专题】525:常见的酸 酸的通性.
【分析】当溶液的pH等于7时,呈中性;当溶液的pH大于7时,呈碱性;当溶液的
pH小于7时,呈酸性。
当溶液的pH小于7时,随着pH的减小酸性增强。
【解答】解:A、鸡蛋清的pH大于7,显碱性,故说法正确;
第7页(共22页)B、苹果汁、葡萄汁的pH都小于7,都显酸性,故说法正确;
C、苹果汁、葡萄汁的pH都小于7,都显酸性,但苹果汁的pH更小,酸性更强,故
说法错误;
D、对于胃酸过多的人比较适宜食用的食物是接近中性或偏碱性的食物,而不适
宜吃酸性食物,故说法正确。
故选:C。
【点评】解答本题要掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具
体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论。
5.(2分)下列关于催化剂的说法正确的是( )
A.催化剂必定加快反应速率
B.反应前后催化剂的化学性质通常会发生改变
C.在酿造工业和制药工业,一般都要用酶作催化剂
D.用氯酸钾制取氧气时,加入催化剂可使生成氧气的质量增加
【考点】6J:催化剂的特点与催化作用.
【专题】521:空气与水.
【分析】在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性
质在反应前后都没有发生变化的物质叫做催化剂(又叫触媒).催化剂的特点
可以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量
和化学性质在化学反应前后保持不变.
【解答】解:A、催化剂能改变其他物质的化学反应速率,也可能是减慢反应速率,
故选项说法错误。
B、反应前后催化剂的化学性质不发生改变,故选项说法错误。
C、在酿造工业和制药工业,一般都要用酶作催化剂,故选项说法正确。
D、催化剂只能改变化学反应速率,对生成物的质量无影响,使用催化剂不能增加
产物的质量,故选项说法错误。
故选:C。
【点评】本题难度不大,考查对催化剂概念的理解,掌握催化剂的特征(“一变二
不变”)是正确解答本题的关键.
第8页(共22页)6.(2分)下列各组物质中的分类正确的是( )
A.氧化物:H O、NO 、Fe O
2 2 3 4
B.碱:Ca(OH)、Ba(OH)、Na CO
2 2 2 3
C.酸:CH COOH、CH 、H SO
3 4 2 4
D.盐:NH NO 、MgCl 、CuO
4 3 2
【考点】A9:常见的氧化物、酸、碱和盐的判别.
【专题】516:物质的分类.
【分析】电离时生成的阳离子都是氢离子的化合物是酸,电离时生成的阴离子都
是氢氧根离子的化合物是碱,由金属离子和酸根离子组成的化合物属于盐,氧
化物是含有两种元素且其中一种元素是氧元素的化合物,据此分析.
【解答】解:A、H O、NO 、Fe O 都是由两种元素组成的且有一种是氧元素的化合
2 2 3 4
物,都属于氧化物,故正确;
B、Na CO 是由钠离子和碳酸根离子组成的化合物,属于盐,故错误;
2 3
C、CH 属于有机物,不属于酸,故错误;
4
D、CuO是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,故错误。
故选:A。
【点评】本题主要考查盐的概念,解答时要分析各种物质的组成,然后再根据酸、
碱、盐、氧化物概念的含义进行分析、判断,从而得出正确的结论.
7.(2分)下列关于二氧化碳与一氧化碳的性质比较不正确的是( )
A.组成:均由碳元素和氧元素组成
B.性质:CO 、CO都可以使澄清石灰水变浑浊
2
C.用途:干冰可用于人工降雨;一氧化碳气体可作燃料
D.危害:二氧化碳会导致“温室效应”;一氧化碳会引起中毒
【考点】6Q:二氧化碳的化学性质;6R:二氧化碳的用途;6S:二氧化碳对环境的影
响;6U:一氧化碳的化学性质;6V:一氧化碳的毒性.
【专题】523:碳单质与含碳化合物的性质与用途.
第9页(共22页)【分析】根据物质的元素组成分析解答;根据一氧化碳难溶于水,具有可燃性、还
原性和毒性;二氧化碳的化学性质有:既不能燃烧也不能支持燃烧,也不供给
呼吸;能与水反应生成碳酸;能使澄清的石灰水变浑浊.
【解答】解:A、一氧化碳和二氧化碳都是由碳元素和氧元素组成的,A正确;
B、二氧化碳可以使澄清石灰水变浑浊,一氧化碳不可以,B错误;
C、CO 的固体﹣﹣干冰升华吸热,可用于人工降雨;CO可用作气体燃料、冶炼金
2
属的还原剂等,C正确;
D、CO 会造成“温室效应”,CO有毒,极易使人中毒,D正确;
2
故选:B。
【点评】本考点考查了二氧化碳、一氧化碳的组成、性质和用途,一氧化碳和二氧
化碳也是中考中的重要考点,二氧化碳的特性是能使澄清的石灰水变浑浊,本
考点综合性强,主要出现在选择题和实验题中.
8.(2分)下列除杂,分离提纯的方法或选用的试剂不正确的是( )
选项 物质 所含杂质 除去杂质的方法
A 硝酸钾 少量氯化钠 重结晶
B N O 通过灼热的铜网
2 2
C CaCl 溶液 稀盐酸 加入过量碳酸钙,过滤
2
D Fe 铁锈 稀硫酸
A.A B.B C.C D.D
【考点】2H:物质除杂或净化的探究;4Q:常见气体的检验与除杂方法;93:酸的化
学性质;9H:盐的化学性质.
【专题】167:物质的分离和提纯;533:物质的分离、除杂、提纯与共存问题.
【分析】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提
纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件
①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂
质.
【解答】解:A、KNO 和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度
3
影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、
第10页(共22页)冷却热饱和溶液使KNO 先结晶出来、再过滤的方法;用重结晶的方法可以除
3
去杂质;故选项所采取的方法正确。
B、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除
去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
C、稀盐酸能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的
碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方
法正确。
D、铁锈的主要成分是氧化铁,能与适量的稀硫酸反应生成硫酸铁和水,但若稀硫
酸过量,会与铁反应,不符合除杂原则,故选项所采取的试剂错误。
故选:D。
【点评】物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂
质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确
解题的关键.
9.(2分)验证Zn、Fe、Cu金属的活动性强弱,下列的实际组合实验方案不能达到
实验目的是( )
A.FeSO 溶液、Zn、Cu
4
B.ZnSO 溶液、稀盐酸溶液、Fe、Cu
4
C.ZnSO 溶液、FeSO 溶液、Cu
4 4
D.ZnCl 溶液、CuCl 溶液、Fe
2 2
【考点】86:金属活动性顺序及其应用.
【专题】524:金属与金属材料.
【分析】根据金属活动性顺序,验证金属的活动性顺序是否合理,可根据“反应则
活泼,不反应则不活泼”进行分析判断,通过分析方案所能得到的结论,确定
是否能得出Zn、Fe、Cu三种金属的活动性顺序。
【解答】解:A、Zn与FeSO 溶液反应置换出铁,说明了活动性锌>铁;Cu与FeSO
4 4
溶液不反应,说明了活动性铁>铜,由此可得的三种金属活动性锌>铁>铜,
故该方案合理。
B、Fe、Cu与ZnSO 溶液均不反应,说明了锌的活动性大于铜、铁;Fe能与稀盐酸
4
第11页(共22页)溶液反应而Cu不反应,说明了铁的活动性大于铜,由此可得的三种金属活动
性锌>铁>铜,故该方案合理。
C、Cu与ZnSO 溶液、FeSO 溶液都不反应,说明了锌、铁的活动性大于铜。但无
4 4
法比较锌、铁的活动性,故该方案不合理;
D、Fe与ZnCl 溶液不反应,说明了活动性锌>铁;Fe能与CuCl 溶液反应置换出
2 2
铜,说明了活动性铁>铜,由此可得的三种金属活动性锌>铁>铜,故该方案
合理。
故选:C。
【点评】本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能
灵活运用是正确解答此类题的关键所在。
10.(2分)类推是化学学习中常用的思维方法,以下类推结果中正确的是( )
A.铝与盐酸反应生成AlCl 和H ,则金属铁与盐酸反应生成FeCl 和H
3 2 3 2
B.碱的水溶液显碱性,所以NaOH的水溶液一定是碱性溶液
C.酸溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的一定是酸的
溶液
D.燃烧一般都伴随着发光、放热现象,所以有发光、放热现象的变化就是燃烧
【考点】85:金属的化学性质;93:酸的化学性质;95:碱的化学性质;H1:燃烧与燃
烧的条件.
【专题】213:化学与能源;524:金属与金属材料;525:常见的酸 酸的通性;526:
常见的碱 碱的通性.
【分析】A、根据金属的化学性质,进行分析判断.
B、根据碱的化学性质,进行分析判断.
C、根据紫色石蕊溶液遇酸性溶液变红,进行分析判断.
D、根据燃烧特征、伴随的现象,进行分析判断.
【解答】解:A、铝与盐酸反应生成AlCl 和H ,金属铁与盐酸反应生成FeCl 和
3 2 2
H ,故选项类推结果错误。
2
B、碱的水溶液显碱性,所以NaOH的水溶液一定是碱性溶液,故选项类推结果正
第12页(共22页)确。
C、酸溶液能使紫色试液变红,但能使紫色石蕊变红的不一定是酸的溶液,也可能
是盐溶液,故选项类推结果错误。
D、燃烧一般都伴随着发光、放热现象,但有发光、放热现象的变化不一定是燃烧
如灯泡发光、放热,故选项类推结果错误。
故选:B。
【点评】本题难度不大,掌握碱的化学性质、金属的化学性质、石蕊溶液的性质、燃
烧的特征等是正确解答本题的关键.
二、解答题(共7小题,满分39分)
11.(5分)请从下面五种物质中选择恰当的物质,将其字母代码填入空格中。
A.涤纶 B.硝酸钾 C.苛性钠 D.生铁 E.油脂
(1)可做复合肥的是 B 。
(2)属于基本营养物质的是 E 。
(3)用于铸造农具的是 D 。
(4)属于有机合成材料的是 A 。
(5)能使酚酞溶液变为红色的碱类物质是 C 。
【考点】8E:生铁和钢;91:酸碱指示剂及其性质;9J:常见化肥的种类和作用;I7:
合成材料的使用及其对人和环境的影响;J2:生命活动与六大营养素.
【专题】144:物质的性质与用途.
【分析】物质的性质决定物质的用途,根据已有的物质的性质进行分析解答即可。
【解答】解:(1)硝酸钾中含有氮元素和钾元素,属于复合材料,故填:B;
(2)油脂属于基本营养物质,故填:E;
(3)生铁,可以用于铸造农具,故填:D;
(4)涤纶属于有机合成材料,故填:A;
(5)苛性钠是碱类物质,能使酚酞溶液变为红色,故填:C。
【点评】本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和
用途是正确解答此类题的关键。
第13页(共22页)12.(6分)(1)下列是与水有关的几个描述,请根据所学知识填写完整:
①自然界中的水大多是 混合物 (选填“混合物”或“纯净物”);
② 活性炭 (填物质名称)具有吸附性,可用于水的净化;
③电解H O时,与直流电源的 负 (选填“正”或“负”)极相连的电极附近
2
得到H .
2
(2)甲、乙、丙三种固体物质的溶解度曲线如图所示,请据图回答下列问题:
④ t ℃时,甲和乙两种物质的溶解度相等.
2
⑤t ℃时,将甲、乙、丙的饱和溶液分别降温到t ℃ 丙 (选填“甲”、“乙”或
3 2
“丙”)变为不饱和溶液.
⑥t ℃时,甲、乙、丙三种饱和溶液的溶质的质量分数由大到小的顺序为 丙>乙
1
>甲 .
【考点】6N:制取二氧化碳的操作步骤和注意点;71:电解水实验;75:水的净化;
7J:饱和溶液和不饱和溶液相互转变的方法;7T:溶质的质量分数、溶解性和溶
解度的关系;A5:纯净物和混合物的判别.
【专题】515:溶液、浊液与溶解度;521:空气与水.
【分析】(1)①根据自然界中的水大多是混合物解答;
②根据活性炭具有吸附性解答;
③根据电解水的实验现象及结论解答;
(2)①溶解度曲线的交点表示该温度下物质的溶解度相等;
②根据物质的溶解度曲线可以判断随着温度的变化,物质的溶解度变化情况,进
一步可以判断溶液是否饱和、溶质质量分数的大小;
③根据饱和时质量分数的计算式 ×100%,即溶解度大则溶质的质量
分数大;
第14页(共22页)【解答】解:(1)①自然界中的水大多是混合物;
②活性炭具有吸附性,可用于水的净化;
③电解H O时,与直流电源的负极相连的电极附近得到H .
2 2
(2)①t ℃时,甲和乙两种物质的溶解度相等.
2
②将t ℃时甲、乙、丙三种物质的饱和溶液分别降温到t ℃时,因为甲和乙的溶解
3 2
度随着温度的降低而减小,所得溶液仍为饱和溶液;
丙物质的溶解度随着温度的降低而增大,所以丙物质变成不饱和溶液;
③饱和时质量分数的计算式 ×100%,即溶解度大则溶质的质量分数
大;t ℃时,甲、乙、丙三种物质的溶解度大小为:丙>乙>甲,饱和溶液的溶质
1
的质量分数由大到小的顺序为丙>乙>甲;
答案:
(1)①混合物;②活性炭;③负;
(2)①t ; ②丙; ③丙>乙>甲,
2
【点评】溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:
同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相
同,也可能不同;温度对不同物质的溶解度影响不同,据此分析解答相关问题.
13.(7分)(1)请用化学符号填空:
①氨分子: NH ;②3个镁离子: 3M g 2 + .
3
(2)如图1为某元素的原子示意图,请据此回答:
③该元素的元素符号为 P ;
④该元素位于元素周期表中的第 3 周期.
(3)如图2是一定条件下,某化学变化的微观示意图,请据图回答问题:
⑤SO 分子中S、O元素原子的质量比为 1 : 1 ;
2
第15页(共22页)⑥S2﹣的核外有 1 8 个电子;
⑦写出该反应的化学方程式 3O +2H S 2H O+2SO .
2 2 2 2
【考点】B3:微粒观点及模型图的应用;B8:原子结构示意图与离子结构示意图;
DF:化学符号及其周围数字的意义;G5:书写化学方程式、文字表达式、电离方
程式.
【专题】132:化学反应模拟图型;513:化学用语和质量守恒定律.
【分析】本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对
象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的
计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质
的化学式,才能熟练准确的解答此类题目.如图1元素的原子示意图可知:该
元素是磷元素,位于元素周期表中的第3周期;如图2中,SO 分子中S、O元
2
素原子的质量比=32:(16×2)=1:1;S2﹣的核外有18个电子;氧气和硫化氢在
点燃的条件下生成水和二氧化硫,配平即可.
【解答】解:(1)①一个氨气分子是由一个氮原子和三个氢原子构成的,氨分子的
化学式为:NH ;故答案为:NH ;
3 3
②离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电
荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,
就在其元素符号前加上相应的数字,故3个镁离子可表示为:3Mg2+;故答案为
3Mg2+;
(2)如图1元素的原子示意图可知:该元素是磷元素,位于元素周期表中的第3
周期;故答案为:③P;④3;
(3)如图2中,SO 分子中S、O元素原子的质量比=32:(16×2)=1:1;S2﹣的核外有
2
18个电子;氧气和硫化氢在点燃的条件下生成水和二氧化硫,配平即可;故答
案为:⑤1:1;⑥18;⑦3O +2H S 2H O+2SO ;
2 2 2 2
【点评】本题主要考查学生对化学用语的书写和理解能力、元素周期表等,题目设
计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面
注重基础,题目难度较易.
第16页(共22页)14.(6分)根据图回答问题.
(1)请写出仪器的名称:① 锥形瓶 ,② 水槽 ;
(2)若用A装置制备氧气时,则反应的化学方程式为
2KClO 2KCl+3O ↑ ;
3 2
(3)用大理石和稀盐酸制取CO 时,能作为发生装置的是 B (用字母A~E填
2
空);
(4)HCl是一种极易溶于水的气体,故用 D (用字母A~E填空)装置来收集.
【考点】6C:实验室制取氧气的反应原理;6L:二氧化碳的实验室制法;G5:书写化
学方程式、文字表达式、电离方程式.
【专题】534:常见气体的实验室制法、检验、干燥与净化.
【分析】(1)熟记仪器的名称;
(2)根据装置特点来确定制取原理,书写化学方程式;
(3)根据用大理石和稀盐酸制取CO 时,反应物的状态还反应条件选择发生装置
2
(4)根据HCl的溶解性和密度选择收集装置.
【解答】解:(1)仪器①是锥形瓶,仪器②是水槽;故填:锥形瓶;水槽;
(2)加热的方法制取氧气,可以是加热高锰酸钾,也可以是加热氯酸钾,但加热高
锰酸钾时,试管口应放一团棉花,A装置试管口没有棉花,所以只能用氯酸钾,
故填:2KClO 2KCl+3O ↑;
3 2
(3)用大理石和稀盐酸制取CO 时,是固液反应,不需加热,所以发生装置选择
2
第17页(共22页)B,故填:B;
(4)HCl极易溶于水,所以不能用排水法收集,在相同条件下气体的相对分子质
量越大,密度越大,因为HCl的相对分子质量为36.5,比空气的平均相对分子
质量29大,所以密度比空气大,所以用向上排空气法收集,故选D.
【点评】本道题主要考查了实验室制取氧气的化学方程式、发生装置和收集装置
的选取、实验步骤和一些实验注意事项.
15.(5分)钠盐种类较多,在实验室里,钠盐通常都摆放在同一药品柜中,小华所
在的化学兴趣小组在整理药品柜时,发现某种试剂瓶外壁两边贴上了新旧两
个标签,分别是“Na SO 溶液”、“Na CO 溶液”,小华认为其原因是:
2 4 2 3
Na CO 溶液的试剂瓶混入了Na SO 溶液,并加贴了新标签.该兴趣小组对溶
2 3 2 4
液的成分进行了探究.请你完成以下探究过程,并将①~⑤处的答案填入答题
卡相应位置.
【提出问题】 该试剂瓶内溶质的化学成分是什么
【提出猜想】猜想Ⅰ:溶质仅为Na SO ;
2 4
猜想Ⅱ:溶质仅为Na CO ;
2 3
猜想Ⅲ:溶质为Na SO 和Na CO .
2 4 2 3
【实验探究】
实验操作 实验现象 实验结论
1.取少量样品于一只洁净试管中,加 猜想Ⅰ不
入足量稀硫酸 成立
有气泡产生
2. 先产生白色沉淀;加入硝酸 猜想
溶液后,有气泡产生,沉淀
取少量样品于另一只洁净试管中 Ⅲ 成
部分溶解
,向其中加入过量的BaCl 溶液,过 立
2
滤,向所得沉淀中加入足量稀硝酸
【问题讨论】试写出加入BaCl 溶液后,生成不溶于硝酸的白色沉淀的化学方程式
2
BaCl +Na SO ═BaSO ↓+2NaCl .
2 2 4 4
【考点】2G:实验探究物质的组成成分以及含量;9H:盐的化学性质;G5:书写化
学方程式、文字表达式、电离方程式.
【专题】537:科学探究.
第18页(共22页)【分析】【提出问题】根据题中信息提出探究的问题;
【实验探究】根据碳酸钠和硫酸反应的现象分析解答;根据碳酸钠和氯化钡反应
的原理分析现象;
【问题讨论】根据硫酸钠和氯化钡反应产生硫酸钡沉淀和氯化钠解答,
【解答】解:
【提出问题】根据题中信息可知是探究该试剂瓶内溶质的化学成分是什么;
【实验探究】1.取少量样品于一只洁净试管中,加入足量稀硫酸,有气泡产生,碳
酸钠和硫酸反应,生成二氧化碳气体,说明有碳酸钠,猜想Ⅰ不成立;
2.取少量样品于另一只洁净试管中,向其中加入过量的BaCl 溶液,过滤,向所得
2
沉淀中加入足量稀硝酸,先产生白色沉淀;加入硝酸溶液后,有气泡产生,沉淀
部分溶解,说明沉淀中有碳酸钡和硫酸钡,碳酸钠和氯化钡反应产生碳酸钡沉
淀和氯化钠;硫酸钠和氯化钡反应产生硫酸钡沉淀和氯化钠;该试剂瓶内溶质
的化学成分是碳酸钠和硫酸钠,猜想Ⅲ成立;
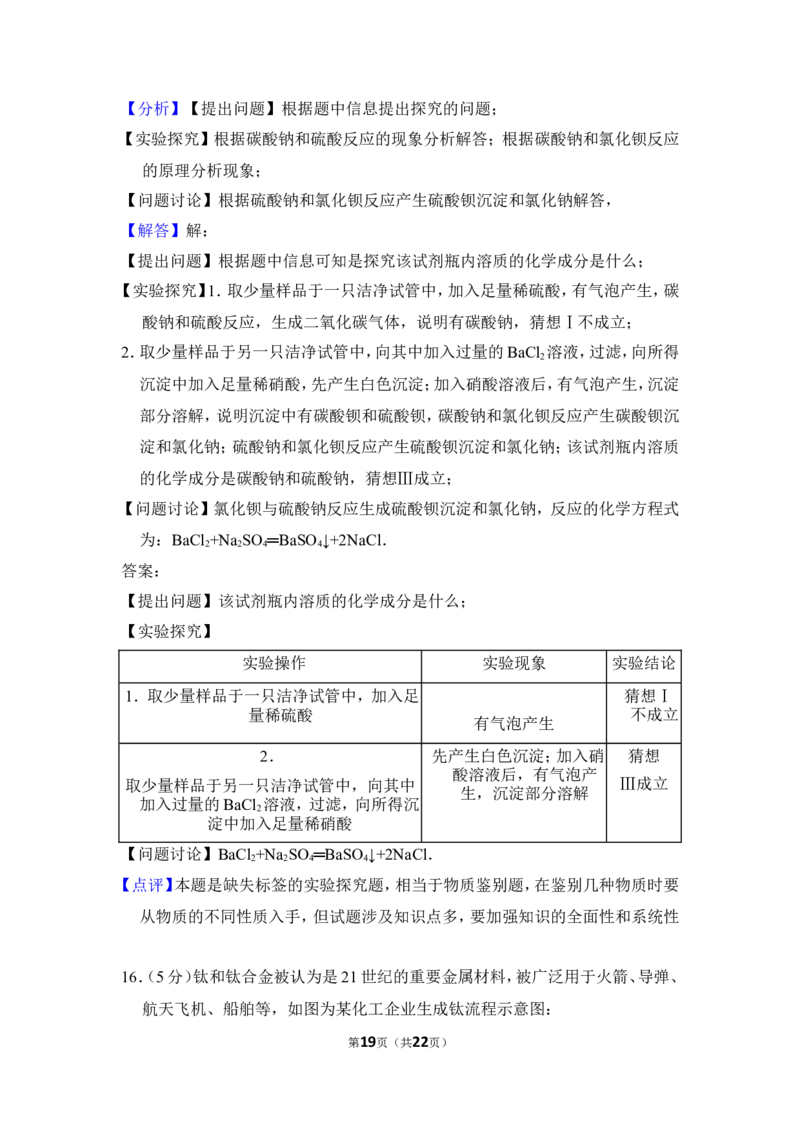
【问题讨论】氯化钡与硫酸钠反应生成硫酸钡沉淀和氯化钠,反应的化学方程式
为:BaCl +Na SO ═BaSO ↓+2NaCl.
2 2 4 4
答案:
【提出问题】该试剂瓶内溶质的化学成分是什么;
【实验探究】
实验操作 实验现象 实验结论
1.取少量样品于一只洁净试管中,加入足 猜想Ⅰ
量稀硫酸 不成立
有气泡产生
2. 先产生白色沉淀;加入硝 猜想
酸溶液后,有气泡产
取少量样品于另一只洁净试管中,向其中 Ⅲ成立
生,沉淀部分溶解
加入过量的BaCl 溶液,过滤,向所得沉
2
淀中加入足量稀硝酸
【问题讨论】BaCl +Na SO ═BaSO ↓+2NaCl.
2 2 4 4
【点评】本题是缺失标签的实验探究题,相当于物质鉴别题,在鉴别几种物质时要
从物质的不同性质入手,但试题涉及知识点多,要加强知识的全面性和系统性
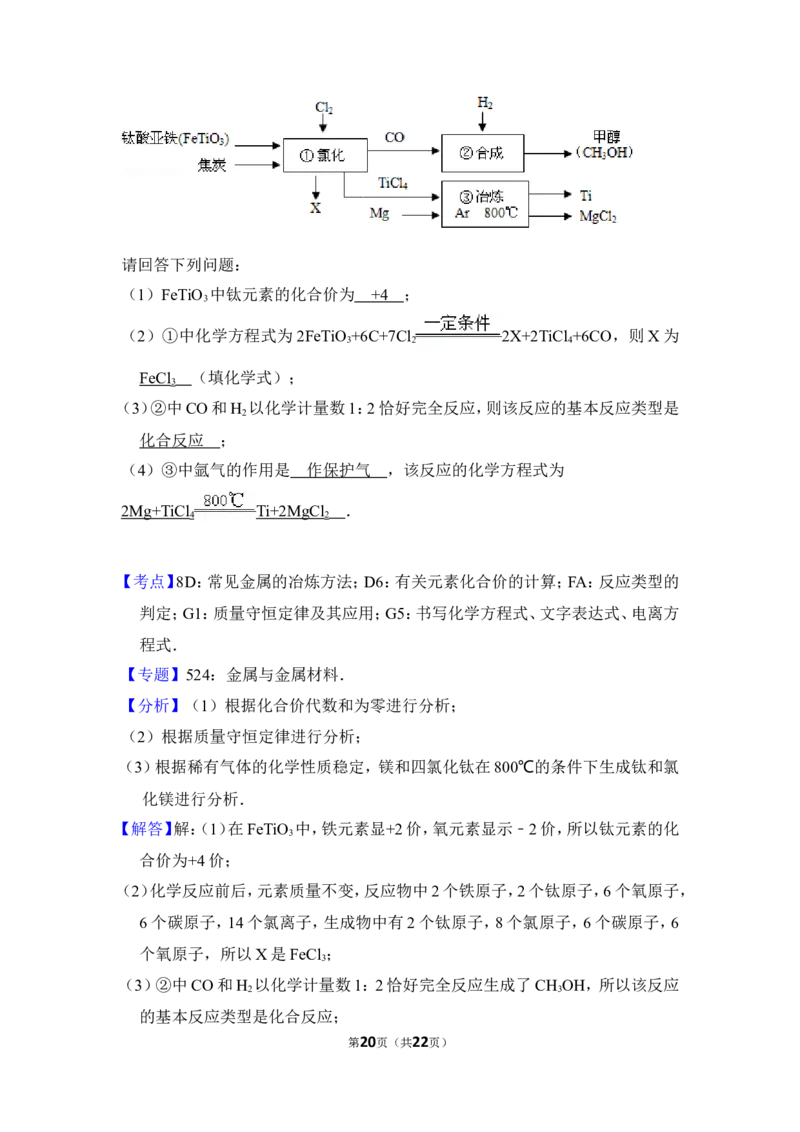
16.(5分)钛和钛合金被认为是21世纪的重要金属材料,被广泛用于火箭、导弹、
航天飞机、船舶等,如图为某化工企业生成钛流程示意图:
第19页(共22页)请回答下列问题:
(1)FeTiO 中钛元素的化合价为 + 4 ;
3
(2)①中化学方程式为2FeTiO +6C+7Cl 2X+2TiCl +6CO,则X为
3 2 4
FeCl (填化学式);
3
(3)②中CO和H 以化学计量数1:2恰好完全反应,则该反应的基本反应类型是
2
化合反应 ;
(4)③中氩气的作用是 作保护气 ,该反应的化学方程式为
2Mg+TiCl Ti+2MgCl .
4 2
【考点】8D:常见金属的冶炼方法;D6:有关元素化合价的计算;FA:反应类型的
判定;G1:质量守恒定律及其应用;G5:书写化学方程式、文字表达式、电离方
程式.
【专题】524:金属与金属材料.
【分析】(1)根据化合价代数和为零进行分析;
(2)根据质量守恒定律进行分析;
(3)根据稀有气体的化学性质稳定,镁和四氯化钛在800℃的条件下生成钛和氯
化镁进行分析.
【解答】解:(1)在FeTiO 中,铁元素显+2价,氧元素显示﹣2价,所以钛元素的化
3
合价为+4价;
(2)化学反应前后,元素质量不变,反应物中2个铁原子,2个钛原子,6个氧原子,
6个碳原子,14个氯离子,生成物中有2个钛原子,8个氯原子,6个碳原子,6
个氧原子,所以X是FeCl ;
3
(3)②中CO和H 以化学计量数1:2恰好完全反应生成了CH OH,所以该反应
2 3
的基本反应类型是化合反应;
第20页(共22页)(4)稀有气体的化学性质稳定,可以作保护气,镁和四氯化钛在800℃的条件下生
成钛和氯化镁,化学方程式为:2Mg+TiCl Ti+2MgCl .
4 2
故答案为:(1)+4;
(2)FeCl ;
3
(3)化合反应;
(4)作保护气,2Mg+TiCl Ti+2MgCl .
4 2
【点评】在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的
提示进行解答.
17.(5分)取8.0g铝土矿(主要成分是Al O ),溶于128.4g稀盐酸中,盐酸恰好完
2 3
全反应.经过滤、干燥后,得到滤渣2.9g,(假定铝土矿样品中所含的杂质不溶
于盐酸).
(1)求铝土矿的纯度 63.7 5 %.
(2)求所得溶液的溶质的质量分数(写出计算过程).
【考点】7U:有关溶质质量分数的简单计算;G6:根据化学反应方程式的计算.
菁
【专题】194:溶质质量分数与化学方程式相结合的计算.
【分析】(1)根据铝土矿和残渣的质量可求出铝土矿的纯度;
(2)根据氧化铝与盐酸的反应和氧化铝的质量可求出氯化铝的质量,再根据溶液
的溶质的质量分数计算.
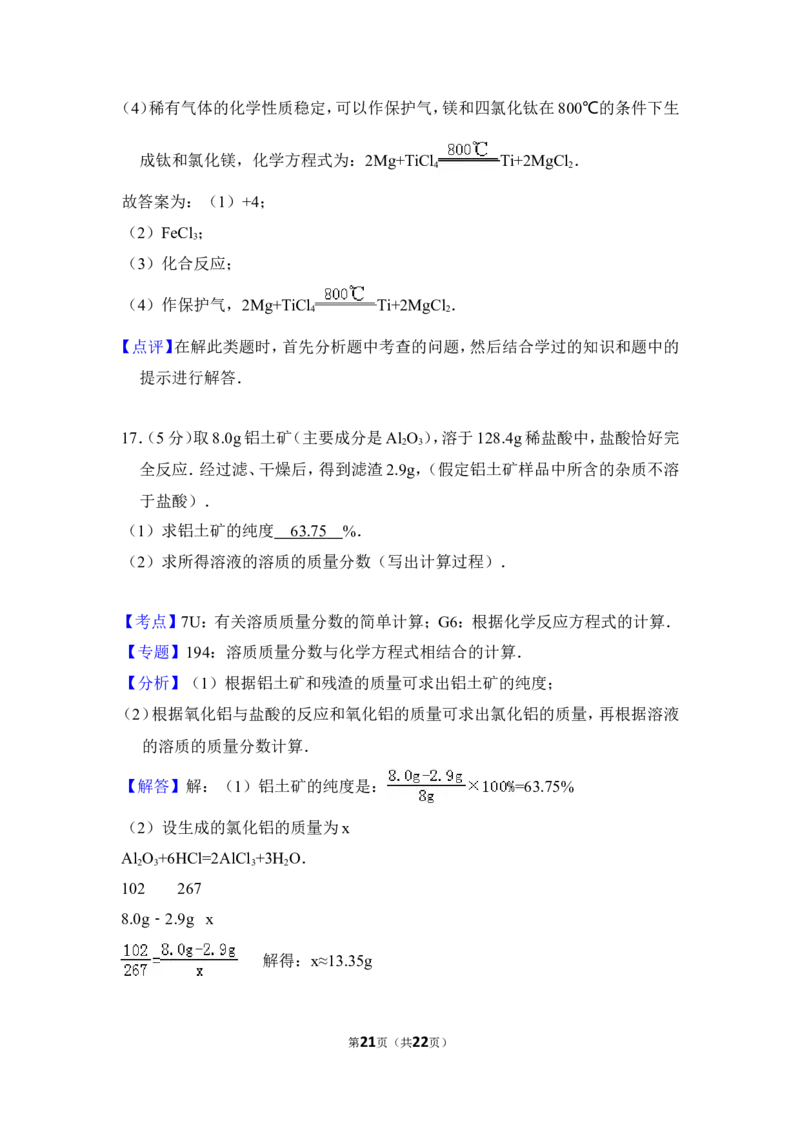
【解答】解:(1)铝土矿的纯度是: =63.75%
(2)设生成的氯化铝的质量为x
Al O +6HCl=2AlCl +3H O.
2 3 3 2
102 267
8.0g﹣2.9g x
解得:x≈13.35g
第21页(共22页)所得溶液的溶质的质量分数是: =10%
故答为:(1)63.75;(2)求所得溶液的溶质的质量分数是10%.
【点评】本题主要考查了根据化学方程式和溶液质量分数的计算,难度不大,主语
书写的格式要规范,计算的数据要准确.
第22页(共22页)