文档内容
2017年四川省绵阳市中考化学试卷
一、选择题(每小题3分,每个小题只有一个选项最符合题目要求)
1.(3分)化学与生活密切相关.下列说法正确的是( )
A.合成纤维、塑料、棉花都属于合成有机高分子材料
B.用肥皂水可鉴别硬水和软水;用明矾净水即得软水
C.福尔马林能杀菌消毒,干冰可作制冷剂,都可用于对食品保鲜
D.碳酸氢钠俗称小苏打,是焙制糕点所用的发酵粉的主要成分之一
2.(3分)“分类”可以使人们有序地研究物质。以下分类正确的是( )
A.碱:苛性钠、纯碱、熟石灰
B.合金:硬铝、青铜、18K金
C.酸:硝酸、硫酸、碳酸氢钠
D.糖类:蔗糖、纤维素、蛋白质
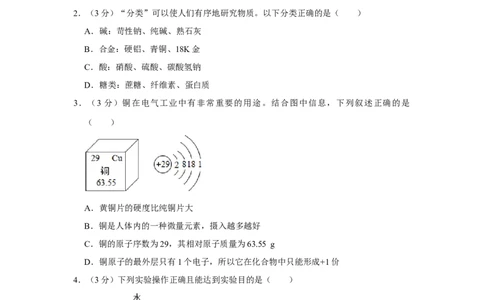
3.(3 分)铜在电气工业中有非常重要的用途。结合图中信息,下列叙述正确的是
( )
A.黄铜片的硬度比纯铜片大
B.铜是人体内的一种微量元素,摄入越多越好
C.铜的原子序数为29,其相对原子质量为63.55 g
D.铜原子的最外层只有1个电子,所以它在化合物中只能形成+1价
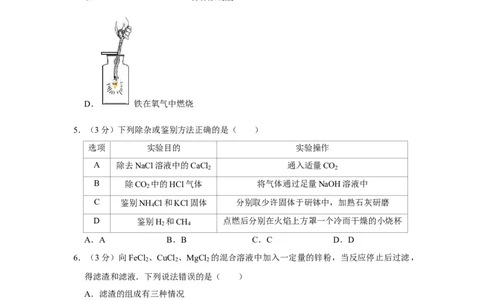
4.(3分)下列实验操作正确且能达到实验目的是( )
A. 探究NaOH固体溶于水的能量变化
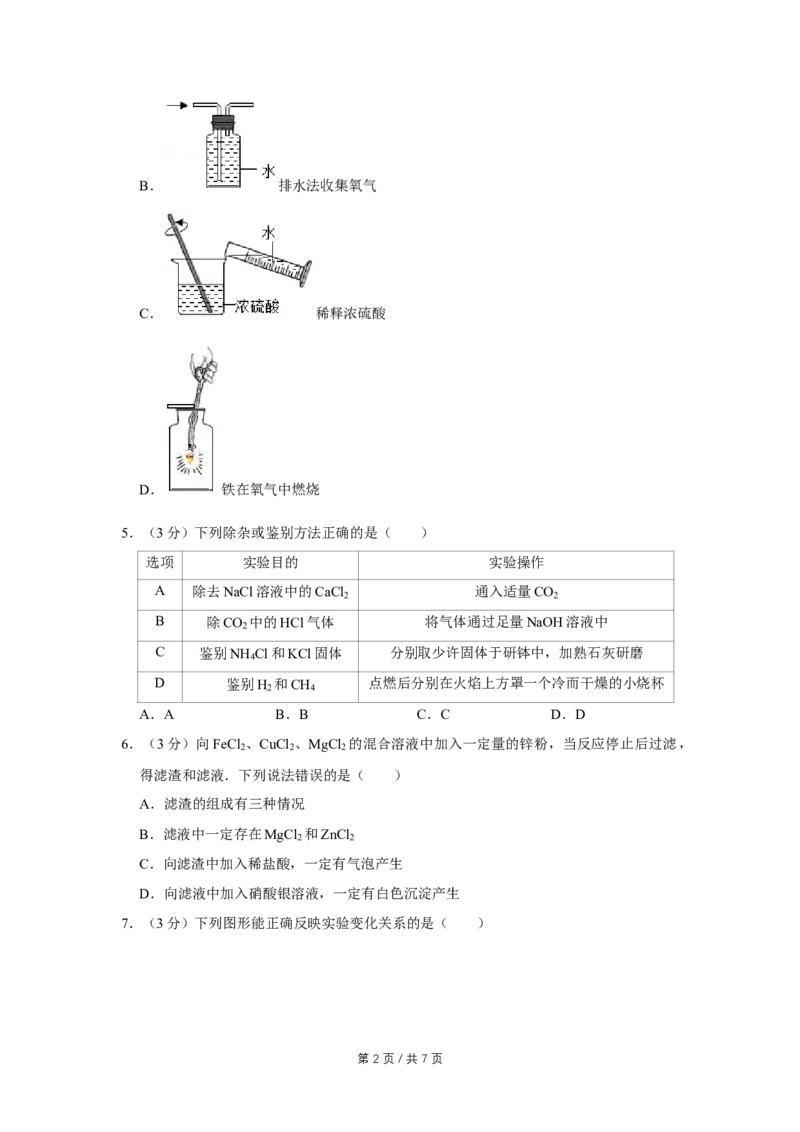
第 1 页 / 共 7 页B. 排水法收集氧气
C. 稀释浓硫酸
D. 铁在氧气中燃烧
5.(3分)下列除杂或鉴别方法正确的是( )
选项 实验目的 实验操作
A 除去NaCl溶液中的CaCl 通入适量CO
2 2
B 除CO 中的HCl气体 将气体通过足量NaOH溶液中
2
C 鉴别NH Cl和KCl固体 分别取少许固体于研钵中,加熟石灰研磨
4
D 鉴别H 和CH 点燃后分别在火焰上方罩一个冷而干燥的小烧杯
2 4
A.A B.B C.C D.D
6.(3分)向FeCl 、CuCl 、MgCl 的混合溶液中加入一定量的锌粉,当反应停止后过滤,
2 2 2
得滤渣和滤液.下列说法错误的是( )
A.滤渣的组成有三种情况
B.滤液中一定存在MgCl 和ZnCl
2 2
C.向滤渣中加入稀盐酸,一定有气泡产生
D.向滤液中加入硝酸银溶液,一定有白色沉淀产生
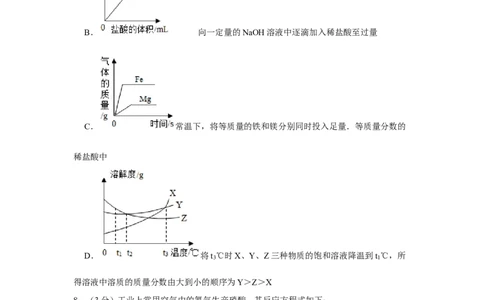
7.(3分)下列图形能正确反映实验变化关系的是( )
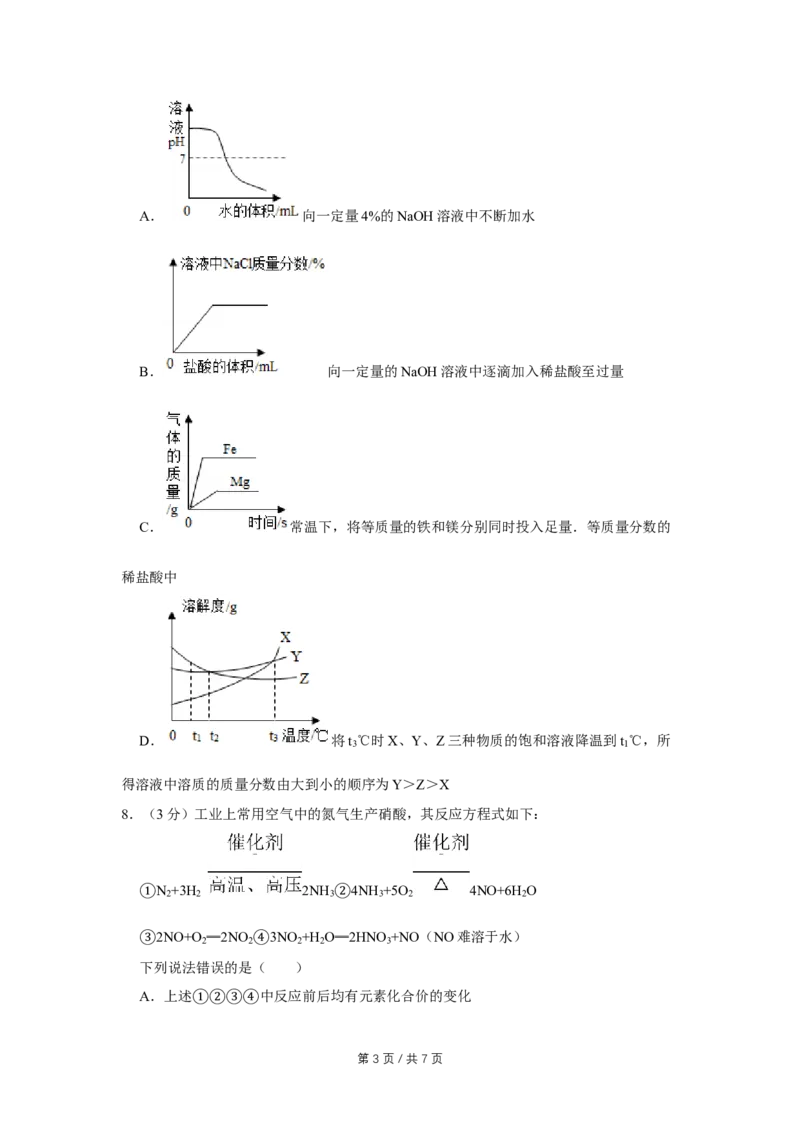
第 2 页 / 共 7 页A. 向一定量4%的NaOH溶液中不断加水
B. 向一定量的NaOH溶液中逐滴加入稀盐酸至过量
C. 常温下,将等质量的铁和镁分别同时投入足量.等质量分数的
稀盐酸中
D. 将t ℃时X、Y、Z三种物质的饱和溶液降温到t ℃,所
3 1
得溶液中溶质的质量分数由大到小的顺序为Y>Z>X
8.(3分)工业上常用空气中的氮气生产硝酸,其反应方程式如下:
N +3H 2NH 4NH +5O 4NO+6H O
2 2 3 3 2 2
① ②
2NO+O ═2NO 3NO +H O═2HNO +NO(NO难溶于水)
2 2 2 2 3
③下列说法错误的是(④ )
A.上述 中反应前后均有元素化合价的变化
①②③④
第 3 页 / 共 7 页B.用H O吸收NO 的过程中通入过量的O 可以提高硝酸的产量
2 2 2
C.反应 都不属于四种基本反应类型中的任何一种,反应 均属于化合反应
D.在密②闭容④器中,将46g NO
2
溶于64g H
2
O中形成HNO
3
溶液①,③其溶质的质量分数约
为38.2%
9.(3分)120℃时,取3g有机物R在氧气中完全燃烧,产物只有CO 和H O.将其燃烧
2 2
产物依次通过足量的浓硫酸和足量的澄清石灰水中,最终浓硫酸增重 1.8g;澄清石灰水
中产生10g沉淀。下列判断正确的是( )
A.R的化学式一定是CH O
2
B.6g R完全燃烧消耗氧气6.4g
C.R中碳元素的质量分数约为85.7%
D.R仅由C、H两种元素组成,其质量比为6:1
二、解答题
10.(7分)X、Y、Z、W是初中化学常见的四种非金属元素.X的一种原子没有中子,Y
的一种单质可用于制铅笔芯,Z是地壳中含量最高的元素,W 是空气中含量最高的单质.
2
回答下列问题:
Y的另一种单质是天然存在的最硬的物质,该单质的名称为 ,Z2﹣的离子结构
①示意图为 .
X、Z、W三种元素可形成一种盐,该盐是一种常见的化肥,其化学式为 .
②实验室检验YZ
2
时发生反应的化学方程式为 .
③钠与Z形成的化合物Na
2
Z
2
常用作潜水艇中的供氧剂,因为Na
2
Z
2
与YZ
2
反应生成
④Na YZ 和Z ,写出其反应的化学方程式 .
2 3 2
X、Y、W三种元素可按质量比2:6:7形成一种的火箭燃料偏二甲肼,其相对分子
⑤质量为60,偏二甲肼在空气中完全燃烧的产物均无污染,其化学方程式为 .
11.(8分)初中化学几种常见物质的相互转化关系如图所示,其中A为无色无味的有毒
气体,B是赤铁矿的主要成分,F常用于改良酸性土壤,H为常见的液态化合物,K是
一种紫红色单质。根据推断回答下列问题:
E溶液的颜色为 ,反应Ⅰ~Ⅲ中属于置换反应的是 (填编号),化合
①物Na DO 中D的化合价为 。
2 4
写出反应Ⅰ的化学方程式 ,该反应在工业上的用途是 。
②写出一个由G制取C的化学方程式 。
③D与K的混合物7 g与足量的E溶液充分反应后,固体质量增加0.8g,则该混合物中
④
第 4 页 / 共 7 页D的质量分数为 。
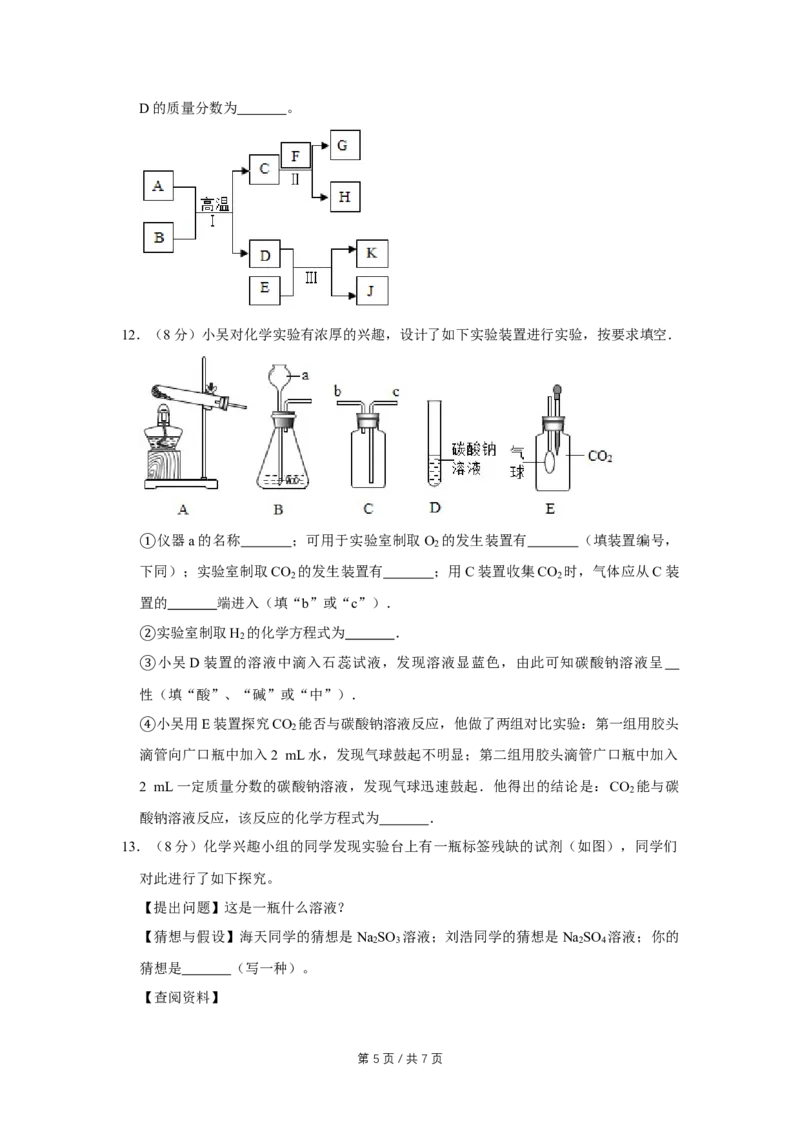
12.(8分)小吴对化学实验有浓厚的兴趣,设计了如下实验装置进行实验,按要求填空.
仪器a的名称 ;可用于实验室制取O 的发生装置有 (填装置编号,
2
①下同);实验室制取CO 的发生装置有 ;用C装置收集CO 时,气体应从C装
2 2
置的 端进入(填“b”或“c”).
实验室制取H 的化学方程式为 .
2
②小吴D装置的溶液中滴入石蕊试液,发现溶液显蓝色,由此可知碳酸钠溶液呈
③性(填“酸”、“碱”或“中”).
小吴用E装置探究CO 能否与碳酸钠溶液反应,他做了两组对比实验:第一组用胶头
2
④滴管向广口瓶中加入2 mL水,发现气球鼓起不明显;第二组用胶头滴管广口瓶中加入
2 mL一定质量分数的碳酸钠溶液,发现气球迅速鼓起.他得出的结论是:CO 能与碳
2
酸钠溶液反应,该反应的化学方程式为 .
13.(8分)化学兴趣小组的同学发现实验台上有一瓶标签残缺的试剂(如图),同学们
对此进行了如下探究。
【提出问题】这是一瓶什么溶液?
【猜想与假设】海天同学的猜想是Na SO 溶液;刘浩同学的猜想是Na SO 溶液;你的
2 3 2 4
猜想是 (写一种)。
【查阅资料】
第 5 页 / 共 7 页Ⅰ白色沉淀BaSO 不溶于水,但要溶于稀盐酸。
3
Ⅱ硝酸具有强氧化性,能将BaSO 氧化成BaSO 。
3 4
ⅢNa SO 与稀盐酸反应产生SO ,SO 能使石灰水变浑浊,也能使品红溶液褪色。
2 3 2 2
【进行实验】
Ⅰ海天同学取适量的该溶液于试管中,滴加稀盐酸,产生无色气体,他认为自己的猜想
成立,而刘浩同学认为他的结论不合理,原因是 。
Ⅱ刘浩同学为了验证自己的猜想,做了如下实验:
取适量的该溶液于试管中,先滴加足量的 BaCl 溶液,再滴加过量稀硝酸,现象为
2
,刘浩同学认为自己的猜想成立。
Ⅲ卓玛同学对刘浩同学的猜想又提出了质疑,她认为加BaCl 和稀硝酸,Na SO 也会产
2 2 3
生沉淀,为了验证自己的观点,做了如下实验:
步骤 操作 实验现象 实验结论
步骤1 取少量该溶液于试管中,滴 无
加足量的BaCl 溶液
2
步骤2 向步骤1的试管中滴加足量 此溶液不是Na SO
2 4
的稀盐酸
步骤3 将步骤2中产生的气体通入 品红溶液褪色
品红溶液
写出卓玛同学实验过程中的化学方程式: , 。
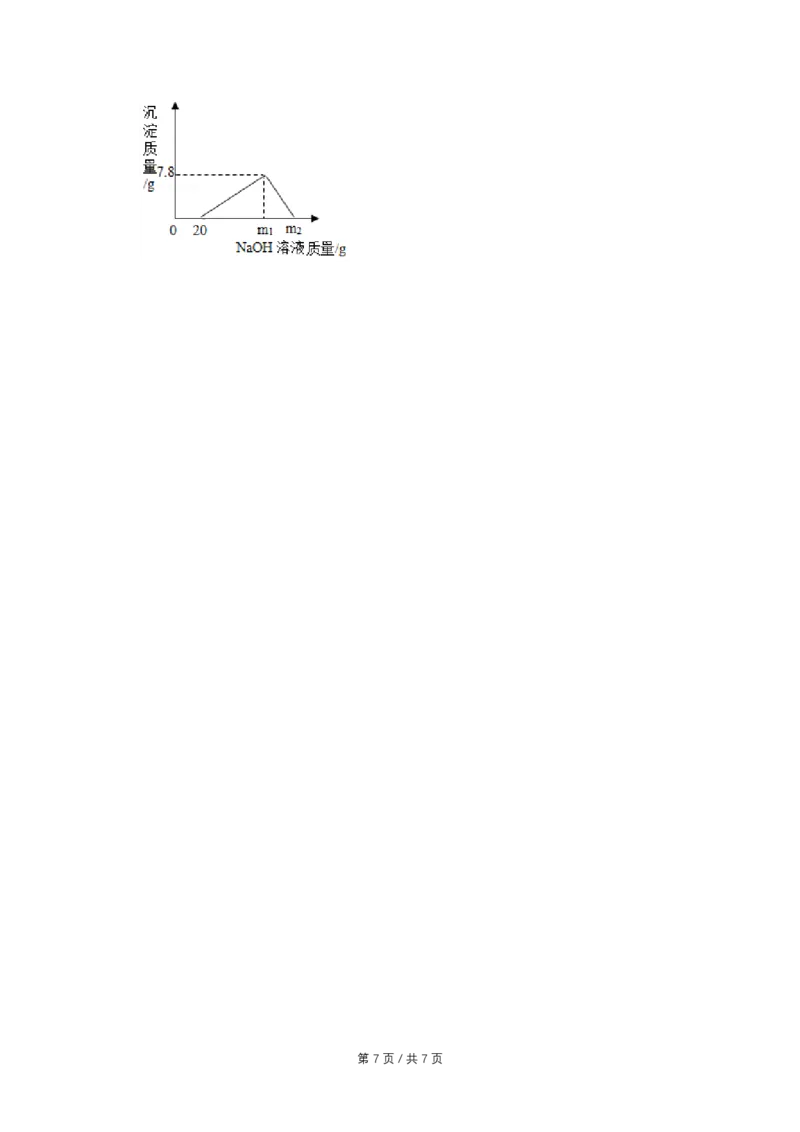
14.(7分)已知:Al(OH) 沉淀可溶于NaOH溶液,其反应方程式为:Al(OH)
3
+NaOH═NaAlO +2H O,现向100 g HCl和AlCl 的混合溶液中逐滴加入质量分数为
3 2 2 3
20%的NaOH溶液,产生沉淀的质量与所加NaOH溶液的质量关系如图所示。回答下列
问题:
(1)原混合溶液中HCl的质量分数是 。
(2)当沉淀达到最大值时生成NaCl的质量是多少?
(3)m = 。
2
第 6 页 / 共 7 页第 7 页 / 共 7 页