文档内容
苏州市 2018 年中考化学试题
选择题(共50分)
1、2018世界环境日中国确定的主题是“美丽中国,我是行动者”,下列做法符合这一主题的
是
A.作物秸秆露天焚烧 B.废旧塑料随意丢弃
C.废旧电池就地填埋 D.生活垃圾分类回收
2、新能源的开发利用是人类社会可持续发展的重要课题。下列属于新能源的是
A.天然气 B.石油 C.氢气 D.煤
3、下列物质属于纯净物的是
A.空气 B.生铁 C.硬水 D.氧气
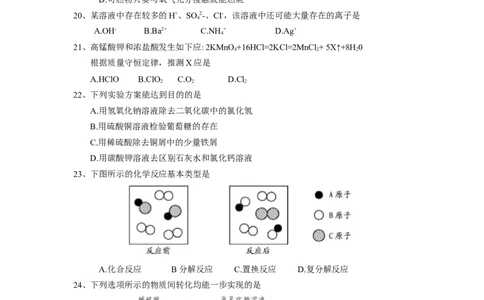
4、下列化学仪器对应的名称正确的是
5、下列变化属于化学变化的是
A.冰雪融化 B.光合作用 C.汽油挥发 D.铁丝弯曲
6、下列过程吸收热量的是
A.氢氧化钠固体溶丁水 B.硝酸铵固体溶于水
C.把水加入生石灰中 D.氢氧化钠溶液与稀硫酸反应
7、下列有关化学用语表示正确的是
A. 氯原子结构示意图:
B 2个氢离子: 2H2+
C. 酒精的化学式C HO
2 6
D. 氧化钠中氧元素是-2价: Na
8、化学让我们的生活更美好,科学家为此作出了很大的努力,其中在制碱工业作出巨大贡献
的是
A.拉瓦锡 B.门捷列夫 C.汤姆生 D.侯德榜
19、下列人体所缺元素与引起的健康问题关系正确的是
A.缺铁会引起贫血 B.缺碘会引起龋齿
C.缺锌会导致甲状腺疾病 D.缺钙会引起坏血病
10、水是生命之源,下列物质的化学式可用“HO”表示的是
2
A.冰 B.可燃冰 C.下冰 D.水银
11、下列气体的排放会导致酸雨形成的是
A. N B. CO C. SO D. O
2 2 2
12、下列标志属于中国节能标志的是
A B C D
13、下列关于浓硫酸的说法正确的是
A.易挥发 B.有腐蚀性 C.无吸水性 D.密度比水水
14、下列有关物质用途的说法正确的是
A.明矾可用作净水剂 B.聚氯乙烯可用来包装食品
C.氢氧化钠可用来治疗胃酸过多 D.铝制容器可用来长期存放酸性食物
15、下列有关实验现象的描述正确的是
A.红磷在空气中燃烧,产生大量白色烟雾
B.用粗砂纸打磨后的铝片放入硫酸铜溶液中,一段时间后,划痕处出现红色物质
C.铁丝在氧气中剧烈燃烧,火星四射,生成红色固体
D.向滴有石蕊的稀盐酸中滴加氢氧化钠溶液至过量,溶液有监色变紫色再变红色
16、下列实验操作正确的是
17、下列关于糖类、蛋白质、油脂和维生素的说法正确的是
A.淀粉没有甜味,所以不属于糖类 B.维生素是人体不可缺少的营养物质
C.油脂属于有机高分子化合物 D.蛋白质中只含有碳、氢、氧三种元素
18、 《茉莉花》是一首脍炙人口的苏南民歌。茉莉花香气的成分有多种,乙酸苯甲酯(C H O)
9 10 2
是其中的一种。下列关于乙酸苯甲酯的说法正确的是
2A.乙酸苯甲酯的相对分子质量为150g
B.乙酸苯甲酯由碳、氢、氧三种元素组成
C.乙酸苯甲酯中碳、氢、氧三种元素质量比为9: 10: 2
D.乙酸苯甲酯分子由碳原子、氢原子、氧分子构成
19、下列说法正确的是
A.空气中氧气的体积分数约为21%
B.洗涤油污可用汽油乳化
C.电解水实验说明水是由氢气和氧气组成的
D.可燃物只要与氧气充分接触就能燃烧
20、某溶液中存在较多的H+、SO 2-、CI-,该溶液中还可能大量存在的离子是
4
A.OH- B.Ba2+ C.NH+ D.Ag+
4
21、高锰酸钾和浓盐酸发生如下应: 2KMnO +16HCl=2KCl=2MnCl + 5X↑+8H0
4 2 2
根据质量守恒定律,推测X应是
A.HClO B.ClO C.O D.Cl
2 2 2
22、下列实验方案能达到目的的是
A.用氢氧化钠溶液除去二氧化碳中的氯化氢
B.用硫酸铜溶液检验葡萄糖的存在
C.用稀硫酸除去铜屑中的少量铁屑
D.用碳酸钾溶液去区别石灰水和氯化钙溶液
23、下图所示的化学反应基本类型是
A.化合反应 B分解反应 C.置换反应 D.复分解反应
24、下列选项所示的物质间转化均能一步实现的是
25、一定质量的某有机化合物完全燃烧,生成2.2gCO 和1.8gH O,另取3.2g该有机化合物在
2 2
O 中完全燃烧,消耗4.8gO ,该有机化合物的化学式可能是
2 2
A.C H B.CH O C.CH D.C HO
2 4 4 4 2 4
3非选择题(共50分)
26、(5分)请用线段连接有对应关系的相邻两行间的点(每个点只能连接1次)
27、(5分)生活中处处有化学,化学已渗透到我们的“衣、食、住、行、医”中。
(1)衣:区分羊毛线和棉纱线的方法是灼烧,羊毛线燃烧时能闻到_________气味。
(2)食:维生素C能增强人体对疾病的抵抗能力,中学生每天要补充60mg的维生素C,
下列物质富含维生素C的是____(填字母) 。
A.橙子 B.猪肉 C.面粉
(3)住:下列属丁直接利用太阳能辐射加热物体而获得热能的是________(填字母)。
A.石蜡燃烧 B.太阳能热水器 C.燃料电池
(4)行:城市交通中大力推广新能源汽车对于改善空气质量的好处是____________。
(5)医:出现低血糖症状时需要尽快补允简萄糖,葡萄糖的化学式是________。
28、(5分)根据下列反应事实写出相应的化学方程式。
(1)稀硫酸与锌粒反应制氢气:___________,
(2)金属铝与氧气反应生成氧化膜:________________;
(3)碳酸钙在高温下分解:________________;
(4)石灰水与硫酸铜溶液反应:________________;
(5)甲烷在足量氧气中充分燃烧:________________;
29、(8分)硝酸钾是实验室常见的一种试剂。
(1)硝酸钾是由___和___构成的(填写微粒符号)。
(2)硝酸钾中钾元素的质量分数是__________(结果用百分数表示,保留到0.1%)。
(3)右图是硝酸钾的溶解度曲线,由图可以总结出硝酸钾的溶解度随温度变化的趋势是
_________。60℃时110g硝酸钾溶于100g水中形成的溶液是____ ( 选填“饱和“或
“不饱和”)溶液,将此时配得的溶液降温至20℃,析出硝酸钾晶体的质量是___g。
4(4)列式计算:用100g10%的硝酸钾溶液配制5%的硝酸钾溶液。需要加水多少亳升?
(水的密度为1.0g·mL-1)
30、(6分)从大理石(主要杂质是氧化铁)中提纯碳酸钙的一种实验流程如下:
(1)反应池I中用硝酸不用稀硫酸的主要原因是______________。
(2)反应池II中加入氨水的目的是______________。
(3)反应池III用生成碳酸钙的化学方程式是______________。
(4)过滤II中所得滤液在农业生产中的一种用途是______________。
31、(6分)化学是一门以实验为基础的科学,化学实验和科学探究离不开实验装置。
5(1)制取气体实验时,首先要对发生的装置进行气密性检查,确保装置不漏气,装置C气
密性检查的方法是________________________。
(2)收集某种气体的方法,主要取决于这种气体的性质,装置E所示的收集方法是
______________,被收集的气体密度_______空气密度(选填“>”,“<”,“=”)。
(3)实验室用大理石与稀盐酸制取并收集一瓶干燥的二氧化碳,所选装置正确的连接顺
序是______→______→______(填装置编号)。
(4)下图所示一氧化碳与氧化铁的反应装置中,虚线方框内装置的作用有___________
_________________________。
32、(7分)(1)控制变量,设计对比试验是实验探究的重要方法。
6(2)观察是学习化学的重要方法。
研究小组进行如下实验,发现均有红棕色二氧化氮气体产生。
查阅资料:4HNO O↑+4NO↑+2H O
3 2 2 2
C+4HNO (浓) CO↑+4NO↑+2H O
3 2 2 2
①【实验1】中所用碎玻璃与浓硝酸不发生化学反应,灼热的碎玻璃在实验中起到的作用
是____________________。
②【实验2】中有红棕色气体产生,能否证明【实验2】中木炭与浓硝酸发生了反应?请做
出判断,并说明理由:________________________________________。
③【实验3】中发现红热的木炭表面有红棕色气体产生,且生成的气体产物中检测出二氧
化碳(体积分数大于0.03%),能否证明【实验3】中木炭与浓硝酸发生了反应?请做出判
7断,并说明理由:________________________________________。
33、探究碳酸氢钠、碳酸钠分别与稀盐酸反应,研究小组进行如下两个实验:
(1)【实验1】同时将足量的稀盐酸倒入锥形瓶甲和锥形瓶乙中。
反应至5s生成气体的速率:碳酸氢钠___碳酸钠(选填“>”,“<”,“=”)。
【实验2】分别将足量的稀盐酸逐滴滴入试管甲和试管乙中,边滴边振荡。
现象为:
①试管甲中的溶液开始时显浅红色,逐滴滴入稀盐酸立即产生大量气泡,浅红色逐渐消
失。
②试管乙中的溶液开始时显红色,滴入稀盐酸没有气泡产生,溶液颜色逐渐变为浅红色
后,继续滴加稀盐酸有大量气泡产生,浅红色逐渐消失。
(2)【反思1】在【实验2】碳酸钠溶液中逐滴滴入稀盐酸,为何刚开始没有大量气泡产生?
研究小组查阅资料,绘制出微观示意图。
①碳酸钠溶液中逐滴滴入稀盐酸,依次发生反应的化学方程式为
________________________、___________________________。
8②相同浓度的碳酸氢钠溶液和碳酸钠溶液的碱性:碳酸氢钠_______碳酸钠(选填“>”,
“<”,“=”)。
(3)【反思2】为何【实验1】中碳酸氢钠最终产生气体的体积较大?
请你列式计算:【实验1】中两种固体完全反应后产生气体的质量各是多少(写出计算过
程,结果保留到0.1g)?
91011