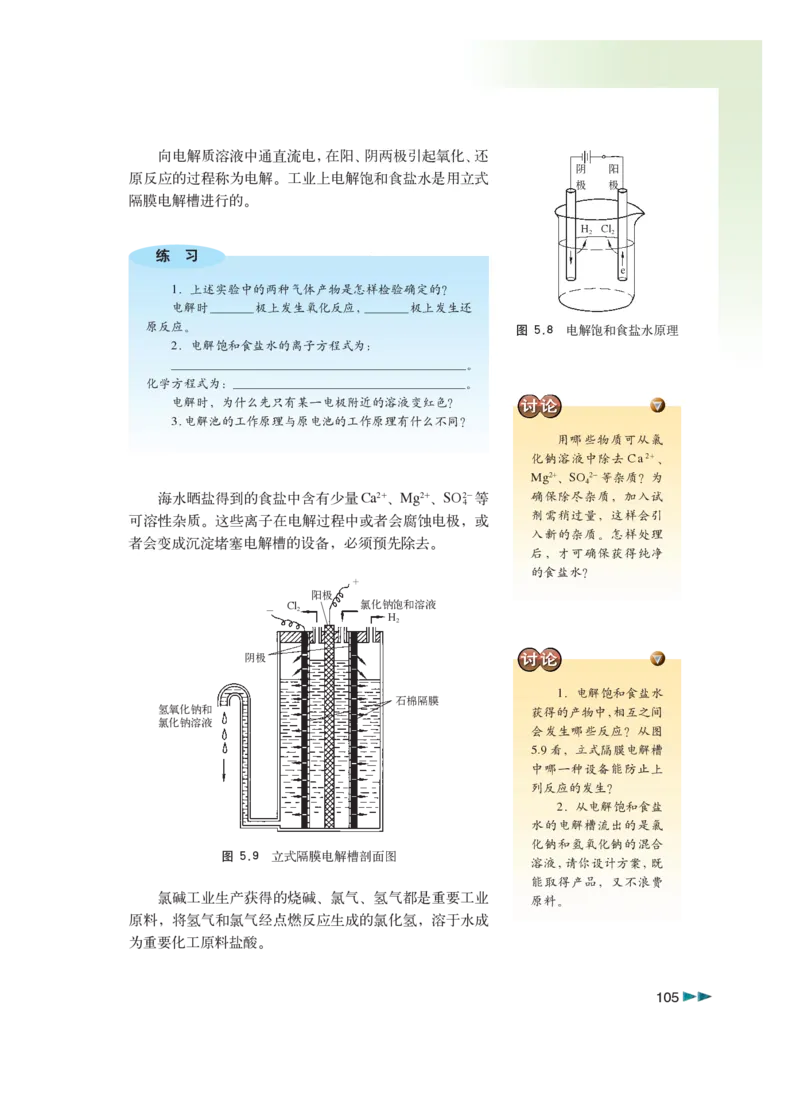
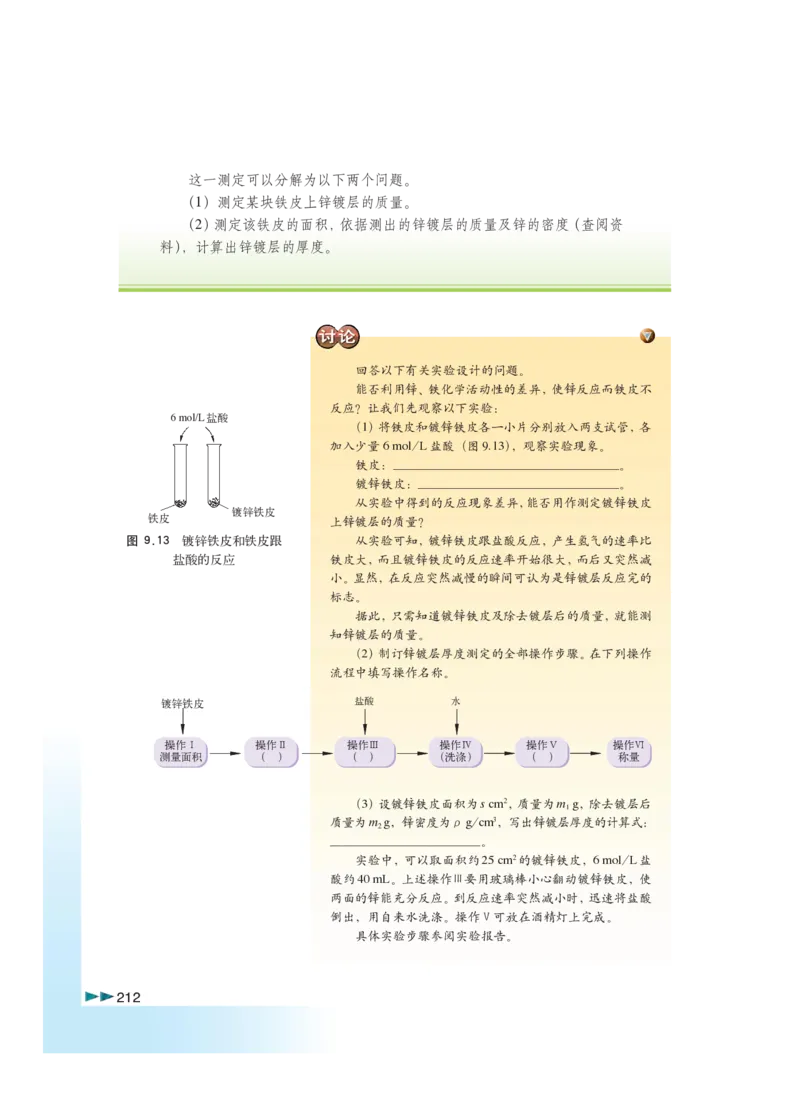
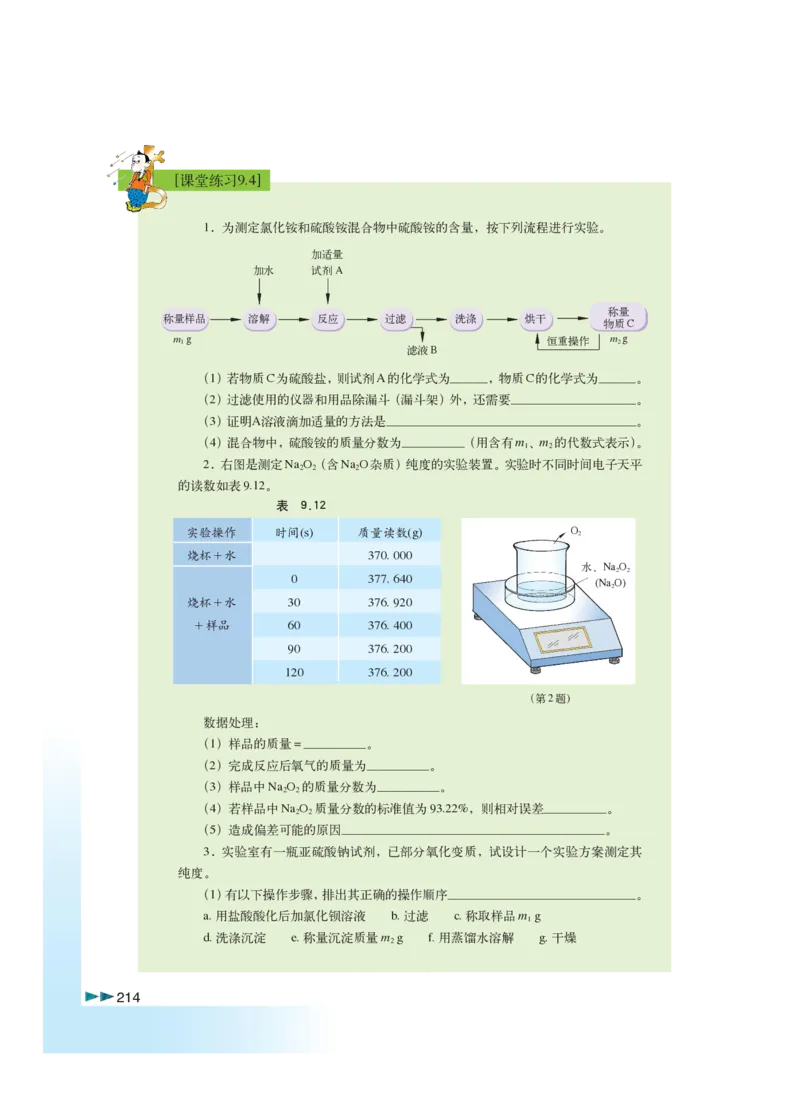
文档内容
高
责任编辑 黄金国 经上海市中小学教材审查委员会 高级中学课本
孙丽伟 级
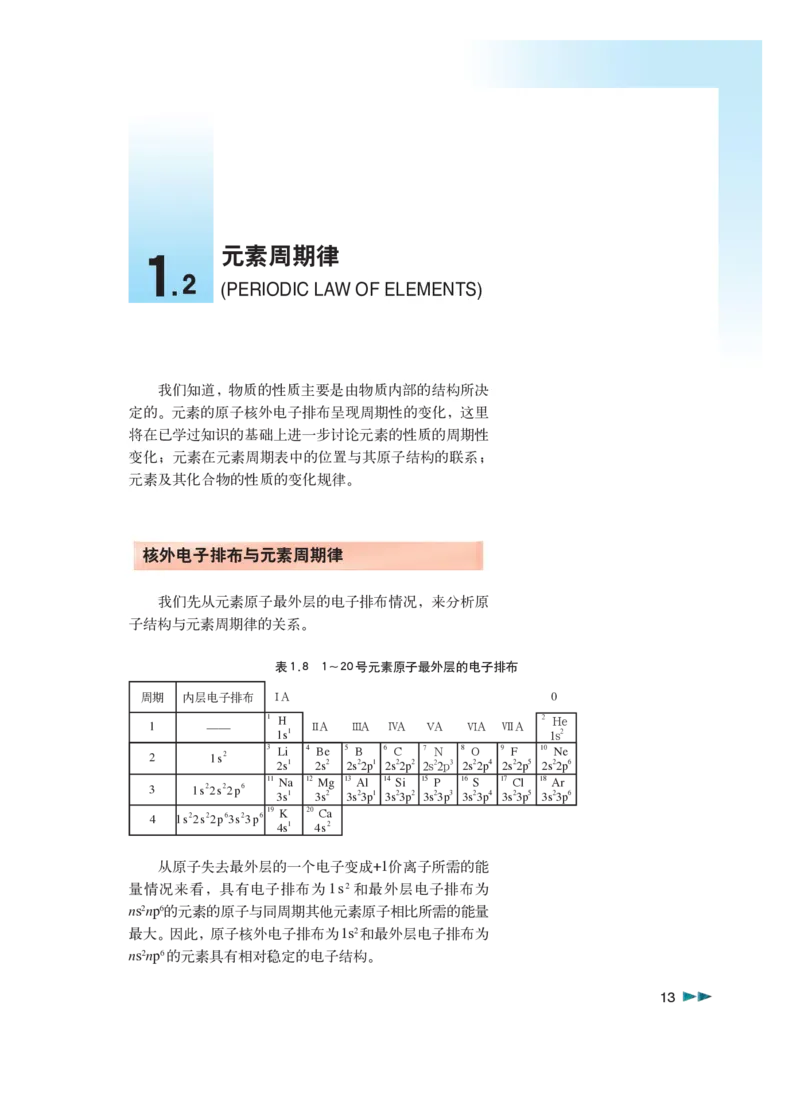
审查准予试用 准用号 Ⅱ -GX-2008009
李玉婷
中
整体设计 陈 蕾
学
课
本
化
学
拓
展
型
课
程
拓 展 型 课 程
(试用本)
)
试
用
本
)
高级中学课本
化 学
拓展型课程
(试用本)
上海市中小学(幼儿园)课程改革委员会
上海世纪出版股份有限公司
出版
上 海 科 学 技 术 出 版 社
(上海钦州南路71号,邮政编码200235)
上海新华书店发行 上海中华印刷厂印刷
开本890×1240 1/16 印张14.75 字数329 000
上
2008年8月第1版 2008年8月第1次印刷
海
ISBN 978-7-5323-9524-8
科
学
定价:16.00元 技
术
出
上海市物价局价格审查批准文号:沪价商专(2008)29号
版
全国物价举报电话:12358
此书如有印、装质量问题,请径向本社调换 社
上海科学技术出版社电话:64089888
上海科学技术出版社高级中学课本
拓 展 型 课 程
(试用本)
上海科学技术出版社目 录
1
原子结构与元素周期律
STRUCTURE OF ATOMS AND
PERIODIC LAW OF ELEMENTS
2◆ 1.1 原子结构
13◆ 1.2 元素周期律
2
化学键和晶体结构
CHEMICAL BOND AND STRUCTURE
OF CRYSTAL
22◆ 2.1 化学键和分子间作用力
37◆ 2.2 晶体
3
化学中的平衡
EQUILIBRIUM IN CHEMISTRY
46◆ 3.1 溶解平衡
51◆ 3.2 化学反应中的平衡
57◆ 3.3 电离平衡
63 ◆ 3.4 水的电离和盐类水解
目录14
离子互换反应和氧化还原反应
IONIC EXCHANGE REACTION AND
REDOX REACTION
70◆ 4.1 离子互换反应
76◆ 4.2 氧化还原反应
5
非金属元素
NONMETALLIC ELEMENTS
88◆ 5.1 非金属单质
94◆ 5.2 一些非金属化合物
104◆ 5.3 化工生产
6
金属元素
METALLIC ELEMENTS
114◆ 6.1 金属及其冶炼
123◆ 6.2 一些金属化合物
目录27
烃
HYDROCARBONS
132◆ 7.1 烃的分类和同系物
137◆ 7.2 烃的命名和同分异构现象
142◆ 7.3 一些重要的烃类和石油化工
8
烃的衍生物
DERIVATIVES OF HYDROCARBONS
154◆ 8.1 卤代烃
161◆ 8.2 醇和酚
170◆ 8.3 醛
175◆ 8.4 羧酸和酯
9
化学实验探究
EXPLORATION OF CHEMICAL
EXPERIMENTS
188◆ 9.1 常见气体的制备和净化
195◆ 9.2 物质的提纯与分离
202◆ 9.3 物质的检验
209◆ 9.4 定量实验
216◆ 9.5 化学实验方法的探究
目录3附录
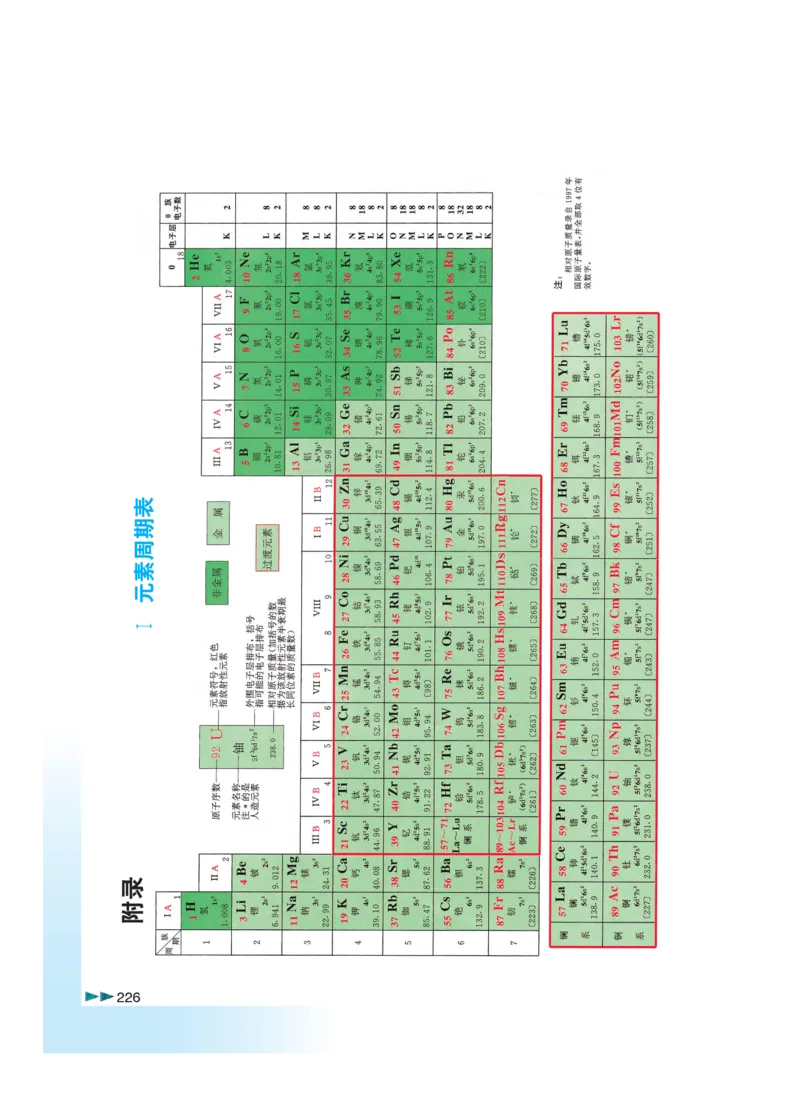
226◆ Ⅰ 元素周期表
227◆ Ⅱ 化学词汇英中文对照表
目录41
原子结构与元素周期律
STRUCTURE OF ATOMS AND PERIODIC LAW OF ELEMENTS
世界是物质的。山川湖海、花草树
木、飞禽走兽,包括我们人类本身,都是
由各种物质组成的。如此丰富多彩、千变
万化、数量庞大的物质,却仅由一百多种
元素的原子通过不同组合和多种结合方
式连接而成的。从揭示原子内部结构的
奥秘出发,可以较清楚地认识原子结构
和各元素性质变化的内在关系。
让我们深入到微小的原子内部,认
识原子的结构,掌握元素性质随原子核
◆ 原子的构成
电荷数变化的周期性规律,从而进一步
◆ 原子核外电子运动状态
认识我们所处的物质世界,掌握物质变
化的规律,有效且适度地利用自然资源, ◆ 原子核外电子排布
使我们的生活更加美好。 ◆ 元素周期律
1
0812896-01-ok Page 1 2011.4.7, 4:09 AM Adobe PageMaker 6.5C/PPC原子结构
1
.1
(ATOMIC STRUCTURE)
原子的构成 同位素
原子是一种很小的微粒,其直径约为 1×10-10m,肉
眼或通过一般的仪器根本无法看见它。
化学史话
科学家“看见”了原子
1982年,宾尼(G. Binnig)和罗雷尔(H. Rohrer)发明扫描隧道显微
镜,并用它观察到了在硅晶体表面的原子图像(图1.1),他们因此荣获1986
年度诺贝尔物理学奖。
图 1.1 扫描隧道显微镜下 图 1.2 我国科学家通过扫描隧道
硅晶体表面的原子图像 显微镜操纵原子刻画的文字
我国科学家于1992年成功地运用自制的扫描隧道显微镜在石墨表面通
过操纵原子刻画出了纳米级的“中国”字样(图1.2)。
2
0812896-01-ok Page 2 2011.4.7, 4:09 AM Adobe PageMaker 6.5C/PPC原子是由位于原子中心的原子核和核外电子构成的。原
子很小,原子核比原子还要小得多,直径只有1×10-15m
左右,体积只占原子体积的千万亿分之一,而它的质量却
几乎等于整个原子的质量。
表 1.1 构成原子的微粒及其相关性质
原子核
构成原子的微粒 电 子
质 子 中 子
1个电子带 1个质子带
电性和电量 不显电性
1个单位负电荷 1个单位正电荷
质量(kg) 9.109 5×10-31 1.672 6×10-27 1.674 8×10-27
相对于1 6 2 C原子 1 **
1 ——— 1.007 2 1.008 6
—的质量* 1 836
12
1
* 12C原子质量为1.992 7×10-26 kg,它的—为1.660 6×10-27 kg。
6 12
** 电子质量与质子质量之比。
原子核主要由带正电荷的质子和不带电荷的中子构成。
每个质子带1个单位正电荷,所以原子核电荷数等于其核内
质子数。
原子作为一个整体不显电性。原子核外电子所带负电
荷的总电量一定和原子核所带正电荷的电量相等。由于每
个电子带一个单位负电荷,所以对原子来说:
原子序数=核电荷数=核内质子数=核外电子数
如果以A代表原子的质量数,Z代表原子核内质子数,
资料库
N代表原子核内中子数,则:
核物理中的一些名称
质量数(A)=质子数(Z)+中子数(N)
在核物理中,把质子
和中子总称为核子。原子
具有相同核电荷数(即质子数)的同一类原子叫做元
核中质子和中子的总数A
素。同种元素原子的核电荷数必然相同,但同种元素原子
称为核子数。质子数和中
的质量数却不一定相同,这是因为同种元素的原子核的质 子数都相同的原子核称为
子数相同,但中子数不同的缘故。 我们把具有相同质子数不 某种核素。
同中子数的原子互称为同位素(isotope)。
3
0812896-01-ok Page 3 2011.4.7, 4:09 AM Adobe PageMaker 6.5C/PPC在自然界中,许多元素都有同位素存在,氢有1H(氕)、
1
2H(氘)、3H(氚)三种同位素,其中2H、3H是制造氢弹的
1 1 1 1
材料。碳元素有12C、13C、14C等几种同位素。铀元素有234U、
6 6 6 92
235U、238U等多种同位素,它们都具有放射性。235U是制造原
92 92 92
子弹的材料和核反应堆的燃料。
同一元素的各种同位素,虽然质量数不同,但它们的
化学性质几乎完全相同。在自然界中同一元素的各种同位
素原子个数的百分数又叫同位素的丰度。人们通过研究发
现,不论元素来自何处或以什么形态存在,同种元素的各
种同位素的丰度一般为一定值。
1
我们知道,国际上采用12C原子质量的—作为相对原
6 12
子质量的基准,如果用这个基准来计算质子和中子的相对
质量,其结果如表1.1所示,它们的近似值都为1。由于原
子的质量近似等于其质子和中子质量之和,所以同位素的
相对原子质量近似地等于其质量数。
同种元素的不同同位素的相对原子质量是不同的。由
于许多元素存在不同的同位素,我们平常说的元素相对原
子质量实际上是该元素各种同位素相对原子质量按其丰度
计算所得的平均值。
例如,氯元素在自然界有35Cl和37Cl两种同位素,它们
17 17
的丰度分别为75.77%和24.23%。两种同位素的相对原子
质量分别为34.969和36.966。那么,氯元素的相对原子质
量为:
34.969×75.77%+36.966×24.23%=35.453
练 习
通常同位素的质量数要比它们的相对原子质量容易得
如果已知某元素有
两种同位素,它们的相 到。如果按该元素的各种同位素的质量数和其丰度计算所
对原子质量分别为A 和 得的平均值,就是该元素的近似相对原子质量。
B,又知它们在自然界的 例如,若按氯元素的两种同位素的质量数和它们的丰
丰度分别为a%和b%。根
度进行计算,氯元素的近似相对原子质量为:
据上述信息,试求出该
元素的相对原子质量。
35×75.77%+37×24.23%=35.485
4
0812896-01-ok Page 4 2011.4.7, 4:09 AM Adobe PageMaker 6.5C/PPC化学史话
居里夫人对放射化学的贡献
玛丽·居里(Marie Sklodowska Curie,1867—1934,
法籍波兰化学、物理学家)是法国科学院第一位女院
士,也是放射化学的奠基人之一。1898年,与其丈夫
皮埃尔·居里在极其艰苦的条件下,依靠科学的推测和
精巧的实验技术,他们先发现了元素钍有放射性,后来
在铀矿物中发现了天然放射性元素钋和镭。为了测得
镭的相对原子质量,她与丈夫一起在简陋的实验室里,
图 1.3 居里夫人
花了45个月时间,从数吨沥青铀矿渣中提炼出了0.1 g
氯化镭,并初步测出镭的相对原子质量为225。
居里夫人在放射化学领域的研究不断取得重大成就。她把一生献给了科
学事业,成为第一位两次获得诺贝尔奖的科学家(1903年物理学奖,1911年
化学奖)。居里夫人一生得到的奖金,包括诺贝尔奖奖金,全部用于科研事业
和资助贫困学生。
原子核外电子运动状态
公路上奔驰的汽车,以及围绕着地球运动的人造卫
星,都可以测定或根据一定的数据计算出它们在某一时刻
所在的位置,并描绘出它们的运动轨迹。这是宏观物体运
动的特征。原子核外电子是一种微观粒子,质量极小(仅 图 1.4 氢原子电子云的剖面
示意图
为9.109 5×10-31 kg),它在原子这样大小的空间(直径
约为0.1 nm)内做高速运动。微观粒子运动的特点是没有
确定的运动轨迹。
科学上应用统计的原理,以每一个电子在原子核外空
间某处出现机会的多少,来描述原子核外电子运动规律。
为直观起见,把电子在原子核外某处出现的机会多少 从氢原子电子云剖
的状况用不同密集程度的小点来表示,就好像电子在原子 面示意图中我们发现,在
离核较近的地方小黑点
核周围形成了云雾,故称电子云。
较密,在离核较远的地方
如图1.4所示是氢原子电子云的剖面示意图。
小黑点较稀。你知道其中
电子云实际上是一种用统计的方法对原子核外电子出
小黑点的疏密所表示的
现机会多少的形象化表示。
意义吗?
在含有多个电子的原子中,不同电子的运动状态是不
5
0812896-01-ok Page 5 2011.4.7, 4:09 AM Adobe PageMaker 6.5C/PPC相同的。我们如何去描述它们的运动状态呢?
(一)电子层
在多电子的原子中,电子具有的能量往往是不同的,它
们的运动区域也不相同。能量低的电子通常在离核较近的
空间范围内运动,能量高的电子通常在离核较远的空间范
围内运动。根据电子的能量差异,以及运动的空间范围离
核远近的不同,核外电子分别处于几个不同的电子层
(electronic shell)。电子层的序数用n表示,通常n值越大,
电子能量越高。
练 习
请在表1.2的括号内填写“高”“低”或“远”“近”。
表 1.2
电子层序数(n) 1 2 3 4 5 6
电子层符号 K L M N O P
电子能量 ( ) ( )
电子离核距离 ( ) ( )
(二)电子亚层
科学研究发现,同一电子层又可分成一个或几个亚层。
电子亚层依次分别用s、p、d、f等符号来表示。第一电子
层只有s亚层,第二电子层有s亚层和p亚层,第三电子层
有s亚层、p亚层和d亚层,第四电子层则有s亚层、p亚层、
d亚层和f亚层。
练 习
请填写表1.3:
表 1.3
电子层序数(n) 1 2 3 4
电子亚层数
电子亚层符号
在多电子原子中,同一电子层中处于不同亚层的电子
能量按s、p、d、f的顺序递增。由此可见,原子核外电子
的能量由所处的电子层和电子亚层共同决定。为了清楚地
6
0812896-01-ok Page 6 2011.4.7, 4:09 AM Adobe PageMaker 6.5C/PPC表示某个电子处于哪个电子层和电子亚层,同时也表示它 练 习
的能量高低,我们将电子层的序数n标在亚层符号的前面。
请将同一原子的2p、
如处于K层的s亚层电子标为1s;处于L层的s亚层和p亚
3d、2s、1s、3 p、4f亚层
层电子,标为2s和2p。我们可以排列出不同亚层中电子能
中的电子按其能量由低
量的高低顺序,例如:E >E >E >E ,E >E >E 。 到高的顺序排列。
4f 4d 4p 4s 4p 3p 2p
不同亚层中电子运动所形成电子云的形状不相同,s亚
层的电子云呈球形,p亚层电子云呈纺锤形。d亚层和f亚
层的电子云形状较复杂,在此不作介绍。 z
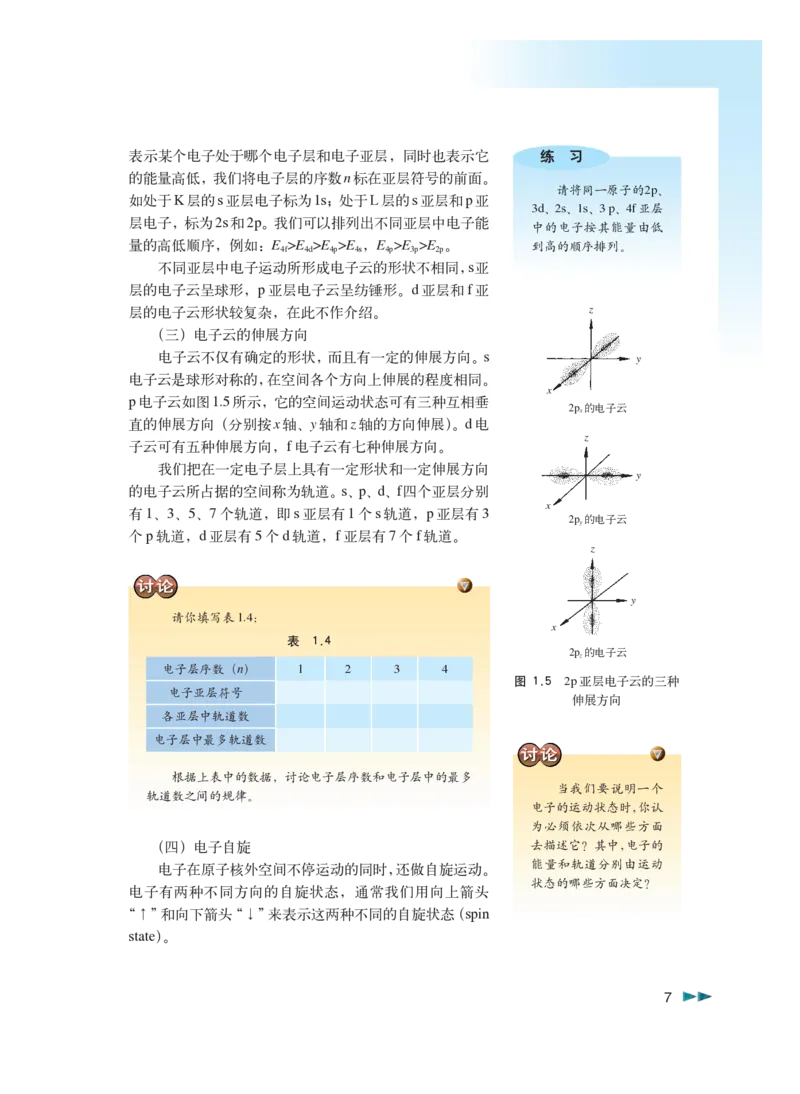
(三)电子云的伸展方向
电子云不仅有确定的形状,而且有一定的伸展方向。s
y
电子云是球形对称的,在空间各个方向上伸展的程度相同。
x
p电子云如图1.5所示,它的空间运动状态可有三种互相垂
2p 的电子云
x
直的伸展方向(分别按x轴、y轴和z轴的方向伸展)。d电
z
子云可有五种伸展方向,f电子云有七种伸展方向。
我们把在一定电子层上具有一定形状和一定伸展方向
y
的电子云所占据的空间称为轨道。s、p、d、f四个亚层分别
x
有1、3、5、7个轨道,即s亚层有1个s轨道,p亚层有3
2p 的电子云
y
个p轨道,d亚层有5个d轨道,f亚层有7个f轨道。
z
y
请你填写表1.4:
x
表 1.4
2p 的电子云
z
电子层序数(n) 1 2 3 4
图 1.5 2p亚层电子云的三种
电子亚层符号
伸展方向
各亚层中轨道数
电子层中最多轨道数
根据上表中的数据,讨论电子层序数和电子层中的最多
当我们要说明一个
轨道数之间的规律。
电子的运动状态时,你认
为必须依次从哪些方面
(四)电子自旋 去描述它?其中,电子的
能量和轨道分别由运动
电子在原子核外空间不停运动的同时,还做自旋运动。
状态的哪些方面决定?
电子有两种不同方向的自旋状态,通常我们用向上箭头
“↑”和向下箭头“↓”来表示这两种不同的自旋状态(spin
state)。
7
0812896-01-ok Page 7 2011.4.7, 4:09 AM Adobe PageMaker 6.5C/PPC核外电子排布式 轨道表示式
科学家在研究原子核外电子排布时发现,在同一轨道
中最多容纳两个自旋方向相反的电子。
在多电子的原子中,处于同一电子层中同一亚层的不
同轨道的电子,其能量是相同的,而处于不同亚层电子的
练 习
能量是不相同的。在第一至第三电子层中,各亚层中轨道
第n电子层中,最多 能量由低到高的顺序为:E H—Br ②酸性:HClO > HBrO
4 4
③热稳定性:HCl > HBr ④酸性:HCl < HBr
(A)②③ (B)①②③ (C)①②④ (D)②③④
6.以下判断中正确的是( )。
(A)原子半径:Al > Na (B)酸性:H SO > H PO
2 4 3 4
(C)热稳定性:NH < PH (D)非金属性:O < S
3 3
7.某元素R原子的质量数为80,已知每个R离子含有45个中子和36个电子。由
这种离子组成的化合物的化学式正确的是( )。
(A) HRO (B) RCI (C) NaR (D) HRO
4
8.某元素A的最高化合价为+a,它的最高价氧化物对应的酸的分子中有b个氧原
子,该酸的分子式是________。
9.A和B是同周期相邻元素,B和C是同主族相邻元素,三种元素的原子序数之
和为28,则A、B、C分别是________、________、________。
10.1~18号元素中有A、B、C、D、E五种元素,A元素是第二周期原子半径最
小的主族元素,B元素的单质能跟冷水剧烈反应产生氢气;C元素原子核外3p电子比
3s电子多3个。D和C为同一周期,其最高价氧化物的水化物的化学式为H DO ,E元
2 3
素的单质是气体,气体密度比氧气小,比氢气大。请回答:
(1)D元素的名称________,最高正价________,最低负价________。
(2)比较A、B、C、D四种元素的原子半径大小________________________。
(3)写出C和B生成的化合物的化学式________________________。
(4)写出E元素的原子电子排布式________________________。
11.阅读下列短文,了解元素周期表的形成过程,并译成中文。
In 1869, Russian chemist Dmitri Mendeleev (1834-1907)and German chemist Lothar
Meyer (1830-1895) published nearly identical schemes for classifying the elements. However,
Mendeleev is usually given more credit than Meyer because Mendeleev published his scheme
first and was more successful at demonstrating its value. Mendeleev wanted to organize the
elements in a way that would help his students learn them more easily. He approached this task
by writing the names of the elements and some of their properties on cards, then arranging the
cards in various ways. Like Newlands, Mendeleev noticed that when he arranged the elements
by increasing atomic mass he could see a periodic repetition of their properties. Mendeleev
eventually produced the first periodic table of the elements. The elements in the same column
have similar properties.
19
0812896-01-ok Page 19 2011.4.7, 4:09 AM Adobe PageMaker 6.5C/PPC小 结
1. 原子结构。
(1) 原子的构成。
质子(Z个)
原子核
中子[(A-Z)个]
原子
(AX)
Z
核外电子(Z个)
(2)核外电子运动状态。
电子层
电子亚层
核外电子运动状态从四个方面描述
电子云伸展方向
电子自旋
(3)原子核外电子排布。
原子核外电子排布遵循的规律:同一轨道中最多容纳两个自旋方向相反的电子;核外电
子排布一般先占有能量最低的轨道,然后依次进入能量较高的轨道;在同一亚层的各个轨道
上,电子排布将尽可能分占不同的轨道,并且自旋方向相同。
2. 元素周期律和元素周期表的要点。
(1)元素的性质随着原子序数的递增而呈周期性变化的规律称为元素周期律,元素周期
表是元素周期律的具体表现形式。
(2)元素的性质随原子序数递增呈周期性变化,本质是元素的原子核外电子随核电荷数
递增呈周期性排布。原子序数=核电荷数。
(3)每个周期的元素,它们的原子核外最外层电子的排布都从ns1开始到ns2np6(或1s2)
结束。周期序数=电子层数。
(4)同一主族,它们的原子的最外层电子数相同,第IA族到第VIIA族分别为ns1到ns2np5。
主族序数=最外层电子数。
(5)同一周期的主族元素中,从左到右元素的原子半径变小,元素的金属性减弱,非金
属性增强。同一主族,从上到下元素的原子半径增大,元素的金属性增强,非金属性减弱。
20
0812896-01-ok Page 20 2011.4.7, 4:09 AM Adobe PageMaker 6.5C/PPC2
化学键和晶体结构
CHEMICAL BOND AND STRUCTURE OF CRYSTAL
我们生活在五光十色的物质世界中,
不同的物质具有不同的性质。物质的各种
性质,不仅跟组成它们的原子的数量、种
类有关,而且与它们的内部结构有关。科
学家通过对物质结构的深入研究,了解和
认识了自然界中的各种物质以及它们之间
的相互关系,并合成出数以千万计的新的
物质分子。至2003 年底,人们发现和合
成的化合物分子已超过了3 000万种。
在本章学习中,我们将初步分析原
子间是通过什么方式构成物质的,构成 ◆ 化学键和分子间作用力
物质的微粒之间存在怎样的相互作用, ◆ 分子结构
从而进一步认识物质的结构,为今后合 ◆ 晶体
成各种各样新的化合物分子,以满足人
们日益增长的多方面的需求打好扎实的
基础。
21
0812896-02-OK Page 21 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC化学键和分子间作用力
2
.1
(CHEMICAL BOND AND INTERMOLECULAR
FORCES)
物质中微粒间相互作用的类型有很多,其中常见的有
离子键、共价键、金属键和分子间作用力等。
离 子 键
金属钠与氟气反应, 在金属钠与氟气的反应过程中,钠原子失去电子形成
生成离子化合物氟化钠, 带一个单位正电荷的钠离子,氟原子得到电子形成带一个
请你用电子排布式分析
单位负电荷的氟离子,当钠离子和氟离子处于某一适当距
反应过程中钠原子与氟
离时,离子间的吸引和排斥作用达到了平衡状态,此时阴、
原子的电子层结构变化
阳离子间就形成了离子键(ionic bond)。
情况。
离子键的本质是阴、阳离子间强烈的静电作用。
在元素周期表中,ⅠA族或ⅡA族的金属与VⅠA、ⅦA族
的非金属之间往往易形成离子键。
微粒之间以离子键结合而形成的化合物是离子化合物。
你认为离子键是不
离子化合物的形成过程可用电子式表示,如氟化钠和氯化
是指阴、阳离子间的静电
钙的形成过程可分别表示为:
引力?哪些元素的微粒
间易形成离子键?
Na + F —→ Na+ [ F ]-
练 习
Ca + 2 Cl —→ [ Cl ]-Ca2+[ Cl ]-
请用电子式表示
CaS和Na O的形成过程。
2
22
0812896-02-OK Page 22 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC资料库
一些离子化合物的熔点
表2.1 一些离子化合物的熔点
在离子化合物中,阴阳离
化合物 熔点(K)
子间存在着较强的离子键,破
NaF 995
坏它需要较高的能量,所以一
CaCl 1 045
2
般离子化合物具有较高的熔
CaS 2 673
点、沸点。
Na O 1 405
2
不同的离子化合物熔点、沸点各不相同,其原因是这些
化合物中离子键的强弱有差异,而这种差异是组成这些化
通过对钠原子与钠
合物的离子结构差异的反映。离子结构的特征主要反映在
离子、硫原子与硫离子的
离子的电荷、离子的电子层结构及离子半径这三个方面。
相互比较,你认为离子所
带电荷的种类和数目跟
(一)离子的电荷 什么有关?
离子的电荷(电性和数值)是离子的重要性质之一。
(二)离子的电子层结构
练 习
主族元素离子的核外电子排布一般都达到最外层是8
电子或2电子(最外层是第一层时)结构,这种电子层结构 试写出并比较Li+、
Be2+、F-、Mg2+、Al3+、S2-、
是比较稳定的。
Cl-核外电子排布式。你
过渡元素离子的核外电子排布比较复杂,如Fe2+ 为
认为它们跟哪一类元素
1s22s22p63s23p63d6,最外层共有14个电子,与稀有气体原子
原子的核外电子层结构
的核外电子排布不相同。 相同?
(三)离子的半径
下列两组数据分别列出的是一些元素的原子与对应阳
离子或阴离子半径数据。
表 2.2
元 素 Li Na K Rb Cs
原子半径(nm) 0.152 0.186 0.231 0.244 0.262 请分析表2.2 两组
数据。你认为对于同种
阳离子半径(nm) 0.068 0.097 0.133 0.147 0.160
元素而言,原子半径与
元 素 F Cl Br I
对应的阳离子或阴离子
原子半径(nm) 0.064 0.099 0.115 0.133 半径之间有怎样的大小
阴离子半径(nm) 0.133 0.181 0.196 0.220 关系?
23
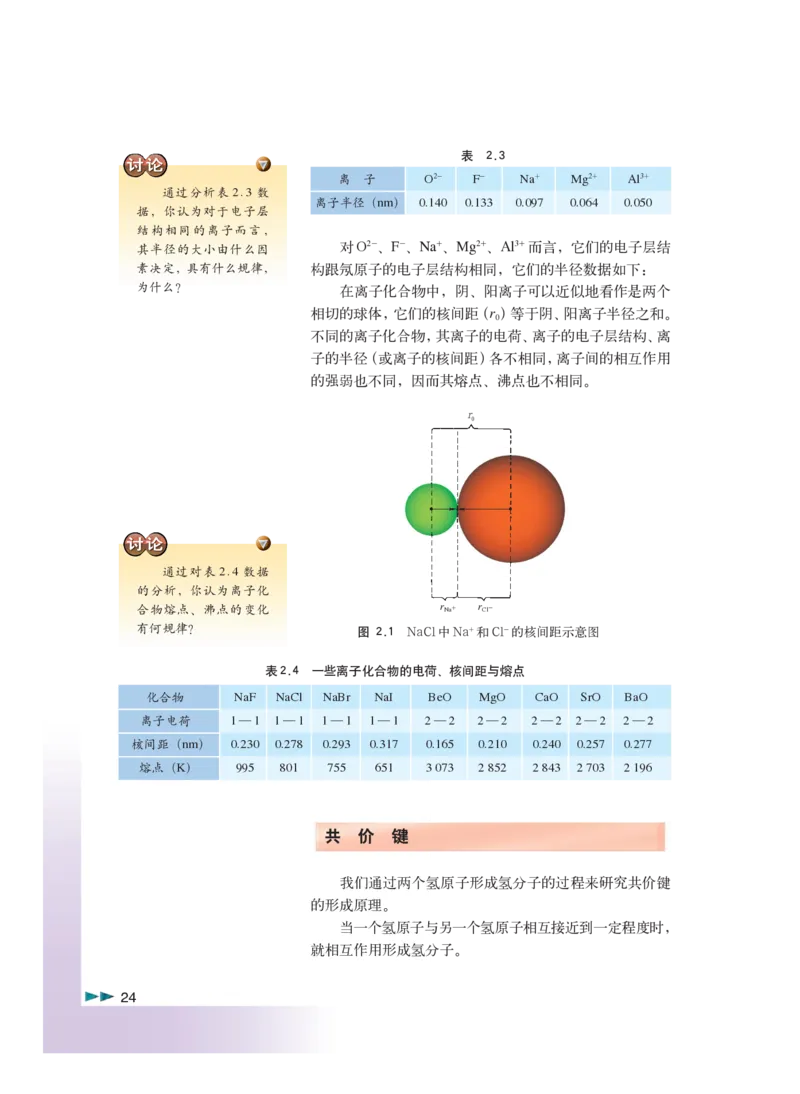
0812896-02-OK Page 23 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC表 2.3
离 子 O2- F- Na+ Mg2+ Al3+
通过分析表2.3 数
离子半径(nm) 0.140 0.133 0.097 0.064 0.050
据,你认为对于电子层
结构相同的离子而言,
其半径的大小由什么因 对O2-、F-、Na+、Mg2+、Al3+而言,它们的电子层结
素决定,具有什么规律, 构跟氖原子的电子层结构相同,它们的半径数据如下:
为什么? 在离子化合物中,阴、阳离子可以近似地看作是两个
相切的球体,它们的核间距(r )等于阴、阳离子半径之和。
0
不同的离子化合物,其离子的电荷、离子的电子层结构、离
子的半径(或离子的核间距)各不相同,离子间的相互作用
的强弱也不同,因而其熔点、沸点也不相同。
r
0
通过对表2.4 数据
的分析,你认为离子化
合物熔点、沸点的变化 r Na+ r Cl-
有何规律?
图 2.1 NaCl中Na+和Cl-的核间距示意图
表2.4 一些离子化合物的电荷、核间距与熔点
化合物 NaF NaCl NaBr NaI BeO MgO CaO SrO BaO
离子电荷 1—1 1—1 1—1 1—1 2—2 2—2 2—2 2—2 2—2
核间距(nm) 0.230 0.278 0.293 0.317 0.165 0.210 0.240 0.257 0.277
熔点(K) 995 801 755 651 3 073 2 852 2 843 2 703 2 196
共 价 键
我们通过两个氢原子形成氢分子的过程来研究共价键
的形成原理。
当一个氢原子与另一个氢原子相互接近到一定程度时,
就相互作用形成氢分子。
24
0812896-02-OK Page 24 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPCH+H—→H
2
在两个氢原子形成氢分子的过程中,电子没有发生转
移,而是两个氢原子通过共用电子对结合形成共价键,其
形成过程可用电子式表示:
1s
H
H·+·H—→H∶H
1s
在化学上,常用一根短线表示一对共用电子,所以氢
H
分子的结构式可表示为H—H。
当两个电子自旋状态不同的氢原子相互接近时,它们
共享电子对,两核间的电子云变得密集,从而对两核同时 图 2.2 用轨道表示式表示
产生吸引作用,使两个氢原子形成稳定的氢分子。 氢分子中的共用电子对
图 2.3 氢原子形成共价键示意图
由上述分析,可以认为原子间通过共用电子对所形成
练 习
的化学键是共价键(covalent bond)。
形成氮分子的每个氮原子提供出了3个2p电子,形成 试用电子式和结构
3对共用电子(图2.4),所以氮原子间形成的是叁键,其 式表示氯气、氯化氢、硫
化氢、氨分子的结构。
电子式和结构式可依次表示为 N N 、N≡N。
1s 2s 2p
N ↑↓ ↑↓ ↑↑↑
1s 2s 2p
N ↑↓ ↑↓ ↓↓↓
图 2.4 用轨道表示式表示氮分子中的共用电子对
在不同的非金属元素原子间,也可以通过共价键形成
化合物分子。
25
0812896-02-OK Page 25 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC资料库
配 位 键
如果将氨气通入盐酸中,其反应的实质可用离子方程式表示:
NH +H+—→NH +
3 4
上述反应原理是怎样的呢?
H
氨分子的电子式是H N ,氮原子最外层上有一对未跟其他原子共用的电
H
子对(孤对电子)。当氨分子跟氢离子作用时,氨分子上的孤对电子进入氢离子
的空轨道,形成共用电子对。铵离子的形成过程可用电子式表示:
H H
[ ]+
H N +H+—→ H N H
H H
这种由一个成键原子单方面提供共用电子对形成的共价键称为配位键
(coordination bond)。配位键可以用A→B来表示,其中A是提供孤对电子的原
子(如NH 分子中的N原子),B是具有空轨道的原子(如H+)。
3
在NH + 中,虽然有一个氮氢键与其他三个氮氢键的形成过程不同,但四个
4
H
+
键的性质却完全相同。所以NH + 结构式既可用 H —N→H 表示,又可用
4
+
H—N—H 表示。
同种元素原子间形成的共用电子对,由于受到两原子
作用的强弱相同,故不偏向任何一方,电子云在两原子间
的分布是均匀的,因而成键原子不显电性。我们把这样的
共价键叫做非极性共价键(简称非极性键)。一般单质分子
内的共价键是非极性键,如氢分子中的氢氢键、氮分子中
在H H和H Cl 分 的氮氮键(N≡N)等。
子中,原子间都是通过共
不同元素原子间形成的共用电子对,受到两原子作用
价键(共用电子对)结合
的强弱不同,故会偏向吸引电子能力较强的一方,使吸引
在一起的,试比较分子中
电子能力较强的一方电子云比较密集,该原子就带部分负
共用电子对受到两个成
键原子作用的相对强弱。 电荷,如HCl分子中的Cl原子;吸引电子能力较弱的原
26
H
[ ]
H
[ ]
H
0812896-02-OK Page 26 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC子带部分正电荷,如HCl分子中的H原子。我们把这样
的共价键叫做极性共价键(简称极性键)。化合物分子内
存在极性键,如氟化氢分子中的氢氟键,水分子中的氢
氧键均为极性键。
资料库
元素的电负性
我们知道,不同元素原子间形成的共价键因共用电子对的偏移而具有极性。
共用电子对偏移程度的大小取决于两个成键原子吸引电子能力的相对强弱。这种
成键原子吸引电子能力的相对强弱,我们用元素的电负性(electronegativity)来
度量。元素的电负性越大,表示该元素的原子吸引电子的能力越强。
根据元素的电负性,可以判断元素的金属性或非金属性的强弱。电负性大的
元素(如F的电负性为4.0),其非金属性较强,易形成阴离子;反之,电负性小
的元素(如Na的电负性为0.9),其金属性较强,容易形成阳离子。
在共价化合物中,可根据两种成键原子对应元素电负性差值的大小,判断共
价键的极性强弱。元素的电负性差值越大,原子间形成键的极性越强。
在习惯上,人们还利用元素的电负性差值近似地判断化学键的类型。一般来
说,当电负性差值大于1.7时,形成的化学键为离子键;当电负性差值小于1.7
时,形成的化学键为共价键。
表 2.5
元 素 Li Be B C N O F
电负性 1.0 1.5 2.0 2.5 3.0 3.5 4.0
元 素 Na Mg Al Si P S Cl
电负性 0.9 1.2 1.5 1.8 2.1 2.5 3.0
我们通常通过共价键的键长、键能、键角来研究共价
键的性质。
(一)键长
在分子中,两个成键原子的核间距叫做键长(bond
length)。例如氢氢键长为0.074 nm,氯氯键长为0.199 nm。
27
0812896-02-OK Page 27 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC表2.6 某些共价键的键长
根据表2.6 中有关
共价键 C—C C==C C≡C C—O C==O
数据,你能推断出影响共
键长(nm) 0.154 0.134 0.120 0.143 0.122
价键键长的因素主要有
哪些吗?其影响的结果 共价键 N—N N==N N≡N
怎样? 键长(nm) 0.146 0.120 0.110
(二)键能
我们知道,氢元素单质的稳定存在形式是氢分子,一般
的加热温度不能使其分解为氢原子,即使温度达到2 000℃
时,分解的氢分子仍不到总数的1%,这说明氢分子分解需
要吸收大量的能量:
键能的大小与键的
牢固程度、分子稳定性之
间有何关系? H —→H+H-436 kJ
2
由上式可知,1 mol气态氢分子分解成2 mol气态氢原
子需要吸收436 kJ能量。这一事实说明,H 分子能量比孤
2
立的H原子能量低得多,所以H 分子比H原子稳定。另外,
2
用化学键的观点来看,1 mol H 分子分解时吸收的436 kJ
2
请根据原子结构及
能量,是用于拆开1 mol氢氢键的。这个能量值就是氢氢键
共价键的有关理论,解释
的键能(bond energy),单位为kJ/mol。
下列事实:
表2.7列出了某些共价键的键能由于键长及键的类型
(1)H O比H S稳定。
2 2
(2)N 比Cl 稳定。 的不同而发生变化的情况。
2 2
表2.7 某些共价键的键长、键能数据
共价键 H—F H—Cl H—Br H—I Cl—Cl Br—Br I—I C—C C=C C—O C=O N≡N
键长(nm) 0.092 0.127 0.141 0.161 0.199 0.228 0.267 0.154 0.134 0.143 0.122 0.110
键能(kJ/mol) 569 432 368 297 243 193 151 347 612 358 805 945
通过对表2.7中有关数据的分析比较,你可以推断出影
响同类分子中共价键键能大小的规律吗?
28
0812896-02-OK Page 28 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC(三)键角
通过研究硫化氢分子的结构,发现其中两个硫氢键
的夹角为92°。在多原子分子中,键与键之间都有一定
的夹角,如甲烷分子中任意两个碳氢键之间的夹角均为
109°28′。我们把这种分子中键和键之间的夹角叫做键角
(bond angle)。
109°28′
92°
图 2.5 H S和CH 分子模型图
2 4
资料库
共价键的饱和性与方向性
1. 饱和性
我们知道,一个氧原子中的两个未成对电子跟两个氢原子中各一个未成对电
子形成两对共用电子对后,便形成了稳定的水分子。其中的氧原子便不能再跟第
三个氢原子形成共用电子对,故不存在H O分子。由于同样的原因,一个氮原子
3
跟氢原子结合生成NH 分子,而不生成NH 、NH 分子,上述事实说明原子在
3 4 5
形成共价键时,结合原子的数目不是任意的,每个原子都有一个最大的成键数。
这就是共价键的饱和性。
2. 方向性
分子中共价键与共价键之间有一定的键角,如硫化氢分子中两个硫氢键的键
角为92°,甲烷分子中任意两个碳氢键的键角为109°28′。共价键的键角是因
为共价键具有方向性引起的。
我们知道,除了s轨道的电子云是球形对称的以外,其他轨道(如p轨道)
的电子云都有一定的伸展方向。
x y
共价键通过共用电子对形成,核间的原子轨道重
叠越大,形成的共价键就越强。因此,共价键总是尽
可能沿着原子轨道重叠最大的方向形成,这是共价键
具有方向性的原因。例如,在硫原子跟氢原子结合生
成H S 分子时,由于硫原子最外层两个未成对电子处
2
于互成直角的两个3p轨道中,两个氢原子的1s轨道
图 2.6 硫原子与氢原子
沿着互为直角的方向分别跟3p轨道重叠,这样形成的
轨道重叠示意图
两个硫氢键的夹角就接近90°。
29
0812896-02-OK Page 29 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC极性分子和非极性分子
课堂实验
静电对不同液流方向的影响
如图2.7所示,在两支滴定管
中分别注入20 mL 蒸馏水和四氯 H 2 O CCl 4
化碳,将它们夹在滴定管夹上。滴
定管下端放置一只大烧杯,分别打
开活塞,让液体慢慢下流成线状。 玻璃棒 玻璃棒
将摩擦带电的玻璃棒或塑料棒接近
液流,观察液流的方向有无变化。 图 2.7 带电玻璃棒靠近液流实验
为什么在带电物体的作用下,水和四氯化碳液流的方
向会不同?这是由水和四氯化碳分子的极性不同引起的。
我们以氯分子和氯化氢分子为例来说明分子的极性情
况。在Cl 分子中,其共价键是非极性键,共用电子对不偏
2
向任何一个原子,所以分子不显示极性,我们把这样的分
子叫做非极性分子(non-polar molecule);在HCl分子中,
氯原子和氢原子形成的是极性共价键,由于氯原子的非金
属性比氢原子强,对电子的吸引能力大,因此共用电子对
偏向氯原子,分子中氯原子一端带部分负电荷,氢原子一
端带部分正电荷,氯化氢分子呈现极性,我们把这样的分
子叫做极性分子(polar molecule)。
氢原子 氧原子
水分子是一种折线型分子,两个氢氧键之间的夹角为
图 2.8 水分子结构示意图
104.5°。氢氧键是极性键,共用电子对偏向氧原子,氧原
子带部分负电荷,氢原子带部分正电荷,从而在整个水分
子中,靠近氧原子一端带负电荷,靠近两个氢原子的一端
带正电荷,正负电荷重心不重合,结果使水分子呈极性。
四氯化碳分子是一种正四面体型分子,碳原子位于正
四面体中心,四个氯原子位于正四面体的四个顶角(四个
C原子 Cl原子 碳氯键中任意两个键之间的夹角均为109°28′),对称地排
图 2.9 四氯化碳分子空间 列在碳原子周围,正负电荷的重心是重合的,所以四氯化
结构示意图 碳分子是非极性分子。
30
0812896-02-OK Page 30 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC对于二氧化碳分子而言,两个碳氧键键角为 180°
(O=C=O),是一种直线型分子,其分子内正负电荷的
重心也是重合的,所以二氧化碳分子也是非极性分子。
人们在实践中发现,Br、I 等溶质易溶于四氯化碳、苯(非极性
2 2
分子)等溶剂,而在水中则难溶或溶解度较小;HCl、NH(极性分子)
3
极易溶于水而难溶于四氯化碳、苯等溶剂。根据以上事实,试从分子
的极性角度归纳出物质溶解性的规律。
资料库
多原子分子的空间构型与分子的极性
由极性键形成的多原子分子,可能是极性分子,也可能是非极性分子,这取
决于分子中各键的空间取向。如果各个极性键由于在空间取向上,正负电荷的重
心重合,则分子是非极性分子;反之,是极性分子。
表2.8 一些多原子分子的空间构型与分子的极性
分子类型 空间构型 分子极性 实 例
ABA 直线形 非极性 CO 、CS
2 2
三原子分子 ABA 折线形 极性 H O 、H S 、SO
2 2 2
ABC 直线形 极性 HCN
AB 平面正三角形 非极性 BF 、BCl
3 3 3
四原子分子
AB 三角锥形 极性 NH 、PH
3 3 3
AB 正四面体形 非极性 CH 、CCl
4 4 4
五原子分子 ABC 四面体形 极性 CHCl 、CH Cl 、
x y 3 2 2
(x+y=4) CH Cl
3
(a) BF 3 (b) NH 3
(c) CH 3 Cl (d) CH 2 Cl 2 (e) CHCl 3
图 2.10 几种分子的空间结构示意图
31
0812896-02-OK Page 31 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC分子间作用力
我们知道,干冰具有升华的性质,它在升华过程中会
吸收大量的热。
CO(s)—→CO(g)-23.2kJ
2 2
图 2.11 飞机播撒干冰实施人工降雨
干冰吸收能量升华时,二氧化碳分子本身的结构没有
发生任何改变,只是二氧化碳分子间的距离增大了。在干
冰中,二氧化碳分子间存在着某种作用力,它升华时吸收
的能量用于克服这种作用力。我们把这种作用力称作分子
间作用力,也称范德华力(van der Waals force)。
范德华力不仅存在于二氧化碳分子间,在其他物质的
资料库 分子间也存在这种作用力。范德华力比化学键弱得多,通
常化学键的键能是几百千焦每摩,而范德华力通常只有几
范德华力
到几十千焦每摩。例如氯化氢分子中氢氯键键能为
范德华(J.D.van der 432 kJ/mol。而氯化氢分子间的范德华力只有20 kJ/mol。所
Waals,1837—1923),荷 以,破坏范德华力要比破坏化学键容易得多。范德华力越
兰物理学家。他首先研究 大,使物质熔化或汽化时克服分子间作用力需要吸收的能量
了分子间的作用,这种作 越大,该物质的熔点、沸点也就越高。但是,由于范德华力
用力就用他的名字命名,
只存在于分子间,它的大小,对物质的化学性质没有影响。
叫做范德华力。
影响范德华力的因素很多。从表2.9可以看出,对于分
子组成和结构相似的物质来说,范德华力一般随着相对分
子质量的增大而增强,表现为沸点的升高。
表2.9 一些物质的相对分子质量与其沸点的关系
物 质 F Cl Br I Ne Ar Kr Xe CH SiH GeH SnH
2 2 2 2 4 4 4 4
相对分子质量 38 71 160 253.8 20 40 83.8 131.3 16 32 76.6 122
沸点(K) 86 239 332 457 26.9 87.1 119.6 164.9 110 161 185 221
32
0812896-02-OK Page 32 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC资料库
水的密度变化与氢键
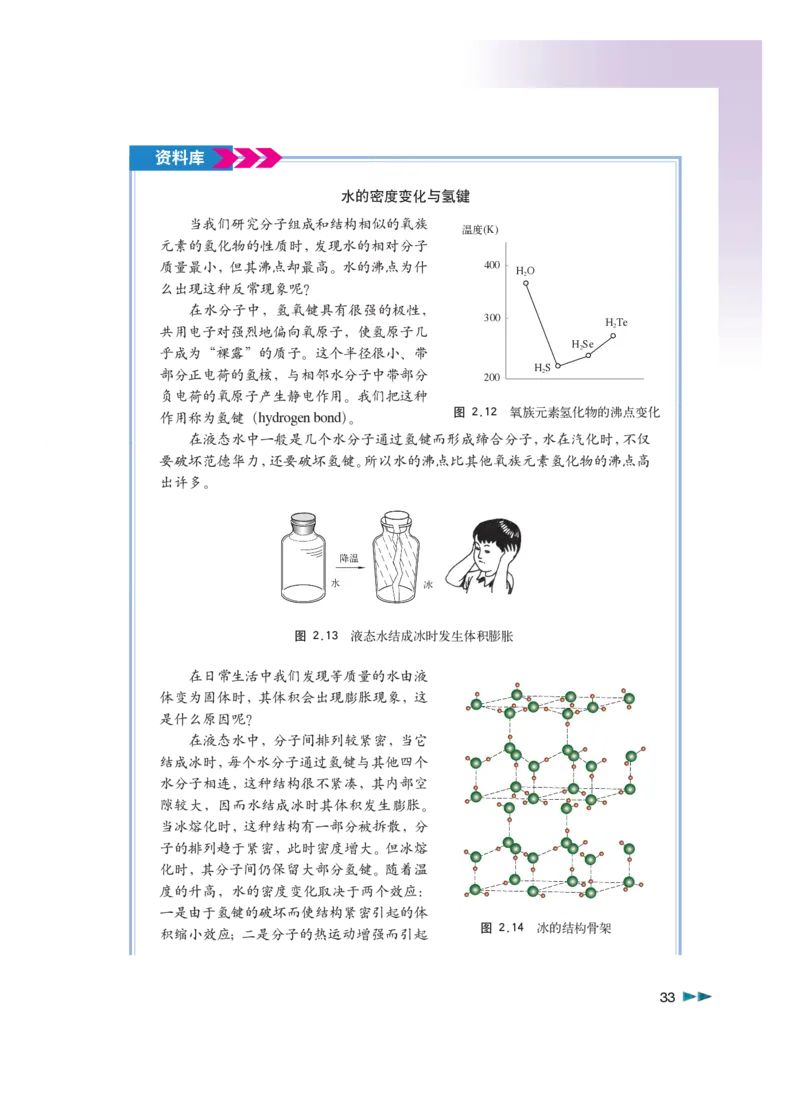
当我们研究分子组成和结构相似的氧族
温度(K)
元素的氢化物的性质时,发现水的相对分子
质量最小,但其沸点却最高。水的沸点为什 400
HO
2
么出现这种反常现象呢?
在水分子中,氢氧键具有很强的极性,
300
HTe
共用电子对强烈地偏向氧原子,使氢原子几 2
HSe
乎成为“裸露”的质子。这个半径很小、带 2
HS
部分正电荷的氢核,与相邻水分子中带部分 2
200
负电荷的氧原子产生静电作用。我们把这种
图 2.12 氧族元素氢化物的沸点变化
作用称为氢键(hydrogen bond)。
在液态水中一般是几个水分子通过氢键而形成缔合分子,水在汽化时,不仅
要破坏范德华力,还要破坏氢键。所以水的沸点比其他氧族元素氢化物的沸点高
出许多。
降温
水 冰
图 2.13 液态水结成冰时发生体积膨胀
在日常生活中我们发现等质量的水由液
体变为固体时,其体积会出现膨胀现象,这
是什么原因呢?
在液态水中,分子间排列较紧密,当它
结成冰时,每个水分子通过氢键与其他四个
水分子相连,这种结构很不紧凑,其内部空
隙较大,因而水结成冰时其体积发生膨胀。
当冰熔化时,这种结构有一部分被拆散,分
子的排列趋于紧密,此时密度增大。但冰熔
化时,其分子间仍保留大部分氢键。随着温
度的升高,水的密度变化取决于两个效应:
一是由于氢键的破坏而使结构紧密引起的体
图 2.14 冰的结构骨架
积缩小效应;二是分子的热运动增强而引起
33
0812896-02-OK Page 33 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC的体积增大效应。从273K到277K,前一个效应占主导地位,此范围内温度升
高,水的体积减小,密度增大;277K以上,当温度升高时,后一个效应占主导
地位,水的体积和密度变化跟前者相反。所以277K时,水的密度最大。
图 2.15 漂浮在海面上的冰山
金 属 键
在人类已经发现的一百多种元素中,金属约占80%,它
们有许多共同的性质,如不透明、有金属光泽、有良好的导
电性、导热性和延展性等等。
表2.10 一些元素单质的物理性质
元素 密度(g/cm3) 热导率[W/(m·K)] 电导率(×108 S/m)
Al 2.70 238 0.38
Fe 7.86 82 0.10
Cu 8.92 400 0.59
S 2.07 0.029 1×10-23
金属的共同性质是由其晶体的内部结构决定的。通过
X射线的研究表明,金属晶体中的金属原子像硬球一样,
一层一层很紧密地堆积在一起形成了晶体(图2.16为几种
类型晶体的结构示意图)。铝晶体中铝原子的堆积形式如
图2.16(c)所示,每一个铝原子为较多铝原子所围绕。
金属原子的价电子较少,这些价电子受到核的作用较
弱,在一定条件下金属原子往往释放出价电子而形成金属阳
34
0812896-02-OK Page 34 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC离子。可以认为,金属晶体是由金属阳离子按一定规律紧密
堆积,而释放出的价电子分布在整个晶体里自由地运动着,
你能从晶体结构的
这些电子不为某个特定原子所拥有,我们将其称作为自由电
角度解释金属铝具有导
子。有人形象地将这样的结构形容为“释去了价电子的金属
电性、导热性和延展性的
离子沉浸在自由电子的海洋里”(图2.17)。 原因吗?
金属离子间跟自由电子存在着较强的作用,使许多金
属离子相互结合在一起。像这种金属离子间通过自由电子
产生的较强的相互作用称为金属键(metallic bond)。通过
金属键形成的晶体是金属晶体。
(a) (b) (c)
图 2.16 三种类型金属晶体的结构示意图 图 2.17 金属晶体内部结构示意图
[课堂练习2.1]
1. 下列分子结构中,各原子的最外层电子都满足8电子稳定结构的是( )。
(A)SF (B)XeF (C)CS (D)CH
6 2 2 4
2. BF 分子的4个原子在同一平面上,它是一个非极性分子,下列推断中,不正确
3
的是( )。
(A)两个硼氟键之间的键角为60°
(B)硼氟键为极性键
(C)三个硼氟键的键能是相同的
(D)三个硼氟键的键长是相等的
3. 下列现象中,能用键能大小解释的是( )。
(A)氮气的化学性质比氧气稳定
(B)常温常压下,溴呈液态,碘呈固态
(C)稀有气体一般很难发生化学反应
(D)硝酸易挥发,而硫酸难挥发
35
0812896-02-OK Page 35 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC4. 从实验测得不同物质中氧氧键的键长和键能数据如表2.11:
表 2.11
氧氧键类型 O2- O- O O+
2 2 2 2
键长(×10-12 m) 149 128 121 112
键能(kJ/mol) X Y Z = 494 W = 628
其中X、Y的键能数据未测定,但可根据规律推导键能的大小顺序为W>Z>Y>X,
该规律是( )。
(A)成键时电子数越多,键能越大
(B)键长越长,键能越小
(C)微粒带电荷越多,键能越大
(D)成键时电子对越偏移,键能越大
5. 在下列物质中:
(A)氨气 (B)氯化钡 (C)氯化铵 (D)干冰 (E)苛性钠 (F)食盐
(G)冰 (H)氦气 (I)双氧水 (J)氢气 (K)铝
(1)只有非极性键的是______。
(2)只有离子键的是______。
(3)只有极性键的是______;其中又是非极性分子的是______。
(4)既有极性键又有非极性键的是______ 。
(5)既有离子键又有极性键的是______。
(6)无任何化学键的是______。
(7)上述物质中存在范德华力的是______,存在金属键的是______
______。
6. 阅读下列短文,理解离子化合物的一些性质:
Many familiar substances are ionic compounds. An example is common salt (chloride).
Sodium chloride and many other ionic compounds are present in sea-water. Crystals of salt are
readily obtained by the partial evaporation of sea-water in a salt pan.
We need to understand the bonding in compounds in order to explain their structure and
physical properties. Ionic compounds:
* are crystalline solids with high melting points;
* conduct electricity, with decomposition at the electrodes, in aqueous solution or when
they are molten;
* are hard and brittle with crystals that cleave easily; are often soluble in water.
36
0812896-02-OK Page 36 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC晶体
2
.2
(CRYSTAL)
晶体是指具有规则的几何外形的固体,它们具有固定
的熔点。
晶体的类型
根据构成晶体的结构微粒及微粒间作用类型的不同,
晶体可分成离子晶体、分子晶体、原子晶体和金属晶体等
类型。 练 习
试描述氯化钠晶体
(一)离子晶体
的结构特点。
你认为氯化钠晶体
能导电吗?要使食盐
图 2.18 氯化钠晶体实物及结构模型
导电需要什么条件,为
什么?
在氯化钠晶体中,每个Na+周围有6个Cl-,而每个Cl-
周围也有6个Na+,它们之间通过离子键的作用结合,并在
空间有规律地排列,形成规则的几何形状。由离子形成的
晶体是离子晶体(ionic crystal)。离子晶体由阴阳离子构成,
不存在单个的分子,所以其化学式严格地说是表示晶体中
阴、阳离子的个数比,而不是表示分子组成的分子式。
37
0812896-02-OK Page 37 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC在离子晶体中,由于阴、阳离子间存在较强的离子键,
所以离子晶体的结构一般比较稳定,密度较大,且具有较
高的熔点、沸点和硬度。如氯化钠的熔点为1 074K,沸点
为1 686K。
(二)分子晶体
分子晶体(molecular crystal)的基本结构微粒是分子,
如干冰是一种典型的分子晶体,其基本结构微粒是CO 分
2
子,CO 分子间通过范德华力相互结合。
2
形成分子晶体的物质类别较多,所有稀有气体元素单
质、大多数非金属单质和大多数共价化合物形成的晶体都
是分子晶体,如Xe、S、P(白磷)、I 、H O、H PO 、CH COOH、
4 2 2 3 4 3
C H(萘)等。
10 8
由于范德华力很弱,所以分子晶体的熔点较低,硬度
较小。如Xe的熔点为161.2K。
请说出你所认识的
干冰的晶体有哪些结构
特点。
图 2.19 干冰的晶体结构模型 图 2.20 美丽的雪花晶体
(三)原子晶体
在原子晶体(atomic crystal)中,我们常以金刚石作为
研究对象来说明原子晶体的结构特点。在金刚石晶体中,每
个碳原子以共价键跟另外4个碳原子结合,键长为0.155nm。
同一碳原子形成的4个共价键中,任意两个键之间的键角为
109°28′,5个碳原子形成一个正四面体结构。金刚石中每
个碳原子位于正四面体的中心,跟它成键的4个碳原子位于
正四面体的顶点,这种正四面体向空间方向发展,构成一
种坚实的、彼此连接的空间网状结构。
原子晶体由原子构成,原子间以强烈的共价键结合,
38
0812896-02-OK Page 38 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC因而其熔点、沸点很高,硬度很大。如金刚石的熔点高达
3 823K,沸点为5 100K,金刚石还是自然界中最硬的物质。
你能说出金刚石晶
体与氯化钠晶体、二氧化
碳晶体在熔点、硬度上有
什么差别吗?说明造成
这种差别的原因。
图 2.21 我国最大的天然金刚 图 2.22 金刚石晶体结构模型
石晶体——常林钻石
常见的原子晶体有金刚石、硅晶体、二氧化硅晶体和
碳化硅(SiC)晶体等。它们被广泛应用于光学研究、地质
勘探、石油钻井及各种加工工具的制造。
图 2.23 镶有金刚石的钻头及石油钻井平台
(四)金属晶体
金属晶体(metallic crystal)由金属离子和自由电子构
成,金属离子间通过自由电子的作用相互结合在一起,自
图 2.24 河南安阳出土的
由电子可以在整个晶体里作自由移动。由于金属晶体的这 商代青铜器——司母戊鼎
一结构特点,金属具有一些特殊的物理性质,如导电性、导
热性、延展性等。
此外,金属晶体还具有金属光泽。当可见光照射到金
属晶体的表面时,晶体中的自由电子可以吸收光能而呈能
量较高状态。这种状态不稳定,电子又可以将吸收的各种
波长的光,大部分辐射出来,回到能量较低的状态,这是金
图 2.25 切割金属钠
属晶体具有金属光泽的原因。
39
0812896-02-OK Page 39 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC资料库 由于不同金属晶体中,金属键的强弱差异非常显著,
因而其熔点和硬度的差异很大。如汞的熔点低于室温
金的延展性
(234.1K),而钨的熔点却高达 (3 688±20)K。
金的延展性特别好,
很容易被拉成线密度为
5×10-4 g/m的金丝或打
成厚度为1×10-8 m的半 试对分子晶体、离子晶体、原子晶体和金属晶体的结构和物理
透明的金箔。 性质进行归纳比较,并填写表2.12:
表 2.12
晶体类型 分子晶体离子晶体原子晶体 金属晶体
基本结构微粒
微粒间作用
你能列举出一些金
熔 点
属在工农业生产、国防、 物理性质
硬 度
科学技术及生活中实际 特点
导电性
应用的例子吗?
典型物质
几种晶体的空间构型
(一)硅晶体
硅晶体(silicon crystal)跟金刚石具有相似的晶体结
构,也是一种原子晶体,1个硅原子与4个硅原子以共价键
结合,5个硅原子形成正四面体结构。这个正四面体向空间
方向发展,形成空间网状晶体。硅晶体中硅硅键的键长为
0.234 nm,比金刚石中碳碳键的键长长。
由于硅晶体跟金刚石的晶体结构相似,因而它们具有
图2.26 硅晶体
相似的物理性质,晶体硅具有很高的熔点(1 683K),晶体
硬而脆。
硅晶体是一种优良的半导体材料,它在现代高科技领
已知碳化硅的晶体
域有着十分广泛的用途,如超大规模集成电路等。
结构跟金刚石和硅晶体
相似,其中碳原子和硅原
(二)石墨
子交替排列。试根据碳化
硅晶体的这一结构特点, 石墨晶体(graphite crystal)呈层状结构。每一层内,每
推断碳化硅、金刚石、硅 个碳原子跟3个碳原子以共价键相结合,碳原子之间排列成
晶体三者熔点由低到高
六边形,一个个六边形排列成平面网状结构。在层与层之
的顺序。
间,相邻碳原子以范德华力结合。
40
0812896-02-OK Page 40 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC石墨是一种灰黑色不透明晶体,有金属光泽,非常难
熔,质软有润滑性。由于石墨中每个碳原子只有3个价电子
形成共价键,还有1个价电子可在层内自由移动,故石墨是
电的良导体。
石墨可用作原子核反应堆的慢化剂、火箭发动机喷管
和电极材料等。
图2.27 石墨晶体结构示意图
化学史话
科学家发现了碳的第三种同素异形体——富勒烯
1985年,科学家克罗托(S.H.W.Kroto)、斯莫利(R.E.Smalley)
和柯尔(R.F.Curl)在研究太空深处的碳元素时,发现有一种碳分子由60
个碳原子组成。它的对称性极高,其分子模型与那个已在绿茵场滚动了多
年、由12块黑色五边形与20块白色六边形拼合而成的足球竟然毫无二致。
因此,当斯莫利等人打电话给美国数学会主席告知这一信息时,这位主席竟
惊讶地说:“你们发现的是一个足球啊!”克罗托在英国《自然》杂志发表
第一篇关于C 论文时,索性就用一张安放在草坪上
60
的足球照片作为C 的分子模型。这种碳分子被称为
60
巴基球。巴基球又叫富勒烯,也称足球烯,是继石墨、
金刚石之后发现的纯碳的第三种独立形态。按理说,
人们早就该发现C 了。它在蜡烛烟黑中,在烟囱灰
60
里就有。然而几十年来,成千上万的化学家都与它失
之交臂。克罗托、斯莫利和柯尔因这一发现,荣获1996
图2.28 C
60
年度诺贝尔化学奖。 分子结构示意图
41
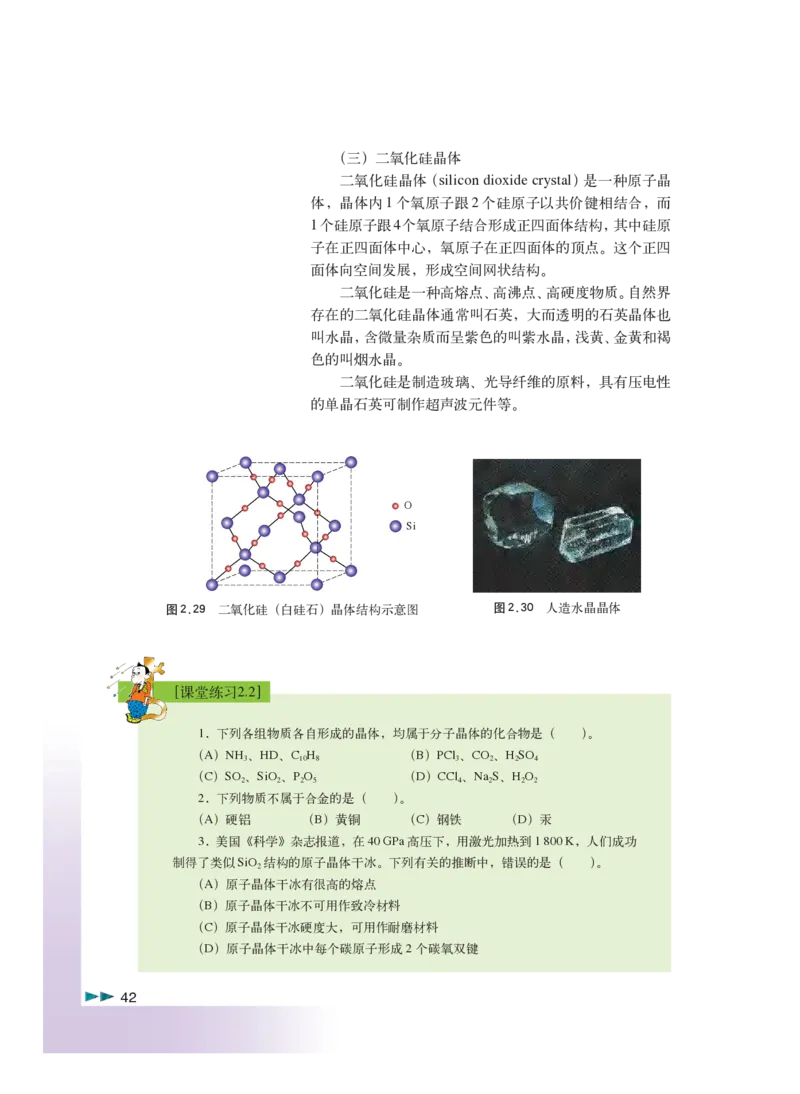
0812896-02-OK Page 41 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC(三)二氧化硅晶体
二氧化硅晶体(silicon dioxide crystal)是一种原子晶
体,晶体内1个氧原子跟2个硅原子以共价键相结合,而
1个硅原子跟4个氧原子结合形成正四面体结构,其中硅原
子在正四面体中心,氧原子在正四面体的顶点。这个正四
面体向空间发展,形成空间网状结构。
二氧化硅是一种高熔点、高沸点、高硬度物质。自然界
存在的二氧化硅晶体通常叫石英,大而透明的石英晶体也
叫水晶,含微量杂质而呈紫色的叫紫水晶,浅黄、金黄和褐
色的叫烟水晶。
二氧化硅是制造玻璃、光导纤维的原料,具有压电性
的单晶石英可制作超声波元件等。
O
Si
图2.29 二氧化硅(白硅石)晶体结构示意图 图2.30 人造水晶晶体
[课堂练习2.2]
1.下列各组物质各自形成的晶体,均属于分子晶体的化合物是( )。
(A)NH 、HD、C H (B)PCl 、CO 、H SO
3 10 8 3 2 2 4
(C)SO 、SiO 、P O (D)CCl 、Na S、H O
2 2 2 5 4 2 2 2
2.下列物质不属于合金的是( )。
(A)硬铝 (B)黄铜 (C)钢铁 (D)汞
3.美国《科学》杂志报道,在40 GPa高压下,用激光加热到1 800 K,人们成功
制得了类似SiO 结构的原子晶体干冰。下列有关的推断中,错误的是( )。
2
(A)原子晶体干冰有很高的熔点
(B)原子晶体干冰不可用作致冷材料
(C)原子晶体干冰硬度大,可用作耐磨材料
(D)原子晶体干冰中每个碳原子形成2 个碳氧双键
42
0812896-02-OK Page 42 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC4.表2.13中数据是对应物质的熔点:
表 2.13
物 质 Na O NaCl AlF AlCl BCl Al O CO SiO
2 3 3 3 2 3 2 2
熔点(℃) 920 801 1 291 190* -107 2 072 -57 1 723
*在2.5×105 Pa条件下测定
据此作出下列判断中错误的是( )。
(A)铝化合物的晶体中既有离子晶体,又有分子晶体
(B)同主族元素的氧化物可形成不同类型的晶体
(C)表中形成分子晶体的物质只有两种
(D)同周期不同主族的氧化物可形成相同类型的晶体
5.碘晶体升华时,下列所述内容发生变化的是( )。
(A)分子内化学键
(B)分子间的作用力
(C)分子内共价键的键能
(D)分子内共价键的键长
6.下列关于化学键的各种说法中,正确的是( )。
(A)在离子晶体里,只存在离子键
(B)共价化合物里,一定不存在离子键
(C)非极性键只存在于双原子的单质分子里
(D)由不同元素组成的多原子分子里,一定只存在极性键
43
0812896-02-OK Page 43 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC小 结
1. 物质中微粒间的相互作用。
表 2.14
作用的类型 产生作用的微粒 作用原理
离子键 阴、阳离子 强烈的静电作用
化
学 共价键 原子 形成共用电子对
键
金属键 金属离子、自由电子 金属离子间通过自由电子产生强烈的相互作用
分作 范德华力 分子 存在于分子间的相互作用
子用
间力 氢 键 水分子等微粒 静电作用
2. 晶体。
表 2.15
晶体类型 结构微粒 微粒间作用 典型实例 物理性质
分子晶体 分子 范德华力(氢键) 干冰 熔点较低、硬度较小
离子晶体 阴、阳离子 离子键 氯化钠晶体 熔点较高、硬度较大
原子晶体 原子 共价键 金刚石 熔点高、硬度大
金属晶体 金属阳离子、 金属键 铝 具有导电性、导热性、
自由电子 延展性
3. 阅读下列短文,理解金属键的形成原理。
A simplified model of metallic bonding is adequate for our purposes. In a metallic lattice, the
atoms lose their outer-shell electrons to become positive ions. The outer-shell electrons occupy new
energy levels, which extend throughout the metal lattice. The bonding is often described as “a sea”
of mobile electrons surrounding a lattice of positive ions. The lattice is held together by the strong
attractive forces between the mobile electrons and the positive ions.
44
0812896-02-OK Page 44 2011.4.7, 4:10 AM Adobe PageMaker 6.5C/PPC3
化 学 中 的 平 衡
EQUILIBRIUM IN CHEMISTRY
平衡是普遍存在的,化学中也存在
着各种平衡,如我们已经学过的溶解平
衡、电离平衡等。本章将进一步对化学中
存在的各种平衡进行探讨和研究,了解
平衡在生产、科技、生活中的应用。
学习过程中要注意各种平衡的内
在联系,使我们能较好理解和掌握化
◆ 溶解平衡
学平衡的一些普遍的规律。还要注意
◆ 化学反应中的平衡
平衡是有条件的,相对的,而不平衡则
◆ 电离平衡
是绝对的。 ◆ 水的电离和盐类的水解
45溶解平衡
3
.1
(EQUILIBRIUM OF SOLUTION)
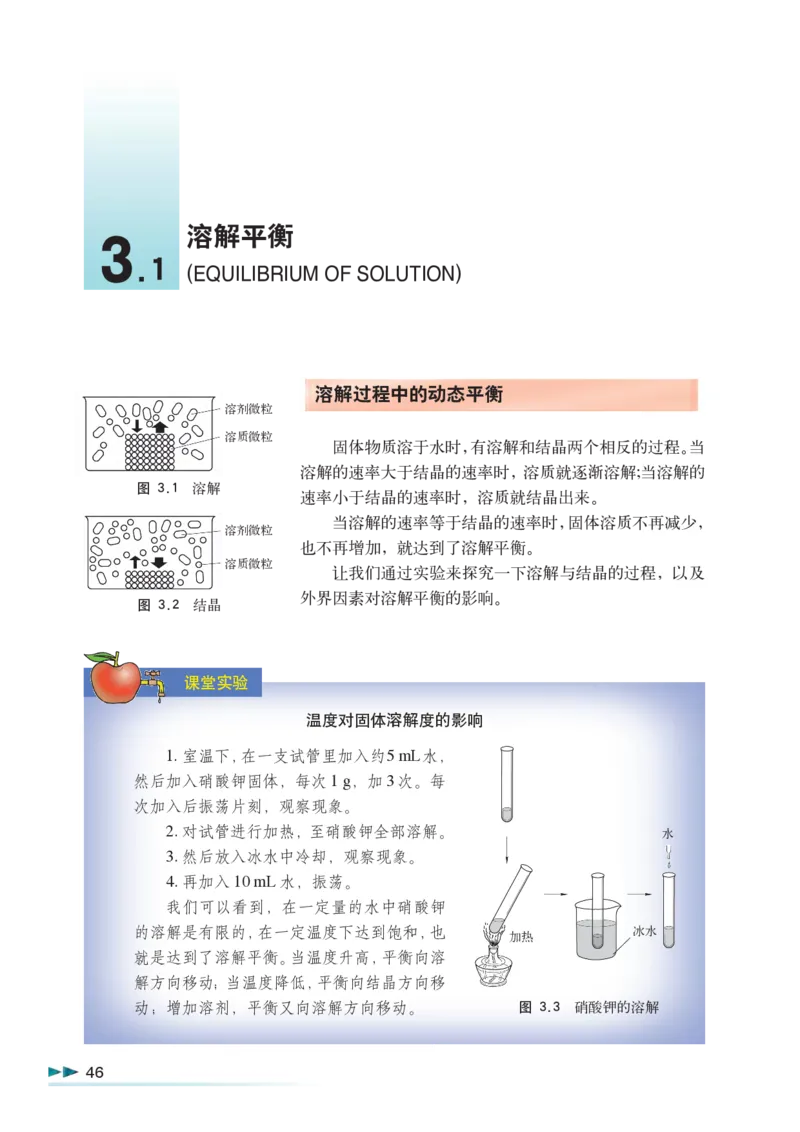
溶解过程中的动态平衡
溶剂微粒
溶质微粒
固体物质溶于水时,有溶解和结晶两个相反的过程。当
溶解的速率大于结晶的速率时,溶质就逐渐溶解;当溶解的
图 3.1 溶解
速率小于结晶的速率时,溶质就结晶出来。
当溶解的速率等于结晶的速率时,固体溶质不再减少,
溶剂微粒
也不再增加,就达到了溶解平衡。
溶质微粒
让我们通过实验来探究一下溶解与结晶的过程,以及
外界因素对溶解平衡的影响。
图 3.2 结晶
课堂实验
温度对固体溶解度的影响
1. 室温下,在一支试管里加入约5 mL水,
然后加入硝酸钾固体,每次1 g,加3次。每
次加入后振荡片刻,观察现象。
2. 对试管进行加热,至硝酸钾全部溶解。 水
3. 然后放入冰水中冷却,观察现象。
4. 再加入10 mL水,振荡。
我们可以看到,在一定量的水中硝酸钾
的溶解是有限的,在一定温度下达到饱和,也 冰水
加热
就是达到了溶解平衡。当温度升高,平衡向溶
解方向移动;当温度降低,平衡向结晶方向移
动;增加溶剂,平衡又向溶解方向移动。 图 3.3 硝酸钾的溶解
46课堂实验
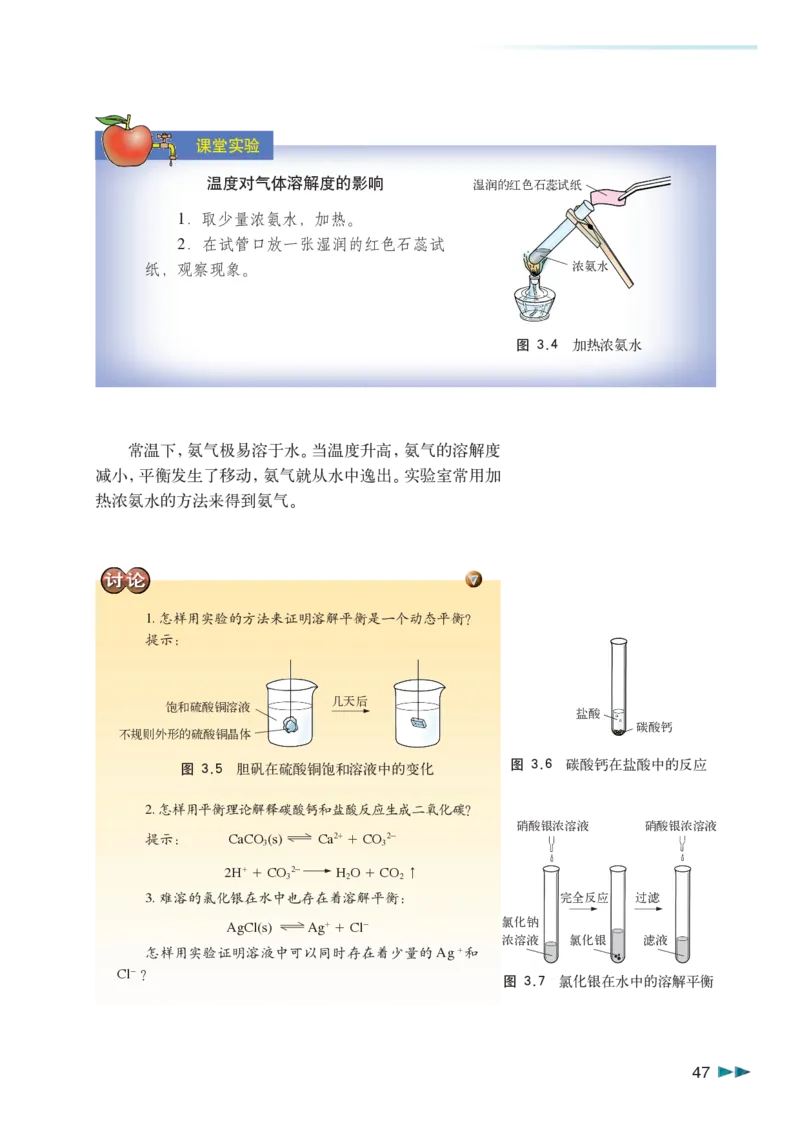
温度对气体溶解度的影响
湿润的红色石蕊试纸
1.取少量浓氨水,加热。
2.在试管口放一张湿润的红色石蕊试
纸,观察现象。 浓氨水
图 3.4 加热浓氨水
常温下,氨气极易溶于水。当温度升高,氨气的溶解度
减小,平衡发生了移动,氨气就从水中逸出。实验室常用加
热浓氨水的方法来得到氨气。
1. 怎样用实验的方法来证明溶解平衡是一个动态平衡?
提示:
几天后
饱和硫酸铜溶液
盐酸
碳酸钙
不规则外形的硫酸铜晶体
图 3.6 碳酸钙在盐酸中的反应
图 3.5 胆矾在硫酸铜饱和溶液中的变化
2. 怎样用平衡理论解释碳酸钙和盐酸反应生成二氧化碳?
硝酸银浓溶液 硝酸银浓溶液
提示: CaCO (s) Ca2++CO 2-
3 3
2H++CO 2- H O+CO ↑
3 2 2
3. 难溶的氯化银在水中也存在着溶解平衡: 完全反应 过滤
氯化钠
AgCl(s) Ag++Cl-
浓溶液 氯化银 滤液
怎样用实验证明溶液中可以同时存在着少量的Ag+和
Cl- ?
图 3.7 氯化银在水中的溶解平衡
47资料库
能溶解气体的金属——钯和铂
银白色的钯(Palladium)和铂(Platinum),它们的化学性质稳定,在空气中不易
被氧化,然而它们却是抓气体的“能手”。据试验,在常温下钯片能吸收比它体
积大700倍的氢气。钯不仅能吸收氢气,还能吸收氧气、氮气、乙烯等许多气体。
另据测定,粉末状的铂在常温下溶解氢气的能力虽然比钯差一些,但是溶解氧气
的能力却比钯强。
X射线研究表明,当氢气溶解到钯中以后,钯的晶格就胀大了,当钯中的氢
气浓度大到某一程度,钯的晶格会转变成另一种更疏松的形式,可见钯的这种性
质与它的结构是有关的。
根据钯和铂的这一奇妙的性质,它们在化学工业上常用作催化剂。例如,在
钯的催化下,液态的油脂可以加氢变成固态;在铂粉的催化下,常温时氢、氧就
会爆炸发生化合。目前,虽然还没有彻底弄清钯和铂的催化原理,但是,人们认
为这与它们能大量溶解气体的性质有关。因为大量溶解了气体,等于把气体浓缩
了,这样就增加了气体分子相互发生碰撞进行反应的机会。
结晶和重结晶
将某些溶液蒸发浓缩,到一定程度就会有晶体析出。这
个使溶质从溶液中析出的过程,称为结晶(crystallization)。
不饱和溶液 蒸发溶剂 饱和溶液 蒸发溶剂 晶体析出
由此可见,在一定温度下使饱和溶液中的溶剂量减少,
使平衡向结晶方向移动,就会有晶体析出。此时溶液仍为
饱和溶液(saturated solution)。
48课堂实验
无水硫酸铜粉末
无水硫酸铜的变色
在硫酸铜饱和溶液中加入少量无水硫酸
铜粉末,振荡后静止,观察现象。 硫酸铜饱和溶液
图 3.8 将无水硫酸铜放入硫酸铜
饱和溶液中
1.上述实验中,为什么固体由白色变成了蓝色?
2.固体的量有何变化?为什么?
如果改变饱和溶液的温度,平衡也会发生移动。通常
降低温度会使固体物质的溶解度减小,使平衡向结晶方向 S(g/100g水)
移动,就会有晶体析出。例如: KNO
3
不饱和KNO 溶液 降低温度 饱和KNO 溶液
3 3
降低温度 有KNO 晶体析出
3
NaCl
有些物质的溶解度随温度的影响不明显,如氯化钠。
当两种或多种溶质在一种溶剂中的溶解度不同,可以
t(℃)
用结晶的方法进行分离和提纯。使结晶出来的晶体溶在适 O
图 3.9 KNO 、NaCl的
当的溶剂里,再经过加热、蒸发、冷却等步骤重新得到晶 3
溶解度曲线
体,这一过程称为重结晶。重结晶常用于精制晶体。
49课堂实验
用重结晶的方法除去硝酸钾中少量的氯化钠
在硝酸钾固体中混有少量氯化钠,如何用实验的方法提纯硝酸钾呢?
实验设计如下:
加适量水溶解 冷却
KNO 固体(混有少量NaCl) 热的浓溶液 溶液中析出晶体
3 加热
过滤 再加适量水溶解 冷却
晶体(还混有极少量NaCl) 热的浓溶液 溶液中析出
加热
过滤
晶体 KNO 晶体
3
请根据以上实验设计方案进行实验,并完成实验报告。
1.为什么该实验中冷却热的饱和溶液时,析出的晶体
主要是硝酸钾?用平衡移动的观点加以说明。
2.为什么还要重结晶?
3.怎样除去氯化钠中少量的硝酸钾?
[课堂练习3.1]
1.用大量的沉淀剂能否从溶液中把一种离子完全除净?为什么?
2.在水中加入一定量的氢氧化钙固体,待充分溶解后达到平衡:
Ca(OH)(s) Ca2++2OH-
2
当分别加入①氧化钙固体,②水,③氯化铵,④氯化钙,⑤氢氧化钠固体时,试
判断氢氧化钙的量是增多,减少,还是不变?
3.重金属在水中既能以化合物的形态存在,也能以离子形态存在。由于重金属化
合物溶解度很小,往往沉积于水底。又由于重金属离子带正电荷,在水中易被带负电
荷的土壤胶粒所吸附,大多数会很快沉降下来。因此,重金属一般都富集在排水口下
游一定范围的底泥中,成为一个长期的次生污染源。一般污染物,在汛期水量的稀释
下,其浓度是降低的,而重金属污染物却并不降低,甚至是升高的,试用溶解平衡等
知识解释。
4.重结晶的主要目的是什么?在操作中要注意些什么?
50化学反应中的平衡
3
.2
(EQUILIBRIUM IN CHEMICAL REACTIONS)
化学反应速率
我们用化学反应速率(chemical reaction rate)来定量表示
化学反应的快慢。通常用单位时间内反应物浓度的减小或
生成物浓度的增大来表示,实际是指一段时间内的平均反
应速率。用不同的反应物或生成物来表示的化学反应速率,
大小可能不一样,它们的比值等于化学方程式中的化学计
量数之比,但都表示相同的化学反应速率。
影响化学反应速率的因素很多,有温度、浓度、压强、
催化剂、固体颗粒大小、光、电、超声波等等。下面通过实
例来进行探究。
探究与实践
1.压强对该反应的
探究锌和硫酸反应速率
化学反应速率有何影
设计有关实验来探究锌和硫酸反应的化学反应速 响?
2.是否需选择合适
率,并根据实验结果对化学反应速率的一些影响因素
的催化剂来加快该反应
进行分析讨论。
的化学反应速率?
设计提示:
1. 不同温度下化学反应速率大小比较。
2. 硫酸浓度不同时,化学反应速率大小比较。
3. 锌的颗粒大小不同时,化学反应速率大小比较。
4. 加入某些物质(如硫酸铜晶体、氯化钡晶体、
硫酸钠晶体等)对化学反应速率的影响。
51化学平衡的特征
在我国广西桂林芦笛岩地下溶洞中,流过微酸性的地
下水,经千百万年“水滴石成”,壮丽的石灰岩令人叹为
观止。
石灰石长期暴露在含有CO 的空气中并反复经受雨淋、
2
日晒或温度变化,不断发生CaCO 与CO 、H O反应生成
3 2 2
Ca(HCO ) ,Ca(HCO ) 分解生成CaCO 沉淀与CO 、H O
3 2 3 2 3 2 2
的反应。
碳酸钙沉淀沉积在岩洞的顶端,就形成了钟乳石。如
果沉积在岩洞的地面,就长成石笋,有的则形成怪异的石
柱,蔚为奇观。
图 3.10 桂林芦笛岩的
石灰岩溶洞
探究与实践
分别探究二氧化碳和溴在水中的平衡
1.探究二氧化碳在水中的平衡。
(1)在厚壁锥形瓶中放入石灰石和稀盐酸,
并将瓶塞塞紧。
(2)当不再看到有气泡产生时,把瓶塞打
开,观察现象,并用平衡移动的观点加以解释。
图 3.11 开瓶塞前水中无气泡,
2.探究溴水中的化学平衡。
开瓶塞后水中冒出气泡
溴水中存在如下化学平衡:
Br +H O H++Br-+HBrO 氢氧化钠溶液 盐酸
2 2
可用下列实验证明溴水中存在着以上平
衡,并使该平衡发生移动。
(1)取少量溴水于一支试管中,观察它
的颜色。
(2)向试管中滴加氢氧化钠溶液,观察
现象。 溴水
(3)再向试管中滴加盐酸,观察现象,
图 3.12 溴水中的化学平衡移动
并用平衡移动的观点加以解释。
根据以上探究可以知道,任何平衡都是动态平衡,即
υ =υ ≠0;在一定条件下达到平衡时,平衡体系中各物
正 逆
52质的量是确定的值,不再发生变化;当外界条件发生变化
时,平衡会发生移动。平衡移动可以用勒夏特列原理解释。
平衡是相对的、暂时的。
平衡转化率
在工业生产中,为了充分利用原料,总是希望反应物
尽可能多地转化为生成物。因此,对可逆反应来说,研究化
学反应达到平衡时,反应物转化成产物的百分率,也就是
一个可逆反应实际可进行的程度,是很有必要的。
指定反应物的起始浓度-该反应物的平衡浓度
某反应的平衡转化率=—————————————————————×100%
该反应物的起始浓度
转化率越大,则该反应进行得越完全,一般地说,生产
的效率也越高。
练 习
表3.1是在CO+H O(g) CO +H 反应中测定的四组不
2 2 2
同情况下的各反应物和生成物的起始浓度和平衡浓度。请计算
第1、3、4组的CO平衡转化率,填入表内。通过计算你可以
得到什么结论?
再计算第2组H 的平衡转化率,填入表内。要提高H 的
2 2
平衡转化率,在温度不变的情况下,可采用哪些措施?
表3.1 在CO+H O(g) CO +H 反应中,
2 2 2
各物质的起始浓度、平衡浓度和平衡转化率(800℃)
起始时各物质浓度(mol/L) 平衡时各物质浓度(mol/L) 平衡转化率(%)
组
别 c(CO) c(H 2 O) c(CO 2 ) c(H 2 ) c(CO) c(H 2 O) c(CO 2 ) c(H 2 ) CO的平 H 2 的平
衡转化率 衡转化率
(1) 0.01 0.01 0 0 0.005 0.005 0.005 0.005 /
(2) 0 0 0.02 0.01 0.006 7 0.006 7 0.013 3 0.003 3 /
(3) 0.002 5 0.03 0.007 5 0.007 5 0.002 1 0.029 6 0.007 9 0.007 9 /
(4) 0.01 0.03 0 0 0.002 5 0.022 5 0.007 5 0.007 5 /
531.表3.1的四组实验,反应物的起始浓度不一。那么,
在一定温度下,无论从正反应开始,还是从逆反应开始,最
后都能达到化学平衡状态吗?
2.计算表3.1的四组实验中,平衡时生成物浓度乘积与
[ c(CO ).c(H ) ]
反应物浓度乘积的比值 ————2 ——2— ,根据计算结果,
c(CO).c(H O)
2
你能得出什么结论。
平衡常数
在一定条件下,当可逆反应达到平衡后,体系中各
物质的浓度不再发生变化,能不能找到各物质的浓度在
表3.2 N +3H 2NH +Q 化学平衡状态时的定量关系呢?
2 2 3
在不同温度时的平衡常数 我们发现,在一定温度下,可逆反应无论从正反应开
始,还是从逆反应开始,又无论反应开始时反应物浓度的
温度(℃) 平衡常数
大小是否相同,当达到平衡时,把生成物浓度指数幂的乘
350 1.847
积除以反应物浓度指数幂的乘积,得到的比值是个常数。
400 0.507
这个常数叫做该反应的化学平衡常数(简称平衡常数,
450 0.152
equilibrium constant),用符号K表示。
对于一般的可逆反应mA+nB pC+gD,当在一定温
度下达到平衡,存在如下关系:
[c(C)]p . [c(D)]g
————————=K
[c(A)]m . [c(B)]n
在800℃时,反应CO+H O(g) CO +H 的K=1.0;
2 2 2
在1 000℃时,该反应的K=1.6。可见在不同的温度下,平
衡常数K的值是不同的。
541.平衡常数K值的大小能不能表示可逆反应进行的程
度?K值大,正向反应进行的程度是越大,还是越小?为什
么?
2.平衡常数与反应物的平衡转化率都能表示反应进行
的程度,它们之间有什么不同?哪一个更能反映出反应的本
质?
3.在使用平衡常数时,为什么一定要指明反应温度?
4.在稀的水溶液中进行的反应,如果反应中有水参加,
水的浓度不必写在平衡常数的表达式中,为什么?
5.在有气态物质参加的反应中,有固体或纯液体物质
参加时,固体物质和纯液体就不要写在平衡常数的表达式
中,为什么?
练 习
写出下列可逆反应的平衡常数表达式。
300℃
1.H (g)+I (g) 2HI(g)
2 2
225℃
2.CO(g)+2H (g) CH OH(g)+Q
2 3
*试从手册中查找上述两个反应的化学平衡常数。
表3.3 两个常见反应的平衡常数K
化学反应 反应温度(℃) 平衡常数
[c(NH )]2
N +3H 2NH 25 K=————3——=5×108
2 2 3 c(N )[c(H )]3
2 2
[c(NO)]2
N +O 2NO 27 K=—————=3.84×10-31
2 2 c(N )c(O )
2 2
根据表3.3你可以得出哪些结论?合成氨反应和氮、氧
的化合反应有什么本质的区别?
55[课堂练习3.2]
1.用化学反应速率的知识解释下列问题:
(1)为什么木炭在纯氧中燃烧比在空气中燃烧剧烈?
(2)为什么要把碳酸氢铵贮放在阴凉的地方?
(3)为什么高炉炼铁时焦炭和铁矿石要粉碎到一定程度?
(4)只有在较高温度时,葡萄糖才能在空气中燃烧发生氧化反应;可是在人体里,
葡萄糖在正常体温(37℃)时就可以被氧化。这是为什么?
2.合成氨工业中,原料气(N 、H 及少量CO、NH 的混合气)在进入合成塔前
2 2 3
常用醋酸二氨合铜(I)溶液来吸收原料气中的CO,其反应方程式是:
Cu(NH ) Ac+CO+NH Cu(NH ) Ac·CO+Q
3 2 3 3 3
(1)必须除去原料气中CO的原因是___________________。
(2)醋酸二氨合铜(I)吸收CO的生产适宜条件应是__________________。
(3)吸收CO后的醋酸铜氨溶液经过适当处理又可再生,恢复其吸收CO的能力以
供循环使用。醋酸铜氨溶液再生的生产适宜条件应是________________。
3.试用平衡常数的表达式,分析增大生成物的浓度对化学平衡的影响。
4.阅读下列短文,谈谈浓度改变对化学平衡移动的影响。
For any equilibrium system, the reaction can be shifted forward or backward by changing
the concentration of a reactant or product. If more of a particular substance is added to a reaction
at equilibrium, the concentration of that substance increases. The reaction will return to
equilibrium by consuming some of the added substance. Conversely, if a substance is removed,
its concentration decreases. The reaction will return to equilibrium by producing more of the
substance that was removed.
56电离平衡
3
.3
(IONIZATION EQUILIBRIUM)
弱电解质的电离
课堂实验
用pH计测定盐酸、醋酸溶液的pH
1.用pH计测定0.1mol/L HCl的pH。
2.用pH计测定0.1mol/L CH COOH的pH。
3
3.比较它们的pH大小,并解释其原因。
图 3.13 用pH计测盐酸、
醋酸溶液的pH
强酸(如盐酸、硝酸、硫酸等)、强碱(如氢氧化钠、
氢氧化钾、氢氧化钙、氢氧化钡等)和绝大多数的盐在
水溶液里都能全部电离,所以它们都是强电解质(strong
electrolyte)。弱酸(如醋酸、碳酸等)、弱碱(如氨水等)在
水溶液里只能部分电离,所以它们都是弱电解质(weak
electrolyte)。水也能发生微弱的电离,所以水是极弱电解质。
葡萄糖、蔗糖等化合物不论在液态或水溶液里都不会电离,
所以,它们都是非电解质(non-electrolyte)。
醋酸在溶液中存在着以下电离平衡:
CH COOH CH COO-+H+
3 3
57碳酸是二元弱酸,它分两步进行电离,因此在水溶液
中存在着以下的电离平衡:
H CO H++HCO-
2 3 3
HCO - H++CO 2-
3 3
氨水中也存在着以下电离平衡:
1.为什么碳酸氢钠
溶液是弱碱性的?请从
NH ·H O NH++OH-
它对水的电离平衡影响 3 2 4
的角度加以分析。
在以上水溶液中,同时存在着水的电离平衡:
2.为什么NaHCO
3
既能和酸反应,又能和碱
反应?写出反应的离子 H O H++OH-
2
方程式。
分析弱电解质在水中的电离平衡时,除了要考虑弱电
解质的电离平衡外还需要考虑水的电离平衡的影响。例如
醋酸在水中电离出来的H+,会抑制水的电离。
化学史话
物理学研究对化学发展的重大促进
1881年,在斯德哥尔摩科学院研究放电现象的阿伦尼乌斯(Svante August
Arrhenius,1859—1927)为了研究溶液中的离子是怎样形成的,开始研究电解
质溶液的导电性。经过3年的努力,1884年,阿伦尼乌斯在他的学位论文中指
出,溶解于水的电解质在不同程度上离解为带正、负电荷的离子,离解程度决定
于物质的本性以及它们在溶液中的浓度,溶液越稀,离解程度越大,在极稀的溶
液中分子完全离解。这个观点在当时引起了很大的争议。为了证实电离观念的正
确,在1886至1888年间,阿伦尼乌斯又进一步研究了电解质的离解对溶液的渗
透压、凝固点降低、沸点上升等性质的影响,并用电导方法测得电解质在溶液中
的离解度。阿伦尼乌斯用实验确定的各种离子的电荷数,阐明了酸、碱、盐等电
解质的化学组成以及它们在化学反应中的定量关系,使电离学说以全新的、定量
的形式得到了大家的认可。
阿伦尼乌斯通过物理学的研究,提出了重要的化学基本理论,树立了多学科
综合研究的典范。1903年,瑞典皇家科学院主席在把诺贝尔化学奖授予这位斯德
哥尔摩大学的物理学教授时说,物理学研究对化学发展的促进,这一事实闪发着
为解开生命之谜的共同目标,不同自然科学间亲缘关系的新光辉。在当前科学高
度发达的时代,多学科的综合研究具有更广阔的前景。因此,我们在学习过程中,
也应注重各学科的渗透和综合。
58电离度和电离平衡常数
课堂实验
用pH计测定甲酸和醋酸的pH
1.用pH计分别测定0.1 mol/L甲酸(HCOOH)和0.1 mol/L醋酸的pH。
2.将0.1 mol/L醋酸溶液加热,然后用pH计测定它的pH。
从上面实验可以看到,不同的弱电解质的电离程度并
不相同,同一种弱电解质在不同温度下的电离程度也不相
同。我们通常用电离度(ionization degree)来定量地表示
弱电解质在水溶液里电离程度的大小。
电解质的电离度(常用符号α表示)是指在一定条件
下,当弱电解质在溶液里达到电离平衡时,溶液里已经电
离的电解质分子数占原来总分子数(包括已电离和未电离)
的百分率。即:
已电离的电解质分子数
α=——————————————×100%
溶液中原来电解质的总分子数
表3.4 25℃时,0.10 mol/L溶液里某些弱电解质的电离度
电解质 化学式 α(%)
氢氟酸 HF 8.0
甲 酸 HCOOH 4.2
醋 酸 CH COOH 1.3
3
表3.5 25℃时,不同浓度
氢氰酸 HCN <0.01
醋酸的电离度
氨 水 NH·H O 1.3
3 2
c(mol/L) α(%)
0.1 1.3
弱电解质的电离度不但与温度有关,还跟溶液的浓度
0.05 1.9
有关。
0.01 4.2
从表3.5可见,当温度一定时,弱电解质的浓度越稀,
它的电离度就越大。这是由于弱电解质溶液加水稀释后, 0.001 12
59减少了离子碰撞结合成分子的机会,结果使电离度增大。
0.001 mol/L醋酸的电离度(α=12%)比0.1 mol/L氢氟酸
的电离度(α=8.0%)还大,当然,不能认为醋酸是比氢氟
酸更强的酸。
因此,使用电离度数值时,除了注意温度外,还必须注
意溶液的浓度,不注明浓度的电离度数值是没有意义的。
电离达成平衡后,溶液中电离出来的各种离子浓度的
乘积跟溶液中未电离的分子浓度之比也是一个常数,这个
常数称为电离平衡常数(简称电离常数,ionization constant),
用K 来表示。
i
以氨水为例,氨水的电离平衡如下:
NH ·H O NH++OH-
3 2 4
它的电离常数可表示为:
c(NH+)·c(OH-)
4
K = —————————
i
c(NH ·H O)
表3.6 一些常见一元酸 3 2
和氨水的电离常数(25℃)
电离常数跟化学平衡常数一样,只随温度的变化而改
电解质 化学式 电离常数K
i
变,不随参与电离平衡的各物质(分子或离子)的浓度变化
氢氟酸 HF 3.53×10-4
而改变。当温度在室温范围内变化时,电离常数的变化不
甲酸 HCOOH 1.77×10-4
大,所以我们通常都用25℃时的电离常数来讨论室温时各
醋酸 CH COOH 1.75×10-5
3 种弱电解质溶液的电离平衡状态。
氢氰酸 HCN 4.93×10-10 表3.6中列出一些常见的一元酸和氨水在25 ℃时的电
氨水 NH·H O 1.77×10-5 离常数。
3 2
练 习
1.写出表3.6中氢氟酸、甲酸、醋酸、氢氰酸电离常数
的表示式。
2.根据表3.6中电离常数的数据,比较氢氟酸、甲酸、醋
酸、氢氰酸的酸性强弱。
表3.7 碳酸的电离常数(25℃)
电解质 化学式 电离常数K
i
碳酸是二元弱酸,分两步电离。表3.7是25 ℃时碳酸
碳酸 H CO K =4.3×10-7
2 3 i1 的电离常数。其中K 表示第一级电离的电离常数,K 表示
i1 i2
K =5.6×10-11
i2 第二级电离的电离常数。
60下面我们以氨水为例,用电离常数来分析温度对电离 练 习
平衡(NH ·H O NH++OH-)移动的影响。
3 2 4
1.写出碳酸电离常
数K 、K 的表达式。
i1 i2
2.从碳酸的电离常
数K 、K 数值的比较可
i1 i2
已知温度升高,NH ·H O的电离平衡常数增大,请填 以得出哪些结论?
3 2
写表3.8。(填“变大”“变小”或“不变”,平衡移动方向填
“→”或“←”。)
表 3.8
温度变化 氨水的K c(NH ·H O) c(NH +) c(OH-) 电离平衡移动方向
i 3 2 4
温度升高
温度降低
电离度与电离常数都可以表示一定条件下弱电解质的
电离程度。它们之间又有什么区别呢?
相同温度时,由于电离度的大小与浓度有关,因此,必
须用相同浓度下电离度的大小来比较弱酸或弱碱之间的相
对强弱。相同温度时,电离常数与浓度无关,所以用电离常
数来比较弱酸或弱碱的相对强弱就比用电离度来比较要方
便得多。
[课堂练习3.3]
1.现有0.1 mol/L氨水,如分别采取下列措施:①通入氨气,②加入氢氧化钠固
体,③加入氯化铵固体,④加入水。
这些措施分别对电离平衡有何影响?这些措施将对氨水里的NH·H O、OH-、NH+
3 2 4
的浓度各有何影响?(将结果填入表3.9)
表 3.9
影响
电离平衡 c(NH·H O) c(NH+) c(OH-)
条件改变 3 2 4
通入氨气
加氢氧化钠固体
加氯化铵固体
加水稀释
612.用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各
100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同量的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,
即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是____________________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH_________1(选填“大
于”“等于”或“小于”)。乙方案中,说明HA是弱电解质的现象是_________。
(A)装盐酸的试管中放出H 的速率快
2
(B)装HA溶液的试管中放出H 的速率快
2
(C)两个试管中产生气体速率一样快
(3)请你评价乙方案中难以实现之处和不妥之处是___________________________
______________________________________________________________________________。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述:
_________________________________________________________________________。
62水的电离和盐类水解
3
.4
(IONIZATION OF WATER AND HYDROLYSIS OF SALTS)
水的电离和溶液的pH
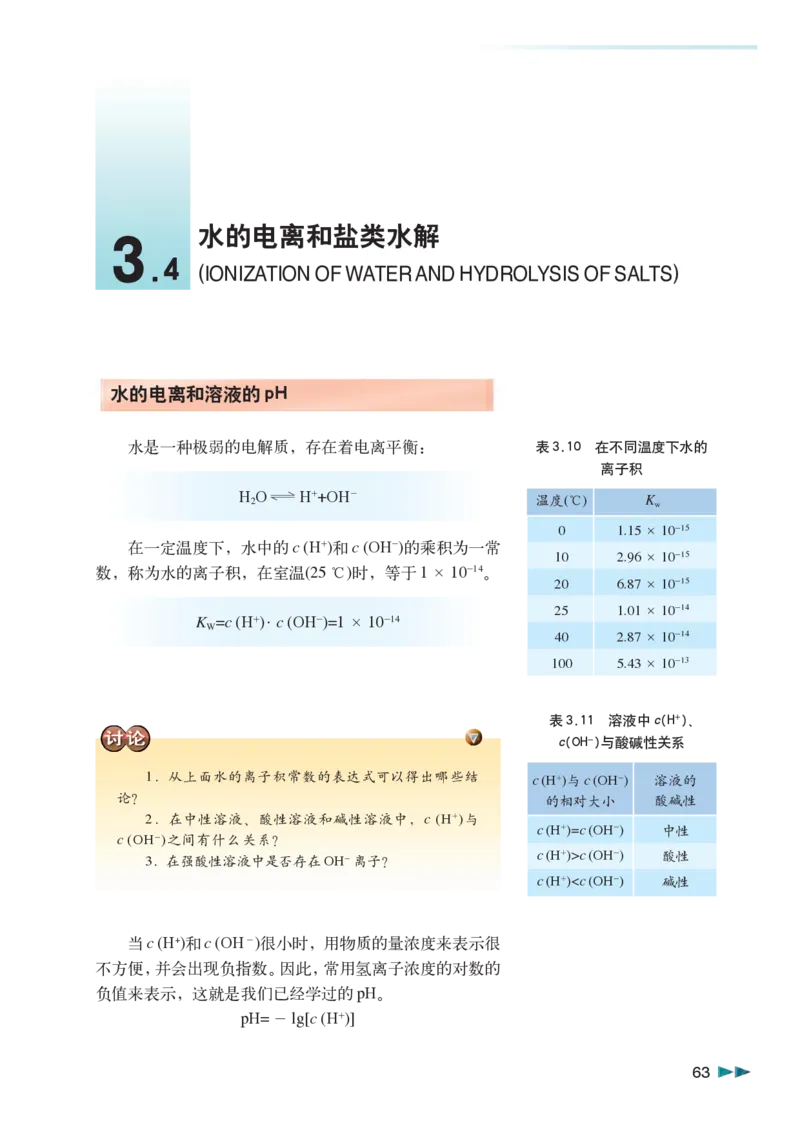
水是一种极弱的电解质,存在着电离平衡: 表3.10 在不同温度下水的
离子积
H 2 O H++OH- 温度(℃) K w
0 1.15×10-15
在一定温度下,水中的c (H+)和c (OH-)的乘积为一常
10 2.96×10-15
数,称为水的离子积,在室温(25℃)时,等于1×10-14。
20 6.87×10-15
25 1.01×10-14
K =c (H+)·c (OH-)=1×10-14
W
40 2.87×10-14
100 5.43×10-13
表3.11 溶液中c(H+)、
c(OH-)与酸碱性关系
1.从上面水的离子积常数的表达式可以得出哪些结 c(H+)与c(OH-) 溶液的
论? 的相对大小 酸碱性
2.在中性溶液、酸性溶液和碱性溶液中,c (H+)与
c(H+)=c(OH-) 中性
c (OH-)之间有什么关系?
c(H+)>c(OH-) 酸性
3.在强酸性溶液中是否存在OH-离子?
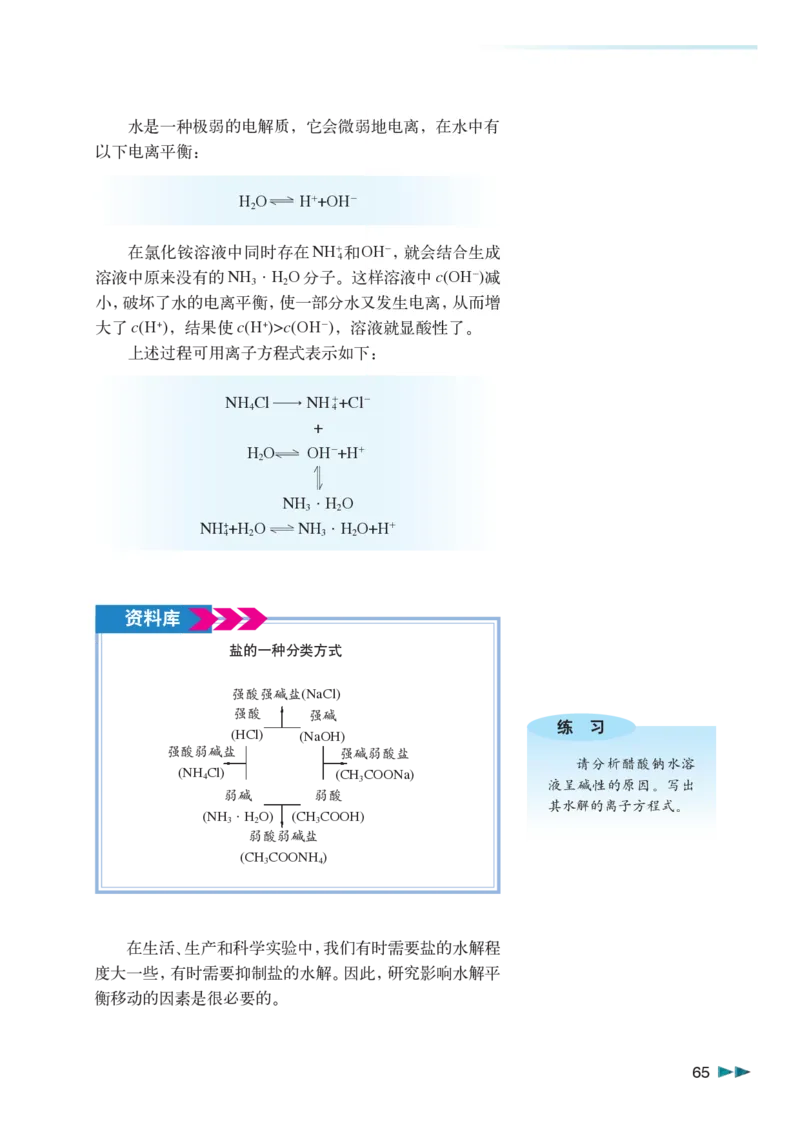
c(H+)c(OH-),溶液就显酸性了。
上述过程可用离子方程式表示如下:
NH Cl—→NH++Cl-
4 4
+
H O OH-+H+
2
NH ·H O
3 2
NH++H O NH ·H O+H+
4 2 3 2
资料库
盐的一种分类方式
强酸强碱盐(NaCl)
强酸 强碱
练 习
(HCl) (NaOH)
强酸弱碱盐 强碱弱酸盐
请分析醋酸钠水溶
(NH Cl) (CH COONa)
4 3 液呈碱性的原因。写出
弱碱 弱酸
其水解的离子方程式。
(NH·H O) (CH COOH)
3 2 3
弱酸弱碱盐
(CH COONH )
3 4
在生活、生产和科学实验中,我们有时需要盐的水解程
度大一些,有时需要抑制盐的水解。因此,研究影响水解平
衡移动的因素是很必要的。
65课堂实验
温度对醋酸钠溶液水解平衡的影响
1.如图(a),在两支试 酚酞溶液
管中,各加入2 mL 0.5 mol/L
醋酸钠溶液和1滴酚酞试液,
观察颜色的变化。
2.如图(b),将其中一
支试管加热后,再与另一支
2 mL 0.5 mol/L醋酸钠
试管比较。
(a) (b)
图 3.14 温度变化对水解平衡的影响
1.盐类水解和酸碱 氯化铁溶液的配制
中和反应有什么关系?
问题思考:将氯化铁溶于蒸馏水配制溶液时常会出现浑
2.中和反应是放热
浊,得不到澄清的氯化铁溶液,这是什么原因?
反应,那么盐类水解是放
[提示:Fe3++3H O Fe(OH) +3H+。]
热反应还是吸热反应? 2 3
浓度改变也会影响水解平衡的移动,采取怎样的措施可
3.从平衡移动原理
配制澄清的氯化铁溶液?
分析上述实验的现象,并
请设计方案,配制1 mol/L的氯化铁溶液50 mL。
得出结论。
[课堂练习3.4]
1.计算下列溶液的pH。
(1)0.40 g氢氧化钠配成100 mL溶液。
(2)把pH=1.00的盐酸稀释为原来体积的100倍。
2.有两瓶pH=2的酸溶液,一瓶是强酸,一瓶是弱酸。现只有pH试纸、石蕊试液、
蒸馏水,简述如何用最简便的实验来判别其中哪瓶是强酸?简述实验过程。
3.写出下列化合物在水中水解的离子方程式。
(1)氯化铁 (2)碳酸钾 (3)硫酸铵 (4)碳酸氢钠
4.试从平衡移动的观点,解释为什么在配制硝酸铝溶液时预先要往水中加入一些
硝酸?
5.碳酸钠溶液中存在哪些离子?碳酸氢钠溶液中存在哪些离子?如果这两种溶液
的物质的量浓度相同,你会比较这两种溶液中各种相同离子的浓度的大小吗?
66小 结
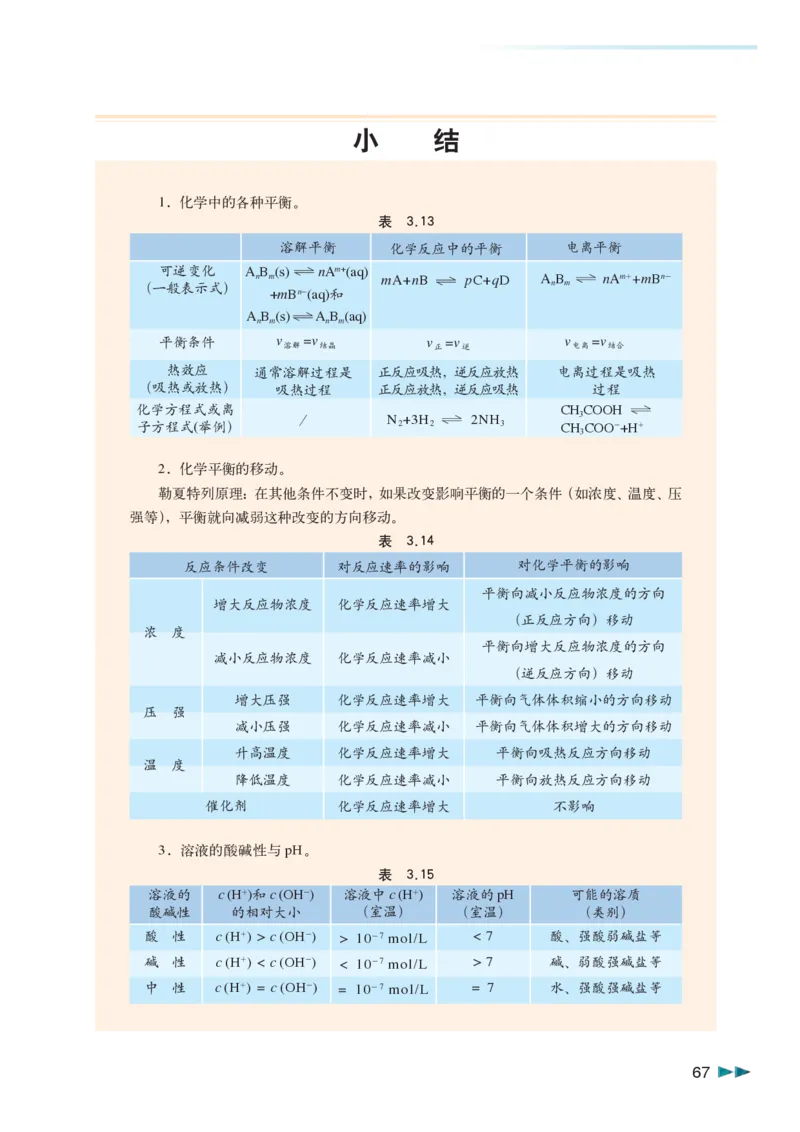
1.化学中的各种平衡。
表 3.13
溶解平衡 化学反应中的平衡 电离平衡
可逆变化 A B (s) nAm+(aq)
n m mA+nB pC+qD A B nAm++mBn-
(一般表示式) n m
+mBn-(aq)和
AB (s) AB (aq)
n m n m
平衡条件 v =v v =v v =v
溶解 结晶 正 逆 电离 结合
热效应 通常溶解过程是 正反应吸热,逆反应放热 电离过程是吸热
(吸热或放热) 吸热过程 正反应放热,逆反应吸热 过程
化学方程式或离 CHCOOH
/ N +3H 2NH 3
子方程式(举例) 2 2 3 CH COO-+H+
3
2.化学平衡的移动。
勒夏特列原理:在其他条件不变时,如果改变影响平衡的一个条件(如浓度、温度、压
强等),平衡就向减弱这种改变的方向移动。
表 3.14
反应条件改变 对反应速率的影响 对化学平衡的影响
平衡向减小反应物浓度的方向
增大反应物浓度 化学反应速率增大
(正反应方向)移动
浓 度
平衡向增大反应物浓度的方向
减小反应物浓度 化学反应速率减小
(逆反应方向)移动
增大压强 化学反应速率增大 平衡向气体体积缩小的方向移动
压 强
减小压强 化学反应速率减小 平衡向气体体积增大的方向移动
升高温度 化学反应速率增大 平衡向吸热反应方向移动
温 度
降低温度 化学反应速率减小 平衡向放热反应方向移动
催化剂 化学反应速率增大 不影响
3.溶液的酸碱性与pH。
表 3.15
溶液的 c(H+)和c(OH-) 溶液中c(H+) 溶液的pH 可能的溶质
酸碱性 的相对大小 (室温) (室温) (类别)
酸 性 c(H+) > c(OH-) > 10-7 mol/L < 7 酸、强酸弱碱盐等
碱 性 c(H+) < c(OH-) < 10-7 mol/L > 7 碱、弱酸强碱盐等
中 性 c(H+) = c(OH-) = 10-7 mol/L = 7 水、强酸强碱盐等
674.阅读。
Le Chatelier’s Principle
Imagine this scene: A daring tightrope walker balances precariously on a thin wire high above
Niagara Falls. The smallest gust of wind could cause the tightrope walker to lose his balance and
plunge into the raging torrent below! Luckily, he is able to maintain his balance by adjusting the long
pole he carries. In a similar way, a chemical reaction at equilibrium can be disturbed and shifted away
from equilibrium. Instead of a gust of wind, the factors that alter chemical equilibria are
concentrations of reactants and products, pressure, and temperature.
You can qualitatively predict the effects of changes in concentrations, pressure, and temperature
using a principle developed by Henri Louis Le Chatelier. Le Chatelier (1850—1936) was trained
in France as a mining engineer. Upon graduation, he joined the faculty of the mining school as a
professor of chemistry. Le Chatelier began studying flames in hopes of preventing mine explosions.
His work eventually led him to establish Le Chatelier’s principle in 1888. Le Chatelier’s principle
states that if a change in conditions is imposed on a system at equilibrium, the equilibrium position
will shift in the direction that tends to reduce that change in conditions. In other words, a reaction
system will shift in the forward or reverse direction to“ undo”, or compensate for, the altering factor.
684
离子互换反应和氧化还原反应
IONIC EXCHANGE REACTION AND REDOX REACTION
化学变化形形色色,多种多样。化学
家们从不同的角度探究化学变化的规
律:如热化学研究的是化学变化中的热
量变化;化学平衡则是讨论化学变化进
行的可能程度等。
本章探究离子之间进行的互换反应
和氧化还原反应的规律,将使我们对化
◆ 离子互换反应及其离子方程式
学变化规律的认识更加全面和深化。
◆ 氧化还原反应及其配平
69离子互换反应
4
.1
(IONIC EXCHANGE REACTION)
我们已经学过电解质在溶液中的反应是离子之间的
反应,这类在溶液中通过离子进行的反应,通常称为离子
反应。
离子反应有两种情况,一种是没有电子转移的,是离
子互换反应;另一种是有电子转移的,属于氧化还原反应。
离子互换反应的实质是什么呢?本节我们将用电离理论及
平衡移动的观点来讨论离子互换反应发生的规律。
离子互换反应的规律
判断以下各组物质在溶液中是否发生离子互换反应,
如能发生反应请完成化学方程式,并按表列内容分析各个
反应(溶液中水电离的H+和OH-不必写出),把分析结果
填入表4.1内。
1.NaOH + HCl →
2.Na CO + CaCl →
2 3 2
3.Na CO + HCl →
2 3
4.CH COONa + HCl →
表 4.1 3
反应 反应前溶液中 恰好反应后 反应前后
生成物
序号 浓度较大的离子 溶液中浓度较大的离子 浓度有明显变化的离子
1
2
3
4
上述四个反应共同的特点:____________。
70从分析可以知道,第2个反应是Ca2+和CO2-结合成难
3
溶物质CaCO ,使Ca2+、CO2-浓度减小,第1、3、4个反
3 3
应是H+分别和OH-、CO2-、CH COO-结合成难电离物质
3 3
H O、H CO 、CH COOH(其中H CO 又分解成CO 和H O),
2 2 3 3 2 3 2 2
使H+和OH-、CO2-、CH COO-浓度减小(这四个反应中,
3 3
Na+、Cl-浓度均没有变化,实际上没有参与离子反应)。所
以,在溶液中发生的离子互换反应一般总是向离子浓度减
少的方向进行。
那么,反应物是难溶物质或弱电解质的离子互换反应
是否符合上述规律呢?
例如,醋酸跟氢氧化钠的中和反应:
CH COOH + NaOH CH COONa + H O
3 3 2
醋酸是弱电解质,在溶液中有如下平衡:
CH COOH CH COO- + H+
3 3
CH COOH电离出来的H+跟氢氧化钠电离的OH-生成
3
更弱的电解质H O,促使上述电离平衡向右移动,CH COOH
2 3
再电离出H+,继续跟OH- 结合。只要有足量的NaOH,
CH COOH的电离平衡向右移动的结果是几乎全部电离,也
3
就是反应完成,生成CH COONa和H O。反应中,CH COO-
3 2 3
离子浓度虽然增加,但由于H O比CH COOH更难电离,溶
2 3
液中OH-和H+离子浓度减少得多,反应向生成H O的方向
2
发生,所以这类反应也符合上述规律。
1 mL 1 mol/L
酸、碱、盐溶液中的离子互换反应 碳酸钠溶液
取3 mL 1 mol/L醋酸溶液,逐滴滴入1 mL 1 mol/L碳酸
钠溶液。
现象:________________________________________。 3 mL 1 mol/L
现根据第3.3节表3.6和表3.7醋酸、碳酸的电离常数数 醋酸溶液
值,用电离平衡移动的观点,讨论上述实验中的反应。 图 4.1 醋酸跟碳酸钠的反应
71从实验现象可知,发生了如下反应:
→
2CH COOH+Na CO 2CH COONa+CO ↑+H O
3 2 3 3 2 2
这一离子互换反应是否向有关离子浓度减少方向进行呢?
醋酸是弱电解质,在溶液中有如下电离平衡:
CH COOH CH COO- + H+
3 3
当加入碳酸钠后,因为CO2-跟H+结合成HCO-,HCO-
3 3 3
又跟H+结合成弱电解质H CO(H CO 分解成CO 和H O),
2 3 2 3 2 2
即:
资料库
CO2-+ H+ HCO-
3 3
能由弱酸——氢硫酸制 HCO-+ H+ H CO
3 2 3
得强酸——硫酸吗? H CO CO ↑+ H O
2 3 2 2
把硫化氢气体通入
硫酸铜溶液,能发生如下 由于H+浓度的减小,使CH COOH电离平衡向右移动,
3
反应: 直至反应完成,生成醋酸钠,并放出了二氧化碳,同时生成
CuSO + HS→CuS↓+HSO 了水。
4 2 2 4
显然HS酸性比HSO 醋酸、碳酸都是弱电解质,但从它们的K K K 的
2 2 4 i、 i1、 i2
弱,但反应还是发生了。 值看,碳酸是相对更弱的电解质,也就是说,醋酸的酸性比
这是由于H 2 S电离出来的 碳酸强。由于CH 3 COOH电离出来的H+比H 2 CO 3 电离出来
S2-(很少),但S2-跟Cu2+ 的H+ 多,平衡向生成H CO 方向移动,即反应向生成H CO
2 3 2 3
结合成极难溶于水的CuS
(CO 和H O)方向进行;相反,若把二氧化碳通入醋酸钠
2 2
沉淀,CuS在溶液中的溶
溶液不会生成醋酸。
解,其电离出来的S2-相对
通过以上讨论,对于酸跟盐的离子互换反应:
更小。因此反应还是向生
成CuS方向进行。
酸 + 盐 新酸 + 新盐
一般来说,总是由相对较强的酸生成相对较弱的酸。
同样,对于碱跟盐生成新碱和新盐的反应,一般来说
是由相对较强的碱生成相对较弱的碱。
72根据以下反应,比较有关酸和碱的强弱:
Na S + 2CH COOH 2CH COONa + H S↑
2 3 3 2
NH Cl + NaOH NaCl + NH·H O
4 3 2
AlCl + 3NH·H O Al(OH) ↓+ 3NH Cl
3 3 2 3 4
离子方程式
练 习
离子反应通常用离子方程式(ionic equation)来表示。
用实际参加反应的离子来表示离子反应的式子叫做离子方
写出下列反应的离
程式。 子方程式。
有的离子反应,可以先写化学方程式,再改为离子方 1. 硫酸中加入氯化
钡溶液。
程式。例如,硫酸和氢氧化钠的反应:
2. 硫酸钠溶液中加
入硝酸钡溶液。
H SO + 2NaOH Na SO + 2H O
2 4 2 4 2 3. 氯化铵溶液中加
入氢氧化钠溶液(加
离子方程式为: 热)。
4. 硫酸铵溶液加入
氢氧化钾溶液(加热)。
H+ + OH- H O
2
有的离子反应只能直接写离子方程式。例如,在Na+、
K+、CO2- 、Cl-的混合溶液中,滴加盐酸,发生H+跟CO2-
3 3
生成CO 和H O的反应。离子方程式为:
2 2
CO2- + 2H+ CO ↑+ H O
3 2 2
化学方程式只表示某一个反应,而离子方程式却表示
了某一类反应。如碳酸钠、碳酸钾等可溶性碳酸盐和盐酸、
硫酸等强酸反应,离子方程式均为上式。
由于离子方程式中删除了实际不参加反应的离子,因
此不仅要配平各种元素的原子数,还要使反应前后离子的
正电荷或负电荷总数相等。
73练 习
下列离子方程式是否正确,如不正确,请加以改正。
1. 碳酸钙跟盐酸反应:CO2-+2H+—→CO ↑+HO
3 2 2
2. 氯化铝溶液跟氨水溶液混合:Al3++3OH-—→Al(OH) ↓
3
3. 碳酸氢钙溶液中加入过量的氢氧化钠:
Ca2++HCO- +OH-—→ CaCO ↓+H O
3 3 2
4. 澄清石灰水中通入过量的二氧化碳:
Ca2++2OH-+CO —→ CaCO ↓+H O
2 3 2
离子方程式书写规律
(1)先写化学方程式(配平)。
(2)把反应物、生成物中 物质的化学式改为离子。
——————
(3)删去反应前后未变化的离子。
(4)检查反应前后原子个数和电荷数是否相等。
[课堂练习4.1]
1.以下反应中,属于离子反应的是( )。
①Fe O + CO ②CaCO + HCl ③H + O ④CuSO + Fe
2 3 3 2 2 4
(A)② (B)①② (C)②④ (D)①③
2.以下反应中,属于离子互换反应的是( )。
①NaOH + HCl ②NH HCO (加热) ③NH Cl + NaOH ④Cu + H SO (浓)
4 3 4 2 4
(A)①④ (B)①③ (C)①③④ (D)②④
3.下列情况能否发生反应,如能反应,写出有关离子方程式:
(1)碳酸钠溶液里加入石灰水。
(2)氯化钙溶液中通入二氧化碳。
(3)碳酸钡滴加盐酸。
(4)在盐酸、氯化钠混合溶液中滴加硝酸银。
(5)在碳酸钠、碳酸氢钠混合溶液中加入盐酸。
(6)碳酸氢铵溶液中加足量氢氧化钠(加热)。
4.以下离子方程式是否正确?如果正确,写明正确;如果不正确,请加以改正。
(1)碳酸氢钙溶液中加盐酸:CO2- + 2H+ —→ CO ↑+ H O
3 2 2
(2)硫酸铜溶液里加入氢氧化钡:Cu2+ + 2OH—→ Cu(OH) ↓
2
(3)碳酸钡加醋酸:BaCO + 2H+ —→ Ba2+ + CO ↑+ H O
3 2 2
(4)硫化亚铁中加稀硫酸:FeS + 2H+ —→ Fe2+ +H S↑
2
745.在50 mL 2 mol/L的氢氧化钠溶液中,通入1.12 L(标准状况)二氧化碳,写出发
生反应的离子方程式:______________。反应后溶液呈____性(填“酸”
“碱”或“中”),有关的离子方程式为__________;若再通入1.12 L(标准状况)
二氧化碳,反应的离子方程式为___________。
6.除去氢氧化钠溶液中少量的碳酸钠杂质,可以向溶液中加入适量的____(填化
学式),有关的离子方程式:_________ 。然后作_________操作,其_
________是较纯净的氢氧化钠溶液。
7.除去碳酸氢钠溶液中少量的碳酸钠杂质。甲、乙两学生各设计了以下方法:
甲学生:向溶液中加入适量的氯化钙,产生沉淀,然后滤去沉淀。
乙学生:向溶液中通入二氧化碳。
请回答:
(1)甲学生操作中有关的离子方程式:__________________。
(2)乙学生操作中有关的离子方程式:__________________。
(3)你认为_____方法比较合理,理由是_______________。
8.在SO 2- 、SO 2- 混合溶液中,加入硝酸钡溶液后,产生沉淀,有关的离子方程式为
4 3
_________,_________。再滴加硝酸,发现沉淀没有明显减少,其原因
是__________;若改为滴加盐酸,发现沉淀也没有明显减少,其原因是____
_____。
9.20 ℃时,氯化银、溴化银的溶解度分别为1.5×10-4 g/100 g水、8.4×10-6 g/100 g水,
试用离子互换反应发生的规律,分析以下两种情况,哪种能发生反应?
(1)氯化银中加溴化钠溶液。
(2)氯化钠溶液中加溴化银。
10.往磷酸钠溶液中加入足量盐酸,可发生如下反应:
Na PO +3HCl—→H PO +3NaCl
3 4 3 4
但把浓磷酸跟氯化钠固体混合后加热,又可发生如下反应:
△
H PO +NaCl—→NaH PO +HCl↑
3 4 2 4
请问为什么第一个反应是用盐酸制磷酸,而第二个反应却能用H PO 制HCl?
3 4
(提示:注意反应物HCl和生成物HCl的状态。)
75氧化还原反应
4
.2
(OXIDATION-REDUCTION REACTION)
在化学反应中,有电子转移(得失或偏移)的反应是氧
化还原反应,这是一类重要的化学反应。氧化还原反应的
发生有什么规律呢?怎样判断氧化剂的氧化能力或还原剂
的还原能力的强弱呢?本节将学习这一类反应的规律。
另外,由于氧化还原反应中有电子转移,不但可以实
现化学能与电能的相互转换,而且还与有原电池作用的金
属电化腐蚀以及电解等有关。本节还将从氧化还原的角度
来认识钢铁电化腐蚀的本质,并利用电化学知识来解决金
属防腐问题。
氧化剂与还原剂
在氧化还原反应中,得到电子的物质叫做氧化剂
(oxidizing agent),失去电子的物质叫做还原剂(reducing
agent)。
练 习
1.把浓盐酸氧化为氯气,找出两种适宜的氧化剂,并写
出化学方程式。
(1)氧化剂_____,
化学方程式_________________。
(2)氧化剂_____,
化学方程式_________________。
2.把溶液中的铜离子还原为金属铜,找出两种适宜的还
原剂,并写出有关的离子方程式。
76(1)还原剂_____,
离子方程式_________________。
(2)还原剂_____,
离子方程式_________________。
归纳填写表4.2:
表 4.2
比较的栏目和举例 氧化剂 还原剂
电子得失
化合价变化
表现出何种性质
自身发生何种反应
常见氧化剂或还原剂
(各举3种)
上述练习中,可以按金属活动性顺序表找出还原剂金
属锌或铁,排在铜后的金属银则不能还原铜离子。
现在我们从还原剂、氧化剂的强弱来分析锌跟铜离子
的反应:
2e
Cu2+ + Zn —→ Cu + Zn2+
在反应中,反应物Zn是还原剂,Cu2+是氧化剂;生成
物Cu是Cu2+还原反应后的产物,简称还原产物(具有还原
性),Zn2+则是氧化产物(具有氧化性)。
比较Zn、Cu的还原性强弱和Cu2+、Zn2+氧化性强弱,
可以得到:
还原性:Zn > Cu 氧化性:Cu2+ > Zn2+
如果我们用下列式子表示一个氧化还原反应:
用氧化剂、还原剂的
强弱说明金属Ag不能还
氧化剂 + 还原剂 还原产物 + 氧化产物
原Cu2+生成Cu的原因。
(提示:如果Ag跟
可以发现,一个自发的氧化还原反应,必定是氧化剂
Cu2+反应,则生成Ag+和
的氧化能力比氧化产物强,还原剂的还原能力比还原产物 Cu,通过比较Ag、Cu的
强。即氧化还原反应,总是氧化性较强的氧化剂和还原性 还原性强弱和Cu2+、Ag+
的氧化性强弱来回答。)
较强的还原剂反应,向生成还原性相对较弱的还原产物和
氧化性相对较弱的氧化产物的方向进行。
77练 习
_
1.已知:2Fe3+ + Cu → 2Fe2+ + Cu2+反应能进行。
其中,氧化剂是____,还原剂是____,还原产
物_____,氧化产物_____。
有关物质的氧化性_____>_____,还原性__
___>_____。
比较Cu2+、Fe3+、Fe2+三种离子的氧化性强弱顺序___
____________。
2.在淡黄色的氯化铁溶液中加入足量的还原铁粉反复振
荡后,溶液逐渐变为浅绿色,生成氯化亚铁。
反应的离子方程式________________,
其中,氧化剂_____,还原剂______,还原产物
______,氧化产物______,转移0.5mol电子时,
能生成_____molFe2+。
氧化还原反应化学方程式的配平
简单的氧化还原反应的化学方程式可以用观察的方法
加以配平。复杂的则要用化合价法来配平,原则是氧化剂
和还原剂得失电子的总数相等,表现为元素的化合价升高
和降低的总数相等。
示例:配平以下化学方程式。
_H O +_KMnO +_H SO —→__K SO +_MnSO +_O +_H O
2 2 4 2 4 2 4 4 2 2
配平步骤:
1.列出化合价的变化:
-1 +7 +2 0
_H O +_KMnO +_H SO —→_K SO +_MnSO +_O +_H O
2 2 4 2 4 2 4 4 2 2
↑
1×2
↓
5
还原剂H O 下方的“↑1×2”表示2个O原子的化合
2 2
价从-1上升为0,共上升2;氧化剂KMnO 下方的“↓5”
4
表示1个Mn原子的化合价从+7降低为+2,降低5。
2.用化合价升高和降低总数相等,配上氧化剂、还原
剂、还原产物(MnSO )、氧化产物(O )前的化学计量数。
4 2
_5 HO +_ 2 KMnO +_HSO —→ _KSO +_ 2 MnSO +_ 5 O +_HO
2 2 4 2 4 2 4 4 2 2
↑
1×2×5
↓
5×2
783.用观察的方法配平其他物质的化学计量数。
_5 H O + _2 KMnO +_ 3 H SO —→_ 1 K SO + _2 MnSO + _5 O + _8 H O
2 2 4 2 4 2 4 4 2 2
资料库
用氧化数法配平化学方程式
在某些化合物中,确定元素的化合价比较困难,如Fe O 、Fe C、CH CH OH
3 4 3 3 2
等,化学上通常用氧化数来代替化合价。
元素的氧化数确定原则除可以出现分数数值和“平均”概念外,与化合价大
体相同。如单质中元素的氧化数为0;离子化合物中,阴、阳离子的电荷数就是
元素的氧化数,阴离子的为负,阳离子的为正;共价化合物中,共用电子对偏出
的为正,偏进的为负,偏出1对为+1,2对为+2,偏进1对为-1,2对为-2。化
合物中各元素氧化数代数和为0。
在简单的化合物中,元素的化合价和氧化数相同。复杂的化合物可根据通
常由不变氧化数的元素(如Na+1、Mg+2、F-1、H+1或O-2等)来计算其他
元素的氧化数。如Fe O 中,根据氧的氧化数为-2,推求铁的氧化数(设为x),
3 4
8
3x+(-2)×4=0,x=+—。又如Na S O 中,推求硫的氧化数(设为x),+1×2+2x+
3 2 2 3
(-2)×3=0,x=+2。
用氧化数法同样可配平氧化还原反应化学方程式,依据是氧化数升高和降低
总数相等。
例如:配平_Fe O +_HNO —→_Fe(NO ) +_NO+_H O
3 4 3 3 3 2
配平步骤:
1.标出氧化数的变化:
+—8
+5 +3 +2
3
Fe O + HNO —→Fe(NO ) +NO+H O
3 4 3 3 3 2
↑1 ↓
—×3 3
3
2.根据氧化数升高和降低总数相等,配上氧化剂、还原剂以及还原产物、氧
化产物的化学计量数。
3Fe O +1HNO —→9Fe(NO ) +1NO+H O
3 4 3 3 3 2
↑1 ↓
—×3×3 3×1
3
3.若氧化剂、还原剂还起其他作用,则化学计量数要作某些调整。
1mol HNO 氧化3mol Fe O 生成9mol Fe(NO ) ,HNO 还要增加(9×3)
3 3 4 3 3 3
mol,以配合生成9mol Fe(NO ) 的需要(即HNO 还起酸性作用)。
3 3 3
3Fe O +(1+27)HNO —→9Fe(NO ) +1NO+H O
3 4 3 3 3 2
4.最后配平其他化学计量数。
3Fe O +28HNO —→9Fe(NO ) +1NO+14H O
3 4 3 3 3 2
79练 习
用化合价法配平以下化学方程式。
1._Zn+_HNO (极稀)—→_Zn(NO ) +_NH NO +_H O
3 3 2 4 3 2
(提示:HNO 起氧化剂作用外,还起酸的作用。)
3
2._HCl+_KMnO —→_KCl+_MnCl +_Cl +_H O
4 2 2 2
(提示:HCl起还原剂作用外,还起酸的作用。)
钢铁的电化腐蚀和电化学保护
钢铁容易腐蚀,全世界每年被腐蚀的钢铁达上亿吨,损
失巨大。其中,最主要是电化学腐蚀。电化学腐蚀是具有原
电池作用过程的一种腐蚀。
电流计
G
Zn Cu-Zn原电池
Cu
如图4.2装置:
现象:_____,_____,_____。
化学过程:
负极( ):电极反应式:______(__反应);
正极( ):电极反应式:______(__反应),
总化学方程式:____________。
稀硫酸
导线中电子流动方向:从__极到__极。
图 4.2 Cu-Zn原电池
1.图4.3的装置(a),铁片浸在稀硫酸中,现象____
___,写出反应的离子方程式_________。
2.图4.3的装置(b),将铁片和石墨棒浸在稀硫酸中,
用导线相连,导线中接有灵敏电流计,组成一个Fe-C原
电池。
现象:__________________。
铁片是__极,电极反应式:__________,
发生____反应。
石墨棒是__极,电极反应式:_________,
发生____反应。
总反应方程式:_______________。
803.图4.3,装置(a)、(b)中稀硫酸浓度相同,那么,装置
(b)中铁的腐蚀速率比装置(a)的铁的腐蚀速率_____(填
“大”或“小”),原因是 _______________。
电流计
G
Fe
C
稀硫酸
(a) (b)
图 4.3 原电池示意图
从反应的结果看,装置(a)、(b)中的反应是完全相同的。
在装置(b)的原电池中,由于作为负极的铁不断地失去电子,
通过导线流向作为正极的石墨,加快了铁的腐蚀。这一结
论将帮助我们理解电化学腐蚀(electrochemical corrosion)
和电化学保护(electrochemical protection)。
钢铁的电化学腐蚀是在潮湿的环境中发生的,在潮湿
情况下钢铁表面吸附有一层水膜,水膜里溶有氧气和二氧
化碳,可起电解质溶液的作用。钢铁又是铁-碳合金,于
是,构成了数量巨大的铁为负极、碳为正极的微小原电池。
在负极Fe上的电极反应是:
Fe - 2e —→ Fe2+(氧化反应)
在正极C上的反应有两种情况,当水膜的酸性较大时,
则溶液中H+得到电子,析出氢气,这叫析氢腐蚀(图4.4)。
2H+ + 2e —→ H(还原反应)
2
电解质溶液
Fe2+
H+ H
2
C
Fe e
图 4.4 钢铁析氢腐蚀示意图
81当水膜的酸性较弱或呈中性时,就由水膜中氧气得到
电子,这叫吸氧腐蚀(图4.5)。
为什么钢铁的电化
学腐蚀比干燥条件下的
一般化学腐蚀要快得 O + 2H O + 4e —→ 4OH-(还原反应)
2 2
多?
O
2
电解质溶液
Fe2+
OH-
e C
Fe
图 4.5 钢铁吸氧腐蚀示意图
在电化学腐蚀中,主要是吸氧腐蚀。
钢铁防腐有许多方法,如表面电镀、涂油漆、研制不锈
钢等。此外,对于经常处于潮湿环境中的大型钢铁设备,如
轮船外壳、河道闸门、地下铁管等,还要采取电化学保护法
来防护。
电化学保护法有两种。一种是外加电流阴极保护法。如
图4.6所示,将钢铁闸门与外加电源负极相连,钢铁闸门为
阴极,外加电源正极再连接一个辅助阳极。只要外加电源
有足够的电压,钢铁腐蚀产生的原电池电流就无法输送,因
此电化学腐蚀被抑制。
另一种是牺牲阳极阴极保护法。如图4.7所示,在轮船
船壳上连接一定数量的锌块,由于锌的还原性比铁强,故
当发生腐蚀时,由锌来代替铁受腐蚀。锌发生氧化反应称
为阳极。这种方法叫牺牲阳极阴极保护法。
- +
e e e e
钢 轮
闸 船
门 船
(阴 海水 壳 Zn2+
极
(阴
) 辅助阳极 极 锌板
)
(不溶性) (牺牲阳极)
图 4.6 外加电流阴极保护法示意图 图 4.7 牺牲阳极阴极保护法示意图
82[课堂练习4.2]
1.现有以下物质(分子或离子):Na、Zn、S、F 、Fe3+、Fe2+、SO 、H O 。
2 2 2 2
其中,只具有氧化性的是_____,只具有还原性的是_____,既具有氧化性又
具有还原性的是_____。
2.以下物质中,通常用作氧化剂的是_____,通常用作还原剂的是____。
C、KMnO (H+)、浓硫酸、H S、H 、Cl 、O 、HNO 。
4 2 2 2 2 3
3.以下情况能否发生反应?试用氧化还原反应发生的规律加以分析,并写出有关的离
子方程式。
(1)氯化钠溶液中滴入溴水_________________________。
(2)碘化钠溶液中滴入溴水_________________________。
4.已知酸性高锰酸钾能氧化氯离子,离子方程式如下:
10Cl-+2MnO-+16H+—→2Mn2++5Cl +8H O
4 2 2
试回答:
(1)该反应的还原产物是_____,氧化产物是_____。
(2)该反应能发生,则氧化性:_____ > _____。
(3)生成0.5mol氯气,则转移____mol电子,消耗____mol H+。
5.配平下列化学方程式:
(1)_HNO(浓)+_Cu—→_Cu(NO ) +_NO +_H O
3 3 2 2 2
(2)_FeSO +_KMnO +_H SO —→_Fe (SO ) +_MnSO +_K SO +_H O
4 4 2 4 2 4 3 4 2 4 2
(3)_Fe2+ +_MnO- +_H+—→_Fe3+ +_Mn2+ +_H O
4 2
(4)_KOH+_Cl —→_KClO +_KCl+_H O
2 3 2
6.(1)钢铁腐蚀一般有化学腐蚀和电化学腐蚀,其主要是_____;电化学腐蚀有
析氢腐蚀和吸氧腐蚀,其主要是_____。
(2)钢铁电化学腐蚀时,如果表面吸附的水膜呈中性或酸性较弱,但只要有氧气存在,
铁会被腐蚀,这种腐蚀叫_____腐蚀。此时,铁作为_____极,铁中含有碳作为_
____极,氧气在_____极还原为_____离子;如果水膜酸性比较强,尽管缺氧
也会腐蚀,这种腐蚀叫_____腐蚀。水膜里的_____离子在炭极上还原为____。
7.通常纯锌跟稀硫酸反应的速率很慢,而不纯的锌(一般含有铁、铜等杂质)反应速
率快,试从原电池作用来解释这一现象。
(提示:含杂质的锌跟酸反应时有原电池作用,锌作负极,比锌不活泼的杂质作正极。)
8.根据下列发生的反应:
Fe+Cu2+ —→Fe2++Cu
2Fe2++Cl —→2Fe3++2Cl-
2
Cu+2Fe3+—→Cu2++2Fe2+
83(1)试判断Fe2+、Fe3+、Cu2+、Cl 氧化性的强弱。
2
(2)判断Fe与Fe3+能否反应,若能反应,试写出有关的离子方程式。
(3)试分析化学方程式 2Fe+3CuCl —→2FeCl +3Cu的错误所在。
2 3
9.镀锌铁皮(白口铁)和镀锡铁皮(马口铁)的镀层破损后,哪一种铁皮更易发
生腐蚀?试从原电池作用原理加以分析。
10.用五种金属A、B、C、D、E进行如下实验。
(1)由A、B两种金属和稀硫酸组成原电池,电流从A极流出。
(2)金属C能从溶液中置换出金属D。
(3)电解含有A、C两种离子的溶液时,阴极上首先析出金属C。
(4)把B、E两种金属放入水中,E能发生反应产生氢气,而B则不能。
试比较这五种金属的活动性强弱:____________________。
84小 结
1.离子互换反应及其离子方程式要点。
(1)溶液中通过离子(离子和离子、离子和原子、离子和分子)进行的反应叫离子反
应,离子反应有离子互换反应(如复分解反应)和离子氧化还原反应两种情况。
(2)离子互换反应一般是向溶液中有关离子的浓度减少(生成弱电解质、难溶性物质或
挥发性物质)的方向进行。
(3)用实际参加反应的离子符号来表示离子反应的式子叫离子方程式,离子方程式可表
示所有同一类型的离子反应。
2.氧化还原反应和电化学腐蚀要点。
(1)在氧化还原反应中,氧化剂发生还原反应,生成还原产物,还原剂发生氧化反应,
生成氧化产物。
氧化剂 + 还原剂 —→ 还原产物 + 氧化产物
如果氧化剂的氧化能力比氧化产物强,还原剂的还原能力比还原产物强,那么该氧化还
原反应就能自发进行。
(2)氧化还原反应配平的依据是化合价升高总数和化合价降低总数相等。
(3)钢铁腐蚀主要是电化学腐蚀,电化学腐蚀是具有原电池作用的一种腐蚀,电化学腐
蚀有析氢腐蚀和吸氧腐蚀两种,主要是吸氧腐蚀。
3.阅读下面英文,你会对氧化还原有较好理解。
Today the words oxidation and reduction have severaltions. Originally,however, oxidation was
used to descriptions in which oxygen was added to a reactant. For exampformation of rust is an
oxidation reaction in which iron metal reacts with oxygen in the presence of water to form rust, or
iron oxide.
4Fe(s) +3O (g) —→ 2Fe O (s)
2 2 3
Similarly, when methane gas (CH)burns, it combines with oxygen to form carbon dioxide and
4
water.
CH (g) +2O (g) —→ CO (g)+2H O(l)
4 2 2 2
The term reduction at first meant the removal of oxygen form a compound. For example, the
Fe O in iron ore can be reduced to obtain iron metal. You may remember that this is normally
2 3
accomplished inside a blast furnace by heating the iron oxide in the presence of carbon.
2Fe O (l) +3C(s) —→ 4Fe(l)+3CO (g)
2 3 2
85The term reduction comes from the fact that the free metal has a lower mass than its oxide
compound. Thus there is a decrease, or reduction, in the mass of the iorn-containing material as the
oxygen is removed.
The words oxidation and reduction are still used to describe the addition or removal of oxygen.
But chemists today use the terms in a much broader way. The broader definitions arise from the fact
that oxygen is very electronegative and tends to gain electrons when it reacts with other substances.
For example, the reaction of magnesium with oxygen produces MgO, an ionic compound containing
Mg2+ ions.
2Mg(s) +O (g) —→ 2MgO(s)
2
You should know that in going from Mg to Mg2+, a magnesium atom loses 2 electrons. Similar
analyses of other oxidation reactions reveal that substances that are oxidized lose electrons. On the
other hand, substances that are reduced gain electrons. Thus it is convenient to define oxidation and
reduction in terms of the movements of electrons.
·Oxidation is the process by which a substance loses one or more electrons.
·Reduction is the process by which a substance gains one or more electrons.
865
非金属元素
NONMETALLIC ELEMENTS
在人类已经发现的一百多种元素中,
大部分是金属元素,小部分是非金属元素。
如果沿着周期表中硼、硅、砷、碲、砹跟
铝、锗、锑、钋之间划一条虚线,虚线的
左面除氢外是金属元素、右面是15种非金
属元素和6种稀有气体元素。虽然非金属
元素的种类只约占六分之一,但它们的单
质和化合物种类繁多、性质形状各异,为
人类提供生活、生产、科学研究所必需的
大量物质。
非金属元素是如何组成单质和化合物
的呢?它们在结构和性质上有什么样的规
◆ 非金属单质的结构和性质
律?掌握了这些规律,既可以更好地使它
们为人类所利用,又可以防止它们对于人 ◆ 卤素、硫、氮、碳的一些化合物
类可能造成的危害,还可以科学合理地去
◆ 烧碱、纯碱的制取和化工生产
创造人类所需的物质,合理利用资源,节
的一些基本原理
约成本,与环境和谐相处,这些都是我们
通过对物质结构、性质的学习,进一步要
认识和研究的问题。
87
0812896-05-OK Page 87 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC非金属单质
5
.1
(NONMETALLIC ELEMENTS)
结构和物理性质
氢气(H )、氧气(O )、溴(Br )、磷(P)、硫(S)
2 2 2
等,都是我们熟悉的非金属单质。非金属元素的单质分子
大多是由两个或两个以上的原子以共价键结合而成的。第
ⅦA族单质都是由两个原子以一个共价键结合而成的双原
子分子;第ⅥA族和第ⅤA族的元素中,处于第二周期的
氧和氮,它们的单质为共价键结合的双原子分子,第三、四
练 习 周期的非金属元素(如S、Se、P、As等)的单质,是由
共价键结合而成的多原子的分子,如S 、P 等,通常我们
8 4
非金属元素构成的
用S和P来表示单质硫和磷;第ⅣA族非金属单质金刚石
单质晶体,有哪些晶体
和晶体硅都属于原子晶体,在这些晶体中,原子通过共价
类型?指出构成这些晶
体基本微粒和这些微粒 键而结合成巨大的分子。
之间作用力的名称。
(a) (b)
(c)
图 5.1 臭氧、斜方硫(S ,rhombic sulfur)、
8
白磷(P ,white phosphorus)的分子结构
4
88
0812896-05-OK Page 88 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC表5.1 非金属单质的分子类型、晶体结构
化学键 形成晶体 晶体的 晶体中结构微粒
分子类型 实 例
类型 的类型 结构微粒 间的作用力
单原子分子 /
氯气、溴
多原子分子
金刚石
晶体硅
一种元素可以形成几种结构不同的单质。碳元素的单
质有金刚石、石墨和富勒烯等。同种元素形成的不同单质,
互称为同素异形体(allotrope)。氧、硫、磷等元素都能形
成同素异形体。
练 习
下列各组物质中,哪些是同素异形体?
(1) 39K和40K (2) H 和D
19 19 2 2
(3) 氧气和臭氧 (4) S 和S
4 8
化学性质
非金属单质参加的反应,绝大多数是氧化还原反应,发
生反应的情况与构成它们的原子的最外层电子构型、原子
半径及非金属单质的结构等有关。
除氢和稀有气体元素外,非金属元素的最外层电子排
布均为ns2np1~5,相对于同周期的金属元素,它们的原子半
径小,价电子多,在反应中倾向于得电子,其单质多显示氧
化性。但有些非金属的单质在反应中显示还原性。同一种
非金属元素的原子,得失电子的数目也可能有差异。大多
数非金属元素所显示的化合价是可变的。
89
0812896-05-OK Page 89 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC资料库
表5.2 常见非金属元素的化合价
族 ⅢA ⅣA ⅤA ⅥA ⅦA
元 素 B C Si N P As O S Se Te F Cl Br I
-4 -4 -3 -3 -3 -2 -2 -2 -2 -1 -1 -1 -1
+2 +1 +1 +1 +1
主要 +4 +4 +2 +4 +4 +4 +3 +3 +3
化合价
+3 +3 +3 +3 +5 +5 +5
+4 +6 +6 +6 +7 +7 +7
+5 +5 +5
非金属单质具有相似的化学性质,除稀有气体外, 非金
属单质一般都能与金属、氢气、氧气、水及某些化合物发生
反应。
(一)跟金属的反应
氯气是强氧化剂,能跟大多数金属反应生成高价的金
属氯化物;硫是弱氧化剂,能跟铁、铜等金属反应生成较低
价态的金属硫化物。
课堂实验
铜和氯、硫的反应
将细铜丝烧热后插入集有氯气的集气瓶中。
可以观察到:________________________________________________。
发生的反应是:______________________________________________。
在一个较短的试管中加入少量硫粉,加热,出现硫蒸气时,将烧热的细
铜丝插入硫蒸气中。
可以观察到:________________________________________________。
发生的反应是: _______________________________________________。
不活泼的非金属单质氮和硅,也能跟活泼的金属反应。
镁带在空气中燃烧,除生成氧化镁外,还生成氮化镁:
90
0812896-05-OK Page 90 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC点燃 练 习
3Mg+N Mg N
2 3 2
试比较氯气、氧气、
一般地说,元素的非金属性越强,其单质的氧化性也 硫分别在一定条件下与
越强,也越容易和金属发生反应。 铁的反应,写出反应的
化学方程式。
(二)跟氢气的反应
非金属单质在不同的条件下能与氢气发生反应。
同周期非金属元素的单质与氢气的反应情况与元素的
非金属性有关,元素非金属性越强,它的单质与氢气就越
容易发生反应,生成的气态氢化物也越稳定。如,第三周期
的非金属元素硅、磷、硫、氯,其中,硫在加热的条件下与
氢气缓慢化合。
△
H + S H S
2 2 比较卤素单质与氢
气反应的条件、反应的热
硅和磷是不能与氢气直接化合的,用间接方法制得的 效应及生成气态氢化物
的稳定性。
甲硅烷(SiH )和磷化氢(PH ),它们都易分解,在空气中
4 3
能自燃。
(三)跟氧气的反应
非金属单质碳、硅、氮、磷、硫,在一定条件下都能跟
练 习
氧气反应。
碳在空气或氧气中燃烧,可能生成二氧化碳,也可能 碳与氧气反应分别
生成一氧化碳。 在什么样的条件下生成
二氧化碳和一氧化碳?
氮气与氧气要在放电的条件下才能发生反应。
怎样使二氧化碳与一氧
化碳相互转化?写出反
放电
N + O 2NO
2 2 应的化学方程式。
无色的一氧化氮气体遇氧气又立即生成红棕色的二氧
化氮气体,二氧化氮又部分转变为四氧化二氮,二氧化氮
还能与水发生反应生成硝酸和一氧化氮。
夏天雷雨中存在的
稀硝酸是怎样产生的?
2NO + O 2NO
2 2
2NO N O
2 2 4
3NO + H O 2HNO + NO
2 2 3
91
0812896-05-OK Page 91 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC课堂实验
氮氧化物和氧气及水的反应
1.
NO O
2
20mL 10mL
图 5.2
如图5.2,一个针筒内装有10mL氧气,将氧气慢慢地推入到装有20mL
一氧化氮气体的另一个针筒中。
观察到:____________________________________________________。
原因是:____________________________________________________。
2.
NO HO
2 2
30mL 10mL
图 5.3
如图5.3,一个针筒内装有约10 mL水,将水慢慢地推入到装有30mL
红棕色的二氧化氮气体的另一个针筒中。
观察到_____________________________________,装气体的针筒中剩
余的气体是___________,体积大小的范围为______________________。
非金属单质与氧气反应时,由于单质的结构不同,反
应所需要的条件也不同,如白磷的着火点是40 ℃,而红
磷的着火点却是240 ℃。白磷和红磷燃烧后都生成五氧
化二磷。
探究与实践
比较白磷、红磷的着火点
请设计一个实验,以证明白磷的着火点远比红磷要低,并完成这个实验。
92
0812896-05-OK Page 92 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC(四)跟化合物的反应
许多非金属单质不与水反应,如氢气、氮气、硫等。氟
试从氧化还原反应
气则与水剧烈反应放出氧气。
程度、反应后溶液的组成
等方面来比较氟气、氯气
2F + 2H O 4HF + O 与水的反应,并推断溴、
2 2 2
碘单质能否分别与水发
生反应以及反应的程度
碳在高温下与水反应生成的混合气体称为水煤气,这
如何。
是工业上获得氢气的方法之一。
高温
C + H O CO + H
2 2
卤素、硫、磷等能分别与强碱溶液反应。非金属单质在
反应中既可作氧化剂,又可作还原剂。例如:
练 习
Cl + 2NaOH NaCl + NaClO + H O
2 2 推断硫与热的氢氧
3Cl + 6NaOH(热溶液) 5NaCl + NaClO + 3H O
2 3 2 化钾反应的产物是什
么?试写出该反应的化
非金属单质发生氧化还原反应时,由于反应条件不同, 学方程式。
反应的产物也可能不同。
[课堂练习5.1]
1.非金属单质的晶体类型是( )。
(A)离子晶体 (B)原子晶体 (C)分子晶体 (D)金属晶体
2.熔沸点很高的非金属单质的晶体中,基本微粒是( )。
(A)离子 (B)原子 (C)分子 (D)电子
3.熔沸点较低的非金属单质的晶体中,基本微粒间的作用力是( )。
(A)共价键 (B)离子键 (C)金属键 (D)分子间作用力
4.下列化合物可由两种单质直接化合得到的是( )。
(A)二氧化氮 (B)二氧化硫 (C)三氧化硫 (D)氯化亚铁
对用两种单质反应生成该化合物的反应,用氧化还原的原理作分析,并对这两个
反应物及对应元素作出有关比较。
5.在非金属单质参加的氧化还原反应中,反应剧烈程度、反应所需条件、反应的
热效应等主要与什么因素有关?还与哪些因素有关?试举例说明。
93
0812896-05-OK Page 93 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC一些非金属化合物
5
.2
(SOME NONMETALLIC COMPOUNDS)
卤化氢
卤化氢(hydrogen halide)在常温下都是无色有刺激气
味的气体,都易溶于水,在空气中与水蒸气形成酸雾,它们
溶于水生成氢卤酸。在氢卤酸中氢氟酸是弱酸,盐酸、氢溴
酸、氢碘酸都是强酸。
资料库
氟化氢熔沸点高的原因
表5.3 卤化氢的熔点和沸点
物质
HF HCl HBr HI
性质
沸点(K) 292.67 188.11 206.43 237.80
熔点(K) 189.61 158.94 186.28 222.36
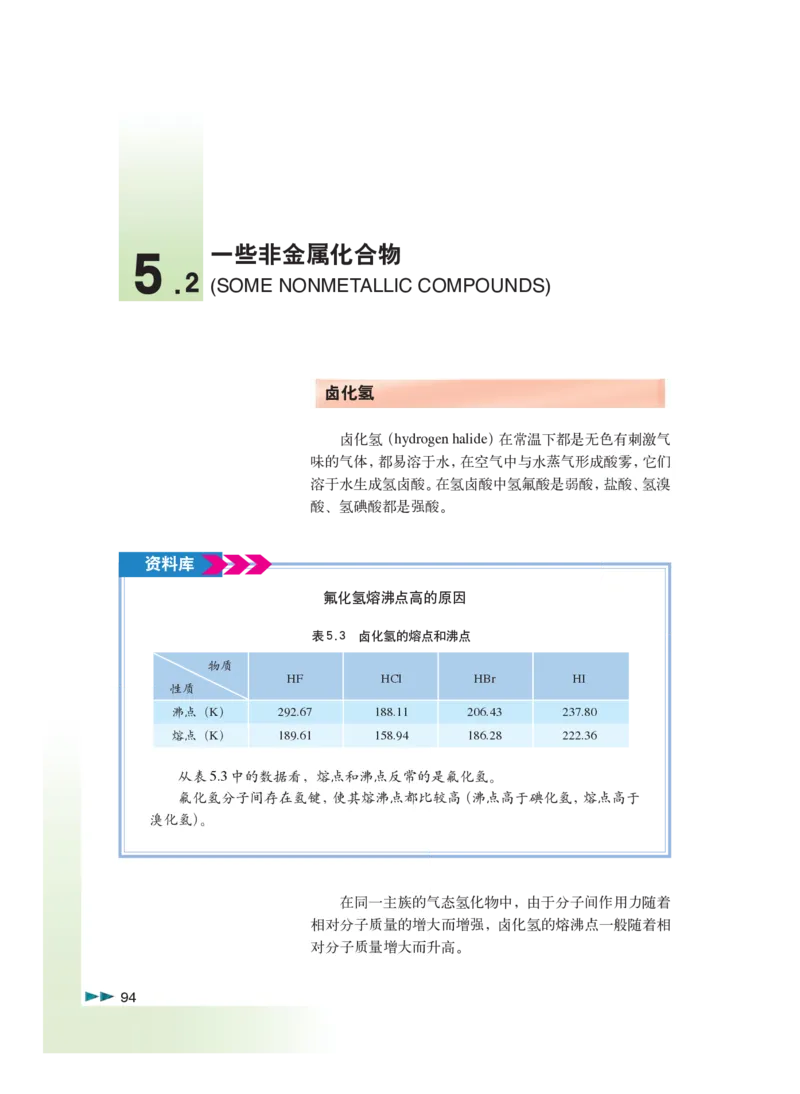
从表5.3中的数据看,熔点和沸点反常的是氟化氢。
氟化氢分子间存在氢键,使其熔沸点都比较高(沸点高于碘化氢,熔点高于
溴化氢)。
在同一主族的气态氢化物中,由于分子间作用力随着
相对分子质量的增大而增强,卤化氢的熔沸点一般随着相
对分子质量增大而升高。
94
0812896-05-OK Page 94 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC试根据元素周期律的理论,比较卤化氢热稳定性的大小。
表5.4 氢卤共价键的键能
共价键 H-F H-Cl H-Br H-I
键能
570.30 431.62 366.35 297.41
(kJ/mol)
卤化氢的热稳定性与氢卤共价键的键能有什么关系?而氢
卤共价键的键能的大小与卤素原子的结构又有什么样的关系?
卤化氢的热稳定性是HF > HCl > HBr > HI。
实验室里可用氯化钠与浓硫酸反应制取氯化氢气体。
可用萤石(CaF )与浓硫酸反应制取氟化氢。
2
CaF + H SO (浓) △ CaSO + 2HF↑
2 2 4 4
因为氢氟酸会腐蚀玻璃,因此反应须在铅制器皿中进
行,氢氟酸应保存在塑料瓶中。
课堂实验
用浓硫酸能制备溴化氢吗?
使用实验室制氯化氢气体的装置,在圆底烧瓶中装入溴化钠,将分液漏
斗中装有的浓硫酸滴入圆底烧瓶,加热进行反应。
观察到:____________________________________________________。
试分析产生现象的原因是:____________________________________
___________________________________________________________________。
(提示:此类实验宜在通风柜中进行。因生成的溴化氢是具有刺激性气
味的有毒气体,应用适当的方式吸收。)
从实验事实和理论推断都可得出,卤化氢的还原性是
为什么浓硫酸分别
HI > HBr > HCl > HF。
与氯化钠、溴化钠反应的
情况会不同?推断碘化
钠与浓硫酸反应能不能
制得纯的碘化氢气体?
说明理由。
95
0812896-05-OK Page 95 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC资料库
表5.5 卤化氢的一些性质的比较
硫化氢有毒 熔 点
硫化氢能使人的中枢 沸 点
神经麻痹;与呼吸酶中的 稳定性
铁质结合,使酶的活动性 还原性
减弱,影响呼吸;它侵入 水溶液的酸性
黏膜会形成有强烈刺激
作用的硫化物。空气中硫
化氢气体的含量不得超
过0.01 mg/L,当硫化氢含 硫的氢化物和氧化物
量较多时,就会迅速使人
感到头疼、恶心、呕吐;
(一)硫化氢
吸入量大时,会使人丧失
在自然界,火山喷发物、有些油气井喷出的气体中,都
意识、昏迷,直至死亡。常
含有硫化氢;动植物及有机垃圾腐烂,也会产生硫化氢。工
接触硫化氢,可引起人的
业上精炼石油,农业上有机肥腐殖,也都有硫化氢逸出而
感官麻痹而难闻到它的气
污染大气。
味,这是十分危险的。
硫化氢是无色有腐卵臭味的气体,有毒,比空气重。实
验室制取和使用硫化氢时要注意通风。
课堂实验
硫化亚铁和酸的反应
在配有带玻璃导管的单孔塞的大试管中,加入几粒硫化亚铁,再加入少
量稀盐酸或稀硫酸,塞紧塞子并把玻璃导管放到酒精灯火焰中。待管口出现
火焰时,先用湿润的品红试纸放到火焰上方检验,再用蒸发皿底压灭火焰。
观察到:______________________________________________________。
在整个实验过程中,发生的反应有:_____________________________
_______________________________________________________________________
_________________________________________________________________。
可得出硫化氢的化学性质:______________________________________
______________________________________________________________________。
96
0812896-05-OK Page 96 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC硫化氢受热会分解:
△
H S H + S
2 2
常温下,1体积水可溶解约2.5体积的硫化氢,硫化氢
的水溶液称为氢硫酸。氢硫酸是弱酸,具有酸的通性。
氢硫酸与某些盐反应,生成的硫化物若不溶于对应的
酸,则反应可以完成。
H S + Pb(NO ) PbS↓+ 2HNO
2 3 2 3
H S + (CH COO) Pb PbS↓+ 2CH COOH
2 3 2 3
硫化铅呈黑色,因此可以用可溶性铅盐的溶液或试纸
来检验硫化氢。实验室中,也可以用硫酸铜溶液来检验或
吸收硫化氢。
CuSO + H S CuS↓+ H SO 在城市的地下管道
4 2 2 4
中,有时会聚集浓度较大
的硫化氢。在进入管道工
除硫化铅外,硫化铜、硫化银等也是黑色的不溶于一
作的施工规则中,应写入
般酸的固体。
怎样的操作要求,才能确
氢硫酸具有很强的还原性,敞开在空气中极易氧化而
保安全?
析出硫,使溶液变浑浊。
2H S+O 2H O+2S↓
2 2 2
练 习
(二)硫的氧化物
硫的氧化物有二氧化硫和三氧化硫。
试说出二氧化硫的
酸性氧化物三氧化硫是一种易挥发的无色晶体,熔点 物理性质和化学性质。
16.8℃,沸点44.8℃。它极易吸水,在空气中冒出强烈的白 二氧化硫对环境有什么
影响?
雾。容易与碱性氧化物、碱反应生成硫酸盐。
97
0812896-05-OK Page 97 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC图 5.4 大气地面自动监测站及时公布SO 等有害气体的含量
2
二氧化硫中的硫元素显示+4价,升高可变为+6价,降
低可变为0价,因此,二氧化硫除具有酸性氧化物的通性及
漂白性外,还具有既能被氧化又能被还原的性质。
课堂实验
硫化氢和二氧化硫的反应
1.将分别集有硫化氢气体和二氧化硫气体的集气瓶,对扣在一起,抽
去毛玻璃片,并上下倒转几次。
观察到:____________________________________________________。
发生的反应为:______________________________________________。
2.将二氧化硫气体慢慢通入到溴水中(尾气用氢氧化钠溶液吸收)。
观察到:____________________________________________________。
发生的反应为:______________________________________________。
结论:______________________________________________________。
1. 分析上述实验中二氧化硫所显示的性质。
2. 除二氧化硫外,我们学过的哪些物质也有漂白性?它
们的漂白作用有什么不同?
98
0812896-05-OK Page 98 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC硝酸和硝酸盐
(一)硝酸
硝酸是一种强酸,它除了具有酸的通性外,还有它本
身的特性:不稳定性与强氧化性。
久置的浓硝酸呈浅
黄色的原因是什么?浓
4HNO 光 4NO ↑+ O ↑+ 2H O
3 2 2 2 硝酸应该如何保存?
探究与实践
硝酸的强氧化性
分析下面三个实验:1. 铜与浓硝酸反应;2. 铜与稀硝酸反应;3. 炭与
浓硝酸反应。
实验现象:1. ____________________________________________,
2. ____________________________________________,
3. ____________________________________________。
反应的化学方程式:1. ____________________________________,
2. ____________________________________,
3. ____________________________________。
浓硝酸和稀硝酸都具有强氧化性,浓硝酸可以氧化除
金、铂等以外的大部分的金属,浓硝酸和浓盐酸按体积比
为1∶3相混合,得到的混合液叫做王水,王水能溶解金、铂
等金属。浓硝酸还能氧化大部分的非金属单质和具有较强
还原性的化合物。
硝酸有广泛的用途可用于制炸药、塑料、医药、染料
等。溶有二氧化氮的浓硝酸可作火箭中的助燃剂。
1.在硝酸亚铁溶液
历史上曾用硝石(NaNO
3
)与浓硫酸反应制取硝酸。
中,加入盐酸,会有什么
现象发生?为什么?
NaNO + H SO (浓)微热 NaHSO + HNO ↑ 2.铝与酸会发生反
3 2 4 4 3
应,为什么可以用铝槽车
来运输浓硫酸或浓硝酸?
99
0812896-05-OK Page 99 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC工业上是将氨气和空气的混合气体通过氧化炉中的
铂-铑合金网发生氨氧化反应,生成一氧化氮和水,过量
实验室用硝酸钠与
空气中的氧气能使一氧化氮进一步氧化,并与水发生反应
浓硫酸加热反应生成硫
而转化为硝酸。
酸钠和硝酸,是否可行?
水
收集器
催化剂
氧化炉
空气
一氧化氮
氨
稀释的硝酸
图 5.5 硝酸工业流程简图
发生的反应是:
Pt-Rh
4NH + 5O 4NO + 6H O
3 2 800℃ 2
4NO + 3O + 2H O 4HNO
2 2 3
课堂实验
实验室制硝酸
按图5.6所示装置进
行实验,先用酒精灯对
玻璃管里的三氧化二铬
玻璃棉 三氧化二铬 玻璃棉
(催化剂)进行加热。然
空气
后把空气鼓入盛有浓氨
碱石灰
水的锥形瓶。当三氧化
二铬保持红热状态时,
浓氨水
移去酒精灯。 石蕊溶液
观察到的明显现象
图 5.6 工业制硝酸的原理
有:_________________
_________________________________________________________________________________________________________________________________________________________________________________
________________________________________________________________。
100
0812896-05-OK Page 100 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC(二)硝酸盐
硝酸盐大多数是无色晶体,易溶于水,受热容易分解。
如将钾、钙、钠的硝酸盐加热,生成相应的亚硝酸盐和氧气。
△
2KNO 2KNO + O ↑
3 2 2
对比三类硝酸盐分
金属活动性顺序中,从镁到铜的硝酸盐受热分解都生
解的异同之处。
成对应的金属氧化物、二氧化氮和氧气。
△
2Cu(NO ) 2CuO+4NO ↑+O ↑
3 2 2 2
汞和银的硝酸盐在较低温度下或光照下就会发生分解,
生成金属单质、二氧化氮和氧气。
2AgNO 光 2Ag + 2NO ↑ + O ↑
3 2 2
硝酸盐是强氧化剂,可燃物质与硝酸盐混合加热会迅
速燃烧。硝酸盐在酸性溶液中也是强氧化剂,在运输、贮藏
和配制溶液时要注意安全。
碳酸钠和碳酸氢钠
碳酸(carbonic acid)是二元弱酸(binary weak acid),
对应盐有正盐和酸式盐两种。碳酸的正盐中,铵盐和碱金
属的盐溶于水。而碳酸的酸式盐都溶于水。
可溶性的金属碳酸盐易发生水解而使溶液呈碱性,其
水解分步进行。
CO2-+H O HCO-+OH-
3 2 3
HCO-+H O H CO +OH-
3 2 2 3
碳酸氢盐的热稳定性较小,加热时,碳酸氢盐易分解。
101
0812896-05-OK Page 101 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC课堂实验
碳酸钠和碳酸氢钠的加热分解
分别将碳酸钠和碳酸氢钠装入配有单孔塞和玻璃导管的大试管,使试管
口略向下倾斜固定在铁架台上,加热,并使导管通入澄清石灰水中。
观察到:_____________________________________________________
____________________________________________________________________________。
碳酸钠比较稳定,不易分解。而碳酸氢钠不稳定,受热
容易分解。
2NaHCO △ Na CO + H O + CO ↑
3 2 3 2 2
碳酸钠易溶于水,碳酸氢钠能溶于水,在相同条件下
碳酸钠的溶解度比碳酸氢钠大。
课堂实验
碳酸钠和二氧化碳的反应
在一个大试管中加入三分之一容积的水,并边加入碳酸钠边振荡,直至
加入的碳酸钠不再溶解为止。静置片刻,把上层清液倒入另一大试管,然后
向此溶液中慢慢通入较纯的二氧化碳气体。
观察到:_____________________________________________________
________________________________________________________________________。
发生的化学反应为:___________________________________________。
碳酸氢盐既能跟酸反应,又能跟碱反应。跟酸反应时,
HCO-结合H+生成二氧化碳和水;跟碱溶液反应时,HCO-
3 3
怎样使碳酸钠与碳
提供H+跟碱溶液中的OH-结合生成水,同时生成的还有
酸氢钠之间发生相互转
CO2-。
化? 3
102
0812896-05-OK Page 102 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC练 习
HCO-+H+ H O+CO ↑
3 2 2 写出碳酸氢钙与足
HCO-+OH- CO2-+H O
3 3 2 量的盐酸、烧碱反应的
离子方程式。
资料库
星 际 分 子
在宇宙星际环境中,由化学反应产生的分子称为星际分子。1968年,人类发
现并证实的第一个星际分子是氨(NH )。这是用特殊的天文实验观察手段配合实
3
验室波谱试验、理论计算和星际化学模型等方法而确定的。到1982年6月,已
发现几十种星际分子。
在已发现的星际分子中,主要含碳、氮、氧、氢,还含有较少的硫和硅,它
们全部是非金属元素。星际分子中稳定的较少,不稳定的基团、离子和分子居多。
星际分子中许多含有不饱和键,碳元素占了80%,且有多种异构现象。
星际分子能在相当宽的温度范围中形成,有着复杂多样和低密度等特征。人
类对浩渺的宇宙星际间丰富多彩的星际分子的研究,是人类探索宇宙的一部分。
[课堂练习5.2]
1.下列关于卤化氢的性质比较中错误的是( )。
(A) 沸点:HF > HI > HBr > HCl
(B) 还原性:HI > HBr > HCl > HF
(C) 酸性:HF > HCl > HBr > HI
(D) 热稳定性:HF > HCl > HBr > HI
2.使用卤化钠与浓硫酸在蒸馏烧瓶中加热能制得的卤化氢气体是( )。
(A) HF (B) HCl (C) HBr (D) HI
3.下列物质的溶液中通入硫化氢不发生反应的是( )。
(A) Na S (B) FeCl (C) FeCl (D) AgNO
2 2 3 3
4.常温下,等体积的下列气体,混合后压强不发生变化的是( )。
(A) H S和SO (B) NH 和HBr (C) SO 和O (D) NO和O
2 2 3 2 2 2
5.加热下列物质发生反应,反应中有两种以上元素参加氧化还原的是( )。
(A) HNO (B) NaHCO (C) Cu(NO )·6H O (D) AgNO
3 3 3 2 2 3
△
6.已知:C + 2H SO(浓) CO ↑+ 2SO ↑+ 2H O。请设计实验证明炭与
2 4 2 2 2
浓硫酸加热反应的产物中有二氧化硫和二氧化碳,画出装置图,指出所用药品的名称。
103
0812896-05-OK Page 103 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC化工生产
5
.3 (CHEMICAL INDUSTRY PRODUCTION)
氯碱工业和联合制碱工业
(一)氯碱工业
电解饱和食盐水可制得烧碱、氯气和氢气,这种工业
生产称为氯碱工业。
课堂实验
电解饱和食盐水
如图5.7,在具支U形管中装入滴有酚酞 - +
阴极 阳极
的饱和食盐水,用分别连接直流电源负极的
铁棒和正极的石墨棒作为电极,进行电解。
并对两支管口逸出的气体作有关试验。
观察到:__________________________
___________________________________。
图 5.7 电解饱和食盐水
在食盐水中,由于氯化钠的电离和水的微弱电离,存在
Na+、H+、Cl-、OH-四种离子。通直流电后,与电源负极相
连的铁棒为阴极,由于H+的氧化性比Na+强,电极周围的
电解时,电子是怎样 H+易得到电子被还原:2H++2e—→H ↑。与电源正极相连
2
流动的? 的炭棒为阳极,在这样的条件下,由于Cl-的还原性比OH-
强,电极周围的Cl-易失电子被氧化:2Cl--2e—→Cl ↑。
2
留在溶液中的是钠离子和氢氧根离子。
104
0812896-05-OK Page 104 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC向电解质溶液中通直流电,在阳、阴两极引起氧化、还
阴 阳
原反应的过程称为电解。工业上电解饱和食盐水是用立式
极 极
隔膜电解槽进行的。
H Cl
2 2
练 习
e
1.上述实验中的两种气体产物是怎样检验确定的?
电解时_______极上发生氧化反应,_______极上发生还
原反应。 图 5.8 电解饱和食盐水原理
2.电解饱和食盐水的离子方程式为:
_________________________________________________。
化学方程式为:_____________________________________。
电解时,为什么先只有某一电极附近的溶液变红色?
3.电解池的工作原理与原电池的工作原理有什么不同?
用哪些物质可从氯
化钠溶液中除去Ca2+、
Mg2+、SO 2-等杂质?为
4
海水晒盐得到的食盐中含有少量Ca2+、Mg2+、SO2-等 确保除尽杂质,加入试
4
剂需稍过量,这样会引
可溶性杂质。这些离子在电解过程中或者会腐蚀电极,或
入新的杂质。怎样处理
者会变成沉淀堵塞电解槽的设备,必须预先除去。
后,才可确保获得纯净
的食盐水?
+
阳极
Cl 氯化钠饱和溶液
- 2
H
2
阴极
1.电解饱和食盐水
石棉隔膜
氢氧化钠和 获得的产物中,相互之间
氯化钠溶液
会发生哪些反应?从图
5.9看,立式隔膜电解槽
中哪一种设备能防止上
列反应的发生?
2.从电解饱和食盐
水的电解槽流出的是氯
化钠和氢氧化钠的混合
图 5.9 立式隔膜电解槽剖面图
溶液,请你设计方案,既
能取得产品,又不浪费
氯碱工业生产获得的烧碱、氯气、氢气都是重要工业
原料。
原料,将氢气和氯气经点燃反应生成的氯化氢,溶于水成
为重要化工原料盐酸。
105
0812896-05-OK Page 105 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC探究与实践
自制家用消毒器
如果用一个小型电解器,装上食盐水进行电解,又使产生的氯气与氢氧
化钠反应,便获得了具有杀菌消毒作用的溶液。请你设计一个这样的家用消
毒器。
化学史话
用电解法发现元素最多的化学家——戴维
英国化学家戴维(Humphry Davy,1778-1829)对意大利物理学家伏特
发明的电池有着极大的兴趣。他首先用电池来研究各种物质,做了很多的电
解实验。1807年,他通过巧妙设计,电解碳酸钾(草木灰)获得了钾;同一
年,他用同样方法获得了钠。当他再次使用电解法试图获得金属钙和镁时,
虽经多次实验,均未获得成功。在他徘徊不前的时候,瑞典化学家柏济力阿
斯的信给了他极大启示。他调整实验,终于又用电解法制得了金属钙,接着
他又用类似的方法制得了镁和钡。
戴维凭着电解法成为发现元素最多的化学家。他一生对电化学进行了卓
越的研究,提出了电解和电压的作用理论,发现并制得了很多活泼金属元素
的单质,否定了氯是“失燃素的盐酸”(舍勒)和“酸必含氧”(拉瓦锡)等
错误观点。他发明的矿工安全灯,至今还在应用。
(二)联合制碱工业
纺织、造纸、制皂等工业需要大量的碳酸钠,随着这些
工业的迅速发展,单纯的依靠盐碱湖中的碳酸钠,已远远
满足不了生产的需要。从18世纪开始,化学家们就开始利
用其他原料来进行纯碱的工业生产。
106
0812896-05-OK Page 106 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC化学史话
纯碱工业的开端——勒布朗法
1788年,法国的勒布朗用浓硫酸使氯化钠转化为硫酸钠,再用焦炭使之
转化成硫化钠,再将硫化钠与石灰石反应得到碳酸钠。他用4年时间设计了
一套生产流程。
虽然勒布朗法耗煤量大,产品质量不高,设备也易被腐蚀,但是解决了
当时纯碱需求的燃眉之急。到19世纪末,这种生产方法才被淘汰。
地球上的海水中含有大量的氯化钠,怎样使氯化钠
转化为碳酸钠呢?比利时科学家索尔维(Ernest Solvay,
1838-1922)利用氯化钠溶液与碳酸氢铵反应,得到溶解
度较小的碳酸氢钠。
NH + CO + H O NH HCO
3 2 2 4 3
NH HCO + NaCl NH Cl + NaHCO ↓
4 3 4 3
过滤得到碳酸氢钠,通过焙烧就可获得碳酸钠。
△
2NaHCO Na CO + CO + H O
3 2 3 2 2
碳酸氢钠分解产生的二氧化碳可循环使用。这种称为
氨碱法的生产,是用煅烧石灰石的方法提供二氧化碳,并
使生石灰转化为消石灰,与分离出的氯化铵反应,产生可
循环使用的氨气。
CaCO 高温 CaO + CO ↑
3 2
CaO + H O Ca(OH)
2 2
2NH Cl + Ca(OH) CaCl + 2NH ↑ + 2H O
4 2 2 3 2
在氨碱法的生产过程中,NaCl利用率仅为72%~74%,
而且在回收氨的过程中,大量氯化钙作为“废液”排出,原
料的利用率低。
我国化学家侯德榜(1890-1974)勇于改进创新,看出
了氨碱法生产的不足之处。他将合成氨法与氨碱法工艺联
107
0812896-05-OK Page 107 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC合,同时制造纯碱和氯化铵,这就是著名的联合制碱法。此
法以食盐、氨气和二氧化碳(合成氨工业的副产品)为原
料。将氨气与二氧化碳先后通入饱和食盐水中,生成碳酸
氢钠沉淀,经过滤、洗涤、煅烧而得产品纯碱。在滤液中,
通入氨,冷冻和加食盐,使氯化铵析出,经过滤、洗涤、干
燥而得氯化铵。此时由食盐所饱和的滤液,可再通入氨气
和二氧化碳,循环使用。与氨碱法相比,本法的优点是能充
分利用食盐中的钠和氯,避免产生大量含氯化钙的废液,并
可节省石灰窑、蒸氨塔等设备。
石灰石
(碳酸钙)
焦炭 气体
盐水 氨化的盐水
二氧化碳
氧化钙
水 水
过滤器
氯化铵溶液 碳酸钠
图 5.10 氨碱法生产纯碱示意图
化工生产的一些基本原理
通过化工生产,人们可以得到各种各样的物质,以满
足生活、生产和科学研究的需要。
例如硫酸、硝酸、盐酸;烧碱、纯碱;塑料、玻璃、水
泥等都是化工生产的产品。橡胶、纤维虽有天然的,但多数
还是化工生产合成的。
(一)充分利用原料
化工生产大多是利用一些原料来转变为需要的产品。
108
0812896-05-OK Page 108 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC由于化学反应中原子是守恒的,这就形成了化工生产的物
料平衡。使原料尽量多地转化为产品是使化工生产降低成
本、提高产量、增加经济效益的关键,如合成氨生产、纯
碱生产中都有原料循环使用的工艺,接触法制硫酸、氨氧
化制硝酸中都利用廉价的空气(氧气)来提高原料气的转
化率。
图 5.11 合成氨生产控制室
(二)充分利用能量
相当多的化工生产需要加热进行反应。不管是电加热,
还是矿物燃料加热,能耗都会使生产成本提高,使用矿物
燃料还会有废气污染环境。
如果生产过程中存在放热步骤,那么就有利用这种能
量的可能性。利用放出的热量对需加热的物料进行预热,便
能起到既降低能耗,又提高生产效率的作用。
如果在生产过程中没有放热步骤,必须要使用燃料时,
也要设计出充分燃烧燃料和充分利用能量的生产工艺和生
产设备。
地球上的石油、煤炭、天然气等矿物能源是有限的,终
将消耗殆尽。生活、生产中怎样利用太阳能、风能、潮汐能
等,是当今开发能源研究的一个重大课题。
图 5.12 列管式热交换器
1.热交换器的主要构造和工作原理是怎样的?举例说
出它的使用意义。
2.举例说明生活或生产中是如何使燃料充分燃烧以达
到充分利用能量的目的?
109
0812896-05-OK Page 109 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC(三)保护环境
化工生产中产生的废气、废水、废渣严重地污染着人
类生存的环境,“绿色化学”就是从源头上防止这种污染。
“绿色化学”是指工业生产的过程中没有(或者极少有)有
毒、有害物质排出,合成产品的原子利用率尽量达到百分
之百。按照这种先进理念设计的生产,当然可以避免环境
污染。
但在目前的化工生产中,还常有“三废”排放,那就必
须进行治理。
例如,用氨水吸收制硫酸的尾气中的二氧化硫。
2NH + H O + SO (NH ) SO
3 2 2 4 2 3
(NH ) SO + H O + SO 2NH HSO
4 2 3 2 2 4 3
用烧碱溶液吸收精制硝酸产生的尾气中的氮氧化物。
2NO + 2NaOH NaNO + NaNO + H O
2 3 2 2
NO + NO + 2NaOH 2NaNO + H O
2 2 2
这种处理不仅可以防止有害物质的排放,也可以同时
生产出一些有用的工业原料。只有环保型的化工生产,才
图 5.13 硝酸尾气吸收装置 符合我国的基本国策,实现可持续发展。
[课堂练习5.3]
1. 电解熔融的氯化钠和饱和食盐水有什么不同?写出电解的电极反应式和化学方
程式。
2.电解饱和食盐水时,需把其中的Ca2+、Mg2+、SO 2-除去,写出除杂过程的所
4
有的离子方程式。
3.氨碱法生产纯碱,在氯化钠溶液中先通入二氧化碳再通入氨气,能不能生成碳
酸氢钠沉淀?把加热碳酸氢钠产生的二氧化碳回收,再通入食盐水循环使用,生产时
需再补充二氧化碳的原因是什么?而使氯化铵与氢氧化钙反应产生的氨气通入食盐水
循环使用,也需补充氨气,这又是为什么?
4.举例说明在化工生产中需遵循哪些原则。
110
0812896-05-OK Page 110 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC小 结
1.非金属单质。
(1)非金属单质有单原子分子、双原子分子、多原子分子和大分子物质等不同的类型,
形成的晶体主要是分子晶体和原子晶体。
(2)非金属单质存在同素异形体。同种元素的原子由于构成晶体类型不同、构成分子的
原子个数不同、分子的构型不同等,都会形成不同性质的单质。
(3)非金属单质分别与金属、氢气、氧气、水、碱等物质反应。反应中,许多元素会
呈现有可变的化合价。反应的状况除取决于组成元素的非金属性强弱外,还受到多种因素
的影响。
2.非金属化合物。
(1)卤化氢的熔点、沸点、热稳定性、还原性、水溶液的酸性,既有规律的递变性,也有
一定特殊性。
(2)硫的气态氢化物——硫化氢和硫的氧化物——二氧化硫都是有毒气体,二氧化硫的
二次污染——酸雨的危害更大。它们所含硫元素的化合价不同,决定了它们具有不同的氧化
还原性。
(3)硝酸有酸性和强氧化性,可氧化大多数金属和非金属单质。浓硝酸不稳定,工业上
用氨氧化法制硝酸。硝酸盐受热都要分解,且随其中金属离子的不同,呈现一定的分解规律。
(4)碳酸钠和碳酸氢钠,在溶解性、溶液的酸碱性、热稳定性、分别与酸、碱的反应等
方面,存在共性,更多的是存在差异性。它们之间可以相互转化。
3.一些化工生产及化工生产的原理。
(1)电解法是化工生产方法之一,电解饱和食盐水生产氯气、烧碱及氢气称为氯碱工业。
(2)氨碱法和联合制碱法都能制得纯碱,但侯德榜改进了氨碱法生产,与合成氨厂联
合,不再产出污染环境的氯化钙,提高氯化钠的利用率,同时生产了有价值的氯化铵。
(3)充分利用原料,尽量降低能耗,严格防止产生“三废”污染环境,是化学工业生产
必须遵循的原理。
4.阅读下面短文,比较无机酸的英文命名和中文命名。
Most acids produce a characteristic anion when they dissolve in water. As a result, the name of
an acid is usually derived from the name of its anion. For acids in which the anion ends in the suffix-
ide (such as chloride), the name of the acid begins with the prefix hydro-. The acid’s name also
includes the root name of the anion and the word acid. In addition, you need to change the suffix of
the anion from -ide to -ic. By these rules, the acid with the formula HCl is named hydrochloric acid.
What would you call the acid with the formula HF? With the formula HI?
Other acids are named without the prefix hydro-. The acid with the formula HNO derives its
3
name from the NO- anion, which is a nitrate ion. HNO is named nitric acid. The names of other
3 3
common acids are shown in the table below.
111
0812896-05-OK Page 111 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPCNames and Formulas of Some Acids
Anion Corresponding Acid Anion Corresponding Acid
F-,fluoride HF,hydrofluoric acid NO-,nitrate HNO ,nitric acid
3 3
Cl-,chloride HCl,hydrochloric acid CO2-,carbonate H CO ,carbonic acid
3 2 3
Br-,bromide HBr,hydrobromic acid SO2-,sulfate H SO ,sulfuric acid
4 2 4
I-,iodide HI,hydroiodic acid PO3-,phosphate H PO ,phosphoric acid
4 3 4
S2-,sulfide H S,hydrosulfuric acid CH COO-,acetate CH COOH,acetic acid
2 3 3
112
0812896-05-OK Page 112 2011.4.7, 4:14 AM Adobe PageMaker 6.5C/PPC6
金属元素
METALLIC ELEMENTS
金属单质具有许多优良的性能。常
温下,除汞以外的金属都呈固态。金属
具有良好的导电性、导热性、延展性和
美丽的光泽。导电性最强的金属是银;延
展性最好的金属是金;硬度最大的金属
是铬;密度最小的金属是锂。由金属形
成的合金性能各异,应用广泛。钛合金
能携人升空,铁合金可护人入海。金属
还能与其他物质发生反应,生成各种重
要的金属化合物。人类的生产和生活都
离不开金属。 ◆ 金属的结构、性质
自然界中,金属元素大多以化合态 ◆ 金属的冶炼
存在,用不同的方法可以将它们从化合 ◆ 一些金属化合物
物中还原出来,这就是金属的冶炼。
研究金属元素、单质及其化合物的
性质,具有十分重要的意义和价值。
113
0812896-06-ok Page 113 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC金属及其冶炼
6
.1
(METALS AND THEIR SMELTING)
资料库 金属元素原子结构的特点
过渡元素
人类已发现了一百一十几种元素,其中大多数是金
元素周期表中从IIIB 属元素。
族到IIB族的10个纵列(包
括镧系、锕系)共六十多
种元素,称为过渡元素,
它们都是金属元素。
1.参考课本后的元素周期表,在下面空白的元素周期
表中,标出金属元素的位置区域。
族
ⅠA 0
周期
1 ⅠⅠA ⅠⅠⅠA ⅠVA VA VⅠA VⅠⅠA
2
3 ⅠⅠⅠB ⅠVB VB VⅠB VⅠⅠB VⅠⅠⅠ ⅠB ⅠⅠB
4
5
6
7
2.金属元素在化合物中都显正价。试分析主族金属元
素的化合价与它在元素周期表中的位置及原子结构的关系。
3.比较钠、铝在元素周期表中的位置、原子结构及性
质,从中可以得到一些什么规律?
114
0812896-06-ok Page 114 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC大多数金属原子的最外层电子数较少,原子半径较大,
容易失去电子。主族金属元素原子在化学反应中失去最外
层电子,显示出的化合价等于原子的最外层电子数。副族
金属元素原子的结构比较复杂,在化学反应中除能失去最
外层的电子外,还能失去排布在次外层d亚层或倒数第三层
的f亚层上的电子,显示出的化合价也比较复杂。如铁在化
学反应中能失去4s轨道中的2个电子成Fe2+,也可能再失
去3d轨道中的1个电子而成Fe3+。 图 6.1 赤铁矿
金属的化学性质
由于金属元素原子的电子层结构的差异,金属单质的
化学活泼性有很大差别。
在金属活动性顺序中,排在前面的金属单质还原性较
强,对应的阳离子较难得到电子,氧化性较弱;排在靠后面
试用实例比较金属
的金属单质还原性较弱,对应的阳离子容易得到电子,氧
活动性顺序表中位置不
化性较强。 同的金属单质及其对应
阳离子还原性、氧化性的
强弱。
(一)金属与非金属的反应
金属与非金属在一定条件下能发生化合反应。同一金
属与不同的非金属反应时,可能得到不同价态的产物。同
一金属与同种非金属反应时,由于反应条件的不同,也可
能得到不同的产物。
例如:钠与氧气反应,在不同条件下可生成氧化钠、过
氧化钠或它们的混合物。
(二)金属与水的反应
在金属活动性顺序表中,氢前面的金属能跟水发生
反应。
课堂实验
钠与水的反应
1. 取一个小烧杯,加入约三分之一的水,再滴入几滴酚酞试液,准备
好能盖住烧杯的表面皿。用镊子取出浸在煤油中的钠,用滤纸吸干煤油,再
115
0812896-06-ok Page 115 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC用小刀切下绿豆大小一块,投入烧杯中,并立即盖好表面皿。
观察到的现象:_______________________。
钠与水反应可能产生什么气体?
______________________________。
2. 设计钠与水反应并收集产生的气体的实验(用常用仪器),画出装
置图。
3. 用图6.2的装置完成钠与水的反应并收集产
生的气体,试验其可燃性。
由实验现象推测钠有哪些物理性质和化学性质。 图 6.2 钠与水反应
课堂实验
钾、镁和水的反应
设计并完成钾、镁分别跟水反应的实验。*
*钾比钠更活泼,钾与水反应的容器要大一些,操作更要小心些。
图 6.3 钾与水反应
碱金属与水发生剧烈反应(Li除外),生成碱并放出
氢气。
2Na+2H O 2NaOH+H ↑
2 2
116
0812896-06-ok Page 116 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC在反应时,因金属钠密度小、熔点低,放出的热量使其
熔化成小球,在水面游动。
镁在冷水中几乎不反应,把镁放在水中加热到沸腾,则
发生反应。 试比较钠、镁、铁与
水反应的条件,分析金属
活泼性强弱与反应条件
△
Mg+2H O Mg(OH) +H ↑
2 2 2 的关系。
锌和铁在高温下都能与水蒸气发生反应。例如:
高温 资料库
3Fe+4H O(g) Fe O +4H
2 3 4 2
金与王水的反应
与酸不反应的不活泼
(三)金属与酸的反应
金属金和铂,可以与王水
比较活泼的金属如锌、铁,它们与稀硫酸或盐酸等发
反应:
生置换反应放出氢气。反应的离子方程式为:
HNO +4HCl+Au
3
HAuCl +NO↑+2H O
4 2
Zn + 2H+ Zn2+ + H ↑
2
Fe + 2H+ Fe2+ + H ↑
2
较不活泼的金属如铜、银,它们与稀硫酸或稀盐酸等 练 习
不反应,但能与浓硫酸、浓硝酸等具有强氧化性的酸发生
写出铜分别与浓硫
反应,生成二氧化硫、氮氧化物等还原产物。铝、铁等金属
酸、浓硝酸和稀硝酸反
在室温下与浓硫酸、浓硝酸会发生钝化。 应的化学方程式。
(四)金属与盐的反应
较活泼的金属可以把相对不活泼的金属从其盐溶液中
置换出来。
练 习
下列各组物质能否发生反应,能发生反应的写出化学方
程式:
1.铜与硝酸银溶液 _______________。
2.锌与硝酸铜溶液 _______________。
3.铁与硫酸锌溶液 _______________。
4.银与硝酸汞溶液 _______________。
117
0812896-06-ok Page 117 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC资料库
贵金属——金和银
金和银在历史上曾作为货币流通,从古到今都用来制作珍贵的装饰品。
在公元前2000年以前,人类不但得到了金,而且会包金、镶金,工艺精致,
拉成的细丝可刺绣,压成的金箔仅0.01mm厚。
金的性质很稳定,不易腐蚀,而且总是金光闪闪。正像人们所说:是金子在
什么地方都会闪光。正由于金的引人注目的外观和稳定的性质,人类发现的第一
种金属就是金。
金或与砂子混聚、或与岩石共生。由于十分分散,沙里淘金或矿中挖金的开采
工作都比较困难。以粗金板为阳极,纯金片为阴极,以金的氯络合物水溶液及游离
盐酸为电解液进行电解,可以对粗金进行提纯,获得纯度达99.95%以上的纯金。
银在自然界中大部分是以化合态存在的,所以银比金发现要晚。银白色的银
也不易生锈,适宜加工成各种器皿、饰品。银导电性非常好,也很贵重。含银矿
石如硫化银,经加热或还原即可得到银。
金属的冶炼
大多数金属以化合态存在于矿石中,金属的冶炼就是
资料库
使化合态的金属元素还原为金属单质。
表6.1 一些矿石的主要成分
在化合物中,金属元素一般以离子存在,由于金属离
矿 石 主要成分 子的氧化性强弱的差异,使它们还原为单质的难易程度不
食 盐 NaCl 同,把它们还原为单质的方法也就不同。
光卤石 KCl·MgCl·6HO 不活泼金属的硫化物或氧化物在加热时就可分解,生
2 2
菱镁矿 MgCO 3 成金属单质。例如,焙烧辰砂(HgS)就可以制取汞,并生
铝土矿 Al O
2 3 成二氧化硫。
重晶石 BaSO
4
芒 硝 Na SO·10H O
2 4 2 HgS + O 焙烧 Hg + SO
赤铁矿 Fe O 2 2
2 3
辉铜矿 Cu S
2
加热氧化汞也可制得汞,同时生成氧气。
黄铁矿 FeS
2
闪锌矿 ZnS
△
黄铜矿 CuFeS 2HgO 2Hg + O ↑
2 2
赤铜矿 Cu O
2
有些金属可以采用还原法来制得。
118
0812896-06-ok Page 118 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC△
CuO + H Cu + H O
2 2
高温
ZnO + C Zn + CO↑
点燃
3MnO + 4Al 3Mn + 2Al O
2 2 3
我国在春秋战国时代,就开始炼铁。铁是现代生产和
生活中使用量最大的金属。
如何用碱式碳酸铜、
炼铁最主要的反应是:
碳酸锌等矿石为原料冶
炼得到铜和锌。写出有关
高温
Fe O + 3CO 2Fe + 3CO 化学方程式。
2 3 2
(赤铁矿石主要成分)
在实际生产中,用焦炭与空气中氧气反应产生一氧
化碳。
资料库
高温
C + O CO
2 2 除去铁矿石中的脉石
高温
CO + C 2CO
2
铁 矿 石 中 的 脉 石
(SiO )熔点高,难除去,
2
生铁中的碳和其他杂质含量较高,为了提高性能和扩
夹杂在铁中影响铁的质量
大用途,我们需要把大部分生铁冶炼成钢。
和性能。所以炼铁时,还
炼钢的主要反应原理,也是通过氧化还原反应,在高
要加入石灰石,使脉石成
温下,用氧化剂把生铁里过多的碳和其他杂质氧化成气体
为熔融状态的硅酸钙炉渣
或炉渣除去。
而除去。
炼钢时常用的氧化剂是空气(或纯氧)等,在高温下, 高温
CaCO CaO+CO ↑
3 2
发生的主要反应如下: 高温
CaO+SiO CaSiO
2 3
高温
2Fe + O 2FeO + Q
2
高温
Si + 2FeO SiO + 2Fe + Q
2
高温
Mn + FeO MnO + Fe + Q
高温
C + FeO CO + Fe - Q
铁水里的一部分硅、锰、碳等元素也会被氧气直接氧
炼铁和炼钢都是利
化,生成的二氧化硅、氧化锰和生铁中含有的硫(主要以
用氧化还原反应,它们之
FeS形态存在)、磷,跟生石灰相互作用成为炉渣排出。
间有哪些不同?
出钢前需加入脱氧剂如硅铁、锰铁、铝等,使氧化亚铁
脱氧。
119
0812896-06-ok Page 119 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC资料库
表6.2 生铁和钢
含碳量(%) 机械性能 机械加工
生铁 2~4.3 硬而脆 可铸不可锻
钢 0.03~2 硬而韧,有弹性 可铸可锻
炼钢时通常加入生石灰来除去生铁中的硫和磷。
高温
FeS + CaO FeO + CaS
2P + 5FeO + 3CaO 高温 5Fe + Ca (PO )
3 4 2
资料库
我国钢铁工业的飞速发展和宝钢的崛起
我国最早的人工冶铁始于公元前六世纪,春秋末到战国初开始了原始的炼
钢,当时的冶铁技术在世界上居领先地位。
新中国成立以后,尤其是改革开放以来,我国钢铁工业得到了飞速的发展。
到2007年,我国的粗钢产量已近4.9×108 t,约是新中国成立以前最高年产量
(1943年,9×105 t)的545倍,居世界首位。
我国最现代化的钢铁企业——上海宝山钢铁总厂一期工程于1985年投入生
产,于1998年成立了宝钢集团有限公司,2007年产粗钢达2.858×107 t。产品
畅销国内外市场,赢利水平居世界领先地位,2007年进入500强钢铁企业第6位。
宝钢实施钢铁精品战略,将建成中国钢铁工业新技术、新工艺、新材料的研
发基地。现代化生产的宝钢就像一颗明珠镶嵌在东海之滨的长江入海口。
活泼金属离子的氧化性很弱,用还原剂无法将它们从
化合物中还原出来。一般采用电解法来制得。如金属钠是
用电解熔融的氯化钠来制取的:
通直流电
2NaCl(熔融) 2Na + Cl ↑
2
金属铝是用电解熔融氧化铝的方法制得的,但氧化铝
熔点很高,很难直接熔融电解。工业上用冰晶石(Na AlF )
3 6
120
0812896-06-ok Page 120 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC作为助熔剂,使氧化铝熔融的温度大大降低,然后通直流
电制取,反应的化学方程式为:
通直流电
2Al O 4Al + 3O ↑
2 3 助熔剂 2
资料库
铝 的 生 产
铝是活泼的金属,用还原法生产需用比铝更活泼的金属与熔融的含铝化合物
反应,难度大,成本也太高。近代工业用电解熔融的氧化铝的方法生产。
自然界中,氧化铝主要存在于铝土矿中,铝土矿中还含有氧化铁和二氧化硅
等杂质。将铝土矿石粉碎后与氢氧化钠反应,生成的硅酸钠与部分偏铝酸钠进一
步反应,形成沉淀,与氧化铁一起被除去。
Al O + 2NaOH 2NaAlO + H O
2 3 2 2
SiO + 2NaOH Na SiO + H O
2 2 3 2
2Na SiO + 2NaAlO + 4H O Na O·Al O ·2SiO ·2H O↓+ 4NaOH
2 3 2 2 2 2 3 2 2
除去沉淀后的溶液中主要成分是偏铝酸钠,在溶液中通入二氧化碳,使偏铝
酸钠成为氢氧化铝沉淀析出,再经过过滤、干燥、灼烧得纯氧化铝。
NaAlO + CO + 2H O Al(OH) ↓+ NaHCO
2 2 2 3 3
△
2Al(OH) Al O + 3H O
3 2 3 2
钢壳内衬的耐火材料中,石墨作槽池兼作阴极,阳极则是固定在可移动导电
杆上的石墨。氧化铝和冰晶石在1 000℃时成为共熔物。通电时发生的反应十分
复杂,可简单地视为:
在阴极:Al3+ + 3e Al
在阳极:2O2- - 4e O ↑
2
生成的熔融状态铝密度大于氧化铝和冰晶石的共熔物,沉在槽底,可不断取
出。阳极石墨会与生成的氧气反应而损耗,因此需要定期补充。
电解质
烟罩 (氧化铝和冰晶石)
阳极
钢壳
石墨
阴极
铝
图 6.4 铝的冶炼
121
0812896-06-ok Page 121 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC表6.3 归纳金属的冶炼方法
金属冶炼的
方法
制得的
金属
[课堂练习6.1]
1.在盛放硫酸铜溶液的小烧杯中,投入一小粒金属钠(立即盖上玻璃片或表面
皿)。试述观察到的现象,并写出可能发生反应的化学方程式。
2.解释下列各项事实:
(1)浓硝酸可装在铝槽车里运输。
(2)铆在铜器具上的铁钉特别易生锈。
(3)钠块须保存在煤油中,镁带可露置在空气中。
3.电解熔融的氯化钠和电解饱和氯化钠溶液时,现象有什么不同?试写出反应的
化学方程式。
122
0812896-06-ok Page 122 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC一些金属化合物
6
.2
(SOME METALLIC COMPOUNDS)
常见的金属化合物有氧化物、碱、盐等。近代,化学家
又合成了金属的络合物、金属有机化合物和金属簇合物等。
本节我们将更深入地学习一些钠、铝、铁的化合物。
过氧化钠
先将金属钠熔化,再通入定量的不含二氧化碳的干空
气,维持温度为180~200 ℃,钠就氧化成氧化钠(Na O)。
2
然后再增加空气的量,并升温至300~400 ℃,即制成纯净
的淡黄色的过氧化钠(sodium peroxide)。
4Na + O 180~2 0 0 ℃ 2Na O
2 2
2Na O + O 300~4 0 0 ℃ 2Na O
2 2 2 2
课堂实验
过氧化钠与水的反应
在盛有少量过氧化钠的试管中加入少量水,用带火星的木条检验放出的
气体,再向试管中滴入酚酞试液。
观察到的现象:_______________________。
写出过氧化钠与水反应的化学方程式:_____________。
123
0812896-06-ok Page 123 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC过氧化钠具有很强的氧化性,也具有漂白性。
过氧化钠分别与水、酸性氧化物和酸反应时,都有氧
比较氧化钠、过氧化
气生成。
钠分别与水、二氧化碳、
盐酸的反应,找出反应的
规律性。 2Na O + 2H O 4NaOH + O ↑
2 2 2 2
2Na O + 2CO 2Na CO + O
2 2 2 2 3 2
2Na O + 2H SO 2Na SO + 2H O + O ↑
2 2 2 4 2 4 2 2
氢氧化铝
在可溶性铝盐溶液中滴入氨水,产生氢氧化铝沉淀。
Al3+ + 3NH ·H O Al(OH) ↓+ 3NH+
3 2 3 4
课堂实验
氢氧化铝和氢氧化钠及盐酸的反应
用上述方法制取氢氧化铝,并将产生的悬浊液分装在两个试管里,分别
向这两个试管中逐滴加入氢氧化钠溶液和盐酸至过量。
观察到的现象:________________________
________________________________。
氢氧化铝能分别与强酸、强碱溶液发生反应。
Al(OH) + 3H+ Al3+ + 3H O
3 2
试用平衡移动原理 Al(OH) 3 + OH- AlO- 2 + 2H 2 O
来解释氢氧化铝既可溶
于强酸溶液,又可溶于强 氢氧化铝在溶液中存在两种电离平衡:
碱溶液的原因。
H+ + AlO- + H O Al(OH) Al3+ + 3OH-
2 2 3
(酸式电离) (碱式电离)
124
0812896-06-ok Page 124 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC学生实验
氢氧化铝的两性
1.(1)把氢氧化钠溶液逐滴加入到氯化铝溶液中至过量,反应时不断
振荡试管。
(2)把氯化铝溶液逐滴加入到氢氧化钠溶液中至过量,反应时不断振荡
试管。
实验现象:① ________________________。
② ________________________。
分析与推理:_________________________
________________________________。
2.(1)把盐酸逐滴加入偏铝酸钠溶液中至过量,反应时不断振荡试管。
(2)把偏铝酸钠溶液逐滴加入盐酸中至过量,反应时不断振荡试管。
实验现象:① ________________________。
② ________________________。
分析与推理:_________________________
________________________________。
有关反应的化学方程式:____________________
________________________________。
资料库
金属有机化合物
碳原子与金属原子通过化学键连接,形成的化合物称为金属有机化合物。如
三甲基铝[Al(CH ) ]就属于金属有机化合物。在20世纪初,格利雅合成的有机镁
3 3
化合物应用于有机合成,获得极大的成功。20世纪50年代以来,研究金属有机
化合物为主的金属有机化学开始迅速发展,并与其他各化学学科相互渗透,成为
化学领域中一个极为活跃的新兴边缘学科。
从形成金属有机物的金属来看,由仅局限于主族金属,逐渐发展到过渡金
属;从形成金属有机物的有机基团看,由烷基逐渐发展到含双键、叁键的不饱和
烃基,甚至一些结构更为复杂的基团。这些金属有机化合物在有机合成中有着非
凡的性能,如区域选择、空间选择、不对称合成、催化作用等等。有人估算,近
30年来,至少有50%以上的有机合成新方法,是通过金属有机物来完成的。因
此,20世纪60年代以来,已有7位金属有机化学家作出优异业绩,获得了诺贝
尔化学奖。
125
0812896-06-ok Page 125 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC练 习 铁盐与亚铁盐
写出铁与下列物质
铁在化合物中一般显示+2价或+3价。Fe2+的溶液呈浅
在一定条件下发生反应
绿色,Fe3+的溶液则呈棕黄色。可以用硫氰化钾、硫氰化铵
的化学方程式。
等溶液来检验溶液中的Fe3+。
1.水蒸气
2.盐酸
3.硝酸铜溶液 Fe3++3SCN- Fe(SCN)
3
血红色
课堂实验
氯化亚铁、氯化铁与硫氰化钾的反应
将氯化亚铁溶液和氯化铁溶液分别注入两个试管里,各滴入硫氰化钾
溶液。
观察到的现象:_______________________。
有明显现象的反应:_____________________。
课堂实验
硫酸亚铁和硫酸铁溶液分别与氢氧化钠反应
向两个试管中分别注入少量新制备的硫酸亚铁溶液和硫酸铁溶液。用
胶头滴管吸取氢氧化钠溶液,分别注入到这两个试管中,在硫酸亚铁溶液
中加入氢氧化钠溶液时,要把滴管头伸到硫酸亚铁溶液内部再注入氢氧化
钠溶液。
观察到的现象:________________________
________________________________。
两个试管中发生的反应:
(1)____________________________。
(2)____________________________。
为什么要把胶头滴管伸到硫酸亚铁的溶液中再注入氢氧化钠溶液?
______________________________。
126
0812896-06-ok Page 126 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC+2价的铁很容易被空气中的氧气氧化而转化为+3价
的铁。
4Fe(OH) +O +2H O 4Fe(OH)
2 2 2 3
+3价的铁如果在还原剂的作用下,也可以转化为+2
价铁。
2FeCl +Fe 3FeCl
3 2
2FeCl +Cu 2FeCl +CuCl
3 2 2
课堂实验
铁的性质试验
1.将稀盐酸加入到盛有铁粉的大试管中(使铁粉有剩余)备用。取大
试管中上层清液,分装三个试管中,各加入硫氰化钾溶液。然后,向这三个
试管中分别加入氯水、双氧水和用气唧鼓入空气。再分别向这三个试管中加
入铁粉和铜粉,振荡。
实验现象:__________________________
________________________________。
分析与推理:_________________________
________________________________。
2.在试管中装入少量碘化钾溶液,并滴入几滴淀粉溶液,振荡,再加
入一滴管氯化铁溶液。
实验现象:__________________________
________________________________。
分析与推理:_________________________
_________________________________。
氧化剂(Cl、O、HO 等)
Fe2+ 2 2 2 2 Fe3+
还原剂(Fe、Cu、HS、KI等)
2
铁盐和亚铁盐在水溶液中都会水解,但Fe3+的水解程
度相对更强些。
127
0812896-06-ok Page 127 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC1.为什么氯化铁可作净水剂?
2.为什么配制铁盐溶液时须滴入酸,配制亚铁盐溶液
时既要滴入酸还需加入少量铁粉?
资料库
人体中的铁
铁在人体中的含量约为4.2~6.1 g,红细胞中的血红蛋白含有人体中72%
的铁。
血液中红细胞中的+2价铁,在肺部与呼吸作用吸入的氧气结合,当血液进
入到身体其他各个部位时,释放出氧气,供人体组织进行氧化作用。红细胞是氧
的优良载体,1 g血红蛋白可载送1.34~1.36 mL的氧气。血红蛋白中的铁除运
送氧气外,还有运送二氧化碳和维持血液酸、碱平衡的作用。
人体缺少铁,会使血红蛋白减少,造成缺铁性贫血,使输氧功能减弱而产生
各种疾病。铁在人体内是循环使用的,且有15%~20%的贮备,但代谢过程、出
血等会使铁流失。平时要食用一些含铁丰富的食品来补充铁。如服用补铁剂则需
在医生的指导下,因为摄入过量的铁,反而会对人的脏器产生危害。
[课堂练习6.2]
1.在潜水艇中常备有一定量的过氧化钠,试述它的作用。
2.为什么明矾可以净水?试述其原因并写出有关的离子方程式。
3.在氯化铁溶液中通入硫化氢气体能发生氧化还原反应,试写出反应的化学方
程式。
128
0812896-06-ok Page 128 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC小 结
1. 金属在元素周期表的位置、原子结构和性质。
金属元素在周期表中位于IA族(除H)、IIA族、副族、VIII族及IIIA~VIA族的左下
部分。多数金属原子的最外层电子数小于4,少数金属原子的最外层电子数大于4,金属原
子的原子半径较大。金属元素的原子结构决定了金属的性质,金属易失电子而具有还原性。
金属的化学性质:
除少数金属(如铂、金)外,都能与氧气、硫等非金属反应。
按金属活动性顺序,钾、钙、钠与冷水反应,镁与沸水反应,生成对应的碱和氢气。锌、
铁等在高温下与水蒸气反应,生成氧化物和氢气。排在氢之前的金属能与酸反应生成盐和
氢气。常温下,铁、铝等金属在浓硫酸或浓硝酸中钝化。除铂、金外,其他金属与浓硫酸、
硝酸反应生成盐和硫、氮的还原产物。铂、金能溶于王水。金属与盐溶液能发生置换反应。
各种金属由于它们结构上的差异而造成了性质的差异,要掌握金属性质的递变规律。
2. 金属冶炼的基本方法有电解法、还原法和加热法。根据金属的活动性差异而选择不
同的方法。
3. 过氧化钠、氢氧化铝和铁盐、亚铁盐的性质。
过氧化钠具有强氧化性,具有漂白作用,能与水、酸、酸性氧化物反应。
氢氧化铝是典型的两性氢氧化物,在水溶液中有两种电离方式,能溶于强酸或强碱
溶液。
+2价铁和+3价铁的代表物是亚铁盐和铁盐,它们在一定条件下通过氧化还原反应相互
转化。
4.阅读与思考。
阅读下述资料,可以使你对碱金属的知识有进一步了解。
The members of Group IA, or the alkali metal family, are lithium(Li), sodium(Na), potassium
(K), rubidium(Rb), cesium(Cs), and francium(Fr).
The name alkali comes from an Arabic word that means ashes. Sodium and potassium
compounds are present in the ashes of burned plants.
All of the alkali metals are soft enough to be cut by a knife. When cut, their shiny metallic
surfaces become exposed to the oxygen in the air. This causes the reactive metals to tarnish rapidly.
Indeed, one of the most remarkable characteristics of the members of this family is their intense
chemical reactivity. All of the alkali metals react with water as well as with air. As you might imagine,
this behavior causes storage problems. The alkali metals are commonly stored in evacuated metal
containers. Once a container is opened, the metals must be placed in oil to protect them from oxygen
and moisture.
Why do you suppose the alkali metals are the most reactive family of metals? You know that
all of these elements possess a single valence electron. Because of their low ionization energies, the
129
0812896-06-ok Page 129 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPCalkali metals readily lose this electron, forming ions with a 1 + charge. The ease with which an atom
loses a valence electron increases as the size of the atom increases. As a result, the reactivity of
alkali metals increases going down the family. Thus lithium reacts moderately with water,
whereas cesium and francium react more explosively with water.
130
0812896-06-ok Page 130 2011.4.7, 4:16 AM Adobe PageMaker 6.5C/PPC7
烃
HYDROCARBONS
烃是由碳和氢两种元素组成的化合
物,由于成键方式不同,可分为烷烃、烯
烃、炔烃和芳香烃等。它们是数量庞大的
有机化合物家族中最基础的物质,其他
各种有机化合物几乎都可以从烃类化合
物衍生出来。本章我们将分类学习各类
烃的组成、结构和化学性质,探究物质结
构和性能的相互关系,学习物质转化的
一些规律。
天然气、煤、石油不仅是人类重要的
能源,也是极其宝贵的资源,其中存在着
许多烃类化合物,它们是基础化工原料,
广泛用于塑料、橡胶、合成纤维以及染
◆ 烷烃、烯烃、炔烃、芳香烃
料、涂料、化妆品、医药等工业生产。性
◆ 系统命名法
能各异的有机化合物的合成使我们的生
◆ 同系物
活更加丰富多彩。但是,地球上的能源和
◆ 同分异构现象
资源是有限的,我们必须用可持续发展
的理念和化学知识来认识如何合理开发 ◆ 取代反应、加成反应、氧化反
利用能源和资源,使烃类的自然资源更
应、聚合反应
好地造福于人类。
131
0812896-07-OK Page 131 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC烃的分类和同系物
7
.1
(CLASSIFICATION OF HYDROCARBONS AND HOMOLOG)
烃的同系物
我们已学过甲烷、乙烯、乙炔、苯等烃类物质,初步掌
握了它们的组成、结构和性质的知识。在烃类中,乙烷和丙
烷的结构和性质都与甲烷相似,分子中的碳原子之间都以
碳碳单键结合成链状,碳原子的其他价键全部跟氢原子相
结合,这样的烃叫做饱和链烃,也叫烷烃(alkane)。
化学上,把结构相似、组成上相差1个或若干个某种原
子团的化合物互称为同系物。烷烃中的甲烷、乙烷、丁烷
图 7.1 乙烷、乙烯、乙炔分
等,它们相差n个CH ,互为同系物。
2
子的球棍模型
在链烃中,还有许多烃,它们分子里的碳原子所结合
的氢原子数比相同碳原子数的烷烃所结合的氢原子数少,
这类烃叫做不饱和链烃。含碳碳双键的不饱和烃叫做烯烃
(alkene),乙烯(CH=CH )是最简单的烯烃。含碳碳叁
2 2
键的不饱和烃叫做炔烃(alkyne),乙炔(CH≡CH)是最
简单的炔烃。
资料库
2008年有机化学名
词中关于同系物的概念
具有共同的化学通 试讨论乙烷、乙烯、乙炔分子结构特点和化学性质的
式,在组成上相差一个 关系。
或几个碳原子基团,化 (提示:乙烷、乙烯、乙炔的化学性质与什么有关?)
学性质相似,物理性质
随碳原子数的增加而规
律性地变化的化合物系
列中的各化合物互为同
系物。
132
0812896-07-OK Page 132 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC资料库
1.试分析下列烯烃和炔烃分子结构及特点。
表 7.2
键能
表 7.1 化学键
(kJ/mol,25℃)
烃 化学式 结构简式
C─C 347
丙烯 C H CH =CH─CH
3 6 2 3
C=C 612
丁烯 C H CH =CH─CH ─CH
4 8 2 2 3
C≡C 838
丙炔 C H CH≡C─CH
3 4 3
丁炔 C H CH≡C─CH ─CH
4 6 2 3
2.试分析上述烯烃和炔烃分子组成的变化规律,推导
烯烃和炔烃分子组成的通式。
烷烃:__________________。
烯烃:__________________。
炔烃:__________________。
我们已经学过苯( )的组成和结构,还有许多与
苯具有相似结构和性质的物质,如甲苯(CH ─ )、乙
3
苯(CH CH ─ )、丙苯(CH CH CH ─ )等分子,
3 2 3 2 2
它们的结构中都有一个苯环,在组成上也依次相差一个
CH 原子团,它们都是苯的同系物。
2
分析甲苯、乙苯、丙苯的分子组成及结构特点,推导苯
的同系物的通式。
表 7.3
有机物 分子式 结构特点 苯的同系物通式
甲苯
乙苯
丙苯
互为同系物的物质,它们的分子结构具有共同的特点,
化学性质很相似。我们根据同系物性质的相似性,对有机
物进行分类。
133
0812896-07-OK Page 133 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC烃的分类
烃分子中碳原子间连接成链状的烃叫做链烃,链烃又
可以分为饱和链烃和不饱和链烃。
苯和苯的同系物是不饱和的环状烃,它们的分子结构中
含有苯环,称为芳香烃,(简称芳烃,aromatic hydrocarbon)。
烃 的 分 类
通式 代表物
饱和烃 烷烃 C n H 2n+2 ______
链烃
C H
烯烃 n 2n ______
不饱和烃
C H
烃 炔烃 n 2n-2 ______
脂环烃
环烃
单环芳烃
芳香烃
多环芳烃
说明:
1. 环烷烃指烃分子中碳原子间连接成环状的烷烃,属于脂
环烷。
2. 苯和苯的同系物属于单环芳烃,通式为C H 。
n 2n-6
[课堂练习7.1]
1.下列分子式所表示的直链烃中属于烯烃的是( )。
(A)C H (B)C H (C)C H (D)C H
12 24 8 14 21 44 9 12
2.下列各组物质,属于同系物的是( )。
(A)CH ─CH ─CH─CH 和CH ─CH ─CH ─CH ─CH
3 2 3 3 2 2 2 3
CH
3
(B)CH=C─CH=CH 和CH ─C≡C─CH ─CH
2 2 3 2 3
CH
3
(C) 和 ─C 2 H 5
(D)CH ─CH=CH─CH 和CH ─C≡C─CH
3 3 3 3
134
0812896-07-OK Page 134 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC3.下列物质中,属于苯的同系物的是( )。
(A)C H (B)C H (C)C H Br (D)C H
8 10 7 16 6 5 8 16
4.下列说法中,正确的是( )。
(A)最简式相同的物质一定属于同系物
(B)通式相同的有机物一定属于同系物
(C)属于同系物的有机物中,碳的质量分数一定相同
(D)属于同系物的有机物,它们的官能团和化学性质相同
5.有关饱和链烃的下列叙述:①都是可燃物;②特征反应是取代反应;③相邻两
个烷烃在组成上相差一个甲基。其中,正确的是( )。
(A)①③ (B)②③ (C)①② (D)只有①
6.某烯烃与H 加成后的产物是CH ─CH─CH─C(CH ) ,则该烯烃的结构式
2 3 3 3
CH CH
3 3
可能有( )。
(A)1种 (B)2种 (C)3种 (D)4种
7.下列关于烃的含碳量的说法,正确的是( )。
(A)烃分子中碳原子数越多,含碳量越高
(B)烃的含碳量越高,在空气中燃烧越充分,火焰越明亮
(C)甲烷是含碳量最低的烃
(D)乙炔是含碳量最高的烃
8.一种气态烷烃X和一种气态烯烃Y组成的混合物10g,其密度为相同条件氢气
密度的12.5倍,该混合气体通过溴水,使溴水增加质量8.4g,则X、Y可能是( )。
(A)甲烷和丙烯 (B)乙烷和乙烯
(C)甲烷和乙烯 (D)乙烷和丙烯
9.10mL某种气态烃,在50mL氧气里充分燃烧,得到液态水和体积为35mL的
混合气体。若所有气体的体积都是在同温同压下测定的,则该气态烃可能是( )。
(A)甲烷 (B)乙烷 (C)丙烷 (D)丁烷
10.实验测得乙烯与氧气混合气体的密度是氢气的14.5倍,可知其中乙烯的质量
分数为( )。
(A)25.0% (B)27.6% (C)72.4% (D)75.0%
11.在一定条件下,将4 g三种炔烃所组成的混合气体与足量的H 充分加成后可
2
生成4.4g对应的三种烷烃,则所得烷烃中一定有( )。
(A)戊烷 (B)丁烷 (C)丙烷 (D)乙烷
12.阅读下列短文。
Have you ever noticed a sign at a service station advertising high-octane gasoline?
Gasoline with a high octane rating burns smoothly and is an efficient fuel. Octane is also one
example of a hydrocarbon, an important class of organic molecules. Hydrocarbons are organic
135
0812896-07-OK Page 135 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPCmolecules that contain only carbon and hydrogen. Like octane, most hydrocarbons make
excellent fuels. They react readily with oxygen to produce carbon dioxide and water, releasing
energy and light in the process.
Aside from their practical uses, hydrocarbons serve as excellent introductions to other
classes of organic molecules. When you learn the properties, structures, and geometries of
hydrocarbons, you learn principles that apply to a host of other carbon compounds. Carbon and
hydrogen are only two elements, but you will be amazed at how diverse and interesting their
combinations can be.
136
0812896-07-OK Page 136 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC烃的命名和同分异构现象
7
.2
(NOMENCLATURE AND ISOMERISM OF HYDROCARBON)
烃的同分异构体
丁烷有两种不同的分子结构。化学上把具有相同分子 练 习
式但具有不同结构的现象叫做同分异构现象(isomerism)。
写出戊烷C H 的
5 12
具有同分异构现象的化合物互称为同分异构体(isomer)。
三种同分异构体的结构
在戊烷的三种同分异构体的分子中,碳原子排列不同, 简式。
这是由于分子中碳原子排列不同所引起的同分异构现象。 _________
___________
烯烃和炔烃的同分异构现象比相应的烷烃复杂。除了
__________。
碳原子排列不同外,还可能由于双键或叁键所在位置不同
而引起同分异构现象。
丁烯的同分异构体如下:
CH=CH─CH ─CH CH ─CH=CH─CH
2 2 3 3 3
1-丁烯(1-butene) 2-丁烯(2-butene)
CH
3
CH ─C=CH
3 2
2-甲基丙烯(2-methylpropene)
苯的同系物中,当苯环上有两个或两个以上侧链时,由
于侧链在苯环上的位置不同可引起同分异构现象。
例如,C H 的同分异构体如下:
8 10
乙苯 邻二甲苯 间二甲苯 对二甲苯
图7.2 戊烷的同分异构体
(ethyl benzene) (o-xylene) (m-xylene) (p-xylene)
137
0812896-07-OK Page 137 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC练 习
写出下列物质的分子式及类别,其中属于同分异构体的
是__________。
表 7.4
CH=CH─CH ─CH─CH CH≡C─CH─CH ─CH CH =CH─C=CH─CH
2 2 3 2 3 2 3
结构简式
CH CH CH
3 3 3
分 子 式
类 别
相同碳原子数的炔烃和二烯烃是同分异构体。
烃的命名
烷烃的命名有习惯命名法和系统命名法。例如,戊烷
(C H )有三种同分异构体,除正戊烷(n-pentane)外,还
5 12
有异戊烷(i-pentane)、新戊烷(neo-pentane),后两种化合
物的命名方法叫习惯命名法,在使用时有局限性。
在有机化学中广泛采用系统命名法,下面对烷烃的系
统命名法作初步介绍。
直链烷烃分子中碳原子数在十个以内的,用甲、乙、丙、
丁、戊、己、庚、辛、壬、癸来表示;碳原子数在十个以上
的,用数字十一、十二、十三等来表示碳原子数,例如,C H
17 36
叫十七烷。
带有支链的烷烃命名步骤如下:
(1)选定分子中最长的碳链为主链,按主链上碳原子
的数目称为“某烷”。
(2)把主链中离支链最近的一端作为起点,用阿拉伯
数字给主链上的各个碳原子依次编号定位,以确定支链的
位置。例如:
1 2 3 4
CH ─CH─CH ─CH
3 2 3
CH
3
(3)把支链作为取代基,把取代基的名称写在烷烃名
称的前面,在取代基的前面用阿拉伯数字注明它在烷烃直
138
0812896-07-OK Page 138 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC链上所处的位置,并在数字与取代基名称之间用“-”短线
隔开。例如:
1 2 3 4
CH ─CH─CH ─CH 2-甲基丁烷
3 2 3
CH (2-methylbutane)
3
(4)如果主链上有相同的取代基,可以将取代基合并
起来,用二、三等数字表示,在用于表示取代基位置的阿拉
伯数字之间要用“,”隔开。如果主链上有几个不同的取代
基,就把简单的写在前面,把复杂的写在后面。例如:
1 2 3 4 5
CH ─CH─CH─CH ─CH 2,3-二甲基戊烷
3 2 3
CH CH (2,3-dimethylpentane)
3 3
CH
3
CH ─CH ─CH ─CH ─C─CH ─CH
3 2 2 2 2 3
CH
2
CH
3
3-甲基-3-乙基庚烷 (3-ethyl-3-methylheptane)
练 习
命名下列化合物:
CH
3
(1)CH ─CH─CH ─CH─CH─CH
3 2 3
CH CH
3 3
__________
CH
3
(2) CH ─CH─CH ─C─CH
3 2 3
CH ─CH ─CH CH
3 2 2 3
__________
139
0812896-07-OK Page 139 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC资料库
烯烃和炔烃的命名
烯烃的命名跟烷烃类似,所不同的是要表示出双键的位置,命名步骤如下:
1. 选定含双键在内的碳原子数目最多的碳链为主链。
2. 把主链中离双键最近的一端作为起点,用阿拉伯数字给主链上的各个碳
原子编号。
3. 双键的位置可以用阿拉伯数字标在某烯烃的前面。例如:
1 2 3 4 1 2 3 4
CH=CH─CH ─CH CH ─C=CH─CH
2 2 3 3 3
CH
3
1-丁烯 2-甲基-2-丁烯
炔烃的命名法与烯烃相同,只要将“烯”字改为“炔”字。例如:
1 2 3 4 5 4 3 2 1
CH ─C≡C─CH CH ─CH─CH ─C≡CH
3 3 3 2
CH
3
2-丁炔(2-butyne) 4-甲基-1-戊炔
(4-methyl-1-pentyne)
苯的同系物命名时,以苯作母体,侧链(烷基)作取代
基,将取代基的名称写在“苯”字的前面。例如:
甲苯 乙苯 丙苯
练 习
当有两个和两个以上取代基时,取代基的位置可用邻、
间、对或阿拉伯数字来表示。例如:
写出C H 烯烃的同
5 10
分异构体,并命名。
_________
___________
___________
___________
___________。 邻二甲苯 间二甲苯 对二甲苯 1,2,4-三甲苯
1,2-二甲苯 1,3-二甲苯 1,4-二甲苯
140
0812896-07-OK Page 140 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC[课堂练习7.2]
1.写出己烷的同分异构体,并用系统命名法命名。
2.用系统命名法命名下列烃。
CH CH
3 3
(1)CH ─CH ─C─CH─CH
3 2 2
C H CH __________________
2 5 3
CH CH ─CH ─CH
3 2 2 3
(2)CH ─CH─CH─CH ─CH __________________
3 2 3
(3) ─CH
3
CH __________________
3
(4) ─C H __________________
2 5
3.写出下列各有机物的结构简式。
(1)2,2,4-三甲基己烷
(2)3,4,6-三甲基-5-乙基辛烷
(3)3,3-二乙基戊烷
(4)2,2,3-三甲基戊烷
4.下列物质中,属于同一物质的是__,互为同分异构体的是__(填编号)。
① CH ─(CH ) CH ② CH=CH─CH ③ CH ─CHCl
3 2 2 3 2 3 3 2
CH
3
④ CH ─CH ⑤ CH ─CH ⑥ CH≡C─CH
2 2 2 2 3
Cl Cl CH
3
5.化学式为CH 的烷烃中,在结构式中含有3个甲基的同分异构体的数目是( )。
7 16
(A)2 (B)3 (C)4 (D)5
6.某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是( )。
(A)C H (B)C H (C)C H (D)C H
3 8 4 10 5 12 6 14
141
0812896-07-OK Page 141 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC一些重要的烃类和石油化工
7
.3
(SOME IMPORTANT HYDROCARBONS AND
PETROCHEMICAL INDUSTRY)
丙 烯
丙烯的分子结构与乙烯相似,都含有碳碳双键,在化
学性质上具有相似性。
丙烯的结构与化学性质
1.写出丙烯的分子式、电子式和结构简式。
________________________
__________________________
__________________________。
2.根据丙烯的结构特点,推测丙烯的化学性质,写出有
食品包装
关的化学方程式。
________________________
__________________________
家用电器
聚丙烯 __________________________。
纤维 3.如何用实验来鉴别乙烷和丙烯。
________________________
__________________________
薄膜
__________________________。
图 7.3 聚丙烯的用途
4.查阅资料,列举聚丙烯的用途。
________________________
__________________________
__________________________。
142
0812896-07-OK Page 142 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC资料库
人 造 羊 毛
腈纶又叫人造羊毛,它是用石油的裂解产物丙烯为原料生产的。丙烯在一定
温度、压力和催化剂存在的条件下,与氨气、氧气反应,生成丙烯腈。
2CH =CH─CH + 2NH + 3O 加温加压 2CH =CH─CN + 6H O
2 3 3 2 催化剂 2 2
丙烯腈在一定条件下聚合生成白色粉末状物质聚丙烯腈。聚丙烯腈进行纺
丝,制成的纤维就是腈纶。腈纶具有质轻、柔软、保暖性好的特点,可加工制成
五颜六色的膨体纱。腈纶可以代替羊毛,制成毛线、毛毯、毛料等纺织品,是合
成纤维家族中的重要成员。
烯烃和炔烃
烯烃的物理性质一般随碳原子数目的增加而发生递变,
表现出由量变引起质变的变化规律。
大多数烯烃是无色物质,几乎都难溶于水,但能溶解
在有机溶剂里。含18个以上碳原子的烯烃常温下一般是
固体。
烯烃物理性质的递变规律
阅读并回答以下问题。
表7.5 几种烯烃的物理性质
名 称 结构简式 常温下状态 熔点(℃) 沸点(℃)
乙 烯 CH=CH 气 -169.2 -103.7
2 2
丙 烯 CH CH=CH 气 -185.2 -47.4
3 2
1-丁烯 CH CH CH=CH 气 -185.3 -6.3
3 2 2
1-戊烯 CH (CH ) CH=CH 液 -138 30
3 2 2 2
1-庚烯 CH (CH ) CH=CH 液 -119 93.6
3 2 4 2
(1)烯烃分子中,随着碳原子数的增加,熔点、沸点发生怎样的变化?常温下,烯烃的状
态跟碳原子数有什么关系?
(2)己烯的分子式为___,常温下是___态,其熔点大于__℃,小于__℃。
143
0812896-07-OK Page 143 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC炔烃和烯烃都是不饱和烃。炔烃的分子里含有碳碳叁
键,其中两个键在较少的能量下便会发生断裂。烯烃和炔
试从饱和链烃与不
烃的化学性质较活泼,能发生加成、氧化、聚合等反应。
饱和链烃的分子结构来
常温下,乙炔、丙炔和丁炔是气体,戊炔以上是液体,
比较烷烃与烯烃、炔烃的
化学性质的主要差异。 高级的炔烃是固体。炔烃的沸点、密度也随着分子里碳原
子数目的增加而递变。
表7.6 几种炔烃的物理性质
名 称 结构简式 常温下状态 熔点(℃) 沸点(℃)
乙 炔 HC≡CH 气 -80.8 (加压) -84.0
丙 炔 CH C≡CH 气 -101.5 -23.2
3
1-丁炔 CH CH C≡CH 气 -125.7 8.1
3 2
1-戊炔 CH (CH ) C≡CH 液 -90 40.18
3 2 2
1,3-丁二烯
化学上把分子中含有两个双键的链烃叫做二烯烃
(diene)。在二烯烃中,最重要的一种是 1,3- 丁二烯
(CH =CH─CH=CH ,1,3-butadiene),它是重要的有
2 2
机化工原料之一。
1,3-丁二烯有两个双键,在加成反应时,两个双键一
资料库
起断裂,又同时生成一个新的双键。例如:
不对称烯烃的加成反应
CH=CH─CH=CH +Br CH ─CH=CH─CH
不对称烯烃跟卤化 2 2 2 2 2
氢、水加成时,氢原子加 Br Br
在含氢较多的碳原子上。
例如: 这种形式的加成叫做1,4加成反应(1,4-addition)。
CHCH= CH +HO 除了生成 1,4 加成产物外,同时还会生成 1,2 加成产物
3 2 2
HPO(硅藻土)
3 4 CH 3 CHCH 3 CH 2 ─ CH ─ CH=CH 2 。在 1,3- 丁二烯加成反应中,
OH
Br Br
1,4加成产物是主要的。
1,3-丁二烯是合成橡胶的主要原料,可以从石油裂解
中得到。
144
0812896-07-OK Page 144 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC天然橡胶与合成橡胶具有相似的结构,可以看作异戊 资料库
二烯(CH=C─CH=CH ,isoprene)的聚合物。
2 2
丁二烯的加成反应
CH
3
丁二烯跟卤素、卤化
氢加成时,一般在低温时
产生较多的1,2加成物,
1.推测二烯烃分子组成的通式。 升高温度有利于1,4加成
2.1-丁烯和1,3-丁二烯是否为同系物,为什么? 反应进行。在极性溶剂中
3.写出用异戊二烯(CH 2 =C─CH=CH 2 )合成聚异戊 反应也有利于1,4加成。
─
CH
3
二烯的化学方程式。
资料库
一些橡胶的组成和用途
橡胶在工农业及国防领域中具有重要的作用。世界橡胶产量中,天然橡胶
仅占15%左右。随着石油化学工业的发展,油田气经高温裂解和分离,提纯可
得到很多制橡胶的原料。合成橡胶由于品种多、性能好,在许多场合已替代和
超过天然橡胶。
合成橡胶分为通用橡胶和特种橡胶。通用橡胶用量较大,如丁苯橡胶、顺丁
橡胶等。特种橡胶在特种条件下使用,具有耐高温、耐低温、耐油、耐化学腐蚀
和高弹性,如硅橡胶、氟硅橡胶等。表7.7列出一些橡胶的组成和用途。
表7.7 橡胶的组成和用途
名 称 单 体 化学组成 特点、用途
CH 2 =CH─C=CH 2 -[ CH 2 ─CH=C─CH 2 -] n 弹性好,做轮胎、胶
天然橡胶
CH CH 管、胶鞋、胶黏剂等
3 3
弹性好、耐磨,做飞机
顺丁橡胶 CH =CH─CH=CH -[ CH ─CH=CH─CH -]
2 2 2 2 n 轮胎等
CH =CH─CH=CH -[ CH CH=CHCH CHCH -] 耐磨、价格低,做外
2 2 2 2 2 n
丁苯橡胶
─CH=CH 胎、地板、鞋毡底等
2
CH 2 =CH─C=CH 2 -[ CH 2 ─CH=C─CH 2 -] n 耐油、难燃、耐老化,可制
氯丁橡胶
Cl Cl 耐油制品、运输带胶黏剂等
CH =CH─CH=CH
2 2 -[ CHCH=CHCH ─CH─CH -] 耐油、耐酸碱,做油封
2 2 2 n
丁腈橡胶 CH =CH
2
CN 垫圈、胶管等
CN
145
0812896-07-OK Page 145 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC合成橡胶
图 7.4 合成橡胶的用途
甲 苯
我们已学过苯的结构和性质,苯的化学性质比烯烃、炔
练 习
烃稳定,但是在一定条件下,苯也能发生某些反应。
写出苯的燃烧反应,
苯的同系物的分子中都有一个苯环,因此苯的同系物
苯分别与液溴、浓硝酸、
在性质上跟苯有许多相似之处。
氢气反应的化学方程式。
甲苯分子中苯环上的氢原子能被别的原子或原子团所
_________
___________ 取代。甲苯能跟浓硝酸与浓硫酸的混合酸发生硝化反应,生
___________ 成三硝基甲苯(trinitrotoluene,即TNT)。
___________
___________ CH 3 CH
3
___________
+ 3HO-NO 浓硫酸 O N— —NO + 3H O
___________ 2 △ 2 2 2
___________。
NO
2
三硝基甲苯是淡黄色针状晶体,不溶于水,平时比较
稳定,即使受热或撞击也不易爆炸。但是,在敏感的起爆剂
引爆下,就发生猛烈爆炸,所以TNT是一种烈性炸药,它
在国防、开矿、筑路、兴修水利等方面有广泛的用途。
由于甲苯分子中甲基和苯环的相互影响,甲苯与苯在
化学性质上存在着一定的差异。
146
0812896-07-OK Page 146 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC在通常情况下,苯不能被氧化剂所氧化。苯的同系物
分子里含有侧链,由于苯环和侧链的相互影响,侧链能被
氧化剂氧化。
苯的同系物在加热回流情况下,能使酸性高锰酸钾溶
液褪色发生氧化反应。
CH COOH
3
KMnO,H+
4
△
甲苯 苯甲酸
资料库
白色污染的危害与治理
塑料制品广泛用于家电、包装材料、日用品、
织物、农用地膜、汽车、军工用品等方面,由于它
质轻、耐用、防水、价廉,深受人们的喜爱。但是,
当人们享受生活之时,由于随意丢弃,塑料制品给
环境造成了污染,塑料袋、白色发泡塑料饭盒等随
处可见。白色污染是指废旧塑料制品的污染。塑料
图 7.5 快餐盒——白色污染
制品中有三分之一是一次性用品,如垃圾袋、尿
布、一次性饭盒等,其回收量仅为1%。
废旧塑料长年不腐烂,很难降解。聚氯乙烯塑
料里残存的氯乙烯与人长期接触,危害人体健康;
环境中的废旧塑料对土壤产生破坏力,隔绝农作物
吸收养分和水分;抛弃在陆地或水体中的塑料袋, 图 7.6 循环再生标志
易被动物误食,使动物惨遭杀身之祸;河道和海洋
中漂浮的塑料袋还会缠住船只的螺旋桨,引起船运事故。
解决白色污染已是人们十分关注的环境问题。最初人们用焚烧的方法,但焚
烧时会产生有害气体污染环境。后来人们又采取填埋方法来处理,但难分解的废
旧塑料越积越多,不仅污染了环境,又占用了人类赖以生存的土地。
解决白色污染必须从源头上入手,开发、推广和使用可降解塑料是解决白色
污染的有效对策。可降解塑料主要有光解塑料和生物降解塑料,当达到使用寿命
时,能自动降解,与自然环境同化。上海市技术监督局于1999年发布了一次性
降解餐具的强制性地方标准,要求产品在一定环境温度和土壤湿度下,埋入土
中,两周后开始降解,九周后全部与土壤融为一体。
147
0812896-07-OK Page 147 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC许多环保专家指出,世界上没有真正的垃圾,只有放错位置的资源。废旧塑
料完全可以回收利用,变废为宝。
许多国家利用废旧塑料来发热、发电、生产汽油,这不仅解决了白色污染问
题,同时也有可观的经济效益。
我国国务院办公厅2007年12月31日发布了《关于限制生产销售使用塑料
购物袋的通知》。通知指出,鉴于购物袋已成为“白色污染”的主要来源,从2008
年6月1日起,在全国范围内禁止生产、销售、使用厚度小于0.025 mm的塑料
购物袋,并实行塑料购物袋有偿使用制度。
石油化工
石油是宝贵的矿物资源,它既是当今的主要能源,又
是十分重要的化工原料,可用于制造化肥、塑料、合成橡
胶、炸药、染料、医药等。
石油主要是各种烷烃、环烷烃和芳香烃组成的混合
物。石油炼制和加工的主要目的是将这些混合物进行一定
程度的分离,同时要将含碳原子多的烃转变成含碳原子较
少的烃。
石油通过分馏得到的汽油、煤油、柴油等轻质油的产
量比较低,仅占石油总产量的25%左右。为了提高轻质油
的产量,可以采用裂化(cracking)的方法从重油中获取轻
质油。
裂化是在一定条件下,将相对分子质量较大、沸点较
高的烃断裂为相对分子质量较小、沸点较低的烃的过程。例
如,在加热、加压和催化剂存在的条件下,十六烷裂化为辛
烷和辛烯。
催化剂
C H C H + C H
16 34 8 18 8 16
加热加压
裂解(cracking)是石油化工生产中采取比裂化更高的
温度(可高达1 000℃以上),使石油分馏产物中的长链烃
断裂成乙烯、丙烯等短链烃的过程。石油裂解气的成分复
图 7.7 芳烃裂解装置 杂,主要成分为乙烯、丙烯、丁二烯、异丁烯、甲烷、乙烷、
148
0812896-07-OK Page 148 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC丁烷、炔烃、硫化氢和碳的氧化物等。裂解气经净化和分
离,就可以得到所需纯度的乙烯、丙烯、丁二烯等有机化工
原料,并用来合成塑料、橡胶等化工产品。
石油化工促进了工业、农业、医药卫生、国防建设等领
域的发展。
资料库
塑料发展简史
1846年 瑞士首次合成硝酸纤维素塑料。
1907年 比利时首次合成酚醛树脂。
1929年 德国制得聚苯乙烯,为现代高分子材料生产奠定了基础。
1933年 英国制得聚乙烯。
1935年 哈佛大学制成尼龙66。
1936年 德国首先在飞机上应用聚甲基丙烯酸甲酯。
1938年 美国制得塑料之王——聚四氟乙烯。
1945年 美国制得有机硅烷。
1963年 意大利制得聚丙烯。
[课堂练习7.3]
1.对丙烯有如下描述:①常温下不是气体,②溶于水生成丙醇,③能发生加聚反
应,④把长链烷烃进行催化裂化可以生成丙烯,⑤丙烯是重要的化工原料。其中,正
确的是( )。
(A)③④⑤ (B)①②③ (C)①③⑤ (D)②③④
2.某烃0.1mol完全燃烧后生成8.96LCO(标准状况),该烃0.1mol能和4.48L H
2 2
(标准状况)发生加成反应。该烃的结构可能是( )。
(A)CH =CH—CH=CH (B)CH —CH=CH—CH
2 2 3 3
(C)CH≡C—CH —CH (D)CH =C(CH )
2 3 2 3 2
点燃
3.天然气、液化石油气燃烧的化学方程式分别为:CH +2O CO +2H O,
4 2 2 2
点燃
C H +5O 3CO +4H O。现有一套以天然气为燃料的灶具,改燃液化石油气,应
3 8 2 2 2
采取的正确措施是( )。
149
0812896-07-OK Page 149 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC(A)两种气体进入量都减小
(B)增大空气进入量或减小液化气进入量
(C)两种气体进入量都增大
(D)减小空气进入量或增大液化气进入量
4.在①乙烷,②乙烯,③乙炔,④苯四种物质的分子中,碳碳键长由长到短的顺
序是( )。
(A)①>②>③>④ (B)①>④>②>③
(C)①>②>④>③ (D)①>③>④>②
5.与橡胶较长时间接触,不会发生反应的是( )。
(A)高锰酸钾溶液 (B)溴水
(C)浓硝酸 (D)氢氧化钠溶液
6.下列反应中,属于氧化反应的是( )。
(A)苯在铁粉作用下与液溴反应 (B)甲苯使酸性高锰酸钾溶液褪色
(C)乙烯使溴水褪色 (D)乙炔跟水反应
7.下列说法中,正确的是( )。
(A)芳香族化合物都有香气
(B)苯和苯的同系物属于芳香烃
(C)分子里含有苯环的化合物是芳香烃
(D)符合通式C H 的有机物是芳香烃
n 2n-6
CH
3
8.写出合成- [ CH ─CH- ] 单体的结构简式:
2 n
___________________________________。
9.写出CH=C─CH=CH 分别与溴加成及加聚反应产物的结构简式。
2 2
CH
3
_________________,_________________。
10.怎样鉴别邻二甲苯、己烷和1-己烯。
11.写出下列反应的化学方程式。
(1) + Cl Fe __________________________。
2
(2) + HNO 浓硫酸 ________________________。
3 △
(3) + H 催化剂 _________________________。
2 △
150
0812896-07-OK Page 150 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC12.阅读下列短文。
Just like saturated hydrocarbons,unsaturated hydrocarbons can be found in cyclic form.
There are cycloalkenes, cycloalkynes, and cyclic hydrocarbons that contain more than one
double or triple bond. However, one unsaturated cyclic hydrocarbon is especially common and
stable. This compound is called benzene. Benzene is a cyclic arrangement of 6 carbon atoms
and 6 hydrogen atoms.
While benzene exists as an individual molecule, its characteristic ring is usually found as
a part of larger molecules. Many of these compounds have distinctive odors, and for this reason
they are often called aromatic compounds. Some foods whose distinctive aromas come from
aromatic compounds include cloves, vanilla beans, and almonds. Other compounds that contain
rings similar to benzene’s ring include nucleic acids, which are key parts of DNA, and several
vitamins, hormones, and pharmaceuticals.
151
0812896-07-OK Page 151 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC小 结
1.本章学习的几类烃的结构特点、通式和化学性质。
结构特点:碳原子间以单键相结合
分子组成通式:C H
n 2n+2
烷 烃
取代反应
主要化学性质 裂化反应
氧化反应
结构特点:分子中有一个碳碳双键
分子组成通式:C H
链烃 烯 烃 n 2n
加成反应
主要化学性质 氧化反应
聚合反应
结构特点:分子中有一个碳碳叁键
烃
炔 烃 分子组成通式:C H
n 2n-2
加成反应
主要化学性质
氧化反应
环烷烃
结构特点:含有苯环,苯环上碳原子之间的键是介于
环烃
单键和双键之间的一种特殊的键
芳香烃 苯的同系物的通式:C H
n 2n-6
取代反应
苯及同系物的主要化学性质 加成反应
氧化反应
(苯的同系物侧链氧化)
2.同系物。
结构相似,在组成上相差一个或若干个某种原子团的化合物互称为同系物。
3.同分异构现象。
具有相同分子式但具有不同结构的现象叫做同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
152
0812896-07-OK Page 152 2011.4.7, 4:17 AM Adobe PageMaker 6.5C/PPC8
烃的衍生物
DERIVATIVES OF HYDROCARBONS
烃的衍生物种类繁多。本章我们将
分类学习一些烃的衍生物,掌握卤代
烃、醇、酚、醛、酸和酯的分子结构特
点、化学性质以及相互转化关系;了解
有机物分子中官能团对化学性质所起的
决定作用;探究一些有机物分子中原子
或原子团间的相互作用及其与性质的关
系。我们还将学习与生命密切相关的油
脂、氨基酸的组成和性质。
有机化合物在生产、生活和医药等
方面有着广泛的应用。人们新发现、合
成的有机化合物每年在急剧增加,有机
化合物在人类的衣食住行、社会经济各
◆ 烃的衍生物、官能团
方面起着愈来愈重要的作用。但是人们
◆ 卤代烃、醇、酚、醛、酸、酯
必须清醒地认识到由于处置不妥而引起
◆ 油脂、氨基酸
的有机化合物对环境的污染和对生物的
◆ 消除反应、酯化反应、水解反
危害。本章我们将用科学的思想和方法
来探究问题,了解有机化合物在社会进 应、氧化反应、还原反应
步与人类文明中所起的作用,为今后学
习有机化学和生命科学打下良好的基础。
153卤代烃
8
.1
(HALOHYDROCARBON)
卤代烃的结构特点
烃分子里的氢原子被卤素原子取代后所生成的化合物
叫做卤代烃。卤代烃的种类很多。根据分子里所含卤素的
不同,卤代烃可分为氟代烃、氯代烃、溴代烃;根据烃基
的不同又可分为饱和卤代烃、不饱和卤代烃和芳香卤代
烃;根据分子里含卤原子的多少可以分为一元卤代烃和多
元卤代烃。
一元卤代烃用R-X表示,其中R代表烃基,X代表卤
原子。一元卤代烷烃的通式可以用C H X来表示。
n 2n+1
卤代烃的性质
卤代烃不溶于水,但溶于有机溶剂,沸点和密度都大
于相应的烃。
154卤 代 烃
阅读表8.1,并回答问题。
表 8.1
卤代烃名称 结构简式 沸点(℃) 相对密度*
一氯甲烷 CH —Cl -24.2 0.9159
3
一氯乙烷 CH —CH —Cl 12.3 0.8978
3 2
1-氯丙烷 CH —CH —CH —Cl 46.6 0.8909
3 2 2
2-氯丙烷 CH —CH—CH
3 3
35.7 0.8617
Cl
1-氯丁烷 CH —CH —CH —CH —Cl 78.44 0.8862
3 2 2 2
2-氯丁烷 CH —CH —CH—CH
3 2 3
68.2 0.8732
Cl
2-甲基-2-氯丙烷 CH
3
CH —C—Cl 52 0.8420
3
CH
3
*系该物质在20℃时的密度与水在4℃时的密度之比。
卤代烃的密度随着烃基中碳原子数目的增加而发生怎样的变化?
___________________________________________________________________。
卤代烃的化学性质通常比较活泼,卤原子能被多种
原子或原子团所取代。卤代烃跟水发生取代反应时,卤原
子被羟基取代,该反应又称水解反应,卤代烃的水解是可
逆的。
图 8.1 溴乙烷分子的比例
模型
探究与实践
卤代烃的水解反应
取两支试管分别滴入15滴溴乙烷,在一支试管中加入5滴硝酸银溶液,
振荡试管,加热。在另一支试管中,先加入1 mL 5%的氢氧化钠溶液,充
分振荡,加热、静置,待液体分层后,用滴管取10滴上层水溶液,并移入
另一洁净的试管中,加入1 mL稀硝酸再滴加数滴硝酸银溶液。
155实验现象:__________________________________________________。
分析与推理:________________________________________________。
结论:
1.加入氢氧化钠的作用:_____________________________________。
加入硝酸的作用:_________________________________________。
2.溴乙烷水解的化学方程式为:
__________________________________________________________________。
稀硝酸 AgNO
3
CHBr与氢
2 5
氧化钠溶液
反应混合物 AgBr沉淀
中的水层液
图 8.2 溴乙烷的水解反应
卤代烃跟强碱(如NaOH或KOH)的醇溶液共热,相
邻的两个碳原子上脱去卤化氢而生成烯烃。例如:
醇
CH ─CH─CH + NaOH —→ CH CH=CH + NaBr + H O
3 2 △ 3 2 2
H Br
有机物在适当条件下,从分子中相邻的两个碳原子上
脱去一个小分子而生成不饱和(双键或叁键)化合物的反
应叫做消除(消去)反应(elimination)。
资料库
卤代烃的消除反应
卤代烃发生消除反应时,氢原子主要从含氢较少的碳原子上脱去。例如:
醇
CH CH CHCH +NaOH—→CH CH=CHCH +NaBr+H O
3 2 3 △ 3 3 2
(占81%)
Br
(CH CH CH=CH ,占19%)
3 2 2
156几种重要的卤代烃
卤代烃有广泛的用途,除了直接应用外,许多卤代烃
常用于制备其他重要的有机化合物。
1. 三氯甲烷(CHCl ,chloroform) 资料库
3
三氯甲烷又名氯仿,是无色,易挥发的液体,难溶于
小心保存氯仿
水,具有特殊气味,应保存在密闭的棕色瓶里。三氯甲烷可
用作溶剂,是合成染料、药品等工业原料;因它具有强烈的
氯仿(CHCl
3
)本身有
毒,而它在日光照射下,
麻醉作用,曾用作麻醉剂。
更能氧化成剧毒的光气,
2. 四氯化碳(CCl ,carbon tetrachloride)
4
因此要保存在棕色瓶中。
四氯化碳是无色、易挥发、不可燃的液体,是良好的非
日光
2CHCl+O —→2COCl+2HCl
极性溶剂,能溶解脂肪、油漆、树脂等物质,也可用来制取 3 2 2
光气
二氟二氯甲烷等有机物。四氯化碳的蒸气有毒,在使用时
要注意通风。
3. 氯乙烯(CH = CHCl,vinyl chloride)
2
氯乙烯是无色的气体,在一定温度、压力及催化剂
存在下能发生加聚反应,生成白色粉末状的聚氯乙烯。
聚氯乙烯塑料常用于雨衣、人造革、塑料薄膜及管道制
品的生产。
4. 氟氯代烷
氟氯代烷大多为无色、无臭的气体,无毒、不燃烧、易
挥发、易液化,广泛用作制冷剂、雾化剂、发泡剂以及电子
航空工业的溶剂、灭火剂等。由于氟氯代烷化学性质稳定,
在大气中随气流上升,在平流层中受紫外线照射,发生光
解,产生氯原子。氯原子起催化作用,破坏臭氧层,导致臭
氧浓度减少,使更多紫外线照射到地面,危害地球上的人
类、动物和植物,并造成全球性的气温变化。为了保护臭氧
层,人类采取了共同行动,签订了以减少并逐步停止生产
和使用氟氯代烷为目标的《保护臭氧层维也纳公约》《关于
消耗臭氧层物质的蒙特利尔议定书》等国际公约。
157资料库
1211灭火剂
1211灭火剂的主要成分是二氟一氯一溴甲烷(CF ClBr),常温常压下呈气
2
态,沸点为-4℃,灭火剂在钢瓶中处于加压液化状态。灭火剂跟燃烧物接触时,
受热而产生溴离子,跟燃烧物产生的氢自由基化合,使燃烧的链反应迅速中止,
把火扑灭。1211适用于扑灭油类、有机溶剂、高压电气设备和精密仪器,灭火效
率比二氧化碳高,灭火后不留痕迹。
资料库
注意食品安全,以防二 英污染
1999年,比利时等四国相继发生禽畜类制品和奶制品被二 英污染事件,在
全球掀起轩然大波,如何保证食品安全以防二 英污染是全球人类关注的环境问
题。目前确认的二 英物质约有几十种,其中以TCDD毒性最强,其化学名称为
2,3,7,8-四氯双苯并二 英,它的结构式为:
Cl─ ─O─ ─Cl
Cl─ ─O─ ─Cl
它的毒性相当于氰化钾的50~100倍。二 英不溶于水,易溶于脂肪,进入
生物体内大多沉积在含脂肪较多的组织里。鱼、肉、禽蛋及其制品最容易受到二
英的污染。
二 英的性质稳定,不易分解,在人体内分解掉50%
就需要5~10年,它一旦进入人体,不易排出体外,在生
物体内富集浓缩。 有
机
食
二 英有很强的致癌性,并具有类似激素的作 品
用,被称为“环境激素”,影响性激素、甲状腺激素、 绿 色
食
品
胰岛素等其他激素,造成神经系统及免疫系统的
无
障碍。 公
害
农
产
环境中的二 英有95%是焚烧城市垃圾产 品
生的,例如,PVC人造革等含氯塑料、含氯防
腐剂的废木材、含氯阻燃剂的纤维制品、废药
图 8.3 食品标志
品等的焚烧,都会产生不同种类的二 英。
158为了防治二 英污染环境,必须遵守环境法规,不随意焚烧垃圾,进行垃圾
分类,研究焚烧条件及废气处理。同时必须增强自我保护意识,少吃生鱼片、生
虾、生蟹等食物,多吃含纤维素的蔬菜等。
[课堂练习8.1]
1.写出下列反应的化学方程式,并指出反应类型。
(1)CH =CH —→CH Cl─CHCl—→CH =CHCl
2 2 2 2 2
(2)CH≡CH—→CH =CHCl—→ -[ CH ─CHCl -]
2 2 n
(3)CH CH CH CH Br与NaOH水溶液共热
3 2 2 2
(4)CH CHCHBrCH 与NaOH的乙醇溶液共热
3 2 3
2.下列变化中属于取代反应的是__________,属于消除反应的是__________,属
于加成反应的是__________。
─Br
(A) -→
(B)CH ─CH─CH ─CH Br—→CH ─CH─CH ─CH OH
3 2 2 3 2 2
CH CH
3 3
(C)CH ─CH─CH Br—→CH ─C=CH
3 2 3 2
CH CH
3 3
(D)CH =C─CH=CH —→CH Br─C=CH─CH Br
2 2 2 2
CH CH
3 3
3.足球运动员在比赛中腿部受伤时,医生常喷洒一种液体物质,使受伤部位皮肤
表面温度骤然下降,减轻伤员的痛感,这种物质是( )。
(A)碘酒 (B)氟利昂 (C)氯乙烷 (D)酒精
4.写出用CH ─CH─CH=CHBr为原料制取CH ─CH─CH ─CHOH和
3 3 2 2
CH CH
3 3
CH ─CH─CH─CH ─OH的化学方程式,并指出反应的类型。
3 2
CH OH
3
5.阅读下列短文。
You know that hydrocarbons are made up of carbon and hydrogen atoms. In certain
reactions, hydrogen atoms in a hydrocarbon can be replaced by other atoms. If the replacement
159atom is an element from the halogen family, an organic compound known as a halocarbon is
formed. In a halocarbon, one or more of the hydrogen atoms of a hydrocarbon have been
replaced by atoms from the halogen family. The general formula for a halocarbon is R-X, where
R symbolizes the hydrocarbon portion of the molecule, and X represents the halogen atom. The
X could stand for fluorine, chlorine, bromine, or iodine. To what group of the periodic table do
these elements belong? The halogen atom in a halocarbon is the functional group in this class
of compounds.
160醇和酚
8
.2
(ALCOHOLS AND PHENOLS)
一元醇
烃分子中一个或几个氢被羟基(-OH)取代而生成的
一类有机化合物叫做醇(alcohol)(芳香烃环上的氢被羟基
取代的则叫酚)。根据醇分子里所含羟基数目的不同,可以
分为一元醇和多元醇,含一个羟基的醇叫做一元醇。
由烷烃衍生的一元醇称为饱和一元醇R-OH,它的通
式是C H OH。
n 2n+1
资料库
醇的系统命名法
醇的命名一般用系统命名法。通常是选择带有羟基的最长碳链为主链,而以
支链为取代基,主链碳原子的编号从离羟基最近的一端开始,按照主链碳原子的
数目称为某醇。取代基的位置用阿拉伯数字标在取代基名称的前面,羟基位置用
阿拉伯数字标在醇名称的前面。例如:
OH
CH ─CH ─CH ─CH ─OH CH ─CH ─CH─CH
3 2 2 2 3 2 3
1-丁醇 (1-butanol) 2-丁醇 (2-butanol)
CH
3
CH ─CH─CH ─CH ─OH CH ─C─CH─CH
3 2 2 3 3
CH CH OH
3 3
3-甲基-1-丁醇 3,3-二甲基-2-丁醇
(3-methy1-1-butanol) (3,3-dimethy1-2-butanol)
161资料库 低级的饱和一元醇为无色中性液体,具
有特殊的气味和辛辣味。甲醇、乙醇和丙醇都
表8.2 几种醇的熔点和沸点
能与水以任意比混溶;含4~11个碳的醇为油
名称 熔点(℃) 沸点(℃) 状液体,部分溶于水;含12个碳以上的醇为
甲醇 -93.9 65 无色无味的蜡状固体,不溶于水。
乙醇 -117.3 78.5 醇分子里的羟基比较活泼,它决定着醇的
丙醇 日光-126.5 97.4 重要性质。
光气
正丁醇 -89.5 117.2
正十二醇 26 255.9
正十六醇 50 344
课堂实验
乙醇跟氢卤酸反应
按图8.4所示装置仪器,在圆底烧瓶里放入少量的溴化钠(约2~3g)加
入少量乙醇,再加入两倍于乙醇的硫酸(1∶1),塞上带有长导管的塞子,长
导管的另一端浸入装有水和冰的试管中,用酒精灯加热烧瓶。片刻后,观察
试管底部的现象。
实验现象:____________________________________________________
_______________________________________________________________。
乙醇跟氢卤酸(溴化钠和浓硫酸反应的产物)反应时,卤原子取代了羟
基生成卤代烃和水。
结论:乙醇跟氢卤酸反应的化学方程式为_______________________。
CHOH
2 5
NaBr
HSO
2 4
冰
水
CHBr
2 5
图 8.4 乙醇跟氢溴酸反应
162乙醇的化学性质
写出用乙醇制取下列物质的化学方程式,并指出反应类型。
表 8.3
制取物质 化学方程式 反应类型
乙醇钠
乙 烯
乙 醚
乙 醛
溴乙烷
乙酸乙酯
甲醇(CH OH)在结构和性质上跟乙醇相似。甲醇最初是
3
由木材干馏得到,因此又称为木精。它是无色、透明的液
体,易燃烧,有酒精的气味。甲醇能与水、乙醇等互溶。甲
醇有毒,饮用后会使人眼睛失明,量多时会致死,工业酒精
中往往含有甲醇,因此不能饮用。
多 元 醇
分子里含有两个或两个以上羟基的醇,分别叫做二元
醇和多元醇,如乙二醇和丙三醇。
资料库
CH ─OH
2
CH ─OH CH─OH
2 表8.4 乙二醇、丙三醇
CH ─OH CH ─OH 的物理性质
2 2
乙二醇 丙三醇
乙二醇 丙三醇
(glycol) (glycerol)
熔点(℃) -11.5 20
乙二醇是无色、黏稠、有甜味的液体,易溶于水和乙
沸点(℃) 197.6 290
醇,它的凝固点很低,如60%的乙二醇水溶液的凝固点
密度
是-49℃。乙二醇常用作溶剂和抗冻剂,是合成树脂、合 1.11 1.26
(g/cm3)
成纤维的重要原料。
丙三醇俗称甘油,是无色、有甜味的黏稠液体,吸水性
163资料库 强,能与水、酒精以任意比互溶。
甘油是一种重要的化工原料,它跟硝酸反应生成的三
心脏病药硝化甘油
硝酸甘油酯,又称硝化甘油,是一些烈性炸药的主要成分。
三硝酸甘油酯在医药 甘油还用于制造油墨、印泥、护肤产品、皮革加工,还可用
上有扩张血管的作用,可
作防冻剂、润滑剂等。
用作心脏病的急救药。
CH ─O─NO
2 2
CH─O─NO
2 苯 酚
CH ─O─NO
2 2
在有机化合物中,羟基跟苯环直接相连的化合物叫做
酚。苯分子里的一个氢原子被羟基取代的生成物叫做苯酚
(phenol)。苯酚俗称石炭酸。
苯酚的分子式是C H O,结构式为:
6 6
O─H
─
C
=
H─C C─H
= ,结构简式为 OH 或C H OH。
6 5
H─C C─H
图 8.5 苯酚分子的比例模型 =
C
─
H
资料库
练 习
苯酚
下列物质中哪些属于酚类?
熔点 43℃ CH OH CH
2 3
沸点 181.7 ℃ (A) (B) OH (C) CHO (D)
COOH
课堂实验
苯酚的物理性质
1.观察苯酚晶体的颜色、状态,并嗅闻气味。
取少量晶体加入试管里,将试管浸在盛有热水的烧杯中,稍后再将试管
浸在盛有冷水的烧杯中。
实验现象:___________________________________________________。
1642.向盛有苯酚晶体的试管中,加入3mL水,振荡试管。先将试管浸入
热水中,然后再将试管浸在冷水中。
实验现象:___________________________________________________。
3.向盛有少量苯酚晶体的试管中,加入2mL乙醇,振荡试管。
推断苯酚的一些物理性质:_______________________________________
__________________________________________________________________
_____________________________________________________________________。
纯净的苯酚是无色、具有特殊气味的针状晶体。苯酚
在空气中因表面部分被氧化而显粉红色。苯酚易溶于乙醇、
乙醚等有机溶剂。常温下,微溶于水,温度升高,则溶解度
增大。当温度高于70℃以上时,能与水以任何比互溶。
苯酚有毒,具有强烈的腐蚀性,使用时必须小心,如不
慎沾到皮肤上,应立即用酒精洗涤。
苯酚与乙醇的分子里都有羟基,但由于羟基所连的烃
基不同,分子里原子或原子团间的相互影响也就不同,因
此苯酚与乙醇有着不同的化学性质。
探究与实践
苯酚的弱酸性
假设:苯酚显示弱酸性。
实验设计:
1.取一支试管,放入少量苯酚 H 2 O 氢氧化钠溶液
晶体,再加入2 mL蒸馏水,振荡试
管,然后滴加数滴紫色石蕊试液。
实验现象:________________
苯酚
_____________________________。
2.取一支试管,加入少量苯酚
图 8.6 苯酚跟氢氧化钠反应
晶体,再加入2 mL水,振荡试管,
然后逐滴加入5%的氢氧化钠溶液,继续振荡试管。
实验现象:__________________________________________________。
结论: 苯酚跟氢氧化钠溶液反应的化学方程式为___________________。
165苯酚跟氢氧化钠反应,生成易溶于水的苯酚钠,苯酚显
示了酸性,苯酚在水分子作用下发生电离。
OH O-
+ H O + H O+
2 3
苯酚的酸性极弱,在水溶液中只能电离出极少量的氢
离子,苯酚溶液不能使石蕊试液变色。
课堂实验
比较苯酚与碳酸酸性的强弱
在上述实验所得的苯酚钠溶液中通入二氧化碳气体。
实验现象:______________________________________________。
在苯酚钠溶液里通入二氧化碳,
生成_____________________________ CO 2
__________________________________。
结论:苯酚钠溶液里通入二氧化
碳反应的化学方程式为____________ 澄清的苯
_________________________________。 酚钠溶液
图 8.7 苯酚钠溶液跟CO 的作用
2
在苯酚钠的水溶液里通入二氧化碳,有苯酚游离出来,
资料库
同时生成碳酸氢钠。
碳酸和苯酚的电离常数
H CO H++HCO-
2 3 3
K =4.3×10-7
i1
HCO- H++CO2- 比较乙醇分子和苯酚分子里羟基上氢原子的活泼性以及
3 3
K =5.6×10-11 苯酚与碳酸酸性的强弱。
i2
OH O-
+H O +H O+
2 3
苯酚和乙醇分子里都含有羟基(-OH)。苯酚分子里的
羟基与苯环相连接,乙醇分子里的羟基与乙基相连接。它
K=1.28×10-10
i
们羟基上的氢原子都比较活泼,苯酚和乙醇都能跟活泼金
166苯酚跟浓溴水反应,生成白色的三溴苯酚沉淀。
OH OH
+ 3Br —→Br Br↓ + 3HBr
2
Br
苯酚跟浓溴水的反应很灵敏,也可用于苯酚的定性检验。
苯酚是一种重要的化工原料,可以用来制造酚醛塑料
(俗称电木)、合成纤维(如锦纶)、医药、染料、农药和炸
药等。
电木开关
炸药
染料
锦纶渔网
软膏
农药
图 8.10 苯酚的用途
[课堂练习8.2]
1.写出乙醇与下列物质起反应的化学方程式。
(1)金属钠__________________________________________________________。
(2)氢溴酸__________________________________________________________。
2.下列四种有机物的化学式皆为C H O。
4 10
① CH CH CHCH ② CH CH CH CH
3 2 3 3 2 2 2
OH OH
CH
3
③ CH CHCH ④ CH —C—CH
3 3 3 3
CH OH OH
2
其中,能被氧化为含相同碳原子数的醛是( )。
(A) ①② (B) 只有② (C) ②③ (D) ③④
1683.写出下列变化的化学方程式。
C H → C H Br → C H OH → CH CHO
2 4 2 5 2 5 3
4.鉴别下列各组物质。
(1)苯、苯酚、甲苯
(2)戊醇、苯酚、己烯、乙苯
5.阅读下列短文。
Just as halogen atoms can be substituted into a hydrocarbon, so can other atoms or groups
of atoms. For example, an-OH group-called a hydroxyl group-might replace one or more
hydrogen atoms. In an alcohol, one or more hydrogen atoms of a hydrocarbon are replaced by
a hydroxyl group. The general formula for an alcohol is R-OH, where R represents the
hydrocarbon portion, and OH- represents the hydroxyl group. The hydroxyl group is the
functional group of an alcohol.
169醛
8
.3
(ALDEHYDES)
乙 醛
O
‖
乙醇能被氧化生成乙醛(CH ─C─H,acetal-dehyde)。
3
乙醛是无色、具有刺激性气味的液体,沸点为20.8℃,熔
点为-121℃,18℃时密度为0.7834 g/cm3。易挥发,能溶
于水,与乙醇、乙醚、氯仿等有机溶剂互溶。乙醛的蒸气对
眼睛和呼吸道黏膜有刺激作用,吸入浓度较大的乙醛蒸气
会引起中毒现象。
O
‖
乙醛分子里的醛基(─C─H)官能团对乙醛的化学性
图 8.11 乙醛分子的比例模型 质起着决定作用。
课堂实验
鉴别乙醇和乙醛
取两支试管,分别加入10%的氢氧化钠溶液2 mL,再滴入2%的硫酸
铜溶液4~6滴,振荡。然后各滴加0.5mL乙醛和乙醇,加热到沸腾。
实验现象: ___________________________________________________。
结论: _______________________________________________________。
(1)乙醛发生__________反应,氢氧化铜发生__________反应。
(2)反应的化学方程式为______________________________________。
取两支洁净的试管,分别加入1 mL 2%的硝酸银溶液,然后一边振荡
170试管,一边各滴入2%的稀氨水,直到产生的沉淀恰好消失为止(所得溶液
称为银氨溶液)。然后再分别滴入3滴乙醛与乙醇,振荡后,把试管放在热水
浴里温热。
实验现象: ___________________________________________________。
结论:乙醛发生__________反应,转化成__________。
乙醛被氧化成乙酸,银离子被还原成金属银,附在试
管内壁,形成银镜。
水浴
CH CHO+2Ag(NH ) OH——→CH COONH +2Ag↓+3NH +H O
3 3 2 3 4 3 2
醛
在有机化合物中,还有一些在分子结构和化学性质上
跟乙醛相似的物质,如甲醛、丙醛(CH CH CHO)、丁醛
3 2
(CH CH CH CHO)等,它们统称为醛类。
3 2 2
练 习
写出甲醛与下列物质反应的化学方程式,指明反应条件
与反应类型。
1.甲醛与银氨溶液反应: __________________________。
2.甲醛与新制的氢氧化铜悬浊液反应:_____________
_________________________________________________。
3.甲醛与氢气反应:_____________________________。
O
‖
醛可用R─C─H来表示,饱和一元醛的通式为C H O。
n 2n
由于醛分子里都含有醛基,它们的化学性质很相似。例如,
它们都能被还原成醇,被氧化成羧酸。
171资料库 醛基很活泼,可以发生很多反应,在有机合成中占有
重要地位。例如,酚醛树脂是用苯酚跟甲醛反应制得的,酚
缩聚反应
醛树脂是使用最早的合成树脂,具有良好的电绝缘性,不
两个或两个以上官能
易燃烧,是电木(塑料)制作的原料。
团的单体相互缩合生成高
分子化合物,同时生成小
OH
O
分子(如水、卤化氢、 氨
‖
和醇等),这种反应叫做 n +nH-C-H—酸→ [ C H O H C H ] + nH O
6 3 2 n 2
缩聚反应。
醛有广泛的用途,是重要的化工原料和化学试剂,醛
能用于药物、香料、染料的合成与制备。
资料库
酚醛树脂的制取
1. 热塑性酚醛树脂的制取。
取一支25 mm×200 mm的试管,加入4 g苯酚和2.5 mL甲醛溶液(密度
约1.1 g/cm3,浓度为36%~38%),再加1 mL浓盐酸,振荡均匀后,塞上带有
直玻璃管(长300 mm)的橡皮塞。按图示装置
把试管放在80~90 ℃的水浴中加热。试管里发
生剧烈反应,继续加热直到生成粉红色的固体树
脂,用铁丝取出固体树脂,并用水冲洗,即可得
到热塑性树脂。
2. 热固性酚醛树脂的制取。
取一支25 mm×200 mm的试管,加入2.5 g
苯酚和3 mL甲醛溶液(密度约1.1 g/cm3,浓度
为36%~38%),再加入1 mL浓氨水(浓度为
25%~28%),振荡均匀后,塞上带有直玻璃管(长
300 mm)的橡皮塞。按图示装置用沸水浴加热约
半小时,直到混合物分成两层。当底层的树脂黏
度增大时,取下试管用水冷却,等树脂固化后倒
出,用水冲洗,即可得到黄色热固性树脂。
图 8.12 酚醛树脂的制取
172含有醛基的有机物有很多。例如葡萄糖分子中就含有
醛基。葡萄糖的分子式为C H O ,结构简式为:
6 12 6
CH OH─CHOH─CHOH─CHOH─CHOH─CHO
2
它是一种多羟基醛。
葡萄糖的化学性质
1.推测葡萄糖的化学性质。
______________________
______________________
______________________。
2.用实验验证葡萄糖分子里含有醛基。
______________________
______________________。
3.写出葡萄糖有关反应的化学方程式。
(1) 在人体中的氧化反应:
______________________。
(2) 与新制的氢氧化铜反应:
______________________。
(3) 银镜反应:
______________________。
(4) 还原反应:
图 8.13 甘蔗、甜菜
______________________。
含有醛基的糖类除了葡萄糖外,还有麦芽糖,它们都 资料库
是还原性糖,蔗糖、淀粉和纤维素是非还原性糖。淀粉、纤
维素、蔗糖水解的最终产物中都含有葡萄糖,因此,我们一 表8.5 糖类
单糖 葡萄糖、果糖
般可以用银氨溶液或新制的氢氧化铜悬浊液来检验它们是
二糖 蔗糖、麦芽糖
否已经发生水解反应。
多糖 淀粉、纤维素
173[课堂练习8.3]
1.下列物质中,在常温下呈气态的是( )。
(A)乙醇 (B)甲醛 (C)乙醚 (D)乙酸
2.下列各组物质,互为同系物的是( )。
(A)CH CHO和CH CH OH (B)C H OH和CH CH OH
3 3 2 6 5 3 2
(C)CH ─OH和C H OH (D)CH CH CHO和(CH ) CHCHO
2 2 5 3 2 3 2
CH─OH
CH ─OH
2
3.下列物质中,能发生银镜反应的是( )。
(A)CH CH OH (B)CH CHO (C)CH CH OCH CH (D)CH COOH
3 2 3 3 2 2 3 3
4.下列物质中,既能发生还原反应,又能发生氧化反应的是( )。
(A)CHCH OH (B)CH CHO (C)CH COOH (D)CH CH Cl
3 2 3 3 3 2
5.丙烯醛的结构式为CH ==CH—CHO。下列有关它的性质叙述中错误的是( )。
2
(A) 能使溴水褪色,也能使高锰酸钾溶液褪色
(B) 在一定条件下与H 充分反应,生成1-丙醇
2
(C) 能发生银镜反应,表现氧化性
(D) 在一定条件下能被空气氧化
6.鉴别下列各组物质。
(1)乙醇、乙醛、苯酚、己烯
(2)乙酸、乙醇、乙醛、苯酚
(3)乙酸、乙醇、葡萄糖、淀粉
7.写出乙醛与下列物质反应的化学方程式。
(1)跟氢气反应___________________________。
(2)跟新制的氢氧化铜反应______________________。
(3)跟氧气反应___________________________。
8.写出用石油裂化气为主要原料,制取乙醛、乙二醛、乙二酸的化学方程式,指
出反应的类型。
174羧酸和酯
8
.4
(CARBOXYLIC ACIDS AND ESTERS)
羧 酸
在有机化合物中,分子里烃基(或氢原子)与羧基
O
‖
(─C─OH,carboxyl group)直接相连接的化合物叫做羧
酸(carboxylic acid)。它可以看作烃分子里的氢原子被羧基
取代后的产物。
根据羧酸分子里羧基的数目不同,羧酸可以分为一元
羧酸、二元羧酸和多元羧酸。
一元羧酸可用R─COOH来表示,饱和一元羧酸的通
式是C H O 。
n 2n 2
由于羧酸分子中都含有相同的官能团——羧基,它们
的化学性质很相似。
练 习
列举并写出乙酸分别跟金属、碱性氧化物、碱、盐、醇
反应的化学方程式。
______________________
______________________
______________________
图 8.14 乙酸分子的比例模型
______________________
______________________。
175甲酸和乙二酸
甲酸(HCOOH)俗称蚁酸(formic acid),是无色、具
有刺激性气味的液体,和水、乙醇等混溶,有腐蚀性。
甲酸的化学性质
1.写出甲酸的结构式。
________________________。
2.推测甲酸具有哪些化学性质。
________________________。
3.用实验来验证甲酸的上述性质,并写出有关反应的化
学方程式。
图 8.15 蚂蚁含甲酸
_________________________
__________________________。
资料库
甲酸在工业上主要用作还原剂、媒染剂,还可作消毒
表8.6 一些有机酸的电离常数
剂等。
名称 电离常数(25 ℃)
乙二酸(HOOC─COOH)俗称草酸(oxalic acid),它
甲酸 1.8×10-4 是最简单的二元羧酸。草酸是无色的透明晶体,通常含有
乙酸 1.8×10-5 两分子结晶水,能溶于水和乙醇。草酸是重要的化工原料,
乙二酸 5.9×10-2(指K ) 可作还原剂,能用于稀有金属的提炼。
i1
苯甲酸 6.5×10-5
资料库
食品防腐剂
为了防止食品变质,很多抗微生物防腐剂广泛用于各种食物,我国目前允许
使用的有苯甲酸及其钠盐和山梨酸及其钾盐。
苯甲酸又名安息香酸,结构简式为 ─COOH(benzoic acid),防腐效果
好。苯甲酸在水中溶解度小,大多使用它的钠盐。苯甲酸钠为白色晶体,易溶于
水和酒精,用于酱油、酱菜、果汁、果酱、汽水、蜜饯等食品的防腐,最大使用
量因食品而异,一般为0.2~1g/kg。苯甲酸钠盐适用的pH 范围为4.5~5。
176O
=
山梨酸的结构简式为CH ─CH=CH─CH=CH─C─OH,山梨酸为无色
3
针状结晶或白色粉末状结晶,在空气中长期放置易氧化变色,微溶于水而溶于有
机溶剂,一般多用其钾盐。山梨酸对霉菌酵母和好气性菌均有抑制作用,防腐效
果随pH升高而降低,山梨酸及其钾盐使用范围较广,还可用于豆、糕点制品等,
允许使用量以山梨酸汁计为0.2~1 g/kg。
国外允许使用的防腐剂还有对羟基苯甲酸酯类、丙酸及其钠盐等。
当然,食品中最好不要使用防腐剂,应提倡食用无食品防腐剂的绿色食品。
高级脂肪酸
在一元羧酸里,有些酸分子里的烃基含有较多的碳原
子,这样的羧酸叫做高级脂肪酸。例如,硬脂酸
(C H COOH,stearic acid)、软脂酸(C H COOH,palmitic
17 35 15 31
acid)和油酸(C H COOH,oleic acid)等都是重要的高
17 33
级脂肪酸。硬脂酸、软脂酸属于饱和高级脂肪酸,常温下呈
固态。油酸的烃基里有一个双键,属于不饱和高级脂肪酸,
常温下呈液态。
高级脂肪酸分子里含有羧基,具有羧酸的性质,它们
能与碱反应生成盐。例如:
C H COOH + NaOH—→C H COONa + H O
17 35 17 35 2
硬脂酸 硬脂酸钠
碳链中不含双键的链状羧酸叫饱和脂肪酸。
碳链中仅有一个双键的脂肪酸叫单不饱和脂肪酸,其
中以油酸居多。茶籽油、橄榄油、花生油和奶油中含油酸
较多。
碳链中含有二个或二个以上双键的脂肪酸叫多不饱和
脂肪酸,如亚油酸、亚麻酸、花生四烯酸等。不饱和脂肪酸
与脂质代谢有密切关系,对胆固醇代谢起着重要作用,是
人体正常生理活动不可缺少的物质。
177酯
酸和醇在加热和浓硫酸存在的条件下发生酯化反应,
生成酯和水。例如:乙酸和乙醇在浓硫酸存在下,生成乙酸
乙酯。
O O
= =
浓硫酸
CH —C—OH+H—O—C H CH —C—O—C H +H O
3 2 5 △ 3 2 5 2
乙酸乙酯是无色透明有香味的液体。乙酸乙酯属于酯
类化合物。
O
资料库
‖
酯可以用R─C─O─R’来表示。其中R和R’可以
乙酸丁酯的性质 相同,也可以不同。当 R 和 R’是烷基时,酯的通式是
C H O 。
沸点 124~126℃ n 2n 2
酯广泛存在于多种水果和花草中。例如,梨里含有乙
熔点 -78℃
酸异戊酯,苹果和香蕉里含有异戊酸异戊酯等。低级酯是
密度 0.883g/cm3
具有芳香气味的液体。酯一般比水轻,难溶于水,易溶于乙
醇和乙醚等有机溶剂。酯可用作溶剂,也可用作制备饮料
和糖果的香料,如乙酸丁酯可用于制香料。
食用香精的应用
日用香精的应用
塑料增塑剂的应用
涂料黏稠剂的应用
杀虫剂灭害灵
图 8.16 酯类物质
178在有酸或碱存在的条件下,酯能发生水解反应,生成
相应的酸和醇。
探究与实践
酯水解反应趋于完全的条件
提出问题:
(1) 酯发生水解反应的条件是什么?
(2) 怎样使酯的水解反应趋于完全?
实验设计:
在3支试管里各加入6滴乙酸乙酯,向第一支试管里加蒸馏水5.5 mL;
向第二支试管里加稀硫酸(1∶5)0.5 mL和蒸馏水5 mL;向第三支试管里加
入30%的氢氧化钠溶液0.5 mL和蒸馏水5 mL。振荡均匀后,把3支试管都
放在70~80℃的水浴里加热几分钟,比较3支试管里乙酸乙酯的变化。
实验现象:_________________________。
结果讨论:
(1) 羧酸的酯化反应与酯的水解反应的关系为:
酯化
RCOOH + HOR’ RCOOR’ + H O
水解 2
(2) 酯水解反应趋于完全的条件是________________。
羧酸酯化反应趋于完全的条件是_______________。
实验说明,在有酸(或碱)存在的条件下,酯跟水发生
水解反应,生成相应的酸(或盐)和醇。乙酸乙酯水解后生
成乙酸和乙醇。
无机酸或碱
CH COOC H +H O CH COOH+C H OH
3 2 5 2 3 2 5
△
酯类水解的程度跟反应的条件有密切关系。当有碱存
在时,碱跟水解生成的酸发生中和反应,酯的水解程度就
大;当只有无机酸存在时,无机酸只起催化作用,它不
能减少水解生成的酸,水解程度就小。
179在实际生产中,可以根据需要,控制一定条件,使反应
向所需要的方向进行。日常生活中用稀的纯碱溶液清洗炊具
表面的油脂,就是应用酯在碱性条件下水解程度较大的缘故。
化学上,用羧酸与醇反应来制取酯,另外,用其他含有
羟基的物质跟羧酸反应也能得到酯。
例如,纤维素分子是由很多单糖单元构成的,每一个
单糖单元有3个羟基,纤维素的化学式可用[CH O·(OH) ]
6 7 2 3 n
表示。纤维素可以用来制造硝酸纤维素酯、乙酸纤维素酯和
粘胶纤维等。
OH
O─NO
2
浓硫酸
(C H O )─ OH + 3n HO─NO ——→ (C H O )─ O─NO + 3n H O
6 7 2 2 △ 6 7 2 2 2
O─NO
OH 2
n n
三硝酸纤维素酯
油脂是由多种高级脂肪酸(如硬脂酸、软脂酸和油酸
等)跟甘油生成的甘油酯。它的结构可以表示如下:
O
‖
R ─C─O─CH
1 2
O
‖
R ─C─O─CH
2
图 8.17 油脂 O
‖
R ─C─O─CH
3 2
结构式里R 、R 、R 代表饱和烃基或不饱和烃基,它
1 2 3
们可以相同,也可以不同。
在酸(或碱、高温水蒸气)存在条件下,油脂跟水能够
发生水解反应,生成甘油和相应的高级脂肪酸(或盐)。例
如,硬脂酸甘油酯在有酸存在的条件下进行水解反应:
图 8.18 硬脂酸
C H COO─CH CH ─OH
17 35 2 2
HSO
2 4
C H COO─CH + 3H O 3C H COOH + CH─OH
17 35 2 △ 17 35
C H COO─CH CH ─OH
17 35 2 2
硬脂酸甘油酯 硬脂酸 甘油
180如果油脂在碱存在的条件下水解,生成高级脂肪酸盐。
这样的水解反应叫皂化反应。肥皂的主要成分是高级脂肪
酸的钠盐。
C H COO─CH CH ─OH
17 35 2 2
△
C H COO─CH + 3NaOH —→ 3C H COONa + CH─OH
17 35 17 35
C H COO─CH CH ─OH
17 35 2 2
工业上利用这个反应来制取肥皂。
氨 基 酸
氨基酸(amino acids)是蛋白质水解的最终产物。它们
可以看做羧酸分子里烃基上的氢原子被氨基(─NH )取 资料库
2
代后的生成物。羧酸分子里离羧基最近的碳原子称为α-
碳原子,该碳原子上的氢原子称为α-氢原子。当α-氢 味 精
原子被氨基取代后,所得的氨基酸就称为α-氨基酸,可用
谷氨酸钠是味精的主
O
要成分,用小麦、面筋、豆
R─CH─C─OH表示。 饼等蛋白质原料经盐酸水
解、过滤、蒸发、结晶等
NH
2
工艺制得。
下面是几种α-氨基酸的名称和结构简式:
甘氨酸(氨基乙酸) NH ─CH ─COOH
2 2
丙氨酸(α-氨基丙酸)CH ─CH─COOH
3
NH
2
苯丙氨酸(α-氨基-β-苯基丙酸)
─CH ─CH─COOH
2
NH
2
谷氨酸(α-氨基戊二酸)HOOC─CH ─CH ─CH─COOH
2 2
NH
2
蛋白质约由20种不同氨基酸组成,其中有8种氨基酸
是人体不能合成的,必须依靠食物摄入(婴儿还需组氨酸)。
181它们是苯丙氨酸、色氨酸、蛋氨酸、赖氨酸、苏氨酸、缬氨
酸、亮氨酸、异亮氨酸,这些氨基酸叫必需氨基酸。常温
下,氨基酸是晶体,可溶于水,但不溶于乙醚。
氨基酸分子里含有羧基和氨基,因此它既可以跟酸反
应,又可以跟碱反应,生成盐。例如:
CH ─COOH CH ─COOH
2 2
+HCl —→
NH NH ·HCl
2 2
氨基乙酸盐酸盐
CH ─COOH CH ─COONa
2 2
+NaOH —→ +H O
2
NH NH
2 2
氨基乙酸钠
两个α-氨基酸经缩合反应,生成的产物叫肽。其
O
‖
中─C─NH─结构叫肽键(peptide bond)。
O
‖
H N─CH─COOH + H N─CH─COOH → H N─CH─C─NH─CH─COOH + H O
2 2 2 2
R R R R
1 2 1 2
由两个α-氨基酸经缩合生成的产物叫二肽,由多个
α-氨基酸缩合生成的产物叫多肽。
资料库
蛋 白 质
蛋白质(proteins)是人体最重要的组成物质,人体的肌肉、肝脏、酶无一不
含有蛋白质。蛋白质在人体中起着调节机体的消化、呼吸、血液循环、神经活动
等作用,它是维持生命的基础物质。
蛋白质是由α-氨基酸通过肽键构成的高分子化合物。蛋白质的相对分子质
182量很大,从几千到几千万。蛋白质在酸、碱或酶的作用下,水解转化成多肽,多
肽进一步水解,最后得到各种α-氨基酸的混合物。
人体所摄入的蛋白质在酶的作用下,发生水解反应,生成氨基酸,氨基酸被
人体吸收后,又重新结合成人体所需的各种蛋白质以维持人体的生命活动。同
时,人体各组织的蛋白质也不断地分解,最后主要生成尿素排出体外。
含8种必需氨基酸的蛋白质叫完全蛋白质(如蛋蛋白、酪蛋白、球蛋白),其
他的叫不完全蛋白质(如玉米蛋白、胶蛋白)。
图 8.19 蛋白质结构的模拟图
[课堂练习8.4]
1.写出下列物质的结构简式。
(1)2-甲基丁酸 (2)丙酸 (3)苯甲酸 (4)乙二酸
2.写出丙烯酸分别跟溴水、氢氧化钠、乙醇反应的化学方程式。
3.写出下列变化的化学方程式。
O
CH CH OH → CH CHO → CH COOH ‖
3 2 3 3 —→ CH C─OCH─CH
3 3
CHBr─CH ─CH → CH = CH─CH →CH ─CH─CH
2 2 3 2 3 3 3
CH
3
OH
4.写出下列物质的结构简式。
(1)硬脂酸钠 (2)丁酸乙酯
(3)硝酸乙酯 (4)油酸甘油酯
1835.鉴别下列各组物质。
(1)乙醇、乙醛、乙酸
(2)甲酸、乙酸、乙酸乙酯
(3)葡萄糖、乙酸、甲酸
6.含不饱和脂肪酸的食物对人体具有重要的生理意义,对胆固醇代谢起着重要作
用。下列物质中属于不饱和脂肪酸的是( )。
(A)油酸 (B)软脂酸 (C)硬脂酸 (D)丁二酸
7.下列物质的主要成分不属于酯类的是( )。
(A)菜籽油 (B)胶棉 (C)酚醛树脂 (D)硝化甘油
8.有四种相同浓度的溶液:①蚁酸,②碳酸,③醋酸,④石炭酸。它们的酸性由
强到弱的顺序是( )。
(A)①③④② (B)④③②①
(C)①③②④ (D)③①④②
9.由—CH 、—OH、—C H 、—COOH 4种基团两两组合而成的化合物中,其
3 6 5
水溶液能使石蕊试液变红的有( )。
(A)2种 (B)3种 (C)4种 (D)5种
10.某有机物能使溴水褪色,也能在一定条件下发生水解反应生成两种有机物,还
能发生加聚反应生成高分子化合物,则此有机物中一定含有下列基团中的( )。
① —CH ② —OH ③ —Cl ④ —CHO ⑤ —C H ⑥ —COOH ⑦ —COOCH
3 2 3 3
(A)①③ (B)②⑥ (C)⑤⑦ (D)④⑤
11.0.1 mol某有机物的蒸气跟过量O 混合后点燃,生成13.2 g CO 和5.4 g水。
2 2
该有机物能跟金属钠反应放出氢气,又能跟新制的氢氧化铜悬浊液共热生成红色沉淀,
此有机物还能跟乙酸反应生成酯类化合物,则此酯类化合物的结构简式可能是( )。
(A)CH —CH(OCH ) —CHO
3 3
OOCCH
3
(B)CH —CH—CHO
3
(C)OHC—CH CH COOCH
2 2 3
OH
(D)OHC—CH —CH—COOH
2
12.有机化合物X,化学式为C H O ,它在氢氧化钠水溶液中回流加热,生成两
5 10 2
种产物,其中一种产物可氧化为丙醛。该有机化合物X是( )。
(A)CHCH COOCH CH (B)CH COOCH CH CH
3 2 2 3 3 2 2 3
(C)CH COOCH(CH ) (D) (CH ) CHCOOCH
3 3 2 3 2 3
13.写出α-氨基酸分别跟盐酸和氢氧化钠反应的化学方程式。
14.写出淀粉、油脂发生水解反应的产物。
18415.下列物质中属于天然高分子化合物的是______,属于合成高分子化合
物的是______。
① 淀粉 ② 葡萄糖 ③ 纤维素 ④ 油脂
⑤ 聚乙烯 ⑥ 天然橡胶 ⑦ 酚醛塑料
16.阅读下列短文。
Take a look at the carbon atom in the middle of the structural formula (RCOOH). This
carbon atom is connected to a hydroxyl group with a single bond and to an oxygen atom with
a double bond. Together, this structure of one carbon atom, two oxygen atoms, and one
hydrogen atom is called a carboxyl group, and is abbreviated—COOH. The hydrogen atom in
a carboxyl group is an acidic hydrogen. For this reason, the hydrocarbon derivatives that contain
a carboxyl group act as acids. They are called carboxylic acids, a name derived from their
characteristic carboxyl group. Carboxylic acids are identified by the presence of a carboxyl
group. The general formula for a carboxylic acid is R—COOH, which shows a carboxyl group
attached to a hydrocarbon group. Carboxylic acids are also called organic acids.
185小 结
1. 烃的衍生物的类别、官能团及其化学性质。
表 8.7
类 别 卤代烃 醇 酚 醛 羧 酸 酯
饱和一元
衍生物 C H X C H O C H O C H O C H O C H O
n 2n+1 n 2n+2 n 2n-6 n 2n n 2n 2 n 2n 2
通式
官能团 ─X ─OH ─OH ─CHO ─COOH
OH O
‖
代表物 C H Cl C H OH CH COOH CHCOOCH
2 5 2 5 CH ─C─H 3 3 2 5
3
(1)取代反应 (1)跟金属钠反应 (1)弱酸性 (1)还原反应 (1)酸的通性 水解反应
主 (2)消除反应 (2)跟氢卤酸反应 (2)取代反应 (2)氧化反应 (2)酯化反应
要
(3)脱水反应 (3)显色反应
化
学
(4)消除反应
性
质
(5)氧化反应
(6)酯化反应
2. 烃的衍生物的相互关系。
水解 氧化 氧化
卤代烃 醇 醛 羧酸
卤代 还原
酯
3. 油脂、氨基酸。
(1)油脂是高级脂肪酸的甘油酯。
油:常温下呈液态,如油酸甘油酯。
油脂
脂肪:常温下呈固态,如硬脂酸甘油酯、软脂酸甘油酯。
(2)蛋白质水解生成氨基酸。
α-氨基酸可用R─CH─COOH表示。
NH
2
1869
化学实验探究
EXPLORATION OF CHEMICAL EXPERIMENTS
化学从孕育到诞生,就是一门实验
科学。当今,化学家们对合成的或新发现
的未知物质的研究,对于化学新理论的验
证,主要手段仍然是实验。只是在实验方
法、工具、仪器、材料,以及实验设计的
广度和精度等方面与过去已大相径庭了。
学好化学,要动手做实验。这不仅有
助于理解和记忆化学知识,还能学会许
多解决问题的科学方法和思维方法,提
高科学观察和实验设计的能力,同时还
能获得探究未知世界的乐趣,培养实事 ◆ 常见气体的制备
求是的科学态度。 ◆ 物质的提纯与分离
我们已经学过许多实验操作和做过 ◆ 无机物的检验
简单的实验设计,本章将进一步充实提 ◆ 定量实验
高,使之形成比较系统的实验基础,为学 ◆ 化学探究实验
习高等化学奠定扎实的基础。
187
09-ok Page 187 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPC常见气体的制备和净化
9
(PREPARATION AND PURIFICATION OF GENERAL
.1
GASES)
中学化学实验中,物质的制备主要是气体的制备。下
面把已学过的气体制备及有关问题作一系统归纳。
制备气体的实验装置
制备气体的实验装置是依据有关制备反应的化学原理
设计的,如反应物状态、性质和反应条件;同时还要求安
全、不污染环境以及操作简便等。
表9.1 气体制备的装置
D
B
A
我们已学过表9.1所列
实
的三类气体制备的装置,这
验
些装置各适合怎样状态的反 装
应物和反应条件? 置
E
C
要求反应物
的状态
反应条件
实 例
188
09-ok Page 188 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPCB、C装置的差异__________。
D、E装置的差异__________。
表 9.2 气体的收集方法
Ⅰ Ⅱ Ⅲ
实验装置
依据气体的性质而采用
被收集气体
不同的气体收集方法,用表
的性质
9.2所列的装置分别收集的气
体具有怎样性质?
实 例
将三类气体发生装置和三种收集方法组合,可以满足
制取气体的一般要求。例如,用氯酸钾、二氧化锰制取氧气
可采用表9.1中气体发生装置A和表9.2中气体收集装置Ⅰ
或Ⅱ。
探究与实践
设计具有启普发生器作用原理的气体发生装置
启普发生器操作简便,安全实用,是实验室必备的气体发生装置。它的
特点是随用随开、随关随停(图9.1)。适合于制取反应物为不溶性块状固体
和液体、反应不需加热的气体,如氢气、二氧化碳等。
课题:用实验室常用仪器及用品,设计具有启普发生器原理的气体发
生装置。
球形漏斗
关闭 开启
活塞
容器
图 9.1 启普发生器的构造和原理
189
09-ok Page 189 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPC设计思路:
(1)分析启普发生器的装置特点和作用原理。
(2)将启普发生器的局部装置变形,寻找替代仪器。
(3)反应物固体、液体各盛放在什么位置?开启时怎样使反应物接触,
关闭时怎样使反应物分开?
常见气体的实验室制法
写出表9.3所列气体的实验室制法的化学原理,并在
表9.1、表9.2中选择合适的气体发生装置和收集方法,填
入编号。
表9.3 几种气体的实验室制法
名 称 试 剂 化学方程式 气体发生装置 收集方法
NH
3
Cl
2
HCl
CH
4
C H (添加温度计)
2 4
C H
2 2
在中学化学里,某种气体的实验室制法虽然有约定俗
成的具体方法(包括试剂和装置等),但也不是一成不变的。
由于试剂和仪器具有一定的通用性,因此,只要化学原理
正确,操作简便,实验安全的,都能用于实验室制取气体。
1.设计一个实验室制取少量二氧化硫的方案。选择何
种试剂?采用何种气体发生装置和收集装置?
2.现要求用启普发生器制取硫化氢气体,应选择何种
试剂?
(提示:均采用酸跟盐的反应。)
190
09-ok Page 190 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPC用下面的实验装置和试剂来制取指定的气体是否合理,
请判断并说明理由。
浓氨水
HO
2 2
盐酸
石灰 次氯酸钙
MnO
2
(a)制氨气 (b)制氧气 (c)制氯气
图 9.2 几种气体制取装置
气体的干燥、净化和尾气吸收
由水溶液反应物制得的气体,往往含有水蒸气,要制
得干燥的气体,可以在发生装置和收集器之间增加一个干
资料库
燥器,干燥器中盛放干燥剂。
干燥剂是对水有结合或吸附作用的物质。用于干燥气
氯化钙与氨的反应
体的干燥剂应与被干燥气体无反应。表9.4列出的是实验室
无水氯化钙能与氨气
常用的干燥剂。
结 合 成 氨 合 氯 化 钙
(CaCl ·4NH 或CaCl ·
2 3 2
表9.4 常用的干燥剂
8NH )。
3
干燥剂 性 质
硅胶(SiO·nH O) 固态,中性,适合于大多数气体的干燥
2 2
无水氯化钙 固态,中性,除氨外,适合于大多数气体的干燥
液态,酸性,氧化性,不适合碱性和易被
浓硫酸
氧化的气体的干燥
碱石灰(NaOH、
固态,碱性,不适合酸性气体的干燥
CaO的混合物)
191
09-ok Page 191 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPC实验室常用的气体干燥器如图9.3所示。
(a)干燥管 (b)U形管 (c)自制洗气瓶
图 9.3 气体干燥器
有害气体
气体的净化是在气体混合物中除去杂质气体的操作,
图9.3的装置均可用于气体的净化。根据净化气体与杂质气
体的性质差异选择相应的吸收剂。例如,除去氢气中的硫
化氢可用氢氧化钠溶液;除去氯气中的氯化氢(盐酸酸
雾)可用饱和食盐水等。
(a)
制备气体时,多余的气体如对环境有害就要增加尾气
吸收装置(图9.4)。吸收装置中盛放的吸收剂都是很容易跟
有害气体反应的试剂,如用氢氧化钠溶液吸收尾气中的氯
气。尾气吸收装置的设计中,要防止吸收剂的倒吸。
(b)
图 9.4 尾气吸收装置
1. 分析图9.4中两种尾气吸收装置能防止倒吸的原理。
2. 请在以下试剂中选择作为氯气、硫化氢气体的吸收剂。
氢氧化钠溶液、硫酸铜溶液、浓硫酸、饱和食盐水、高
锰酸钾溶液。
192
09-ok Page 192 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPC[课堂练习9.1]
1.下列实验室制取气体的方法中,正确的是( )。
(A)CO:用大理石和稀硫酸反应
2
(B)Cl:将氯化钠晶体、二氧化锰和浓硫酸共热
2
(C)CH :用醋酸钠晶体(CH COONa·3H O)与碱石灰共热
4 3 2
(D)C H:将电石和食盐水在启普发生器中反应
2 2
2.简要回答下列问题:
(1)为什么用稀硝酸跟硫化亚铁反应不能制取硫化氢气体?
(2)二氧化硫有还原性,浓硫酸有氧化性,为什么用浓硫酸跟亚硫酸钠反应能制
取二氧化硫气体?
3.在实验室用氯酸钾制取氧气并收集的装置,还能用来制取和收集的气体是( )。
(A)NH (B)CH (C)SO (D)C H
3 4 2 2 4
4.怎样检验下列装置的气密性(除水之外,不能再用其他实验用品)?
(a) (b)
(第4题)
5.用右图装置收集以下6种气体:Cl 、HCl、SO 、NH 、NO、
2 2 3 a b
CH 。
4
(1)若装置干燥,气体从a管进入,可收集的气体是___。
(2)若装置干燥,气体从b管进入,可收集的气体是___。
(3)若装置充满水,可收集的气体是_____,此时气体应
(第5题)
从_____管进入(填“a”或“b”)。
6.在下列制取收集气体的装置中,都放一小团棉花,试说明原因。
水
KMnO
4
棉花
棉花
棉花
电石
(第6题)
193
09-ok Page 193 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPC7.如图装置能否制得干燥的下列气体:CO 、Cl 、HCl、SO 、NO。如能则请
2 2 2
填表9.5。
A
B C D
(第7题)
表 9.5
盛放试剂
气体名称 仪器D检验集满气体的方法
仪器A 仪器B 仪器C
8.除去CO 中含有的SO ,采用的方法是( )。
2 2
①NaOH ②品红溶液 ③亚硫酸钠溶液 ④酸性高锰酸钾溶液
(A)①③ (B)①④ (C)③④ (D)②④
9.检验SO 中含有的CO ,应采用的方法是( )。
2 2
(A)通过澄清石灰水
(B)通过品红溶液
(C)依次通过酸性高锰酸钾和澄清石灰水
(D)依次通过碳酸氢钠溶液和澄清石灰水
194
09-ok Page 194 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPC物质的提纯与分离
9
(PURIFICATION AND ISOLATION OF CHEMICAL
.2
SUBSTANCES)
为了研究物质的性质和组成,常常需要把混合物进行
提纯和分离。将混合物中的主要成分或指定成分分离出来,
而把其他杂质除去,称为物质的提纯;将混合物中各组成
物质分开,得到比较纯净的物质(恢复到原来的状态或指
定状态),称为物质的分离。
物质提纯分离的基本操作
1.过滤。
过滤(filtration)是将不溶性固体和液体分离的方法(图
9.5)。
思考:过滤操作中,为什么要使漏斗下端导管贴紧烧
杯内壁?
2.蒸发和结晶。
这是从溶液中分离出固体溶质的方法,蒸发操作如图
9.6所示。蒸发可以将溶剂蒸发完全使溶质析出,这时得到
图 9.5 过滤
的是溶液中的全部溶质(往往是不太纯的物质);也可以蒸
发部分溶剂使之成为浓溶液。
思考:蒸发时,当接近蒸干时为什么要停止加热,利用
余热将溶液蒸干?
结晶也是一种从溶液中分离出固体溶质的方法。当溶
液加热浓缩或蒸发至接近饱和(在液面中有一薄层晶体
膜),然后冷却浓溶液,使其中含量最多、其溶解度随温度
降低而减少较多的溶质从溶液中析出,这一过程叫结晶。在
结晶过程中,由于杂质会较多地残留在母液中,因而得到 图 9.6 蒸发
195
09-ok Page 195 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPC资料库 的是较纯的物质。如果需要更纯的物质,可以再一次结晶,
多次结晶的操作叫重结晶。重结晶是提纯许多无机物的主
加热氯化铝、氯化铁水溶液
要方法。
氯化铝、氯化铁溶液 思考:结晶水合物(如胆矾CuSO·5H O、皓矾等)和
4 2
在蒸发时,由于Fe3+、Al3+ 某些易水解的挥发性酸的盐类(如氯化铝AlCl 等)从溶液
3
水解随温度升高渐趋强 中析出,为什么一定要用结晶的方法?
烈,生成的盐酸挥发,故 3.蒸馏。
当溶液蒸干时,得到的将 蒸馏(distillation)是利用液体混合物各组分的沸点不
是Al(OH)
3
、Fe(OH)
3
或
同,使低沸点液体先汽化变成蒸气,再由蒸气冷凝成液体,
Al O 、Fe O 。
2 3 2 3 从而把它从液体混合物中分离出来的操作。
蒸馏装置由蒸馏烧瓶、温度计、冷凝管、接液管和锥形
瓶装配而成(图9.7)。
1.蒸馏装置中,温
水
度计的水银球为什么要
放在蒸馏烧瓶支管口?
2.冷凝管的水流方 水
向为什么要与蒸气方向
相反?
(a) (b)
图 9.7 蒸馏装置
(a)普通蒸馏装置
(b)标准口蒸馏装置,即玻璃仪器都有标准接口相互连接
4.分液和萃取。
分液是把两种互不相溶的液体分离开来的操作,分液
操作一般在分液漏斗中进行,如图9.8所示。
萃取(extraction)是利用某种溶质在互不相溶的溶剂
里的溶解度不同,用一种溶剂(称萃取剂)把这种溶质从另
图 9.8 分液 一种溶液中分离出来的操作。如用四氯化碳萃取溴水中的
溴。萃取后一般要进行分液操作。
196
09-ok Page 196 2011.4.9, 10:43 PM Adobe PageMaker 6.5C/PPC资料库
渗 析
渗析(dialysis)是纯化胶体的操作,利用半
淀粉胶体和
透膜不能透过胶体粒子,而能透过离子和小分子 食盐溶液
的性质,将溶胶中的溶质离子或小分子分离除去 半透膜
(图9.9),如用渗析可除去淀粉溶液(胶体)中的 蒸馏水
Na+和Cl-。
图 9.9 渗析
物质提纯与分离的实验设计
物质的提纯,要依据被提纯物质和杂质性质的差异选
择适宜的方法,在实际操作中,还要注意:
1.不能引入新的杂质。
2.尽量减少被提纯物质的损失。
3. 使用试剂除去杂质时,要求反应后的产物容易与被
提纯物分离。
探究与实践
在硝酸钾和少量硫酸钾的混合物中分离出硝酸钾
要求:依据硝酸钾、硫酸钾的溶解度随温度变化的差异(表9.6),用结
晶的方法来提纯。
表9.6 硝酸钾和硫酸钾的溶解度(g/100g 水)
t(℃) 0 10 20 40 60 80 90
KNO 13.9 21.2 31.6 61.3 106 167 203
3
K SO 7.4 9.3 11.1 14.8 18.2 21.4 22.9
2 4
实验步骤设计:在以下流程的空位中,填写操作名称并回答有关思考
问题。
197
09-ok Page 197 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC过量 适量
试样 蒸馏水
KNO 晶体 重复操作Ⅰ
混合 冷却 3 烘干
至操作Ⅲ
操作Ⅰ 操作Ⅱ 操作Ⅲ 操作Ⅳ KNO 3 晶体
残液
思考:
1.操作Ⅳ后获得的硝酸钾为什么要重复再一次结晶?
2.操作Ⅳ,残液的成分是什么?
课堂实验
氯化钠的提纯
课题:除去氯化钠固体中少量的硫酸钠、氯化钙。
要求:选择合适的试剂使硫酸钠转化成沉淀来除去。
实验步骤设计:在以下流程的空位中填写操作名称,并回答思考中的有
关问题。
试样 蒸馏水 试剂A(稍过量) 试剂B(稍过量) 试剂C
沉淀 沉淀 调节pH 蒸发
操作Ⅰ 操作Ⅱ 操作Ⅲ 操作Ⅳ
滤渣 NaCl
晶体
思考:
1.试剂A是____,试剂B是____,稍过量的原因是什么?
2.操作Ⅲ得到的滤渣的成分是什么?
3.试剂C是____,为什么要调节滤液pH?
4.最后得到的氯化钠与试样中的氯化钠质量是否相等?
(提示:分析全部提纯操作中氯化钠质量可能的损失或增加。)
198
09-ok Page 198 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC学生实验
分离氯化铁和氯化铝的混合溶液
1. 本课题能学到哪些知识、方法和技能,确定分离的方法。
2. 怎样将以下实验步骤(3)的滤液制成氯化铝溶液,在空白处写出简明实验
步骤和画出操作图。
3. 完成本课题需要哪些实验用品?
将讨论的结果填入有关实验报告中,在实验室中完成实验步骤(1)至实验步
骤(5)。
实验步骤:
(1)取10 mL待分离 (2)逐滴滴加6 mol/L氢 (3)将上述混合物过滤
的混合溶液于小烧 氧化钠溶液,直至产生沉
杯中 淀不再继续溶解为止
氢氧
化钠
(7) (6) (4)将滤纸上
的固体用蒸
馏水洗涤后
盐酸
移入小烧杯
中,逐滴滴入
2mol/L盐酸,
直至固体完全
滤液 溶解为止 滤液
(8) (5)取2 mL
上述溶液,
滴加硫氰化
钾溶液,观
察现象
199
09-ok Page 199 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC[课堂练习9.2]
1.下列仪器中,常用于分离物质的是( )。
①漏斗 ②分液漏斗 ③容量瓶 ④天平 ⑤量筒 ⑥胶头滴管 ⑦蒸馏烧瓶
(A)①③⑥ (B)①②⑦ (C)②⑤⑦ (D)③④⑤
2.指出下列实验操作的错误或不妥之处,分析后果并加以改正。
(1)用蒸发至干的方法得到AlCl 晶体。
3
(2)蒸馏时,温度计水银球插入蒸馏混合液中。
(3)分液时,分液漏斗中下层液体从下口放出后,换一承接器再放出上层液体。
(4)用蒸馏的方法降低水中钙镁离子的含量。
3.下列分离物质的方法中,根据微粒大小分离的是( )。
(A)萃取 (B)重结晶 (C)沉降 (D)渗析
4.粗盐中含有Ca2+、Mg2+、SO2-等杂质离子,精制时所用试剂为盐酸、氯化钡溶
4
液、碳酸钠溶液和氢氧化钠溶液,加入试剂的顺序是______________,
并写出有关的离子方程式 __________________________
_____________________________________。
5.下列物质提纯除去括号内的杂质,写出应加入的试剂(不能引入新的杂质)。
(1)FeCl(FeCl ),加入试剂______,有关离子方程式______。
2 3
(2)NaOH(Na CO ),加入试剂______,有关离子方程式______。
2 3
6.某溶液中含有较多的Na SO 和少量的Fe (SO ) ,若用此溶液制取芒硝
2 4 2 4 3
(Na SO·10H O),可供选择的操作有:①加适量硫酸;②加金属Fe;③冷却结晶;
2 4 2
④加过量氢氧化钠溶液;⑤过滤;⑥加强热脱去结晶水;⑦加热浓缩。
正确的操作步骤(用编号填入,可重复选择)为______________。
画出操作流程图。
7.用含少量铁的氧化铜制取氯化铜晶体(CuCl·2H O)。试样经稀盐酸溶解、过
2 2
滤后得pH=2的滤液,将滤液作如下操作:
通Cl 加入试剂A,调节pH
2
滤液 溶液 滤液
氧化 沉淀反应 过滤 结晶 CuCl·2HO
(Cu2+、Fe2+、Cl-) 2 2
沉淀B
200
09-ok Page 200 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC提供信息:已知在pH范围为4~5时,Fe3+几乎完全水解而沉淀,而Cu2+不水解。
(1)写出通入Cl 后,反应的离子方程式______________。
2
(2)在沉淀反应中,加入的试剂A是______,目的是______(均选
择填空)。
a.NaOH b.CuO c.提高溶液的pH d.降低溶液的pH
e.使Fe3+完全沉淀 f.使Cu2+完全沉淀
(3)沉淀B的化学式______,写出形成B的离子方程式______。
(4)结晶的方法是______(用编号填入)。
a.过滤 b.冷却 c.蒸发浓缩 d.蒸发至干
201
09-ok Page 201 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC物质的检验
9
.3
(IDENTIFICATION OF CHEMICAL SUBSTANCES)
物质的检验是物质分析的主要内容,通过物质检验可
以知道物质的各种成分及组成,再加上定量分析可得到各
种成分的含量。
科学研究、国民经济、军事国防等各部门都广泛进行
物质的分析和检验。近几十年来,随着物质分析方法的进
步,各种高精密检测仪器的涌现,人们不仅能检出毫克、微
克数量级的物质,还能捕捉到纳克痕量级物质的存在。
未知物的检验按怎样的顺序进行?其中包括哪些检验
方法和操作?怎样设计合适的检验步骤,以便能迅速推断
出结论?本节将把以前所学的无机物检验的知识归纳、提
高,形成较清晰的系统知识。
物质检验的一般顺序
我们知道,对未知物是无机物的检验实质是对其组成
离子的检验,大多数情况下是把未知无机物转化成溶液试
样,再通过溶液中的离子反应来检验的。最后是分析各检
验反应的现象,综合推论得出结论。
无机物检验的一般顺序如下:
外表观察
初 灼烧试验 阳离子检验
步 溶液试样 分析综合
试样 试 的pH 检验 得到结论
验 水溶性试验 阴离子检验
酸溶性试验
202
09-ok Page 202 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC课堂实验
孔雀石的检验
对某碳酸盐矿物,如孔雀石(碱式碳酸铜)作检验的初步试验。
(1)外表观察。
观察记录:_________________________。
(2)灼烧试验:取少量固体试样,研磨成粉末放在试管中加热,观察。
现象:___________________________。
(3)水溶性试验:取少量试样粉末,用少量
蒸馏水溶解(可加热),观察。
现象:________________
_____________________。
(4)酸溶性试验:取少量试样粉末,加入少
量稀盐酸,观察。
现象:________________
图 9.10 孔雀石
_____________________。
初步试验中,外表观察包括观察固体试样的颜色、色
泽、硬度等,对液体、气体试样特别要注意其气味。灼烧试
验是对试样作加热和灼烧,观察试样是否有颜色变化、气
体放出或熔化、升华现象。水溶性试验,不仅可获得有关试
样组成的信息,而且能了解如何制备成供检验分析的溶液
试样。对于不溶于水的固体还要作酸溶性试验,观察是否
溶于酸(如盐酸、稀硫酸、硝酸等)以及溶于酸时是否有气
体放出等。
物质检验时应注意:
1.取用尽可能少的样品和试剂。
2.多步检验时,一般要另取试样,以免试剂之间的
干扰。
3.所加检验用的试剂,不能含有待检离子。
4.按设计的步骤作检验时,每一步检验后,要作肯定
或否定的结论,逐步缩小范围,最终获得结论。
203
09-ok Page 203 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC离子检验的常用方法
用以检验某种离子的反应都应具有明显的外部特征,
即有可观察的现象,而且是该离子能区别于其他离子的特
征现象。按现象的差异,离子检验的常用方法有沉淀法、显
色法和气体法(表9.7)。
表9.7 离子检验的方法
检验方法 含 义 示 例
Cl- :滴加硝酸银溶液、
硝酸,产生白色沉淀
检验反应中有沉淀
沉淀法 SO2- :滴加氯化钡溶液、
的产生或溶解 4
1. 如何鉴别碳酸钠、 盐酸或硝酸钡溶液、硝酸,
亚硫酸钠两种无色溶液? 产生白色沉淀
2. 只用一种试剂鉴
检验反应有溶液颜 Fe3+:滴加硫氰化钾溶液
别四种无色溶液:氯化 显色法
色的变化 产生红色溶液
钠、氯化铵、硫酸钠和硫
酸铵。 检验反应能产生气
CO2-:用稀盐酸酸化,产
3. 不用其他试剂,利 体,根据气体的颜色、 3
生无色、无刺激性气体,将
用未知溶液的相互反应 气体法 气味或气体再跟一定
气体通入澄清石灰水,产生
来鉴别四种无色溶液:碳 试剂反应的明显现象
白色沉淀
酸钠、稀盐酸、氯化钙和 加以确认
氯化钠。
离子检验的课题有多种形式。有确定某物质离子组成
的鉴定,有多种离子溶液的鉴别,也有在混合离子溶液中
检出某几种离子等。
检验时一般要求选用合适的试剂,设计较少的操作步
骤,达到现象明显,操作简捷的要求。例如,只用一种试剂
鉴别多种溶液的课题。
纸上层析法
在某些分子或离子混合溶液的分离、检验时,因它们
的化学性质十分相近,用一般的化学方法分离十分困难;
在混合状态下,也很难进行检验。此时,可采用纸上层析
法(paper chromatography)来分离和检验。
204
09-ok Page 204 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC纸上层析法有上升纸层析法和径向纸层析法两种。上
升纸层析法如图9.11所示,先取一张条形滤纸,将欲分离
的混合离子溶液(试样)点滴在滤纸的一端,然后把这一端
浸入水和有机溶剂的混合液中,这种混合溶液叫做展开剂。
由于不同离子在水和有机溶剂里的溶解度不同,因此当展
开剂沿滤纸向上流动时,试样中的各种离子就会随展开剂
以不同的速率在滤纸上展开。如果试样中的离子是有颜色
的,则可在滤纸的不同高度上看到不同离子的色斑,如果
是无色离子,则可用适当方法使其显现出来。
径向纸层析法是利用圆形滤纸进行层析的方法(图
9.12),将试液点滴在滤纸的中心,然后如图把滤纸剪开一
条,剪到点样痕迹处,将小条向下折成直角,滤纸平放在培
养皿上,滤纸小条向下浸入培养皿中的展开剂里。一段时
间后,滤纸上会出现各组分的圆环色斑。
2cm
滤纸
m
c 试液点滴
8 滤纸
1
试液点滴
展开剂
1.5cm
滤纸
展开剂
图 9.11 上升纸层析法 图 9.12 径向纸层析法
课堂实验
纸 上 层 析
1.上升纸层析法分离彩色墨水。
在一条形滤纸下端滴上一滴彩色墨水,放置晾干或电吹风吹干后,再补
滴一次(可重复2~3次)。
在试管中加入展开剂(乙醇、丁醇、1 mol/L 硫酸铵溶液按体积比
1∶1∶1配制),然后将滤纸挂在试管内,待彩色墨水中各组分逐渐展开。
现象:_________________________。
结论:彩色墨水由________________组成。
205
09-ok Page 205 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC2.径向纸上层析检验Fe3+和Cu2+。
如图9.12,在滤纸中央点滴FeCl 和CuCl 混合溶液,放置晾干或电吹
3 2
风吹干后,再补滴一次(可重复2~3次)。
将丙酮和6 mol/L 盐酸按体积比9∶1配制成展开剂,取10 mL展开剂
注入培养皿中,然后将滤纸剪开的小条浸入展开剂中,待Fe3+、Cu2+在滤纸
上展开。
2
当展开达滤纸直径约—时,取下滤纸,可观察到现象:_______
3
_________。
将硫氰化钾溶液用喷雾器喷在滤纸上,滤纸出现现象:_______
_______,检验出Fe3+。
然后将滤纸放在盛有浓氨水的培养皿中,用氨水熏*,观察到现象:_
_____________,检验出Cu2+。
*Cu2+跟氨分子结合成绛蓝色的[Cu(NH ) ]2+络离子,使Cu2+显现出来。
3 4
学生实验
离子的检验
实验内容:
(1)限用一种试剂鉴别四种无色溶液:Al(SO)、MgCl、NaNO 和NHCl。
2 4 3 2 3 4
选用试剂:_________________________。
现象与结论:________________________。
(2)利用试样间的相互反应鉴别四种无色溶液:AgNO 、Na CO 、KI和
3 2 3
HNO 。
3
简要实验步骤:_______________________。
现象与结论:________________________。
(3)检验某未知溶液中可能含有Fe3+、Na+、NH+、Cl-、CO2-、SO2-中
4 3 4
的三种离子(由教师任意设定,如Fe3+、NH+、Cl-等)。
4
简要实验步骤:_______________________。
现象与结论:________________________。
206
09-ok Page 206 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC1.本实验需要哪些实验用品?
2.设计这3个实验的实验步骤。
提示:实验(3)的设计应注意,开始时,必须考虑全部阴
离子和阳离子,再根据每一步实验现象,作出肯定或否定的
判断,逐步缩小范围,最终得到结论。
将讨论及实验结果填入有关实验报告中。
[课堂练习9.3]
1.以下各组溶液中,用盐酸、氢氧化钠都能鉴别的是( )。
①Al(NO ) 、AgNO ②Na CO 、NaCl ③NaHCO 、MgCl ④Fe (SO ) 、FeCl
3 3 3 2 3 3 2 2 4 3 3
(A)①② (B)③④ (C)①③ (D) ②④
2.以下各组物质只用一种试剂来鉴别它们,写出试剂名称、现象和结论。
表 9.8
实 验 待检物质 鉴别试剂 现 象 结 论
(1) NaHCO、KNO、NaSiO 三种溶液
3 3 2 3
(2) NHCl、BaCl、NaCO 三种溶液
4 2 2 3
(3) FeS、MnO、CuO三种固体
2
3.检验碳酸钠粉末中含有少量氢氧化钠和氯化钠,现设计以下检验流程,回答有
关问题。
加稀硝酸,再加
试样 加试剂A 加酚酞试液 试剂B
蒸馏水
溶液
溶解 沉淀反应 过滤 检验① 检验②
滤渣弃去
(1)试剂A是__,加试剂A的目的是__________________。
(2)检验①中加酚酞试液是检验_________。
(3)检验②中,将稀硝酸加至____,再加试剂B____,检验____。
4.一瓶澄清透明的溶液,可能含有Cl-、SO2-、CO2-、NH+和Na+中的一种或某
4 3 4
几种,表9.9列出实验步骤和记录。
207
09-ok Page 207 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC表 9.9
实验操作 现象记录
(1)用pH试纸检验溶液pH pH为10~11
(2)作焰色反应 亮黄色
(3)取少量试样溶液,加浓氢氧化钠溶液后,微热 无刺激性气体产生
(4)另取少量试液,滴加稀硝酸至酸性 产生气体
(5)用第(4)步试液滴加氯化钡溶液; 产生沉淀
静置,取上层清液,继续滴加氯化钡溶液 无浑浊
(6)再取上层清液于另一试管,滴加硝酸银溶液 有沉淀
回答:
(1)溶液中肯定存在_____,肯定不存在_____,可能存在_____。
(2)对上述操作作怎样的改变,才能对可能存在的离子作出肯定或否定的检验?
(3)为什么先检验CO2-,再检验SO2- ?为什么最后检验Cl-?
3 4
5.有一瓶澄清溶液,其中可能存在下列离子:NH+、Fe3+、K+、Al3+、Ba2+、Mg2+、
4
SO2-、I-和CO2-。对该溶液进行如下实验,记录如表,请对每一步实验作出相应的判
4 3
断,填入表9.10内。
表 9.10
实验操作 现 象 判 断
(1)观察 溶液为无色透明
(2)用pH试纸检验 溶液呈酸性
(3)取部分溶液加入四
四氯化碳层无紫色出现
氯化碳及氯水
(4)另取少量溶液逐滴 有白色沉淀,逐渐增加,
滴加氢氧化钠溶液 后又逐渐溶解直至澄清
有刺激性气体产生,
(5)再将上述溶液加热
使湿润红色石蕊试纸变蓝
(6)另取部分溶液,加
出现白色沉淀
入硝酸钡溶液
透过蓝色钴玻片观察有
(7)进行焰色反应
浅紫色火焰
结论:该溶液中含有的离子是_____________________。
208
09-ok Page 208 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC定量实验
9
.4
(QUANTITATIVE EXPERIMENTS)
定量测定是物质分析的又一个重要内容,也是研究物
质变化规律,获得化学理论的主要手段。
我们已经学过几种定量测定方法。一种是通过测定物
质变化前后的质量,得到定量结果的重量法,如胆矾中结
晶水含量的测定。一种是通过测定溶液完全反应时消耗的
体积的滴定法(化学上又叫容量法),如用已知浓度的酸或
碱测定未知浓度的碱或酸。此外,还有测定气体体积的气
体法等。
这里将进一步学习进行定量实验的实验设计,通过实
验操作,进一步体验误差分析的重要性。
定量实验的设计
设计定量实验的一般步骤:
1.确定方法:通过课题分析,寻找合适的化学原理
(需要时查阅有关资料),确定测定的方法和大体流程。
2.设计步骤:制定操作步骤(或操作流程),确定直
接测定的物理量和计算式。
3.控制误差:分析操作步骤中,要先知道哪些操作
会影响测定的准确性。很多情况下,为控制实验误差,要增
加必要的步骤,如过滤后沉淀的洗涤、称量前物质的烘干等。
4.选择用品:选择必要的试剂和仪器装置。
实例:设计两种方法(重量法、滴定法各一种)测定工
业用纯碱(杂质为氯化钠)中碳酸钠的质量分数。
课题分析:如采用重量法,可称取一定质量的试样,配
209
09-ok Page 209 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC制成溶液后,选择一种试剂使碳酸钠转化成沉淀,再称量
沉淀的质量,并计算出试样中碳酸钠的质量。如采取滴定
法,则在称取一定质量的试样配制成溶液后,用已知浓度
的标准盐酸溶液来滴定(用甲基橙作指示剂,由黄色滴至
橙色来确定滴定终点),根据标准盐酸消耗的体积计算试样
中碳酸钠的质量。
操作步骤(流程)设计:
1.重量法。
试样 蒸馏水 试剂A 蒸馏水
称量 溶解 沉淀反应 过滤 洗涤 烘干 称量
m g m g
1 2
滤液 洗涤水
恒重操作
2.滴定法。
1.当试剂A是__
标准盐酸
时,沉淀是______ 试样 蒸馏水 甲基橙 (c mol/L)
(以下根据确定的试剂A
回答)。写出试样中碳酸
钠的质量分数的计算式: 称量 溶解 量取待测液 滴定
___________
m g VmL 20mL
1
__________。
2.洗涤沉淀(一般
需洗涤2~3次)是除去
吸附在沉淀上的何种离
子?怎样判断这些离子 1.写出滴定反应的化学方程式:__________
基本洗涤除尽? _____,设标准盐酸浓度为0.1240 mol/L,消耗18.60 mL,
3.分析在操作时,何 则20 mL待测液中碳酸钠的物质的量为____mol,V mL
种情况会产生测定误差 试样中碳酸钠的物质的量为____mol。
(偏高、偏低各举一 试样中碳酸钠的质量分数的计算式是________
例)? ____________。
2.为什么要在相同条件下滴定两次取其平均值?
3.分析产生误差的因素(偏高、偏低各举一例)。
210
09-ok Page 210 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC学生实验
测定含有少量氯化钠的碳酸氢钠的含量
课题要求:
(1)对固体试样,用滴定法测定。
(2)设计实验步骤,同时指出影响准确性的操作注意点。
(3)拟订实验目的,并写出主要实验用品。
(4)实验后,处理数据,对结果作误差分析,完成实验报告。
讨论(回答以下有关实验设计的问题):
(1)取5g固体试样(假设碳酸氢钠的含量为90%),溶解成100mL溶
液(用容量瓶定容),取出 20 mL用标准盐酸滴定,若盐酸的消耗体积
为 15~20mL,则标准盐酸的浓度范围为_______mol/L。
(2)选用的指示剂是_________。
(3)写出你认为重要的操作注意点(两点):___________。
(4)设固体试样m g,溶成100mL后,取20mL,用c mol/L标准盐酸
滴定,消耗体积VmL,则该试样中碳酸氢钠质量分数的计算式为____
________。
实验步骤(流程):
试样 水 指示剂 标准盐酸
取出20mL
称量 溶解、定容 滴定 做第二次实验
100mL
具体实验步骤参阅实验报告。
学生实验
镀锌铁皮锌镀层厚度的测定
铁皮表面镀锌是钢铁防锈的常用方法。下面我们用简单的化学方法测定
锌镀层的厚度。
211
09-ok Page 211 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC这一测定可以分解为以下两个问题。
(1)测定某块铁皮上锌镀层的质量。
(2)测定该铁皮的面积,依据测出的锌镀层的质量及锌的密度(查阅资
料),计算出锌镀层的厚度。
回答以下有关实验设计的问题。
能否利用锌、铁化学活动性的差异,使锌反应而铁皮不
反应?让我们先观察以下实验:
6 mol/L盐酸
(1)将铁皮和镀锌铁皮各一小片分别放入两支试管,各
加入少量6 mol/L盐酸(图9.13),观察实验现象。
铁皮:__________________。
镀锌铁皮:________________。
从实验中得到的反应现象差异,能否用作测定镀锌铁皮
镀锌铁皮
铁皮 上锌镀层的质量?
图 9.13 镀锌铁皮和铁皮跟 从实验可知,镀锌铁皮跟盐酸反应,产生氢气的速率比
盐酸的反应 铁皮大,而且镀锌铁皮的反应速率开始很大,而后又突然减
小。显然,在反应突然减慢的瞬间可认为是锌镀层反应完的
标志。
据此,只需知道镀锌铁皮及除去镀层后的质量,就能测
知锌镀层的质量。
(2)制订锌镀层厚度测定的全部操作步骤。在下列操作
流程中填写操作名称。
镀锌铁皮 盐酸 水
操作Ⅰ 操作Ⅱ 操作Ⅲ 操作Ⅳ 操作Ⅴ 操作Ⅵ
测量面积 ( ) ( ) (洗涤) ( ) 称量
(3)设镀锌铁皮面积为scm2,质量为m g,除去镀层后
1
质量为m g,锌密度为ρg/cm3,写出锌镀层厚度的计算式:
2
____________。
实验中,可以取面积约25cm2的镀锌铁皮,6mol/L盐
酸约40mL。上述操作Ⅲ要用玻璃棒小心翻动镀锌铁皮,使
两面的锌能充分反应。到反应速率突然减小时,迅速将盐酸
倒出,用自来水洗涤。操作Ⅴ可放在酒精灯上完成。
具体实验步骤参阅实验报告。
212
09-ok Page 212 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC学生实验
测定含有少量氧化钠的过氧化钠的纯度(选做)
思考与讨论(方案设计):
(1)过氧化钠和氧化钠的性质有哪些差异?
(2) 在试样(已知一定质量)中加入何种试剂会产生何种生成物,设想
用重量法或滴定法等测量哪些物理量,从而确定其中过氧化钠的量?
将设计方案填入表9.11:
表 9.11
所用试剂及有关 直接测定的物理量 现象记录
方 案 简要操作步骤
化学方程式 及有关计算方法
方案1
方案2
方案3
按滴定法进行实验,操作步骤如下:
(1)称取约2.000 g试样,溶解于适量的蒸馏水中,待氧气放完后用容
量瓶定容为100 mL待测液。
(2)用滴定管(用蒸馏水洗净后再用待测液润洗)取20.00 mL待测液
于锥形瓶中,加1~2滴甲基橙试液。
(3)另取一支滴定管(用蒸馏水洗净后再用标准盐酸溶液润洗)注入标
准盐酸溶液,进行滴定。至溶液由黄色至橙色,30s不变时为滴定终点。记录
读数。
(4)重复操作再滴定一次。
(5)数据处理和误差分析。
数据处理:先计算20.00 mL待测液中氢氧化钠的质量,然后计算全部
试样(质量m g)与水反应生成氢氧化钠的质量(m g),最后计算过氧化钠
1 2
的纯度。
80×78m -62×78m
Na O % = 1 2 ×100%
2 2
80×16m
1
具体实验内容参阅实验报告。
213
09-ok Page 213 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC[课堂练习9.4]
1.为测定氯化铵和硫酸铵混合物中硫酸铵的含量,按下列流程进行实验。
加适量
加水 试剂A
称量
称量样品 溶解 反应 过滤 洗涤 烘干
物质C
m 1 g 恒重操作 m 2 g
滤液B
(1)若物质C为硫酸盐,则试剂A的化学式为___,物质C的化学式为___。
(2)过滤使用的仪器和用品除漏斗(漏斗架)外,还需要__________。
(3) 证明A溶液滴加适量的方法是____________________。
(4)混合物中,硫酸铵的质量分数为_____(用含有m 、m 的代数式表示)。
1 2
2.右图是测定Na O(含Na O杂质)纯度的实验装置。实验时不同时间电子天平
2 2 2
的读数如表9.12。
表 9.12
实验操作 时间(s) 质量读数(g) O
2
烧杯+水 370. 000
水、NaO
2 2
0 377. 640
(NaO)
2
烧杯+水 30 376. 920
+样品 60 376. 400
90 376. 200
120 376. 200
(第2题)
数据处理:
(1)样品的质量=_____。
(2)完成反应后氧气的质量为_____。
(3)样品中Na O 的质量分数为_____。
2 2
(4)若样品中Na O 质量分数的标准值为93.22%,则相对误差_____。
2 2
(5)造成偏差可能的原因_____________________。
3.实验室有一瓶亚硫酸钠试剂,已部分氧化变质,试设计一个实验方案测定其
纯度。
(1)有以下操作步骤,排出其正确的操作顺序_______________。
a. 用盐酸酸化后加氯化钡溶液 b. 过滤 c. 称取样品m g
1
d. 洗涤沉淀 e. 称量沉淀质量m g f. 用蒸馏水溶解 g. 干燥
2
214
09-ok Page 214 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC(2)样品中Na SO 的质量分数为_______(用含有m 、m 的代数式表示)。
2 3 1 2
(3)用盐酸酸化要过量,氯化钡溶液也要过量,原因是___________
_____________________________________ 。
(4)洗涤沉淀的目的是______,如何检验已洗涤干净_________。
4.实验室有CuO和铜粉的混合物,请利用给出的实验仪器及试剂设计两种方法测
定样品中氧化铜的质量分数。
表 9.13
实验 有关化学方程式 实验所用仪器 实验需直接测定的物理量
(1)
(2)
实验可能用到的仪器:①天平,②启普发生器,③硬质玻璃管,④泥三角,⑤烧杯,
⑥坩埚,⑦酒精灯,⑧玻璃棒,⑨漏斗,⑩干燥管。
实验可能用到的试剂:a. 锌粒 b. 稀硫酸 c. 氯化钠溶液 d. 浓硫酸
215
09-ok Page 215 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC化学实验方法的探究
9
(EXPLORATION OF CHEMICAL EXPERIMENTAL
.5
METHODS)
科学的本质是探究。在化学科学中,人们对物质及其
变化规律的认识,除某些外观性状的描述之外,几乎全部
是从实验探究中获得的。
实验探究的内容十分广泛,有探究新物质的性质,探
究化学变化的规律,探究概念之间的关系,得到对科学理
论的确认等。
在物质制备中,所选的反应原理是否恰当,应选定怎
样的反应装置和提纯方法,也是实验探究的重要内容。
探究的基本方法之一是假设(可能的预测、猜测)和检
验,即对未知问题的答案,运用已有的知识作出某种假设,
再用实验来肯定或否定你的假设。
本节将通过若干探究实验,进一步认识实验探究的基
本过程。
一个探究实验的范例
CH 3 COONa 问题背景:取一个小烧杯,注入10 mL 0.1 mol/L醋
酸溶液,使用pH试纸,测定溶液的pH,约为 _____。
向小烧杯中加入少许固体醋酸钠,待完全溶解后,再
CHCOOH 测定溶液的pH,发现pH增大,约为______。
3
探究问题:固体醋酸钠使醋酸溶液pH增大的原因。
图 9.14 醋酸溶液中加入
假设1:醋酸钠溶液呈碱性,中和了醋酸电离出来的
醋酸钠固体
H+,使溶液
C
(H+)降低。
假设2:加了固体醋酸钠后,溶液中CH COO-离子浓
3
度增加,使醋酸电离平衡向左移动,使c(H+)降低。
216
09-ok Page 216 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC哪一种假设正确呢?
分析 :假设1的依据是醋酸钠溶液的碱性中和醋酸的
酸性,假设2的依据是醋酸钠使溶液中CH COO-离子浓度
3
增加,抑制醋酸的电离。如果能寻找某种中性的醋酸盐,加
到醋酸溶液中,如果溶液pH不变,则假设1正确;如果溶
液pH仍增大,则假设2正确。
检验假设的方案:在0.1 mol/L醋酸溶液中加入 __,
待完全溶解后,测定溶液pH,约为 ___,pH___(填
“增大”“减小”或“不变”),证明假设 ___ 正确。
探究与实践
苯酚钠和二氧化碳反应的探究
课题:二氧化碳跟苯酚钠反应生成苯酚,另一产物为什么是碳酸氢钠而不是
碳酸钠?
课题分析:二氧化碳跟苯酚钠的反应,用离子方程式表示如下:
O- OH
+ CO +H O —→ +HCO-
2 2 3
O- OH
根据“盐+酸—→新盐+新酸”的反应模式看, 能转化成 ,说明H CO
2 3
OH
(CO 、H O)的酸性比 强。而H CO 只生成HCO-,不能继续生成CO2-。可
2 2 2 3 3 3
O-
能的原因是H CO 属于二元酸,只能把第一个H+(一级电离)交给 ,却没有
2 3
O-
能力继续把第二个H+(二级电离)交给 。
据此,形成如下假设。 OH
假设:HCO-的酸性(电离出H+的能力)比 弱。
3
检验:
(1)查阅有关资料,从理论上对假设作肯定或否定的回答。
提示:查阅教材中苯酚、碳酸的电离常数K的数值。
________________________________。
217
09-ok Page 217 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC(2)设计一个实验,从实践上检验假设是否正确。
提示:
OH
(1) (酸)能否把H+交给CO2-形成HCO-(当做新酸看)。
3 3
OH ONa
(2)查阅资料: 和 的水溶性,据此设计有显著现象的实验。
实验方案:__________________________
_______________________________。
现象和结论:_________________________
_______________________________。
物质制备反应装置等的探究
作为科学研究的化学实验就是科学探究,作为学习科
学的化学实验同样具有探究的含义,要用探究的科学态度
来学习、操作化学实验。例如,某一反应用于物质制备时,
需要探究确定反应的条件、选用怎样的实验装置和提纯的
方法等。下面,通过实验室制备乙酸丁酯探究确定反应的
装置和提纯的方法。
学生实验
制备乙酸丁酯
课题要求:
(1)阅读制备乙酸丁酯的化学原理,选择制备的反应装置。
(2)根据乙酸、1-丁醇、乙酸丁酯的性质,确定乙酸丁酯的提纯方法。
(3)完成实验和实验报告。
实验原理及有关资料:
乙酸丁酯由乙酸和1-丁醇在浓硫酸、环境温度115~125℃条件下通过
酯化反应制得:
218
09-ok Page 218 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC浓硫酸
CH COOH+C H OH—→CH COOC H +H O
3 4 9 △ 3 4 9 2
酯化反应有一定的可逆性,制备中一般通过提高相对价廉的乙酸浓度和
及时移去生成物水,能使反应转化率达90%。
乙酸丁酯是一种带水果香味的液体。沸点126.3℃,密度0.88g/cm3。微
溶于水,能与乙醇等互溶。乙酸丁酯是常用的有机溶剂,在油漆涂料工业中
有重要用途。
1-丁醇是一种略带刺激性气味的液体。沸点117.2℃,密度0.81g/cm3,
能溶于水和有机溶剂。
首先,由于乙酸丁酯的沸点较高,故采取制备溴苯、硝基苯的方法即先
制备、后提纯。制备反应器可选择大试管,反应完成后再将反应液倒入分液
漏斗中洗涤,进行提纯操作。提纯乙酸丁酯可选用水、碳酸钠溶液洗涤。其
次制备乙酸丁酯的环境温度较高,不能用水浴。为防止温度过高(易碳化),
可用石棉网控制,即把大试管放在石棉网上方的空气中。最后,由于乙酸易
挥发,且反应较缓慢,故采用制备硝基苯的装置,即用长玻璃导管作空气冷
凝回流,以提高反应转化率。
具体实验装置和实验步骤参阅实验报告。
1. 回忆学过的制备溴苯、硝基苯、乙酸乙酯的实验装置,
根据反应条件从中设计制备乙酸丁酯的简易装置。
2. 反应混合物中除乙酸丁酯外,还有乙酸、丁醇、硫酸
和水。根据它们的性质,怎样提纯乙酸丁酯?
学生实验
过氧化氢分解速率的研究(选做)
课题背景:过氧化氢(hydrogen peroxide)是一种氧化剂,也是一种实
用的消毒杀菌剂。过氧化氢在空气中会缓慢分解释放氧气,多种催化剂如二
氧化锰、三氯化铁、碘化钾等能加快过氧化氢的分解。
219
09-ok Page 219 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC2H O —→ 2H O + O ↑
2 2 2 2
要求:
(1)探究反应速率随时间的变化情况,连续测定过氧化氢分解产生
氧气的体积,绘制时间-氧气体积曲线,推求某时段的平均反应速率(用
单位时间里产生氧气的体积表示)。
(2)探究温度对反应速率的影响。
仪器及操作:
如图9.15装置,左边A是Y形试管作反
应器,D是烧杯作水浴用。右边是量气管B
和能上下移动的水准管C,量气管与水准管
下面用胶管连通。
在Y形试管一端注入2 mL 3%过氧化
氢,另一端注入 1 mL 1 mol/L 氯化铁溶
液。连接好反应器和量气管,进行气密性
图 9.15 过氧化氢分解装置
检验。然后将量气管的水面用水准管调至
A.Y形试管;B.量气管;C.水准管;
上端0刻度。 D.水浴烧杯;E. 温度计
记录室温,测定室温时过氧化氢分解速率。
倾斜Y形试管使其中两种溶液反应,同时(注意必须同时)每隔30 s或
1 min,从量气管水面高度读出氧气体积(读至0.1 mL),数据记录入表格。
用水浴将温度提高10℃,在过氧化氢和三氯化铁相同用量和浓度下,测
定过氧化氢的分解速率。
研究温度对该反应速率的影响。
1.怎样进行装置的气密性检查?
2.读取氧气的体积时,为什么必须注意使量气管与水
准管内的水面保持一样高度?
3.设计数据记录表格。怎样将时间、氧气体积数据表
转化为时间-氧气体积曲线?
(提示:曲线应光滑,使各点距曲线最近。)
220
09-ok Page 220 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPCV(O)(mL)
2
4.图9.16上X点(2min时)、Y点(6min时)气体产
Y
20
生的速率为什么不同?哪一时刻快?
5.怎样计算过氧化氢的平均反应速率(用单位时间里
产生氧气的体积表示)。 X
10
提示:从数据记录表和时间-氧气体积曲线均可推求某
时刻内平均反应速率,如求反应开始至2min内的平均速率,
1 2 3 4 5 6 7 t(min)
XA 10
v 平均 = = =5.0(mL/min)。 图 9.16 时间-氧气体积曲线
OA 2
6.设计温度对过氧化氢分解速率影响的实验方案。
[课堂练习9.5]
1. 向氢氧化钠溶液中滴加几滴酚酞试液,溶液呈红色,再逐滴加入新制饱和氯水,
当滴加至某一滴时,红色褪去。
(1)对这一现象的说明有两种假设,请写出另一种假设。
假设一:氯水中的H+中和了OH-,酚酞呈无色。
假设二:______________________________。
(2)现要求用实验验证上述两种假设哪一种正确,写出实验过程和逻辑判断。
实验过程:_____________________________。
如果现象为_____,则假设一正确;如果现象为_____,则假设二正确。
2. 市售的加碘盐加的是碘酸钾或碘化钾。
(1)在加碘盐的包装袋上印有注意事项“防潮、防热、避光贮存”“煮好菜后放盐
保持碘效”等,请用文字或化学方程式说明上述注意事项。
(2)已知:5I-+IO-+6H+—→3I +3H O,假设盐中加的是碘酸钾,如何检验
3 2 2
碘酸钾?写出简要实验步骤和现象(酸剂用家庭使用的醋)。
(3)假设盐中加的是碘化钾,请设计一种试纸,能快捷地检验出碘化钾,同时说
明该试纸的使用方法。
3. 某学生利用图9.15的实验装置作过氧化氢分解速率的实验,数据记录如表9.14。
试剂用量:2 mL 3%H O ,1 mL 1 mol/L FeCl 。
2 2 3
表 9.14
时
间
O (m
体 in
2 积 ) 1 2 3 4 5 6 7 8 9 10
(m
L
)
温度(℃)
14 1.3 2.8 4.5 6.4 7.8 8.9 9.9 10.7 11.7 12.0
25 6.9 11.0 12.6 13.3 13.8 14.2 14.6 14.8 15.2 15.3
221
09-ok Page 221 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC(1)在下图上画出不同温度的时间-氧气体积曲线(用两种不同颜色表示,曲线
应光滑,使各点离曲线最近)。
(2)14℃,0~2 min的v =_____,4~6 min的v =_____,速率
平均 平均
减小的原因是_____。
(3)25℃时,0~2 min的v =____,与14℃比较,速率增大的原因是__
平均
_________。
V(O)(mL)
2
20
10
O 2 4 6 8 t(min)
(第3题)
4. A compound was analyzed and found to contain 13.5 g Ca, 10.8 g O and 0.675 g H. What
is the empirical formula for the compound?
STRATEGY SOLUTION
(1)Analyze You are given the mass of each element in the compound and
are asked to find the empirical formula.
(2)Plan First convert the mass of each element to a number of moles
using molar mass.
Then find the lowest whole-number ratio of moles.
(3)Solve Find mole amounts:
1 mol Ca
13.5 g Ca× =0.337 mol Ca
40.08 g Ca
1 mol O
10.8 g O× =0.675 mol O
16.0 g O
1 mol H
0.675 g H× =0.668 mol H
1.01 g H
Divide each mole value by the smallest number of moles (0.337 mole):
0.337 mol Ca
=1.00 mol Ca
0.337
222
09-ok Page 222 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC0.675 mol O
=2.00 mol O
0.337
0.668 mol H
=1.98 mol H
0.337
This mole ratio of the elements can be rounded to 1 Ca∶2 O∶2 H and
is represented by the subscripts in the empirical formula.The empirical
formula is CaO H . Because 2 moles of O and 2 moles of H in an ionic
2 2
compound probably means 2 moles of OH- ions, the empirical formula
can be rewritten as Ca(OH) .
2
(4)Evaluate The empirical formula can be confirmed by comparing the percentage
composition of the elements given in the problem to the percentage
composition of Ca(OH) . In both cases Ca=54.1%, O=43.2%, and
2
H=2.70%.
Practice Problems
① Determine the empirical formula for a compound containing 2.128 g Cl and 1.203 g Ca.
② Determine the empirical formula for a compound containing 7.30 g Na, 5.08 g S and
7.62 g O.
223
09-ok Page 223 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC小 结
1.本章知识体系和学习方法。
物质提纯的基本操作
物质的提纯与分离 通过“氯化钠的提纯”学习实验设计
学生实验:分离氯化铁和氯化铝的混合溶液
常见气体的制备和净化
物质制备(常见气体的制备)
学生实验:制备乙酸丁酯
物质检验和常用方法
物质的检验
学生实验:离子的检验
化学实验 物质分析
通过“测定工业用纯碱中碳酸钠的质量分数”学习实验设计
定量实验 测定含有少量氯化钠的碳酸氢钠的含量
学生实验 镀锌铁皮锌镀层厚度的测定
测定含有少量氧化钠的过氧化钠的纯度(选做)
通过固体醋酸钠使醋酸溶液pH增大的原因学习实验探究的基本方法
实验探究 苯酚钠和二氧化碳反应的探究
学生实验 乙酸丁酯反应装置和提纯方法的探究
过氧化氢分解速率的研究(选做)
学习方法:通过典型范例,理解原理和各操作步骤的目的。在动手操作中,学会观察、
记录、分析现象,作出结论。
2.请选择若干种气体从制备的化学原理、气体发生装置、收集方法、检验、净化、干
燥和吸收等方面进行纵向归纳。又从几种气体发生装置、几种收集方法、几种干燥装置等对
多种气体的制备作横向归纳。
3.列表比较各种物质分离操作的原理和适用范围。
4.离子检验的基础是单一离子的检验方法,请列表归纳。常见的离子检验的课题有哪
几种类型?每种类型各举一例说明该种检验的一般思路。
5.定量测定的一般步骤。
课题分析 —→ 测定的化学原理(有关化学方程式、直接测定的物理量、计算式等)
—→ 实验操作步骤(各步的目的,影响准确性的关键操作等) —→ 数据处理(包括误差分
析等)—→ 小结(问题和讨论)
224
09-ok Page 224 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC6.化学实验方案设计的一般要求:
一个完整的实验方案应有如下内容:实验名称、实验目的、实验原理、实验用品、实验
步骤、现象记录和结果处理(定量测定还包括误差分析)、问题和讨论。
实验方案的设计实质是利用我们掌握的化学知识,寻找一定的操作步骤去解决一个化学
问题。
225
09-ok Page 225 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC表
期
周
素
元
Ⅰ
录
附
226
09-ok Page 226 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPCⅡ 化学词汇英中文对照表
acetaldehyde 乙醛 3 - ethyl - 3 - methylheptane 3 - 甲基 - 3 - 乙基庚烷
1,4 - addition 1,4 - 加成 extraction 萃取
alcohol 醇 filteration 过滤
alkane 烷烃 formic acid 蚁酸,甲酸
alkene 烯烃 glycerol 甘油
alkyne 炔烃 glycol 乙二醇
allotrope 同素异形体 graphite crystal 石墨晶体
amino acid 氨基酸 halohydrocarbon 卤代烃
aromatic hydrocarbon 芳香烃 hydrogen halide 卤化氢
atomic crystal 原子晶体 ionic bond 离子键
atomic number 原子序数 ionic crystal 离子晶体
binary weak acid 二元弱酸 ionic equation 离子方程式
bond angle 键角 ionization constant 电离常数
bond energy 键能 ionization degree 电离度
1,3 - butadiene 1,3 - 丁二烯 i - pentane 异戊烷
1 - butene 1 - 丁烯 isomer 同分异构体
2 - butene 2 - 丁烯 isomerism 同分异构现象
carbon tetrachloride 四氯化碳 isoprene 异戊二烯
carbonic acid 碳酸 isotope 同位素
carboxyl group 羧基 metallic bond 金属键
carboxylic acid 羧酸 metallic character 金属性
chemical reaction rate 化学反应速率 metallic crystal 金属晶体
chloroform 氯仿 2 - methylbutane 2 -甲基丁烷
covalent bond 共价键 2 - methylpropene 2 -甲基丙烯
cracking 裂化,裂解 molecular crystal 分子晶体
crystallization 结晶 m - xylene 间二甲苯
dialysis 渗析 neo - pentane 新戊烷
diene 二烯烃 non - electrolyte 非电解质
2,3 - dimethylpentane 2,3 - 二甲基戊烷 non - metallic character 非金属性
distillation 蒸馏 non - polar molecule 非极性分子
electrochemical corrosion 电化学腐蚀 n - pentane 正戊烷
electrochemical protection电化学保护 oleic acid 油酸
elimination 消除反应 oxalic acid 草酸,乙二酸
equilibrium constant 平衡常数 oxidizing agent 氧化剂
ethyl benzene 乙苯 o - xylene 邻二甲苯
227
09-ok Page 227 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPCpalmitic acid 软脂酸 silicon dioxide crystal 二氧化硅晶体
paper chromatography 纸上层析法 stearic acid 硬脂酸
peptide bond 肽键 strong electrolyte 强电解质
phenol 苯酚 1,2,4 - trimethyl benzene 1,2,4 - 三甲苯
polar molecule 极性分子 trinitrotoluene 三硝基甲苯
p - xylene 对二甲苯 vinyl chloride 氯乙烯
reducing agent 还原剂 weak electrolyte 弱电解质
silicon crystal 硅晶体
228
09-ok Page 228 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC说 明
本册教材根据上海中小学(幼儿园)课程改革委员会制定的课程方
案和《上海市中学化学课程标准(试行稿)》编写,供高中三年级试用。
本教材由上海市长宁区教育局主持编写,经上海市中小学教材审查
委员会审查准予试用。
本册教材的编写人员:
主编:姚子鹏 副主编:陈基福 洪东府
特约撰稿人:(按姓氏笔划为序)阮锦莲 陆惊帆 高 清
本册教材(试验本)原特约撰稿人:(按姓氏笔划为序)
阮锦莲 陆惊帆 杨卫国 施永新 高 清
欢迎广大师生来电来函指出教材的差错和不足,提出宝贵意见。上
海中小学课程教材改革委员会办公室地址:上海市陕西北路500号(邮
政编码:200041),联系电话:62560016(总机转)、52136338;出版社电
话:64089888。
声明 按照《中华人民共和国著作权法》第二十三条,关于“为实
施九年制义务教育和国家教育规划而编写出版教科书,除作者事先声明
不许使用的外,可以不经著作权人许可,在教科书中汇编已经发表的作
品片段或者短小的文字作品、音乐作品或单幅的美术作品、摄影作品,但
应当按照规定支付报酬,指明作者姓名、作品名称”的有关规定,我们
已尽量寻找原作者支付报酬。原作者如有关于支付报酬事宜可及时与出
版社联系。
229
09-ok Page 229 2011.4.9, 10:44 PM Adobe PageMaker 6.5C/PPC