文档内容
1 2 3 4 5 6 7 8 9 10 11 12 13 14
D A B D C B A C C A C C D B
15.参考答案:(除标注外,每空2分)
(1)适当升高温度、粉碎废渣、搅拌、适当提高酸的浓度(1分)
(2)8(1分); 4s24p1 (1分)
(3)GaO + 6H+ +8Cl- = 2GaCl - + 3H O ;将Fe(Ⅲ)还原为Fe(Ⅱ)(或Fe3+→Fe2+),防
2 3 4 2
止在萃取时与GaCl -共萃,影响纯度
4
(4)分液漏斗(1分,多写烧杯不扣分);GaO -+3e-+2H O = Ga +4OH- (或[Ga(OH) ]
2 2 4
-+3e- = Ga +4OH-)
(5)Ga(C2H5)3 +3H
2
O → Ga(OH)
3
+ 3C
2
H
6
↑ ; sp2杂化
16.【答案】
(1)煤油或石蜡油 (1分) AD (2分)(全对得2分,少选给1分,有错不给分 )
(2)2Na + 2HO = 2NaOH + H↑ (2分) (物质正确,配平错误不给分;气体箭头不加给
2 2
1分); 由实验可知:三者溶液中HO+分别相差106倍,HO+浓度相差显著,但反应时间几
3 3
乎相同,说明钠在三种溶液中优先与水发生了反应。(2分)(提到Na与酸反应本质就是
与水反应就给分)
(3)钠失去电子形成溶剂化电子:HO + e- ⟶ HOe- ; 溶剂化电子发生变化HOe- ⟶
2 2 2
OH- + H ,OH-遇到酚酞变红色。(2分)
(4)当盐酸浓度大于1mol/L时,随浓度增大,生成NaCl固体逐渐增多,沉积在金属钠表
面的NaCl越多,扩散慢,从而降低化学反应速率。(2分)
方案:取质量相等形状几乎一样的钠块,分别投入足量的等体积的 PH=1的盐酸、PH=1
的氢氟酸中,记录金属钠反应完的时间。(2分)(没有体现控制变量法不给分;设计以
PH=1的醋酸做对照实验不给分)
预测现象:若投入PH=1的氢氟酸中耗时更长,说明猜想正确。(2分)(或PH=1的盐酸
酸中耗时更短也给分)
17.(1) ①. 高温 ( 1分 )
a.该反应为放热反应,若A点反应到达平衡,则温度更高条件下,乙烯的产
②率应更低
( 2分 )
b. 催化剂活性降低,导致反应速率减慢 ( 1分 )
(2) ①. 或0.19 ( 2分 ) . 增大 ( 1分 )
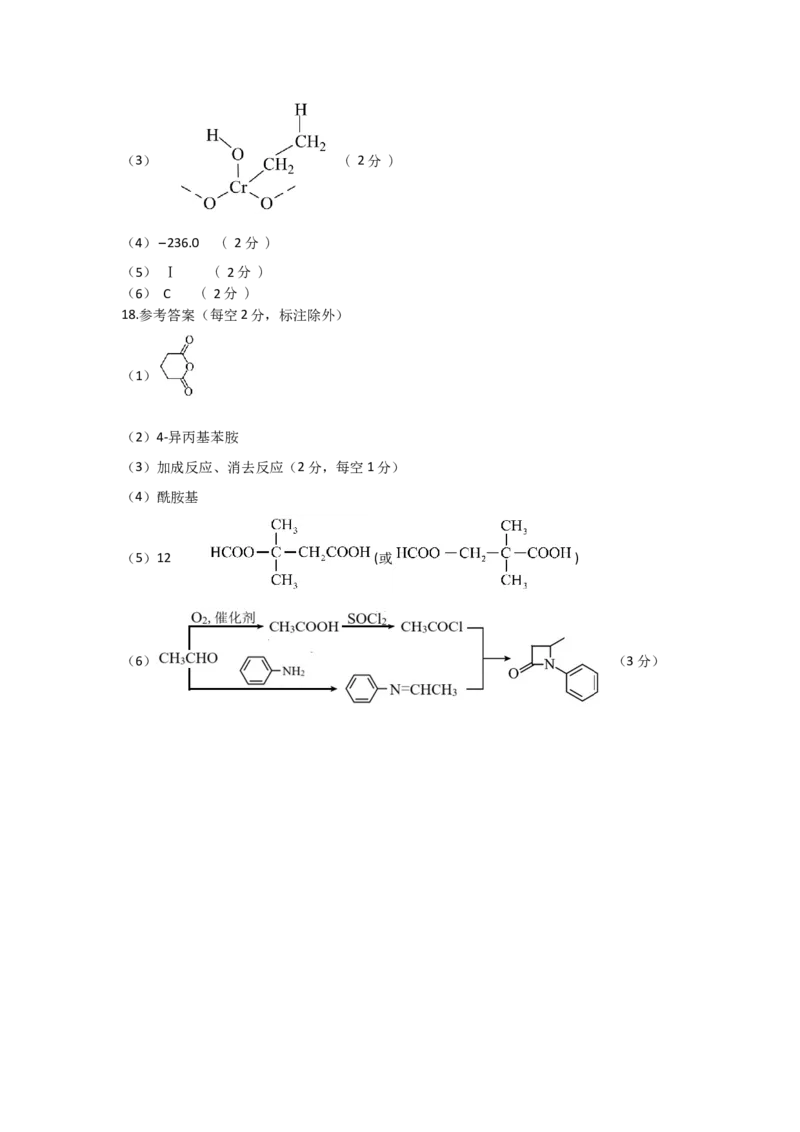
②(3) ( 2分 )
(4)−236.0 ( 2分 )
(5) Ⅰ ( 2分 )
(6) C ( 2分 )
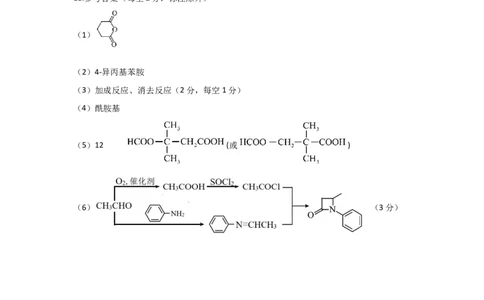
18.参考答案(每空2分,标注除外)
(1)
(2)4-异丙基苯胺
(3)加成反应、消去反应(2分,每空1分)
(4)酰胺基
(5)12 (或 )
(6) (3分)