文档内容
高级中学课本
高中二年级第二学期
(试用本)
上海科学技术出版社目 录
11
认识碳氢化合物的多样性
UNDERSTAND THE DIVERSITY OF
HYDROCARBON
3◆ 11.1 碳氢化合物的宝库——石油
17◆ 11.2 石油化工的龙头——乙烯
26◆ 11.3 煤化工和乙炔
36◆ 11.4 一种特殊的碳氢化合物——苯
12
初识生活中的一些含氧有机化合物
PRELIMINARY RECOGNIZE SOME
ORGANIC COMPOUNDS CONTAINING
OXYGEN IN DAILY LIFE
49◆ 12.1 杜康酿酒话乙醇
58◆ 12.2 醋和酒香
62◆ 12.3 家庭装潢说甲醛
目录113
检验一些无机化合物
IDENTIFY SOME INORGANIC
COMPOUNDS
73◆ 13.1 离子的检验
79◆ 13.2 混合物的检验
附录
88◆ Ⅰ 元素周期表
89◆ Ⅱ 化学词汇英中文对照表
2目录11
认识碳氢化合物的多样性
UNDERSTAND THE DIVERSITY OF HYDROCARBON
◆ 煤、石油、天然气是宝贵的资源 ◆ 取代反应、加成反应和聚合反应
◆ 甲烷、乙烯、乙炔、苯的结构与性质 ◆ 同系物和同分异构体
1碳
是一种极为奇妙的元素。虽然它仅占地壳质
量的0.027%,但含碳的化合物却占地球
上已发现和合成的化合物的90%以上。碳
对人类衣、食、住、行、用具有重要的意义。纤维、橡
胶、塑料、染料、涂料、药物,甚至组成生物体的物质,
如糖类、脂肪、蛋白质、核酸等,都是含碳的化合物——
有机化合物。
数量庞大、性能各异、用途广泛、对人类至关重要
的各种有机化合物,都可看成是从碳氢化合物衍生出来
的。要认识有机化合物的复杂性和多样性,可从天然气、
石油和煤入手,先认识一下最简单的一类有机化合物——
碳氢化合物。
2碳氢化合物的宝库——石油
11
.1
(THE TREASURY OF HYDROCARBON —— PETROLEUM)
工业的血液和炼油
石油(petroleum)是重要的能源和宝贵的资源。人们
称之为“工业的血液”。石油燃烧的热值高,运输和储存方
便。20世纪50年代以来,在世界能源消费结构中,石油
跃居首位。
石油提炼出的产品有几千种。其中作为电站、汽车、轮
船、飞机、坦克等的燃料占石油产品总产量的很大部分;而
液化气是居民生活应用的优质燃料。在现代生活中,人们
的衣、食、住、行、用都直接或间接与石油产品有关。塑料、
合成橡胶、合成纤维三大合成材料,绝大部分靠石油来生
产。石油已成为国家现代化建设的战略物资,在国民经济
发展和国防建设中占有重要地位。
图 11.1 东海石油探井
图 11.2 炼油装置
3化学史话
哪一个国家最早利用石油
在伊拉克幼发拉底河两岸有六千多年历史的古建筑中,有使用沥青砂浆
的迹象,是最早利用石油的佐证。我国东汉时期(公元1世纪)著名史学家
班固在《汉书·地理志》中记有:“高奴有洧水可 。”这里说的“可 ”即
“可以燃烧”的就是石油,“高奴”即今陕西延长县。“石油”一词始见于北宋
沈括(11世纪)所著《梦溪笔谈》,该书卷二十四指出“ 延境内有石油”。
【资料库】 我国是世界上最早发现和利用石油的国家之一。新中
国成立前,我国基本上没有自己的石油工业。新中国成立
2006年世界 后,我国的石油工业有了很大发展。新中国成立初期开发
石油产量和储量继 了新疆克拉玛依油田,20世纪60年代初开发了大庆油田。
续小幅增长,石油 以后又开发了胜利、大港、华北、中原等石油基地。到20
探明储量估计为 世纪80年代末,我国开发的大小油田已有160多处。此外,
1.805×1011 t。中
我国拥有油气资源较丰富的大陆架。
国约2.2×109 t。
石油中所含的化合物种类繁多,必须经过炼制才能使
用。石油的炼制主要有分馏、裂化、重整、精制。
我国自20世纪80年代初开始进行海洋石油的普查和勘
探。目前,我国原油加工能力跃居世界第四位,2006年原
油产量为1.8×108 t。
拓展视野
石油之战——20世纪70年代石油危机的由来
自第二次世界大战结束到1973年间,国际石油市场一直被美国、英国
的7家石油公司所垄断。西方国家利用廉价的石油原料,实现了经济的结构
调整和繁荣。
石油产地主要在发展中国家,如中东地区已探明的石油储量占世界的
60%以上。沙特阿拉伯、伊朗、伊拉克、科威特和南美的委内瑞拉等5国的
石油出口量曾占世界总出口量的80%。在20世纪60年代初他们成立了“石
油输出国组织(欧佩克,OPEC)”与上述7家公司相对抗。此后,又有8国
先后加入,OPEC成员扩大到13个。
41973年10月中东战争爆发,阿拉伯产油国以石油为武器,对西方国家
实行石油禁运,并收回了原油标价大权,在两个月后提价近4倍。直到20世
纪70年代末油价不断上涨,1979年油价约是1973年的10倍。
石油涨价使发达国家政治、经济及日常生活受到严重影响,这就是20
世纪70年代的石油危机。
石油是由远古时代的海洋或湖泊中的动植物遗体在地
【资料库】
下经过漫长复杂的变化而形成的黏稠状液体。石油呈黑色
或深棕色,有特殊气味,不溶于水,密度比水稍小,没有固 石油的组成
定的熔点和沸点。
石油主要是由各
石油主要含有碳、氢两种元素。碳元素占83%~87%,
种烷烃、环烷烃和芳
氢元素占10%~14%,还含有少量的氮、氧、硫及微量的磷、
香烃组成的混合物。
钾、硅、铁、镁等元素。
大部分是液态烃,同
开采出来未经处理的石油叫原油,原油中含水、氧化
时也溶有气态烃和固
钙和氯化镁等盐类,必须经过脱水、脱盐等处理。
态烃。
经过脱水、脱盐等处理的石油主要是各种碳氢化合物
组成的混合物。其中,含碳原子数少的沸点低,含碳原子数
多的沸点高。因此,将石油加热至沸腾,通过分馏塔,可以
把石油分成不同沸点范围的蒸馏产物,这就是石油的分馏
(fractionation),分馏出来的各种成分叫馏分(fraction),每
一种馏分仍然是多种碳氢化合物的混合物。
图 11.3 石油勘探示意图
5课堂实验
如图11.4所示装置,在分馏装置
底部容器中加入三分之一体积的石
c
油,把分馏装置中部三个测温探头跟
b
a
数字测温仪连接,分馏装置顶部气体
逸出口跟盛有酸性高锰酸钾溶液的双
球U形验气管相连。
1.实验前,分馏装置中塔间的3
个温度分别为: 图 11.4 石油的分馏
a_____, b_____,
c_____。
2.加热分馏装置容器底部,当塔间温度a升至160 ℃左右时,停止加
热,此时,塔间b、c的温度分别为:
b_____, c_____。
3.观察3个塔间和顶部双球U形验气管中的现象。
记录:____________________________
_________________________________
_________________________________。
石油经过分馏,在塔的三个塔间里分别得到沸点不同
的馏分。这三种馏分的沸点依次递减,说明它们所含有机
物分子里的碳原子数逐渐减少。顶部导出的气体能使酸性
高锰酸钾溶液褪色。
图 11.5 工业石油分馏*
图 11.6 石油分馏的产品和用途
*炼油厂里石油分馏的原理跟上述实验一样,分馏在分馏塔(fractional column)里进行。
6表 11.1 石油分馏产品及其用途
分馏产品 分子所含碳原子数 沸点范围 用 途
溶 剂 油 C ~C 30~150 ℃ 在油脂、橡胶、油漆生产中作溶剂
5 8
汽 油 C ~C 220 ℃以下 飞机、汽车以及各种汽油机燃料
5 11
航空煤油 C ~C 150~250 ℃ 喷气式飞机燃料
10 15
煤 油 C ~C 180~310 ℃ 拖拉机用燃料、工业洗涤剂
11 16
使用各种柴油机的汽车、军舰、轮
柴 油 C ~C 200~360℃
15 18
船、坦克、拖拉机、火车等的燃料
润滑油(锭子油、 机械上的润滑剂、减少机械磨损、
C ~C
16 20
机油、汽缸油等) 防锈
重
凡 士 林 C ~C 360℃以上 润滑剂、防锈剂、制药膏
18 22
石 蜡 C ~C 制蜡纸、绝缘材料
油 20 30
沥 青 C ~C 铺路、建筑材料、防腐涂剂
30 40
石 油 焦 主要成分是C 制电极、生产SiC等
注:表内所示沸点范围不是绝对的,在生产时常需根据具体情况变动。
表 11.2 丁烷、戊烷、己烷的沸点 【资料库】
物 质 沸点 (℃)
家用的液化石油
丁烷(butane) -0.5
气,主要成分为丙
戊烷(pentane) 36
烷、丁烷等。它们都
己烷(hexane) 69
是气体石油产品,加
压后变成液体装在
图 11.7 液化石油气钢瓶
钢瓶中。
甲 烷
碳氢化合物又称作烃。石油分馏出来的有机物大部分
是链状烃,其中最简单的烃是甲烷(methane),甲烷的分子
式为CH ,与石油伴生的油田气含甲烷31%~90%,天然气
4
的主要成分也是甲烷。
图 11.8 甲烷的开采
7拓展视野
我国海底富含“可燃冰”
“可燃冰”是天然气(甲烷类)被包进由水分子组成的笼中,在海底低
温与压力下形成的透明结晶。1m3“可燃冰”释放出的能量相当于164 m3的
天然气的能量。目前公认的全球“可燃冰”总能量是所有煤、石油、天然气
能量总和的2~3倍。美国和日本最早在各自海域发现了它。我国近年来也
开始对其进行研究。
长期以来,有人认为位于亚热带地区的我国南海海域不可能存在“可燃
冰”,因为这里没有冻土带。然而,不久前,广州地质调查局利用地震波探
测海底地表反射,发现了中国南海海域有“可燃冰”存在。由于特殊的物理
性能,天然气和水可以在高压和2~5 ℃的温度范围内结晶,而南海海底
600~2 000m范围的温度和压力都很适合“可燃冰”的生成。我国南海海底
巨大的“可燃冰”带的能源总量估计相当于中国石油总能量的一半。
据悉,在我国东海“可燃冰”的蕴藏量也很可观。我国科学工作者根据
天然气水合物存在的低温和高压的必备条件,找出了“可燃冰”存在的温度
和压力范围,并根据地温梯度,结合东海的地质条件,勾画出“可燃冰”的
分布区域。以此计算出“可燃冰”的稳定带的厚度,对它的资源量作了初步
评估。
专家预测,“天然气水合物”即“可燃冰”有可能成为人类高效的新能源。
纯净的甲烷在空气里安静地燃烧,生成二氧化碳和
水,1 mol甲烷完全燃烧放出890 kJ热量。
点燃
CH + 2O CO + 2H O
4 2 2 2
甲烷,熔点-182.5 ℃,沸点-164 ℃,在水中溶
图 11.9 生产沼气
解度很小,是一种清洁的气体燃料。空气中含甲烷
5%~15.4%(体积)时,遇火花会发生爆炸。煤层中甲
烷(常称为瓦斯)在煤坑道中聚集,形成的甲烷和空气
的混合物是引起煤矿爆炸的根源。为了防止发生爆炸
事故,必须采取通风、严禁烟火等安全措施。因此,在
进行甲烷燃烧实验时,必须先检验甲烷的纯度。
甲烷在隔绝空气的条件下加热到1 000 ℃以上会分
解成炭黑和氢气。
8高温
CH C + 2H
4 2
炭黑是橡胶工业的重要原料,是黑色颜料、油漆、涂料
中的主要着色剂。
课堂实验
甲烷与氯气反应
取一支大试管(直径25 mm、长200 mm),
用排饱和食盐水的方法收集4体积氯气,然后通
入1体积甲烷,把装有混合气体的试管倒置在盛
有饱和食盐水的水槽里,用日光或高压汞灯的紫
外线照射,观察现象。
实验现象:____________。
图 11.10 甲烷与氯气反应
甲烷在光照下与氯气发生反应,甲烷分子里的4个氢原
思考与练习
子能逐个被氯原子所代替,生成4种取代产物。甲烷与氯气
反应生成一氯甲烷(CH Cl,chloromethane)和氯化氢。反 1.写出甲烷在光照
3
下与氯气反应的化学方
应生成的一氯甲烷分子里还有3个氢原子,这些氢原子仍可
程式。
被氯原子代替,因此反应继续进行,依次生成二氯甲烷
2.取代反应与置换
(CH Cl ,dichloromethane)、三氯甲烷又叫氯仿(CHCl ,
2 2 3 反应有什么区别?
chloroform)和被4个氯原子取代的四氯化碳(CCl ,carbon
4
tetrachloride)。
H
有机物分子里的某些原子或原子团被其他原子或原子
··········
团所代替的反应叫做取代反应(substitution)。 H ··· ·· ·· ···C ····· ····· H
··········
科学家们对有机物经过长期的研究,发现有机物的性 H
质和它们的组成以及原子的连接方式(价键)有关。对甲烷 电子式
来说,碳原子最外层的4个电子分别与具有一个电子的氢原
H
子形成4个共价键,结合成CH 。
4
H C H
那么,甲烷分子里各个原子在空间的分布情况是怎样
H
的呢?
结构式
9探究与实践
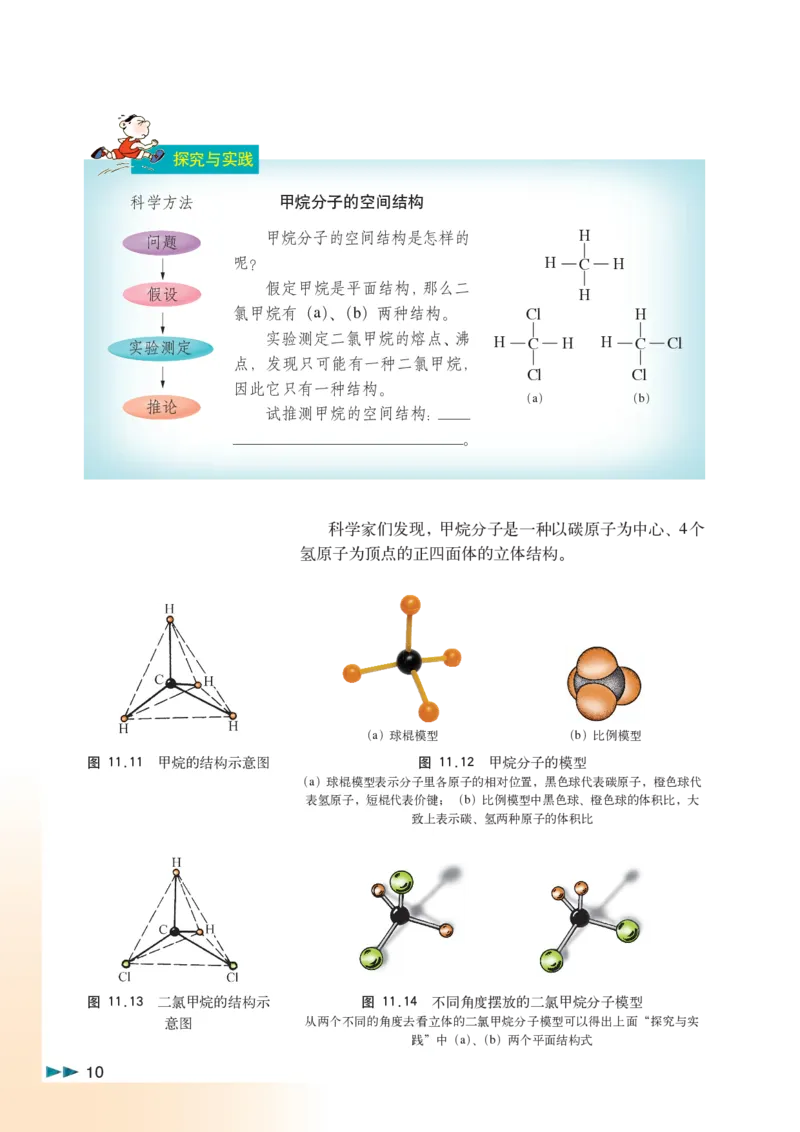
科学方法 甲烷分子的空间结构
甲烷分子的空间结构是怎样的 H
问题
呢? H C H
假定甲烷是平面结构,那么二
假设 H
氯甲烷有(a)、(b)两种结构。 Cl H
实验测定二氯甲烷的熔点、沸
实验测定 H C H H C Cl
点,发现只可能有一种二氯甲烷,
Cl Cl
因此它只有一种结构。
(a) (b)
推论
试推测甲烷的空间结构:__
_______________。
科学家们发现,甲烷分子是一种以碳原子为中心、4个
氢原子为顶点的正四面体的立体结构。
(a)球棍模型 (b)比例模型
图 11.11 甲烷的结构示意图 图 11.12 甲烷分子的模型
(a)球棍模型表示分子里各原子的相对位置,黑色球代表碳原子,橙色球代
表氢原子,短棍代表价键; (b)比例模型中黑色球、橙色球的体积比,大
致上表示碳、氢两种原子的体积比
图 11.13 二氯甲烷的结构示 图 11.14 不同角度摆放的二氯甲烷分子模型
意图 从两个不同的角度去看立体的二氯甲烷分子模型可以得出上面“探究与实
践”中(a)、(b)两个平面结构式
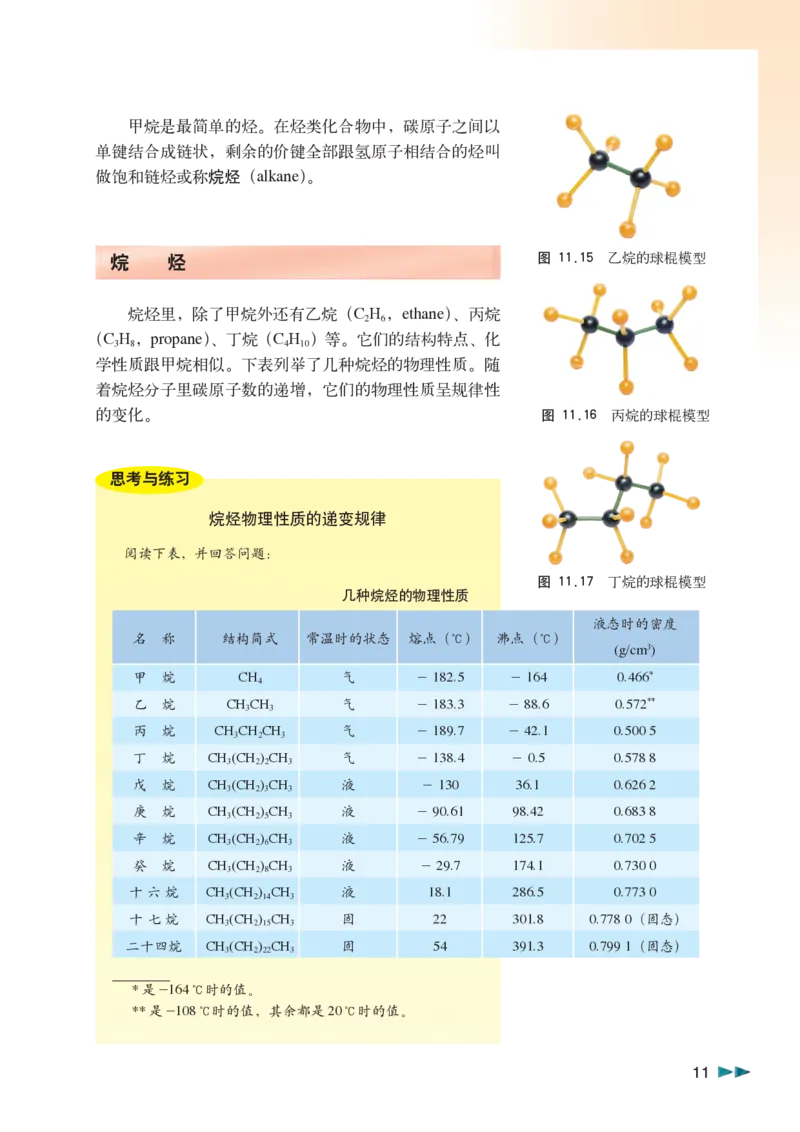
10甲烷是最简单的烃。在烃类化合物中,碳原子之间以
单键结合成链状,剩余的价键全部跟氢原子相结合的烃叫
做饱和链烃或称烷烃(alkane)。
烷 烃 图 11.15 乙烷的球棍模型
烷烃里,除了甲烷外还有乙烷(C H ,ethane)、丙烷
2 6
(C H ,propane)、丁烷(C H )等。它们的结构特点、化
3 8 4 10
学性质跟甲烷相似。下表列举了几种烷烃的物理性质。随
着烷烃分子里碳原子数的递增,它们的物理性质呈规律性
的变化。 图 11.16 丙烷的球棍模型
思考与练习
烷烃物理性质的递变规律
阅读下表,并回答问题:
图 11.17 丁烷的球棍模型
几种烷烃的物理性质
液态时的密度
名 称 结构简式 常温时的状态 熔点(℃) 沸点(℃)
(g/cm3)
甲 烷 CH 气 -182.5 -164 0.466*
4
乙 烷 CH CH 气 -183.3 -88.6 0.572**
3 3
丙 烷 CH CH CH 气 -189.7 -42.1 0.5005
3 2 3
丁 烷 CH (CH ) CH 气 -138.4 -0.5 0.5788
3 2 2 3
戊 烷 CH (CH ) CH 液 -130 36.1 0.6262
3 2 3 3
庚 烷 CH (CH ) CH 液 -90.61 98.42 0.6838
3 2 5 3
辛 烷 CH (CH ) CH 液 -56.79 125.7 0.7025
3 2 6 3
癸 烷 CH (CH ) CH 液 -29.7 174.1 0.7300
3 2 8 3
十 六 烷 CH (CH ) CH 液 18.1 286.5 0.7730
3 2 14 3
十 七 烷 CH (CH ) CH 固 22 301.8 0.7780(固态)
3 2 15 3
二十四烷 CH (CH ) CH 固 54 391.3 0.7991(固态)
3 2 22 3
*是-164 ℃时的值。
**是-108 ℃时的值,其余都是20 ℃时的值。
111.烷烃分子中随着碳原子数的增加,熔点、沸点发生怎样
的变化?常温下,烷烃的状态跟碳原子数有什么关系?
2.相邻烷烃分子组成有什么差异,写出烷烃分子中碳原子
数和氢原子数的关系式。
3.己烷的分子式为 ______,常温下是 ______态,
由上表数据推测其熔点大于_____℃,小于_____℃。
化学上,把结构相似、在分子结构式上相差一个或若干
个某种原子团的化合物互称为同系物(homologue)。在烷烃
中,甲烷、乙烷、丙烷等相差n个CH ,它们互为同系物。
2
烷烃的通式为C H (n≥1)。互为同系物的各种物质化学
n 2n+2
性质很相似。在通常状况下,烷烃都很稳定,在空气中可以
点燃,在光照条件下都能与氯气发生取代反应。
烷烃中,有很多物质的分子
【资料库】
组成完全相同,但性质却不同。例
如,有两种熔点、沸点和密度都不
正丁烷、异丁烷的物理性质
同的丁烷,它们的分子组成都是
比 项 正丁烷 异丁烷
C H 。为了区别起见,人们把它
4 10
熔点 (℃) -138.4 -159.6
们分别叫做正丁烷(n-butane)和
沸点 (℃) -0.5 -11.7
异丁烷(iso-butane)。
液态时密度 (g/cm3) 0.578 8 0.557 为什么这两种组成完全相同
的丁烷有不同的性质呢?因为有
机物的性质不仅与它们的组成元
素和连接方式有关,还与它们分子里原子的连接次序有关。
也就是说分子式或组成(composition)相同的化合物,只要
它们分子里原子连接次序和方式不同,即具有了不同的结
构(structure),它们就会有不同的性质。这两种丁烷分子
的结构不同因而具有不同的性质。
正丁烷分子里的4个碳原子连接成直链,异丁烷分子有
支链。
12H H H
H H H H
H C C C H
H C C C C H
H H
H H H H H C H
正丁烷 H
异丁烷
图 11.18 正丁烷的球棍模型 图 11.19 异丁烷的球棍模型
化合物的分子式相同而结构不同的现象,叫做同分异
构现象(isomerism),具有同分异构现象的化合物互称为同
分异构体(isomer)。
例如,戊烷(C H )有三种同分异构体。
5 12
正戊烷(n-pentane) 异戊烷(iso-pentane) 新戊烷(neo-pentane)
图 11.20 戊烷的同分异构体的球棍模型
表 11.3 正戊烷、异戊烷、新戊烷的沸点、熔点和密度
比 项 沸点 (℃) 熔点 (℃) 密度 (g/cm3)
正戊烷 36.1 -130 0.6262
异戊烷 27.8 -159.9 0.6201
新戊烷 9.5 -16.5 0.6135
13拓展视野
数量庞大的有机化合物
19世纪,德国化学家凯库勒(Friedrich August Kekule,1829—1896)
及英国化学家库帕(Archilbald Scott Couper,1831—1892)先后提出了四
价碳及碳原子间可以相互连接成链的学说。碳碳之间互相连接成链,构成碳
架结构,可形成无数种有机化合物。
四价碳及碳链学说的提出,使人们开始真正认识到有机化合物中原子间的结
合方式,解开了为什么由少数几种元素能构成数量庞大的有机化合物之谜。
烃分子失去1个氢原子后所剩余的部分叫做烃基,烷烃
表 11.4 烃基
分子失去1个氢原子后所剩余的部分叫做烷基(alkyl),烷
烷 基
基一般用“R—”表示。
—CH 甲基 (methyl)
3 有机物种类繁多,分子组成和结构比较复杂,所以有
—C H 乙基 (ethyl)
2 5 机物的命名十分重要。
—CH 2 CH 2 CH 3 丙基 (propyl) 碳原子数从1到10的烷烃用天干命名法,即甲、乙、丙、
丁、戊、己、庚、辛、壬、癸,以后则为十一、十二……
如果烷烃带有支链,天干命名法就不能满足需要,下面介
绍一种通用的系统命名法,这种命名法的步骤如下:
1. 选定分子里最长的碳链作主链,并按主链上碳原子
的数目称为某烷。
2. 把主链中离支链较近的一端作为起点,用1、2、3…
数字给主链的各个碳原子依次编号。
3. 把支链作为取代烃基。取代烃基和名称写在烷烃名
称的前面,并用阿拉伯数字注明它在烷烃直链上的位置,在
数字和烃基名称间用“-”隔开。
4. 相同的取代烃基可合并起来用二、三等数字表示。表
示取代基位置的阿拉伯数字之间用“,”分开。
例如:
1 2 3 4 5
CH — CH — CH — CH — CH
3 2 3
— —
CH CH
3 3
2,3-二甲基戊烷
(2,3-dimethyl pentane)
14若有不同的取代基时,简单的烃基写在前面,复杂的写在
后面,在两个取代基之间的阿拉伯数字前后都要用“-”隔开。
例如:
7 6 5 4 3 2 1
CH — CH — CH — CH — CH — CH — CH
3 2 2 2 3
CH CH
2 3
CH
3
2-甲基-4-乙基庚烷
(2-methyl-4-ethyl heptane)
[思考与复习11.1]
1.下列物质中属于烃类的是( )。
(A)CH Cl (B)C H NO
3 6 5 2
(C)C H (D)C H OH
4 10 2 5
2.下列物质中不能和氯气发生取代反应的是( )。
(A)CH (B)CCl
4 4
(C)CH Cl (D)CH Cl
2 2 3
3.互为同分异构体的烷烃不可能具有相同的( )。
(A)分子式 (B)通式
(C)相对分子质量 (D)结构式
4.下列有机物中,是烷烃同系物的是( )。
(A)C H (B)C H
5 10 3 8
(C)C H (D)C H
2 2 6 6
5.丙烷(C H )和十七烷(C H )互为________。
3 8 17 36
6.某直链烷烃分子中有20个氢原子,它的分子式是__________,名称
是________。
7.写出CH —CH—CH—CH 的一氯代物可能有的结构简式。
3 3
CH CH
3 3
8.某气体含碳82.7%,含氢17.3%,在标准状况下的密度是2.59 g/L,求该气体的
分子式。
9.目前,燃气助动车使用量较大,但由于助动车发动机结构简单,汽油燃烧不充
分,带来了严重的空气污染,下列措施中错误的是( )。
(A)在现有助动车的排气管上装一个“催化转化器”,使烃充分燃烧,使CO、NO
转化为CO 和N
2 2
15(B)开发研制使用石油液化气为燃料的助动车
(C)使用高标号的汽油
(D)推广电动助动车
10.上海城市居民所使用的燃料主要是管道煤气,但某些地区已开始使用东海天
然气作为民用燃料。管道煤气的主要成分是CO、H 和少量烃类,天然气的主要成分是
2
CH 。燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是 ________。
4
如果将燃烧管道煤气的灶具改烧天然气,灶具的改进方法是________(填
“增大”或“减小”) 进风口。如不作改进可能产生的不良后果是_________
_______________________________________
_____________________________________ 。
16石油化工的龙头——乙烯
11
.2
(THE LEADING ROLE OF PETROCHEMICAL
INDUSTRY —— ETHYLENE)
石油化工的兴起
石油不仅是重要的能源,而且是宝贵的资源。由石油
炼制得到的许多化工原料进一步加工制得的化工产品广泛
用于农业、工业、国防建设、医药卫生,以及日常生活各个
领域。石油化工的兴起促进了整个世界的进步和发展。
图 11.21 颗粒形石油化工原料
图 11.22 石油化工产品及其用途
石油化工是炼油的继续和发展。当石油分馏得到的燃料
油愈来愈不能满足社会日益增长的需要时,人们就将分馏出
来用途较少的重油隔绝空气高温加热,把相对分子质量较
17大、沸点较高的重油裂化(cracking)成相对分子质量较小、
沸点较低的烃作燃料油。裂化的方式有热裂化(500~600 ℃)
和催化裂化(460~520 ℃)。在石油裂化中还会产生少量乙
烯等小分子化合物。
课堂实验
石蜡的催化裂化
在试管里放入4 g石蜡和3 g粉末状氧化铝,给试管加热。待石蜡熔化
后再持续加热5~10 min,点燃导出管口的尾气。观察试管里的现象,并嗅
闻其中的气味。
C
A
B
图 11.23 催化裂化实验简易装置 图 11.24 催化裂化装置
A催化裂化;B部分裂化气冷凝;C裂化气 工业上常使用人工合成的硅酸铝、分子筛等
导出口 作催化剂
实验现象:__________________________
________________________________。
【资料库】 为满足化学工业对乙烯的需求,科学家们将重油催
化裂解(700~1 000 ℃)生产乙烯(ethylene),于是石
第一个乙烯生产基地
油化工诞生了。
1920年美国联合碳 高分子化合物聚乙烯(polyethylene)可以用乙烯合
化公司研究高温裂解制 成,这是一种用途广泛的塑料。
乙烯成功。1923年建成 高分子工业的兴起,首先要在理论上有所突破。德
了第一个生产乙烯的石 国著名化学家施陶丁格(Hermann Staudinger,1881—
油化工基地。 1965)在大量研究基础上,从理论上提出了高分子学说。
18化学史话
高分子化学学科的开拓者
——施陶丁格
施陶丁格是德国化学家。20世纪20年代,他将天
然橡胶氢化,得到了氢化天然橡胶,证明了天然橡胶不
是小分子缔合的结果,而是相对分子质量大的化合物,
正式提出了“高分子化合物”的概念,提出了高分子化
合物黏度与平均式量的关系式,从而建立了高分子化
学学科,并因此获得了1953年诺贝尔化学奖。 图 11.25 施陶丁格
人们最初是将乙烯通过高压合成聚乙烯的。高压装置
设备比较昂贵,不利于大规模工业生产,而且高压聚乙烯
的性能又不令人满意。为此,各国科学家进行反复试验,德
国化学家齐格勒发明了一种催化剂,成功地在低压下合成
了聚乙烯,聚乙烯工业迅速发展起来了。
化学史话
攻克聚乙烯工业化生产的“堡垒”
1963年诺贝尔化学奖授予德国化学家齐格勒(Karl Ziegler, 1898—
1973)和意大利化学家纳塔(Giulio Natta, 1903—1979)。齐格勒发明了在
低压下将乙烯合成聚乙烯的催化剂。低压合成聚乙烯生产成本低,设备投资
少,工艺简单,产物性能优良。纳塔改进了齐格勒的催化剂,把丙烯聚合成
结构很规则的定向聚丙烯。齐格勒和纳塔开发的催化剂被称为齐格勒-纳塔
催化剂。
为了纪念这两位科学家的业绩,人们在德国普朗克煤炭研究院建造了一
座他们的双人铜像。
这两位科学家的发明,使聚乙烯、聚丙烯等高聚物可以大规模生产,对
乙烯和丙烯等原料的需求量剧增,推动了20世纪50年代以来石油化工的迅
速发展。
19乙 烯
乙烯为无色易燃气体,熔点-169 ℃,沸点-103.7 ℃,
几乎不溶于水,难溶于乙醇,是石油化工最重要的基础原
料。乙烯产品广泛用于农业、工业、交通、军事等领域,用
于制造塑料、合成纤维、合成橡胶、有机溶剂等。乙烯是植
物生长的调节剂,可作果实催熟剂等。乙烯已成为现代石油
化工的一个龙头产品。
乙烯生产的发展推进了石油化工基础原料和产品的发
展,因此常把乙烯产量作为衡量石油化工发展水平的标志,
也是一个国家综合国力的表现。
目前,我国乙烯生产能力跃居世界前列。2006年我国乙
图 11.26 农用塑料薄膜
烯产量达9.41×106t。上海石化目前拥有年产1.5×105t和
7×105t两套乙烯生产装置,是我国最大的乙烯生产基地。
【资料库】
2006年上海石化乙
烯年产量9.6×105 t。
上海石化乙烯年产
量持续保持高产稳产
态势。
图 11.27 上海石化
乙烯的分子式是C H ,与碳原子数相同的乙烷相比较,
2 4
乙烯分子比乙烷(C H )分子少两个氢原子。
2 6
根据乙烯的分子组成,写出乙烯的电子式和结构式。
图 11.28 乙烯的分子模型
20课堂实验
乙烯的实验室制法及其性质
在烧瓶里注入酒精和浓硫酸(体积比1:3)
的混合液约20 mL(配制此混合液应在冷却和
搅拌下将15 mL浓硫酸慢慢倒入5 mL酒精
中),放入几片碎瓷片。加热,使温度迅速升
到170 ℃,酒精即脱水变成乙烯,用排水集气
法收集乙烯。再将气体分别通入溴水及酸性高
锰酸钾溶液,观察现象。
图 11.29 乙烯的制取
现象:_______________
____________________。
制取乙烯的化学方程式:___________________。
乙烯分子里含有碳碳双键,其中的一个键容易断裂,可
加上其他的原子或原子团。乙烯与溴水中的溴反应时,两个
溴原子分别加在双键的两个碳原子上,生成1,2-二溴乙烷。
H H H H
H-C=C-H + Br-Br H-C-C-H
Br Br
1,2-二溴乙烷
(1,2-dibromoethane)
含有碳碳双键的烃叫做烯烃(alkene)。乙烯是最简单
也是最重要的烯烃。
含有碳碳双键或碳碳叁键的烃称为不饱和烃
(unsaturated hydrocarbon)。双键和叁键称为不饱和键,与
不饱和键相连的碳原子称为不饱和碳原子。有机物分子里
不饱和碳原子和其他原子或原子团直接结合而生成新物质
的反应叫做加成反应(additive reaction)。
乙烯在空气中燃烧时,火焰明亮,同时产生黑烟。1 mol
乙烯完全燃烧放出1 411 kJ热量,这是一个氧化反应。
21点燃
C H + 3O 2CO + 2H O
2 4 2 2 2
乙烯使酸性高锰酸钾溶液褪色,也属于氧化反应。
在适当的温度、压强和催化剂存在条件下,乙烯分子
里碳碳双键中的一个键断裂后,碳原子之间能相互结合成
很长的碳链。
CH =CH + CH =CH + CH =CH + …
2 2 2 2 2 2
…-CH -CH -CH -CH -CH -CH -…
2 2 2 2 2 2
反应的化学方程式可以简写为:
nCH =CH -[ CH -CH - ]
2 2 2 2 n
聚乙烯
由相对分子质量小的化合物分子互相结合成为相对分子
质量很大的化合物的反应,称为聚合反应(polymerization)。
拓展视野
高分子化合物
高分子化合物简称高分子,为相对分子质量从几千到几十万甚至几百万
的化合物。高分子中成千上万的原子通过共价键连接起来。
高分子一词一般指的是有机高分子。完全由人工方法合成的高分子是由
一种或几种小分子通过聚合制成的,所以叫做聚合物。用作原料的小分子称
做单体。单体聚合成高分子的反应就是聚合反应。单体聚合成的相对分子质
量较小的产物称低聚物;两种或两种以上单体一起聚合称共聚合,产物称共
聚物。
聚合反应主要有两大类。一是链式聚合反应,如烯烃类单体的加成聚
合,简称加聚;二是逐步聚合反应,如双官能团的二元酸与二元胺的缩合聚
合,简称缩聚。
乙烯聚合成聚乙烯的反应也是加成反应,所以又称加
聚反应。
22图 11.30 聚乙烯高分子化合物
图 11.31 聚乙烯制品
装食品的塑料袋和容器是用聚乙烯制成的,加工时不掺增塑剂和稳定剂,使用时安全无毒
拓展视野
烯 烃
分子里含有碳碳双键(C=C)的不饱和链烃叫做烯烃。通常我们说的
烯烃是指含一个碳碳双键的烯烃。烯烃分子比相应的烷烃分子少两个氢原
子,它的通式是C H (n≥2)。烯烃同系物也是依次相差一个CH 原子团,
n 2n 2
随着分子中碳原子数的增加,它们的物理性质呈现有规律的递变。烯烃里其
他同系物的化学性质与乙烯相类似。
二烯烃和合成橡胶
分子里含有两个双键的链烃叫做二烯烃,例如1,3- 丁二烯(1,3-
butadiene, CH =CH-CH=CH )、异戊二烯(isoprene,CH =C-CH=CH )
2 2 2 2
-
CH
3
23都是二烯烃里重要的同系物。二烯烃比烯烃多一个双键,少两个氢原子,所
以二烯烃的通式是C H (n≥4)。
n 2n-2
与烯烃一样,二烯烃分子里碳碳双键中的一个键容易断裂,也能发生加
成、聚合反应。合成橡胶就是以丁二烯、异戊二烯等为单体聚合而成的。
早在1879年科学家用天然橡胶制成异戊二烯单体。第一次世界大战期
间,德国的海上运输被封锁,切断了天然橡胶的输入,他们于1917年首次
用2,3-二甲基-1,3-丁二烯(2,3-dimethyl-1,3-butadiene)生产了合成橡胶。
在战争期间,甲基橡胶共生产了2 350 t。
按使用特性划分,橡胶可分为通用型和特种橡胶两大类。通用型合成橡
胶是指可以部分或全部代替天然橡胶使用的胶种,例如,
丁苯橡胶、异戊橡胶、顺丁橡胶等,主要用于制造各
种轮胎及一般工业橡胶制品;特种橡胶是有特殊性
能并用于特种场合的橡胶,例如,硅橡胶、氟橡胶、
聚硫橡胶等,这类橡胶可具有耐高温、耐油、耐臭
氧、耐老化和高气密性等特点。这类橡胶用量虽小,却
是不可缺少的胶种。
由于橡胶分子中含有双键,它长期受空气和日光的作
用,会被氧化而变硬、变脆,这就叫橡胶的
老化。工业上用硫处理橡胶,使线形橡
胶分子交联起来形成硫化橡胶,以
改善橡胶的性能,使它具有较高
的强度、韧性、良好的弹性、化
学稳定性和耐腐蚀性等。
图 11.32 橡胶制品
[思考与复习11.2]
1.用化学方程式表示下列物质间的转变。
CH CH OH
3 2
CH BrCH Br CH =CH CH CH
2 2 2 2 3 3
CH CH Br [ CH CH ]
3 2 2 2 n
242.液化石油气的主要成分是( )。
(A)甲烷、乙烯 (B)丙烷、丁烷
(C)甲烷、氢气 (D)乙烯、一氧化碳
3.相同物质的量的乙烷和乙烯完全燃烧,所需氧气的质量比是( )。
(A)3∶7 (B)1∶2 (C)7∶6 (D)1∶1
4.关于乙烯用途的下列说法中,不正确的是( )。
(A)制造塑料 (B)制取有机溶剂
(C)用作果实催熟剂 (D)用作燃料
5.下列物质中,与溴水混合,振荡静置后,混合液分成两层,溴水层几乎无色的
是( )。
(A)己烯 (B)煤油 (C)戊烷 (D)四氯化碳
CH
3
-
6.写出合成 [ CH -CH ] 的烯烃分子的结构简式: 。
2 n
7.在标准状况下,将4 L乙烷和乙烯的混合气体通过溴水,充分反应后气体体积
减少2.4 L。求混合气体中乙烯所占的体积分数。
8.用乙烯为原料生产聚乙烯5×105 t,生产过程中实现“零排放”,原料的利用
率为99%,试计算消耗乙烯多少万吨。
9.某烃0.1 mol完全燃烧生成8.96 L二氧化碳(标准状态)和7.2 g水,该烃的
密度为2.5 g/L(标准状态),求这种烃的分子式。
10.阅读下面短文,说出乙烯的生产过程和用途。
The first member of the alkene series is a colorless gas with a characteristic sweetish odor.
It burns with a luminous, smoky flame. With air or oxygen, it forms a highly explosive mixture.
It is usually presented in illuminating gas to the extent of a few percent.
Ethylene is obtained today from the gases liberated during the cracking process in gasoline
production. It is also produced from natural gas, which is a mixture of gaseous paraffins, by
cracking under special conditions. The separation of ethylene from the other products is readily
accomplished.
Ethylene is used by growers of citrus fruits since it hastens ripening. Exposure of a green-
colored fruit to an atmosphere of ethylene develops the highest yellow or orange color. Ethylene
also finds use as an anesthesia and in some respects it is superior to ether.
25煤化工和乙炔
11
.3
(COAL CHEMICAL INDUSTRY AND ACETYLENE)
【资料库】
煤和煤化工
煤的分布
煤是一种矿物燃料,煤在国民经济建设和日常生活中
煤资源分布在世 占有重要的地位。
界各地,但比较集中 在人类历史上,蒸汽机的发明推动了产业革命,而煤
地分布在北纬30°以
逐渐成为了主要能源。
上地区。预测储量:
煤是由远古时代植物经过漫长复杂的变化而转变成的
苏联居首位,美国次
固体可燃物。它是由有机物、无机物所组成的复杂混合物。
之,我国居第三位。
主要组成元素是碳,此外还含有少量的氢、氮、硫、氧以及
三者之和占全球煤资
微量的硅、铝、钙、铁等元素。
源的90%。
表 11.5 无烟煤的化学组成
元 素 质量分数(%)
C 85.0
H 5.0
O 7.6
N 0.7
S 1.7
图 11.33 煤的形成
26煤是非再生能源,又是宝贵的资源。煤作为燃料燃烧 【资料库】
时只利用了其价值的一部分,同时,燃烧产生的二氧化硫
和氮氧化物对环境会造成严重污染。 煤的形成
合理开采和综合利用煤资源需要解决的问题是如何使
按生物演化过程,
煤转化为清洁的能源,如何提取和分离煤中所含的宝贵的
地球的历史可分为古
化工原料。
生代、中生代和新生
煤的综合利用有煤的气化、煤的干馏和煤的液化等。
代三大时期。
煤的气化是让煤在氧气不足的情况下部分氧化,使煤
气候温湿、植物
中的有机物转化为氢气、甲烷和一氧化碳等气体物质。气
茂盛始于古生代中期,
体燃料可作为城市的管道煤气,同时经分离提纯后可得到
距今有3亿年之久。
重要的化工原料。
科学家们提出的现代
煤的干馏是把煤隔绝空气加强热使它分解。煤经过干 成煤理论认为煤化过
馏能生产出焦炭、煤焦油、粗氨水和焦炉气等。焦炭可用于 程是:植物→泥炭(腐
冶金、电石、合成氨造气、燃料等。煤焦油可以通过分馏制 蚀泥)→褐煤→烟煤→
得重要的化工原料。焦炉气的重要成分是氢气、甲烷,其中 无烟煤。
混有少量的一氧化碳、二氧化碳、乙烯等其他气体。
图 11.34 煤化工生产 图 11.35 煤化工产品
课堂实验
煤的干馏
把烟煤粉放在铁管(或瓷管或硬质
试管)里隔绝空气加热,观察U形管里
发生的变化,并点燃U形管管口的气体。
实验现象:__________
_________________
_________________。
图 11.36 煤的干馏
27煤磨成煤粉后和一些燃料油混合在催化剂作用下加氢,
得到的液化产物叫做人造石油。
我国的煤炭资源极为丰富,总储量居世界第三位。我
国又是世界上最大的耗煤国家,在能源结构中煤炭占70%,
而且煤的利用率还需提高。因此煤的综合利用是十分重要
的问题。
在煤的开发和利用过程中,要合理处理“废气”、“废
水”和“废渣”,做到减少污染,保护环境。
表 11.6 我国煤、石油、天然气储量的世界排位(2006年)
比 项 探明储量 排 位
煤 1.145×1011 t 第3位
石油 2.2×109 t 第12位
天然气 7.554×1011 m3 第3位
拓展视野
矿石燃料能用多少年
20世纪60年代以前,煤是世界上最重要的能源,但后来石油的比重
越来越大,发达国家的能源消耗以石油为主,而发展中国家仍以煤为主要
能源。
矿石燃料的资源有限,按目前能耗水平,地球上煤的开采只能维持约
200年,而石油和天然气只能维持50年左右,许多发达国家早已开始充分利
用水力资源和其他新能源。
从导电高分子说起
2000年诺贝尔化学奖表彰的研究成果是发现了有机高
聚物可以导电。科学家将聚乙炔(polyacetylene)用碘或溴
掺杂以后,聚乙炔的电导率提高了7个数量级,从而改变了
塑料不导电的观念,开发了有机高分子导电材料。
28化学史话
2000年化学诺贝尔奖的贡献与启示
长期以来,塑料以其良好的绝缘性能广泛用于电器工业。随着科学的发
展,人们发现有机聚合物不仅可作绝缘体,也可以作为导电体。
2000年化学诺贝尔奖得主是日本化学家白川英树(Hideki Shirakawa,
1936— )、美国化学家麦克迪尔米德(Alan MacDiarmid, 1927— )和美国
物理学家黑格(Alan Heeger, 1936— )。白川英树的研究生因催化剂加得太
多而无意中合成出了前人没有制得的具有金属光泽的薄膜状聚乙炔,这三位
科学家联合进行研究,发现用碘或溴蒸气处理(掺杂)过的聚乙炔,电导率
提高了7至9个数量级,显示出接近金属的电导率。这一发现改变了塑料不
导电的观点,成功开发了导电性高分子材料,为各种光、电材料、薄型轻质
电池和手机显示屏开辟了广阔前景,高分子导体已成为21世纪令人瞩目的
新材料研究方向之一。
几位科学家重视开创性研究和研究成果的转化,他们给人类带来的不仅
是财富,而且更多的是启示。
合成聚乙炔塑料的原料是乙炔,长期以来工业上曾用
煤为主要原料来制取乙炔。
把煤置于隔绝空气的密闭炼焦炉内加热,分解出焦炉
气、煤焦油等物质后留下的固体物质叫焦炭。把焦炭、生石
灰放在电炉里高温反应,可以得到电石,即碳化钙。将制得
的电石与水反应可得到乙炔。用这种方法来制取乙炔要消
耗大量的电能。
CaO + 3C 2 5 0 0 ~ 3 00 0 ℃ CaC + CO
电炉 2
CaC + 2H O HC CH↑+ Ca(OH)
2 2 2
石油化工的兴起和大量天然气的开采,使乙炔的生产
从用煤为原料转为用石油和天然气为原料。但近年来,由
于石油价格猛升,用煤制乙炔的前景又被看好了。
29乙 炔
乙炔(acetylene)俗名电石气,分子式是C H 。纯净的
2 2
乙炔是无色、无臭的气体,微溶于水,易溶于有机溶剂。由
电石生成的乙炔中因混有磷化氢和硫化氢等杂质而有特殊
的气味。
乙炔的分子结构特点和化学性质
根据乙炔的分子组成,写出乙炔的电子式和结构式,并推
测乙炔可能具有哪些化学性质。
图 11.37 乙炔的分子模型
课堂实验
乙炔的实验室制法及其性质
在烧瓶里放几小块碳化钙,旋开分液漏
斗活塞,使水慢慢滴下,用排水法收集乙炔。
观察乙炔的颜色、状态。
点燃制得的乙炔。
把纯净的乙炔分别通入盛有酸性高锰酸
钾溶液和溴水的试管里,观察现象。
现象:_______________
图 11.38 制取乙炔
____________________
___________________。
与乙烯相似,乙炔容易被氧化和起加成反应。
乙炔燃烧时火焰明亮,产生黑烟,并放出大量的热能。
1 mol乙炔完全燃烧放出1 300 kJ热量。
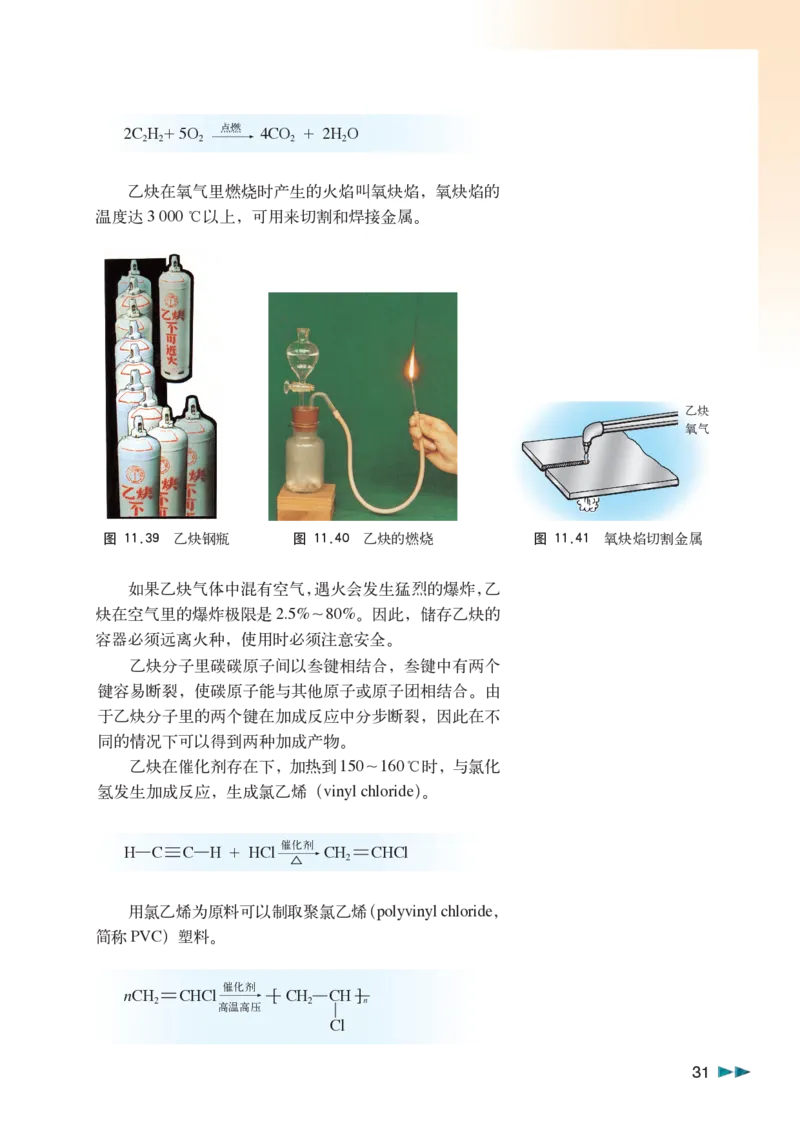
302C H + 5O 点 燃 4CO + 2H O
2 2 2 2 2
乙炔在氧气里燃烧时产生的火焰叫氧炔焰,氧炔焰的
温度达3 000 ℃以上,可用来切割和焊接金属。
乙炔
氧气
图 11.39 乙炔钢瓶 图 11.40 乙炔的燃烧 图 11.41 氧炔焰切割金属
如果乙炔气体中混有空气,遇火会发生猛烈的爆炸,乙
炔在空气里的爆炸极限是2.5%~80%。因此,储存乙炔的
容器必须远离火种,使用时必须注意安全。
乙炔分子里碳碳原子间以叁键相结合,叁键中有两个
键容易断裂,使碳原子能与其他原子或原子团相结合。由
于乙炔分子里的两个键在加成反应中分步断裂,因此在不
同的情况下可以得到两种加成产物。
乙炔在催化剂存在下,加热到150~160 ℃时,与氯化
氢发生加成反应,生成氯乙烯(vinyl chloride)。
催化剂
H C C H + HCl CH CHCl
2
用氯乙烯为原料可以制取聚氯乙烯(polyvinyl chloride,
简称PVC)塑料。
催化剂
nCH CHCl [ CH CH ]
2 2 n
高温高压
Cl
31拓展视野
阻燃纤维
把氯乙烯或溴乙烯掺入腈纶高分
子中,就制成了能阻止燃烧的纤维,叫
做阻燃纤维,这种纤维一旦着火后,会
使火势越来越小,直至自动熄灭。
阻燃纤维独特的性能是天然纤维
和其他合成纤维所没有的,因此,它广
泛应用于航空、航海领域,并逐渐进入
日常生活。
图 11.42 消防服
【资料库】
塑料加工
在聚氯乙烯中
掺入一些高沸点的
有机化合物(增塑
剂)能使坚硬的聚
氯乙烯变得柔软。
加工聚氯乙烯
塑料时,加入发泡
剂,能制出疏松多孔 (a)玩具 (b)软管
的泡沫塑料。 图 11.43 塑料制品
拓展视野
几种常见的塑料
由乙烯聚合而生成的聚乙烯,具热塑性。纯品呈乳白色,手感似蜡,耐
化学腐蚀,电绝缘性能极优。它主要用以制造薄膜(如食品袋、农用薄膜等)、
容器、管道、日用品等,并作为电视、雷达等高频绝缘材料。
聚丙烯是一种半结晶的热塑性塑料,具有较高的耐冲击性,强韧,抗多
种有机溶剂和酸碱腐蚀,在工业上有广泛的应用。例如,用作输送管道、化
32学容器及设备衬里、表面涂层等防腐材料。也可用于作电绝缘性的制件,如
电视机座架,高电压杯,电线圈架,电缆等。
聚氯乙烯由氯乙烯聚合而成,耐腐蚀、不易着火。它可用于制造合成纤
维(氯纶)和塑料。按所加增塑剂的多少,可制成软质和硬质的热塑性塑料。
前者可以制造透明的薄膜(如台布、雨衣等)、人造革及电线的保护套层等,
后者可以制造板材、阀门及管道等。工业用聚氯乙烯塑料有毒,其薄膜不宜
包装食品。
聚苯乙烯由苯乙烯聚合而成,具热塑性。纯品透明,耐化学腐蚀,电绝
缘性能优良,但性脆。它可用于制造电绝缘材料、日用品、薄膜和泡沫塑料
等。色彩斑斓的塑料玩具很多是聚苯乙烯的制品。
聚四氟乙烯是塑料的后起之秀,冠称“塑料王”,它是一种白色、半
透明的结晶聚合物。由于分子中的氟原子与碳原子紧密结合,使碳链的牢
度大大增强,从而具有很多独特的优异性能。聚四氟乙烯耐酸、碱腐蚀,
在-26.9 ℃的低温和250 ℃的高温下不变性。它的电绝缘性好,不受电磁波
影响。聚四氟乙烯可制造低温设备,可作耐腐蚀的反应器,作金属电线的外
皮。由于它对人体无害,可制造人工骨骼、软骨和医疗器械。另外,它还用
于制造雷达及短波器材等。
图 11.44 聚四氟乙烯的用途
聚四氟乙烯作为烹调用具的涂料又称特氟隆。在使用特氟隆餐具时应注
意温度不宜过高,否则会使聚四氟乙烯分解产生有毒物质危害人体健康。
聚甲基丙烯酸甲酯俗称有机玻璃,由甲基丙烯酸甲酯聚合而成,具有热
塑性、耐光、高度透明、质轻、不易破裂等优点,可作玻璃的代用品。常用
作飞机上的透明罩盖或窗玻璃,也在牙科医疗中做假牙和牙托。
用甲醛和苯酚合成的酚醛树脂具热固性。电木是在酚醛树脂中加入填
料,再加工成型的。将酚醛树脂涂于片状材料上,可压制成层压塑料,广泛
用于电绝缘材料、日用品等。家具用的密度板就是酚醛树脂和木屑在加热下
压制成型的。加工不当,密度板会释放出甲醛,危害健康。
33比较乙烷、乙烯、乙炔分子组成、结构特点、
化学性质的异同
烃 乙 烷 乙 烯 乙 炔
分子式
碳的质量分数
结构简式
结构特点
取代反应
加成反应(与溴水反应)
氧化反应(与酸性高锰酸钾溶液反应)
拓展视野
高分子材料的分子设计
当今世界上,塑料、橡胶、合成纤维三大合成
材料年产量已达上亿吨。
材料生产目前正向着从结构—性能—实施的
关系中进行分子设计,以合成指定结构的功能高
分子材料。
发光塑料是一种低辐射聚合物,在这种塑料
材料上加上一定电压后会发光。这种材料可用于
制造警告标志和广告灯,还可应用于体积小、电
图 11.45 新型塑料
压低的产品开发。
[思考与复习11.3]
1.下列各组物质中,能用溴水或酸性高锰酸钾溶液鉴别的是( )。
(A)乙烷、乙烯 (B)乙炔、丙烯
(C)己烷、庚烷 (D)乙炔、丁二烯
342.在标准状况下,将0.672 L的乙炔通入溴水,最多能跟多少克2%的
溴水发生反应?
3.物质的量相同的乙烷、乙烯和乙炔完全燃烧后,生成的二氧化碳和
水的物质的量是否相等?产生的热量是否相等?用化学方程式来说明。
(1 mol乙烷燃烧生成液态水和气态二氧化碳时放出1 588 kJ热量)
4.有a L乙烯和乙炔的混合气体,与氢气发生加成反应时消耗氢气
1.25a L,则混合气体中乙烯和乙炔的体积比是( )。
(A)1∶1 (B)4∶1 (C)2∶1 (D)3∶1
5.下列关于煤的使用中错误的是( )。
(A)煤是非再生能源,储量有限,应停止使用
(B)煤既是一种能源,又是宝贵的资源,要综合利用,提高煤的利用率
(C)煤运输使用方便,我国应合理开采煤、使用煤
(D)我国是以煤炭为主要能源,为了减少大气污染煤在加工和燃烧时要
进行脱硫处理
6.现在人们已能合成自然界并不存在的许多性能优良的有机高分子
材料。
(1)由氯乙烯制取聚氯乙烯的反应属于 反应。
(2)适合于合成聚氯乙烯的原料是( )。
(A)CH ,Cl (B)CH CH ,HCl
4 2 3 3
(C)CH≡CH,HCl (D)CH =CH ,HCl
2 2
(3)下列聚氯乙烯塑料用途中不正确的是( )。
(A)下水管道 (B)塑料雨披
(C)食品容器 (D)衣物包装袋
7.2000年,诺贝尔奖表彰的研究成果是成功实现聚乙炔导电性,从中
你获得什么启示?
8.为了节约资源和能源,保护环境,下列做法中错误的是( )。
(A)回收一次性物品,分类处理
(B)多使用纸盒包装袋
(C)用布制袋购物
(D)焚烧废弃的塑料袋
9.查阅有关资料,了解塑料废弃物的危害及解决方法。
35一种特殊的碳氢化合物—苯
11
.4
(A SPECIAL HYDROCARBON——BENZENE)
苯
煤高温干馏所得的煤焦油里含几百种有机化合物,工
业上,可以用分馏的方法分离出其中重要的化工原料。在
170 ℃以下蒸馏出来的馏出物中主要含苯、甲苯(toluene)、
二甲苯(xylene)等有机物。在石油化工中是使直链烷烃环
化、脱氢后大量生产苯、甲苯和二甲苯的。
图 11.46 苯的生产
表 11.7 煤焦油的分馏产物及用途
温 度 馏出物 用 途
化工原料、合成纤维、
170 ℃以下 苯、甲苯、二甲苯
合成橡胶、塑料、溶剂
170~230 ℃ 酚、萘 染料、炸药、农药
230 ℃以上 蒽、沥青 筑路材料、电极
36在这些有机物中,最重要的化合物是苯。苯是无色带有
特殊气味的液体,分子式为C H ,沸点80 ℃,熔点5.5 ℃,
6 6
密度比水小,在660体积的水中只能溶解1体积的苯。
苯由碳、氢两种元素组成,其中碳的质量分数大,燃烧
时产生黑烟,火焰明亮。1 mol苯完全燃烧放出6 520 kJ热量。
点燃
2C H + 15O 12CO + 6H O
6 6 2 2 2
比较苯分子(C H )与具有相同碳原子数的烷烃分子
6 6
(己烷,C H ),发现苯分子所含有的氢原子少得多,苯似
6 14
乎是一种不饱和烃。那么它的化学性质跟烯烃、炔烃是否
相似呢?
课堂实验
比较苯与烯烃、炔烃的化学性质
1. 在试管里加入1 mL酸性高锰酸钾溶液,再滴加数滴苯,振荡试管。
2. 在试管里加入1 mL溴水,再滴加数滴苯,振荡试管。
实验现象:__________________________
_________________________________
________________________________。
3. 分别安装好实验室制取乙烯和乙炔的装置。
4. 取两支试管,各滴入1 mL酸性高锰酸钾溶液,将乙烯和乙炔分别通
入酸性高锰酸钾溶液中,振荡试管。
5. 另取两支试管,各滴入1 mL溴水,将乙烯和乙炔分别通入溴水中,
振荡试管。
实验现象:__________________________
_________________________________
________________________________。
从实验结果得知,苯与烯烃和炔烃在性质上有很大的
差别。事实证明,苯通常不能与水中的溴发生加成反应,不
能被酸性高锰酸钾氧化。
苯分子里的氢原子能否被其他原子或原子团所取代呢?
37课堂实验
苯与液溴反应
按图11.47所示装置,在具支试管里放入铁丝
球,另取一支试管将苯和液溴按4∶1体积比混合。
在分液漏斗里加入2.5 mL混合液,在双球U形管
里注入四氯化碳,导管通入盛硝酸银溶液的试管
里。开启活塞,逐滴加入苯和液溴的混合液。反
应后将具支试管里的液体倒入盛有氢氧化钠溶液
的烧杯里。
实验现象:_______________
A
B
______________________
______________________ 图 11.47 苯与液溴反应
______________________。
回答问题:
1.双球U形管里盛放四氯化碳的作用是:____________
________________________________。
2.反应中,铁丝起__________作用。
3.写出苯与液溴反应的化学方程式。
______________________________。
4.写出试管B中反应的离子方程式。
______________________________。
苯在催化剂(铁屑或溴化铁)作用下,分子里的氢原子
被溴原子所取代,生成无色的溴苯(bromobenzene)。同样
苯分子里的氢原子还能被其他卤素原子或原子团所取代。
38课堂实验
苯的硝化反应
取一支大试管,加入1.5 mL浓硝酸和2 mL浓硫酸,
摇匀,冷却。在混合酸中慢慢滴加1 mL苯,并不断摇
动,使其混合均匀。然后将试管放在60 ℃的水浴中加热
10min后,把混合物倒入另一只盛水的烧杯里。
实验现象:_________________
_________________________
________________________。
图 11.48 苯的硝化
可以看到,试管底部有油状物质生成,这是苯与硝酸
反应的产物硝基苯(C H NO , nitrobenzene)。
6 5 2
硝酸里的原子团-NO 叫做硝基。苯与硝酸反应时,硝
2
基取代了苯分子里的氢原子,发生取代反应,这个反应叫
做硝化反应(nitration)。
浓硫酸
C H + HO-NO C H -NO + H O
6 6 2 6 5 2 2
硝基苯
苯在加热和催化剂(镍)的作用下,能与氢气起加成反
应,生成环己烷(C H )。
6 12
催化剂
C H + 3H C H
6 6 2 6 12
环己烷
苯的化学性质
化学方程式 反应类型
与酸性高锰酸钾溶液
与液溴(Fe)
与浓硝酸(浓硫酸)
与H
2
在空气中燃烧
391825年,英国化学家法拉第(Michael Faraday, 1791—
1867)首次发现了苯,并确定了苯的分子式是C H 。从分
6 6
子式看,苯应是一个极不饱和的烃,但它却很难起一般不
饱和烃所起的加成反应。关于苯的结构一直困惑着化学家。
1861年捷克中学教师洛希米德(Joseph Loschmidt, 1821—
1895)提出了苯的环状结构。1866年德国化学家凯库勒提
出了苯是单、双键交替的平面环状化合物,称为苯的凯库
勒式,苯的这一结构式的提出对当时有机化学与有机化学
工业发展起着重要的作用。
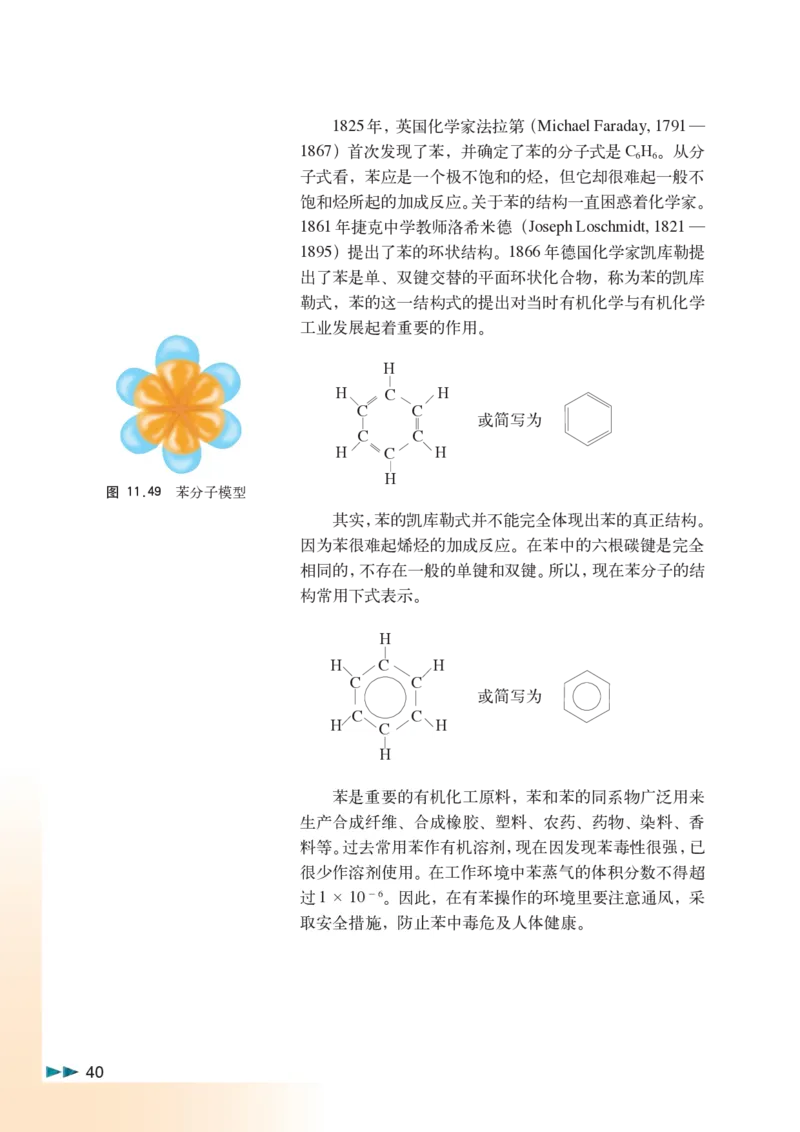
H
H C H
C C
或简写为
C C
H C H
H
图 11.49 苯分子模型
其实,苯的凯库勒式并不能完全体现出苯的真正结构。
因为苯很难起烯烃的加成反应。在苯中的六根碳键是完全
相同的,不存在一般的单键和双键。所以,现在苯分子的结
构常用下式表示。
H
H C H
C C
或简写为
C C
H C H
H
苯是重要的有机化工原料,苯和苯的同系物广泛用来
生产合成纤维、合成橡胶、塑料、农药、药物、染料、香
料等。过去常用苯作有机溶剂,现在因发现苯毒性很强,已
很少作溶剂使用。在工作环境中苯蒸气的体积分数不得超
过1×10-6。因此,在有苯操作的环境里要注意通风,采
取安全措施,防止苯中毒危及人体健康。
40拓展视野
芳 香 烃
自然界里存在不少具有芳香气息的化合物,如香兰素、香豆素、大茴香
醛等,它们都具有苯环,因此含苯环的化合物通称芳香族化合物。
含有苯环结构的化合物很多,如甲苯(C H )、乙苯(C H ,
7 8 8 10
ethylbenzone)、二甲苯(C H )等化合物的分子里都含有一个苯环结构,它
8 10
们都属于芳香烃,是苯的同系物。苯分子里的一个氢原子被甲基(CH — )
3
取代后生成甲苯,被乙基(CH CH —)取代后生成乙苯,两个氢原子被两
3 2
个甲基取代后生成二甲苯。二甲苯有三种同分异构体。
C H
2 5 CH
CH 3
3
CH
3
CH
3 CH
3 CH
3
乙苯 邻二甲苯 间二甲苯 对二甲苯
o-xylene m-xylene p-xylene
[思考与复习11.4]
1.下列物质中不能使溴水褪色的是( )。
(A)乙烯 (B)1,2-二溴乙烯 (C)乙炔 (D)己烷
2.下列各种烃完全燃烧,生成二氧化碳和水的物质的量之比为1∶1
的是( )。
(A)甲烷 (B)乙烷 (C)乙烯 (D)苯
3.下列各组物质可以用分液漏斗分离的是( )。
(A)溴和四氯化碳 (B)苯和溴苯
(C)硝基苯和水 (D)汽油和苯
4.用苯的凯库勒式分别写出苯与溴、与硝酸加硫酸和在催化剂存在下
与氢反应的化学方程式。
5.苯与溴发生取代反应,将生成的溴化氢全部通入足量的硝酸银溶液
中,生成溴化银沉淀94 g,求生成溴苯多少克。
416.查阅有关资料,了解苯及其同系物对人体健康的危害,在使用苯时
如何防止苯中毒。
7.阅读下面短文,比较苯和烯烃的性质。
The simplest aromatic compounds is benzene, C H . By studying this sub-
6 6
stance we shall learn a great deal about the characteristics of the entire class.
Benzene (sometimes called benzol) was discovered in 1825 by E. Faraday. He
obtained it by fractional distillation of an oil which was a by-product of the
manufacture of illumination gas from whale oil. Twenty years later, the substance
was isolated from coal tar and its chemical investigation continued by A. W.
Hofmann.
The analysis and relative molecular mass of benzene correspond to the
formula C H , it is thus a member of a series of hydrocarbons with the general
6 6
formula C H . Although the formula suggests that it is a highly unsaturated
n 2n-6
substance, it is very different indeed from an unsaturated open-chain hydrocarbon.
It reacts neither with bromine water nor potassium permanganate solution. These
two reagents, as we have seen, invariably react with aliphatic hydrocarbons
having one or more double linkages.
42小 结 与 思 考
1.有机物的组成及特点。
(1)含碳元素的化合物(除碳的氧化物、碳化物、碳酸盐等外)。
(2)有机物的特点:种类繁多;大多数有机物难溶于水,易溶于有机溶剂;受热容易分
解,容易燃烧;熔点低;大多数有机物是非电解质,不易导电。
(3) 有机物之间的反应较为复杂,常伴有副反应。
(4)比较有机物与无机物的性质,用什么方法来判断下列物质属于有机物:①植物油;
②尼龙布;③雨披;④油漆;⑤酒精。
2.烃的组成、分类及其性质。
(1)烃。
只由碳和氢两种元素组成的有机物。
(2)烃的分类。
饱和链烃(烷烃)C H (n≥1)
n 2n+2
链烃
单烯烃
烯烃
不饱和链烃 二烯烃
烃 炔烃
饱和环烃(环烷烃)
环烃 不饱和环烃
芳香烃
(3)甲烷、乙烯、乙炔、苯的分子结构特点和性质。
甲烷属于饱和链烃,比较稳定,在一定条件下能起取代、氧化和分解等反应。
乙烯属于不饱和链烃,含碳碳双键。易起加成、氧化和聚合反应。
乙炔属于不饱和链烃,含碳碳叁键。易起加成、氧化反应。
苯属于不饱和环烃,苯中碳碳键十分独特。能起取代、加成、燃烧等反应。
3.同系物、同分异构体。
结构相似、在分子结构式上相差一个或若干个某种原子团的化合物互称为同系物。分子
式相同而结构不同的化合物互称为同分异构体。
4.有机化学反应类型。
取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。
加成反应:有机物分子里不饱和碳原子跟其他原子或原子团直接结合而生成新物质的反应。
聚合反应:相对分子质量小的化合物分子互相结合成为相对分子质量很大的化合物的
反应。
5.煤、石油、天然气。
(1)煤。
① 煤是由有机物、无机物所组成的复杂混合物。主要组成元素是碳,此外还含有少量
43的氢、氮、硫、氧等元素。
② 煤的综合利用有煤的气化、煤的干馏和煤的液化。煤的干馏是把煤隔绝空气加强热
使它分解。
③ 为什么要大力提倡煤的综合利用?
(2)石油。
① 石油主要是各种烷烃、环烷烃、芳香烃的混合物。
② 石油炼制:
分馏——根据各成分的沸点不同分离成一系列的产品。
裂化——使较长的碳链断裂成较短的碳链。
裂解——采取比裂化更高的温度。
③ 举例说明石油在国民经济发展与国防建设中的重要作用。
(3)天然气。
① 天然气的主要成分是甲烷,另外还含有乙烷、丙烷等小分子烷烃。
甲烷是清洁的气体燃料。
② 在农村推广生产沼气具有什么意义?
6.互称为同系物的物质中,下列叙述中错误的是( )。
(A)结构相似
(B)性质不同
(C)分子间可能相差若干个CH 原子团
2
(D)可能分子式相同
7.相对分子质量为72,其一氯代物只有一种的烷烃,它的结构式为( )。
(A)CH —CH —CH —CH —CH
3 2 2 2 3
(B)CH —CH —CH —CH
3 2 2 3
(C)CH —CH —CH—CH
3 2 3
CH
3
CH
3
(D)CH — C —CH
3 3
CH
3
8.下列各组有机物,不互为同分异构体的是( )。
CH
3
CH CH
2 3
(A)CH —CH—CH 与CH —CH—CH —CH —CH
3 3 3 2 2 3
CH
3
(B)CH —CH —CH —CH 与CH —CH—CH
3 2 2 3 3 3
44CH CH CH
3 3 3
(C)CH —CH —CH 与CH —CH —CH—CH
2 2 2 3 2 3
CH CH
3 3
(D)CH—CH 与CH —C—CH
2 3 3
CH CH CH
3 3 3
9.下列各组有机物中,属于同系物的是( )。
(A)C H 与C H (B)C H 与C H
2 4 2 2 3 8 5 12
(C)C H 与C H (D)C H 与C H
2 2 6 6 2 4 4 10
10.已知某烃组成中碳氢质量比是9∶2,在标准状况下,密度为1.964 g/L。试写出该
烃的分子式。
11.用苯可以萃取溶解于水中的溴或碘,这是利用苯的什么性质?在萃取过程中,苯层
在上面还是水层在上面?为什么?萃取后苯层呈什么颜色?
12.当苯与溴发生取代反应时,将生成的溴化氢全部通入足量硝酸银的溶液,生成溴化
银沉淀9.39 g。问有多少克苯与溴起了反应?生成溴苯多少克?
13.某气态烃10 mL,加入100 mL氧气,完全燃烧后,冷却至室温,体积变为75 mL,
再通入足量的石灰水后干燥,气体的体积变为35 mL,求该烃的分子式。
14.在标准状况下,某气态烃112 mL,完全燃烧后生成二氧化碳和水蒸气的体积比是
3∶4,把燃烧产物通过碱石灰,碱石灰质量增加1.02 g,求气态烃的分子式。
15.有机生活垃圾进入江河,在微生物的作用下氧化分解,但大量垃圾进入江河,造成
水质污染的主要表现是( )。
(A)使水体产生有毒物质
(B)降低水体中溶解氧的含量
(C)使水中CO 含量下降
2
(D)使水中溶解氧含量增加
16. 若大量使用以石油为原料的一次性塑料餐具,不仅浪费严重,塑料餐盒的处理成本
高,再利用价值低,而且采用的材料在很长时间内不会分解,造成白色污染。下列说法中正
确的是( )。
(A)开发理想的可降解的塑料餐具
(B)燃烧塑料餐盒,减少白色污染
(C)将塑料餐盒填埋
(D)将塑料餐盒回收,重新加工使用
17.我国西部地区石油、天然气、煤等化石燃料丰富。
(1)化石燃料是( )能源。(多项选择)
(A)一次 (B)两次
(C)可再生 (D)不可再生
45(2)把煤炭转化为焦炭、煤焦油和焦炉气等过程叫( )。
(A)干馏 (B)分馏
(C)催化重整 (D)裂化
(3)我国三峡工程将提供的水电,相当于每年燃烧3×107 t原煤火力发电厂生产的电
能,因此三峡工程有助于控制( )。
(A)氮氧化物的排放 (B)温室效应
(C)碳氢化合物的排放 (D)白色污染
4612
初识生活中的一些含氧有机化合物
PRELIMINARY RECOGNIZE SOME ORGANIC
COMPOUNDS CONTAINING OXYGEN IN DAILY LIFE
◆ 羟基、羧基、醛基官能团 ◆ 消去反应、酯化反应、氧化反应、还原反应
◆ 乙醇、乙酸、甲醛、乙醛的分子结构和性质 ◆ 乙醇的工业制法
47有
机化合物的种类繁多,应用广泛。在有机化
合物中,除了我们已经学过的由碳、氢两种
元素组成的烃类外,还包括由碳、氢、氧或
氮、硫等其他元素组成的有机化合物。酒精、醋酸、合
成纤维、橡胶、塑料、染料、药物等都是这类常用的有
机化合物。
本章我们将学习一些含氧的有机化合物,如乙醇、
乙酸、甲醛、乙醛,认识它们的结构、性质以及用途。通
过探究活动了解学习有机化合物的方法,认识有机反应
的特点,为今后进一步学习有机化学打下基础。
48杜康酿酒话乙醇
12
.1
(TALK ABOUT ETHANOL STARTED FROM DU KANG
MADE WINE)
酒中精华——乙醇
早在4 000年前,我们的祖先就用酒曲使淀粉发酵来酿
酒。
【资料库】
淀粉在有催化剂存在和加热条件下发生水解反应,生
成葡萄糖。
酒的乙醇含量
催化剂 含乙醇的质
(C H O ) + nH O nC H O 饮用酒
6 10 5 n 2 6 12 6 量分数
淀粉 葡萄糖
啤酒 3%~5%
葡萄糖在催化剂的作用下生成乙醇。
葡萄酒 6%~20%
黄酒 8%~15%
C H O 催化剂 2C H OH + 2CO ↑
6 12 6 2 5 2
白酒 35%以上
拓展视野
杜康与酒
传说我国古代有个牧羊人名叫杜康,有一天,他把小米装在竹筒里,带
着竹筒去牧羊。他将竹筒放在一棵树下,忘了吃小米。半个月后,他再次来
到树下,发现了竹筒,打开竹筒,一股清香飘逸出来。他尝了一口,令人陶
醉。于是他带回去给村里人喝,人人都夸奖好喝。此后,他便改行酿酒,办
起杜康酒店,酿成的酒特别甘醇,从此杜康成了酒的别名。
49酒的主要成分是乙醇,乙醇俗称酒精。酿造酒里酒精的
浓度较低,约为12%~16%,人们称之为水酒;用蒸馏法可
怎样检验酒精里是否
以得到乙醇含量较高的高浓度酒。
含有水?
拓展视野
酒对人体的作用
我国有悠久的酿酒历史,也有饮酒的习俗。在《本
草纲目》中记载:“酒辛者能散,苦者能降,甘者居中而
缓,淡者利小便,用为向导,可以通行一身之表。”
酒中的乙醇在人体中酶的催化作用下氧化为乙醛,
乙醛又可以进一步氧化为乙酸。乙酸能增强细胞的活
力,故适量饮酒对人体还是有益的。但过量饮酒时,乙
醇使人体中酶的催化作用减弱甚至失去。过多的乙醇和
乙醛会刺激神经系统,使脑细胞的类脂物质发生化学变
化,导致脑细胞膜硬化,从而产生一系列不良反应,引
图 12.1 葡萄酒
起酒精中毒,所以要避免酗酒行为的发生。
【资料库】
血液中乙醇含量对人行为的影响
血液中乙醇的质量分数(%) 人的行为
清醒程度降低,协调性减弱,
0.05
反应时间迟缓15%~25%
0.10 视觉敏感度降到32%
协调性严重障碍,眩晕,摇
0.25
晃,感觉损伤
0.35 外部感觉麻木,体温下降
0.40 半数的人死于酒精中毒
50探究与实践
推测乙醇的分子结构
1.从乙醇分子式进行推测。
乙醇的分子式为C H O,乙醇分子可能存在的结构简式为:_____
2 6
________________。
2. 实验测定结果。
一定量乙醇与钠完全反应,放出氢气的体积如下(换算成标准状况):
乙醇质量(g) 氢气体积(L)
1.15 0.28
1.84 0.448
2.30 0.56
3. 由实验数据可分析得到:
(1) 1 mol乙醇与钠完全反应,生成 ___ mol氢气,即 ___ mol氢
原子。
(2) 1 mol乙醇分子中存在的活泼氢原子为 ___ mol。
4. 推测。
乙醇分子可能的结构简式为:________________。
图 12.2 乙醇分子的比例模型
乙醇分子是由乙基(-C H )和羟基(-OH)组成的。
2 5
乙醇分子可以看作乙烷分子中的氢原子被羟基取代后
比较乙醇和乙烷分子
生成的产物。烃分子里的氢原子能被其他原子或原子团所
结构的不同点。
取代,生成一系列新的有机化合物,如一氯甲烷、乙醇等。
这些有机化合物从结构上分析,都可以看作由烃衍变而来
的,所以叫做烃的衍生物(derivatives of hydrocarbon)。
51乙醇 (20℃时,密度 0.789 g/cm3,沸点 78.5℃,熔
点-117.3℃) 是无色、透明、有特殊香味的液体,它密度比
水小,易挥发,能溶解多种无机物和有机物,能跟水以任意
比例互溶。
乙醇和乙烷具有不同的化学性质,这是因为乙醇中取
代氢原子的羟基起着重要的作用。这种决定有机化合物的
化学特性的原子或原子团叫做官能团 (functional group)。乙
醇分子里的官能团是羟基 (-OH,hydroxyl)。
乙醇和浓硫酸快速加热到170 ℃左右,每个乙醇分子
会脱去一个水分子生成乙烯分子。在适当条件下,有机化
合物分子内脱去小分子而生成不饱和 (双键或叁键) 化合物
的反应,叫做消去反应 (elimination)。
浓硫酸
C H OH CH =CH ↑ + H O
2 5 170 ℃ 2 2 2
拓展视野
乙 醚
乙醇和浓硫酸共热到140 ℃左右,每两个乙醇分子间会脱去一个水分子
而生成乙醚 (ether)。
H H H H H H H H
浓硫酸
H-C-C-O H+HO-C -C-H H-C-C-O-C-C-H+H O
140 ℃ 2
H H H H H H H H
乙醇的脱水反应随反应条件 (温度) 不同,脱水的方式不同,产物也不
同。所以,我们可以根据物质的化学性质,按照实际需要控制反应条件,使
化学反应朝着我们需要的方向进行。
乙醚是无毒、易挥发的液体,熔点-116.2 ℃,沸点34.5 ℃,有特殊的
气味。乙醚密度比水小,微溶于水,是一种优良的有机溶剂,常用作天然产物
的萃取剂或反应介质。乙醚蒸气很容易着火,空气中如果混有1.9%~36.8%
(体积分数) 的乙醚蒸气,遇火或电火花就会发生剧烈爆炸。因此,使用乙醚
时要特别小心。
乙醚是比较安全的全身麻醉药。早在1842年,美国外科医生朗格首先
用乙醚作麻醉药用于拔牙。4年后,牙科医生莫顿发现乙醚不仅麻醉效果好,
52而且安全,于是在马萨诸塞州举行了公开表演。从此,乙醚开始作为外科手
术的麻醉剂。但乙醚吸入量过大时,可引起患者呼吸系统麻痹,心跳骤停。
现在已使用效果更好的吸入全麻药,乙醚的应用显著减少,一般仅作为成人
全身麻醉的辅助用药。
乙醇在空气中燃烧,火焰呈淡蓝色。
1. 乙醇是一种二次能
C H OH(l) + 3O (g) 2CO (g) + 3H O(l) + 1 367 kJ
2 5 2 2 2 源,用乙醇作燃料有什么
优点?
2.查阅资料,比较相
同质量的甲烷和乙醇燃烧
时放出热量的大小。
图 12.3 用乙醇汽油为燃料的汽车
拓展视野
乙醇汽油的推广和使用
乙醇汽油中的乙醇添加量一般为8%~10%。巴西和美
国是最早推广乙醇汽油的国家,至今已有20多年历史。巴
西是世界上最大的乙醇生产国,美国是世界上第二大乙醇生
产国。此外,新西兰、法国、瑞典、加拿大、墨西哥、哥伦
比亚、菲律宾及肯尼亚等国也生产乙醇汽油。
随着经济持续发展,我国对石油的需求不断增加,石油
进口量也逐年增长。我国正在开发燃料酒精等石油替代品。 图 12.4 乙醇汽油
推广和使用乙醇汽油,既节省了石油资源,又能减少汽车尾
气污染。
目前,我国乙醇生产的主要原料是粮食、甘蔗等。从长远分析,木薯是
取代甘蔗、玉米等原料的理想替代物。在同样的土地资源条件下,种植木薯
比种植甘蔗产量高;用木薯生产乙醇无废料,利用效率高。
53学生实验
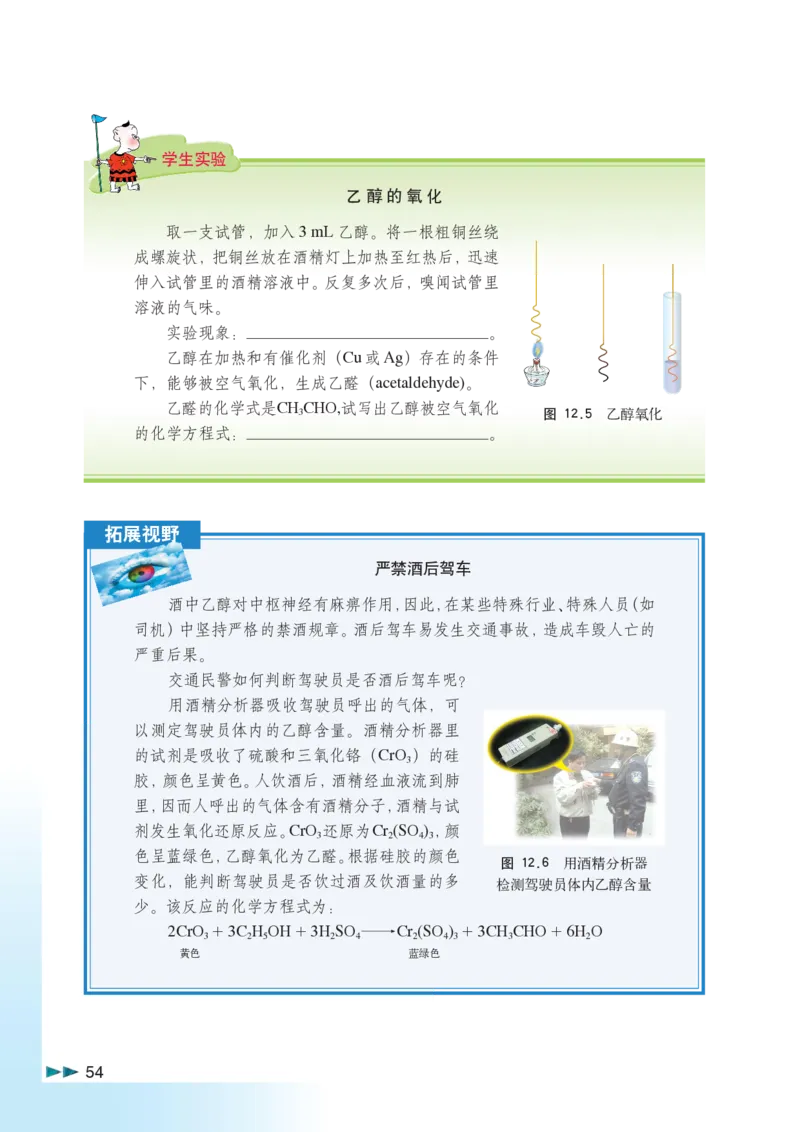
乙醇的氧化
取一支试管,加入3 mL乙醇。将一根粗铜丝绕
成螺旋状,把铜丝放在酒精灯上加热至红热后,迅速
伸入试管里的酒精溶液中。反复多次后,嗅闻试管里
溶液的气味。
实验现象:_______________。
乙醇在加热和有催化剂(Cu或Ag)存在的条件
下,能够被空气氧化,生成乙醛(acetaldehyde)。
乙醛的化学式是CH CHO,试写出乙醇被空气氧化
3 图 12.5 乙醇氧化
的化学方程式:_______________。
拓展视野
严禁酒后驾车
酒中乙醇对中枢神经有麻痹作用,因此,在某些特殊行业、特殊人员(如
司机)中坚持严格的禁酒规章。酒后驾车易发生交通事故,造成车毁人亡的
严重后果。
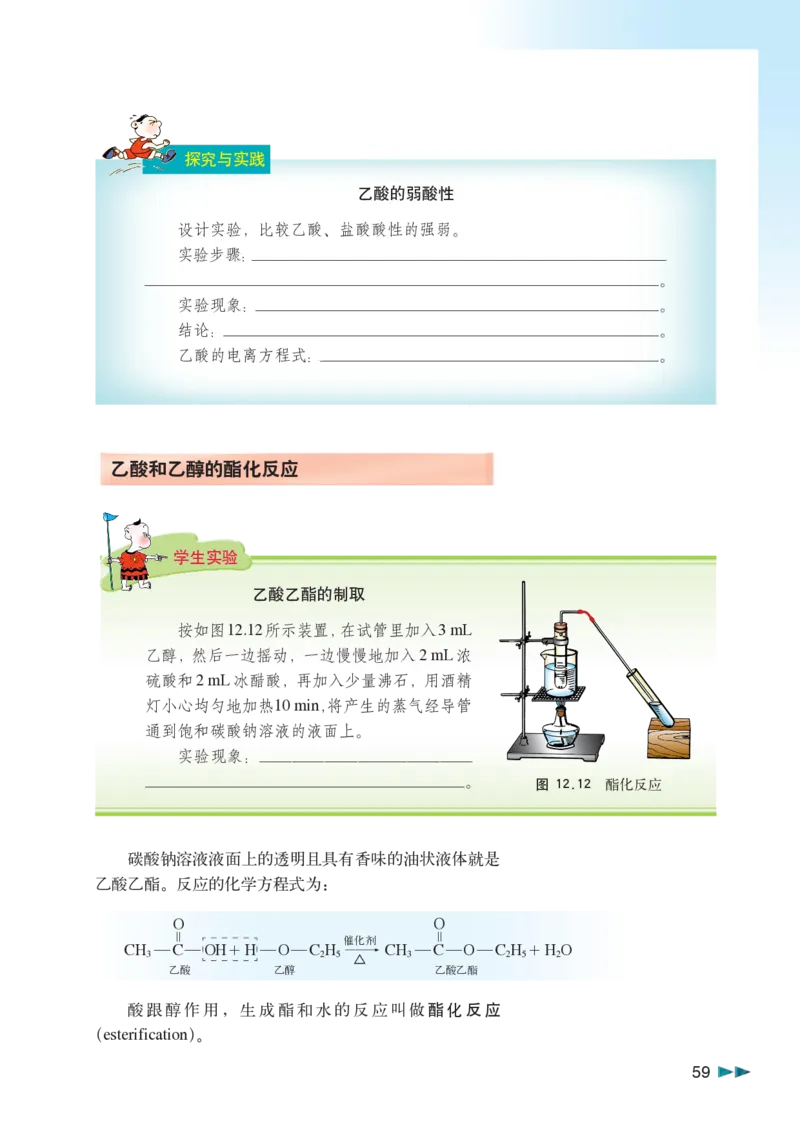
交通民警如何判断驾驶员是否酒后驾车呢?
用酒精分析器吸收驾驶员呼出的气体,可
以测定驾驶员体内的乙醇含量。酒精分析器里
的试剂是吸收了硫酸和三氧化铬(CrO )的硅
3
胶,颜色呈黄色。人饮酒后,酒精经血液流到肺
里,因而人呼出的气体含有酒精分子,酒精与试
剂发生氧化还原反应。CrO 还原为Cr (SO ) ,颜
3 2 4 3
色呈蓝绿色,乙醇氧化为乙醛。根据硅胶的颜色
图 12.6 用酒精分析器
变化,能判断驾驶员是否饮过酒及饮酒量的多
检测驾驶员体内乙醇含量
少。该反应的化学方程式为:
2CrO + 3C H OH + 3H SO Cr (SO ) + 3CH CHO + 6H O
3 2 5 2 4 2 4 3 3 2
黄色 蓝绿色
54乙醇的工业制法
古时候,人们将淀粉、糖蜜等物质进行发酵来制酒。含
淀粉的高粱、玉米、薯类等粮食作物发酵后,再进行蒸馏,
可制得95%的乙醇。目前,发酵法制取乙醇仍是一种重要
的方法。
随着石油化工的发展,用乙烯为原料来生产乙醇的方
法得到广泛的应用。
乙烯在加热、加压和催化剂存在的条件下,跟水反应生
成乙醇。用这种方法制取乙醇叫做乙烯水化法。 乙醇
中草药
思考与练习
1. 人们常把中草药浸泡在酒精中来制取药酒,这是利用
乙醇的什么性质?
2. 写出乙烯水化反应的化学方程式:
_______________________。 图 12.7 乙醇萃取中草药
乙醇燃料
乙醇汽油
乙酸
1.怎样用石油裂解气
为原料来制取乙醇?
2.查阅资料,列举乙
玉米
山芋 乙醚 醇的重要用途。
图 12.8 制取乙醇的原料和乙醇的用途
55拓展视野
固体酒精和一些醇类化合物
固体酒精易点燃,火焰温度均匀,携带方
便。它适合于宾馆、酒店、家庭及其他餐饮业
使用,也是旅游、地质考察等野外作业者加热
食品的理想热源。
制作固体酒精的配方很多,主要原料是
95%的酒精、石蜡、硬脂酸等。
除乙醇外,还有一些在结构和性质上与
图 12.9 固体酒精
乙醇很相似的物质,如甲醇(methanol)。甲
醇有毒,饮用后,使人失明,甚至死亡。工业酒精中往往掺入甲醇,所以,
不能用工业酒精作为原料来生产饮用酒。
含有两个及两个以上羟基的醇叫做多元醇,如乙二醇(glycol)和丙三
醇(glycerol)。它们的结构式可以表示如下:
CH —OH
2
CH —OH
2 CH—OH
CH —OH
2 CH —OH
2
乙二醇 丙三醇
乙二醇易溶于水和乙醇,60%的乙二醇的凝固点是-49 ℃,常用作内
燃机的抗冻剂。
丙三醇俗称甘油,用途很广,常用来制造硝化甘油、防冻剂、润滑剂和
甜味剂等。
【资料库】
羟基跟苯环直接相连的化合物叫做酚,苯
酚的结构简式为 —OH。
56[思考与复习12.1]
1. 写出下列反应的化学方程式,并指出反应条件和反应类型。
C H O
6 12 6
C H C H OH C H OC H
2 4 2 5 2 5 2 5
2. 下列物质中,属于醇类的是 ( )。
(A) CH OH (B) CH —O—CH (C) CH CHO (D) CH —C—OH
3 3 3 3 3
=
O
3. 下列物质中可用来检验酒精中是否含有水分的是 ( )。
(A) 生石灰 (B) 石灰石 (C) 无水硫酸铜 (D) 无水氯化钙
4. 下列关于乙醇的用途中,错误的是 ( )。
(A) 配消毒剂 (B) 制药酒 (C) 作燃料 (D) 作麻醉剂
5. 下列燃料中,作为二次能源且不污染大气的是 ( )。
(A) 石油 (B) 煤 (C) 天然气 (D) 乙醇
6. 某炼油厂每天制得乙烯6.72×103 m3 (标准状况),用乙烯来制乙醇,理论上可
制得95%的酒精多少吨?
7. 某有机物2.3 g完全燃烧后,生成4.4 g二氧化碳和2.7 g水,测得该有机物的蒸
气的密度为2.054 g/L (标准状况),求该有机物的分子式。
57醋和酒香
12
.2
(VINEGAR AND SCENT OF WINE)
酒的氧化产物——乙酸
酒中含有某些金属离子,这些离子能起催化作用,使
想一想
乙醇跟空气中的氧气发生缓慢氧化反应而生成乙醛,乙醛
酒以香醇为上品, 进一步氧化成乙酸(acetic acid),乙酸与乙醇反应生成少量
为什么酒存放得越久,
具有香味的乙酸乙酯(ethyl acetate)。
香味越浓?
乙酸是重要的有机酸,乙酸的分子式是C H O ,结构
2 4 2
O
=
简式为CH —C—OH,简写为CH COOH。乙酸分子中的
3 3
O
=
官能团—C—OH(或—COOH)叫做羧基(carboxyl)。
乙酸是具有强烈刺激性气味的无色液体。当温度低于
16.6 ℃时,乙酸凝结成冰状晶体,所以无水乙酸又称冰醋
酸。乙酸易溶于水和乙醇。我们日常生活中作为调味品的
食醋含有3%~5%的乙酸。
【资料库】
乙酸
沸点 117.9 ℃
熔点 16.6 ℃
图 12.10 食醋 图 12.11 乙酸分子的比例模型
58探究与实践
乙酸的弱酸性
设计实验,比较乙酸、盐酸酸性的强弱。
实验步骤:__________________________
________________________________。
实验现象:_________________________。
结论:___________________________。
乙酸的电离方程式:_____________________。
乙酸和乙醇的酯化反应
学生实验
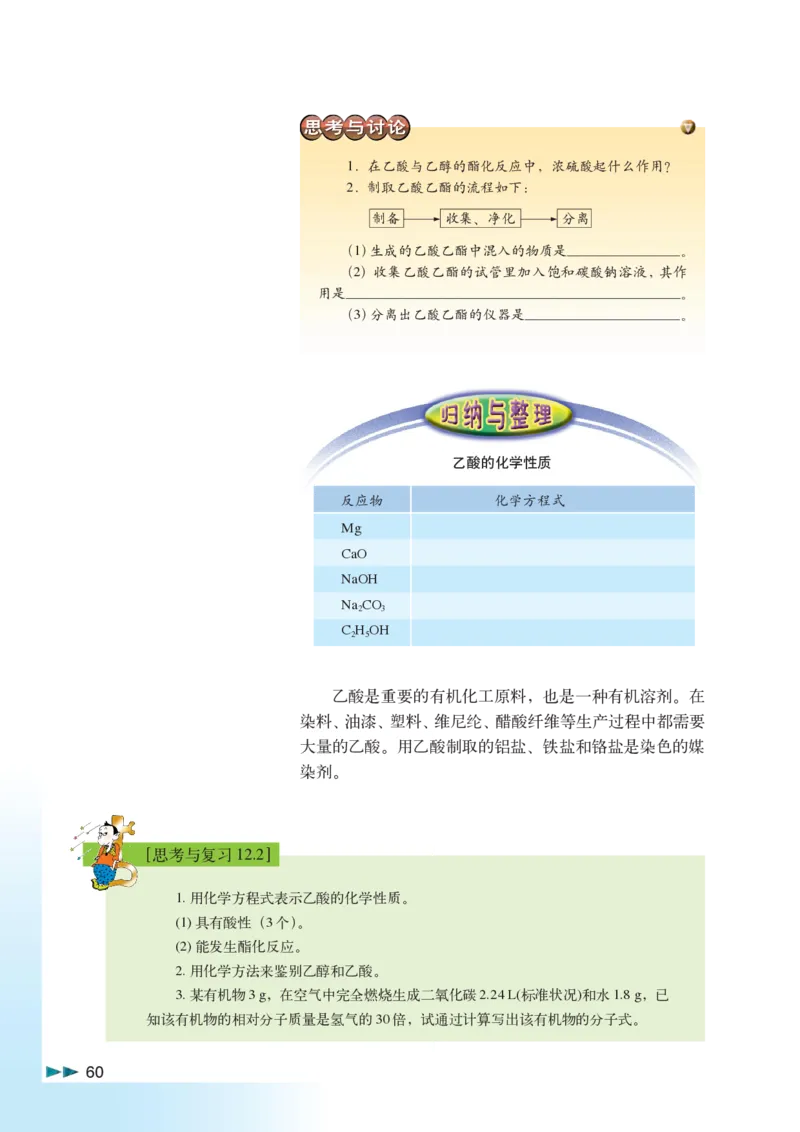
乙酸乙酯的制取
按如图12.12所示装置,在试管里加入3 mL
乙醇,然后一边摇动,一边慢慢地加入2 mL浓
硫酸和2 mL冰醋酸,再加入少量沸石,用酒精
灯小心均匀地加热10 min,将产生的蒸气经导管
通到饱和碳酸钠溶液的液面上。
实验现象:_____________
____________________。
图 12.12 酯化反应
碳酸钠溶液液面上的透明且具有香味的油状液体就是
乙酸乙酯。反应的化学方程式为:
O O
= =
催化剂
CH —C—OH + H—O—C H CH —C—O—C H + H O
3 2 5 3 2 5 2
乙酸 乙醇 乙酸乙酯
酸跟醇作用,生成酯和水的反应叫做酯化反应
(esterification)。
591.在乙酸与乙醇的酯化反应中,浓硫酸起什么作用?
2.制取乙酸乙酯的流程如下:
制备 收集、净化 分离
(1)生成的乙酸乙酯中混入的物质是________。
(2) 收集乙酸乙酯的试管里加入饱和碳酸钠溶液, 其作
用是________________________。
(3)分离出乙酸乙酯的仪器是___________。
乙酸的化学性质
反应物 化学方程式
Mg
CaO
NaOH
Na CO
2 3
C H OH
2 5
乙酸是重要的有机化工原料,也是一种有机溶剂。在
染料、油漆、塑料、维尼纶、醋酸纤维等生产过程中都需要
大量的乙酸。用乙酸制取的铝盐、铁盐和铬盐是染色的媒
染剂。
[思考与复习12.2]
1. 用化学方程式表示乙酸的化学性质。
(1) 具有酸性(3个)。
(2) 能发生酯化反应。
2. 用化学方法来鉴别乙醇和乙酸。
3. 某有机物3 g,在空气中完全燃烧生成二氧化碳2.24 L(标准状况)和水1.8 g,已
知该有机物的相对分子质量是氢气的30倍,试通过计算写出该有机物的分子式。
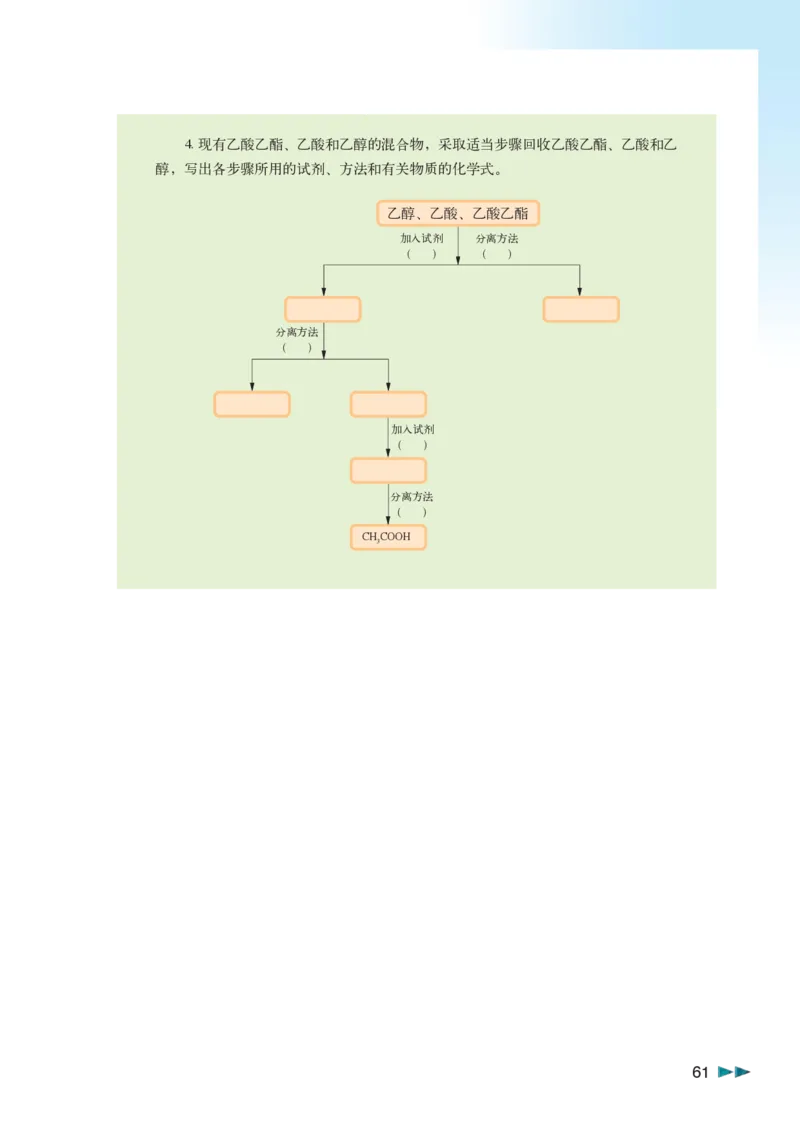
604. 现有乙酸乙酯、乙酸和乙醇的混合物,采取适当步骤回收乙酸乙酯、乙酸和乙
醇,写出各步骤所用的试剂、方法和有关物质的化学式。
乙醇、乙酸、乙酸乙酯
加入试剂 分离方法
( ) ( )
分离方法
( )
加入试剂
( )
分离方法
( )
CHCOOH
3
61家庭装潢说甲醛
12
.3
(DISCUSS FORMALDEHYDE FROM DECORATION OF HOUSE)
近年来,室内装修引发污染的事件越来越多。某些新
甲醛 装修的居室内散发出刺激性的气味,使人流泪,鼻腔和喉
咙感到不适,严重时引起中毒,其主要原因是使用了不合
格的建筑材料。例如,中密度板和胶合板在生产中使用酚
醛树脂作为黏合剂,如果黏合剂的质量和使用不符合标准,
这些板材会在室内持续释放出甲醛,当遇热和潮解时释放
量更大。
图 12.13 胶合板释放出甲醛
表12.1 不同浓度甲醛对人体的影响
甲醛的质量分数(1×10-6) 健康效应
0.05~1.0 嗅觉刺激
神经生理效应
0.05~1.5
(脑电图改变,光反应)
0.01~2.0 眼刺激
0.10~25 上呼吸道刺激
5.0~30 下呼吸道和肺部作用
50~100 肺水肿、炎症、肺炎
>100 死亡
62拓展视野
谨防服装引起的甲醛污染
甲醛
纯棉服装颇受人们的青睐,但纯棉服装易
起皱,洗涤后须熨烫。因此,纯棉免烫服装应
运而生。但是,免烫工艺应用不当,会造成服
装的甲醛超标,引起甲醛污染。因此,在选择
纯棉免烫衣服时要注意其中的甲醛含量。 图 12.14 服装制品
甲醛的结构和性质 【资料库】
甲醛
甲醛(methanal)又叫蚁醛(formaldehyde),是一种无
沸点 - 21 ℃
色、具有强烈刺激性气味的气体,易溶于水,浓度约为40%
熔点 - 92 ℃
的甲醛水溶液叫做福尔马林(formalin)。
O
=
甲醛的分子式是CH O,它的结构式是H—C—H,简
2
写为HCHO。
O
=
甲醛分子中的醛基(—C—H,aldehyde group)官能
团对甲醛的主要化学性质起决定作用。
图 12.15 甲醛分子的
比例模型
课堂实验
甲醛的氧化
在洁净的试管里加入1 mL 2%的硝酸银溶液,
然后,一边摇动试管,一边逐渐滴入2%的稀氨水,
直到最初产生的沉淀恰好溶解为止(得到的溶液
叫做银氨溶液)。再加入3滴甲醛溶液,振荡后把
试管放在热水浴里温热。
实验现象:______________
_____________________。
图 12.16 银镜反应
63反应中甲醛被氧化成甲酸,银离子被还原成金属银附
在试管的内壁上,形成银镜,所以这个反应叫做银镜反应。
银镜反应是检验有机物中是否含有醛基的常用方法
之一。
课堂实验
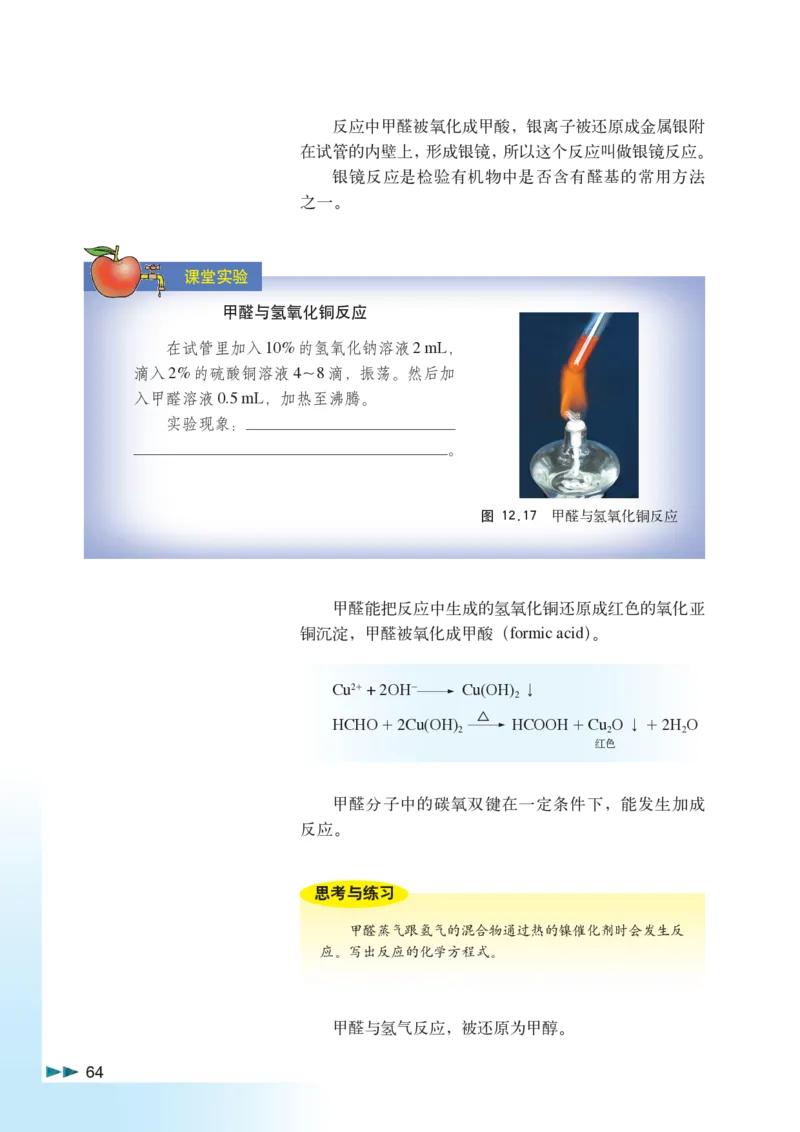
甲醛与氢氧化铜反应
在试管里加入10%的氢氧化钠溶液2 mL,
滴入2%的硫酸铜溶液4~8滴,振荡。然后加
入甲醛溶液0.5 mL,加热至沸腾。
实验现象:_____________
____________________。
图 12.17 甲醛与氢氧化铜反应
甲醛能把反应中生成的氢氧化铜还原成红色的氧化亚
铜沉淀,甲醛被氧化成甲酸(formic acid)。
Cu2+ + 2OH- Cu(OH) ↓
2
HCHO + 2Cu(OH) HCOOH + Cu O↓ + 2H O
2 2 2
红色
甲醛分子中的碳氧双键在一定条件下,能发生加成
反应。
思考与练习
甲醛蒸气跟氢气的混合物通过热的镍催化剂时会发生反
应。写出反应的化学方程式。
甲醛与氢气反应,被还原为甲醇。
64用途广泛的甲醛
甲醛是一种重要的有机原料,应用于塑料工业 (如制酚
醛树脂、聚甲醛等)、合成纤维工业、制革工业等。甲醛的
水溶液具有杀菌和防腐能力,是一种良好的杀菌剂。福尔
马林常用来浸制生物标本。0.1%~0.5%稀甲醛溶液用于浸
种,给种子消毒。
在生产和生活中要提高环境保护的意识,防止甲醛污
染。在以甲醛为原料的生产过程中要严格检测产品的甲醛
含量,凡是甲醛浓度超标的建筑材料和服装不能进入市
场;禁止生产含甲醛的食品,以免危害人体健康。
图 12.18 福尔马林浸制生物
标本
拓展视野
禁用含甲醛的食品
甲醛是有机化工原料,但某些人为了追求暴利,把含有甲醛的化学物质
作漂白剂,用在快餐面、牛百叶、粉丝、腐竹等加工中。
含甲醛的漂白剂不仅破坏食物的营养成分,而且会引起过敏,刺激肠
道,使肝、肾受损,严重时将危及生命。
除甲醛外,还有一些在分子结构和化学性质上都跟甲
醛相似的物质,如乙醛(C H O,acetaldehyde),乙醛的结
2 4 思考与练习
H O O
= = 写出下列反应的化学
构式是H—C—C—H , 简写为CH —C—H。 方程式(注明反应条件)。
3
1. 乙醇氧化为乙醛。
H
2. 乙醛还原为乙醇。
乙醛是一种无色、具有刺激性气味的液体,密度比水 3. 乙醛与新制的氢氧
小,沸点是20.8 ℃。乙醛易挥发,易燃烧,能跟水、乙醇、 化铜反应。
乙醚、氯仿等互溶。
乙醛分子中的碳氧双键能够发生加成反应,在加热和
催化剂镍的存在下,与氢气发生加成反应,乙醛被还原为
乙醇。
乙醛还能够被弱氧化剂如银氨溶液或新制氢氧化铜氧
化为乙酸。
65学生实验
乙醛的氧化反应
1. 乙醛与新制的氢氧化铜反应。
在试管里加入10%氢氧化钠溶液2 mL,滴入2%硫酸铜溶液4~8滴,
振荡。然后加入乙醛溶液0.5 mL,加热到沸腾。
实验现象:_________________________。
2. 乙醛的银镜反应。
在洁净的试管里加入1 mL 2%的硝酸银溶液,然后一边摇动试管,一
边逐渐滴入2%的稀氨水,直到最初产生的沉淀恰好溶解为止(得到银氨溶
液)。然后再加入3滴乙醛溶液,振荡后,把试管放在热水浴里温热。
实验现象:_________________________。
[思考与复习12.3]
1. 下列物质中,属于纯净物的是( )。
(A) 福尔马林 (B) 消毒酒精
(C) 固体酒精 (D) 冰醋酸
2. 下列各组混合物中,不能互溶的是( )。
(A) 乙醇和碘水 (B) 乙醇和乙酸
(C) 甲醛和水 (D) 苯和水
3. 下列各组物质中,化学组成相同的是( )。
(A) 福尔马林、甲醛 (B) 固体酒精、乙醇
(C) 冰醋酸、乙酸 (D) 食醋、乙酸
4. 下列物质中,不能用于食品加工的是( )。
(A) 甲醛 (B) 乙醇 (C) 乙酸 (D) 纯碱
5. 下列过程属于氧化反应的是( )。
(A) 乙醇 乙醚 (B) 甲醛 甲醇
(C) 甲醛 甲酸 (D) 乙酸 乙酸乙酯
6. 试鉴别乙醇、乙酸和甲醛三种溶液。
7. 某有机物含氢6.67%,含碳40%,含氧53.33%,该有机物的蒸气的密度为
1.34 g/L (标准状况),试推测该有机物的分子式。
668. 阅读短文:
Ethanol, or ethyl alcohol is the alcohol associated with“ alcoholic” beverages. It has been
made for at least 6 000 years by the addition of yeast to solutions that are rich in either sugars
or starches. The yeast cells obtain energy from enzyme-catalyzed reactions that convert these
sugars or starches to ethanol and CO .
2
C H O (aq) 2CH CH OH(aq) + 2CO (g)
6 12 6 3 2 2
When the alcohol reaches a concentration of 10 to 12% by volume, the yeast cells die.
Brandy, rum, gin, and the various whiskeys that have a higher concentration of alcohol are
prepared by distillation of the alcohol produced by the fermentation reaction just described.
Ethanol is not as toxic as methanol, but it is still dangerous. Blood alcohol levels of 1.5 to
3 grams per liter result in intoxication, and levels of 4 to 6 grams per liter can lead to coma or
death. The breath analyzer used to detect drunken drivers operates on the basis of the fact that
persons who have been drinking exhale some alcohol when they breathe. The alcohol in the
breath is collected and allowed to react with the dichromate (Cr O2-) ion in acid solution.
2 7
3CHCHOH(aq) + 2CrO2-(aq) + 16H+(aq) 3CHCOOH(aq) + 4Cr3+(aq) + 11HO(l)
3 2 2 7 3 2
The Cr O2-ion is orange and the Cr3+ion is green, so the extent of this reaction can be
2 7
followed by monitoring the color of the solution.
Ethanol is oxidized to CO and HO by alcohol dehydrogenase enzymes in the body. This
2 2
reaction gives off 30 kilojoules of energy per gram, which makes ethanol a better source of
energy than carbohydrates(17 kJ/g) and almost as good a source of energy as fat (38 kJ/g). An
ounce of 80-proof liquor can provide as much as 3% of the average daily caloric intake, and
drinking alcohol can contribute to obesity. Many alcoholics are malnourished, however,
because of the lack of vitamins in the calories they obtain from alcoholic beverages.
67小 结 与 思 考
1. 乙醇的分子结构特点和性质。
(1) 乙醇的分子式为C H O,结构简式为CH —CH —OH,乙醇分子可以看作乙烷分
2 6 3 2
子里的氢原子被羟基 (—OH) 取代的产物。乙醇分子的官能团是羟基。
(2) 乙醇与浓硫酸共热到170 ℃,生成乙烯;乙醇与浓硫酸共热到140 ℃,生成乙醚。
(3) 乙醇在催化剂存在和加热条件下,氧化成乙醛。
(4) 乙醇跟乙酸与浓硫酸共热生成乙酸乙酯。
2. 乙醇的工业制法。
工业上可用粮食为原料,在酶催化作用下,淀粉水解生成葡萄糖,葡萄糖在酶催化作用
下生成乙醇。
工业上,用石油裂解气乙烯为原料,在催化剂作用下与水发生加成反应,生成乙醇。
3. 乙醇的用途。
乙醇是清洁的能源,目前世界上很多国家大力推广使用乙醇燃料。乙醇用于配制消毒酒
精。工业上用乙醇作溶剂,配制多种试剂。
4. 乙酸的分子结构特点和性质。
O
=
(1) 乙酸的分子式为C H O ,结构简式为CH —C—OH,乙酸分子可以看作甲烷分子
2 4 2 3
O
=
里的氢原子被羧基 (—C—OH) 取代的产物。乙酸的官能团是羧基。
(2) 乙酸是弱酸,具有酸的通性,能分别与金属、金属氧化物、碱、盐反应。
(3) 乙酸跟醇能发生酯化反应生成酯。
5. 乙酸的用途。
乙酸是重要的有机化工原料,用于染料、油漆、塑料、合成纤维等化工生产,乙酸可用
来制取铝盐、铁盐等媒染剂。
6. 甲醛的分子结构特点和性质。
O O
= =
(1) 甲醛的分子式为CH O,结构式为H—C—H,官能团是醛基 (—C—H)。
2
(2) 甲醛与硝酸银的氨溶液混合后加热,被氧化为甲酸并析出银,该反应又叫银镜反应。
甲醛与新制的氢氧化铜混合后加热,被氧化为甲酸并生成红色的氧化亚铜。
(3) 甲醛跟氢气混合,在催化剂存在下加热被还原为甲醇。
7. 甲醛的用途。
浓度约为40%的甲醛水溶液又叫福尔马林,可用来浸制标本。甲醛可用于塑料、黏合
剂、服装、合成纤维等工业生产。甲醛有毒,在生产和生活中要防治甲醛污染。
8. 几种有机反应的类型。
(1) 消去反应。
有机化合物在适当条件下,从一个分子内脱去一个小分子而生成不饱和(双键或叁键)化
68合物的反应,叫做消去反应。
(2) 酯化反应。
酸与醇作用,生成酯和水的反应,叫做酯化反应。
(3) 氧化反应。
乙醇分子中脱去两个氢原子,氧化成乙醛。甲醛分子中得到一个氧原子,被氧化成甲酸。
(4) 还原反应。
甲醛与氢气反应生成甲醇是还原反应。
9. 禁止用工业酒精配制饮用酒,这是因为工业酒精中常含有少量可使人中毒的 ( )。
(A) 甲醇 (B) 乙酸 (C) 甲醛 (D) 丙三醇
10. 下列物质中,不能从溴水中萃取溴的是 ( )。
(A) 四氯化碳 (B) 酒精 (C) 苯 (D) 汽油
11. 23 g乙醇完全燃烧,需要空气的体积 (标准状况) 是 ( )。
(A) 33.6 L (B) 67.2 L (C) 160 L (D) 320 L
12. 下列关于乙酸的叙述中,不正确的是 ( )。
(A) 乙酸易溶于水和乙醇
(B) 乙酸是具有强烈刺激性气味的液体
(C) 无水乙酸又称冰醋酸,是纯净物
(D) 乙酸分子式是C H O ,有4个氢原子,不是一元酸
2 4 2
13. 下列说法中,不正确的是 ( )。
(A) 乙醇脱水生成乙醚是消去反应
(B) 甲醛与银氨溶液反应被氧化为甲酸
(C) 甲醛与氢气的反应是还原反应
(D) 乙醇脱水生成乙烯是消去反应
14. 鉴别乙酸、甲醛不能选用的试剂是 ( )。
(A) 银氨溶液 (B) 新制的氢氧化铜
(C) 碳酸钠溶液 (D) 氢氧化钠溶液
15. 除去乙酸乙酯中少量的乙酸可选用的试剂是 ( )。
(A) 饱和碳酸钠溶液 (B) 水 (C) 氢氧化钠溶液 (D) 浓硫酸
16. 下列关于甲醛的用途中,错误的是 ( )。
(A) 制黏合剂 (B) 合成塑料 (C) 制防腐剂 (D) 漂白食品
17. 在下表各空格中填上由相应的基团或官能团所构成的物质的名称:
O O
基团或官能团 = =
—C—H —C—OH
—CH
3
—OH
6918. A是石油化工的原料,C是食醋的重要成分。在一定条件下,它们的衍变关系如下:
加水 氧化
A B C
浓硫酸
D
试写出:
(1) B的结构简式___________________。
(2) A→B的化学方程式___________________,反应类型_____________。
(3) 生成D的化学方程式___________________,D的名称_____________。
19. 某有机物1.2 g完全燃烧生成0.896 L二氧化碳(标准状况)和0.72 g水,其蒸气的密
度为2.679 g/L(标准状况),推测该有机物的分子式。
7013
检验一些无机化合物
IDENTIFY SOME INORGANIC COMPOUNDS
◆ 溶液中阴、阳离子的检验
◆ 混合溶液中离子的鉴定
◆ 固体混合物的成分分析
71检
验未知物质(单一或混合)的成分是化学
分析的重要内容。化合物是否纯净需要检
验;混合物中包含哪些物质需要检验;生产
的材料是否合格需要检验;饮用水是否符合标准需要检
验……科学研究、工业生产、社会生活的许多方面都要
用到检验。因此,物质的检验不仅具有重要的科学意义
而且还有重要的应用价值。
通过对一些无机物的检验,了解检验方法;学会根
据检验要求设计实验步骤,并根据实验现象进行推论。
这样,可以对物质的检验有一个初步的了解,并学会简
单的检验操作。
72离子的检验
13
.1
(IDENTIFICATION OF IONS)
物质的检验包括鉴定和鉴别。
物质的鉴定是确定一种物质的成分或确定混合物中的
各种成分。将两种或两种以上的物质一一区分开来是物质
的鉴别。
无机物酸、碱、盐类的鉴定反应,基本上都是溶液中的
离子反应。如果待测物是固体,一般先要把它配制成溶液,
然后鉴定其中的离子。
我们已学过某些阴、阳离子的检验,本节将进行归
纳,并进一步学习某种物质的鉴定、几种物质的鉴别等。
溶液中阴、阳离子的检验
用于检验的化学反应,一般应条件温和(如常温或稍
加热),操作简便,并具有明显的反应现象(如颜色变化、
沉淀的生成或溶解、生成气体等)。
请在下列空白处填写实验现象或化学式,并指出氯离
子和硫酸根离子的检验方法。
Cl- ____
氯化钡溶液
SO2- ____ (__色) _______
4
稀盐酸
CO2- ____ (__色) _______
3
73SO2- ____ (__色) _______
4
硝酸银溶液 稀硝酸
Cl- ____ (__色) _______
CO2- ____ (__色) _______
3
Cl-的检验方法:______________。
SO2-的检验方法:______________。
4
1.在检验硫酸根离
子和氯离子时能否先加
酸再加氯化钡溶液或硝 检验溶液中的阳离子,除部分金属离子可用焰色反应
酸银溶液?
外,一般采用滴加氢氧化钠溶液的方法,很多金属阳离子
2.为什么以上实验
能与氢氧根离子生成不同颜色和性质的氢氧化物沉淀;溶
过程还不能检验碳酸根
液中若有铵根离子,加热时会有氨气产生。
离子?怎样检验碳酸根
离子? 请在以下空白处填上实验现象或化学式。
NH+ ___ (有____气味,能使湿润的红色石蕊试纸____)
4
Mg2+ ___ (__色)
氢氧化钠溶液
Al3+ ___ (__色,加过量氢氧化钠溶液___,加氨水___)
Fe3+ ___ (__色)
Cu2+ ___ (__色)
NH+的检验方法:_______________。
4
Fe3+的检验方法:_______________。
物质的鉴定
一般无机盐类的鉴定,是通过某些反应检验出该物质
中的阴离子和阳离子,从而确定该物质的组成。
检验物质时,一般要先观察试样(待检验的物质样品)
的外表,观察它的颜色、状态、挥发性(嗅闻气味)等。如
果试样是白色固体或无色溶液,则可排除一些有色离子存
在的可能。
如果试样是固体,一般先检验它是易溶还是难溶,再
把它们配制成溶液。然后,移取少量配制好的溶液,检验其
中含有哪些阴、阳离子。
74拓展视野
物质的“酸溶”
某些不溶于水而能溶于酸的盐类,可用“酸溶”来配成溶液,取“酸溶”
后的溶液来检验其中的阳离子。有时,“酸溶”也是检验阴离子的过程。例
如,用盐酸溶解硫化亚铁时有腐卵气味的硫化氢产生,证明含有硫离子。
课堂实验
鉴定某种化肥的主要成分是硫酸铵
1. 观察试样。描述试样外观性状:_______________。
2. 溶解性试验: 在小烧杯中加入约10 mL蒸馏水,逐步加入约2 g试
样,不断搅拌,观察现象。
3. 在试管中加入少量试样溶液,逐滴加入氯化钡溶液,再滴加盐酸,观
察现象。
4. 另取少量试样溶液,加入氢氧化钠溶液,用酒精灯加热,将湿润的红
色石蕊试纸放在试管口,观察现象。
结论:____________________________。
学生实验
氯化铁的鉴定
要求: 写出实验步骤、实验操作后,作出结论。完成实验报告。
实验步骤 实验现象 解释和结论
结论:_________________________。
75多种物质的鉴别
物质的鉴别是把几种物质区分开来。过程是首先分析
被鉴别物质的性质差异,选定某种物理方法或化学方法,然
后进行实验操作,最后依据实验现象的不同,确定它们各
是什么物质。
鉴别时,通常将未知试样加以编号,如①号试样、②号
试样……以免混淆。有多种方法可选用时,一般应选用操
作简单、现象明显、实验次数较少的方法。如果试样是溶
液,则可先鉴别溶液的酸、碱性。对于多种未知试样,第1
次实验尽可能将它们分为两组,再分别对各组试样进行第
2、3次实验。
无机物如酸、碱、盐等物质的鉴别通常采用离子检验
的化学方法。
课堂实验
离子溶液的鉴别
现有四瓶溶液,它们是硫酸钠、氯化钾、碳酸钠和氯化铵。试设计实验
步骤,并用实验将它们一一区分开来。
设计提示: 这四瓶溶液均呈无色透明,不能用物理方法加以区分,可以
用它们所含的阳离子或阴离子特性反应将它们区分开来。
这四种溶液中各含有SO2-、Cl-和CO2-等离子,若在四种溶液中加入氯
4 3
化钡溶液(或硝酸钡溶液),有两种产生沉淀,另两种没有沉淀而分为两组。
在有沉淀产生的溶液中继续加入盐酸(或硝酸),沉淀溶解的是碳酸钠,沉淀
不溶解的是硫酸钠。另两种没有沉淀的,另取试样,可用阳离子的特性反应
来区分。
另外,利用这四种溶液的酸碱性可以区分出氯化铵(酸性)和碳酸钠(碱
性),中性的硫酸钠、氯化钾溶液,可以用氯化钡溶液加以区分。
实验步骤 实验现象 解释和结论
1. 分别给四种试样加以编号
2.
3.
76学生实验
几种化肥的鉴别
课题:农业生产中常用的化肥有氯化铵、硫酸铵、硝酸铵和碳酸氢铵,
它们都是白色固体,试通过实验把它们一一区别开来。
要求:设计实验步骤,进行实验操作,根据现象作出结论。完成实验
报告。
思考:它们的阳离子全部都是铵离子,是否要检验铵离子的存在?
实验步骤 实验现象 分析和结论
1. 将白色粉末编号后,
各取少量用蒸馏水分别
配制成20~30 mL待测
液,写上相应编号
2.
[思考与复习13.1]
1.以下有关溶液所含离子鉴定的操作中,所得结论是否正确?若不正确,说明理
由,并加以改正。
(1)滴加硝酸银溶液产生白色沉淀,说明溶液中一定存在Cl-。
(2)滴加盐酸产生气体,说明溶液中一定存在CO2-。
3
(3)先滴加盐酸,再滴加氯化钡溶液,产生白色沉淀,说明溶液中一定存在SO2-。
4
(4)滴加氢氧化钠溶液,无刺激性气体产生,说明溶液中不存在NH+。
4
2.在酸性溶液中,下列各组离子能大量共存的是( )。
(A)Ca2+、Na+、CO2-、SO2- (B)NH+、Fe3+、Cl-、NO-
3 4 4 3
(C)Na+、Ag+、Cl-、NO- (D)NH+、Na+、OH-、SO2-
3 4 4
773.以下离子方程式中,错误的是( )。
(A)氢氧化镁跟硫酸 Mg(OH) + 2H+ Mg2+ + 2H O
2 2
(B)碳酸钙跟盐酸 CO2- + 2H+ CO ↑+ H O
3 2 2
(C)溴化钾跟氯水 2Br- + Cl Br + 2Cl-
2 2
(D)硝酸银跟盐酸 Ag+ + Cl- AgCl↓
4. 鉴定某种白色固体是纯碱(Na CO ·10H O),写出鉴定的化学原理、现象和
2 3 2
结论。
提示: 要分别检验钠离子、碳酸根离子和结晶水。
5. 鉴别三种无色溶液,它们分别是硫酸铵、氯化钠和碳酸钾。某学生设计了方案
一,试根据实验现象写出结论。请再设计方案二,并完成于实验报告中。
实验步骤 实验现象 解释和结论
(1)在三支试管中加入编 ①号: 产生气泡, ①号溶液是 ______,
号后的三种溶液,各滴加 ②、③号: 无现象变化 有关离子方程式:____
方 少量盐酸 ____________
案
一 (2)在②、③号试管中再 ②号: 有白色沉淀生成, ②号溶液是 ______,
滴加氯化钡溶液 ③号: 无现象变化 ③号溶液是 ______,
有关离子方程式: ____
____________
方
案
二
6. 怎样用一种试剂鉴别硝酸铵、硫酸钠、硝酸钠和硫酸铵四种溶液,写出试剂名
称、产生的现象和结论。
提示: 注意限定只能使用一种试剂;选择的试剂既要能和阴离子反应,又要能和
阳离子反应,这两者应有明显的差异。
78混合物的检验
13
.2
(IDENTIFICATION OF MIXTURE)
在实际工作中,我们经常需要确定某种混合物(溶液
或固体)的成分。
我们已经学习了NH+、Cl-、SO2-、CO2-等离子的鉴定
4 4 3
和鉴别,也知道了无机物(如酸、碱、盐)的检验主要是所
含离子的检验。那么,如何用实验方法检验出混合物中各
物质所含的离子,推断出混合物的成分?
混合溶液中离子的检出
一种澄清透明的溶液中,可能含有下列离子:Al3+、
NH+、SO2-、CO2-、Cl-。某学生设计了如下的实验方案,试
4 4 3
根据以下实验现象,推断该溶液中存在什么离子,不存在
什么离子,不能确定存在什么离子。
实验步骤和现象:
1.将溶液滴在蓝色石蕊试纸上,试纸呈红色。
2.取少量溶液,用稀硝酸酸化后,滴加氯化钡溶液,
产生白色沉淀,滴加氯化钡至不再沉淀为止。
3.将上一步中的溶液(有沉淀)静置,取上层澄清液
体,加入硝酸银溶液,产生白色沉淀。
4.另取试样,逐滴加入氢氧化钠溶液至过量,先生成
白色沉淀,而后沉淀全部溶解。
根据实验现象进行推断,要灵活应用肯定和排除两种
方法。推论过程如下:
根据步骤1的现象,证明溶液有酸性,可排除CO2-;
3
79根据步骤2的现象,可证明存在SO2-;根据步骤3的现象,
4
虽有白色溶液却不能肯定存在Cl-,因为步骤2中加入氯化
钡溶液,带进了Cl-;根据步骤4的现象,证明溶液中有Al3+。
实验没有对NH+进行直接的检验,又没有否定NH+的理由,
4 4
所以NH+不能确定是否存在。
4
结论:
溶液中存在SO2-、Al3+;溶液中不存在CO2-;溶液中
4 3
不能确定是否存在Cl-、NH+。
4
要确定溶液中是否存在Cl-和NH+,对上述实验过程要作
4
怎样的改进或再进行怎样的操作?
显然,实验不能确定Cl-和NH+是该实验方案的缺陷。
4
将步骤2加入的BaCl 改为Ba(NO ) 。若步骤3仍有白色沉
2 3 2
淀,则可肯定Cl-的存在,若没有白色沉淀,则Cl-不存在。
在操作步骤4时,嗅闻或稍加热后嗅闻有无刺激性气体,就
能作出对NH+的检验。
4
拓展视野
离子检验时如何排除干扰
在检验某种离子时,其他离子可能会跟加入的鉴定试剂反应,因而观察
不到正确的现象。例如,OH-就会干扰Cl-的检验,因为硝酸银溶液会跟OH-
反应生成黑色氧化银沉淀,观察不到白色氯化银沉淀。为了排除OH-的干
扰,可以先滴加稀硝酸(酸化),中和溶液中的OH-后,再用硝酸银溶液检
验Cl-。
同样,在鉴定SO2-时,先用稀硝酸将溶液酸化,可避免CO2-的干扰。
4 3
80课堂实验
混合溶液中的离子检验
某种未知溶液中可能有K+、NH+、Cl-、H+和SO2-中的三种或四种离
4 4
子,试设计方案,进行实验确定所含的离子。
设计提示: 先测试溶液pH。若溶液中性,可判断不存在H+、NH+,溶
4
液酸化后依次检验SO2-、Cl-。若溶液呈酸性,判断存在H+,可能存在NH+,
4 4
直接检验SO2-、Cl-,另取溶液检验NH+。取原液用焰色反应检验K+。
4 4
实验步骤 实验现象和结论
固体混合物的成分分析
混合物的检验就是确定混合物的组成成分,对于无机
物(如酸、碱、盐)而言,主要是运用离子检验的方法来确
定混合物各组分所含的离子,进而确定组成成分。
探究与实践
分析某固体混合物的成分
有一瓶固体混合物,可能含有硫酸铜、氯化钾、氢氧化钠、碳酸钠和硫
酸铵中的两种,请设计实验步骤,通过实验来确定这两种物质。
分析和设计:
1. 先要分析试样中各可能成分的特性,如硫酸铜溶液呈蓝色、KCl的
焰色反应呈紫色,Na CO 跟酸反应产生气体等,这些均可作为检验的切入
2 3
口。同时注意,试样中各可能成分两两反应的情况。
812. 将试样处理成溶液,有以下三种可能情况:
溶液中有蓝色沉淀。推断:含有CuSO ,NaOH或Na CO 。
4 2 3
再用酸来确定是NaOH还是Na CO 。
2 3
加水 蓝色溶液。推断:含有CuSO ,不含有NaOH、Na CO 。
固体试样 4 2 3
接下去只需检验另一种组分是KCl还是(NH ) SO 。
4 2 4
无色溶液。推断:不含有CuSO 。
4
3. 对无色溶液可作以下检验:
测定pH 若呈碱性,可推断含有NaOH、Na 2 CO 3 中的任一
种或都有;若呈酸性,则含有(NH ) SO 。
4 2 4
滴加HNO
无色澄清溶液 3 若产生气体,推断含有Na CO 等。
2 3
若无沉淀,则不含有(NH ) SO ,继续加
4 2 4
AgNO 检验Cl-;若有沉淀,则含有
滴加HNO 3 、Ba(NO 3 ) 2 3
(NH ) SO ,使SO2- 充分沉淀后,加
4 2 4 4
AgNO 检验Cl-。
3
对澄清溶液三个实验现象的分析,可得出混合物的两种组成。如溶液呈碱性,加
HNO 有气体,又无SO2-、Cl-,则混合物的两种组分是NaOH和Na CO 。
3 4 2 3
本混合物的检验,除以上实验顺序外,还有其他合理的顺序。在实际检验时,因
为只存在两种物质,故往往做到某一步,即能结束实验。
将实验结果记入下表:
实验步骤 实验现象和结论
结论:____________________________。
82混合物检验的实验设计
我们已经学习了几个混合物检验的实例。知道实验设
计,形成合理的检验步骤,是混合物检验的重要内容。现
在归纳如下。
1. 设计前准备。
明确检验的范围和要求,观察试样的外观性状,分析
可能存在的物质或离子的特性,形成检验的大体思路。如
上述“探究与实践”中,先处理成溶液试样,根据溶液试样
的各种情况,对溶液作阴离子检验。
2. 拟定实验方案。
初步试验包括溶解实验和测定溶液的pH等。许多情况
下测定试样溶液的pH能判断所含离子的范围,如溶液呈酸
性,可判断不存在OH-、CO2-,存在H+,可能存在NH+、
3 4
Al3+等。
确定离子检验的顺序。检验某些离子时,其他离子对
它没有干扰则可直接先检验。如Cl-、SO2-、CO2-中可先用
4 3
酸检验CO2-,而Cl-、SO2-不存在干扰。但某些离子之间
3 4
存在相互干扰,如Cl-、SO2-中加入硝酸银溶液产生白色沉
4
淀,由于Ag SO 微溶,而不能肯定Cl-、否定SO2-,必须
2 4 4
先用硝酸钡溶液将SO2-充分沉淀后,取上层清液滴加硝酸
4
银溶液来检验Cl-。
在多步检验中,如第1步所加试剂干扰第2步检验时,
应另取原试样做实验。
3. 实验方案反思和修正。
在实验操作及现象推理过程中,如发现实验步骤或所
加试剂有问题,要及时修正,直至得到检验的结果。
混合物检验是一个极富创造性的工作,一般可以设计
出多种方案,我们要善于比较各种检验方案的合理成分,形
成自己的有个性的方案。
83学生实验
实验推断混合物的成分
课题:有一包白色粉末,可能是由硫酸铝、碳酸钙、氯化钡、硝酸钠中
的两种或三种组成,试通过实验推断这包白色粉末的成分。
要求:设计实验步骤,进行实验操作,根据现象确定这包白色粉末的
成分。
实验步骤 实验现象 分析和结论
结论:白色粉末的成分为___________________。
[思考与复习13.2]
1.某溶液主要含有碳酸钠、氢氧化钠及少量的氯化钠。现分别取样检验下列离子,
请完成以下表格。
离子 选用试剂和方法 实验现象
OH-
Na+
CO2-
3
Cl-
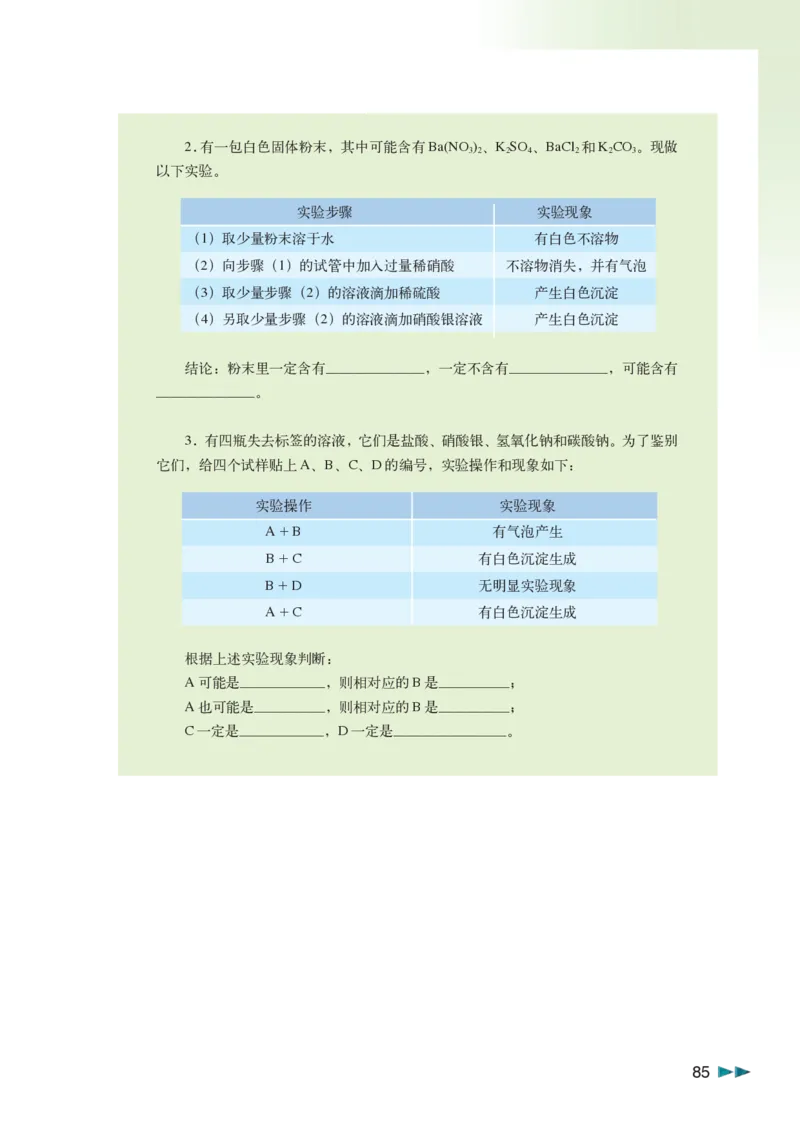
842.有一包白色固体粉末,其中可能含有Ba(NO )、K SO 、BaCl 和K CO 。现做
3 2 2 4 2 2 3
以下实验。
实验步骤 实验现象
(1)取少量粉末溶于水 有白色不溶物
(2)向步骤(1)的试管中加入过量稀硝酸 不溶物消失,并有气泡
(3)取少量步骤(2)的溶液滴加稀硫酸 产生白色沉淀
(4)另取少量步骤(2)的溶液滴加硝酸银溶液 产生白色沉淀
结论:粉末里一定含有_______,一定不含有_______,可能含有
_______。
3.有四瓶失去标签的溶液,它们是盐酸、硝酸银、氢氧化钠和碳酸钠。为了鉴别
它们,给四个试样贴上A、B、C、D的编号,实验操作和现象如下:
实验操作 实验现象
A + B 有气泡产生
B + C 有白色沉淀生成
B + D 无明显实验现象
A + C 有白色沉淀生成
根据上述实验现象判断:
A可能是______,则相对应的B是_____;
A也可能是_____,则相对应的B是_____;
C一定是______,D一定是________。
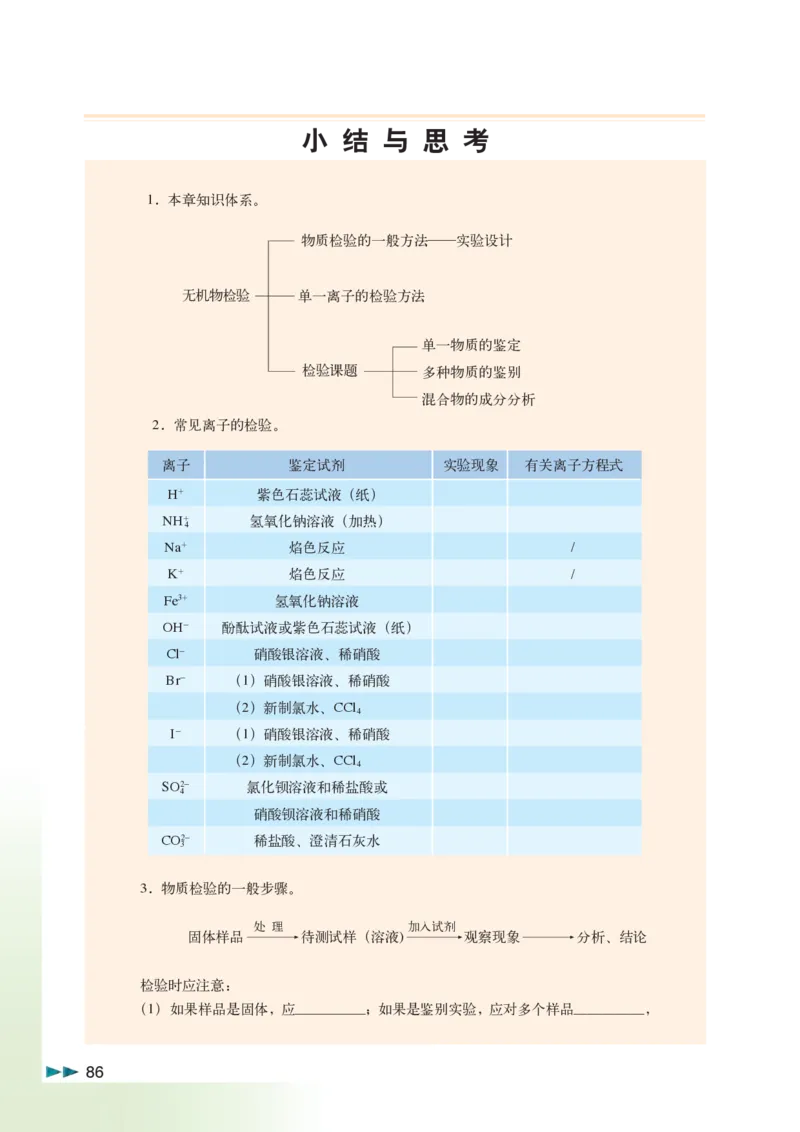
85小 结 与 思 考
1.本章知识体系。
物质检验的一般方法——实验设计
无机物检验 单一离子的检验方法
单一物质的鉴定
检验课题 多种物质的鉴别
混合物的成分分析
2.常见离子的检验。
离子 鉴定试剂 实验现象 有关离子方程式
H+ 紫色石蕊试液(纸)
NH+ 氢氧化钠溶液(加热)
4
Na+ 焰色反应 /
K+ 焰色反应 /
Fe3+ 氢氧化钠溶液
OH- 酚酞试液或紫色石蕊试液(纸)
Cl- 硝酸银溶液、稀硝酸
Br- (1)硝酸银溶液、稀硝酸
(2)新制氯水、CCl
4
I- (1)硝酸银溶液、稀硝酸
(2)新制氯水、CCl
4
SO2- 氯化钡溶液和稀盐酸或
4
硝酸钡溶液和稀硝酸
CO2- 稀盐酸、澄清石灰水
3
3.物质检验的一般步骤。
处 理 加入试剂
固体样品 待测试样(溶液) 观察现象 分析、结论
检验时应注意:
(1) 如果样品是固体,应_____;如果是鉴别实验,应对多个样品_____,
86如果前一步加入的试剂对下一步检验有干扰,应_____。
(2) 分析检验范围和要求,设计实验步骤。多步实验中应注意检验的顺序,防止检验某
一离子时,其他离子的干扰。
(3) 分析应注意从现象到结论的逻辑推理。
4.怎样鉴定草木灰里含有碳酸钾?列表写出实验步骤、现象、结论,并写出有关离子
方程式。
实验步骤 实验现象 分析和结论
5.试设计一个实验方案,把含有NH+、Ca2+和Fe3+的溶液中的各个阳离子进行分离,
4
最后分别制成NH Cl、CaCl 和FeCl 三种溶液。
4 2 3
提示:要求一次取样后,采用连续的实验把三种阳离子分开,哪些试剂可以使三种离子
逐一转化成不同状态而达到分离?
6.A、B、C是三种能溶于水的白色固体,它们的水溶液都显碱性,焰色反应都显黄色。
对A、B、C实验的结果如下:
(1)A + B C + H O
2
(2)B (s) C+ CO + H O
2 2
C + H O
2
不同条件
(3)A + CO
2
B
由此可以推断:A是_____________,B是_____________,C是__________________。
写出C跟CO 反应的化学方程式:____________________________________________。
2
7.某混合液可能是由下列五种溶液中的两种混合而成的:(NH ) SO 、NaOH、MgSO 、
4 2 4 4
AlCl 、BaCl 。在该混合物中滴入氢氧化钠溶液,有白色沉淀生成,继续滴加氢氧化钠溶液,
3 2
沉淀完全消失。在整个实验(加微热)中没有气体产生,试推断混合液是由哪几种溶液混合
而成并说明理由。
87表
期
周
素
元
Ⅰ
录
附
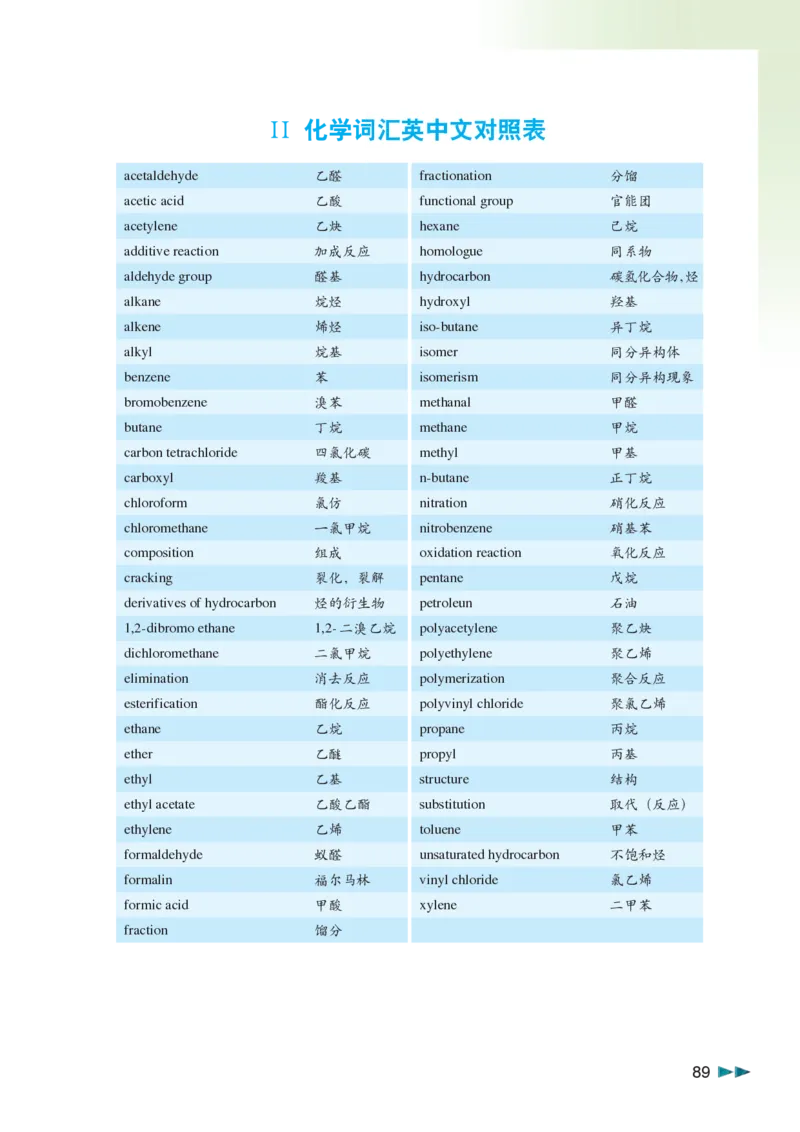
88Ⅱ 化学词汇英中文对照表
acetaldehyde 乙醛 fractionation 分馏
acetic acid 乙酸 functional group 官能团
acetylene 乙炔 hexane 己烷
additive reaction 加成反应 homologue 同系物
aldehyde group 醛基 hydrocarbon 碳氢化合物,烃
alkane 烷烃 hydroxyl 羟基
alkene 烯烃 iso-butane 异丁烷
alkyl 烷基 isomer 同分异构体
benzene 苯 isomerism 同分异构现象
bromobenzene 溴苯 methanal 甲醛
butane 丁烷 methane 甲烷
carbon tetrachloride 四氯化碳 methyl 甲基
carboxyl 羧基 n-butane 正丁烷
chloroform 氯仿 nitration 硝化反应
chloromethane 一氯甲烷 nitrobenzene 硝基苯
composition 组成 oxidation reaction 氧化反应
cracking 裂化,裂解 pentane 戊烷
derivatives of hydrocarbon 烃的衍生物 petroleun 石油
1,2-dibromo ethane 1,2-二溴乙烷 polyacetylene 聚乙炔
dichloromethane 二氯甲烷 polyethylene 聚乙烯
elimination 消去反应 polymerization 聚合反应
esterification 酯化反应 polyvinyl chloride 聚氯乙烯
ethane 乙烷 propane 丙烷
ether 乙醚 propyl 丙基
ethyl 乙基 structure 结构
ethyl acetate 乙酸乙酯 substitution 取代(反应)
ethylene 乙烯 toluene 甲苯
formaldehyde 蚁醛 unsaturated hydrocarbon 不饱和烃
formalin 福尔马林 vinyl chloride 氯乙烯
formic acid 甲酸 xylene 二甲苯
fraction 馏分
8990说 明
本册教材根据上海市中小学(幼儿园)课程改革委员会制定的课程
方案和《上海市中学化学课程标准(试行稿)》编写,供高中二年级第二
学期试用。
本教材由上海市长宁区教育局主持编写,经上海市中小学教材审查
委员会审查准予试用。
参加本册教材修改的有:
姚子鹏 陈基福 洪东府 阮锦莲 陆惊帆
欢迎广大师生来电来函指出教材的差错和不足,提出宝贵意见。上
海市中小学(幼儿园)课程改革委员会办公室地址:上海市陕西北路500
号(邮政编码200041),联系电话62560016(总机转)、52136338。出版
社电话64089888。
声明 按照中华人民共和国“著作权法”第二十三条中,关于“为
实施九年制义务教育和国家教育规划而编写出版教科书,除作者事先声
明不许使用的外,可以不经著作权人许可,在教科书中汇编已经发表的
作品片段或者短小的文字作品、音乐作品或单幅的美术作品、摄影作品,
但应当按照规定支付报酬,指明作者姓名、作品名称”的有关规定,我
们已尽量寻找原作者支付报酬。原作者如有关于支付报酬事宜可及时与
出版社联系。
9192