文档内容
绝密★考试结束前
学年第二学期温州十校联合体期末联考
2024
高二年级化学学科 试题
考生须知:
1.本卷共8页满分100分,考试时间90分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Na-23 S-32 I-127 Ga-70
一、选择题(本大题共 16 小题,每小题 3 分,共 48 分。每小题列出的四个备选项中只
有一项是符合题目要求的,不选、多选、错选均不得分)
1.下列分子属于极性分子的是 ( )
A.CCl B.CO C.P D.NH
4 2 4 3
2.下列化学用语表述正确的是 ( )
A.乙烯的球棍模型:
B.用电子式表示 HCl的形成过程:
C.基态铬原子的价层电子轨道表示式:
D.用电子云轮廓图表示Cl-Cl的σ键的形成示意图:
3.下列关于元素及其化合物的性质说法不 . 正 . 确 . 的是 ( )
A.NaOH与铝粉反应会释放出大量气体,可作管道疏通剂
B.SO 具有氧化性,可作暂时性漂白剂
2
C.柠檬酸酸性比H CO 强,能除去水垢[主要成分为CaCO 、Mg(OH) ]
2 3 3 2
D.HNO 具有腐蚀性和挥发性,使用时应注意防护和通风
3
4.甘氨酸铜[Cu(NH₂CH COO) ]可作催化剂,下列说法正确的是 ( )
2 2
A.电离能:I (N)>I (O)>I (C)
1 1 1
B.电负性:χ(N)>χ(O)>χ(C)
C.离子半径:r(H–)>r(O2–)>r(N3–)
D.沸点:CH COOH>NH CH COOH
3 2 2
5.利用右图装置进行铁上镀铜的实验。下列说法不正确的是 ( )
A.铁片上析出铜的反应为 Fe+Cu2+==Cu+Fe2+
B.镀铜过程中溶液中铜离子的浓度基本不变
C.镀铜前用NaOH溶液,盐酸分别除去铁片上的油污和铁锈
D.以[Cu(NH ) ]SO 溶液为电镀液,可使镀层平滑光亮
3 4 4
6.已知反应:2F +2NaOH=OF +2NaF+H O,N 为阿伏加德罗常数的值,若消耗44.8L(标准状况)F ,
2 2 2 A 2
下列叙述错误的是 ( )
A.F 是氧化剂,NaOH是还原剂
2
B.生成的NaF质量为84g
C.转移的电子数为4N
A
D.生成的H O含有孤电子对数为3N
2 A
高二化学学科 试题 第1页(共8页)7.N 表示阿伏伽德罗常数的值,下列说法不正确的是 ( )
A
A.1mol[Cu(NH ) ]2+中配位键个数为4N
3 4 A
B.标准状况下,5.6L甲烷和乙炔的混合气体中含有的σ键数目小于N
A
C.1mol晶体硅含有共价键数目为4N
A
D.1L0.1mol L 氨水中,含氮微粒数目为0.1N
A
8.下列说法不正确的是 ( )
A.纸张中的纤维素之间通过氢键和范德华力相结合
B. 卤代烃与NaOH溶液共热、滴加AgNO 溶液后根据沉淀颜色可判断卤原子种类
3
C.质谱图显示CH OH的最大质荷比为32
3
D.通过X射线衍射可确定氨基酸的空间结构
9.下列方程式正确的是 ( )
A.向银氨溶液中滴加足量的盐酸:
Ag NH
3
2
OH 3H Ag 2NH
4
H
2
O
B.用铁电极电解饱和食盐水,阳极的电极反应为:2Cl-―2e-=Cl ↑
2
C.明矾溶液与过量氨水混合:
D.苯酚钠溶液中通入CO :
2
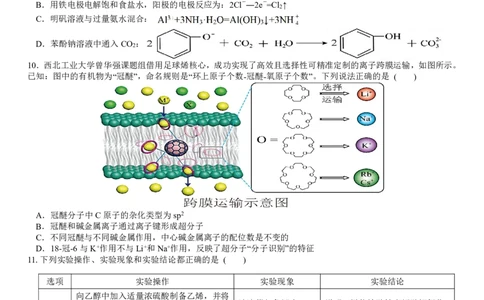
10.西北工业大学曾华强课题组借用足球烯核心,成功实现了高效且选择性可精准定制的离子跨膜运输,如图所示。
已知:图中的有机物为“冠醚”,命名规则是“环上原子个数-冠醚-氧原子个数”。下列说法正确的是 ( )
A.冠醚分子中C原子的杂化类型为sp2
B.冠醚和碱金属离子通过离子键形成超分子
C.不同冠醚与不同碱金属作用,中心碱金属离子的配位数是不变的
D.18-冠-6与K+作用不与Li+和Na+作用,反映了超分子“分子识别”的特征
11.下列实验操作、实验现象和实验结论都正确的是 ( )
选项 实验操作 实验现象 实验结论
向乙醇中加入适量浓硫酸制备乙烯,并将
A 溶液紫红色褪去 说明乙烯能被酸性高锰酸钾氧化
产生的气体直接通入酸性高锰酸钾溶液中
向装有Cu(OH) 固体的两支试管中分别加
2
B Cu(OH) 均溶解 Cu(OH) 是两性氢氧化物
2 2
入稀硝酸和浓氨水。
C 将SO 通入Ba(NO ) 溶液中 产生白色浑浊 反应生成的BaSO 难溶于水
2 3 2 4
为探究Fe与水蒸气高温反应的固体产物
中铁元素的化合价,取少量固体产物于试
前者溶液变血红色, 固体产物中铁元素有+2、+3两种
D 管中,加入足量的稀盐酸溶解,分成两份;
后者溶液紫色褪去。 化合价。
一份中滴加硫氰化钾溶液,另一份中滴加
高锰酸钾溶液。
高二化学学科 试题 第2页(共8页)12.“双碳”背景下,CO 的资源化利用成为全世界的研究热点。电催化还原CO 制备甲酸,原理如图甲所示,电解
2 2
质溶液为KOH。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的
变化如图乙所示。
Q (生成还原产物X所需要的电量)
已知:FE% x 100% 其中,Q nF,n表示电解生成还原产物X所转移电子的
Q (电解过程中通过的总电量) X
总
物质的量,F 表示法拉第常数。下列说法正确的是( )
A.电极a是电解池的阴极,电极反应式为CO +2e–+2H O=HCOOH+2OH–;
2 2
B.当电解电压为U V时,电解过程中含碳还原产物的FE%为0的原因是因为在该电压下电解池的电极不发生
1
化学反应;
C.当电解电压为U V时,电解生成的C H 和HCOO的物质的量之比为1:1;
3 2 4
D.为降低系统能耗,对图甲装置改进,搭建“(阴阳极)共产甲酸耦合系统”,可将b极区KOH电解液更换
为KOHCH OH混合溶液;
3
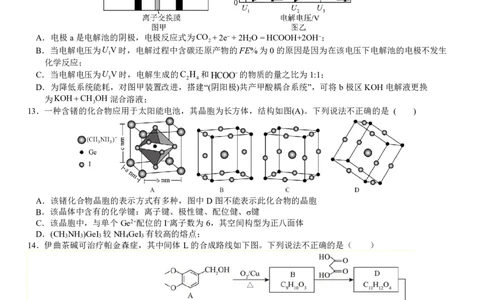
13.一种含锗的化合物应用于太阳能电池,其晶胞为长方体,结构如图(A)。下列说法不正确的是 ( )
A.该锗化合物晶胞的表示方式有多种,图中D图不能表示此化合物的晶胞
B.该晶体中含有的化学键:离子键、极性键、配位健、σ键
C.该晶胞中,与单个Ge2+配位的I–离子数为6,其空间构型为正八面体
D.(CH NH )GeI 较NH GeI 有较高的熔点;
3 3 3 4 3
14.伊曲茶碱可治疗帕金森症,其中间体L的合成路线如下图。下列说法不正确的是( )
高二化学学科 试题 第3页(共8页)A.若E的核磁共振氢谱只有1组峰,E的结构简式是
B.有机物F( )既能与酸反应,又能与碱反应,其中与碱反应的产物之一是甲酸钠
C.IJ的反应中Na S O 的作用是作还原剂
2 2 4
D.BD的反应物 的酸性弱于乙二酸
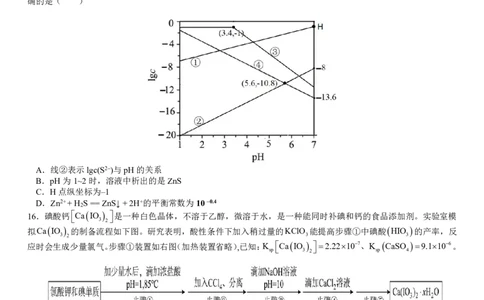
15.室温下,向 c(Al3+)、c(Zn2+)均为 0.1mol·L–1 的混合溶液中持续通入 H S 气体,始终保持 H S 饱和即
2 2
c(H S)=0.1mol·L–1,通过调节pH可使Al3+生成Al(OH) 沉淀,Zn2+生成ZnS沉淀,体系中lgc与pH的关系如下图所
2 3
示,c为HS–、S2–、Al3+和Zn2+的浓度,单位均为mol·L–1。(已知:H S的K =1.0×10–7;K =1.3×10–13)下列说法不正
2 a1 a2
确的是( )
A.线②表示lgc(S2–)与pH的关系
B.pH为1~2时,溶液中析出的是ZnS
C.H点纵坐标为–1
D.Zn2++H S==ZnS↓+2H+的平衡常数为10–0.4
2
16.碘酸钙
CaIO
3
2
是一种白色晶体,不溶于乙醇,微溶于水,是一种能同时补碘和钙的食品添加剂。实验室模
拟CaIO 的制备流程如下图。研究表明,酸性条件下加入稍过量的KClO 能提高步骤①中碘酸HIO 的产率,反
3 2 3 3
应时会生成少量氯气。步骤①装置如右图(加热装置省略),已知:K
sp
CaIO
3
2
2.22107、K
sp
CaSO
4
9.1106。
下列说法正确的是( )
A.步骤①中反应结束后需持续通入氮气一段时间或者将溶液继续煮沸、
加热一段时间,把氯气排入氢氧化钠溶液中吸收。
B.步骤①控制反应温度为85℃是为了防止盐酸挥发。
C.因步骤①中盐酸也会与氯酸钾反应生成少量氯气,
所以把盐酸改用硫酸酸化更合理。
D.步骤⑤得到的晶体用乙醇洗去其中的杂质。
高二化学学科 试题 第4页(共8页)二、非选择题(本大题共 4 小题,共 52 分)
17.(16分)I.歼-10CE在最近的印巴冲突中大放光彩,其中的半导体GaN有源相控阵雷达极大的吸引了世界的
目光。已知GaN成键结构与金刚石相似,晶体中只存N-Ga键。在众多领域发挥重要作用。
(1)关于Ga和镓的化合物下列说法中正确的是 ▲ 。
A.基态Ga原子的电子排布式为:[Ar]4S24P1
B.由以上推测GaN属于共价晶体,N原子的杂化方式为sp3
C.一定条件下,Ga(OH) 受热可分解生成Ga O
3 2 3
D.已知Ga的熔点为29.8℃,沸点2403℃,所以Ga可以做核反应的导热剂
(2)已知在GaN晶体中存在配位键。说明Ga与N原子间可形成配位键的原因 ▲ 。
(3)Ga的化合物很多,GaF 的熔点高于1000℃,GaCl 的熔点为77.9℃。请说明熔点差距的原因是 ▲ 。
3 3
(4)一种GaN晶胞如图甲,三个晶胞围成一个六棱柱,如图乙,则每个N原子周围距离最近的N原子数目为 ▲ 。
已知六棱柱底面边长为anm,高为bnm,试GaN晶体的密度= ▲ g·cm-3。(已知阿伏加德罗常数为N )
A
Ⅱ.氮化镓材料是制造大功率和高频微波电子器件的理想半导体材料。现在工业上通常从铝土矿中提取Ga并制备GaN
的工艺流程如图所示。
已知:①镓的熔点是29.8℃,沸点是2403℃;②氮化镓不溶于水,熔点是1700℃;③镓与铝同主族,镓的化学性质
与铝相似,金属的活泼性:Zn>Ga>Ni>Cu 。
(1)①写出氧化镓与热氢氧化钠溶液反应的离子方程式 ▲ ;
②通入NH 3 在1.0.0.0.℃. 和N..i做 . 催 . 化 . 剂 . 条件下热转化生成GaN的化学方程式是 ▲ 。
(2)图中“酸浸”的目的是 ▲ 。
18.(12分)氢能是一种极具发展潜力的清洁能源,以下是有关氢气制取和利用:
(1)阿根廷科学家MasVeronica等人利用Ni(Ⅱ)、Al(Ⅲ)层状复合催化剂进行了乙醇、水蒸气重整制氢的研究。
其主要反应为:
反应I C H OH(g)+3H O(g) 2CO (g)+6H (g) ΔH =+173.3kJ·mol−1
2 5 2 2 2 1
反应Ⅱ C H OH(g)+H O(g) 2CO(g)+4H (g) ΔH =+255.7kJ·mol−1
2 5 2 2 2
①反应I自发进行的条件是 ▲ 。(填“高温”、“低温”或“任意温度”)。
②一定温度下,若在恒容密闭容器中发生上述反应,下列说法正确的是 ▲ 。
A.选择合适的催化剂,可以加快正反应速/率,提高平衡时CO 的物质的量百分数
2
B.增大C H OH(g)的浓度可以提高C H OH(g)的平衡转化率
2 5 2 5
C.若气体的平均相对分子质量保持不变,说明反应体系已达平衡
D.向密闭容器中加入H O(g),容器中的压强增大,反应I、Ⅱ均逆向移动
2
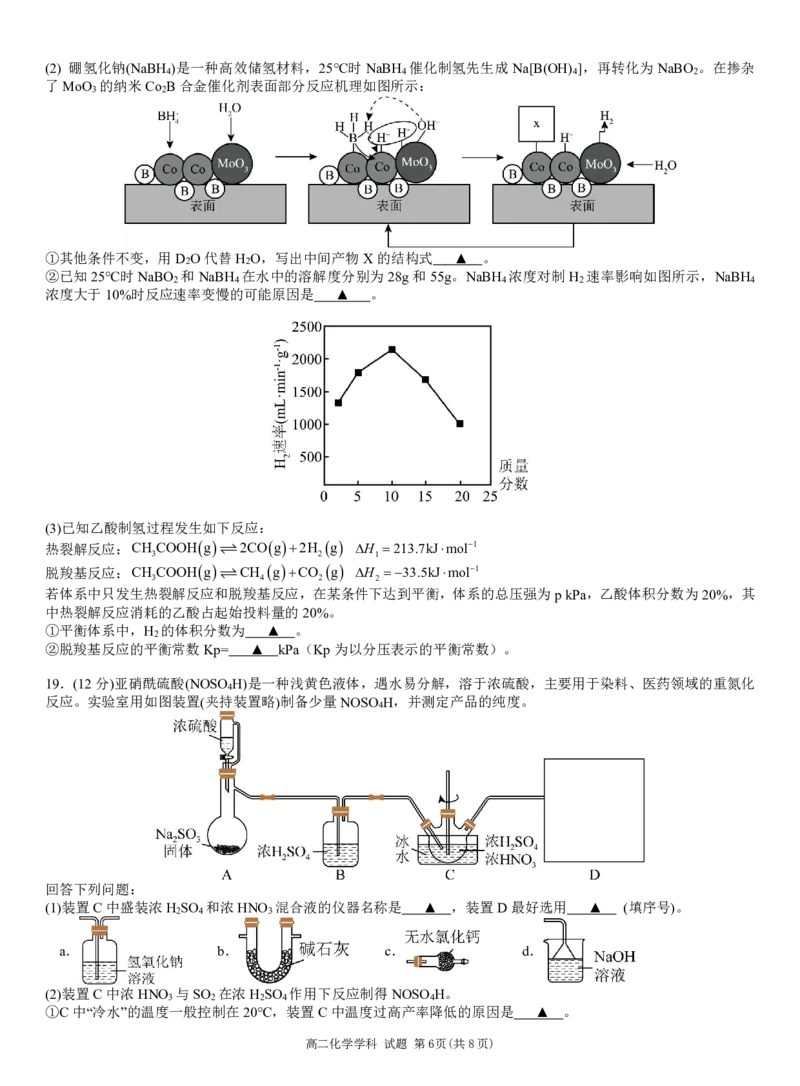
高二化学学科 试题 第5页(共8页)(2) 硼氢化钠(NaBH )是一种高效储氢材料,25℃时NaBH 催化制氢先生成Na[B(OH) ],再转化为NaBO 。在掺杂
4 4 4 2
了MoO 的纳米Co B合金催化剂表面部分反应机理如图所示:
3 2
①其他条件不变,用D O代替H O,写出中间产物X的结构式 ▲ 。
2 2
②已知25℃时NaBO 和NaBH 在水中的溶解度分别为28g和55g。NaBH 浓度对制H 速率影响如图所示,NaBH
2 4 4 2 4
浓度大于10%时反应速率变慢的可能原因是 ▲ 。
(3)已知乙酸制氢过程发生如下反应:
热裂解反应:CH COOHg 2COg2H g H 213.7kJmol1
3 2 1
脱羧基反应:CH COOHg CH gCO g H 33.5kJmol1
3 4 2 2
若体系中只发生热裂解反应和脱羧基反应,在某条件下达到平衡,体系的总压强为pkPa,乙酸体积分数为20%,其
中热裂解反应消耗的乙酸占起始投料量的20%。
①平衡体系中,H 的体积分数为 ▲ 。
2
②脱羧基反应的平衡常数Kp= ▲ kPa(Kp为以分压表示的平衡常数)。
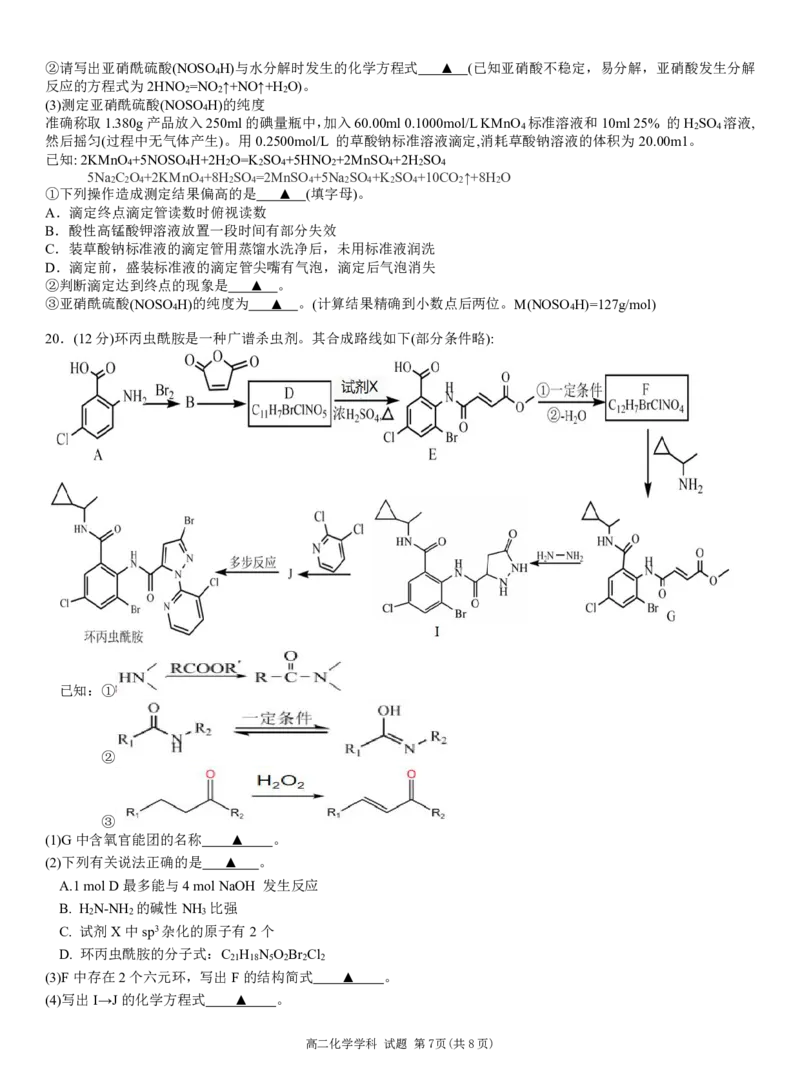
19.(12分)亚硝酰硫酸(NOSO H)是一种浅黄色液体,遇水易分解,溶于浓硫酸,主要用于染料、医药领域的重氮化
4
反应。实验室用如图装置(夹持装置略)制备少量NOSO H,并测定产品的纯度。
4
回答下列问题:
(1)装置C中盛装浓H SO 和浓HNO 混合液的仪器名称是 ▲ ,装置D最好选用 ▲ (填序号)。
2 4 3
a. b. c. d.
(2)装置C中浓HNO 与SO 在浓H SO 作用下反应制得NOSO H。
3 2 2 4 4
①C中“冷水”的温度一般控制在20℃,装置C中温度过高产率降低的原因是 ▲ 。
高二化学学科 试题 第6页(共8页)②请写出亚硝酰硫酸(NOSO H)与水分解时发生的化学方程式 ▲ (已知亚硝酸不稳定,易分解,亚硝酸发生分解
4
反应的方程式为2HNO =NO ↑+NO↑+H O)。
2 2 2
(3)测定亚硝酰硫酸(NOSO H)的纯度
4
准确称取1.380g产品放入250ml的碘量瓶中,加入60.00ml0.1000mol/LKMnO 标准溶液和10ml25% 的H SO 溶液,
4 2 4
然后摇匀(过程中无气体产生)。用0.2500mol/L 的草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00m1。
已知:2KMnO +5NOSO H+2H O=K SO +5HNO +2MnSO +2H SO
4 4 2 2 4 2 4 2 4
5Na C O +2KMnO +8H SO =2MnSO +5Na SO +K SO +10CO ↑+8H O
2 2 4 4 2 4 4 2 4 2 4 2 2
①下列操作造成测定结果偏高的是 ▲ (填字母)。
A.滴定终点滴定管读数时俯视读数
B.酸性高锰酸钾溶液放置一段时间有部分失效
C.装草酸钠标准液的滴定管用蒸馏水洗净后,未用标准液润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
②判断滴定达到终点的现象是 ▲ 。
③亚硝酰硫酸(NOSO H)的纯度为 ▲ 。(计算结果精确到小数点后两位。M(NOSO H)=127g/mol)
4 4
20.(12分)环丙虫酰胺是一种广谱杀虫剂。其合成路线如下(部分条件略):
已知:①
②
③
(1)G中含氧官能团的名称 ▲ 。
(2)下列有关说法正确的是 ▲ 。
A.1molD最多能与4molNaOH 发生反应
B. H N-NH 的碱性NH 比强
2 2 3
C. 试剂X中sp3杂化的原子有2个
D. 环丙虫酰胺的分子式:C H N O Br Cl
21 18 5 2 2 2
(3)F中存在2个六元环,写出F的结构简式 ▲ 。
(4)写出I→J的化学方程式 ▲ 。
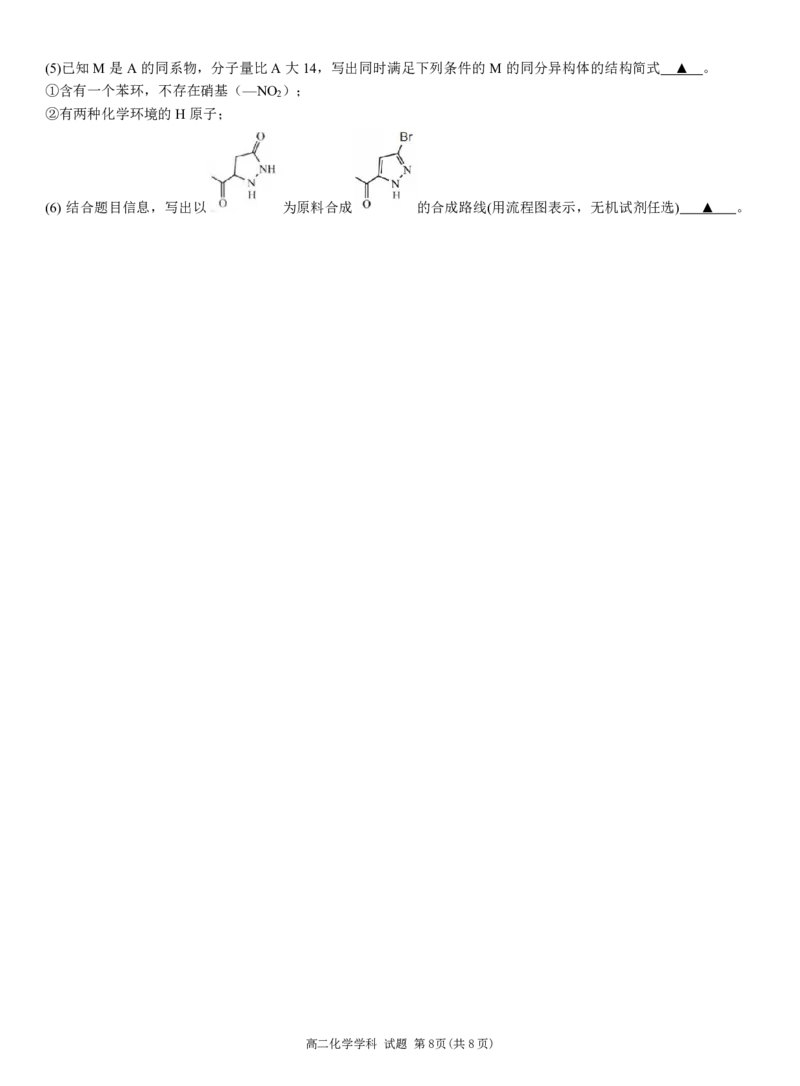
高二化学学科 试题 第7页(共8页)(5)已知M是A的同系物,分子量比A大14,写出同时满足下列条件的M的同分异构体的结构简式 ▲ 。
①含有一个苯环,不存在硝基(—NO );
2
②有两种化学环境的H原子;
(6) 结合题目信息,写出以 为原料合成 的合成路线(用流程图表示,无机试剂任选) ▲ 。
高二化学学科 试题 第8页(共8页)