文档内容
南宁三中2025届毕业班五月第二次适应性测试参考答案
题目 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C B C D A D B C D C B B D C
15. 【答案】(1) 球形冷凝管(1分) P O (或无水CaCl ) (2) 氨水电离导致NH 浓度
2 5 2 3
小,产物产率小,且OH-浓度过大产生Co(OH) 沉淀。
2
2CoCl +8NH +H O +2NH Cl=2CoNH ClCl 2H O
(3)A (4) 2 3 2 2 4 3 5 2 2
(5)乙醇 (6)76.01%(或0.76) (7)小于
16.【答案】(1) 适当加热、搅拌、将矿石粉碎、适当增大硫酸浓度等(1分)
Δ
(2)3MnO +2FeS+12H+ 3Mn2++2Fe3++2S+6H O
2 2
(3) 还原Cu2+、Fe3+ (4) CD 4.9~5.7
(5) Mn2++2H O-2e-=MnO +4H+ (6) 降低(1分)
2 2
(7) FDCA形成的分子间氢键更多
17.【答案】(1)CH g2H SgCS g4H g H 233.5 kJmol1
4 2 2 2
(2)①AB ②CS ③950~1050℃时,以反应Ⅰ为主,随着温度升高,反应Ⅰ平衡右移程
2
度比反应Ⅱ右移程度大,所以S 的体积分数会增大;1050~1150℃之间,反应Ⅱ平衡移动程度
2
增大的幅度大于反应Ⅰ,S 的体积分数会减小
2
④92.3%(或0.923) 121kPa (3)C
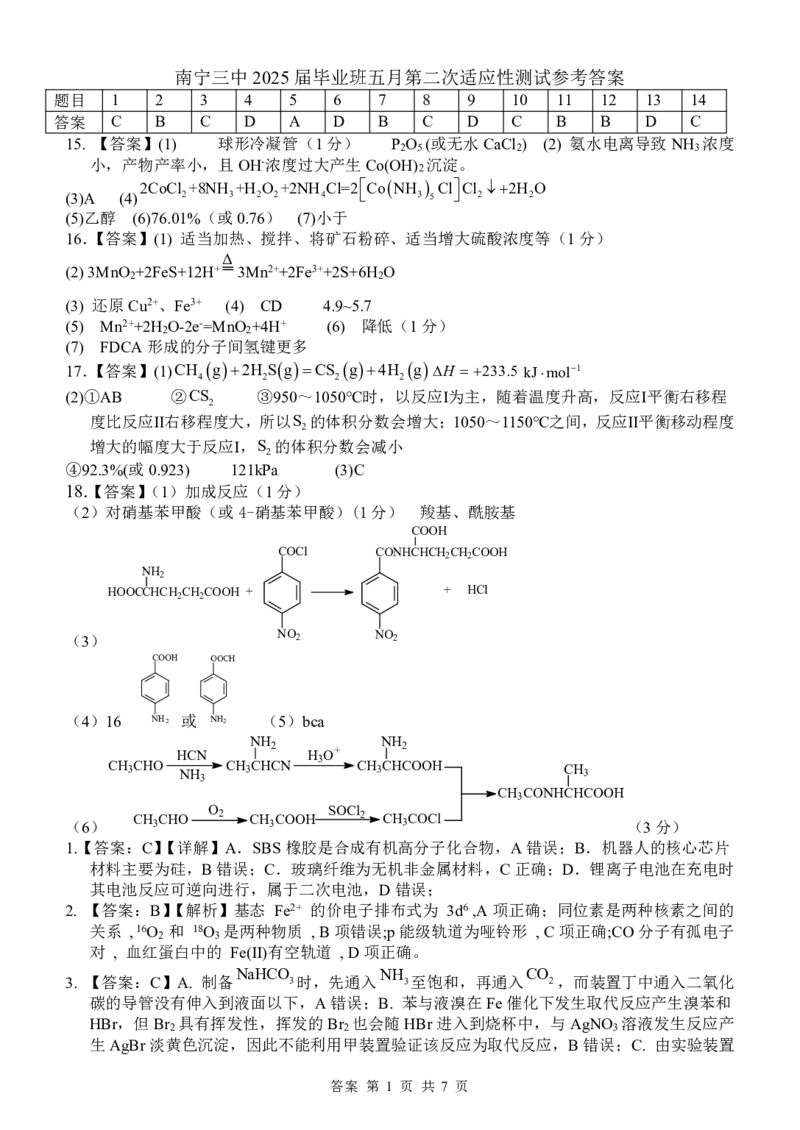
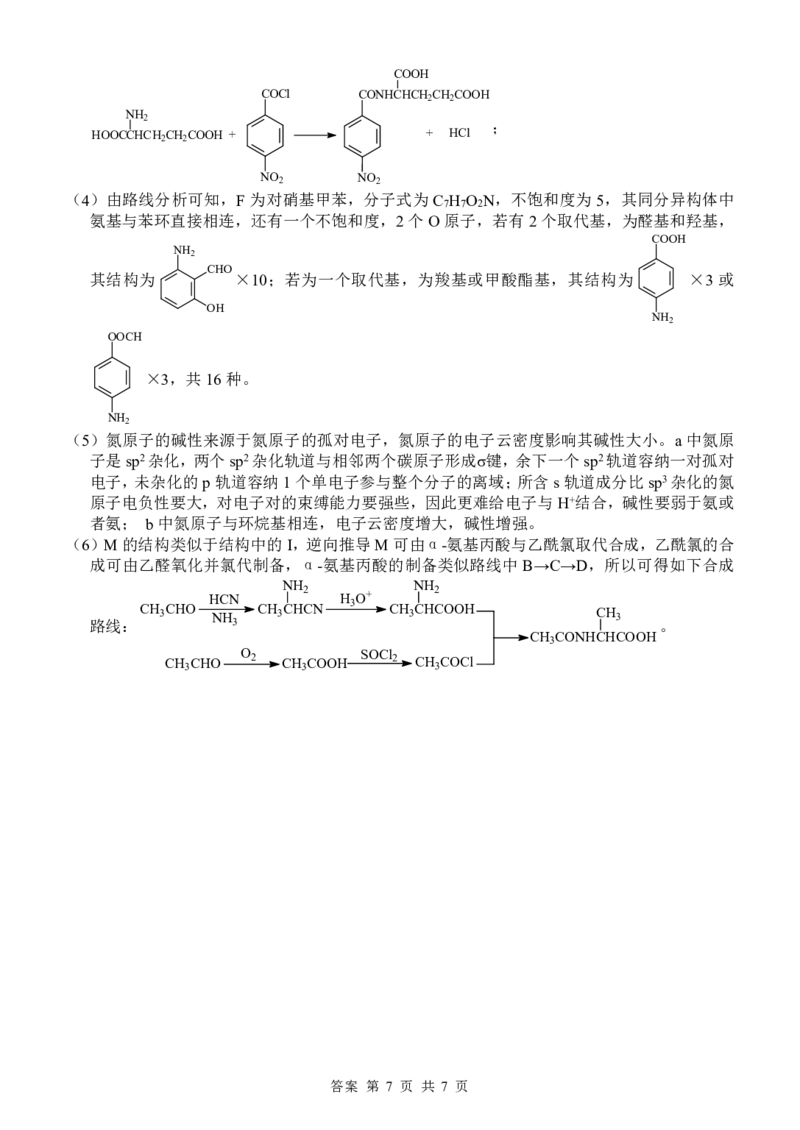
18.【答案】(1)加成反应(1分)
(2)对硝基苯甲酸(或4-硝基苯甲酸)(1分) 羧基、酰胺基
COOH
COCl CONHCHCH2CH2COOH
NH2
HOOCCHCH2CH2COOH + + HCl
(3) NO2 NO2
COOH OOCH
(4)16 NH2 或 NH2 (5)bca
NH NH
HCN 2 H 3 O+ 2
CH 3 CHO NH CH 3 CHCN CH 3 CHCOOH CH 3
3
CH CONHCHCOOH
3
(6) CH 3 CHO O 2 CH 3 COOH SOCl 2 CH 3 COCl (3分)
1.【答案:C】【详解】A.SBS橡胶是合成有机高分子化合物,A错误;B.机器人的核心芯片
材料主要为硅,B错误;C.玻璃纤维为无机非金属材料,C正确;D.锂离子电池在充电时
其电池反应可逆向进行,属于二次电池,D错误;
2. 【答案:B】【解析】基态 Fe2+ 的价电子排布式为 3d6,A项正确;同位素是两种核素之间的
关系 ,16O 和 18O 是两种物质 ,B项错误;p能级轨道为哑铃形 ,C项正确;CO分子有孤电子
2 3
对 , 血红蛋白中的 Fe(II)有空轨道 ,D项正确。
NaHCO NH CO
3. 【答案:C】A. 制备 3时,先通入 3至饱和,再通入 2,而装置丁中通入二氧化
碳的导管没有伸入到液面以下,A错误;B. 苯与液溴在Fe催化下发生取代反应产生溴苯和
HBr,但Br 具有挥发性,挥发的Br 也会随HBr进入到烧杯中,与AgNO 溶液发生反应产
2 2 3
生AgBr淡黄色沉淀,因此不能利用甲装置验证该反应为取代反应,B错误;C. 由实验装置
答案 第 1 页 共 7 页图可知,与直流电源正极相连的锌电极做阳极,Zn-2e-=Zn2+,铁在阴极,电解质溶液为硫酸
Mg2
锌溶液,阴极上Zn2++2e-=Zn,可以实现在铁上镀锌的实验目的,C正确D. 由于 要水解,
MgCl
MgOH
蒸发 2溶液得到 2,不能达到实验目的,D错误。
4.【答案:D】【详解】A.NH 、NF 中心原子均为sp3杂化,且都有一个孤电子对,中心原子
3 3
相同,配位原子H的电负性小于F,用于N-F成键的电子对更偏向氟,氮周围电子云密度减
小,斥力较小,键角较小,A正确;B.氟的电负性大于氯的电负性,F-C的极性大于Cl-C
的性,使-CF 的极性大于-CCl 的极性,导致CF COOH的羧基中的羟基的极性更大,更易电
3 3 3
离出H+,故酸性:CF COOH>CCl COOH,故B正确;C.对羟基苯甲酸形成分子间氢键,
3 3
邻羟基苯甲酸形成分子内氢键,分子间氢键能使物质的熔沸点升高,分子内氢键能使物质的
熔沸点降低,则沸点:对羟基苯甲酸>邻羟基苯甲酸,故C正确;D.用杯酚分离C 和C
60 70
体现了超分子具有分子识别的特征,不是体现了具有自组装特征,D错误;
5. 【答案:A】A. 向澄清石灰水中滴加少量草酸溶液生成草酸钙和水,A正确;B.铅酸蓄电
PbSO PbO
池充电时阳极 4失去电子生成 2,阳极电极反应为
PbSO 2H O2e=PbO 4HSO2
4 2 2 4 ,B错误;C. 将SO 通入酸性KMnO 溶液中,溶液
2 4
紫色褪去即Mn转化为Mn2+,则S被氧化为硫酸根,故离子方程式为:
5SO 2MnO2H O5SO22Mn2 4H
2 4 2 4 ,C错误;D. 醛与足量银氨溶液发生的反应为
甲醛与足量银氨溶液共热反应生成碳酸铵、氨气、银和水,反应的化学方程式为HCHO+
2Ag(NH ) ++2OH-水浴加热4Ag↓+6NH ↑+2NH ++CO 2-+2H O,D错误。
3 2 3 4 3 2
6.【答案:D】【详解】A.已知一个S 分子中含有8个S-S键,则32gS 分子中含S-S键的数目
8 8
32g
为 ×8N mol-1 =N ,A错误;B.由于SO2会发生水解,故100mL0.1mol/LNa SO
(328)g/mol A A 3 2 3
溶液中,SO2的数目小于0.01N ,B错误;
3 A
C.由题干信息可知,反应②为3S +48OH-=16S2-+8SO2 +24H O,其中氧化产物为SO2和还原
8 3 2 3
产物为S2-,则二者物质的量之比为1:2,C错误;D.反应①1molSO 反应,转移电子数为4N ,
2 A
D正确。
7.【答案:B】【分析】同周期中基态Y原子未成对电子数最多,Y为ⅤA族元素;基态Z原子价
层电子排布式为nsnnp2n,n=2,Z为O元素,则Y为N元素;Z和R位于同主族,则R为S
元素;基态M的d能级达到全充满结构,对应Cu(基态Cu的价电子排布为3d10),则M为
Cu;根据
MYX
3
4
RZ
4
X
2
Z,可知X为H,综上所述:X为H、Y为N、Z为O、R为S、
M为Cu,据此解答。【详解】A.电子层数越多,半径越大,电子层结构相同,核电荷数越
大,半径越小,原子半径:YN>ZO>XH,A错误;B.根据同主族从上往下第一电
离能减小,则O>S,N的2p能级半满,第一电离能大于同周期相邻元素,则N>O,所以
第一电离能:YN>ZO>RS,B正确;C.氢化物稳定性: NH >H S,C错误;
3 2
D.
CuNH
3
4
SO
4
是稳定的配合物,向
CuNH
3
4
SO
4
溶液中加入NaOH溶液,不会生成
Cu(OH) ,D错误;
2
8.【答案:C】【解析】A.分子中手性碳有2个 A项错误。B.消去反应的有机产物最
多有3种,出现双键的位置 B项错误。C.红外光谱可以鉴定化学键和官能团,图
答案 第 2 页 共 7 页中含氧官能团有羟基、羰基、醚键三种,C项正确。D.1mol有机物最多可与7molH 发生加成
2
反应,D项错误。
9.【答案】D【详解】A.根据Li+移动方向可知:b极为正极,a极为负极;充电时,b极为阳
极,a极为阴极,故电极电势b极高于a极,A正确;B.放电时,电子由负极a流出经外电
路负载流入正极b,B正确;C.充电时,b极为阳极,失去电子,电极反应
为L:iLaZrTaOxe xLiLi LaZrTaO ,C正确;D.放电时:外电路通过1mol电子时,
1x
b极减少1molLi+ ,质量为7g,a极1molLi+ 得到电子变为锂增重7g,充电时:外电路通过
1mol电子时,a极失去电子迁移1molLi+ 到b极,a极质量减少7g,b极1molLi+ 得到电子
变为锂增重7g,两电极质量变化差值为14g,D错误;
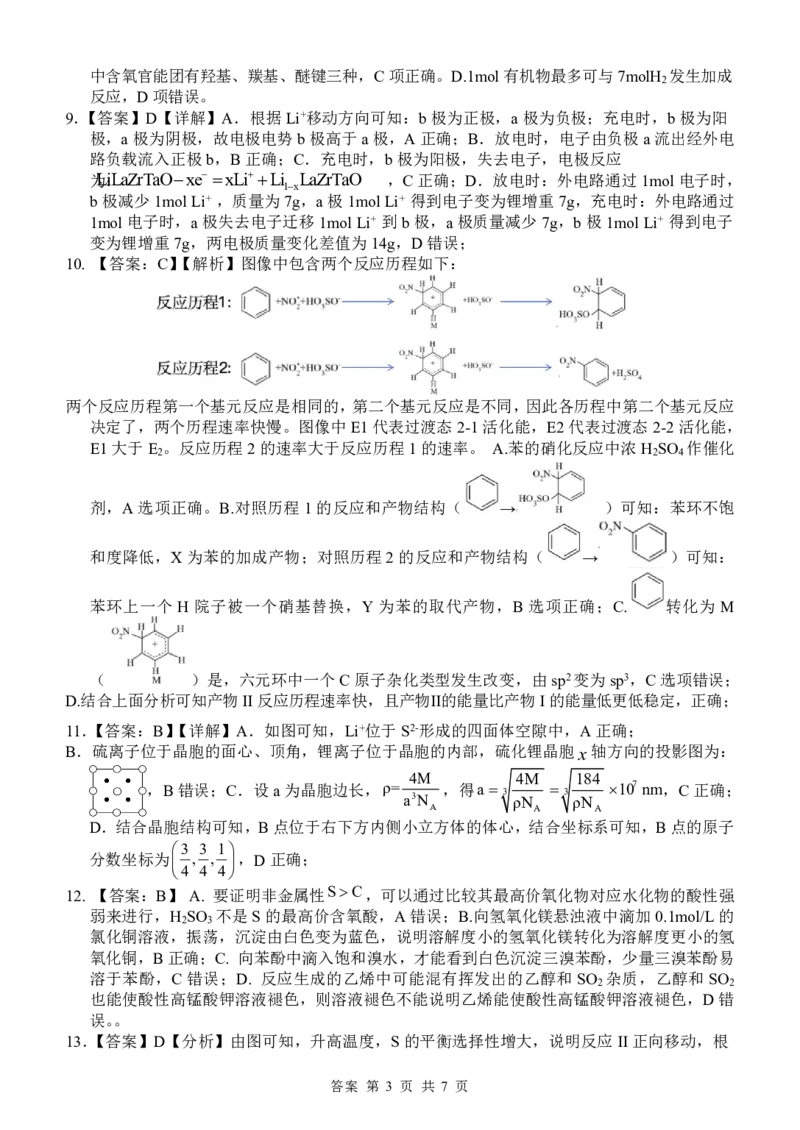
10. 【答案:C】【解析】图像中包含两个反应历程如下:
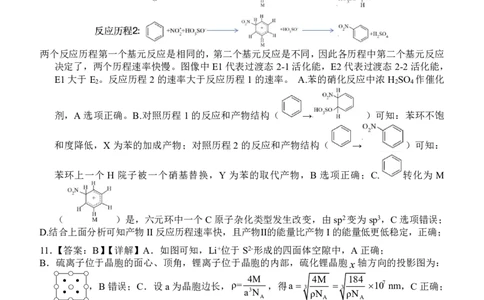
两个反应历程第一个基元反应是相同的,第二个基元反应是不同,因此各历程中第二个基元反应
决定了,两个历程速率快慢。图像中E1代表过渡态2-1活化能,E2代表过渡态2-2活化能,
E1大于E 。反应历程2的速率大于反应历程1的速率。 A.苯的硝化反应中浓H SO 作催化
2 2 4
剂,A选项正确。B.对照历程1的反应和产物结构( → )可知:苯环不饱
和度降低,X为苯的加成产物;对照历程2的反应和产物结构( → )可知:
苯环上一个 H 院子被一个硝基替换,Y 为苯的取代产物,B 选项正确;C. 转化为 M
( )是,六元环中一个C原子杂化类型发生改变,由sp2变为sp3,C选项错误;
D.结合上面分析可知产物II反应历程速率快,且产物Ⅱ的能量比产物I的能量低更低稳定,正确;
11.【答案:B】【详解】A.如图可知,Li+位于S2-形成的四面体空隙中,A正确;
B.硫离子位于晶胞的面心、顶角,锂离子位于晶胞的内部,硫化锂晶胞x轴方向的投影图为:
4M 4M 184
,B错误;C.设a为晶胞边长,ρ= ,得a
3
3
107 nm,C正确;
a3N ρN ρN
A A A
D.结合晶胞结构可知,B点位于右下方内侧小立方体的体心,结合坐标系可知,B点的原子
3 3 1
分数坐标为 , , ,D正确;
4 4 4
12. 【答案:B】 A. 要证明非金属性SC,可以通过比较其最高价氧化物对应水化物的酸性强
弱来进行,H SO 不是S的最高价含氧酸,A错误;B.向氢氧化镁悬浊液中滴加0.1mol/L的
2 3
氯化铜溶液,振荡,沉淀由白色变为蓝色,说明溶解度小的氢氧化镁转化为溶解度更小的氢
氧化铜,B正确;C. 向苯酚中滴入饱和溴水,才能看到白色沉淀三溴苯酚,少量三溴苯酚易
溶于苯酚,C错误;D. 反应生成的乙烯中可能混有挥发出的乙醇和SO 杂质,乙醇和SO
2 2
也能使酸性高锰酸钾溶液褪色,则溶液褪色不能说明乙烯能使酸性高锰酸钾溶液褪色,D错
误。。
13.【答案】D【分析】由图可知,升高温度,S的平衡选择性增大,说明反应II正向移动,根
答案 第 3 页 共 7 页据勒夏特列原理,正反应是吸热反应,即ΔH >0,随着温度升高,反应I逆向移动,COS的
2
量减少,而反应II正向移动,S的量增加,已知曲线b表示COS的平衡选择性,所以曲线c
表示S的平衡选择性,曲线a表示SO 的平衡转化率;
2
【详解】A.随着温度升高,反应I逆向移动,COS的量减少,而反应II正向移动,S的量增加,
已知曲线b表示COS的平衡选择性,所以曲线c表示S的平衡选择性,A正确;
B.由图可知,升高温度,S的平衡选择性增大,说明反应II正向移动,根据勒夏特列原理,正
反应是吸热反应,即ΔH >0,B正确;
2
C.设起始n(SO )=1mol,n(CO)=3mol,在1400K下,SO 平衡转化率为80%,则转化的
2 2
n(SO )=0.8mol,COS平衡选择性为50%,则生成n(COS)=0.8mol×50%=0.4mol,生成
2
n(S)=0.4mol。根据反应I生成n(CO )=0.8mol×2=1.6mol,剩余
2
n(CO)=3mol−0.8mol×3+0.4mol=1.0mol。对于反应SO (g)+2CO(g)⇌ S(g)+2CO (g),平衡时
2 2
n(SO )=1mol−0.8mol=0.2mol,n(CO)=0.4mol,n(S)=0.4mol,n(CO )=1.6mol。因为是恒压体系,
2 2
体积比等于物质的量之比,设平衡时总体积为V,根据平衡常数表达式
n(S) n(CO )
×( 2 )2
V V
0.41.62
K= = =5.12,C正确;D.反应I是气体分子数减小的反应,增大
n(SO ) (n(CO) 0.21.02
2 × )2
V V
压强,反应I正向移动,从而使SO 的平衡转化率增大,D错误。
2
14.【答案】C【分析】随着pH增大,c(H+)减小,c(HAc)减小,c(Ac−)增大,所以曲线Ⅱ对应HAc
的分布系数(随pH增大而减小),曲线Ⅲ对应Ac−的分布系数(随pH增大而增大),据此分
析解题。【详解】A.随着pH减小,c(H+)增大,AgAc(s)+H+(aq) Ag+(aq)+HAc(aq),平衡
正向移动,随pH减小lgc(Ag+)增大,曲线I代表lgc(Ag+) 与pH的关系,A正确;
B.当pH=4.5时,溶液中存在物料守恒c(Ag+)=c(Ac−)+c(HAc),电荷守恒
c(Ag+)+c(H+)=c(Ac−)+c(NO-)+c(OH−),联立可得c(HAc)+c(H+)=c(NO-)+c(OH−) ,pH=4.5时,
3 3
c(H+)>c(OH−),所以c(HAc)