文档内容
化学参考答案及解析
一、选择题(本大题共 16 小题,每小题 3 分,共 48 分。每个小题列出的四个备选项中只有一个是
符合题目要求的,不选、多选、错选均不得分)
1. 【答案】A
【解析】A.NO 为非金属氧化物,溶于水不是自身导电,故 NO 不属于电解质;B.CH COOH 是
2 2 3
电解质;C.CaCO 属于盐,熔融态导电,CaCO 是电解质;D.水是电解质。
3 3
2. 【答案】A
【解析】聚合氯化铝可作为混凝剂与其氧化性无关。
3. 【答案】C
【解析】OF 电子式为 。
2
4. 【答案】D
【解析】K Cr O 是氧化剂,C H OH 是还原剂,故 A 正确;1molC H OH 中含有 σ 键的数目为
2 2 7 2 5 2 5
8 N ,0.5 mol C H OH 中含有 σ 键的数目为 4N ,故 B 正确;每 1 mol 反应转移电子数为 12
A 2 5 A
N ,则生成 1mol CH COOH 转移电子的数目为 4N ,故 C 正确;氧化产物和还原产物物质的量
A 3 A
之比为 3︰2,故 D 错误。
5. 【答案】D
【解析】ClO- 氧化 I-,两者不能共存,故A 错误;Fe3+、SCN- 结合生成Fe(SCN),不能共存,
3
故B 错误;SO2-、Pb2+形成 PbSO 沉淀,故 C 错误。
4 4
6. 【答案】C
【解析】尿素是生物体内蛋白质代谢分解的主要含氮终产物,故A 正确;尿素可通过无机物制备
得到,故B 正确;尿素在水中不电离,故C 错误;酰胺基一般是近中性的,同浓度时尿素溶液碱
性弱于氨水,故D 正确。
7. 【答案】B
【解析】普通玻璃中加入某些金属氧化物,能够得到彩色玻璃,故 A 正确;橡胶硫化使其结构由线
型转变为网状,可以提高其强度、韧性和化学稳定性,故 B 错误;钢中加入某些稀土元素,可以增
强抗腐蚀性、耐热性,故C 正确;布洛芬进行成酯修饰,对胃、肠道刺激减弱,故 D 正确。
8. 【答案】C
【解析】图①装置生成的乙炔气体中含有 H S、PH 等还原性杂质,故 A 错误;铜与稀硝酸反应
2 3
生成 NO,故 B 错误;I-能和 I 反应生成 I -,故浓 KI 溶液可以分离 I 和 CCl ,故 C 正确;
2 3 2 4
FeCl 加热易水解,不能得到无水 FeCl 晶体,故D 错误。
3 3
9. 【答案】B
【解析】根据核磁共振氢谱和质谱判断出该有机物为异丁醇(CH ) CHOH。
3 2
10. 【答案】B
【解析】碳酸钠溶液吸收 NO :2NO +Na CO =NaNO +NaNO +CO ,故 A 正确;氯化银悬浊液
2 2 2 3 2 3 2
中加入浓氨水:AgCl+2NH =[Ag(NH ) ]+ +Cl-,故 B 错误;碘化钾溶液在空气中氧化变质:
3 3 2
4I-+O+2HO =2I+4OH-,故 C 正确;羧基的酸性大于酚羟基,故水杨酸中加入少量氢氧化钠溶
2 2 2
液,如图所示,故D 正确。
第 10 题
解图11. 【答案】A
【解析】A 为丙酮,丙酮易溶于水和有机溶剂,故 A 错误;B 中含有羧基和羟基两种含氧官能团,
故 B 正确;由Y 结构可知,X 的结构简式为 CH OH,故 C 正确;苯酚通过以下合成路线可制
3
备
,故 D 正确。
第 11 题
解图
12. 【答案】D
【解析】由题意可知,A、B、C、D、E 分别为:H、N、Al、P、S 元素。A 项,N、P 均可与 H
形成含 18 电子的二元化合物,分别为 N H 和 PH ,故 A 正确。B 项,AlN 熔点高、绝缘性好,
2 4 3
故 B 正确。C 项,PH 和 H S 中心原子均为 sp3 杂化,故C 正确。D 项,硫酸与磷酸难挥发的原
3 2
因是存在分子间氢键,故 D 错误。
13. 【答案】A
【解析】A 项,在提取锂、分解有机物过程中,Li 元素的价态未发生变化,故A 错误。
14. 【答案】D
【解析】A 项,由图可知生成 α-萘磺酸的活化能更小,萘环上 α 的活性大于 β 位活性,故 A 错
误。B 项,反应未达平衡时,适当提高反应的温度,生成 β-萘磺酸的反应活化能大,速率增加的
更快,比例降低,故B 错误。C 项,β-萘磺酸能量低,更稳定,故 C 错误。D 项,β-萘磺酸更稳
定,选择相对较长的反应时间,可获得高产率的β-萘磺酸,故 D 正确。
15. 【答案】D
【解析】A 项,c(H+)≈ =3×10−3mol/L,故 A 正确。B 项,(CH COO) Ca 溶液中存在
3 2
c(CH COO−)>c(Ca2+)>c(OH−)>c(CH COOH)>c(H+),故 B 正确。C 项,由二者溶度积可知,
3 3
√c ∙ Ka
常温下,在水中的溶解度:CaSiO >CaCO ,故 C 正确。D 项,(CH COO) Ca 转化为 CaCO
3 3 3 2 3
的 离 子 反 应 方 程 式 为 : 2CH COO-+Ca2++HCO=CaCO↓+2CHCOOH , 其 平 衡
3 2 3 3 3
常 数
K= = ≈19,故 D 错误。
2
𝑐(𝐶𝐻3𝐶𝑂𝑂𝐻) 𝐾𝑎1𝑐(𝐻2𝐶𝑂3)∙𝐾𝑎2𝑐(𝐻2𝐶𝑂3)
16. 【答𝑐(𝐶案𝐻3】𝐶𝑂C𝑂 − ) 2 ∙𝑐(𝐶𝑎 2+ )∙𝑐(𝐻2𝐶𝑂3) [𝐾𝑎(𝐶𝐻3𝐶𝑂𝑂𝐻)] 2 ∙𝐾sp(CaC𝑂3)
【解析】步骤 I,调节 pH 为酸性,可以抑制 Cl 、Br 和水反应,故 A 正确;液体混合物①到液
2 2
体混合物②目的为将低浓度 Br 富集为高浓度的 Br ,故 B 正确;步骤 III 使用盐酸,会引入 Cl
2 2 2
杂质同时消耗BrO -,故 C 错误;步骤 IV 为蒸馏操作,故D 正确。
3
二、非选择题(本大题共 4 小题,共 52 分)
17.(16 分)
【答案】
I.
(1)K OI(1 分) 8(1 分)
3
(2)A(2 分)(3)①三角锥形(1 分)<(1 分) 酸性 P >H O+,反应 ΔS >0(各 1 分,共 2 分)
3
②H P O
n+2 n 3n+1
H+
(1 分) ②(1 分) 4II.
(1)KCl 溶液(2 分)
(2)蒸发浓缩、冷却结晶、过滤(2 分)
(3)重结晶(2 分)
【解析】
I.
(2)A 项,电负性:O>I>P,正确。B 项,K+<P3−<I−,错误。C 项,第一电离能:N>O>P,
错误。D 项,为激发态P 原子的排布式,错误。
(3)②由链状多磷酸的结构可推出其通式为 H P O 。②处 P 原子上仅连接一个羟基。羟基中氧
n+2 n 3n+1
氢键的极性更强,更易电离出H+。
II.
(2) K Cr O 受热易分解,需采用蒸发浓缩、冷却结晶、过滤的方法。
2 2 7
18.(12 分)
【答案】
(1)D(2 分)
(2)b(2 分)
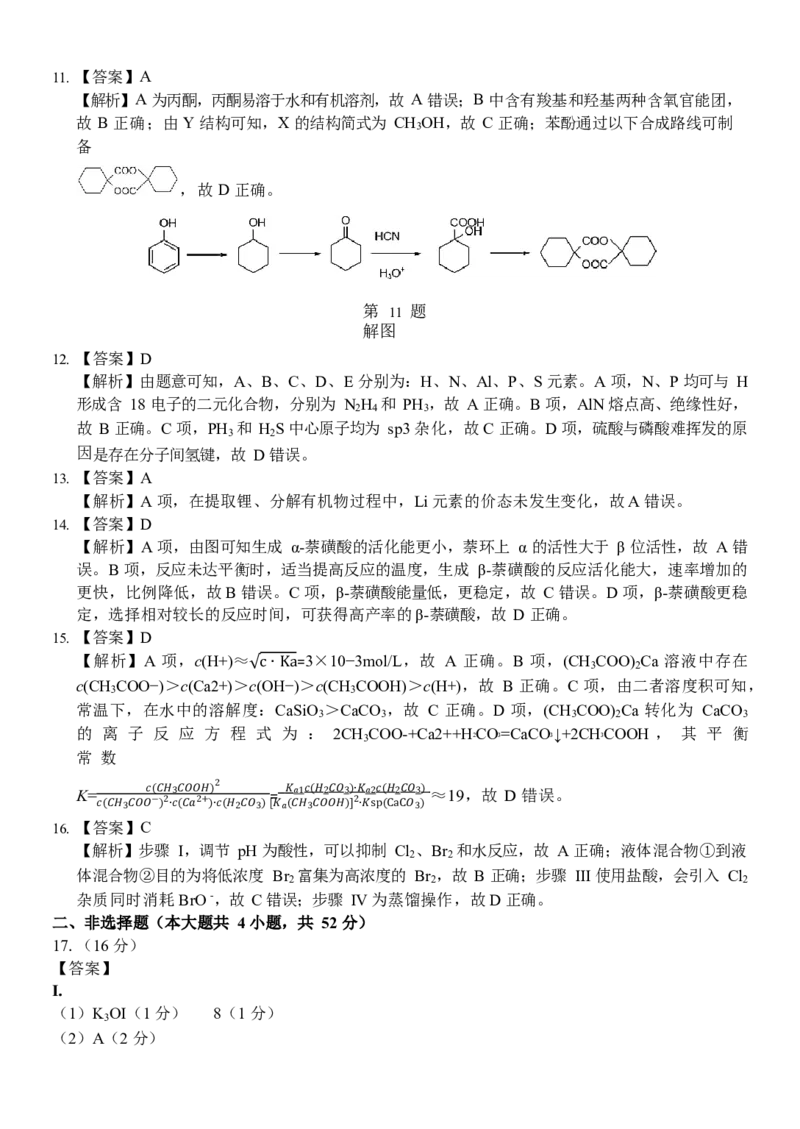
(3) ①温度升高,反应 I、II 均逆移,CO 浓度增大。CO 浓度增大对反应Ⅱ的影响超过了温度升高
的影响。(2 分)
②如下图所示(最高点比原来低,温度比原来高,各 1 分,共 2 分)
第 18(3)
题解图
(4)①75%(2 分) ②CO-2e-+O2-=CO (2 分)
2
【解析】
(2)反应Ⅰ的 ΔS<0、反应Ⅱ的 ΔS≈0,由公式ΔG=ΔH-T·ΔS,可知应为线条b。
(3)②压强增大有利于反应Ⅰ,因此最高点比原来低,温度比原来高。
19.(12 分)
【答案】
(1)温度过高造成 Fe (SO ) 分解,使其不能与 LiFePO 反应生成可溶性 Li SO ,致使锂浸出率下
2 4 3 4 2 4
降。(2 分)
(2)Fe(OH) (2 分)
3
(3)CD(2 分)
(4)bafc(2 分)
(5)1)96.2%(2 分) 2)煮沸(1 分) 除去 CO (其他合理答案亦可)(1 分)
2【解析】
(1) 步骤 I,焙烧温度过高造成 Fe (SO ) 分解,使其不能与LiFePO 反应生成可溶性Li SO ,致
2 4 3 4 2 4
使锂浸出率下降。
(2) 步骤 III 滤渣的主要成分为 Fe(OH)
3
(3) 焙烧前将原料粉碎有利于加快反应的速率,故 A 正确;FePO 、Fe O 杂质难溶于水,故步骤
4 2 3
II 滤渣为 FePO 、Fe O ,故 B 正确;步骤 II、III 获取滤液,步骤 IV 获取滤渣,洗涤目的不同。
4 2 3
Li CO 溶解度随温度升高而降低,故步骤 IV 应使用热水洗涤,C 错误;Li CO 微溶于水,步
2 3 2 3
骤 IV 沉淀剂应选用饱和的碳酸钠溶液,D 错误。
(4) 步骤 V,提纯粗产品的操作为:加水溶解,通入足量 CO 使碳酸锂转化为碳酸氢锂,加入NaOH
2
除镁,再次通少量的 CO 消耗碳酸锂和氢氧化锂,减少损失,90℃蒸发溶剂至溶液中出现大量
2
晶体,使碳酸氢锂分解,停止加热,趁热过滤,洗涤、干燥。故正确的操作顺序为:bafc
(5)①n(H SO 消耗)=2×12.5×10-3—0.2×24×10-3×0.5×5=0.013mol,n(Li CO )=n(H SO 消
2 4 2 3 2 4
耗)=0.013mol,碳酸锂的质量分数为:(0.013×74)÷1.000×100%=96.2%;
②操作时缺少了煮沸除去CO ;CO 溶于水,将使得硫酸消耗量偏小,从而使得计算值偏小。
2 2
20.(12 分)
【答案】
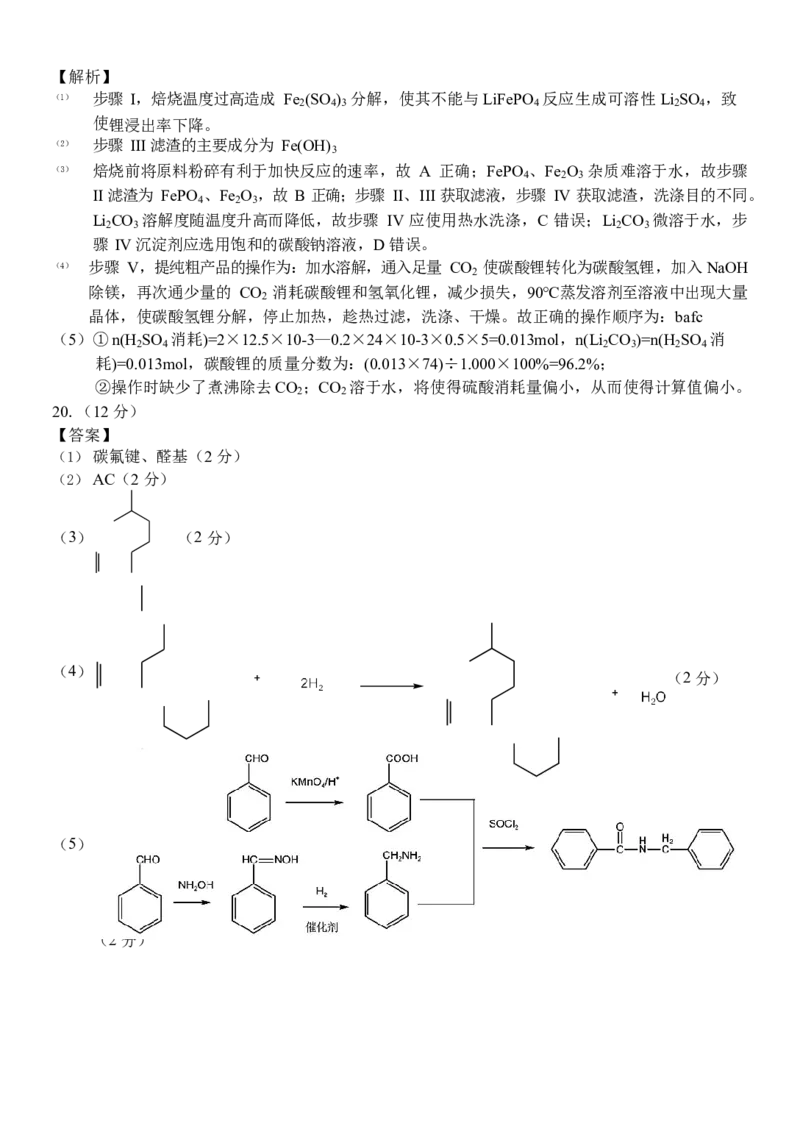
(1)碳氟键、醛基(2 分)
(2)AC(2 分)
(3) (2 分)
(4)
(2 分)
(5)
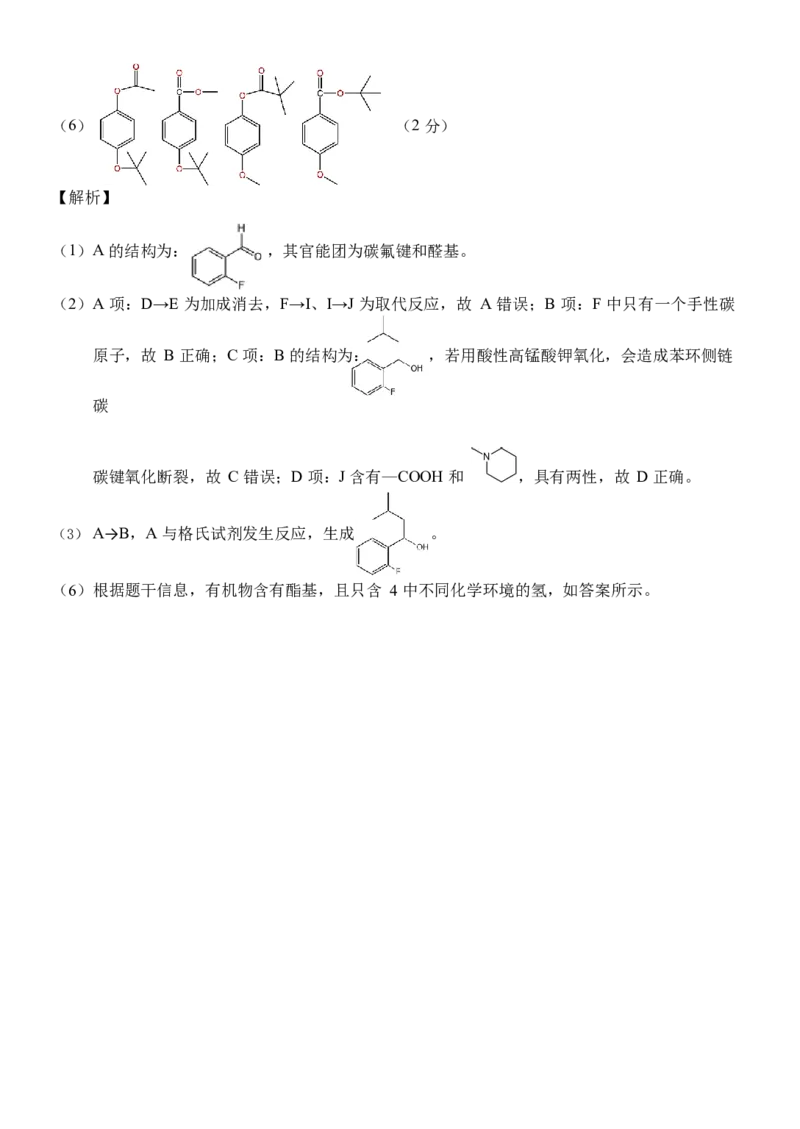
(2 分)(6) (2 分)
【解析】
(1)A 的结构为: ,其官能团为碳氟键和醛基。
(2)A 项:D→E 为加成消去,F→I、I→J 为取代反应,故 A 错误;B 项:F 中只有一个手性碳
原子,故 B 正确;C 项:B 的结构为: ,若用酸性高锰酸钾氧化,会造成苯环侧链
碳
碳键氧化断裂,故 C 错误;D 项:J 含有—COOH 和 ,具有两性,故 D 正确。
(3)A→B,A 与格氏试剂发生反应,生成 。
(6)根据题干信息,有机物含有酯基,且只含 4 中不同化学环境的氢,如答案所示。