文档内容
化学试题
可能用到的相对分子质量:H1 Li 7 C12 N14 O16 S32 Pb207 Sn119 Zn 65 I 127
一、单项选择题(每题3分,共45分)
1.历经十年传承积淀,形成精湛的东阿阿胶传统工艺,包括洗皮、泡皮、晾皮、刮毛、铡皮、
化皮、打沫、除渣、浓缩、挂旗、凝胶、切胶等工序。下列工序与化学实验中的原理不具有
对应关系的是( )
选项 A B C D
工序
化学
实验
2. 化学在生产生活和科技发展中发挥着重要的作用,下列说法不正确的是( )
A.医用酒精可使细菌的蛋白质变性 B.碳酸钙可调节水泥的硬化速率
C.铁强化酱油可减少缺铁性贫血的发生 D.漂粉精可用于游泳池的消毒
A. A B. B C. C D. D
3.下列化学用语正确的是( )
A.甲醛中键的电子云轮廓图: B.镁原子最外层电子云轮廓图:
n
C.用电子式表示CaO 的形成过程:
2
D.H O 分子的球棍模型:
2 24. 已知298K,101kPa时,2H (g)+O (g)=2H O(l) △H=-571.6kJ∙mol-1,H 的临界温度(能
2 2 2 2
够液化的最高温度)为32.98K,下列说法错误的是( )
..
A. 氢气燃烧热△H=-285.8kJ∙mol-1
B. 题述条件下2molH 和1molO ,在燃料电池中完全反应,电功+放热量=571.6kJ
2 2
C. 氢能利用的关键技术在于安全储存与运输
D. 不同电极材料电解水所需电压不同,产生2gH (g)消耗的电功相同
2
5.制备(NH ) Fe(SO ) ·6H O的实验中,需对过滤出产品的母液(pH<1)进行处理。常温下,
4 2 4 2 2
分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
A.通入过量Cl :Fe2+、H+、NH +、Cl-、SO 2-
2 4 4
B.加入少量NaClO溶液:NH +、Fe2+、H+、SO 2-、ClO-
4 4
C.加入过量NaOH溶液:Na+、Fe2+、NH +、SO 2-、OH-
4 4
D.加入过量NaClO和NaOH的混合溶液:Na+、SO 2-、Cl-、ClO-、OH-
4
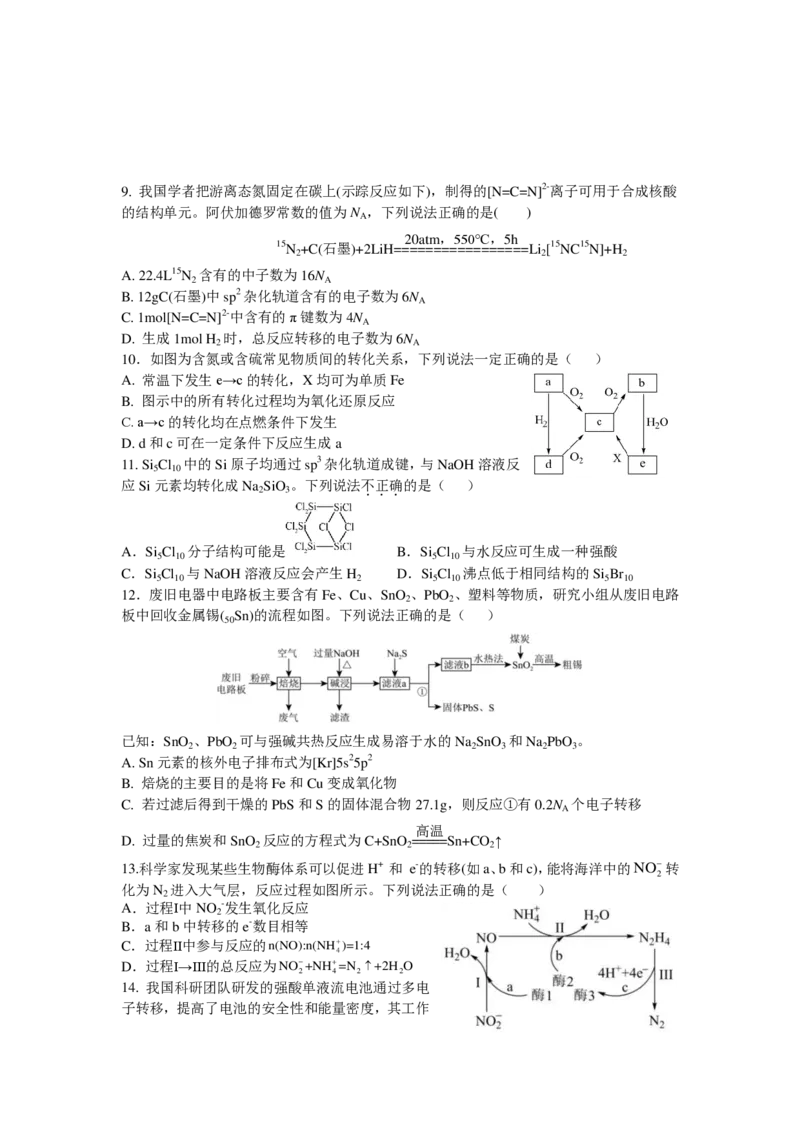
6.《天工开物》介绍了锌的冶炼方法:把炉甘石(ZnCO )和煤炭饼装入炼锌罐(如图所示),泥
3
封,“其底铺薪,发火煅红”,“冷定毁罐取出”。已知:锌的熔点为 419℃,沸点为 907℃。
下列说法错误的是( )
A. 反应区中,生成的气体只有CO
2
B. 冷凝区中,锌由气态转化为液态,理论上该区温度控制在
419~907℃
C. “冷定”后取锌的原因是防止Zn在较高的温度下被氧化
D. 炉甘石炼锌法中,气体的生成有利于该还原过程的发生
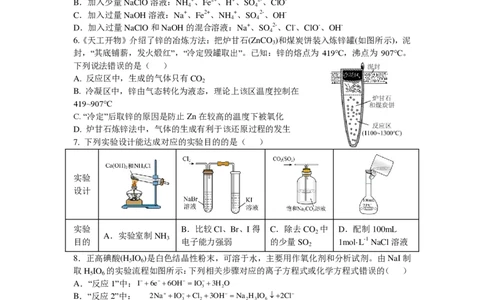
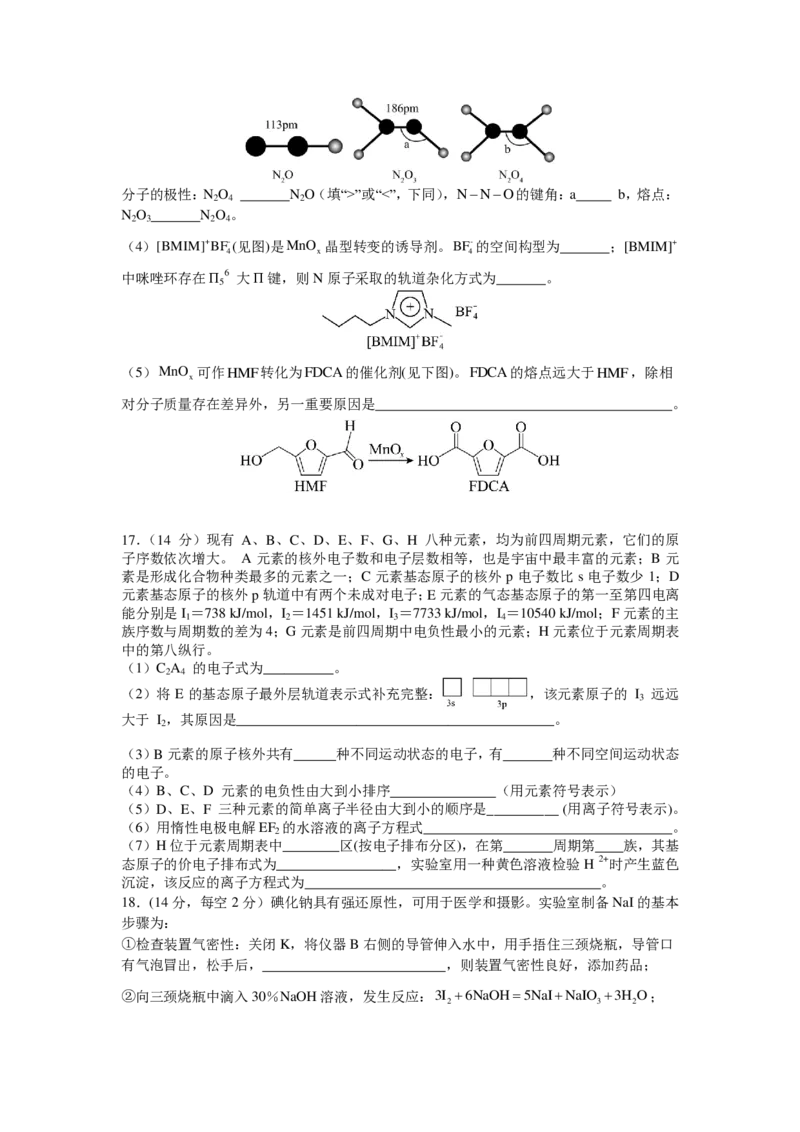
7. 下列实验设计能达成对应的实验目的的是( )
实验
设计
实验 B.比较Cl、Br、I得 C.除去CO 中 D.配制100mL
A.实验室制NH 2
目的 3 电子能力强弱 的少量SO 1mol·L-1 NaCl溶液
2
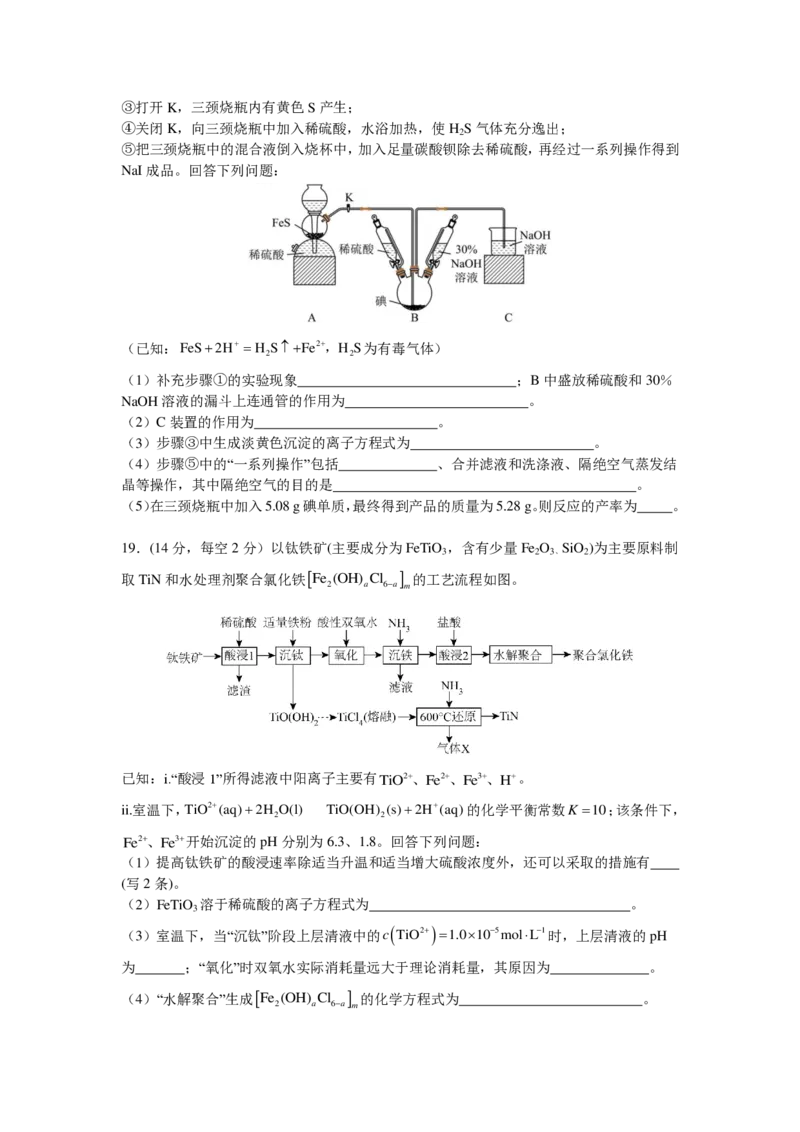
8.正高碘酸(H IO )是白色结晶性粉末,可溶于水,主要用作氧化剂和分析试剂。由NaI制
5 6
取H IO 的实验流程如图所示:下列相关步骤对应的离子方程式或化学方程式错误的( )
5 6
A.“反应1”中:I6e6OH IO3H O
3 2
B.“反应2”中: 2NaIOCl 3OH Na H IO 2Cl
3 2 2 3 6
C.“反应3”中:Na H IO 5Ag Ag IO 2Na3H
2 3 6 5 6
D.“反应4”中:4Ag IO 10Cl 10H O4H IO 20AgCl5O
5 6 2 2 5 6 29. 我国学者把游离态氮固定在碳上(示踪反应如下),制得的[N=C=N]2-离子可用于合成核酸
的结构单元。阿伏加德罗常数的值为N ,下列说法正确的是( )
A
20atm,550℃,5h
15N +C(石墨)+2LiH=================Li [15NC15N]+H
2 2 2
A. 22.4L15N 含有的中子数为16N
2 A
B. 12gC(石墨)中sp2杂化轨道含有的电子数为6N
A
C. 1mol[N=C=N]2-中含有的π键数为4N
A
D. 生成1mol H 时,总反应转移的电子数为6N
2 A
10.如图为含氮或含硫常见物质间的转化关系,下列说法一定正确的是( )
A. 常温下发生e→c的转化,X均可为单质Fe
B. 图示中的所有转化过程均为氧化还原反应
C. a→c的转化均在点燃条件下发生
D. d和c可在一定条件下反应生成a
11. Si Cl 中的Si原子均通过sp3杂化轨道成键,与NaOH溶液反
5 10
应Si元素均转化成Na SiO 。下列说法不正确的是( )
2 3 ...
A.Si Cl 分子结构可能是 B.Si Cl 与水反应可生成一种强酸
5 10 5 10
C.Si Cl 与NaOH溶液反应会产生H D.Si Cl 沸点低于相同结构的Si Br
5 10 2 5 10 5 10
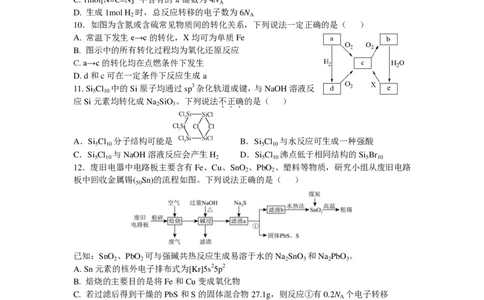
12.废旧电器中电路板主要含有Fe、Cu、SnO 、PbO 、塑料等物质,研究小组从废旧电路
2 2
板中回收金属锡( Sn)的流程如图。下列说法正确的是( )
50
已知:SnO 、PbO 可与强碱共热反应生成易溶于水的Na SnO 和Na PbO 。
2 2 2 3 2 3
A. Sn元素的核外电子排布式为[Kr]5s25p2
B. 焙烧的主要目的是将Fe和Cu变成氧化物
C. 若过滤后得到干燥的PbS和S的固体混合物27.1g,则反应①有0.2N 个电子转移
A
高温
D. 过量的焦炭和SnO 反应的方程式为C+SnO =====Sn+CO ↑
2 2 2
13.科学家发现某些生物酶体系可以促进H+ 和 e-的转移(如a、b和c),能将海洋中的NO转
2
化为N 进入大气层,反应过程如图所示。下列说法正确的是( )
2
A.过程Ⅰ中NO -发生氧化反应
2
B.a和b中转移的e-数目相等
C.过程Ⅱ中参与反应的n(NO):n(NH)=1:4
4
D.过程Ⅰ→Ⅲ的总反应为NO+NH=N +2H O
2 4 2 2
14. 我国科研团队研发的强酸单液流电池通过多电
子转移,提高了电池的安全性和能量密度,其工作原理如图所示。下列说法错误的是
A. 放电时,电极N的电势高
B. 放电时,每消耗0.07molCd,右室有0.01molBr-生成
C. 充电时,H+向电极M区移动,阴极区pH减小
D. 充电时,阳极区存在反应:2IBr-10e-+6H O=Br +2IO-+12H+
2 2 3
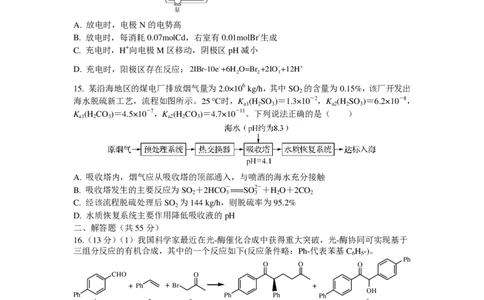
15. 某沿海地区的煤电厂排放烟气量为2.0×106 kg/h,其中SO 的含量为0.15%,该厂开发出
2
海水脱硫新工艺,流程如图所示。25 ℃时,K (H SO )=1.3×10-2,K (H SO )=6.2×10-8,
a1 2 3 a2 2 3
K (H CO )=4.5×10-7,K (H CO )=4.7×10-11。下列说法正确的是( )
a1 2 3 a2 2 3
A. 吸收塔内,烟气应从吸收塔的顶部通入,与喷洒的海水充分接触
B. 吸收塔发生的主要反应为SO +2HCO-===SO2-+H O+2CO
2 3 3 2 2
C. 经该流程脱硫处理后SO 为144 kg/h,则脱硫率为95.2%
2
D. 水质恢复系统主要作用降低吸收液的pH
二、解答题(共55分)
16.(13分)(1)我国科学家最近在光-酶催化合成中获得重大突破,光-酶协同可实现基于
三组分反应的有机合成,其中的一个反应如下(反应条件略:Ph-代表苯基C H -)。
6 5
Ph
O O O
CHO O
+ Ph +Br +
OH
Ph Ph Ph Ph
1a 2a 3a 4a 5a
溴代丙酮 (主产物) (副产物)
下列说法正确的有_______。
A.在1a、2a和3a生成4a的过程中,有π键断裂与σ键形成
B.在4a分子中,存在手性碳原子,并有20个碳原子采取sp2杂化
C.在5a分子中,有大π键,可存在分子内氢键,但不存在手性碳原子
(2)水分子的VSEPR模型与其空间结构模型不同,原因是_______
(3)三种氮氧化物的结构如下所示:分子的极性:N O N O(填“>”或“<”,下同),NNO的键角:a b,熔点:
2 4 2
N O N O 。
2 3 2 4
(4)[BMIM]+BF-(见图)是MnO 晶型转变的诱导剂。BF-的空间构型为 ;[BMIM]+
4 x 4
中咪唑环存在Π 6 大Π键,则N原子采取的轨道杂化方式为 。
5
(5)MnO 可作HMF转化为FDCA的催化剂(见下图)。FDCA的熔点远大于HMF,除相
x
对分子质量存在差异外,另一重要原因是 。
17.(14 分)现有 A、B、C、D、E、F、G、H 八种元素,均为前四周期元素,它们的原
子序数依次增大。 A 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素;B 元
素是形成化合物种类最多的元素之一;C 元素基态原子的核外 p 电子数比 s电子数少 1;D
元素基态原子的核外p轨道中有两个未成对电子;E元素的气态基态原子的第一至第四电离
能分别是I =738 kJ/mol,I =1451 kJ/mol,I =7733 kJ/mol,I =10540 kJ/mol;F元素的主
1 2 3 4
族序数与周期数的差为4;G元素是前四周期中电负性最小的元素;H元素位于元素周期表
中的第八纵行。
(1)C A 的电子式为__________。
2 4
(2)将 E 的基态原子最外层轨道表示式补充完整: ,该元素原子的 I 远远
3
大于 I ,其原因是_____________________________________________。
2
(3)B元素的原子核外共有______种不同运动状态的电子,有 种不同空间运动状态
的电子。
(4)B、C、D 元素的电负性由大到小排序 (用元素符号表示)
(5)D、E、F 三种元素的简单离子半径由大到小的顺序是__________ (用离子符号表示)。
(6)用惰性电极电解EF 的水溶液的离子方程式 。
2
(7)H位于元素周期表中________区(按电子排布分区),在第 周期第 族,其基
态原子的价电子排布式为_________________,实验室用一种黄色溶液检验H 2+时产生蓝色
沉淀,该反应的离子方程式为 。
18.(14分,每空2分)碘化钠具有强还原性,可用于医学和摄影。实验室制备NaI的基本
步骤为:
①检查装置气密性:关闭K,将仪器B右侧的导管伸入水中,用手捂住三颈烧瓶,导管口
有气泡冒出,松手后, ,则装置气密性良好,添加药品;
②向三颈烧瓶中滴入30%NaOH溶液,发生反应:3I 6NaOH5NaINaIO 3H O;
2 3 2③打开K,三颈烧瓶内有黄色S产生;
④关闭K,向三颈烧瓶中加入稀硫酸,水浴加热,使H S气体充分逸出;
2
⑤把三颈烧瓶中的混合液倒入烧杯中,加入足量碳酸钡除去稀硫酸,再经过一系列操作得到
NaI成品。回答下列问题:
(已知:FeS2H H SFe2,H S为有毒气体)
2 2
(1)补充步骤①的实验现象 ;B中盛放稀硫酸和30%
NaOH溶液的漏斗上连通管的作用为 。
(2)C装置的作用为 。
(3)步骤③中生成淡黄色沉淀的离子方程式为 。
(4)步骤⑤中的“一系列操作”包括 、合并滤液和洗涤液、隔绝空气蒸发结
晶等操作,其中隔绝空气的目的是 。
(5)在三颈烧瓶中加入5.08 g碘单质,最终得到产品的质量为5.28 g。则反应的产率为 。
19.(14分,每空2分)以钛铁矿(主要成分为FeTiO ,含有少量Fe O SiO )为主要原料制
3 2 3、 2
取TiN和水处理剂聚合氯化铁Fe (OH) Cl 的工艺流程如图。
2 a 6a m
已知:i.“酸浸1”所得滤液中阳离子主要有TiO2、Fe2、Fe3、H。
ii.室温下,TiO2(aq)2H O(l) TiO(OH) (s)2H(aq)的化学平衡常数K 10;该条件下,
2 2
Fe2、Fe3开始沉淀的pH分别为6.3、1.8。回答下列问题:
(1)提高钛铁矿的酸浸速率除适当升温和适当增大硫酸浓度外,还可以采取的措施有
(写2条)。
(2)FeTiO 溶于稀硫酸的离子方程式为 。
3
(3)室温下,当“沉钛”阶段上层清液中的c TiO2 1.0105molL1时,上层清液的pH
为 ;“氧化”时双氧水实际消耗量远大于理论消耗量,其原因为 。
(4)“水解聚合”生成Fe (OH) Cl 的化学方程式为 。
2 a 6a m(5)TiN具有高硬度、耐磨损、化学稳定性好等特性,在工具涂层、切削工具应用广泛。
已知生成物气体X中有2种成分,其中一种是N ,则制备TiN的反应中,氧化剂与还原剂
2
物质的量之比为 ;该流程中,能循环利用的物质是 (填化学式)。