文档内容
惠州市实验中学 2026 届高三 12 月阶段性检测
化 学
可能用到的相对原子质量:H—1 C—12 O—16 Fe—56 Co—59 Ni—59
一、选择题(本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每
小题4分。在每小题列出的四个选项中,只有一项符合题目要求)
1.历史文物见证中华文化的源远流长。下列历史文物主要由硅酸盐材料制成的是
A.贾湖骨 C.西汉直裾素纱襌 D.三星堆遗址出土的玉
B.太阳神鸟金饰
笛 衣 璋
2.吸烟有害健康,烟草的焦油中含有一种强烈的致癌物苯并芘,结构简式如图,下列关于
该物质说法正确的是
A.易溶于水 B.共有10个氢原子
C.C-H键是极性共价键 D.不能发生取代反应
3.现代科技,增强国力,增进民生福祉。下列说法正确的是
A.“嫦娥五号”采回的月壤中的3He与地球上的2He互为同位素
B.无液氦亚3 K低温扫描探针显微镜仅使用少量氦气,He是第ⅠA族元素
C.“人造太阳”是全球首个聚变发电装置,原料1 mol重水(DO)质量为18 g
2
D.AG600“鲲龙”是大型灭火/水上救援水陆两栖飞机,水的电子式为H︰O︰H
4.劳动创造美好生活。下列劳动项目与所述化学知识没有关联的是
选项 劳动项目 化学知识
A 农业上用波尔多液防治农作物病害 Cu2+会使蛋白质变性
B 用KSCN溶液检验菠菜中是否含Fe3+ Fe3++3SCN-=Fe(SCN)
3
C 使用明矾处理污水 Al(OH) 胶体具有吸附性
3
D 擦干已洗净铁锅表面的水,以防生锈 铁与水蒸气反应生成Fe O
3 4
5.现代电子设备中常用到多种材料。下列说法错误的是
A. 制作某些塑料外壳的聚苯乙烯,其单体是
B. 电脑CPU芯片通常以高纯单晶硅为基础材料,单晶硅属于分子晶体
C. 手机中的锂离子电池放电时,将化学能转化为电能
D. 印刷电路板(PCB)常用FeCl 溶液腐蚀铜箔,该过程发生了化学变化
3
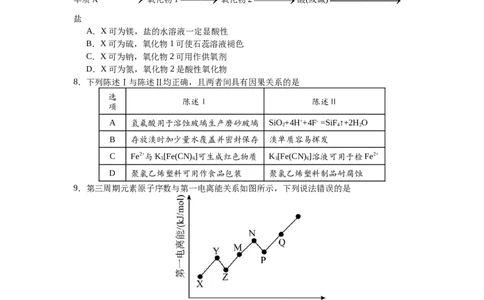
6.用下列装置进行实验,能达到实验目的的是A.制备氢氧化铁胶 B.测定氯水的pH C.萃取振荡时放 D.证明乙炔可使溴
体 气 水褪色
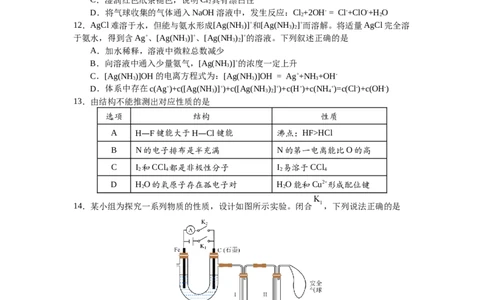
7.能满足下列物质间直接转化关系,且推理成立的是
单质X 氧化物1 氧化物2 酸(或碱)
盐
A.X可为镁,盐的水溶液一定显酸性
B.X可为硫,氧化物1可使石蕊溶液褪色
C.X可为钠,氧化物2可用作供氧剂
D.X可为氮,氧化物2是酸性氧化物
8.下列陈述Ⅰ与陈述Ⅱ均正确,且两者间具有因果关系的是
选
陈述Ⅰ 陈述Ⅱ
项
A 氢氟酸用于溶蚀玻璃生产磨砂玻璃 SiO+4H++4F- =SiF↑+2H O
2 4 2
B 存放溴时加少量水覆盖并密封保存 溴单质容易挥发
C Fe2+与K[Fe(CN) ]可生成红色物质 K[Fe(CN) ]溶液可用于检Fe2+
3 6 3 6
D 聚氯乙烯塑料可用作食品包装 聚氯乙烯塑料制品耐腐蚀
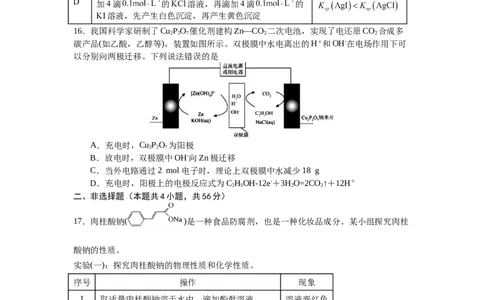
9.第三周期元素原子序数与第一电离能关系如图所示,下列说法错误的是
A.气态氢化物稳定性:N
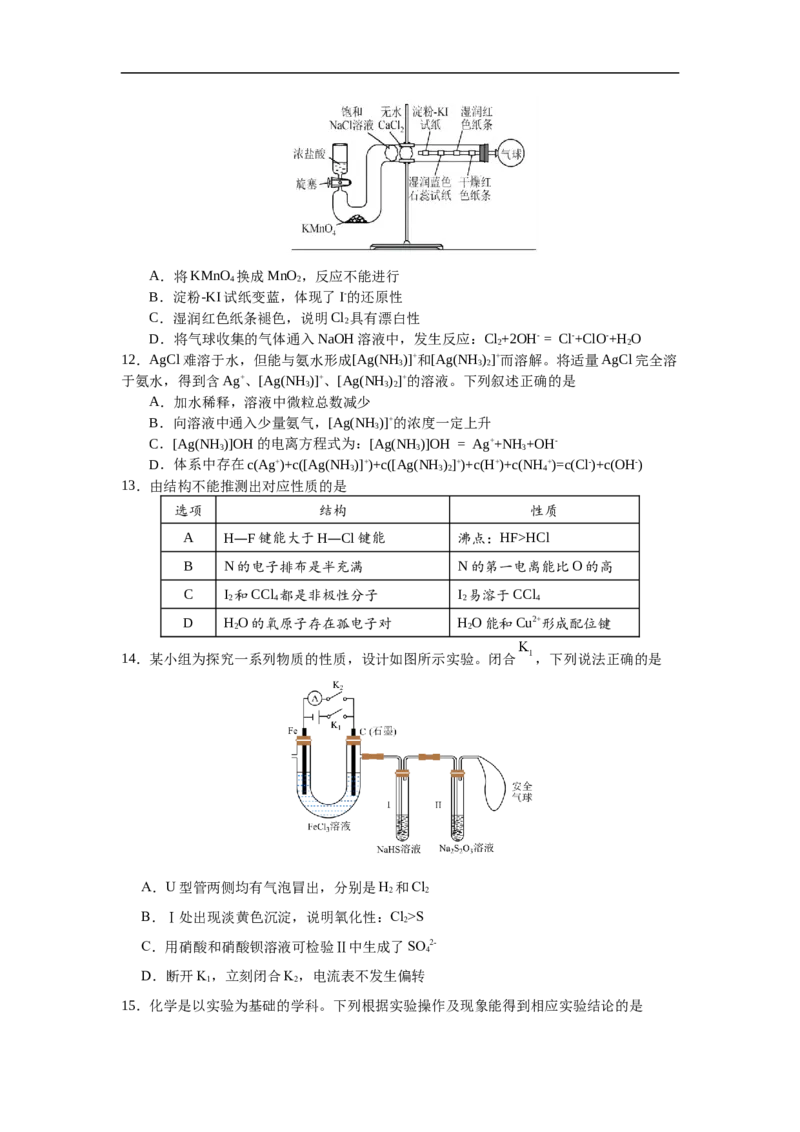
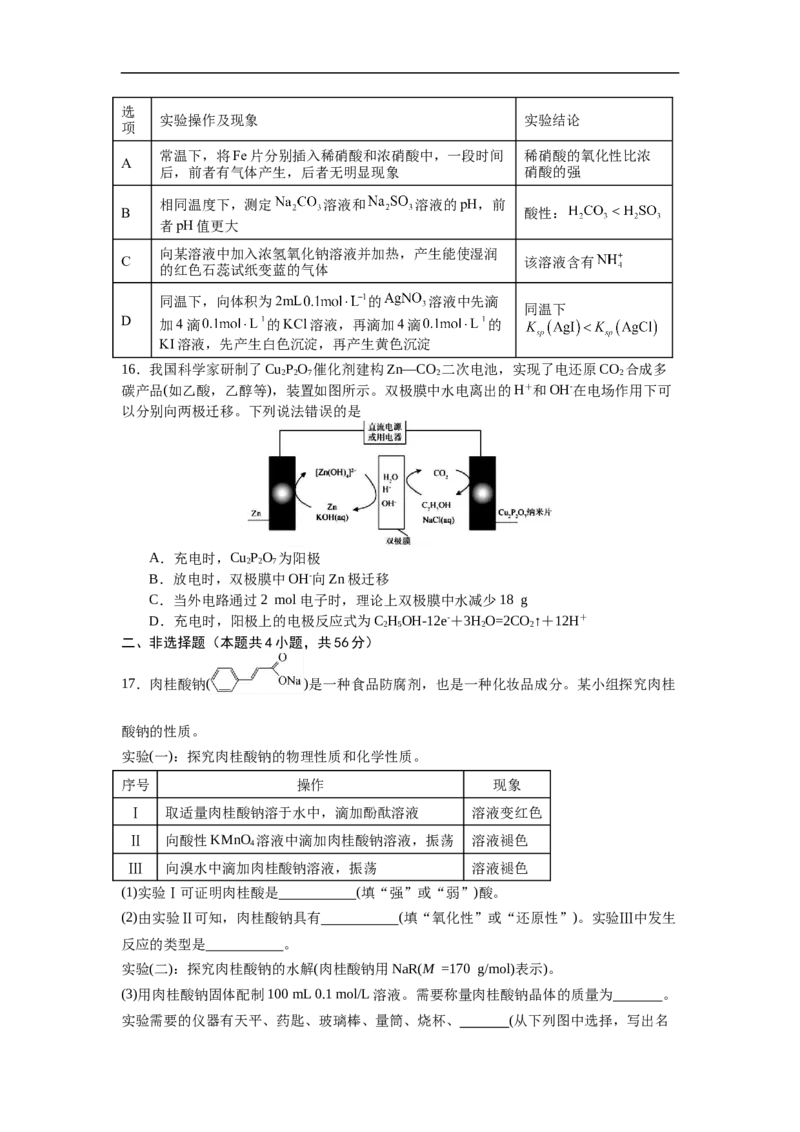
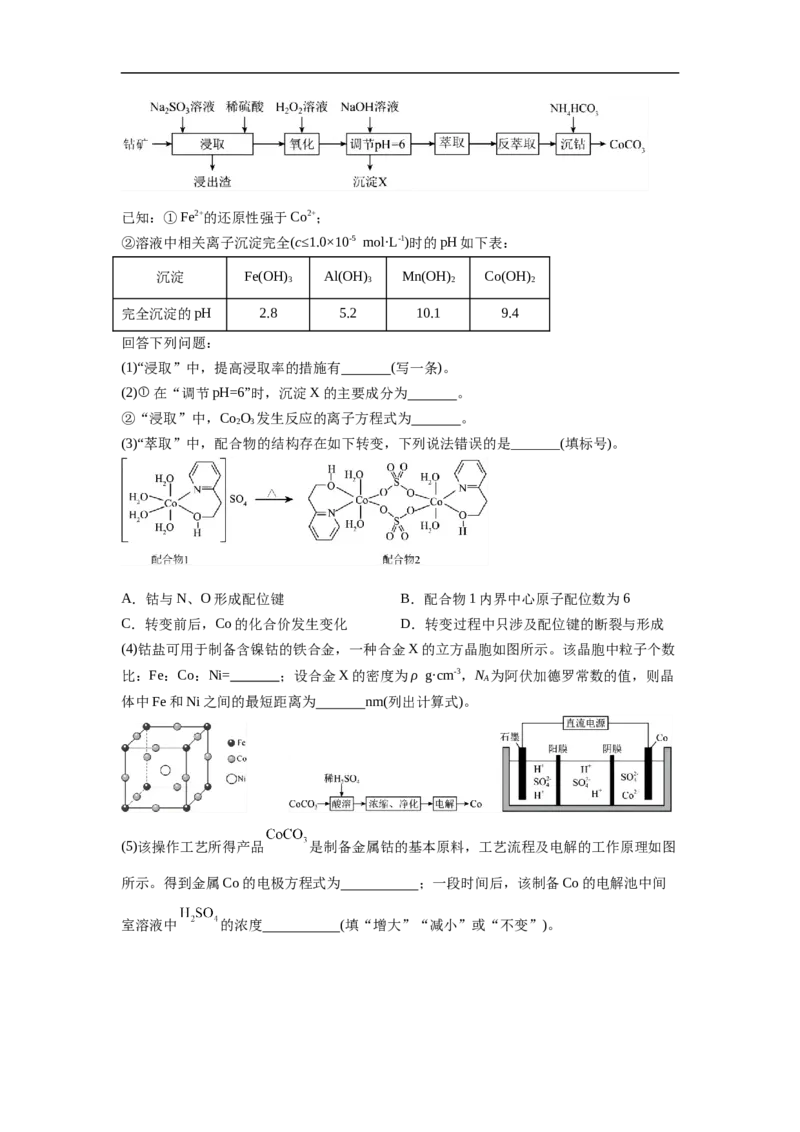
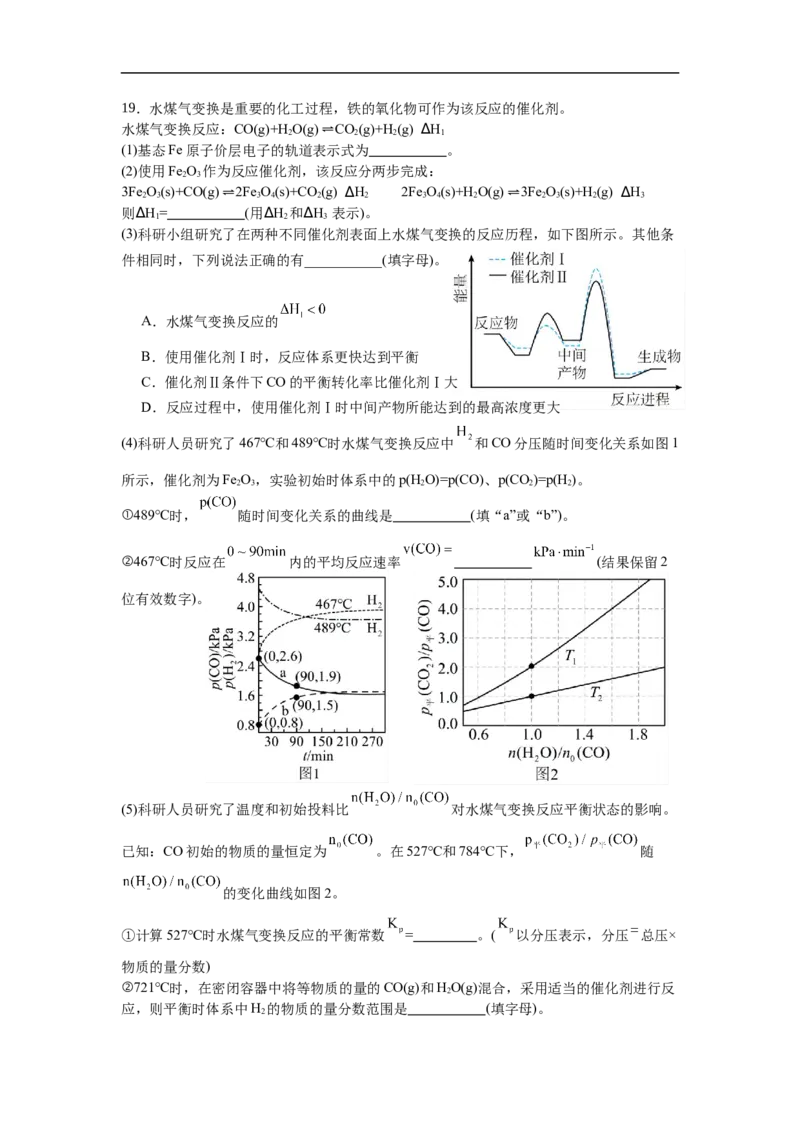
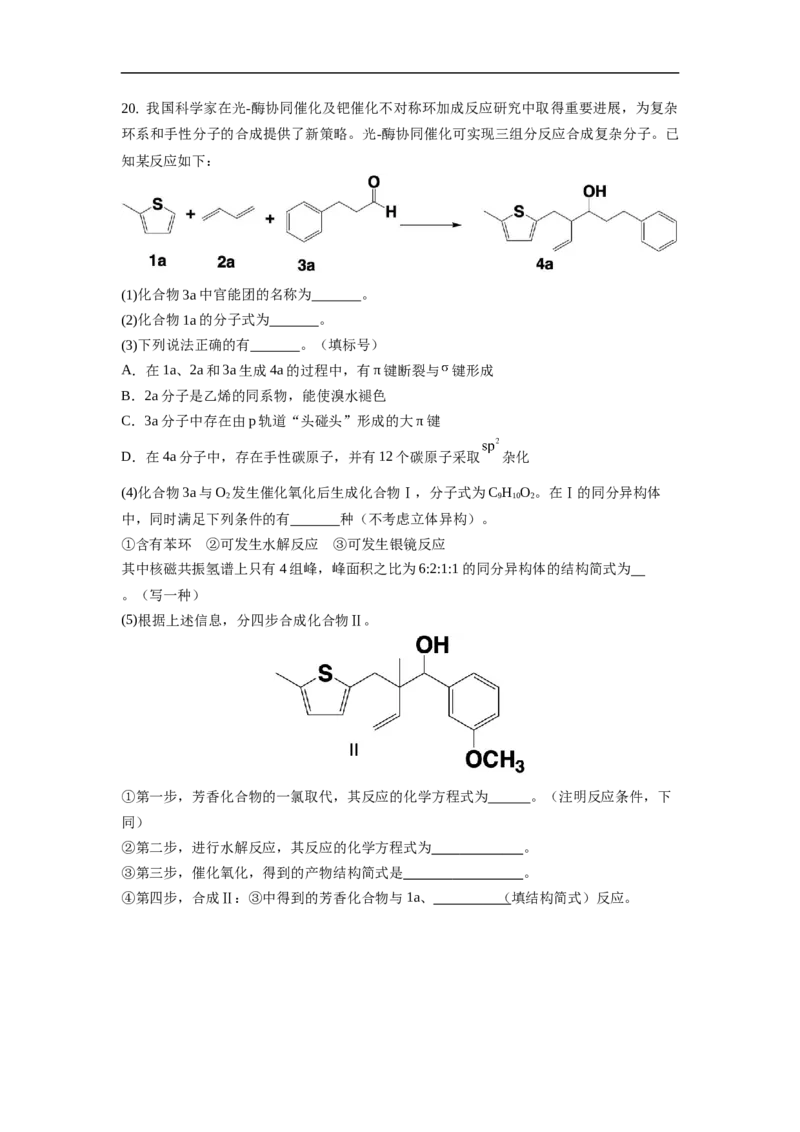
HCl B N的电子排布是半充满 N的第一电离能比O的高 C I 和CCl 都是非极性分子 I 易溶于CCl 2 4 2 4 D HO的氧原子存在孤电子对 HO能和Cu2+形成配位键 2 2 14.某小组为探究一系列物质的性质,设计如图所示实验。闭合 ,下列说法正确的是 A.U型管两侧均有气泡冒出,分别是H 和Cl 2 2 B.Ⅰ处出现淡黄色沉淀,说明氧化性:Cl>S 2 C.用硝酸和硝酸钡溶液可检验Ⅱ中生成了SO 2- 4 D.断开K,立刻闭合K,电流表不发生偏转 1 2 15.化学是以实验为基础的学科。下列根据实验操作及现象能得到相应实验结论的是选 实验操作及现象 实验结论 项 常温下,将Fe片分别插入稀硝酸和浓硝酸中,一段时间 稀硝酸的氧化性比浓 A 后,前者有气体产生,后者无明显现象 硝酸的强 相同温度下,测定 溶液和 溶液的pH,前 B 酸性: 者pH值更大 向某溶液中加入浓氢氧化钠溶液并加热,产生能使湿润 C 该溶液含有 的红色石蕊试纸变蓝的气体 同温下,向体积为2mL 的 溶液中先滴 同温下 D 加4滴 的KCl溶液,再滴加4滴 的 KI溶液,先产生白色沉淀,再产生黄色沉淀 16.我国科学家研制了Cu PO 催化剂建构Zn—CO 二次电池,实现了电还原CO 合成多 2 2 7 2 2 碳产品(如乙酸,乙醇等),装置如图所示。双极膜中水电离出的H+和OH-在电场作用下可 以分别向两极迁移。下列说法错误的是 A.充电时,Cu PO 为阳极 2 2 7 B.放电时,双极膜中OH-向Zn极迁移 C.当外电路通过2 mol电子时,理论上双极膜中水减少18 g D.充电时,阳极上的电极反应式为C HOH-12e-+3HO=2CO↑+12H+ 2 5 2 2 二、非选择题(本题共4小题,共56分) 17.肉桂酸钠( )是一种食品防腐剂,也是一种化妆品成分。某小组探究肉桂 酸钠的性质。 实验(一):探究肉桂酸钠的物理性质和化学性质。 序号 操作 现象 Ⅰ 取适量肉桂酸钠溶于水中,滴加酚酞溶液 溶液变红色 Ⅱ 向酸性KMnO 溶液中滴加肉桂酸钠溶液,振荡 溶液褪色 4 Ⅲ 向溴水中滴加肉桂酸钠溶液,振荡 溶液褪色 (1)实验Ⅰ可证明肉桂酸是 (填“强”或“弱”)酸。 (2)由实验Ⅱ可知,肉桂酸钠具有 (填“氧化性”或“还原性”)。实验Ⅲ中发生 反应的类型是 。 实验(二):探究肉桂酸钠的水解(肉桂酸钠用NaR(M =170 g/mol)表示)。 (3)用肉桂酸钠固体配制100 mL 0.1 mol/L溶液。需要称量肉桂酸钠晶体的质量为 。 实验需要的仪器有天平、药匙、玻璃棒、量筒、烧杯、 (从下列图中选择,写出名称)。 (4)为了探究外界条件对NaR水解的影响,该小组设计如表所示实验: 序 0.1 mol/LNaR溶液/mL 蒸馏水/mL 温度/℃ 测定pH 号 Ⅰ 10.0 0 25 A 1 Ⅱ 5.0 a 25 A 2 Ⅲ 10.0 0 45 A 3 ①补充数据: 。 ②设计实验Ⅰ、Ⅱ的目的是 。 ③已知NaR水解为吸热反应,甲同学预测:AA ,二者矛盾的主要原 1 3 1 3 因是 。 (5)该小组通过测定不同温度下NaR的水解常数K ,确定温度对NaR水解程度的影响。 h 【查阅资料】 , 为NaR溶液起始浓度。 试剂和仪器:一定浓度的NaR溶液、0.100 0 mol·L-1盐酸、甲基橙溶液、pH计。 【设计实验】测定45℃下NaR的水解常数K ,补充下表中实验。 h 序号 实验 记录的数据 取20.00mLNaR溶液,滴几滴甲基橙溶液,用0.1000 mol/L盐酸 盐酸体积为V Ⅳ 滴定至终点 mL Ⅴ 测定45℃纯水的pH x Ⅵ (补充) y 分别在55℃、65℃下重复上述实验。 【实验处理】 45℃下,K = (用含V、x、y的计算式表示)。 h 【实验结论】K(65℃)>K(55℃)>K(45℃),升高温度,NaR水解程度增大。 h h h 18.钴及其化合物在磁性材料、电池材料、超硬材料及催化剂等领域有广泛应用。工业上 以钴矿[主要成分为CoO、Co O、Co(OH) ,含少量的SiO、Al O、FeO、MnO 等]为原料 2 3 2 2 2 3 2 制取CoCO,的工艺流程如图所示。 3已知:①Fe2+的还原性强于Co2+; ②溶液中相关离子沉淀完全(c≤1.0×10-5 mol·L-1)时的pH如下表: 沉淀 Fe(OH) Al(OH) Mn(OH) Co(OH) 3 3 2 2 完全沉淀的pH 2.8 5.2 10.1 9.4 回答下列问题: (1)“浸取”中,提高浸取率的措施有 (写一条)。 (2)①在“调节pH=6”时,沉淀X的主要成分为 。 ②“浸取”中,Co O 发生反应的离子方程式为 。 2 3 (3)“萃取”中,配合物的结构存在如下转变,下列说法错误的是_______(填标号)。 A.钴与N、O形成配位键 B.配合物1内界中心原子配位数为6 C.转变前后,Co的化合价发生变化 D.转变过程中只涉及配位键的断裂与形成 (4)钴盐可用于制备含镍钴的铁合金,一种合金X的立方晶胞如图所示。该晶胞中粒子个数 比:Fe:Co:Ni= ;设合金X的密度为ρ g·cm-3,N 为阿伏加德罗常数的值,则晶 A 体中Fe和Ni之间的最短距离为 nm(列出计算式)。 (5)该操作工艺所得产品 是制备金属钴的基本原料,工艺流程及电解的工作原理如图 所示。得到金属Co的电极方程式为 ;一段时间后,该制备Co的电解池中间 室溶液中 的浓度 (填“增大”“减小”或“不变”)。19.水煤气变换是重要的化工过程,铁的氧化物可作为该反应的催化剂。 水煤气变换反应:CO(g)+H 2 O(g)⇌CO 2 (g)+H 2 (g) ∆H 1 (1)基态Fe原子价层电子的轨道表示式为 。 (2)使用Fe O 作为反应催化剂,该反应分两步完成: 2 3 3Fe 2 O 3 (s)+CO(g)⇌2Fe 3 O 4 (s)+CO 2 (g) ∆H 2 2Fe 3 O 4 (s)+H 2 O(g)⇌3Fe 2 O 3 (s)+H 2 (g) ∆H 3 则∆H= (用∆H 和∆H 表示)。 1 2 3 (3)科研小组研究了在两种不同催化剂表面上水煤气变换的反应历程,如下图所示。其他条 件相同时,下列说法正确的有___________(填字母)。 A.水煤气变换反应的 B.使用催化剂Ⅰ时,反应体系更快达到平衡 C.催化剂Ⅱ条件下CO的平衡转化率比催化剂Ⅰ大 D.反应过程中,使用催化剂Ⅰ时中间产物所能达到的最高浓度更大 (4)科研人员研究了467℃和489℃时水煤气变换反应中 和CO分压随时间变化关系如图1 所示,催化剂为Fe O,实验初始时体系中的p(H O)=p(CO)、p(CO)=p(H)。 2 3 2 2 2 ①489℃时, 随时间变化关系的曲线是 (填“a”或“b”)。 ②467℃时反应在 内的平均反应速率 (结果保留2 位有效数字)。 (5)科研人员研究了温度和初始投料比 对水煤气变换反应平衡状态的影响。 已知:CO初始的物质的量恒定为 。在527℃和784℃下, 随 的变化曲线如图2。 ①计算527℃时水煤气变换反应的平衡常数 = 。( 以分压表示,分压 总压× 物质的量分数) ②721℃时,在密闭容器中将等物质的量的CO(g)和HO(g)混合,采用适当的催化剂进行反 2 应,则平衡时体系中H 的物质的量分数范围是 (填字母)。 2A. B. C. D.20. 我国科学家在光-酶协同催化及钯催化不对称环加成反应研究中取得重要进展,为复杂 环系和手性分子的合成提供了新策略。光-酶协同催化可实现三组分反应合成复杂分子。已 知某反应如下: (1)化合物3a中官能团的名称为 。 (2)化合物1a的分子式为 。 (3)下列说法正确的有 。(填标号) A.在1a、2a和3a生成4a的过程中,有π键断裂与 键形成 B.2a分子是乙烯的同系物,能使溴水褪色 C.3a分子中存在由p轨道“头碰头”形成的大π键 D.在4a分子中,存在手性碳原子,并有12个碳原子采取 杂化 (4)化合物3a与O 发生催化氧化后生成化合物Ⅰ,分子式为C H O。在Ⅰ的同分异构体 2 9 10 2 中,同时满足下列条件的有 种(不考虑立体异构)。 ①含有苯环 ②可发生水解反应 ③可发生银镜反应 其中核磁共振氢谱上只有4组峰,峰面积之比为6:2:1:1的同分异构体的结构简式为 。(写一种) (5)根据上述信息,分四步合成化合物Ⅱ。 ①第一步,芳香化合物的一氯取代,其反应的化学方程式为 。(注明反应条件,下 同) ②第二步,进行水解反应,其反应的化学方程式为 。 ③第三步,催化氧化,得到的产物结构简式是 。 ④第四步,合成Ⅱ:③中得到的芳香化合物与1a、 ( 填结构简式)反应。