文档内容
{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}濮阳外国语学校 2023 级高三上学期第二次质量检测
化学试题答案
题号 1 2 3 4 5 6 7 8 9 10
答案 C B D A A D D C A C
题号 11 12 13 14
答案 D B B D
1. 【答案】C
【详解】A.食品加工时,可适当添加食品添加剂和防腐剂等,如苯甲酸钠,故A错误;B.废
旧电池中含有重金属等金属离子,会造成土壤污染,水体污染等,故B错误;C.天然气主
要成分为甲烷,不完全燃烧会产生一氧化碳等有毒气体,故C正确;
D.含磷洗涤剂的排放,使水中磷过多,造成水中藻类疯长,消耗水中溶解的氧,水体变浑
浊,故D错误;故选C。
2.【答案】B
【详解】A.Cl 和NaOH溶液反应产生NaCl、NaClO、H2O,除了Cl 和H O不能拆写其
2 2 2
余均可拆写为离子,A 项正确;B.食醋为弱酸不能拆写为离子,反应为
2CH COOH+CaCO =Ca2++2CH COO-+CO +H O,B 项错误;C.FeCl 将 Cu 氧化为 CuCl
3 3 3 2 2 3 2
而自身被还原为FeCl ,反应为2Fe3++Cu=2Fe2++Cu2+,C项正确;D.Na S将Hg2+转化为沉
2 2
淀除去,反应为Hg2++S2−=HgS↓,D项正确;故选B。
3.【答案】D
1.7g
【详解】A.1.7gH O 的物质的量为 =0.05mol,则含有氧原子数为0.1N ,A不正确;
2 2 A
34g/mol
标准状况下,11.2LCl 的物质的量为0.5mol,通入水中后只有一部分Cl 与水反应生成H+、
2 2
Cl-和HClO,所以溶液中氯离子数小于0.5N
A
,B不正确;5.6g铁粉与0.1L1molL1的HCl
的溶液充分反应,产生的氢气的分子数目为0.05N ,C错误;60gSiO 的物质的量为1mol 其
A 2
中 Si-O 键数目为4N ,D正确
A
4.【答案】A
【详解】A.由分析可知,E为氨气、G为氮气、Q为一氧化氮、R为二氧化氮、T为硝酸,
五种物质中氮元素的化合价分别为+3价、0价、+2价、+4价、+5价,氮元素化合价依次升
高,故A正确;B.氨分子不能电离出自由移动的离子,属于非电解质,故B错误;C.一
氧化氮能与氧气反应生成二氧化氮,则一氧化氮不能用排空气法收集,故C错误;D.铜与
浓硝酸反应生成二氧化氮,不能生成一氧化氮,故D错误;
答案第1页,共4页
{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}5.【答案】A
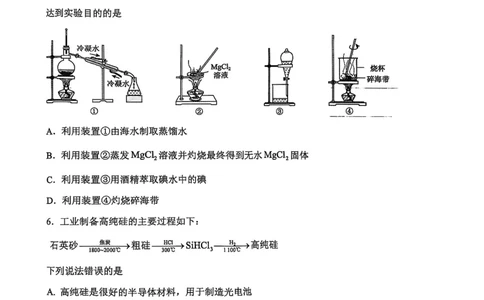
【详解】A.海水中水的沸点较盐沸点低,可选图中蒸馏装置制取蒸馏水,A正确;B.蒸
发MgCl 溶液并灼烧最终得到MgO固体,B错误;C.萃取时,萃取剂不能与溶剂互溶,
2
酒精能与水以任意比例互溶,不能用于萃取碘水中的碘,C错误;D.灼烧碎海带应在坩埚
中进行,D错误。故选A。
6.【答案】D
【详解】A.高纯硅是很好的半导体材料,用于制造光电池 ,A正确;B.石英砂与焦炭在
高温
1800~2000℃高温下反应生成Si和CO,反应的化学方程式为SiO +2C Si+2CO↑,B正
2
确;C.SiHCl 遇水易发生水解,遇氧气易发生自燃,同时H 与O 在高温下易发生爆炸,
3 2 2
为防止SiHCl 的水解和自燃、H 的爆炸,原料气HCl和H 应充分除水和氧气,C正确;
3 2 2
D.石英砂的主要成分是SiO ,SiO 是共价晶体,不存在单个分子,D不正确;
2 2
7.【答案】D
高温
【详解】A.3Fe+4H O Fe O +4H ,A错误;B.向某溶液中通入Cl ,然后再加入
2 3 4 2 2
KSCN 溶液变红色,不能说明溶液中有Fe2+,可能是Fe3+;C.室温下,Fe遇浓硫酸钝化,
C错误;D高铁酸盐(FeO 2-)可用于饮用水的消毒,由此可推测,高铁酸盐(FeO 2-)具
4 4
有强氧化性
8.【答案】C
9.【答案】A
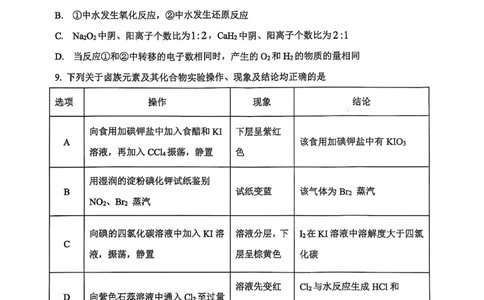
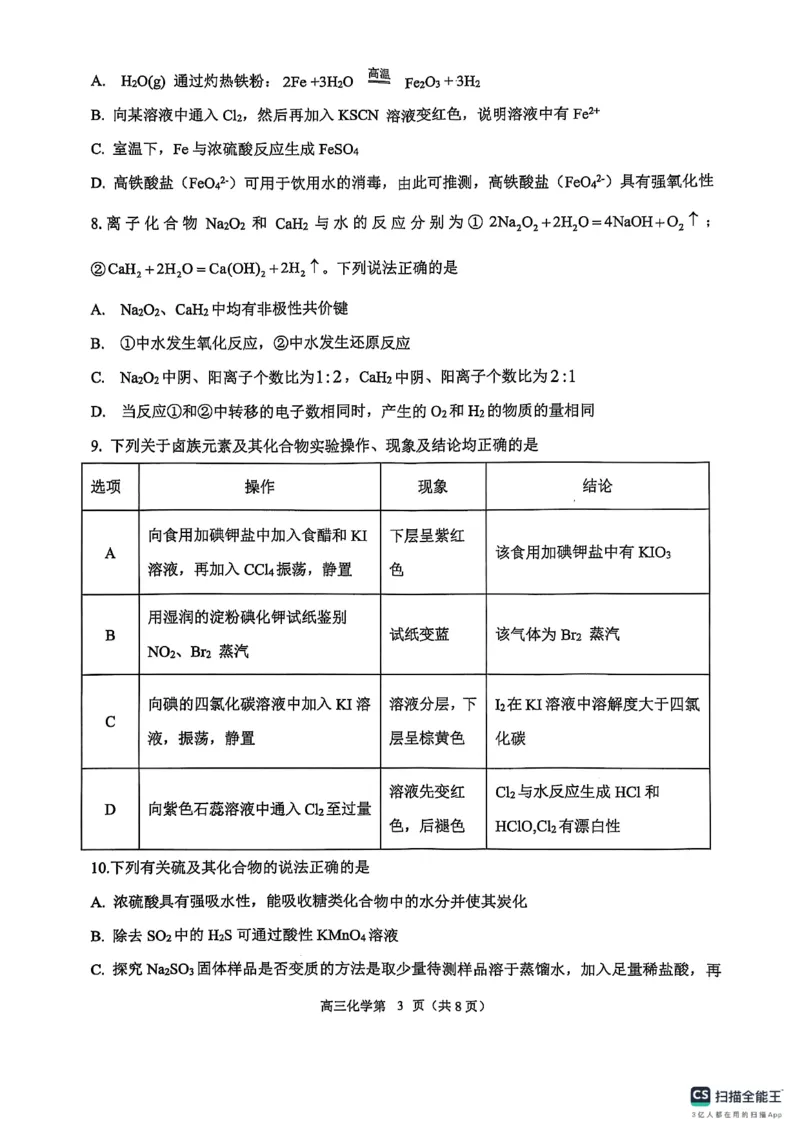
【详解】A.向食用加碘钾盐中加入食醋和KI溶液,再加入CCl 振荡,静置,下层呈紫红色,
4
该使用加碘钾盐中有KIO ,A正确;B.用湿润的淀粉碘化钾试纸鉴别NO 、Br 蒸汽,试纸
3 2 2
变蓝,该气体可能为Br 蒸汽或者NO ;C.四氯化碳密度大于水,溶液分层,上层呈棕黄色,
2 2
C项错误;D.Cl 没有漂白性,HClO有漂白性,D项错误
2
10.【答案】C
【详解】A.浓硫酸使糖类化合物炭化,利用的是浓硫酸的脱水性,A不正确;KMnO 溶液
4
也可以和SO 反应;C.探究Na SO 固体样品是否变质的方法是取少量待测样品溶于蒸馏水,
2 2 3
加入足量稀盐酸,再加入BaCl2 溶液,若有白色沉淀产生,则样品已经变质,C正确
D.过量SO 与Na SO 反应生成NaHSO , 总反应的化学方程式为5SO +2Na S+2H O==3S↓
2 2 3 3 2 2 2
+4NaHSO ,D项错误。
3
答案第2页,共4页
{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}11.【答案】D
【详解】A.图1所示过程①发生的是反应Ⅰ,该过程焓变小于零,是放热反应,过程②是NH
3
的分解,由反应Ⅰ-反应Ⅱ×3可得2NH gN g3H gΔH92.4kJmol1,焓变大于零,
3 2 2
该过程是吸热反应,A正确;B.反应Ⅱ是放热反应,生成物能量大于反应物能量,图2所
示能量变化示意图正确,B 正确;C. .根据盖斯定律,反应Ⅰ-2×反应Ⅱ得
N H
g
N
g
2H
g
ΔH95.4kJmol1,C正确;D.由于反应Ⅰ为放热反应,因此
2 4 2 2
断开3molN H g中的化学键吸收的能量小于形成1molN g和4mol NH g中的化学键
2 4 2 3
释放的能量,D错误
12.【答案】B
13.【答案】B
【详解】A.酸性锌锰干电池,锌筒为负极,石墨电极为正极,故A正确;B.原电池工作
时,阳离子向正极(石墨电极)方向移动,故B错误;C.MnO 发生得电子的还原反应,故C
2
正确;D.锌筒为负极,负极发生失电子的氧化反应Zn-2e- Zn2+,故D正确;
14.【答案】D
【详解】A.浸渣的成分有PbSO 、铜;B. 沉锰条件下物质的氧化性S O 2- >MnO
4 2 8 2
C. 沉锰后的溶液中金属阳离子主要有Fe3+、 Co2+ 、Zn2+;D.沉钴时发生反应的离子方程式
为2Co2++5ClO-+5H O==2Co(OH) ↓+Cl-+4HClO,正确
2 3
15.(16分,每空2分)
1
【答案】(1) ① a ② H g O gH Ol ΔH 286 kJmol1 (2)=
2 2 2 2
(3)-291.9kJ/mol (4) ①< ② -160 (5) HCOO2OH2e=HCOH O H SO
3 2 2 4
【详解】(1)①由题意可知,氢气在氧气中的燃烧反应为反应物总能量大于生成物总能量的
放热反应,则反应的能量变化可以用图a表示;②由2mol氢气与足量氧气充分燃烧生成液
572kJ
态水时放出572kJ热量可知,氢气的燃烧热ΔH 286kJmol1,反应的热化学方
2mol
1
程式为H g O gH Ol ΔH 286kJmol1。
2 2 2 2
(2)相同条件下反应的焓变H只与反应物的总能量和生成物的总能量有关,与反应条件
无关,则同温同压下,氢气和氯气在光照和点燃条件下的焓变H相等。
(3)ΔH 反应物键能总和-生成物键能总和
答案第3页,共4页
{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#} 3154.8kJmol1941.7kJmol1 6283.0kJmol1 291.9kJmol1。
(4)由图可知,等量的MgBr 和MgCl 分解得到单质镁和卤素单质,MgCl 需要吸收的能
2 2 2
量更多,说明其热稳定性更高,所以热稳定性:MgBr MgCl 。由图可知①
2 2
MgsBr gMgBr s ΔH 524kJmol1,②
2 2
MgsI gMgI s ΔH 364kJmol1,结合盖斯定律可知①-②得到
2 2
MgI sBr gMgBr sI g ΔH 160kJmol1。
2 2 2 2
(5)HCOOH碱性燃料电池中,HCOO-发生失去电子的反应生成HCO-,所在电极为负极,
3
电极反应式为HCOO2OH2e=HCOH O,正极Fe3+得电子生成Fe2+,电解质储罐中
3 2
O 氧化Fe2+生成Fe3+,Fe3+循环使用,电解质储罐中O 氧化Fe2+生成Fe3+的离子方程式为
2 2
O +4Fe2++4H+=4Fe3++2H O,结合最终得到K SO 可知物质A为H SO ;
2 2 2 4 2 4
16.(每空2分,共16分)
催化剂、加热
【答案】(1) 球形干燥管 4NH + 6NO 5N + 6H0
3 2 2
(2)不能 NH 与 CaCl 反应
3 2
(3)除去挥发出来的HNO ②④
3
(4) 2NO+3HClO+H O==2NO - +3Cl-+5H+ 溶液pH 越小,溶液中HClO的浓度越大,氧
2 3
化NO的能力越强。
17.(共12分,每空2分)
(1)增大接触面积,提高焙烧效率 (2)SiO、CaSO
2 4
(3) 将Fe2氧化为Fe3 H O 2Fe2 2H 2Fe3 2H O
2 2 2
(4)3.4≤pH <4.7 (5) 蒸发浓缩、冷却结晶
18.(共14分,每空2分)
(1) 四 Ⅷ 3s23p2
(2)SiCl +3H O=H SiO +4HCl
4 2 2 3
850C
(3)焰色反应 (4) 5.9107 6Co(OH)
2
+O
2
2Co
3
O
4
+6H
2
O
(5)4Co O +6Li CO +O =12LiCoO +6CO
3 4 2 3 2 2 2
答案第4页,共4页
{#{QQABZQSUggiIAIJAAQhCAQVyCkGYkBEAACgGQBAUIAABwQFABAA=}#}