文档内容
2024 年 1 月“七省联考”考前化学猜想卷
化学·全解全析
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F19 Na 23 Cl 35.5 Mn 55 Fe 56
Cu 64 Ag 108 Cs 133 Ba 137
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学与生产生活、社会发展息息相关,下列说法不正确的是
A.铬是硬度最高的金属,常添加在不锈钢中以增强其耐腐蚀性
B.飞船返回舱表层材料中的玻璃纤维属于天然有机高分子
C.卡塔尔光伏电站实现了将光能转化为电能,用到的材料主要为硅单质
D.在合金中加入适量稀土金属可改善合金的性能,因而稀土元素又被称为“冶金工业的维生素”
【答案】B
【解析】A.铬是硬度最高的金属,常添加在不锈钢中以增强其耐腐蚀性、硬度,A正确;
B.玻璃纤维属于合成高分子化合物,不属于天然有机高分子化合物,故B错误;
C.硅为常用的半导体材料,卡塔尔光伏电站实现了将光能转化为电能,用到的材料主要为硅单质,故C
正确;
D.在合金中加入适量稀土金属可改善合金的性能,使合金具有各种不同的性能,因而稀土元素又被称为
“冶金工业的维生素”,故D正确;
故选B。
2.下列化学用语表达正确的是
A. 用系统命名法命名为3−甲基丁酸
B.空间填充模型 既可以表示甲烷分子,也可以表示四氯化碳分子
C. 分子中,碳原子与氧原子之间形成的共价键类型为 键
D.基态铍原子最外层电子的电子云轮廓图:
【答案】A【解析】A. 是羧酸,用系统命名法命名为3-甲基丁酸,故A正确;
B. 可以表示甲烷分子,但是不能表示CCl 分子,因为Cl原子的半径比C原子大,与比例模型中
4
的原子大小不符,故B错误;
C.甲醇分子中C原子sp3杂化,O原子sp3杂化,CHOH分子中,碳原子与氧原子之间形成的共价键类型
3
为sp3-sp3σ键,故C错误;
D.基态铍原子电子排布式为1s22s2,最外层电子在s轨道,电子云轮廓是球形的,故D错误;
故选A。
3.金粉溶于过氧化氢-浓盐酸可以安全环保的制备氯金酸( ),其化学方程式为
。设 为阿伏加德罗常数的值,下列说法正确的是
A.消耗1molAu,反应转移的电子数为
B.消耗2molHCl生成的 分子数为
C.消耗85g ,产物中形成的配位键数目为
D.2mol液态水中含有的氢键数目为
【答案】A
【解析】A.由方程式可知,2molAu参与反应,转移电子的物质的量为8mol,因此消耗1molAu,反应转
移的电子数为4N ,A正确;
A
B.由方程式可知,每消耗8molHCl生成1molO ,因此消耗2molHCl生成的O 分子数为0.25N ,B错误;
2 2 A
C.每个H[AuCl ]中含有4个配位键,85gHO 的物质的量为:n= = =2.5mol,由方程式知,
4 2 2
5molH O 反应生成2molH[AuCl ],因此消耗85gHO,产物中形成的配位键数目为4N ,C错误;
2 2 4 2 2 A
D.1mol冰中含有2mol氢键,液态水中的氢键小于冰,因此2mol液态水中含有的氢键数目小于4N ,D
A
错误;
故选A。
4.下列叙述对应的离子方程式正确的是
A.向饱和NaOH溶液中通入过量 析出白色晶体:
B.白色沉淀CuCl溶于 - 溶液得到深蓝色溶液:
C.向 溶液中滴入酸化的 溶液产生白色沉淀:
D.向 溶液中滴入 溶液产生黑色沉淀和气泡:
【答案】D【解析】A.向饱和NaOH溶液中通入过量 析出白色晶体即产生沉淀,故离子方程式为
,A错误;
B.沉淀在离子方程式书写时不能拆,故白色沉淀CuCl溶于 - 溶液得到深蓝色溶液的离子
方程式为 ,B错误;
C.硝酸具有强氧化性,能够将NaHSO 氧化为硫酸钠,硫酸钠与硝酸钡反应生成难溶于酸的硫酸钡,向
3
NaHSO 溶液中滴入酸化的Ba(NO ) 溶液产生白色沉淀的离子方程式为:
3 3 2
,C错误;
D.向KMnO 溶液中滴入HO 溶液产生黑色沉淀(MnO )和气泡(O),根据氧化还原反应配平可得该
4 2 2 2 2
反应的离子方程式为 ,D正确;
故答案为:D。
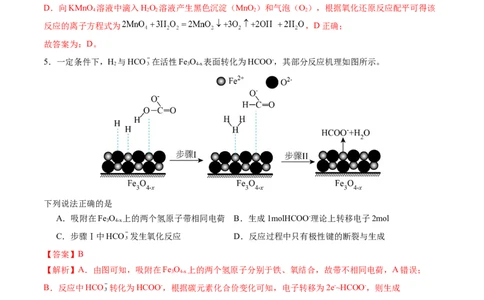
5.一定条件下,H 与HCO 在活性Fe O 表面转化为HCOO-,其部分反应机理如图所示。
2 3 4-x
下列说法正确的是
A.吸附在Fe O 上的两个氢原子带相同电荷 B.生成1molHCOO-理论上转移电子2mol
3 4-x
C.步骤Ⅰ中HCO 发生氧化反应 D.反应过程中只有极性键的断裂与生成
【答案】B
【解析】A.由图可知,吸附在Fe O 上的两个氢原子分别于铁、氧结合,故带不相同电荷,A错误;
3 4-x
B.反应中HCO 转化为HCOO-,根据碳元素化合价变化可知,电子转移为2e-~HCOO-,则生成
1molHCOO-理论上转移电子2mol,B正确;
C.步骤Ⅰ中HCO 失去氧,发生还原反应,C错误;
D.反应过程中氢气和HCO 转化为HCOO-和水,反应中存在氢氢键、氢氧键断裂,氢氧键、碳氢键的生
成,故还存在氢氢非极性键断裂,D错误;
故选B。
6.分子之间可通过空间结构和作用力协同产生某种选择性,从而实现分子识别。下图是一种分子梭,在
链状分子A上有两个不同的识别位点。下列说法错误的是A.分子B含有醚键,属于冠醚,可以与分子A形成超分子
B.在碱性情况下,环状分子B与带有正电荷的位点1的相互作用较强
C.在分子B上引入某些基团后可携带其他离子,通过识别位点实现离子转运
D.通过加入酸、碱或盐,均能实现分子梭在两个不同状态之间的切换
【答案】D
【分析】由题可知,在酸性条件下,A分子中位点2的烷胺基结合H+而带正电荷,与环状分子B的作用力
增强;在碱性条件下,环状分子B与带有正电荷的位点1的相互作用较强。因此,通过加入酸或碱,可以
实现分子梭在两个不同状态之间的切换。
【解析】A.分子B含有醚键,根据B的结构可知B属于冠醚,可以与分子A形成超分子,A正确;
B.根据分析,在碱性条件下,环状分子B与带有正电荷的位点1的相互作用较强,B正确;
C.B属于冠醚,在分子B上引入某些基团后可携带其他离子,通过识别位点实现离子转运,C正确;
D.根据分析,通过加入酸、碱,能实现分子梭在两个不同状态之间的切换,加入盐不一定能使实现分子
梭在两个不同状态之间的切换,D错误;
故选D。
7.电解硫酸钠溶液制取电池正极材料 的前驱体 ,其工作原理如图所示:
下列说法不正确的是
A.a是直流电源的正极,石墨电极发生氧化反应
B.交换膜A是阴离子交换膜,通电一段时间,Ⅰ室pH降低
C.当产生 的 时,标准状况下纯钛电极上至少产生 气体
D.若将纯钛电极直接放入Ⅱ室,则纯钛电极上会有金属与前驱体附着而使产率降低【答案】C
【分析】由图可知,前驱体在III室生成,则II室的金属阳离子进入III室,交换膜B为阳离子交换膜,则
右侧纯钛电极为阴极,电极反应式为2HO+2e-=H +2OH-,OH-与金属阳离子结合得到前驱体,为保持电
2 2
荷守恒,交换膜A为阴离子交换膜,左侧石墨电极为阳极,电极反应式为2HO-4e-=O +4H+,所以电解
2 2
过程实际上是电解水。
【解析】A.由上述分析可知,石墨为阳极,发生氧化反应,则a为电源的正极,故A正确;
B.由分析可知,交换膜A为阴离子交换膜,左侧电极反应式为2HO-4e-=O +4H+,产生H+,故pH降低,
2 2
故B正确;
C.每生成 的 ,就相当于生成0.2mol OH-,由电极反应式2HO+2e-=H +2OH-可
2 2
知,会生成0.1mol H ,在标准状况下的体积为2.24L,故C错误;
2
D.纯钛电极若直接放入II室,会导致接受电子的物质不是水而是金属离子,导致金属单质的生成,附着
在前驱体上导致产率的降低,故D正确;
答案选C。
8.甘草素是从甘草中提炼制成的甜味剂,其结构如图所示。下列说法错误的是
A.该分子具有旋光性 B.分子中至少有5个碳原子共直线
C.可使酸性 溶液褪色 D.1mol甘草素最多可通过加成反应消耗
【答案】B
【解析】A.连接4个不同原子或原子团的碳原子为手性碳原子,甘草素中有1个手性碳原子,手性碳有
旋光性,则该分子具有旋光性,A项正确;
B.甘草素分子结构中含有苯环结构,对角线上的四个原子共线,若碳原子共线,则至少有3个碳原子共
直线,B项错误;
C.甘草素含有酚羟基,能使酸性高锰酸钾溶液褪色,C项正确;
D.甘草素含有两个苯环,一个羰基,1mol甘草素,最多可以通过加成反应消耗7mol氢气,D项正确;
答案选B。
9.短周期主族元素X、Y、Z、W的原子序数依次增大,Y和W位于同主族,一种化合物的结构如图所示。
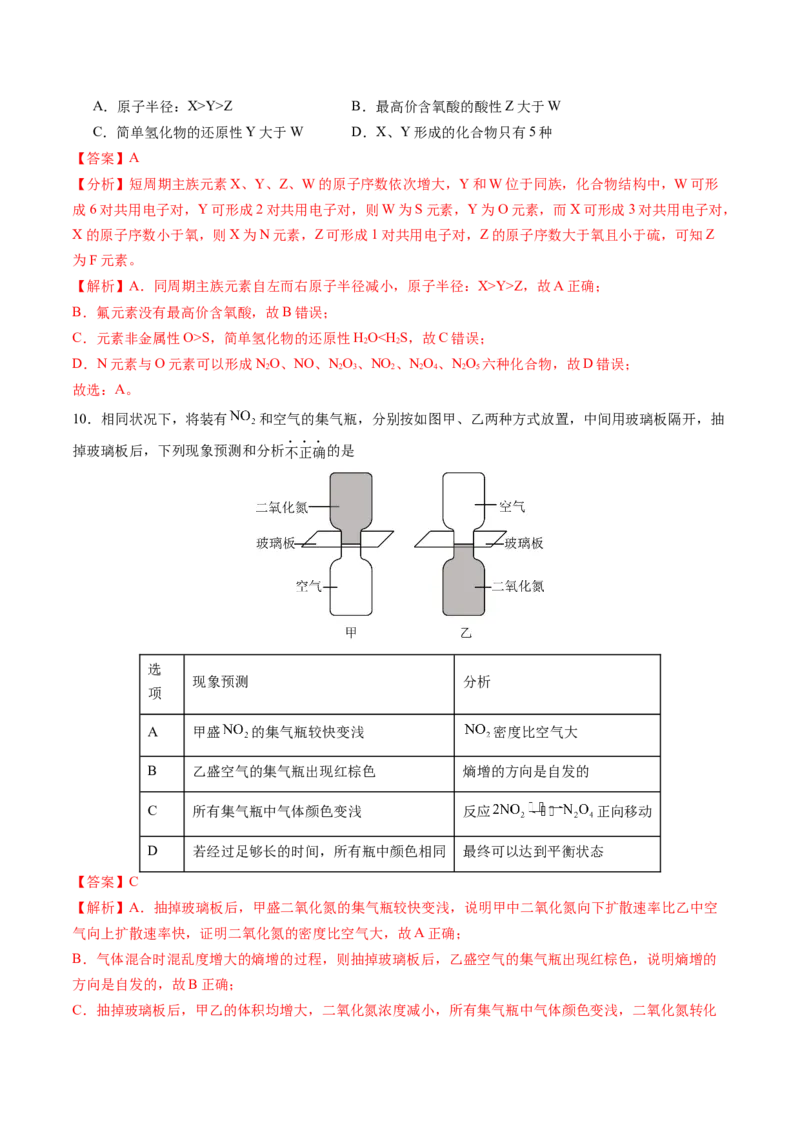
下列叙述正确的是A.原子半径:X>Y>Z B.最高价含氧酸的酸性Z大于W
C.简单氢化物的还原性Y大于W D.X、Y形成的化合物只有5种
【答案】A
【分析】短周期主族元素X、Y、Z、W的原子序数依次增大,Y和W位于同族,化合物结构中,W可形
成6对共用电子对,Y可形成2对共用电子对,则W为S元素,Y为O元素,而X可形成3对共用电子对,
X的原子序数小于氧,则X为N元素,Z可形成1对共用电子对,Z的原子序数大于氧且小于硫,可知Z
为F元素。
【解析】A.同周期主族元素自左而右原子半径减小,原子半径:X>Y>Z,故A正确;
B.氟元素没有最高价含氧酸,故B错误;
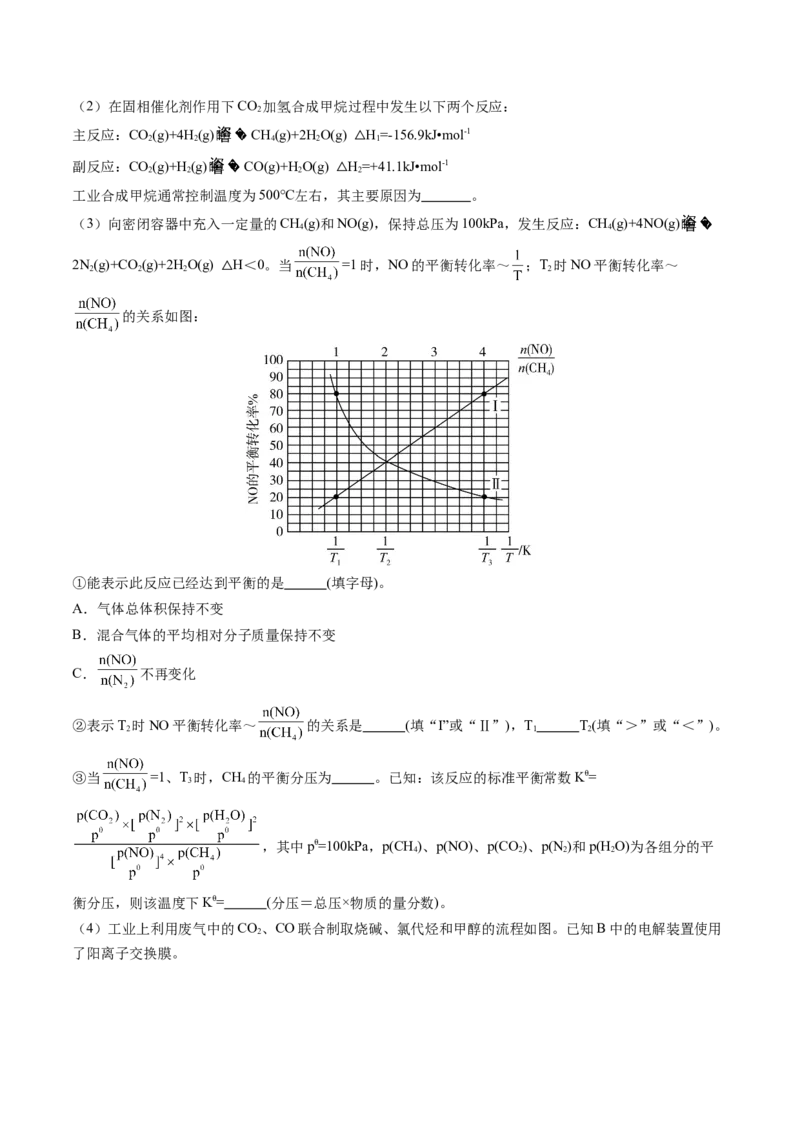
C.元素非金属性O>S,简单氢化物的还原性HOT;
1 2
③当 =1、T 时,因曲线I是表示当 =1时,NO的平衡转化率~ 的图像,由曲线I可看出
3在T 时NO平衡转化率为80%,列三段式:
3
CH 的平衡分压为100kPa kPa,该温度下Kθ=
4
;
(4)B装置电解饱和食盐水生成氢气、氯气、氢氧化钠,总反应的离子方程式为2HO+2Cl-
2
H↑+2OH-+Cl↑。
2 2
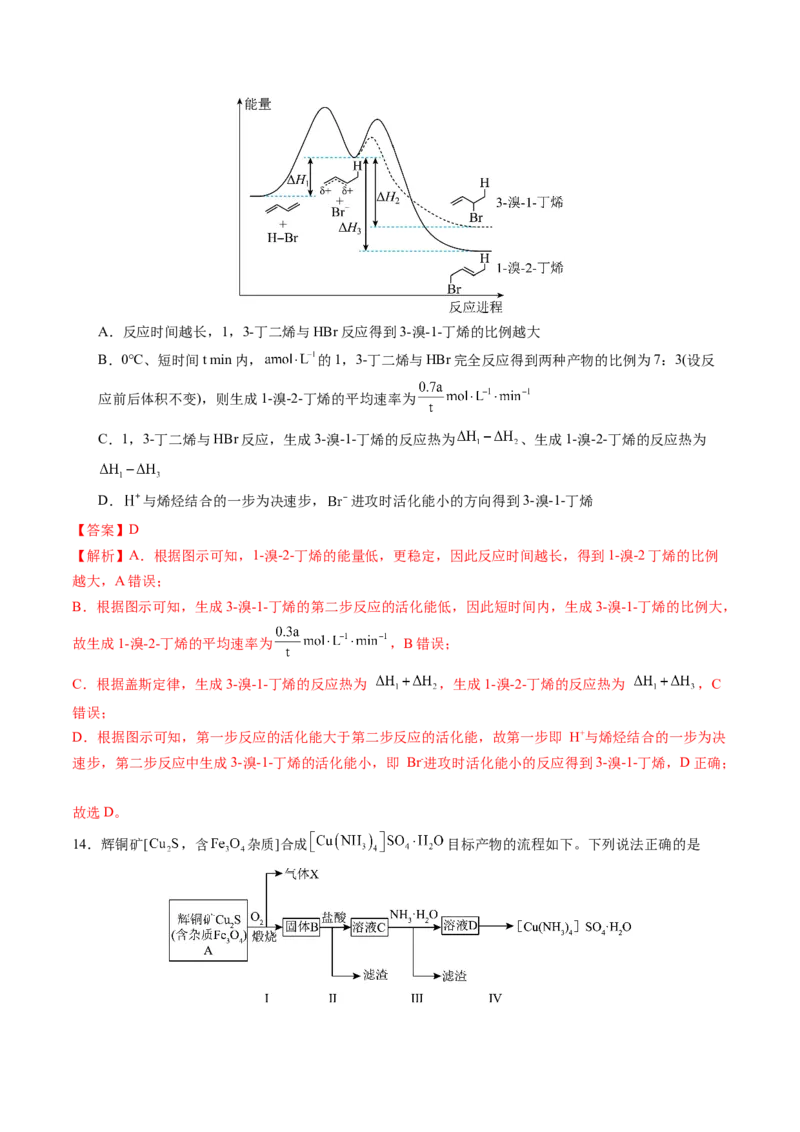
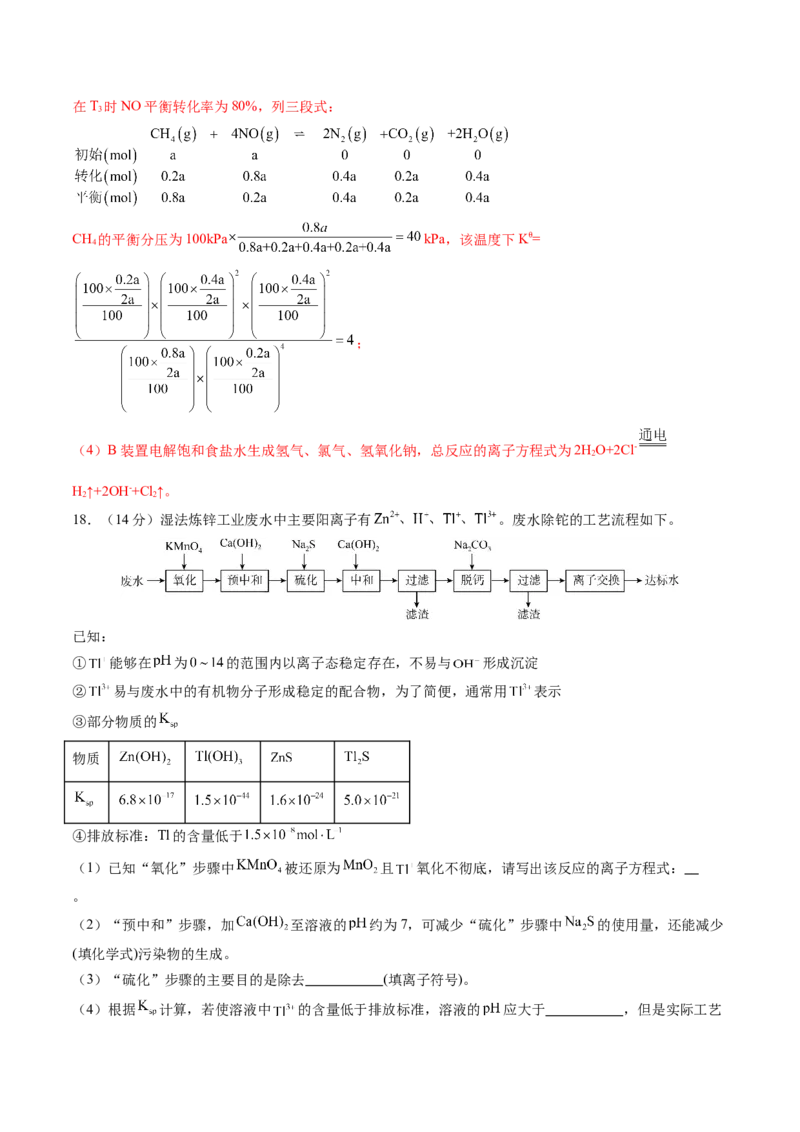
18.(14分)湿法炼锌工业废水中主要阳离子有 。废水除铊的工艺流程如下。
已知:
① 能够在 为 的范围内以离子态稳定存在,不易与 形成沉淀
② 易与废水中的有机物分子形成稳定的配合物,为了简便,通常用 表示
③部分物质的
物质
④排放标准:Tl的含量低于
(1)已知“氧化”步骤中 被还原为 且 氧化不彻底,请写出该反应的离子方程式:
。
(2)“预中和”步骤,加 至溶液的 约为7,可减少“硫化”步骤中 的使用量,还能减少
(填化学式)污染物的生成。
(3)“硫化”步骤的主要目的是除去 (填离子符号)。
(4)根据 计算,若使溶液中 的含量低于排放标准,溶液的 应大于 ,但是实际工艺流程需在“中和”步骤加 至溶液的 约为9,此时仍只有 左右的铊离子能得到去除,其可能
原因是 。
(5)“脱钙”步骤的目的是 。
(6)“离子交换”步骤中可用普鲁士蓝{ }(其摩尔质量为 )中的 与残
余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的 如下[ 未标出,占据四个互不
相邻的小立方体(晶胞的 部分)的体心]。若该晶体的密度为 ,则 和 的最短距离为
(设 为阿伏伽德罗常数的值)。
【答案】(每空2分)(1) (2)HS
2
(3)Zn2+和Tl+ (4)2 第一步氧化时 氧化不彻底, 也会溶解部分离子在溶液中
(5)除去加入的钙离子 (6)
【分析】废水经过高锰酸钾氧化后, 被氧化 ,加入氢氧化钙进行预中和,中和废水中所含H+调节
溶液pH,为下一步硫化做准备,加入硫化钠后Zn2+和Tl+生成 沉淀和 沉淀,继续加入氢氧化钙使
Zn2+和 沉淀完全后过滤,加入碳酸钠,与滤液中的钙离子反应生成碳酸钙沉淀,过滤,滤液经过离子
交换进一步除去溶液中残余铊离子,达到达标水。
【解析】(1)根据所给信息 被还原为 , 被氧化 ,可得该反应的离子方程式为
;
(2)因为溶液中含有氢离子,与硫化步骤中要加入的硫离子会反应生成硫化氢有毒气体,所以要加
至溶液的 约为7;
(3)硫化钠中的硫离子和Zn2+和Tl+生成 沉淀和 沉淀;
(4)根据 , 的排放标准为 ,则, ,所以pH为2;“中和”步骤加 至溶液的
约为9,此时仍只有 左右的铊离子能得到去除,其可能原因是第一步氧化时 氧化不彻底, 也
会溶解部分离子在溶液中;
(5)加入碳酸钠,与滤液中的钙离子反应生成碳酸钙沉淀,从而除去前面步骤中引入的钙离子;
(6)设 和 的最短距离为a,根据已知条件晶体的密度为 ,普鲁士蓝摩尔质量为 ,
从晶胞的 部分图示结构可知 和 的最短距离为晶胞参数的 ,由图示可知 和 分别位于立
方体的四个顶点,而 位于棱的中点,故该单元中含有的 数和 数相等,都为 , 的
个数为 ,根据电荷守恒可知 数为 ,因此该单元的摩尔质量为 ,则有 ,
那么 。
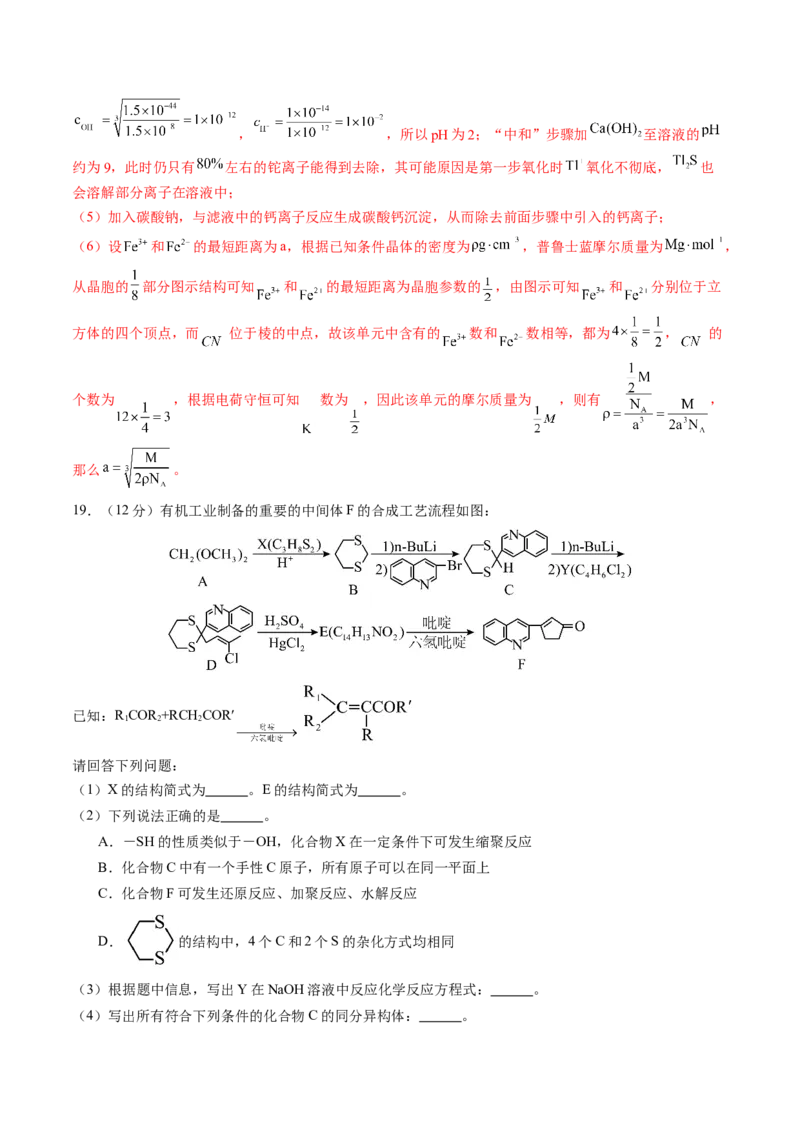
19.(12分)有机工业制备的重要的中间体F的合成工艺流程如图:
已知:R COR +RCH COR′
1 2 2
请回答下列问题:
(1)X的结构简式为 。E的结构简式为 。
(2)下列说法正确的是 。
A.-SH的性质类似于-OH,化合物X在一定条件下可发生缩聚反应
B.化合物C中有一个手性C原子,所有原子可以在同一平面上
C.化合物F可发生还原反应、加聚反应、水解反应
D. 的结构中,4个C和2个S的杂化方式均相同
(3)根据题中信息,写出Y在NaOH溶液中反应化学反应方程式: 。
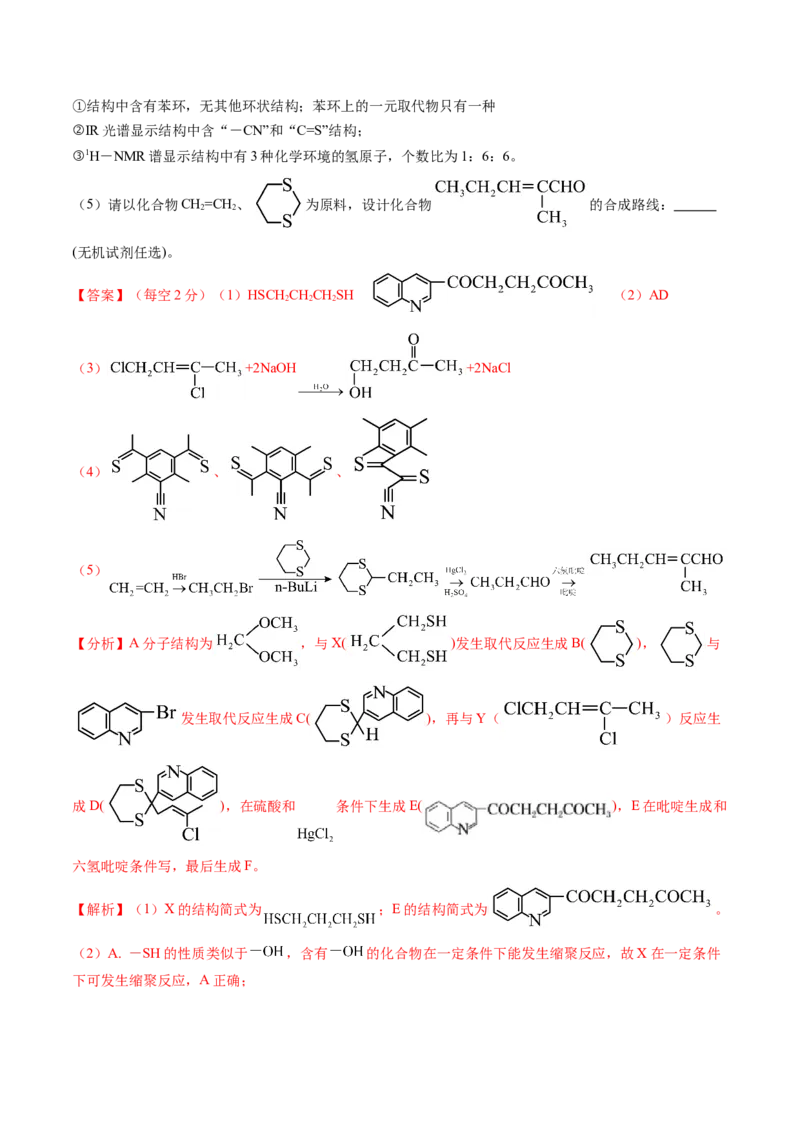
(4)写出所有符合下列条件的化合物C的同分异构体: 。①结构中含有苯环,无其他环状结构;苯环上的一元取代物只有一种
②IR光谱显示结构中含“-CN”和“C=S”结构;
③1H-NMR谱显示结构中有3种化学环境的氢原子,个数比为1:6:6。
(5)请以化合物CH=CH 、 为原料,设计化合物 的合成路线:
2 2
(无机试剂任选)。
【答案】(每空2分)(1)HSCH CHCHSH (2)AD
2 2 2
(3) +2NaOH +2NaCl
(4) 、 、
(5)
【分析】A分子结构为 ,与X( )发生取代反应生成B( ), 与
发生取代反应生成C( ),再与Y( )反应生
成D( ),在硫酸和 条件下生成E( ),E在吡啶生成和
六氢吡啶条件写,最后生成F。
【解析】(1)X的结构简式为 ;E的结构简式为 。
(2)A. -SH的性质类似于 ,含有 的化合物在一定条件下能发生缩聚反应,故X在一定条件
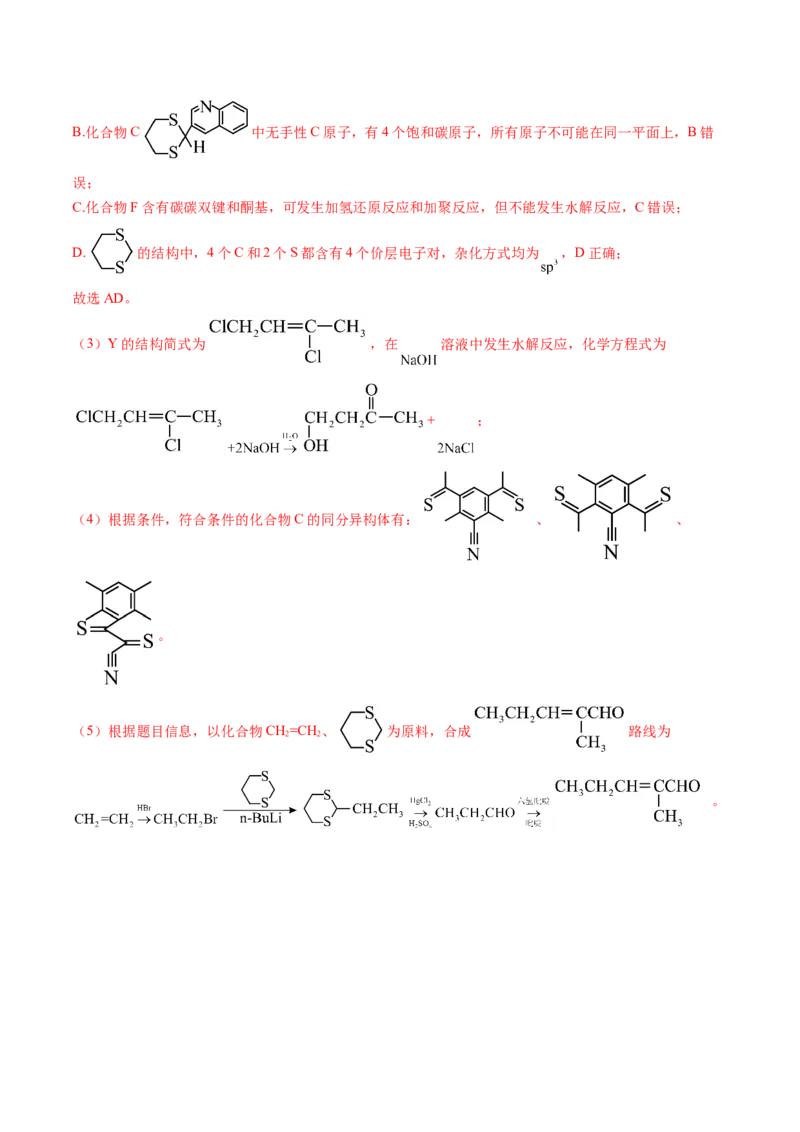
下可发生缩聚反应,A正确;B.化合物C 中无手性C原子,有4个饱和碳原子,所有原子不可能在同一平面上,B错
误;
C.化合物F含有碳碳双键和酮基,可发生加氢还原反应和加聚反应,但不能发生水解反应,C错误;
D. 的结构中,4个C和2个S都含有4个价层电子对,杂化方式均为 ,D正确;
故选AD。
(3)Y的结构简式为 ,在 溶液中发生水解反应,化学方程式为
+ ;
(4)根据条件,符合条件的化合物C的同分异构体有: 、 、
。
(5)根据题目信息,以化合物CH=CH 、 为原料,合成 路线为
2 2
。