文档内容
2 0 2 5 年 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 王双奕
粉笔教师教育 粉笔教师目
录
content
1 化学反应与能量
2 化学反应速率和化学平衡
3 水溶液中的离子平衡
4 电化学基础化学反应与能量P120
一、化学反应与能量的变化
(一)化学基本反应
化学反应是指有新物质生成的反应。
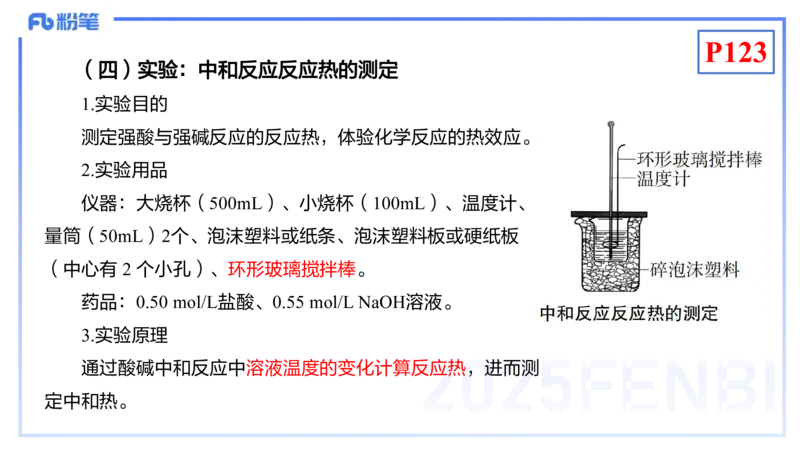
(二)化学键与化学反应中能量变化的关系
当物质发生化学变化时,反应物中的旧化学键断裂要吸收能量,而生
成物中新化学键的形成要放出能量。即化学反应不仅有新物质生成,还伴
随着能量变化。因此,化学键的断裂和形成是化学反应中能量变化的主要
原因。P121
(三)反应热
在等温条件下,化学反应体系向环境释放或从环境吸收的热量叫作
反应热,反应热在特定条件下等于焓变,用符号 ∆H 表示,单位一般采
用 kJ/mol。
综上,化学反应可分为放热反应和吸热反应。P121P121P121
【粉笔提示】
判断放热反应与吸热反应的注意事项:
(1)不能将反应类型(放热反应或吸热反应)与反应条件(是否需要加
热)相联系,误认为放热反应不需要加热。
(2)不能将化学反应与能量变化过程等同起来,化学反应中必然有能量
的变化,但有能量变化的却不一定是化学反应。例如,水蒸气变成液态水会
放出能量,但这一过程属于物理变化。P122
(3) 绝大多数吸热反应需在加热条件下进行,但也有部分吸热反应
不加热也能进行,如 Ba(OH) ·8H O 与 NH Cl 的反应等。
2 2 4
(4)如果某反应是放热反应,那么该反应的逆反应必然是吸热反应,
反之亦然。P127P122
(四)热化学方程式
1.定义
表示参加反应物质的物质的量和反应热的关系的化学方程式叫作热化
学方程式。
2.意义
不仅表明了化学反应中的物质变化,同时也表明了化学反应中的能量
变化。P122
3.书写要求
(1)应注明反应热的符号(“+”或“-”)、数值和单位(kJ/mol)。
(2)注意反应热 ∆H 与测定条件(温度、压强)有关。因此书写热化学方
程式时应注明 ∆H 的测定条件。绝大多数反应的 ∆H 是在25 ℃、101 kPa下测定
的,这时可不注明温度和压强。
(3)注意若反应物和生成物的聚集状态不同,反应热数值也不同。因此,
必须注明物质的聚集状态(s、l、g、aq)才能完整地体现出热化学方程式的意
义。对于化学式形式相同的同素异形体,还必须注明名称,如 C(金刚石,s)。P122
(4)注意热化学方程式中各物质化学式前面的化学计量数可表示该物质的
物质的量,因此化学计量数可以是整数,也可以是分数。
(5)由于 ∆H 与参加反应物质的物质的量有关,所以方程式中化学式前面
的化学计量数必须与 ∆H 相对应,如果化学计量数加倍,则 ∆H 也必须要加倍。
当反应逆向进行时,其反应热与正反应的反应热数值相等,符号相反。
例:① Fe O (s) + 3CO(g) = 2Fe(s) + 3CO (g) ∆H =-25kJ·mol-1
2 3 2 1
② 2Fe O (s) + 6CO(g) = 4Fe(s) + 6CO (g) ∆H = 2∆H =-50kJ·mol-1
2 3 2 2 1
③ 2Fe(s) + 3CO (g)= Fe O (s) + 3CO(g) ∆H =- ∆H =25kJ·mol-1
2 2 3 3 1P127P123
二、燃烧热与中和热
(一)燃烧热
在 101 kPa时,1mol 纯物质 完全燃烧生成指定产物时所放出的热量,叫
作该物质的燃烧热。燃烧热的单位一般为 kJ/mol 。生成指定产物指可燃物中
的碳元素变为CO (g),氢元素变为H O(l),硫元素变为SO (g),氮元素变为
2 2 2
N (g)等。
2
q:哪一个方程对应的是氢气的燃烧热?
2H (g)+O (g)===2H O(l) △H
2 2 2 1
H (g)+1/2 O (g)===H O(g) △H
2 2 2 2
H (g)+1/2 O (g)===H O(l) △H
2 2 2 3P123
(二)中和热
在稀溶液中,强酸与强碱发生中和反应生成 1 mol 液态水所放出的热
量叫作中和热。
表示为 H+(aq)+OH-(aq) = H O(l) ∆H=-57.3 kJ/mol。
2
q:判断1/2Ba(OH) (aq)+1/2H SO (aq) = H O(l) + 1/2BaSO (s) ∆H 对应的
2 2 4 2 4
热效应是否是中和热?P123
(三)燃烧热和中和热的比较
燃烧热 中和热
能量变化 放热反应
相同点
∆H ∆H<0,单位:kJ/mol
反应物的量 1 mol可燃物(O 的量不限) 可能是1 mol,也可能是0.5 mol
2
不同点
生成物的量 不限量 H O(l)是1 mol
2P123
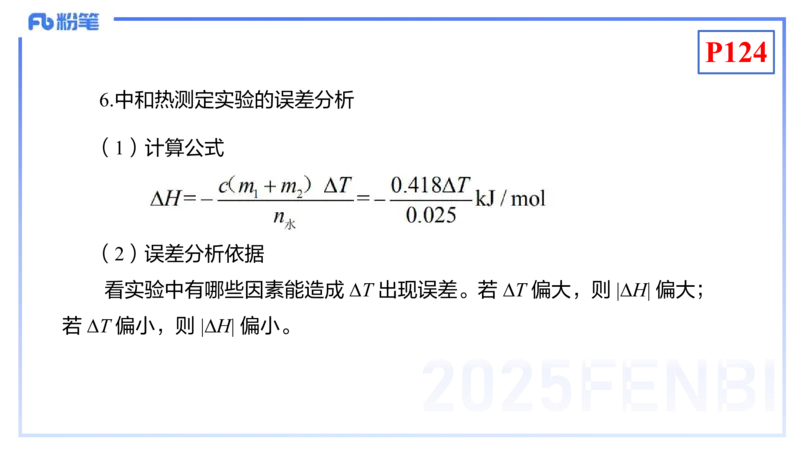
(四)实验:中和反应反应热的测定
1.实验目的
测定强酸与强碱反应的反应热,体验化学反应的热效应。
2.实验用品
仪器:大烧杯(500mL)、小烧杯(100mL)、温度计、
量筒(50mL)2个、泡沫塑料或纸条、泡沫塑料板或硬纸板
(中心有 2 个小孔)、环形玻璃搅拌棒。
药品:0.50 mol/L盐酸、0.55 mol/L NaOH溶液。
3.实验原理
通过酸碱中和反应中溶液温度的变化计算反应热,进而测
定中和热。P124
4.实验步骤
第一步:用量筒量取 50mL 0.50mol/L 盐酸,倒
入小烧杯中,测量并记录其温度(T )。
1
第二步:用另一量筒量取 50mL 0.55mol/L NaOH
溶液,测量并记录其温度(T )。
2
第三步:将量筒中的 NaOH 溶液迅速倒入盛有盐
酸的小烧杯中,立即盖好盖板,用环形玻璃搅拌棒轻
轻搅拌,观察温度计的示数变化,准确读出并记录反
应体系的最高温度(T )。
3P124
5.实验注意事项
(1)配制的盐酸和 NaOH 溶液的浓度须准确,且 NaOH 溶液的浓度
须稍大于盐酸的浓度,以确保盐酸被完全中和。为使测得的中和热更准确,
所用盐酸和 NaOH 溶液的浓度宜小不宜大(不大于1mol/L),以防浓酸、
浓碱溶液稀释时放热。
(2)实验操作时动作要快,隔热保温效果要好,以减少热量损失。P124
(3)温度计的水银球部分要完全浸没在溶液中,而且要稳定一段时
间后读数,以提高所测温度的准确度。
(4)实验时必须用强酸、强碱溶液,避免弱酸、弱碱电离吸热引起
误差。且酸碱反应生成的盐必须是可溶性的。
(5)实验需重复 3 次,取测量数据的平均值作为计算依据。P124
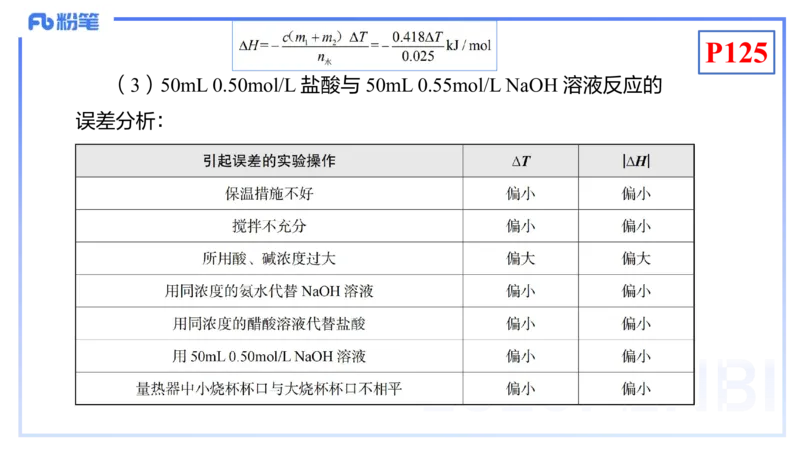
6.中和热测定实验的误差分析
(1)计算公式
(2)误差分析依据
看实验中有哪些因素能造成 ∆T 出现误差。若 ∆T 偏大,则 |∆H| 偏大;
若 ∆T 偏小,则 |∆H| 偏小。P125
(3)50mL 0.50mol/L 盐酸与 50mL 0.55mol/L NaOH 溶液反应的
误差分析:P125
三、盖斯定律
盖斯定律是计算反应热的重要依据,在生产和科学研究中有着重要
意义。其内容为:化学反应不管是一步完成还是分几步完成,其反应热
是相同的,也就是说,化学反应的反应热只与反应的始态和终态有关,
而与反应的具体途径无关。P125
例如:
∆H=∆H +∆H 或 ∆H =∆H-∆H ,所以热化学方程式间可进行“+”“-”
1 2 1 2
等数学运算。
依据盖斯定律,对几个热化学方程式进行移项、变向、(乘以某个数后)相
加减等多种数学运算,可得到新反应或新过程的 ∆H。P127书上无
在标准状况下,石墨燃烧反应的焓变为 -393.7 kJ/mol,金刚石燃烧反
应的焓变为 -395.6 kJ/mol。则石墨转变为金刚石的反应焓变为( )。
A. -789.3 kJ/moI B. +1.9 kJ/mol
C. -1.9 kJ/mol D. 0P125
四、能源
能源就是提供能量的资源,包括化石燃料(煤、石油、天然气)、
阳光、风力、流水、潮汐以及柴草等。能源的开发和利用可以衡量一个
国家或地区的经济发展和科学技术水平。我国目前使用的主要能源是化
石燃料,化石燃料蕴藏量有限,不能再生。必须注意节约现有能源,开
发新能源。P126
(一)能源的分类
【粉笔提示】
生物质能所属类别需要注意题干的问法,若为杂草、秸秆等,则为一次
能源,且为常规能源;若为秸秆等经发酵后制得的沼气,则为二次能源,且
为新能源。P126
(二)各种能源的特点
1.传统燃料。柴草是农村使用的重要能源,但利用率低,且污染严重。
2.化石燃料。目前使用的主要能源,蕴藏量有限,不能再生,最终会
枯竭,属于不可再生能源。
3.新能源。来源丰富,多数可再生,无污染或污染小,可能成为未来
的主要能源。但也有缺点:太阳能的能量密度低,使用成本高;氢能的储
存、运输困难;风能不稳定,受地区、气候影响大。P126
(三)化石燃料的使用
1.燃料充分燃烧的条件:
①有足量的空气;②燃料与空气有足够大的接触面积。
2.煤的使用:
①煤是重要的化工燃料;
②煤是发热量很高的燃料,开采成本较低;
③煤直接燃烧产生 SO 等有毒有害气体和烟尘,对环境造成严重污染;
2
④煤作为固体燃料,燃烧反应速率慢,热利用率低;
⑤可通过清洁煤技术,如煤的液化和气化以及实行烟气净化脱硫等,
大大减少燃煤对环境的污染,提高煤燃烧的热利用率。P126
(四)新能源的开发
1.调整和优化能源结构,降低煤在能源结构中的比例,节约油气资源,
加大科技投入,加快新能源开发等。
2.进一步探索研究太阳能、地热能、海洋能、氢能、风能等新能源。P128书上无化学反应速率和化学平衡P128
一、化学反应速率
1.定义
化学反应速率是用来衡量化学反应进行快慢程度的物理量。指在一定条件下,反
应物转变成为生成物的速率。
2.表示方法
(1)定性表示
如用沉淀出现的快慢、气泡生成的剧烈程度等来定性说明反应的快慢。
定性说明时,通常是笼统地对整个反应而言,如中和反应很快、酯化反应较慢。P128
(2)定量表示
在容积不变的反应器中,通常用单位时间内反应物浓度的减少或
生成物浓度的增加来表示。
c
v
t
(ν:化学反应速率;Δc:浓度变化量;Δt:反应时间)
单位:mol/(L·min) 或 mol·L-1·min-1 ;
mol/(L·s) 或 mol·L-1·s-1。P128P129
3.理解化学反应速率时注意
(1)化学反应速率是指一段时间内的平均速率,且反应速率均取正值,
即 ν > 0。
(2)化学反应速率不用固体或纯液体物质的“浓度变化”来表示。
(3)同一个化学反应,在同一段时间内,用不同物质表示反应速率时,
数值可能相同或不同,但表达的意义却相同。P129
(4)在同一反应中用不同的物质来表示反应速率时,其数值之比等于
各物质的化学计量数之比。
如化学反应: mA(g)+nB(g) = pC(g)+qD(g) 的
ν(A) : ν(B) : ν(C) : ν(D)= m : n : p : qP129
二、影响化学反应速率的因素
(一)有效碰撞理论
1.碰撞理论
1918年,路易斯(lewis)根据气体分子运动论,提出了碰撞理论。
碰撞理论的要点:
(1)反应物分子间只有发生碰撞才有可能发生反应,或者说碰撞是反应发生的
先决条件。
(2)只有少部分碰撞能引发化学反应,大多数反应物微粒之间的碰撞是无效碰撞。
(3)单位时间内有效碰撞的次数越多,反应速率越快。
(4)活化能越大,活化分子越少,反应速率就越慢。P129
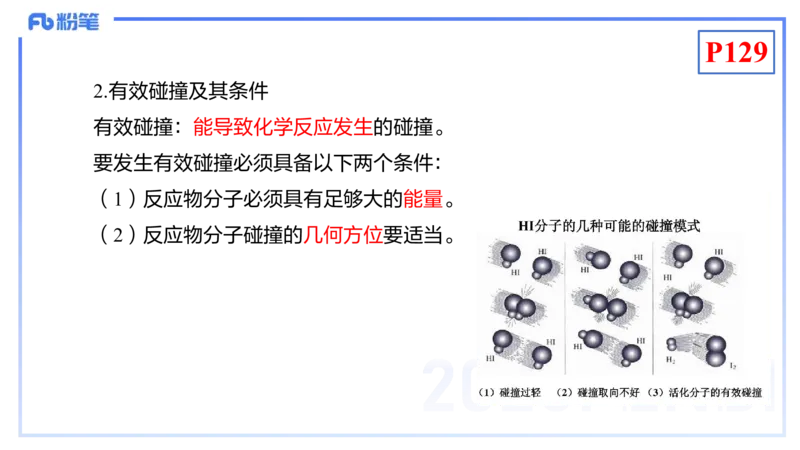
2.有效碰撞及其条件
有效碰撞:能导致化学反应发生的碰撞。
要发生有效碰撞必须具备以下两个条件:
(1)反应物分子必须具有足够大的能量。
(2)反应物分子碰撞的几何方位要适当。P130
3.活化分子与活化能
活化分子:能够发生有效碰撞的分子。
活化能:活化分子比普通分子多出的那部分能量(或普通分子转化成活化
分子所需的最低能量)。P130
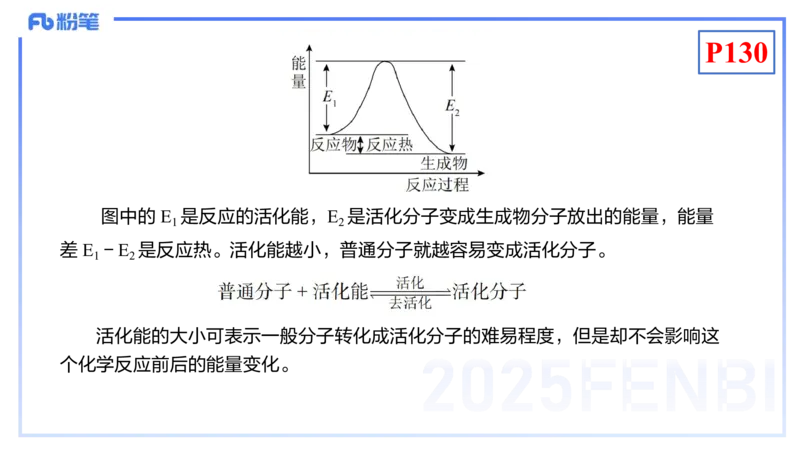
图中的 E 是反应的活化能,E 是活化分子变成生成物分子放出的能量,能量
1 2
差 E -E 是反应热。活化能越小,普通分子就越容易变成活化分子。
1 2
活化能的大小可表示一般分子转化成活化分子的难易程度,但是却不会影响这
个化学反应前后的能量变化。P130
活化能低→普通分子易变成活化分子→活化分子百分数大→有效碰撞
次数多→反应速率快。
【粉笔提示】
有关活化能需要了解:
1.温度对某反应的速率的影响程度,大致反映了该反应的活化能的大小。
2.自然条件下活化能较高的反应:岩石的风化、溶洞的形成、矿物的形
成等。P130
3.有些反应,速率极大,当反应物相互接触时,瞬间发生反应,而且温度
对其反应速率几乎没有什么影响,其活化能接近于零。
例如:
(1)离子反应:H+和OH-、Ag+和Cl-在水溶液中混合时,反应几乎都
是在瞬间内完成的;
(2)距地面约50~85km的大气层,平均温度只有-50℃,但是存在于其
中的大量自由原子之间的反应,却几乎不需要“克服”活化能。
这两类反应活化能几乎为零的原因,是在反应之前反应物已经成为自由
的离子或原子,不再需要破坏或减弱化学键。