文档内容
西安中学 2026 届高三质量检测考试(三)
化学试题
(时间:75分钟 满分:100分 )
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Fe-56 Cu-64
一、选择题(共 14 小题,每小题 3 分,共 42 分。在每小题给出的四个选项
中,只有一项是符合题目要求的)
1.近年来我国科学家在诸多领域取得新突破,下列说法正确的是( )
A.实现聚氯乙烯塑料高效转化为燃油,聚氯乙烯和燃油都是混合物
B.确认火星内部存在固态内核,其主要成分是铁镍合金,铁和镍都是ds区元素
C.开发高效钙钛矿太阳能电池,其发电时能量转化形式:化学能→电能
D.建成亚洲最深油气井“深地一号”,其使用的金刚石钻头属于金属晶体
2.下列化学用语表示正确的是( )
A.BCl 的电子式为
3
B.激发态Li原子的轨道表示式为
C.Fe3+的离子结构示意图为
D.OF 的球棍模型为
2
3.下列有关实验操作或处理的说法正确的是( )
A.滴定读数时,应双手分别持滴定管上下端保证其处于竖直状态
B.浓硫酸沾到皮肤上,立即用 的 溶液冲洗
C.用过滤法分离苯和2,4,6—三溴苯酚的混合物
D.与氢氧化铁胶体制备、性质实验有关的实验图标有 、 、 等
4.奥司他韦(化合物M)是目前治疗流感的常用药物,其合成路线如下(其中某些步
骤省略)。下列说法正确的是 ( )
A.Y能使溴水和酸性高锰酸钾溶液褪色,但原理不同B.Z中所有碳原子可能共平面
C.X、M均可以发生水解反应和加成反应
D.M中含有6种官能团
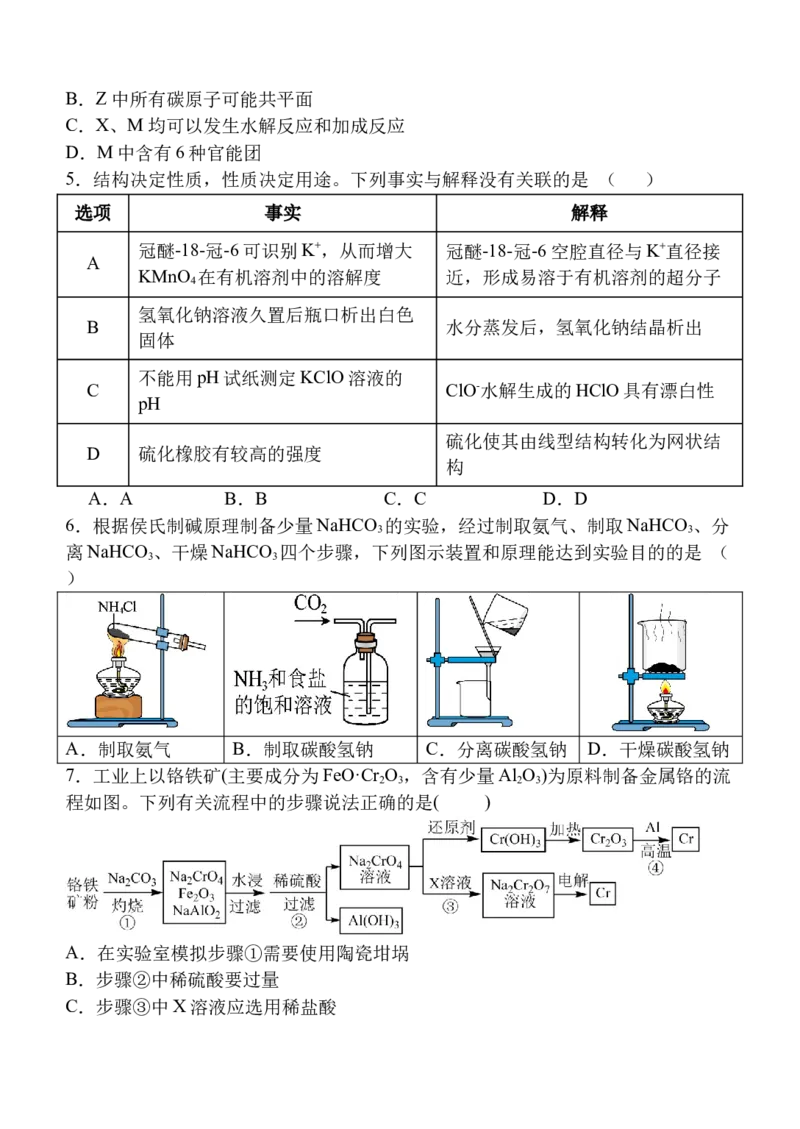
5.结构决定性质,性质决定用途。下列事实与解释没有关联的是 ( )
选项 事实 解释
冠醚-18-冠-6可识别K+,从而增大 冠醚-18-冠-6空腔直径与K+直径接
A
KMnO 在有机溶剂中的溶解度 近,形成易溶于有机溶剂的超分子
4
氢氧化钠溶液久置后瓶口析出白色
B 水分蒸发后,氢氧化钠结晶析出
固体
不能用pH试纸测定KClO溶液的
C ClO-水解生成的HClO具有漂白性
pH
硫化使其由线型结构转化为网状结
D 硫化橡胶有较高的强度
构
A.A B.B C.C D.D
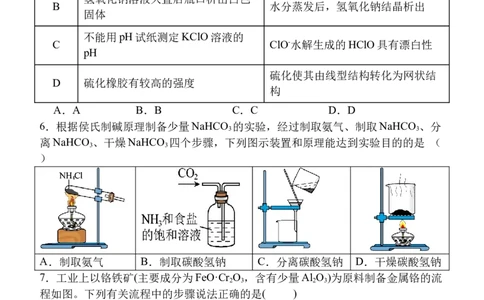
6.根据侯氏制碱原理制备少量NaHCO 的实验,经过制取氨气、制取NaHCO 、分
3 3
离NaHCO 、干燥NaHCO 四个步骤,下列图示装置和原理能达到实验目的的是 (
3 3
)
A.制取氨气 B.制取碳酸氢钠 C.分离碳酸氢钠 D.干燥碳酸氢钠
7.工业上以铬铁矿(主要成分为FeO·Cr O ,含有少量Al O )为原料制备金属铬的流
2 3 2 3
程如图。下列有关流程中的步骤说法正确的是( )
A.在实验室模拟步骤①需要使用陶瓷坩埚
B.步骤②中稀硫酸要过量
C.步骤③中X溶液应选用稀盐酸D.步骤④的反应原理可在野外作业中用于焊接钢轨
8.短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数
是其电子层数的2倍,X、Y的核电荷数之比为3:4。W-的最外层为8电子结构。金
属单质Z在空气中燃烧生成的化合物可与水发生氧化还原反应。下列说法正确的是(
)
A.X与Y能形成多种化合物,一般条件下都能与Z的最高价氧化物的水化物发生
反应
B.原子半径大小:XW
C.化合物Z Y和ZWY 都只存在离子键
2 3
D.Y、W的某些单质或两元素之间形成的某些化合物可作水的消毒剂
9.下列反应的离子方程式书写错误的是( )
A.碱性条件下用 NaClO氧化Fe (SO ) 制备Na FeO :3ClO−+2Fe3++10OH−=2FeO 2-
2 4 3 2 4 4
+3Cl−+5H O
2
B.用酸性KMnO 溶液吸收空气中的SO :5SO +2MnO −+2H O=5SO 2−+2Mn2++4H+
4 2 2 4 2 4
C.少量SO 气体通入NaClO溶液中:2ClO−+H O+SO =2HClO+SO 2−
2 2 2 3
D.1.5mol Cl 与1mol FeI 混合反应:3Cl +2Fe2++4I− = 2Fe3++2I +6Cl−
2 2 2 2
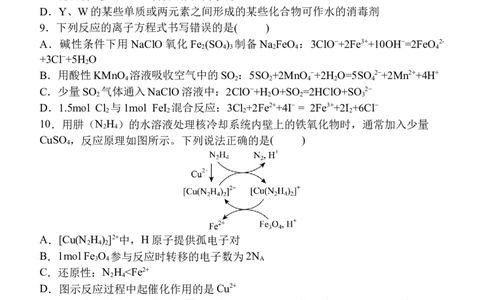
10.用肼(N H )的水溶液处理核冷却系统内壁上的铁氧化物时,通常加入少量
2 4
CuSO ,反应原理如图所示。下列说法正确的是( )
4
A.[Cu(N H ) ]2+中,H原子提供孤电子对
2 4 2
B.1mol Fe O 参与反应时转移的电子数为2N
3 4 A
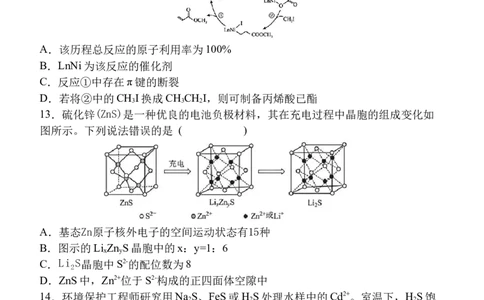
C.还原性:N H c(S2- )
2
D.向0.01mol·L-1的FeCl 溶液中加入等体积0.2mol·L-1的Na S溶液,不能形成FeS
2 2
沉淀。
二、非选择题(共58分)
15. (14分)[Co(NH ) ]Cl (三氯化六氨合钴)可用于磷酸盐检测和钴盐制造等。其制
3 6 3
备装置图(省略加热和夹持装置)及步骤如下:
步骤 :将NH Cl固体溶在水中,加入研细的CoCl ·6H O晶体,溶解得到混合溶
4 2 2
液。
步骤ii:将混合溶液转移至三颈烧瓶中,加入催化剂活性炭,再依次打开活塞a和
b,加入浓氨水与H O 溶液,水浴加热至55℃,保持20min。
2 2
步骤iii:趁热过滤,冷却后向滤液中加入适量浓盐酸,过滤、洗涤、干燥,得到
[Co(NH ) ]Cl 粗产品。
3 6 3
回答下列问题:
(1)[Co(NH ) ]Cl 中钴元素的化合价是 。
3 6 3
(2)仪器m的名称是 ,所盛装的试剂是 (填标号)。
a.碱石灰 b.浓硫酸 c.无水氯化钙
(3)写出三颈烧瓶中总反应的化学方程式为 。
(4)步骤ii中“水浴加热至55℃”的原因是
。
(5)步骤iii中“趁热过滤”的目的是
。
(6)若用10.0g CoCl ·6H O(M=238g/mol)进行实验,最终得到8.0g[Co(NH ) ]Cl
2 2 3 6 3
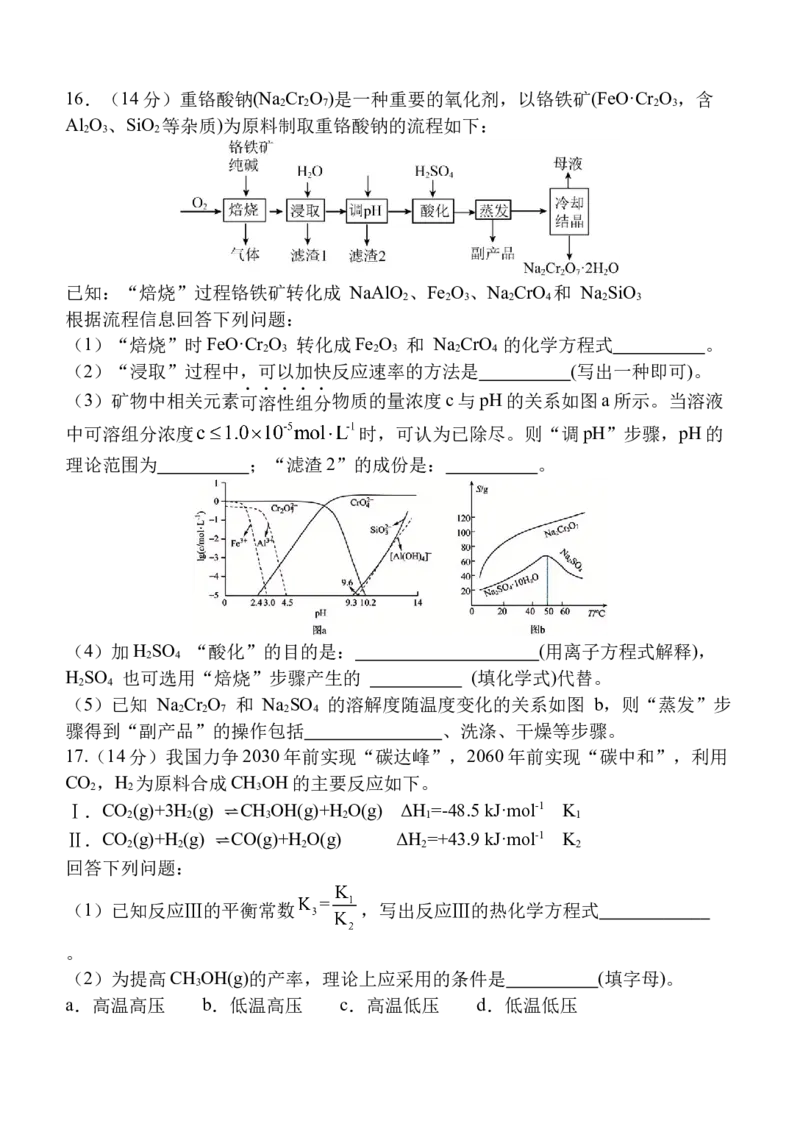
(M=267.5 g/mol)粗产品,则产率为 。(保留三位有效数字)16.(14分)重铬酸钠(Na Cr O )是一种重要的氧化剂,以铬铁矿(FeO·Cr O ,含
2 2 7 2 3
Al O 、SiO 等杂质)为原料制取重铬酸钠的流程如下:
2 3 2
已知:“焙烧”过程铬铁矿转化成 NaAlO 、Fe O 、Na CrO 和 Na SiO
2 2 3 2 4 2 3
根据流程信息回答下列问题:
(1)“焙烧”时FeO·Cr O 转化成Fe O 和 Na CrO 的化学方程式 。
2 3 2 3 2 4
(2)“浸取”过程中,可以加快反应速率的方法是 (写出一种即可)。
(3)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图a所示。当溶液
中可溶组分浓度 时,可认为已除尽。则“调pH”步骤,pH的
理论范围为 ;“滤渣2”的成份是: 。
(4)加H SO “酸化”的目的是: (用离子方程式解释),
2 4
H SO 也可选用“焙烧”步骤产生的 (填化学式)代替。
2 4
(5)已知 Na Cr O 和 Na SO 的溶解度随温度变化的关系如图 b,则“蒸发”步
2 2 7 2 4
骤得到“副产品”的操作包括 、洗涤、干燥等步骤。
17.(14分)我国力争2030年前实现“碳达峰”,2060年前实现“碳中和”,利用
CO ,H 为原料合成CH OH的主要反应如下。
2 2 3
Ⅰ.CO (g)+3H (g) CH OH(g)+H O(g) ΔH =-48.5 kJ·mol-1 K
2 2 ⇌ 3 2 1 1
Ⅱ.CO (g)+H (g) CO(g)+H O(g) ΔH =+43.9 kJ·mol-1 K
2 2 ⇌ 2 2 2
回答下列问题:
(1)已知反应Ⅲ的平衡常数 ,写出反应Ⅲ的热化学方程式
。
(2)为提高CH OH(g)的产率,理论上应采用的条件是 (填字母)。
3
a.高温高压 b.低温高压 c.高温低压 d.低温低压(3)一定温度下,向压强恒为p MPa的密闭容器中通入1molCO (g)和3molH (g),
2 2
充分反应后,测得CO 平衡转化率为50%,CH OH选择性为80%,该温度下
2 3
CH OH的分压为 。 [甲醇的选择性= ×100%]
3
(4)研究者向恒压(3.0MPa)密闭装置中通入反应物混合气(混合比例 ),
测定甲醇时空收率随温度的变化曲线如图所示。(甲醇时空收率是表示单位物质的量
催化剂表面甲醇的平均生成速率)。
①请解释甲醇时空收率“抛物线”前半段升高的原因: 。
②为获得最大的甲醇时空收率,根据图像选择催化剂最佳配比和反应最佳反应温度
为 (填字母)。
A.Ni Ga ,210℃ B.NiGa,220℃ C.NiGa,240℃ D.Ni Ga ,
5 3 5 3
220℃
(5)在一定催化剂催化作用下CO 加氢合成甲酸发生反应如下:
2
CO (g)+H (g)
⇌
HCOOH(g) ΔH=−30.9kJ⋅mo l−1。
2 2
该反应的Arrhenius经验公式的实验数据如图中的曲线d所示,
已知Arrhenius经验公式为 (Ea为活化能,k为速率常数,R和C为常
数),则该反应的活化能Ea= kJ·mol-1。改变外界条件,实验数据如图中的
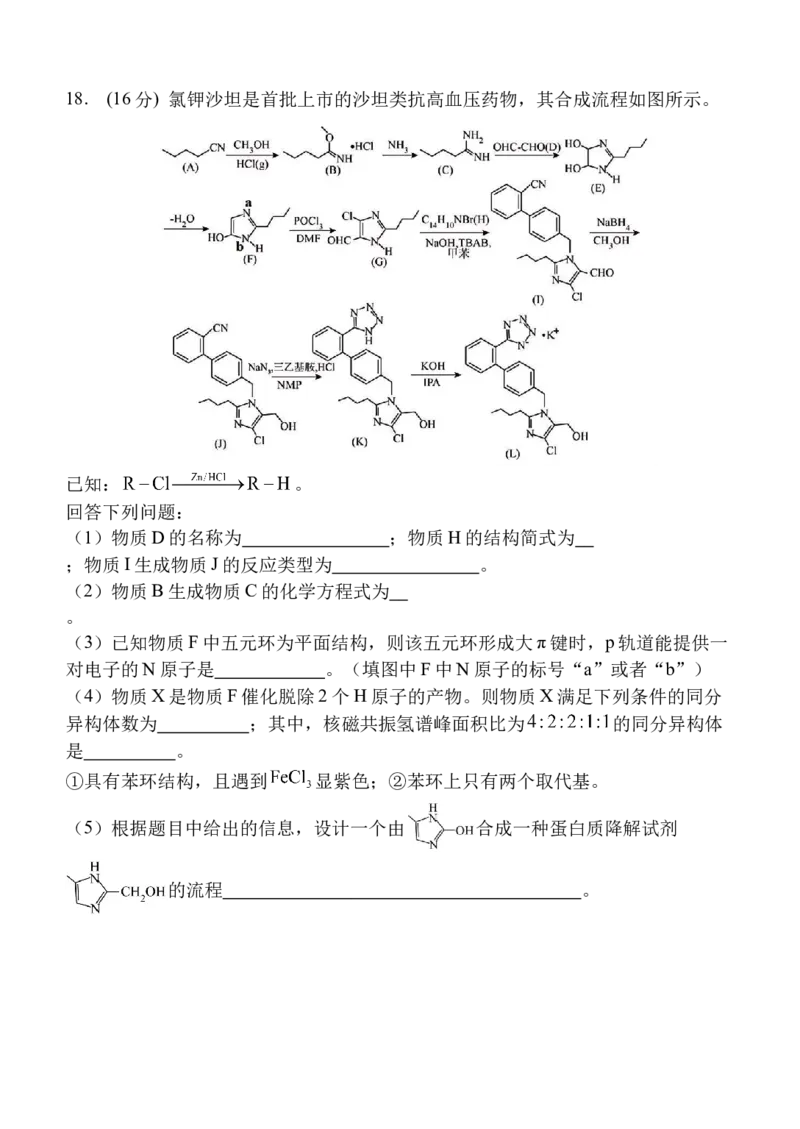
曲线e所示,则实验可能改变的外界条件是 。18. (16分) 氯钾沙坦是首批上市的沙坦类抗高血压药物,其合成流程如图所示。
已知: 。
回答下列问题:
(1)物质D的名称为 ;物质H的结构简式为
;物质I生成物质J的反应类型为 。
(2)物质B生成物质C的化学方程式为
。
(3)已知物质F中五元环为平面结构,则该五元环形成大π键时,p轨道能提供一
对电子的N原子是 。(填图中F中N原子的标号“a”或者“b”)
(4)物质X是物质F催化脱除2个H原子的产物。则物质X满足下列条件的同分
异构体数为 ;其中,核磁共振氢谱峰面积比为 的同分异构体
是 。
①具有苯环结构,且遇到 显紫色;②苯环上只有两个取代基。
(5)根据题目中给出的信息,设计一个由 合成一种蛋白质降解试剂
的流程 。