文档内容
吉林省“BEST 合作体”2024-2025 学年度下学期期末考试高二
A. B . C . D .
化学试题
4、下列有机物命名正确的是( )
本试卷分选择题和非选择题两部分,共 19题,共 100 分,共 4 页。考试时间为 75分钟。考试
结束后,只交答题卡。
A. :苯甲酸甲酯 B. :顺-2-丁烯
第Ⅰ卷 选择
可能用到的相对原子质量:H:1 C:12 B:11 N:14 O:16 Mg:24 S:32 Cl:35.5 Cu:64
题
一、单项选择题(15 小题,每小题 3 分,共 45 分) C. :2-戊醛 D. :二溴乙烷
1、下列化学用语表示正确的是( )
5、物质结构决定其性质,下列实例与解释有错误的( )
A.基态铝原子核外能量最高的电子电子云轮廓图可表示为: 选
实例 解释
项
聚乙炔中含共轭大 π键,π电子能够在分子链上自
B.HF 分子间的氢键 A 聚乙炔可用于制备导电高分子材料
由移动而具有导电性
C.HClO 的结构式:H-Cl-O
臭氧 O 在四氯化碳中的溶解度高
B 3 臭氧 O 是极性分子,但分子极性较小
于在水中的溶解度 3
C 熔点:SiO >CO SiO 为共价晶体,CO 为分子晶体
D.CO23− 的空间结构: (三角锥形) 2 2 2 2
酸性高锰酸钾溶液氧化甲苯,加入 18-冠-6 为超分子,K+可以进入其空腔,进而在静电
2、化学与我们的生活、生产密切相关,下列说法中错误的是( ) D
冠醚(18-冠-6)可加快反应速率 作用下提高 MnO 4-在有机相中的溶解度
A.单一波长的 X 射线通过晶态 SiO 时,记录仪上会产生明锐的衍射峰
2
6、下列方程式书写错误的是( )
B.离子液体熔点低且有良好的导电性,可用作原电池的电解质
C.常见食用油在空气中被氧化产生异味,与其分子中含有酯基有关 A.丙烯醛(CH CHCHO)与足量溴水反应:CH CHCHO + Br CH BrCHBrCHO B.用
2 2 2 2
D.量子通信材料螺旋碳纳米管与石墨烯互为同素异形体 Na 2 SO 3 溶液吸收少量 Cl 2 :3SO23− + Cl 2 + H 2 O 2HSO−3 + 2Cl− + SO 42−
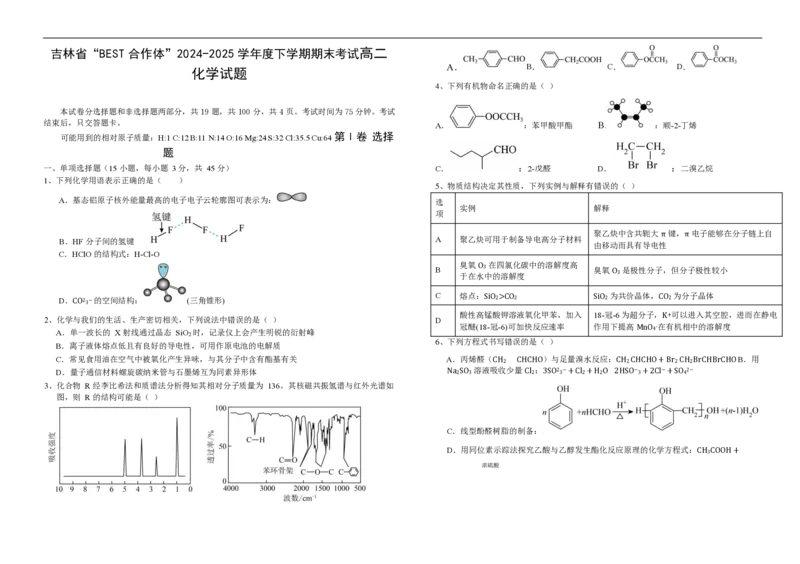
3、化合物 R 经李比希法和质谱法分析得知其相对分子质量为 136。其核磁共振氢谱与红外光谱如
图,则 R 的结构可能是( )
C.线型酚醛树脂的制备:
D.用同位素示踪法探究乙酸与乙醇发生酯化反应原理的化学方程式:CH COOH +
3
浓硫酸H18OC2H5 CH3CO18OC2H5 + H2O A.I 与乙二酸二甲酯互为同系物
B.Ⅲ中所有氧原子不可能处于同一平面
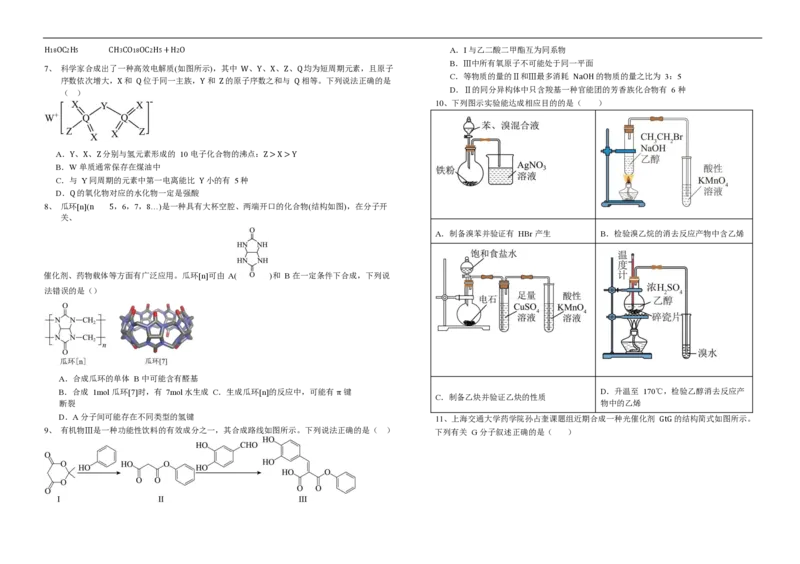
7、 科学家合成出了一种高效电解质(如图所示),其中 W、Y、X、Z、Q 均为短周期元素,且原子
C.等物质的量的Ⅱ和Ⅲ最多消耗 NaOH 的物质的量之比为 3:5
序数依次增大,X 和 Q 位于同一主族,Y 和 Z 的原子序数之和与 Q 相等。下列说法正确的是
D.Ⅱ的同分异构体中只含羧基一种官能团的芳香族化合物有 6 种
( )
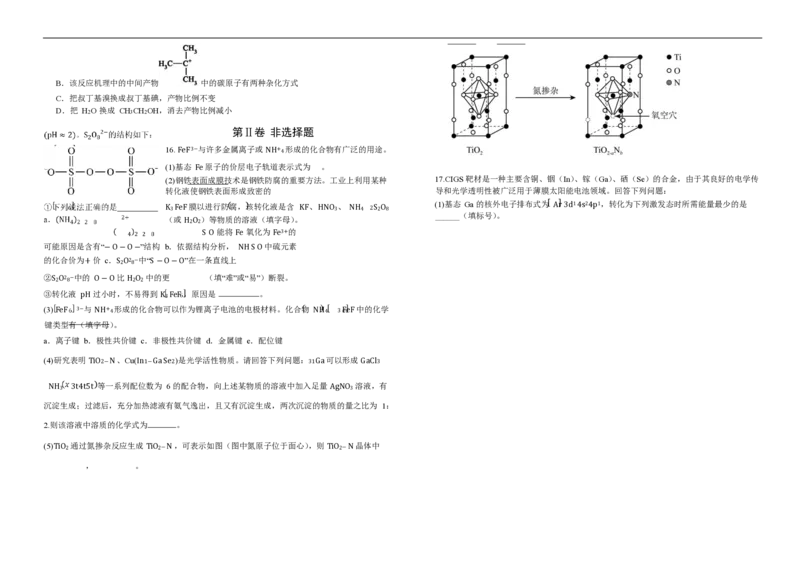
10、下列图示实验能达成相应目的的是( )
A.Y、X、Z 分别与氢元素形成的 10 电子化合物的沸点:Z > X > Y
B.W 单质通常保存在煤油中
C.与 Y 同周期的元素中第一电离能比 Y 小的有 5 种
D.Q 的氧化物对应的水化物一定是强酸
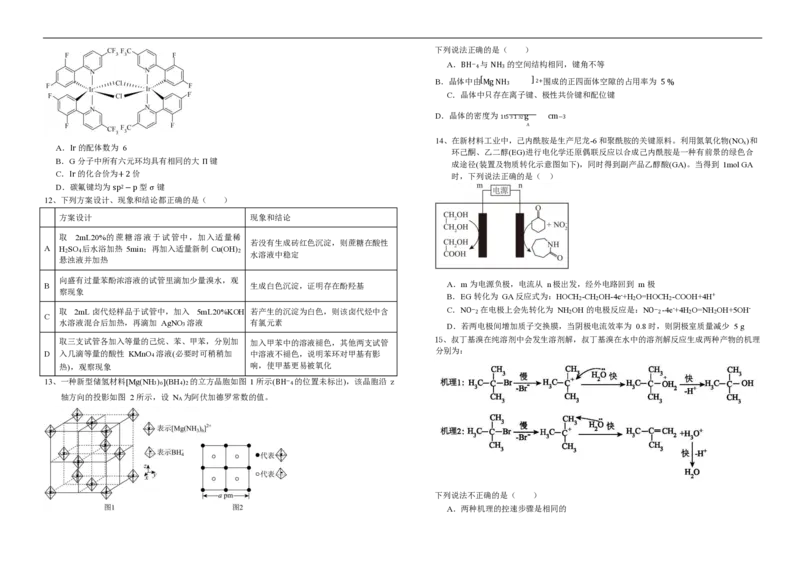
8、 瓜环[n](n 5,6,7,8…)是一种具有大杯空腔、两端开口的化合物(结构如图),在分子开
关、
A.制备溴苯并验证有 HBr 产生 B.检验溴乙烷的消去反应产物中含乙烯
催化剂、药物载体等方面有广泛应用。瓜环[n]可由 A( )和 B 在一定条件下合成,下列说
法错误的是()
A.合成瓜环的单体 B 中可能含有醛基
B.合成 1mol 瓜环[7]时,有 7mol 水生成 C.生成瓜环[n]的反应中,可能有 π键 D.升温至 170℃,检验乙醇消去反应产
C.制备乙炔并验证乙炔的性质
断裂 物中的乙烯
D.A 分子间可能存在不同类型的氢键 11、上海交通大学药学院孙占奎课题组近期合成一种光催化剂 GtG 的结构简式如图所示。
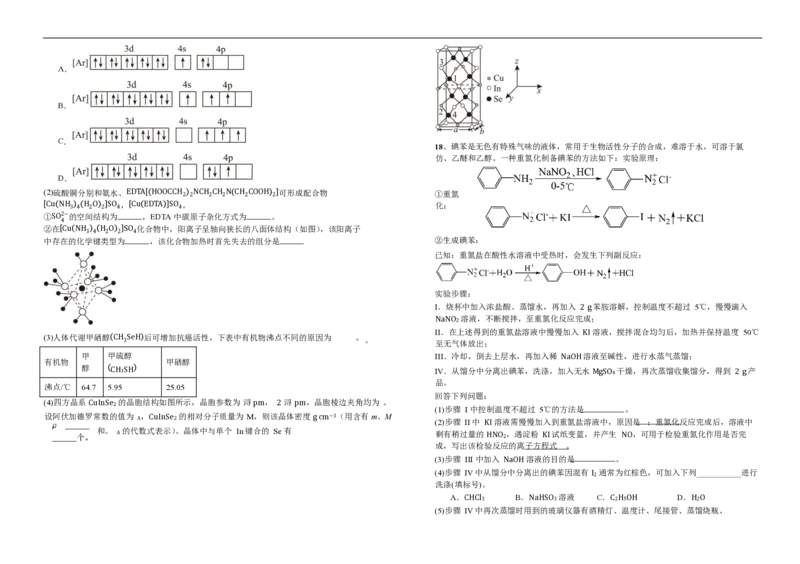
9、 有机物Ⅲ是一种功能性饮料的有效成分之一,其合成路线如图所示。下列说法正确的是( ) 下列有关 G 分子叙述正确的是( )下列说法正确的是( )
A.BH−4 与NH
3
的空间结构相同,键角不等
B.晶体中由Mg NH 2+围成的正四面体空隙的占用率为 5 %
3
C.晶体中只存在离子键、极性共价键和配位键
D.晶体的密度为 1t5 3 1 32 g cm−3
A
14、在新材料工业中,己内酰胺是生产尼龙-6 和聚酰胺的关键原料。利用氮氧化物(NO )和
x
A.Ir 的配体数为 6
环己酮、乙二醇(EG)进行电化学还原偶联反应以合成己内酰胺是一种有前景的绿色合
B.G 分子中所有六元环均具有相同的大 Π键
成途径(装置及物质转化示意图如下),同时得到副产品乙醇酸(GA)。当得到 1mol GA
C.Ir 的化合价为+ 2 价 时,下列说法正确的是( )
D.碳氟键均为 sp2 − p 型 σ键
12、下列方案设计、现象和结论都正确的是( )
方案设计 现象和结论
取 2mL20%的蔗糖溶液于试管中,加入适量稀
若没有生成砖红色沉淀,则蔗糖在酸性
A H SO 后水浴加热 5min;再加入适量新制 Cu(OH)
2 4 2
水溶液中稳定
悬浊液并加热
向盛有过量苯酚浓溶液的试管里滴加少量溴水,观
B 生成白色沉淀,证明存在酚羟基 A.m 为电源负极,电流从 n 极出发,经外电路回到 m 极
察现象
B.EG 转化为 GA 反应式为:HOCH -CH OH-4e-+H O=HOCH -COOH+4H+
2 2 2 2
取 2mL 卤代烃样品于试管中,加入 5mL20%KOH 若产生的沉淀为白色,则该卤代烃中含 C.NO− 2 在电极上会先转化为 NH 2 OH 的电极反应是:NO− 2 -4e-+4H 2 O=NH 2 OH+5OH-
C
水溶液混合后加热,再滴加 AgNO 溶液 有氯元素
3 D.若两电极间增加质子交换膜,当阴极电流效率为 0.8 时,则阴极室质量减少 5 g
取三支试管各加入等量的己烷、苯、甲苯,分别加 加入甲苯中的溶液褪色,其他两支试管 15、叔丁基溴在纯溶剂中会发生溶剂解,叔丁基溴在水中的溶剂解反应生成两种产物的机理
分别为:
D 入几滴等量的酸性 KMnO 溶液(必要时可稍稍加 中溶液不褪色,说明苯环对甲基有影
4
热),观察现象 响,使甲基更易被氧化
13、一种新型储氢材料[Mg(NH
3
)
6
](BH
4
)
2
的立方晶胞如图 1 所示(BH−4 的位置未标出),该晶胞沿 z
轴方向的投影如图 2 所示,设 N 为阿伏加德罗常数的值。
A
下列说法不正确的是( )
A.两种机理的控速步骤是相同的B.该反应机理中的中间产物 中的碳原子有两种杂化方式
C.把叔丁基溴换成叔丁基碘,产物比例不变
D.把 H O 换成 CH CH OH,消去产物比例减小
2 3 2
第Ⅱ卷 非选择题
16. FeF 3−与许多金属离子或 NH+4 形成的化合物有广泛的用途。
(1)基态 Fe 原子的价层电子轨道表示式为 。
(2)钢铁表面成膜技术是钢铁防腐的重要方法。工业上利用某种 17.CIGS 靶材是一种主要含铜、铟(In)、镓(Ga)、硒(Se)的合金,由于其良好的电学传
转化液使钢铁表面形成致密的 导和光学透明性被广泛用于薄膜太阳能电池领域。回答下列问题:
K
3
FeF 膜以进行防腐,该转化液是含 KF、HNO
3
、 NH
4
2S
2
O
8
(1)基态 Ga 的核外电子排布式为 Ar 3d1 4s24p1,转化为下列激发态时所需能量最少的是
______(填标号)。
(或 H O )等物质的溶液(填字母)。
2 2
S O 能将 Fe 氧化为 Fe3+的
可能原因是含有“− O − O −”结构 b.依据结构分析, NH S O 中硫元素
的化合价为+ 价 c.S
2
O28−中“S − O − O”在一条直线上
②S
2
O28−中的 O − O 比 H
2
O
2
中的更 (填“难”或“易”)断裂。
③转化液 pH 过小时,不易得到 K FeF ,原因是 。
3
(3) FeF 3−与 NH+ 4 形成的化合物可以作为锂离子电池的电极材料。化合物 NH 4 3 FeF 中的化学
键类型有(填字母)。
a.离子键 b.极性共价键 c.非极性共价键 d.金属键 e.配位键
(4)研究表明 TiO2− N 、Cu(In1− Ga Se2)是光学活性物质。请回答下列问题: 31Ga 可以形成 GaCl3
NH 3t4t5t 等一系列配位数为 6 的配合物,向上述某物质的溶液中加入足量 AgNO 溶液,有
3 3
沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为 1:
2.则该溶液中溶质的化学式为 。
(5)TiO 2 通过氮掺杂反应生成 TiO 2− N ,可表示如图(图中氮原子位于面心),则 TiO 2− N 晶体中
, 。A .
B .
C .
18、碘苯是无色有特殊气味的液体,常用于生物活性分子的合成,难溶于水,可溶于氯
仿、乙醚和乙醇。一种重氮化制备碘苯的方法如下:实验原理:
D .
(2)硫 酸铜分别和氨水、 EDTA HOOCCH 2 2 NCH 2 CH 2 N CH 2 COOH 2 可形成配合物 ①重氮
Cu NH H O SO , Cu EDTA SO 。 化:
3 4 2 2 4 4
① SO 2− 的空间结构为 , EDTA 中碳原子杂化方式为 。
4
② 在 Cu NH H O SO 化合物中,阳离子呈轴向狭长的八面体结构(如图),该阳离子
3 4 2 2 4
中存在的化学键类型为 ,该化合物加热时首先失去的组分是 ②生成碘苯:
已知:重氮盐在酸性水溶液中受热时,会发生下列副反应:
实验步骤:
I.烧杯中加入浓盐酸、蒸馏水,再加入 2 g 苯胺溶解,控制温度不超过 5℃,慢慢滴入
NaNO 溶液,不断搅拌,至重氮化反应完成;
2
II.在上述得到的重氮盐溶液中慢慢加入 KI 溶液,搅拌混合均匀后,加热并保持温度 50℃
(3)人 体代谢甲硒醇 CH 3 SeH 后可增加抗癌活性,下表中有机物沸点不同的原因为 。 。 至无气体放出;
甲 甲硫醇 III.冷却,倒去上层水,再加入稀 NaOH 溶液至碱性,进行水蒸气蒸馏;
有机物 甲硒醇
醇 CH 3 SH IV.从馏分中分离出碘苯,洗涤,加入无水 MgSO 4 干燥,再次蒸馏收集馏分,得到 2 g 产
品。
沸点/℃ 64.7 5.95 25.05
回答下列问题:
(4)四方晶系 CuInSe 的晶胞结构如图所示,晶胞参数为 浔 pm, 2 浔 pm,晶胞棱边夹角均为 。
2
(1)步骤 I 中控制温度不超过 5℃的方法是 。
设阿伏加德罗常数的值为
A
,CuInSe
2
的相对分子质量为 M,则该晶体密度 g cm−3(用含有 m、M
(2)步骤 II 中 KI 溶液需慢慢加入到重氮盐溶液中,原因是 ;重氮化反应完成后,溶液中
和。 的代数式表示)。晶体中与单个 In 键合的 Se 有
A 剩有稍过量的 HNO ,遇淀粉 KI 试纸变蓝,并产生 NO,可用于检验重氮化作用是否完
2
成,写出该检验反应的离子方程式 。
(3)步骤 III 中加入 NaOH 溶液的目的是 。
(4)步骤 IV 中从馏分中分离出的碘苯因混有 I 通常为红棕色,可加入下列___________进行
2
洗涤(填标号)。
A.CHCl B.NaHSO 溶液 C.C H OH D.H O
3 3 2 5 2
(5)步骤 IV 中再次蒸馏时用到的玻璃仪器有酒精灯、温度计、尾接管、蒸馏烧瓶、和 ;碘苯的产率为 %(保留一位小数;摩尔质量:苯胺 3 g mol−1,碘苯
2 4 g mol−1)。
(6)碘苯在有机合成中易与金属 Mg 反应生成格氏试剂 C H MgI,原因除了 Mg 的还原性强外,还可
5
能是 。
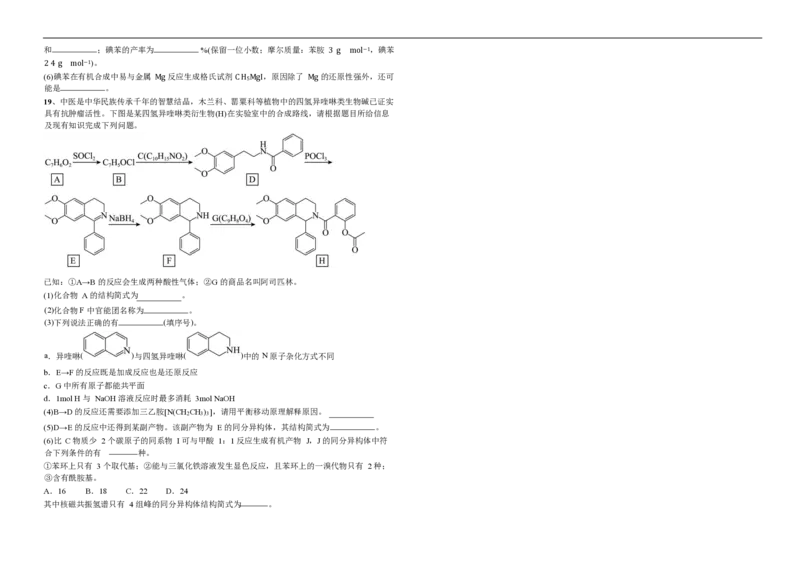
19、中医是中华民族传承千年的智慧结晶,木兰科、罂粟科等植物中的四氢异喹啉类生物碱已证实
具有抗肿瘤活性。下图是某四氢异喹啉类衍生物(H)在实验室中的合成路线,请根据题目所给信息
及现有知识完成下列问题。
已知:①A→B 的反应会生成两种酸性气体;②G 的商品名叫阿司匹林。
(1)化合物 A 的结构简式为 。
(2)化 合物 F 中官能团名称为 。
(3)下 列说法正确的有 (填 序号 )。
a .异喹啉 ( ) 与四氢异喹啉 ( )中 的 N 原子杂化方式不同
b.E→F 的反应既是加成反应也是还原反应
c.G 中所有原子都能共平面
d.1mol H 与 NaOH 溶液反应时最多消耗 3mol NaOH
(4)B→D 的反应还需要添加三乙胺[N(CH CH ) ],请用平衡移动原理解释原因。
2 3 3
(5)D→E 的反应中还得到某副产物。该副产物为 E 的同分异构体,其结构简式为 。
(6)比 C 物质少 2 个碳原子的同系物 I 可与甲酸 1:1 反应生成有机产物 J,J 的同分异构体中符
合下列条件的有 种。
①苯环上只有 3 个取代基;②能与三氯化铁溶液发生显色反应,且苯环上的一溴代物只有 2 种;
③含有酰胺基。
A.16 B.18 C.22 D.24
其中核磁共振氢谱只有 4 组峰的同分异构体结构简式为 。