文档内容
专题 07 原子结构 化学键
内容概览
考点01 原子结构
考点02 核素、同位素
考点03 化学键
考点01 原子结构
1.(23-24高一上·北京通州·期末)某离子的原子核里有n个质子,该离子的电子层排布与氩原子相同,
此离子所带的电荷可能是
A.+(n-18) B.-n C.-(n+18) D.+(18-n)
【答案】A
【分析】氩原子的结构示意图为 ,某离子的电子层排布与氩原子相同,则该离子可能是K+、
Ca2+、Cl-等。
【解析】A.若是K原子则n=19,K+所带的电荷为+(19-18),A正确;
B.不可能存在带-n电荷的离子满足以上条件,B错误;
C.不可能存在带-(n+18)电荷的离子满足以上条件,C错误;
D.若n=16则对应的离子为+(18-16),但+2硫离子的核外电子排布式与氩原子不同,无满足以上条件的带
+(18-n) 电荷的离子,D错误;
故选A。
2.(22-23高一上·北京东城·期末)下列叙述正确的是
A.电子的能量越低,运动区域离核越远
B.某原子K层上只有一个电子
C.稀有气体元素原子的最外层都排有8个电子
D.当M层是最外层时,最多可排布18个电子
【答案】B
【解析】A.电子的能量越低,运动区域离核越近,电子的能量越高,运动区域离核越远,A错误;
B.氢原子K层上只有一个电子,B正确;
C.氦为稀有气体元素,其最外层只有2个电子,C错误;
D.由电子的排布规律可知,M层最多排18个电子,但为最外层时,最多可排8个电子,D错误;
答案选B。
3.(23-24高一上·上海·期末)下列微粒中,具有相同的电子层数与最外层电子数的是
学科网(北京)股份有限公司A.He与Li B. 与 C. 与 D. 与Ar
【答案】BC
【解析】A.He与Li核外电子层数分别为:1、2,最外层电子数分别为:2、1,A不符合题意;
B. 与 核外都是10个电子,具有相同的电子层数与最外层电子数,B符合题意;
C. 与 核外都是18个电子,具有相同的电子层数与最外层电子数,C符合题意;
D. 与Ar的核外电子层数分别为2、3,最外层电子数分别为8和8,D不符合题意;
故答案为:BC。
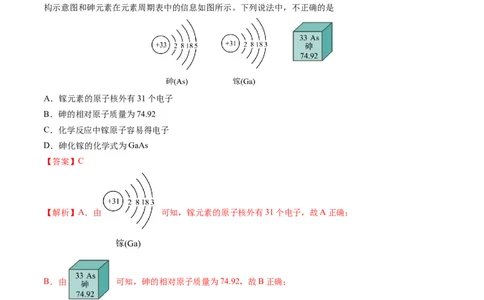
4.(23-24高一上·广东省茂名市·期末)神舟载人飞船使用了砷化镓太阳能电池。砷(As)、镓(Ga)的原子结
构示意图和砷元素在元素周期表中的信息如图所示。下列说法中,不正确的是
A.镓元素的原子核外有31个电子
B.砷的相对原子质量为74.92
C.化学反应中镓原子容易得电子
D.砷化镓的化学式为GaAs
【答案】C
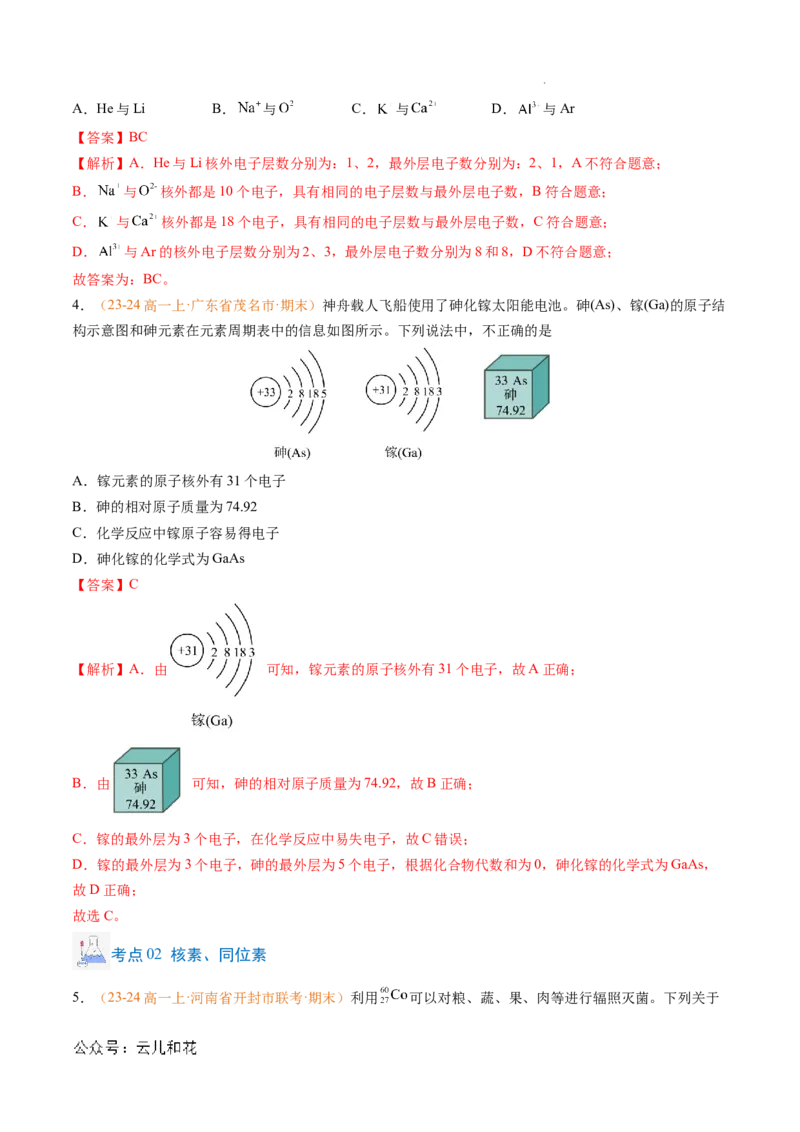
【解析】A.由 可知,镓元素的原子核外有31个电子,故A正确;
B.由 可知,砷的相对原子质量为74.92,故B正确;
C.镓的最外层为3个电子,在化学反应中易失电子,故C错误;
D.镓的最外层为3个电子,砷的最外层为5个电子,根据化合物代数和为0,砷化镓的化学式为GaAs,
故D正确;
故选C。
考点02 核素、同位素
5.(23-24高一上·河南省开封市联考·期末)利用 可以对粮、蔬、果、肉等进行辐照灭菌。下列关于
学科网(北京)股份有限公司的说法中,正确的是
A.质子数为27 B.中子数为60 C.质量数为87 D.核外电子数为33
【答案】A
【解析】 的质子数为27、质量数为60,核外电子数为27,中子数为60—27=33,故选A。
6.(23-24高一上·重庆·期末)2023年9月29日,国家航天局发布消息,探月工程嫦娥六号计划于2024
年前后实施发射。我国科学家已在嫦娥五号取回的月壤中检测出了3He。下列关于3He的说法不正确的是
A.质量数为3 B.与4He互为同素异形体
C.与4He互为同位素 D.中子数为1
【答案】B
【解析】A.元素符号左上角的数字为质量数,3He的质量数为3,故A正确;
B.同素异形体是同种元素形成的不同单质,3He与4He不互为同素异形体,故B错误;
C.同位素是质子数相同、中子数不同的同种元素的不同原子,3He与4He互为同位素,故C正确;
D.He的质子数为2,则3He的中子数为1,故D正确;
故选B。
7.(23-24高一上·安徽省合肥市六校联盟·期末)下列叙述或化学用语正确的是
A. 和 互为同位素 B. 的电子式:
C.HClO的结构式: D.中子数为18的氯原子:
【答案】D
【解析】A. 和 是由氢元素不同同位素构成的单质分子,不是同位素,故A错误;
B. 是离子化合物,电子式为 ,故B错误;
C.HClO的结构式: ,故C错误;
D.中子数为18的氯原子质量数为35,该原子表示为 ,故D正确;
选D。
8.(23-24高一上·四川省绵阳市·期末)我国自主三代核电“华龙一号”的反应堆中可能存在 + n→
Ba+ Kr+3 n的核反应,下列说法正确的是
A. Y与 Kr互为同位素 B. Kr、 Kr互为同素异形体
C. 的中子数为143 D.Ba是第五周期第ⅡA族元素
【答案】C
【分析】核素的表示方法为:元素符号左下角为质子数,左上角为质量数;
学科网(北京)股份有限公司【解析】A. Y与 Kr质子数不同,不是同一种元素,不互为同位素,A错误;
B. Kr、 Kr是同种元素的不同原子,互为同位素,而不是互为同素异形体,B错误;
C. 的中子数为 ,C正确;
D.Ba的质子数为56,是第六周期第ⅡA族元素,D错误;
故选C。
9.(23-24高一上·四川省成都市·期末)我国在可控核聚变研究上处于世界领先水平,其反应为:
。下列说法错误的是
A. 原子符号可以表示为T B. 是两种不同的核素
C. 的中子数为2 D. 粒子的质量相同
【答案】D
【解析】A. 原子中子数为3-1=2,符号可以表示为T,故A正确;
B. 具有一定质子数,中子数不同,是两种不同的核素,故B正确;
C. 的质量数为4,质子数为2,中子数为质量数-质子数=4-2=2,故C正确;
D. 粒子质量数分别为2、3,两者的质量不同,故D错误;
故选D。
10.(23-24高一上·福建省福州市·期末)下列化学用语正确的是
A. 与 互为同位素 B.镁离子的结构示意图:
C. 与 互为同素异形体 D. 和 互为同分异构体
【答案】C
【解析】A. 与 是不同原子,不能互为同位素,A错误;
B.镁离子的核电荷数为12,离子结构示意图为 ,B错误;
C. 与 是氧元素的不同单质,互为同素异形体,C正确;
D. 和 的分子式不同,不是同分异构体,D错误;
答案选C。
11.(23-24高一上·安徽省芜湖市·期末)下列化学用语正确的是
A.质量数为37的氯原子: B.HCl的电子式:
学科网(北京)股份有限公司C.氟原子的结构示意图: D.CO 的电子式:
2
【答案】A
【解析】A.质量数为37的氯原子,其质子数为17,则可表示为 ,A正确;
B.HCl为共价化合物,由原子构成,其电子式为 ,B不正确;
C.氟原子的核电荷数为9,核外电子数为9,结构示意图为 ,C不正确;
D.CO 分子中,C原子与每个O原子各形成2对共用电子,其电子式为 ,D不正确;
2
故选A。
12.(23-24高一上·北京市东城区·期末)“东方超环”钨铜偏滤器利用了钨熔点高、耐高温的性质。钨
(W)有五种稳定的核素。下列关于钨( )的说法中,不正确的是
A.质子数为74 B.中子数为112 C.质量数为186 D.核外电子数为260
【答案】D
【解析】 的质子数为74,质量数为186,中子数为186-74=112,核外电子数=质子数=74,故D不正
确;
答案选D。
考点03 化学键
13.(23-24高一上·河南省开封市联考·期末)下列物质中,含有极性共价键的是
A. B. C. D.
【答案】B
【解析】A.碘单质中只含非极性共价键,故A错误;
B.HCl中只含极性共价键,故B正确;
C.氯化镁中只含离子键,故C错误;
D.KBr中只含离子键,故D错误;
故选B。
14.(23-24高一上·四川省绵阳市·期末)下列含氯元素的物质中,属于离子化合物的是
A.HClO B.Cl C.HCl D.MgCl
2 2
【答案】D
【解析】A.HClO只含共价键,属于共价化合物,故A不合题意;
B.Cl 是非金属单质,故B不合题意;
2
C.HCl只含共价键,属于共价化合物,故C不合题意;
学科网(北京)股份有限公司D.MgCl 含有离子键,属于离子化合物,故D符合题意;
2
故本题选D。
15.(23-24高一上·广东省茂名市·期末)下列物质中,只含离子键,不含共价键的是
A. B. C. D.
【答案】B
【解析】A.NaO 为离子化合物,Ca2+和 之间形成离子键, 中含有O-O非极性共价键,故A项不
2 2
符合题意;
B.氯化镁为离子化合物,Mg2+和Cl-之间形成离子键,故B项符合题意;
C.氯化铵为离子化合物,铵根离子和Cl-之间形成离子键,铵根离子中含有N-H极性共价键,故C项不符
合题意;
D.CHCOOH为共价化合物,只含有共价键,故D项不符合题意;
3
故本题选B。
16.(23-24高一上·北京市东城区·期末)下列物质的电子式书写正确的是
A. B. C. D.
【答案】A
【解析】
A.水是共价化合物,O与每个H共用1对电子,其电子式为 ,故A正确;
B.氯化钠是离子化合物,钠离子和氯离子存在离子键,其电子式为 ,故B错误;
C.二氧化碳是共价化合物,碳与每个氧共用两对电子,其电子式为 ,故C错误;
D.氨气是共价化合物,氨气分子中N、H原子间共用1对电子对,氮原子需满足8电子稳定结构,电子式
为 ,故D错误;
答案为A。
17.(23-24高一上·重庆·期末)下列变化过程中,无化学键断裂的是
A.甲烷燃烧 B.蔗糖溶于水 C.NaOH固体溶于水 D.HSO 溶于水
2 4
【答案】B
【解析】A.甲烷燃烧为化学反应,存在化学键的断裂,故A不符合题意;
B.蔗糖溶于水,蔗糖、水都是以分子形式存在,没有化学键的断裂,故B符合题意;
C.NaOH固体溶于水发生电离,离子键断裂,故C不符合题意;
D.HSO 溶于水电离出H+,有共价键的断裂,故D不符合题意;
2 4
故选:B。
18.(23-24高一上·湖南省名校联考联合体·期末)反应 放热且产生
气体,可应用于石油开采,解决冬季开采石油井下结蜡难题。下列说法正确的是
学科网(北京)股份有限公司A. 的电子式为 B. 的结构示意图为
C. 的结构式为 D. 的空间结构为 形
【答案】D
【解析】
A. 为阳离子,带有1个单位正电荷,其电子式为[ ]+,A错误;
B. 的核外只有10个电子,故 的结构示意图为 ,B错误;
C. 分子的电子式为 ,结构式为 ,C错误;
D. 分子中含有2个 极性键,空间结构为 形,D正确;
本题选D。
19.(23-24高一上·北京市东城区·期末)氢气在氯气中燃烧时发生反应: 。下列说法不正
确的是
A. 在 中安静燃烧时,发出苍白色火焰,放出热量
B. 发生了氧化反应, 发生了还原反应
C.反应过程中,包含非极性键的断裂和极性键的形成
D.用电子式表示 的形成过程:
【答案】D
【解析】A.纯净的氢气在氯气里安静的燃烧,发出苍白色火焰,A正确;
B.氢元素化合价升高,被氧化,故氢气发生氧化反应,氯元素化合价降级,故氯气发生还原反应,B正
确;
C.反应过程中,断H-H、Cl-Cl非极性键,形成H-Cl极性键,C正确;
D.氯化氢是共价化合物,形成氯化氢使是共用电子对,不是得失电子,D错误;
答案选D。
20.(23-24高一上·吉林省长春市东北师范大学附属中学·期末)下列过程中,共价键被破坏的是
① 溶于水;②溴蒸气被木炭吸附;③酒精溶于水;④ 气体溶于水;⑤碘升华;⑥ 受热分解;
⑦氢氧化钠熔化;⑧ 溶于水
A.④⑥⑦ B.④⑤⑧ C.②⑤③ D.①④⑥
【答案】D
学科网(北京)股份有限公司【解析】① 溶于水生成氧气,其中的O和O之间的共价键被破坏,①正确;
②溴蒸气被木炭吸附,是物理变化,共价键不被破坏,②错误;
③酒精溶于水,不能发生电离,共价键不被破坏,③错误;
④HCl气体溶于水电离成H+和Cl-,共价键被破坏,④正确;
⑤碘升华,破坏分子间作用力,共价键不被破坏,⑤错误;
⑥ 受热分解生成单质碘和氢气,共价键的破坏,⑥正确;
⑦氢氧化钠熔化破坏离子键,共价键不被破坏,⑦错误;
⑧ 溶于水破坏离子键,共价键不被破坏,⑧错误;①④⑥符合题意;
故选D。
1.(23-24高一上·江苏省南京市·期末)Se是人体必需的微量元素, 的原子核内中子数是
A.44 B.78 C.34 D.112
【答案】A
【解析】根据原子符号中,左下角的数字为质子数,左上角的数字为质量数,中子数=质量数-质子数,质
子数=原子核外电子数,因此 的质子数为34,质子数=原子核外电子数=34,质量数为78,中子数=78-
34=44,故选A。
2.(23-24高一上·湖北省A9高中联盟·期末)下列化学用语错误的是
A.含8个中子的碳原子:14C
B.CO 的结构式:O=C=O
2
C.KCl形成过程:
D.Mg原子结构示意图:
【答案】C
【解析】A.,质量数等于质子数加中子数,因此含8个中子的碳原子质量数为8+6=14,则原子核内有8
个中子的碳原子表示为:14C,故A正确;
B.二氧化碳为直线形结构,碳与氧均形成的是双键,结构式为: ,故B正确;
C.氯化钾的形成过程有电子得失,氯化钾是离子化合物,因此形成过程为: ,
故C错误;
D.Mg原子核外有12个电子,分布在 3个电子层,最外层有 2个电子,Mg的原子结构示意图的是
,故D正确;
学科网(北京)股份有限公司故答案选C。
3.(23-24高一上·河南省开封市联考·期末)雷雨天时空气中有 生成。下列说法正确的是
A. 和 互为同位素
B. 和 的相互转化是物理变化
C.等物质的量的 和 含有相同的质子数
D.在相同的温度和压强下,等体积的 和 含有相同的分子数
【答案】D
【解析】A. 和 是氧元素形成的不同单质,互为同素异形体,故A错误;
B. 和 的相互转化是化学变化,故B错误;
C.等物质的量的 和 含有的氧原子数不同,质子数也不同,故C错误;
D.根据阿伏加德罗定律,在相同的温度和压强下,等体积的 和 含有相同的分子数,故D正确。
答案选D。
4.(23-24高一上·吉林省长春市东北师范大学附属中学·期末)下列描述正确的是
A. 与 是同素异形体 B. 的分子结构模型是
C.氚的原子结构模型是 D. 的离子结构示意图是
【答案】C
【解析】A.16O 与18O 是同一种物质,不是同素异形体,A错误;
2 2
B.二氧化碳为直线形分子,B错误;
C.氚有1个质子、2个中子、1个电子,其原子结构模型为: ,C正确;
D.18O2−的核电荷数为8,带有2个单位的负电荷,其核外电子数为10,为 ,D错误;
故答案为:C。
5.(23-24高一上·广东省广州市·期末)“天问一号”探测器成功着陆火星、“华龙一号”核电海外投
产、北斗卫星导航系统全面开通、“奋斗者”号载人潜水器成功坐底,均展示了我国科技发展的巨大成
就。下列相关叙述不正确的是
A.火星陨石中的 中子数为20
B.核电站反应堆所用铀棒中含有的 与 互为同位素
学科网(北京)股份有限公司C.“北斗卫星”的授时系统“星载铷钟”中铷元素的单质若遇水会剧烈放出
D.“奋斗者”号载人潜水器球壳所使用的钛合金具极高的硬度和抗压性,能承受深海高压
【答案】A
【解析】A. 中子数=质量数-质子数=20-10=10,A错误;
B. 与 的质子数都为92,中子数分别为143、146,是质子数相同、中子数不同的同一元素,两者
互称同位素,B正确;
C.铷是活泼金属,比钠金属性更强,可与水快速反应放出氢气,C正确;
D.“奋斗者”号载人潜水器球壳所使用的钛合金性能优异,能承受深海高压,D正确;
答案选A。
6.(23-24高一上·陕西省名校·期末)下列物质中既含有离子键,又含有非极性共价键的是
A. B. C. D.
【答案】A
【解析】A. 是离子化合物,含有 和 之间的离子键和氧原子与氧原子之间的非极性共价键,
A项正确;
B. 是离子化合物,含有 和 之间的离子键和氧原子与硫原子之间的极性共价键,B项错
误;
C.NaOH是离子化合物,含有 和 之间的离子键和氧原子与氢原子之间的极性共价键,C项错
误;
D. 是离子化合物,含有 和 之间的离子键和氮原子与氢原子之间的极性共价键,D项错
误;
故选A。
7.(23-24高一上·江西省新余市·期末)研究发现,在饮用水、食物或牙膏中添加氟化物,能起到预防龋
齿的作用。这是因为氟离子能与羟基磷灰石发生反应,该反应为
。下列说法正确的是
A.中子数为17的磷原子: B. 的电子式为:
C. 的离子结构示意图 D. 中既存在共价键又存在离子键
【答案】D
【解析】A.中子数为17的磷原子,质量数为32,正确的符号为: ,A错误;
B. 的电子式为: ,B错误;
学科网(北京)股份有限公司C. 的离子结构示意图为: ,C错误;
D.钙离子和氟离子以及钙离子和磷酸根离子之间存在离子键,磷酸根离子内存在共价键,D正确;
答案选D。
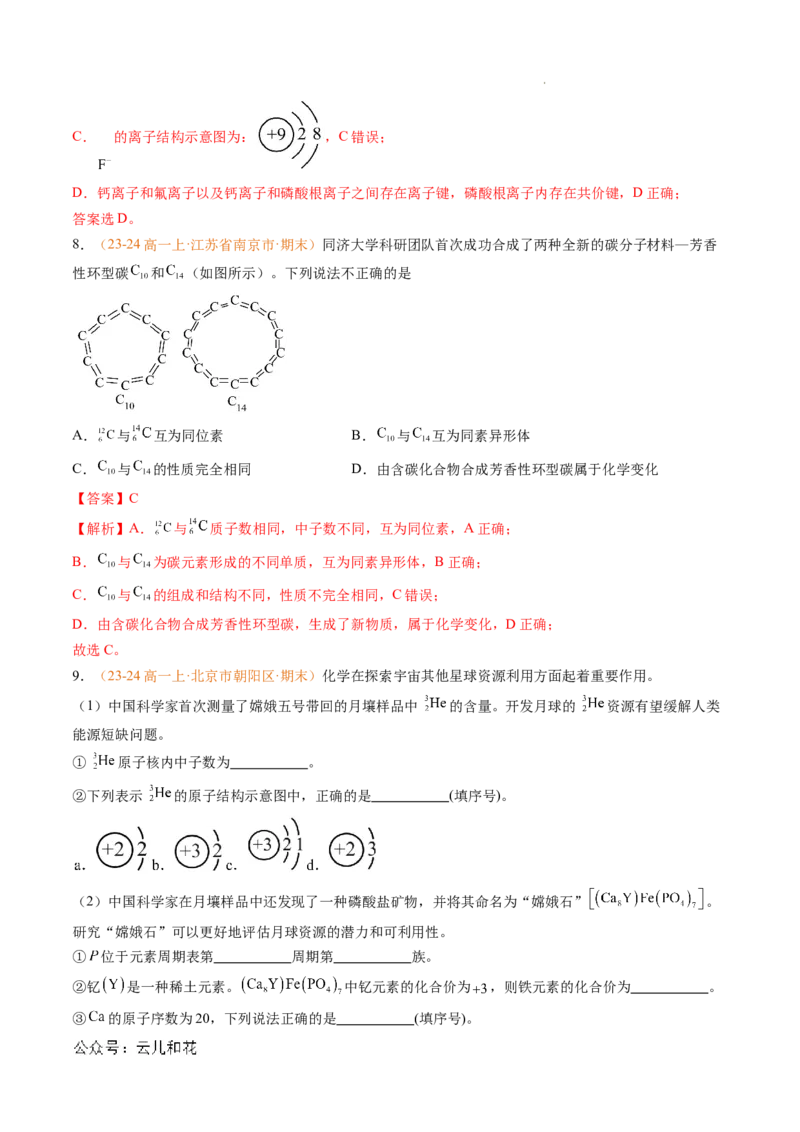
8.(23-24高一上·江苏省南京市·期末)同济大学科研团队首次成功合成了两种全新的碳分子材料—芳香
性环型碳 和 (如图所示)。下列说法不正确的是
A. 与 互为同位素 B. 与 互为同素异形体
C. 与 的性质完全相同 D.由含碳化合物合成芳香性环型碳属于化学变化
【答案】C
【解析】A. 与 质子数相同,中子数不同,互为同位素,A正确;
B. 与 为碳元素形成的不同单质,互为同素异形体,B正确;
C. 与 的组成和结构不同,性质不完全相同,C错误;
D.由含碳化合物合成芳香性环型碳,生成了新物质,属于化学变化,D正确;
故选C。
9.(23-24高一上·北京市朝阳区·期末)化学在探索宇宙其他星球资源利用方面起着重要作用。
(1)中国科学家首次测量了嫦娥五号带回的月壤样品中 的含量。开发月球的 资源有望缓解人类
能源短缺问题。
① 原子核内中子数为 。
②下列表示 的原子结构示意图中,正确的是 (填序号)。
(2)中国科学家在月壤样品中还发现了一种磷酸盐矿物,并将其命名为“嫦娥石” 。
研究“嫦娥石”可以更好地评估月球资源的潜力和可利用性。
① 位于元素周期表第 周期第 族。
②钇 是一种稀土元素。 中钇元素的化合价为 ,则铁元素的化合价为 。
③ 的原子序数为20,下列说法正确的是 (填序号)。
学科网(北京)股份有限公司属于短周期元素 原子半径:
能与冷水反应 碱性:
(3)火星上含有丰富的 和 资源,科学家设想利用如下反应为火星电站发电、人员取暖等。
①写出 的电子式: 。
②推测 能否与 反应,从原子结构角度说明理由: 。
【答案】(1)1 a
(2)三 ⅤA +2 cd
(3) 钠的原子半径大于镁原子,失电子能力大于镁原子,钠能与二氧化碳反应
【解析】(1)① 原子核内中子数=3-2=1;
② 的原子结构示意图中有一个电子层,核电荷数=核外电子数=2,原子结构示意图为: ,故
选a;
(2)①P元素核电荷数=核外电子数=质子数=15,元素周期表第三周期第ⅤA族;
②钇(Y)是一种稀土元素。(Ca Y)Fe(PO) 中钇元素的化合价为+3,Ca元素化合价+2价, 的化合价-3
8 4 7
价,则铁元素的化合价为+2价;
③a.Ca属于长周期元素,故a错误;
b.K、Ca为同周期元素,原子半径:Ca<K,故b错误;
c.Ca的金属性大于Na,Ca能与冷水反应,故c正确;
d.金属性Ca>Mg,最高价氧化物对应水化物碱性:Ca(OH) >Mg(OH) ,故d正确;
2 2
故答案为:cd;
(3)①MgO是离子化合物,电子式为 ;
②Na和Mg为同周期元素,原子半径依次减小,钠的原子半径大于镁原子,失电子能力较强,钠的金属性
大于Mg,则钠和二氧化碳能反应。
10.(23-24高一上·北京市东城区·期末)冬季燃煤排放的大量活性溴化合物 能通过光解释放溴自由
基 和氯自由基 ,从而影响大气中自由基( 等)的浓度,其原理如图所示:
学科网(北京)股份有限公司【资料】①自由基是存在未成对电子的原子或原子团。
②氢氧自由基 的电子式可表示为 。
(1) 的结构式为 。
(2) 所含化学键类型为 ;溴元素的化合价为 价,从原子结构的角度解释其
原因: 。
(3)由 可知,溴自由基具有强 (填“氧化性”或“还原性”)。
(4)下列说法正确的是 (填字母)。
a.一个 自由基有17个电子
b. 与 互为同素异形体
c.排放大量 会造成臭氧层破坏
d.溴氧自由基 中溴元素的化合价为 价
【答案】(1)
(2)共价键(或极性共价键) 与 位于同一主族,最外层电子数均为7,电子层数
,原子半径 ,得电子能力 ,共用电子对偏向 一方
(3)氧化性
(4)abc
【解析】(1)HBrO分子中氧原子分别和H原子、Br原子形成一对共用电子对,HBrO的结构式为:H-O-
Br;
(2)BrCl为共价化合物,氯原子和溴原子形成一对共用电子对,所含化学键类型为共价键(或极性共价
键);氯原子半径小,对共用电子对吸引能力强,共用电子对偏向氯原子,BrCl中氯元素化合价为-1价,
溴元素的化合价为+1价,从原子结构的角度解释其原因为:Cl与Br位于同一主族,最外层电子数均为
7,电子层数ClBr,共用电子对偏向Cl一方;
(3)由Hg+2Br→HgBr 可知,汞元素化合价升高,证明溴自由基具有强氧化性;
2
(4)a.一个 自由基有电子=1+8×2=17,故a正确;
b. 与 是氧元素的不同单质,互为同素异形体,故b正确;
c.由图可知,BrCl能通过光解释放溴自由基 和氯自由基 ,溴自由基与臭氧O 结合生成溴氧自
3
由基 ,排放大量 会消耗臭氧,造成臭氧层破坏,故c正确;
学科网(北京)股份有限公司d.溴氧自由基 中氧元素化合价为-2价,其中O存在未成对电子,则溴元素的化合价为+1价,故d
错误;
故答案为:abc。
学科网(北京)股份有限公司